Изобретение относится к медицине, а именно к хирургии, к способу лечения хронических ран с использованием тромбоцитарной аутоплазмы.
Острые и хронические повреждения кожи, несмотря на очевидный прогресс методов терапии, остаются серьезной проблемой здравоохранения. По оценкам, в мире ежегодно производится более 100 миллионов хирургических разрезов, количество ран травматического происхождения свыше 50 миллионов, причем лечение ожогов и хронических ран, как правило, более длительное и дорогостоящее [Александрушкина, Н.А. Экспериментальные модели оценки заживления кожных ран у грызунов: методология и ограничения трансляционных исследований / Н.А. Александрушкина, В.С. Попов, П.И. Макаревич // Гены и Клетки. - 2022. - Т. 17, № 3. - С. 10-11. - EDN BGSIVR].
Раны, несмотря на разностороннее развитие современной медицины, остаются одной из главных проблем в хирургии вследствие частой встречаемости, а также из-за высоких затрат рабочего времени и материальных ресурсов для их лечения. Раневой процесс является сложным комплексом ответных реакций организма на повреждение и характеризуется определенной фазностью своего течения.
Благодаря более подробному изучению патофизиологии и патогенеза раневого процесса стали возможными не только назначение пациентам более эффективного и патогенетически обоснованного лечения, но и поиск, разработка и внедрение новых современных высокоэффективных методик в процессе лечения ран [Тамразова О.Б. Репаративная терапия «малых» ран с позиции дерматолога и косметолога // Аллергология и иммунология в педиатрии. 2019. № 2 (57). С. 4-12. doi:10.24411/2500-1175-2019-00006].
Раневой процесс является сложным комплексом нейрогуморальных, клеточных, микробиологических механизмов, в результате которого при отсутствии осложнений путем последовательно сменяющих друг друга фаз образуется рубец и происходит возвращение тканей к их практически нормальной структуре и функциям.
Под влиянием ряда неблагоприятных факторов раневой процесс может осложняться или затягиваться и принимать хроническое течение. Хронические раны часто застаиваются в фазе воспаления или испытывают нарушение в течение пролиферативной фазы. Среди осложнений встречаются серомы, раневые гематомы, расхождения ран, некрозы мягких тканей, образование гипертрофических рубцов и келоидов.
Основными целями лечения во второй фазе раневого процесса являются стимуляция репарации, защита образующейся грануляционной ткани, а также профилактика вторичного инфицирования [Лечение ран в зависимости от фазы раневого процесса / Е.В. Муромцева, К.И. Сергацкий, В.И. Никольский и др. // Известия высших учебных заведений. Поволжский регион. Медицинские науки. - 2022. - № 3 (63). - С. 93-109. - DOI 10.21685/2072-3032-2022-3-9. - EDN CBPSIU].
Для стимуляции процесса регенерации ран известно использование концентрированных суспензий тромбоцитов. При дегрануляции тромбоцитов происходит высвобождение ряда биологически активных веществ, которые являются основными регуляторами репаративных процессов. Так, тромбоциты выступают в качестве источника факторов роста, цитокинов и хемокинов, которые обеспечивают направленную миграцию прогениторных клеток в зону раневого дефекта, стимулируют их пролиферацию и дифференцировку, что оказывает благоприятный эффект на течение раневого процесса [Современные методы стимуляции процесса регенерации послеоперационных ран / А.М. Морозов, А.Н. Сергеев, Н.А. Сергеев и др. // Сибирское медицинское обозрение. - 2020. - № 3 (123). - С. 7. - DOI 10.20333/2500136-2020-3-. - EDN WHYDTP].
Достаточно интересным методом для стимуляции регенеративных процессов является введение тромбоцитарной аутоплазмы. Не являющаяся токсичной или иммунореактивной аутоплазма, содержащая тромбоциты, ускоряет естественные механизмы регенерации благодаря наличию в тромбоцитах факторов роста. Кроме того, аутоплазма модулирует и регулирует функцию первичных факторов роста. Упомянутое свойство отличает факторы роста аутоплазмы, содержащей тромбоциты, от рекомбинантных факторов роста, каждый из которых отвечает за отдельный механизм регенерации [Greenlagh D.G. The role of growth factors in wound healing. J Trauma, 1996; 41: 159-167].
Принципиальным преимуществом метода Plasmoactive™ применения аутоплазмы, обогащенной тромбоцитами, является возможность увеличивать количество тромбоцитов в тканях путем увеличения объёма вводимой плазмы. Данное свойство присуще только естественному, жидкому состоянию плазмы.
В мировой практике широко используются концентраты клеток собственной крови для улучшения репарации ран. Используются как инъекционные методы, так и местное применение концентратов. Однако при местном применении аутоплазмы возникает ряд сложностей: в условиях открытого пространства достаточно быстро происходит денатурация белков плазмы и гибель клеточного концентрата; использование различных пленочных покрытий, приготовленных из концентратов аутокрови, достаточно трудоемко и дорого.
Существует ряд методов стимуляции заживления ран с использованием тромбоцитарной аутоплазмы.
Известен способ лечения трофических язв мягких тканей. Предварительно проводят активизацию аутоплазмы путем центрифугирования в течение 5 мин с последующим добавлением к ней 10% раствора хлористого кальция из расчета 1:1. Затем смесь термостатируют в течение 20 мин при температуре 40°C, получая стабилизированную биологически активную пленку. После обработки язвы и прилегающей к ней ткани ударной волной 100-1000 ударов на см2 при силе удара 0,1 мДж/1 мм2 и обработки язвы стерильным нейтральным раствором на язву наносят полученную пленку и укрывают асептической повязкой. Процедуру повторяют 7-8 раз с интервалом в 5 дней (Патент № 2593582 C1, Российская Федерация, МПК A61N 7/00, A61K 35/16, A61P 17/02. Способ консервативного лечения трофических язв мягких тканей, № 2015113078/14, заявл. 09.04.2015, опубл. 10.08.2016 / И.В. Канксиди, Ю.С. Кузнецов, Д.В. Туркин, Г.К. Карипиди, заявитель Общество с ограниченной ответственностью "НикоМед" (ООО "НикоМед"). - EDN ZEWKNN).
Недостатками данного метода являются необходимость активации тромбоцитарной аутоплазмы, использования термостата и аппарата для ударно-волновой терапии. Воздействие тромбоцитарной аутоплазмы в предлагаемом методе планируется на поверхности раневого дефекта.
Известен способ лечения трофических язв венозной этиологии. Способ включает введение пациенту обогащенной тромбоцитами аутоплазмы и регионарное введение лимфостимулирующих препаратов в оптимальных дозах эффективным курсом лечения, при этом аутоплазму вводят субульцерозно (Патент № 2639123 C, Российская Федерация, МПК A61K 35/16, A61K 31/167, A61K 38/47. Способ местного лечения трофических язв венозной этиологии, № 2016139062, заявл. 04.10.2016, опубл. 19.12.2017 / Ю.М. Шутов, О.А. Шумков, Н.И. Севрюкова, заявитель Федеральное государственное бюджетное образовательное учреждение высшего образования "Новосибирский государственный медицинский университет" Министерства здравоохранения Российской Федерации (ФГБОУ ВО НГМУ Минздрава России). - EDN TEXASV).
Недостатками данного метода является введение аутоплазмы субульцерозно, что может быть сложнодостижимо при больших размерах и глубине раневого дефекта.
Технической задачей заявляемого изобретения является ускорение заживления раневых дефектов за счет воздействия на гуморальные и клеточные факторы иммунного ответа и воздействие на процессы репаративной регенерации.
Техническим результатом заявляемого изобретения является использование собственной плазмы пациента, обогащенной тромбоцитами, для модулирования регенерации пораженных тканей и активации собственных гуморальных и клеточных факторов защиты во время течения воспалительного процесса путем сочетания инъекционного введения по периферии раны и местного воздействия на раневой дефект.
Указанный технический результат достигается тем, что предложен способ лечения хронических ран с использованием тромбоцитарной аутоплазмы, включающий антибактериальную и регенерационную терапию раневого процесса, отличающийся тем, что дополнительно производят введение аутоплазмы, обогащенной тромбоцитами, при этом для получения аутоплазмы забирают венозную кровь, затем полученную обогащенную тромбоцитами аутоплазму разделяют на две части, одну из которых в объеме 4 мл смешивают с 3,0 мл биопленки BIOFILM, а оставшуюся часть полученной аутоплазмы, обогащенной тромбоцитами, вводят инъекционной иглой, отступая от края раневого дефекта 6-8 мм, на глубину 8-10 мм с интервалами между вколами 8-10 мм, а затем смесь аутоплазмы и биопленки BIOFILM наносят на поверхность раневого дефекта и закрывают стерильным материалом.
Возможность достижения технического результата обеспечивается тем, что сочетание аутоплазмы, обогащенной тромбоцитами, и гидрогеля (биопленки) BIOFILM позволяет увеличить длительность действия аутоплазмы и дополнить её эффективность компонентами, входящими в состав биопленки (гидрогеля): вода, д-пантенол, ксантановая камедь, лецитин, склероциевая камедь, пуллулан, сквалан, гиалуроновая кислота, аллантоин, аргинин, метилхлоризотиазолинон, метилизотиазолинон.
Предлагаемый способ осуществляется следующим образом:
1. Выполняется забор венозной крови пациента в пробирки из набора Medical Case Plasmoactive (согласно методике, в вакуумную пробирку набирается 10 мл крови). Объем набираемой венозной крови зависит от площади раневого дефекта.
2. Выполняется центрифугирование крови в пробирке Medical Case Plasmoactive (из 10 мл забранной венозной крови при сепарации получается 4,0 - 4,5 мл плазмы, обогащенной тромбоцитами).
3. Аутоплазма, обогащенная тромбоцитами, разделяется на две части. 4,0 мл аутоплазмы смешивается с гидрогелем биопленкой (гидрогелем) BIOFILM компании Medical Case.
4. Оставшаяся аутоплазма, обогащенная тромбоцитами, набирается в шприцы для инъекций.
5. Обрабатывают операционное поле раствором антисептика.
6. Шприцом с инъекционной иглой 0,3×13 мм по краю раневого дефекта, отступая от края около 6-8 мм, на глубину около 8-10 мм с интервалами около 8-10 мм вводится аутоплазма.
7. Аутоплазма, смешанная с биопленкой (гидрогелем) BIOFILM, наносится на раневую поверхность.
8. Рана закрывается стерильной салфеткой.
По нашим данным, применение процедуры введения аутоплазмы, обогащенной тромбоцитами, инъекционно и местно в сочетании с биопленкой (гидрогелем) BIOFILM у пациентов с хроническими ранами показало, что метод оказывает положительное воздействие и у большинства пациентов наблюдается выраженная положительная динамика в течение раневого процесса. Были исследованы две группы пациентов, сопоставимые по возрасту, давности заболевания и выраженности проявлений заболевания. В обеих группах использовано одинаковое ведение ран: применялась мазь «Левометил» и сетчатые повязки «Бранолинд». В основной группе к традиционному ведению ран добавлено инъекционное и местное использование в сочетании с биопленкой (гидрогелем) аутоплазмы, обогащенной тромбоцитами. Инъекции и местное применение аутоплазмы использовались на следующий день после хирургической обработки раны и повторялись спустя 7 суток. Результатами комплексной терапии явилось: исчезновение гнойного отделяемого было достигнуто на 2,5 сутки от момента начала лечения, грануляции появлялись на 5,1 сутки.
В то время, как у пациентов группы сравнения гнойное отделяемое из раны прекращалось на 5 сутки, исчезновение болевого синдрома - на 6,6 сутки, появление грануляций было отмечено на 9,2 сутки.
Приводим клинические примеры осуществления способа.
Пример 1
Пациент А. 68 лет, находился на лечении в хирургическом отделении с 08.05.23 по 11.07.23 с диагнозом: Диабетическая стопа справа. Флегмона правой стопы. Сепсис. Инсулиннезависимый сахарный диабет с множественными осложнениями. ИБС. Атеросклеротическая болезнь сердца Гипертоническая болезнь 3 ст., неконтролируемая АГ, избыточная масса тела ИМП 29,41 кг/м2. ХБП 4 СКФ - 29,41 мл/мин, риск 4 (очень высокий). ХСН 2А ФК2. Диабетическая ретинопатия. Диабетическая нефропатия, стадия мироальбуминурии (протеинурия). Диабетическая полинейропатия, дистальная, симметричная. Хроническая анемия тяжелой степени тяжести.
08.05.23 выполнена операция: Некрэктомия. 10.05.23 Вскрытие, дренирование гнойника. В послеоперационном периоде применялась мазь «Левометил» и сетчатые повязки «Бранолинд». При осмотре отмечено отсутствие роста грануляционной ткани и эпителизации раны.
23.05.23 Выполнено введение 8,0 мл аутоплазмы, обогащенной тромбоцитами, по периферии раны, отступая 6 мм от краев, иглой для инъекций 0,3×13 мм на глубину 8 мм с интервалом между вколами 8 мм. Также 4,0 мл аутоплазмы смешано с 3,0 мл биопленки (гидрогеля) BIOFILM и нанесено на раневую поверхность.
25.05.23 выполнена операция: Некрэктомия.
При наблюдении: с 6-го дня отмечается появление грануляций, очищение раневой поверхности.
На 30-й день процедура инъекционного введения аутоплазмы и местного нанесения аутоплазмы в смеси с биопленкой (гидрогелем) BIOFILM повторено.
На 45 день выполнена пересадка кожного лоскута. В динамике отмечается удовлетворительное течение раневого процесса и хорошая приживаемость кожного лоскута.
Пример 2
Пациентка Ш. 55 лет, находилась на лечении в хирургическом отделении с 13.06.23 по 23.06.23 с диагнозом: Хронический остеомиелит костей левой голени. Флегмона левой голени. Сахарный диабет 2 тип, среднетяжелое течение.
13.06.23 выполнена операция: вскрытие и дренирование гнойника. В послеоперационном периоде применялась мазь «Левометил» и сетчатые повязки «Бранолинд».
15.06.23 Выполнено введение 4,0 мл аутоплазмы, обогащенной тромбоцитами, по периферии раны, отступая 8 мм от краев, иглой для инъекций 0,3×13 мм на глубину 10 мм с интервалом между вколами 10 мм. Также 4,0 мл аутоплазмы в смеси с 3,0 мл биопленки (гидрогеля) BIOFILM нанесено на раневую поверхность.
На 5-й день от момента введения отмечено появление грануляций.
Последняя явка на 28-й день - рана активно гранулирует, чистая.
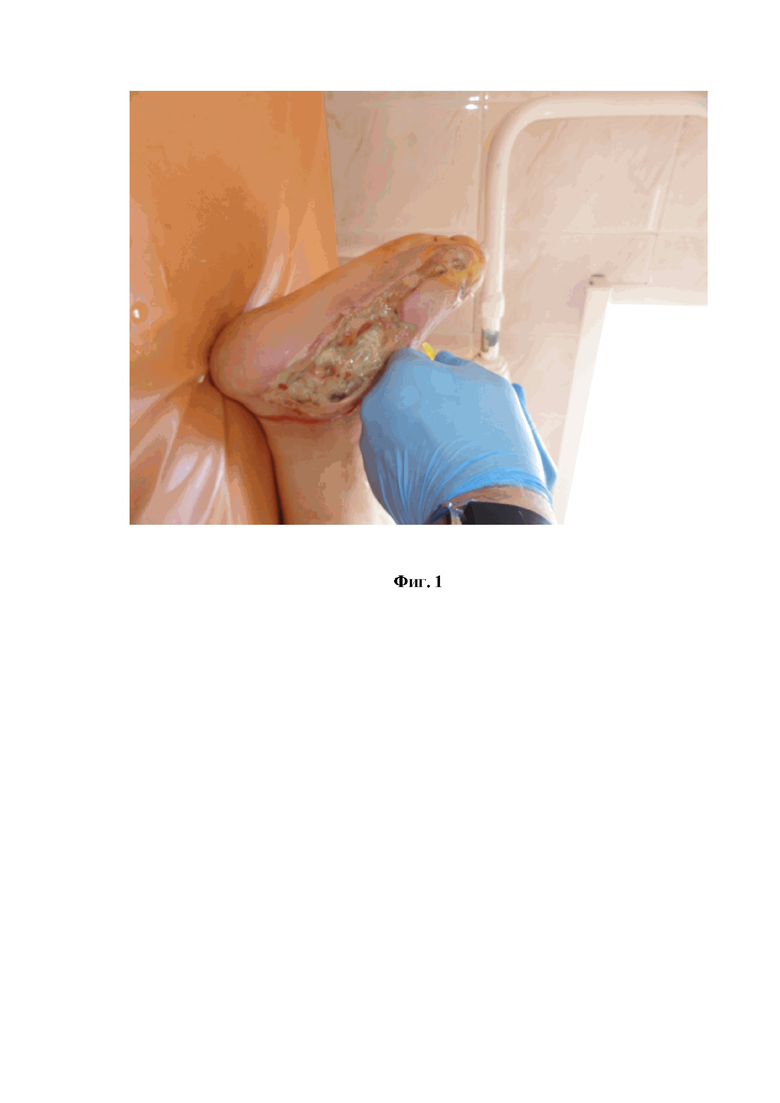
На фиг.1 представлен процесс введения аутоплазмы пациенту А. (1 день).
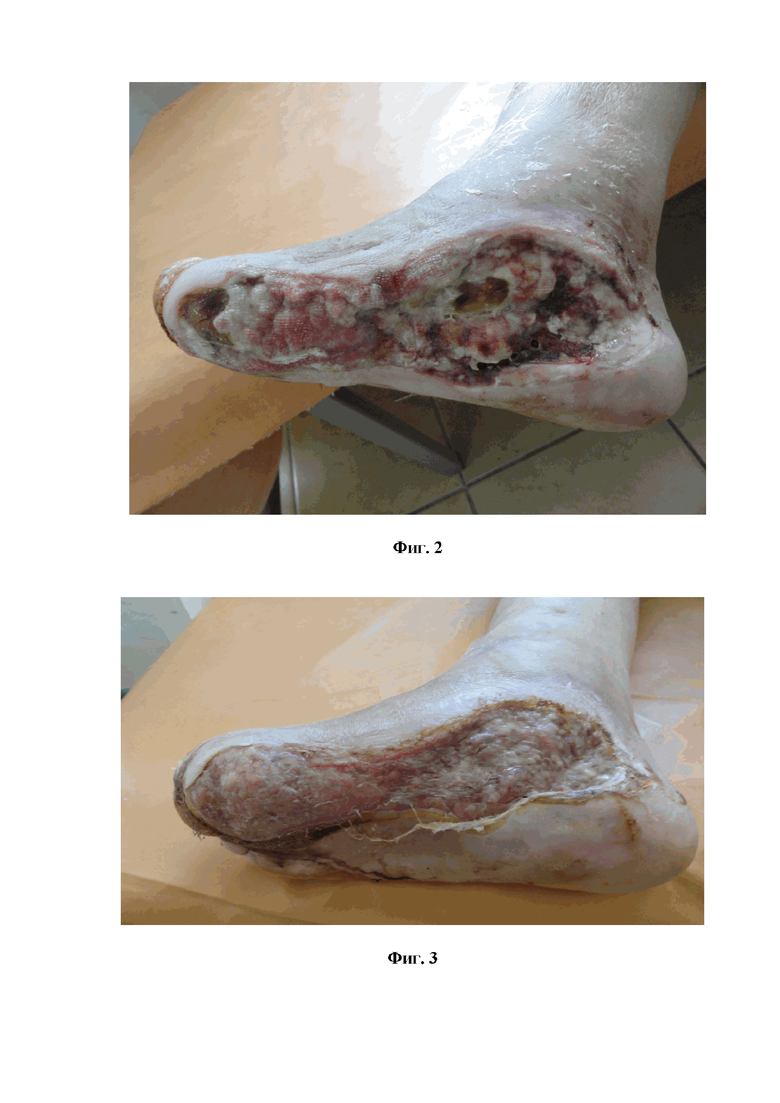
На фиг.2 представлен внешний вид раны пациента А. (6 день).
На фиг.3 представлен внешний вид раны пациента А. после пересадки кожного лоскута. (48 день).
Таким образом, решается техническая задача - ускорение заживления раневых дефектов за счет воздействия на гуморальные и клеточные факторы иммунного ответа и воздействие на процессы репаративной регенерации.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ лечения острого простатита с использованием тромбоцитарной аутоплазмы | 2024 |
|
RU2823476C1 |
| Способ местного лечения трофических язв венозной этиологии | 2016 |
|
RU2639123C1 |
| Способ лечения острого орхоэпидидимита с использованием тромбоцитарной аутоплазмы | 2024 |
|
RU2819996C1 |
| Способ регионального лечения трофической язвы | 2016 |
|
RU2657806C2 |
| СПОСОБ ПРОФИЛАКТИКИ ПЕРИИМПЛАНТАТНОГО МУКОЗИТА ПРИ ДЕНТАЛЬНОЙ ИМПЛАНТАЦИИ У ПАЦИЕНТОВ С СОПУТСТВУЮЩИМ ПАРОДОНТИТОМ | 2018 |
|
RU2705380C1 |
| СПОСОБ ЭНДОСКОПИЧЕСКОГО ЛЕЧЕНИЯ ГАСТРОДУОДЕНАЛЬНЫХ ЯЗВ | 2016 |
|
RU2644934C1 |
| Способ лечения трофических нарушений кожи у пациентов с тяжелым поражением головного мозга | 2020 |
|
RU2752747C1 |
| СПОСОБ ЛЕЧЕНИЯ ДЕФЕКТОВ КОЖИ И МЯГКИХ ТКАНЕЙ У БОЛЬНЫХ САХАРНЫМ ДИАБЕТОМ И СПОСОБ ВВЕДЕНИЯ ПРЕПАРАТА ДЛЯ НЕГО | 2017 |
|
RU2679449C1 |
| Способ лечения хронических ран | 2016 |
|
RU2627814C1 |
| СПОСОБ АУТОДЕРМОПЛАСТИКИ | 2022 |
|
RU2805189C1 |
Изобретение относится к медицине и может найти применение в урологии для лечения пациентов с хроническими ранами. Способ включает антибактериальную и регенерационную терапию раневого процесса. Дополнительно производят введение аутоплазмы, обогащенной тромбоцитами, при этом для получения аутоплазмы забирают венозную кровь. Затем полученную обогащенную тромбоцитами аутоплазму разделяют на две части, одну из которых в объеме 4 мл смешивают с 3,0 мл биопленки BIOFILM, а оставшуюся часть полученной аутоплазмы, обогащенной тромбоцитами, вводят инъекционной иглой, отступая от края раневого дефекта 6-8 мм, на глубину 8-10 мм с интервалами между вколами 8-10 мм. Затем смесь аутоплазмы и биопленки BIOFILM наносят на поверхность раневого дефекта и закрывают стерильным материалом. Изобретение дает возможность использования собственной плазмы пациента, обогащенной тромбоцитами, для модулирования регенерации пораженных тканей и активации собственных гуморальных и клеточных факторов защиты во время течения воспалительного процесса. 3 ил., 2 пр.
Способ лечения хронических ран с использованием тромбоцитарной аутоплазмы, включающий антибактериальную и регенерационную терапию раневого процесса, отличающийся тем, что дополнительно производят введение аутоплазмы, обогащенной тромбоцитами, при этом для получения аутоплазмы забирают венозную кровь, затем полученную обогащенную тромбоцитами аутоплазму разделяют на две части, одну из которых в объеме 4 мл смешивают с 3,0 мл биопленки BIOFILM, а оставшуюся часть полученной аутоплазмы, обогащенной тромбоцитами, вводят инъекционной иглой, отступая от края раневого дефекта 6-8 мм, на глубину 8-10 мм с интервалами между вколами 8-10 мм, а затем смесь аутоплазмы и биопленки BIOFILM наносят на поверхность раневого дефекта и закрывают стерильным материалом.
| Способ лечения хронических ран | 2016 |
|
RU2627814C1 |
| Способ аутодермопластики расщепленным кожным лоскутом для восстановления кожного покрова при ожогах | 2020 |
|
RU2753136C1 |
| Прибор для определения разрывного усилия, удлинения и утомляемости пряжи | 1929 |
|
SU19835A1 |
| Ванна для восстановления хлоридов меди и благородных металлов | 1928 |
|
SU22893A1 |
| WO 2009152374 A2, 17.12.2009 | |||
| Биопленки: основные методы исследования: учебно-методическое пособие / Марданова А.М | |||
| с соавт | |||
| - Казань: К(П)ФУ, 2016, 42 с | |||
| SLESACZECK T | |||
| et al | |||
| Autologous derived, platelet-rich plasma gel in the treatment of | |||
Авторы
Даты
2025-02-06—Публикация
2024-05-22—Подача