Изобретение относится к фармацевтике и медицине, а именно к способам получения форм 5-фторурацила, которые можно применять в терапии колоректального рака.
Колоректальный рак – третье по распространенности онкологическое заболевание в мире, на долю которого приходится порядка 10% всех случаев онкологических заболеваний, и вторая по значимости причина смертности от онкологических заболеваний во всем мире [Ansa B.E., Coughlin S.S., Alema-Mensah E. et al. Evaluation of Colorectal Cancer Incidence Trends in the United States (2000-2014). // J Clin Med. – 2018. – Vol.7. – №:22. – P. 310-321.]. Колоректальный рак чаще всего обнаруживается на II или III стадии [Siegel RL, Miller KD, Goding Sauer A, Fedewa SA, Butterly LF, Anderson JC, Cercek A, Smith RA, Jemal A. Colorectal cancer statistics, 2020. CA Cancer J Clin. 2020 May;70(3):145-164. doi: 10.3322/caac.21601. Epub 2020 Mar 5. PMID: 32133645]. Для пациентов, имеющих высокий риск развития заболевания (IIB стадия), рекомендуется использование адъювантной химиотерапии. Она назначается в дополнение к первичному лечению методом хирургического вмешательства с целью предотвратить повторное развитие опухоли. Химиотерапия заключается во внутривенном приеме оксалиплатина и 5–фторурацила с лейковорином. Такая комбинация препаратов известна как FOLFOX. Химиотерапия назначается на 6 месяцев [Федянин М.Ю., Гладков О.А., Гордеев С.С., Карачун А.М., Козлов Н.А., Мамедли З.З. и соавт. Практические рекомендации по лекарственному лечению рака ободочной кишки, ректосигмоидного соединения и прямой кишки. Злокачественные опухоли: Практические рекомендации RUSSCO #3s2, 2022 (том 12). 401–454].
Среди химиотерапевтических соединений 5-фторурацил является одним из наиболее широко используемых для лечения колоректального рака. Вводимый в виде внутривенной инфузии, 5-фторурацил распространяется по всему организму [Glavas Dodov M, Calis S, Crcarevska MS, Geskovski N, Petrovska V, Goracinova K. Wheat germ agglutinin-conjugated chitosan-Ca-alginate microparticles for local colon delivery of 5-FU: development and in vitro characterization. Int J Pharm. 2009 Nov 3;381(2):166-75. doi: 10.1016/j.ijpharm.2009.06.037] и вызывает тяжелые желудочно-кишечные (рвота, тошнота, плохой аппетит), нервные, гематологические, сердечные, дерматологические токсические эффекты [Olukman M, Şanlı O, Solak EK. Release of Anticancer Drug 5-Fluorouracil from Different Ionically Crosslinked Alginate Bead. Journal of Biomaterials and Nanobiotechnology, Vol.3 No.4, 2012].
Доставка 5-фторурацила в кишечник может уменьшить системные побочные эффекты и обеспечить более эффективную терапию колоректального рака. Достижение оптимальной концентрации непосредственно в опухолевом очаге может уменьшить дозу и продолжительность терапии по сравнению с лечением инъекционной лекарственной формой 5-фторурацила [Rahman Z, Kohli K, Khar RK, Ali M, Charoo NA, Shamsher AA. Characterization of 5-fluorouracil microspheres for colonic delivery. AAPS PharmSciTech. 2006 May 26;7(2):E47. doi: 10.1208/pt070247]. Поэтому разработка пероральной формы 5-фторурацила, обеспечивающей его доставку в кишечник, является актуальной задачей фармацевтики.
В настоящее время отсутствуют пероральные формы 5-фторурацила. Это связано с тем, что 5-фторурацил при первом прохождении через печень при пероральном приеме характеризуется высоким метаболизмом (>80%), что приводит к снижению его эффективной концентрации до момента достижения кишечника, где сосредоточен опухолевый процесс [Das M, Ghosh B, Sen S, Ghosh LK. Formulation and Optimization of Controlled Release 5-Fluorouracil Tablets for Colonic Delivery. J Young Pharm. 2017;9(2):192-6].
Задачей изобретения является получение новой пероральной формы 5-фторурацила для терапии колоректального рака, обеспечивающей уменьшение системных побочных эффектов и локализацию 5-фторурацила в очаге поражения.
Техническим результатом является получение пероральной формы 5-фторурацила (гранулят), которая является кишечнорастворимой.
Технический результат достигается способом получения, характеризующимся тем, что 1% раствор альгината натрия смешивают с 5-фторурацилом по типу суспензии в соотношение 13:1 и стабилизируют полисорбатом-80; затем смесь добавляют каплями в 10% водный раствор хлорида кальция с добавлением 0,2% полисорбата-80; полученные микрокапсулы отфильтровывают, высушивают в сухожаровом шкафу при температуре 60°С до постоянной массы, измельчают и смешивают с наполнителем; полученную порошковую смесь подвергают грануляции в присутствии 30% водной дисперсии сополимера метакриловой кислоты и этилакрилата 1:1, содержащей 1% поливинилпирролидона, 0,7% лаурилсульфата натрия и 2,3% полисорбата-80 в качестве эмульгаторов; протирают через сито, высушивают до постоянной массы и покрывают составом 15% водной дисперсии сополимера метакриловой кислоты и этилакрилата 1:1, содержащей 0,35% лаурилсульфата натрия и 1,15% полисорбата-80 в качестве эмульгаторов.
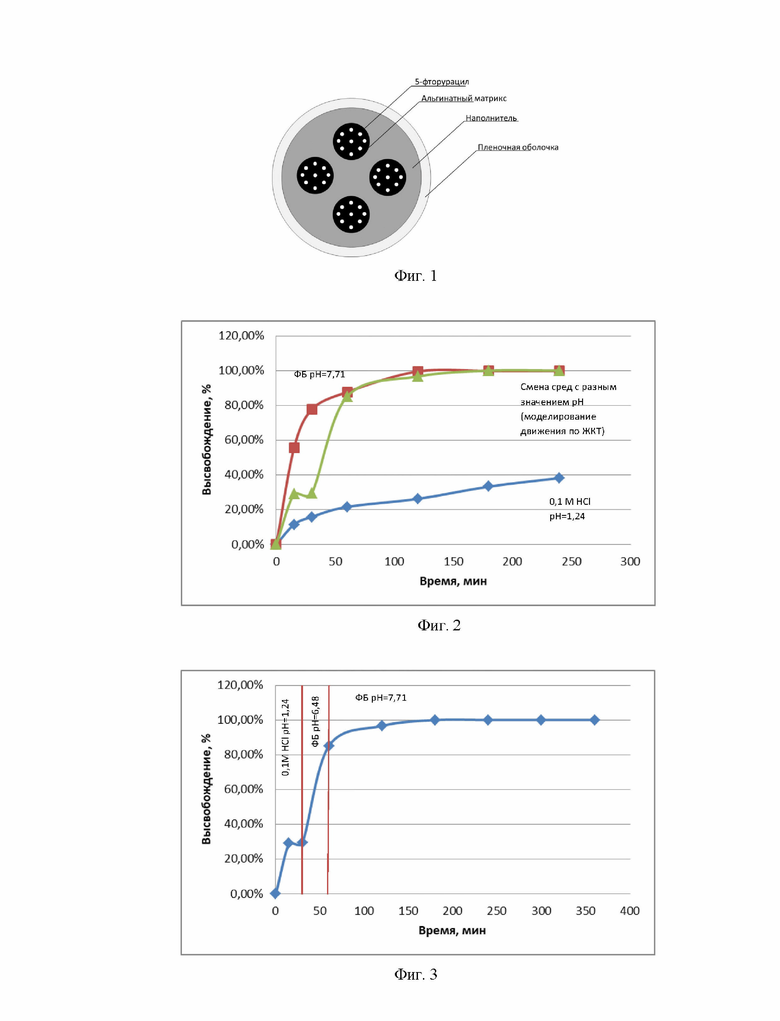
Способ поясняется графическими материалами, где на фиг. 1 представлена схема кишечнорастворимой гранулы 5-фторурацила, полученной по предложенному способу; на фиг. 2 представлена кинетика высвобождения 5-фторурацила из пероральной формы в различных средах; на фиг. 3 представлена кинетика высвобождения 5-фторурацила из пероральной формы в средах, моделирующих среды желудочно-кишечного тракта.
Способ осуществляют следующим образом:
1% раствор альгината натрия смешивают с 5-фторурацилом по типу суспензии в соотношение 13:1 и стабилизируют полисорбатом-80. Полученную смесь добавляют каплями в 10% водный раствор хлорида кальция с добавлением 0,2% полисорбата-80 до образования микрокапсул (около 5 минут). Полученные микрокапсулы отфильтровывают. Затем микрокапсулы сушат в сухожаровом шкафу при температуре 60°С до постоянной массы. Высушенные микрокапсулы механически измельчают. После измельчения смешивают с фармацевтически приемлемым наполнителем. Затем полученную порошковую смесь подвергают грануляции в присутствии 30% водной дисперсии сополимера метакриловой кислоты и этилакрилата, взятых в соотношении 1:1, содержащей 1% поливинилпирролидона, 0,7% лаурилсульфата натрия и 2,3% полисорбата-80 в качестве эмульгаторов, и протирают через сито. Полученный гранулят сушат до постоянной массы. Полученные гранулы обкатывают в дражировочном котле и покрывают составом 15% водной дисперсии сополимера метакриловой кислоты и этилакрилата, взятых в соотношении 1:1, содержащей 0,35% лаурилсульфата натрия и 1,15% полисорбата-80 в качестве эмульгаторов.
По предложенному способу, используя в качестве наполнителя сахароза-крахмал 1:2, и сито с сеткой диаметром 1,25 мм были получены гранулы белого цвета диаметром 1,25 мм. Состав компонентов масс.%: гранул (фиг. 1) следующий: 5-фторурацил - 12,00%; соли альгиновой кислоты - 1,60%; наполнитель - 84,40%; пленочная оболочка из сополимера метакриловой кислоты и этилакрилата 1:1, содержащая 0,35% лаурилсульфат натрия и 1,15% полисорбата-80 - 2,00%.
У полученных гранул проверена способность растворения при различных рН. Полученный по предложенному способу гранулят 5-фторурацила частично подвергается разрушению при рН=1,24, что соответствует среде желудка, (высвобождается 29% 5-фторурацила через 30 минут и выходит на плато при данном значение pH) и легко разрушается при рН=7,71, что соответствует среде толстого кишечника, (высвобождается 78% 5-фторурацила за 30 минут и 100% 5-фторурацила через 2 часа). Полученные данные подтверждают возможность доставки 5-фторурацила в кишечник при пероральном применении полученной формы.
Кинетика высвобождения 5-фторурацила из полученного гранулята была оценена in vitro в условиях, моделирующих биологические среды желудочно-кишечного тракта (ЖКТ).
Для моделирования среды желудка использовалась 0,1 М хлористоводородная кислота с pH=1,24; среды тонкой кишки - фосфатный буферный раствор с рН=6,48; среды толстой кишки - 0,1 М фосфатный буферный раствор с pH=7,71.
Время отбора проб:
0,1М хлористоводородная кислота (0,1 M HCl рН=1,24) - 15 минут; 30 минут.
Фосфатный буферный раствор с рН=6,48 (ФБ рН=6,48) - 30 минут; 60 минут
0,1 М фосфатный буферный раствор с pH=7,71 (ФБ рН=7,71) - 60 минут; 120 минут; 180 минут; 240 минут.
Оценка высвобождения 5-фторурацила из гранулята проводилась путем смены сред, различающихся значением рН (моделирование продвижение гранулята при пероральном приеме по ЖКТ). Смена сред осуществлялась следующим образом: 30 минут гранулы находились в среде с рН 1,24 (имитация среды желудка); затем 60 минут – в среде с рН 6,48 (имитация среды тонкого кишечника); и 240 минут – в среде с рН 7,71 (имитация среды толстого кишечника).
Количественное определение высвобождения 5-фторурацила проводилось методом УФ-спектрометрии при длине волны 265 нм, в кварцевой кювете с толщиной слоя 10 мм при разведении в 10 раз. Данные получали на приборе UV-Vis спектрофотометр UV-1800 («Shimadzu», Япония). Результаты количественного определения 5-фторурацила представлены на фиг. 2 и фиг. 3.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПЕРОРАЛЬНЫЕ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ МЕСАЛАЗИНА | 2017 |
|
RU2744576C2 |
| ПОКРЫВАЮЩАЯ КОМПОЗИЦИЯ, ПОДХОДЯЩАЯ ДЛЯ ФАРМАЦЕВТИЧЕСКИХ ИЛИ НУТРИЦЕВТИЧЕСКИХ ЛЕКАРСТВЕННЫХ ФОРМ | 2011 |
|
RU2599023C2 |
| ЖЕЛУДОЧНО-РЕЗИСТЕНТНАЯ ФАРМАЦЕВТИЧЕСКАЯ ИЛИ НУТРИЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С УСТОЙЧИВОСТЬЮ К ВОЗДЕЙСТВИЮ ЭТАНОЛА | 2012 |
|
RU2649806C2 |
| СОДЕРЖАЩИЙ ФАРМАЦЕВТИЧЕСКИЙ АГЕНТ СОСТАВ С ПОКРЫТИЕМ | 2004 |
|
RU2372893C2 |
| ВВОДИМАЯ ПЕРОРАЛЬНО ФАРМАЦЕВТИЧЕСКАЯ ГРАНУЛА ЭПИДЕРМАЛЬНОГО ФАКТОРА РОСТА | 2011 |
|
RU2540503C2 |
| ПЕЛЛЕТЫ ХОЛЕСТИРАМИНА, ПЕРОРАЛЬНЫЕ КОМПОЗИЦИИ ХОЛЕСТИРАМИНА И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2782016C2 |
| ПЕРОРАЛЬНЫЙ СОСТАВ ХОЛЕСТИРАМИНА И ЕГО ПРИМЕНЕНИЕ | 2017 |
|
RU2750937C2 |
| ПЕРОРАЛЬНЫЙ СОСТАВ ХОЛЕСТИРАМИНА И ЕГО ПРИМЕНЕНИЕ | 2017 |
|
RU2750944C2 |
| ПРЕПАРАТ АКТИВАТОРА ГЛЮКОКИНАЗЫ ДЛЯ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2017 |
|
RU2728824C1 |
| ПЕРОРАЛЬНЫЕ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НИКОТИНАМИДА | 2017 |
|
RU2738114C2 |
Настоящее изобретение относится к способу получения кишечнорастворимой пероральной формы 5-фторурацила, характеризующемуся тем, что 1% раствор альгината натрия смешивают с 5-фторурацилом по типу суспензии в соотношении 13:1 и стабилизируют полисорбатом-80; смесь добавляют каплями в 10% водный раствор хлорида кальция с добавлением 0,2% полисорбата-80; полученные микрокапсулы отфильтровывают, высушивают в сухожаровом шкафу при температуре 60°С до постоянной массы, измельчают и смешивают с наполнителем, в качестве которого используют сахарозу-крахмал в соотношении 1:2; полученную порошковую смесь подвергают грануляции в присутствии 30% водной дисперсии сополимера метакриловой кислоты и этилакрилата 1:1, содержащей 1% поливинилпирролидона, 0,7% лаурилсульфата натрия и 2,3% полисорбата-80 в качестве эмульгаторов, протирают через сито, высушивают до постоянной массы и покрывают составом 15% водной дисперсии сополимера метакриловой кислоты и этилакрилата 1:1, содержащей 0,35% лаурилсульфата натрия и 1,15% полисорбата-80 в качестве эмульгаторов. Настоящее изобретение обеспечивает получение пероральной формы 5-фторурацила (гранулят), которая является кишечнорастворимой. 3 ил.
Способ получения кишечнорастворимой пероральной формы 5-фторурацила, характеризующийся тем, что 1% раствор альгината натрия смешивают с 5-фторурацилом по типу суспензии в соотношении 13:1 и стабилизируют полисорбатом-80; смесь добавляют каплями в 10% водный раствор хлорида кальция с добавлением 0,2% полисорбата-80; полученные микрокапсулы отфильтровывают, высушивают в сухожаровом шкафу при температуре 60°С до постоянной массы, измельчают и смешивают с наполнителем, в качестве которого используют сахарозу-крахмал в соотношении 1:2; полученную порошковую смесь подвергают грануляции в присутствии 30% водной дисперсии сополимера метакриловой кислоты и этилакрилата 1:1, содержащей 1% поливинилпирролидона, 0,7% лаурилсульфата натрия и 2,3% полисорбата-80 в качестве эмульгаторов, протирают через сито, высушивают до постоянной массы и покрывают составом 15% водной дисперсии сополимера метакриловой кислоты и этилакрилата 1:1, содержащей 0,35% лаурилсульфата натрия и 1,15% полисорбата-80 в качестве эмульгаторов.
| Harpreet Kaur et al., Enteric coated 5-fluorouracil capsules designed to achieve intestinal targeting / International journal of pharmaceutical, chemical and biological sciences, 2013, Vol.3, N.4, pp.1215-1223 | |||
| Shashank Tummala et al., 5-Fluorouracil enteric-coated nanoparticles for improved apoptotic activity and therapeutic index in treating |
Авторы
Даты
2025-02-14—Публикация
2023-11-16—Подача