Изобретение относится к медицине, в частности к онкологии и торакальной хирургии.
В настоящий момент существует десятки вариантов формирования дигестивного анастомоза после гастрэктомии в том числе с резекцией дистальной части пищевода для достижения R0 резекции. Однако выбор оптимального метода анастомозирования остается дискутабельным ввиду существующих проблем в виде несостоятельности и неудовлетворительными факторами в отдаленный период (рефлюкс, стеноз) [1]. Наиболее изученными и широко используемыми в клинической практике является формирование анастомоза по М.И. Давыдову [2]. Альтернативным вариантом формирования анастомоза является механический способ, но, несмотря на его «простоту» формирования, существуют лимитирующие факторы в его повсеместном использовании.
При восстановлении желудочно-кишечного тракта, анастомоз в большинстве случаев формируют между пищеводом и сформированной Ру-петлей.
Грозным осложнением после гастрэктомии является несостоятельность пищеводно-тонкокишечного (или пищеводно-коло) анастомоза [3]. Частота несостоятельности варьирует по данным отечественных и зарубежных авторов от 4-10% [4,5,6]. Летальность по данным систематического обзора Aurello P. et.al. составляет 26,6% [6]. Несостоятельность анастомоза после эзофагэктомии может привести к увеличению продолжительности интенсивной терапии и пребывания в стационаре, в том числе в отделении реанимации и интенсивной терапии (ОРИТ), значительным затратам лечения, увеличению послеоперационной смертности и снижению качества жизни, учитывая потенциальную стриктуру после несостоятельности [7].
Факторами риска несостоятельности анастомоза по данным ретроспективного обзора 3827 пациентов в одном онкологической центре с большим объемом операций на желудке показал, что мужской пол (Р=0,001), предоперационное/интраоперационное переливание крови (Р<0,001), наличие сердечно-сосудистых заболеваний (Р=0,023) и расположение опухоли (в кардиальном отделе) (Р<0,001) являются предикторами несостоятельности анастомоза. [8].
С целью повышения безопасности и успешного функционального результата хирурги многих поколений стремились к улучшению методик формирования анастомоза. Путем решения проблем, возникающих при формировании анастомоза, создавались подходы, позволяющие их или полностью, или частично нейтрализовать.
Таким образом, проблема несостоятельности анастомоза после гастрэктомии и резекции пищевода является актуальной, несмотря на усовершенствование хирургических методик, и шовного материала.
При систематическом поиске среди источников нами не найдено упоминаний о применении предложенного нами способа формирования анастомоза.
Известен способ формирования инвагинационного эзофагоеюноанастомоза по К. Н. Цацаниди (1962): «пересеченную и мобилизованную петлю кишки проводят через окно в брыжейке поперечноободочной кишки. Через кишку проводят две кетгутовые нити и выводят их на расстоянии 15 см от орального края кишки. При гастроеюнопластике их проводят через просвет кишки. Накладывают шов на заднюю губу анастомоза. Концами ранее проведенных кетгутовых нитей прошивают с двух сторон через все слои пищевод с кишкой. Нити завязывают. Сшивают переднюю стенку анастомоза узелками внутрь. Потягивая кетгутовые нити и надвигая кишку на пищевод, инвагинируют его в просвет кишки на глубину 2 см. Спереди и сзади накладывают по 3-4 поддерживающих шва между пищеводом и кишкой. Кишку у анастомоза фиксируют к диафрагмально-пищеводному листку брюшины. Кетгутовые нити срезают, место прокола ушивают» [9].
Недостатком данного метода является формирование анастомоза «конец в конец», что технически более сложно, чем «конец в бок». Также формирование второго ряда швов осуществляется путем узловых швов, что может вызвать их прорезывание в адвентициальном слое пищевода. Фиксацию к диафрагме в настоящее время является спорным вопросом, так как диафрагма является подвижным органом, и может вызвать отрыв сформированных швов между областью анастомоза и диафрагмой с последующей несостоятельностью.
Техническим результатом предлагаемого решения является создание эффективного и безопасного анастомоза, который обладает надежностью и удовлетворительными функциональными результатами.
Указанные технические и лечебные результаты при осуществлении изобретения достигаются за счет того, что также как и в известном способе выполняют формирование анастомоза после гастрэктомии, в нашем случае формирование анастомоза также возможно при гастрэктомии с резекцией пищевода при умеренном натяжении тканей.
Особенность заявленного способа заключается в том, что выполняется формирование Ру-петли, петля тощей кишки пересекается в 20-25 см от связки Трейца. Далее исходя из архитектоники формируется мобильная Ру-петля длинной 60 см. После выбора уровня длины кишки формируется межкишечный анастомоз «бок в бок».
При отсечении желудка от пищевода накладывается зажим Сатинского на пищевод. Пищевод пересекается сначала циркулярно: адвентиция и мышечный слой, далее после его сокращения отсекается одним движением подслизисто-слизистый слой.
Далее Ру-петлю проводят через мезоколон в бессосудистой зоне. Начинается формирование эзофагоэнтероанастомоза.
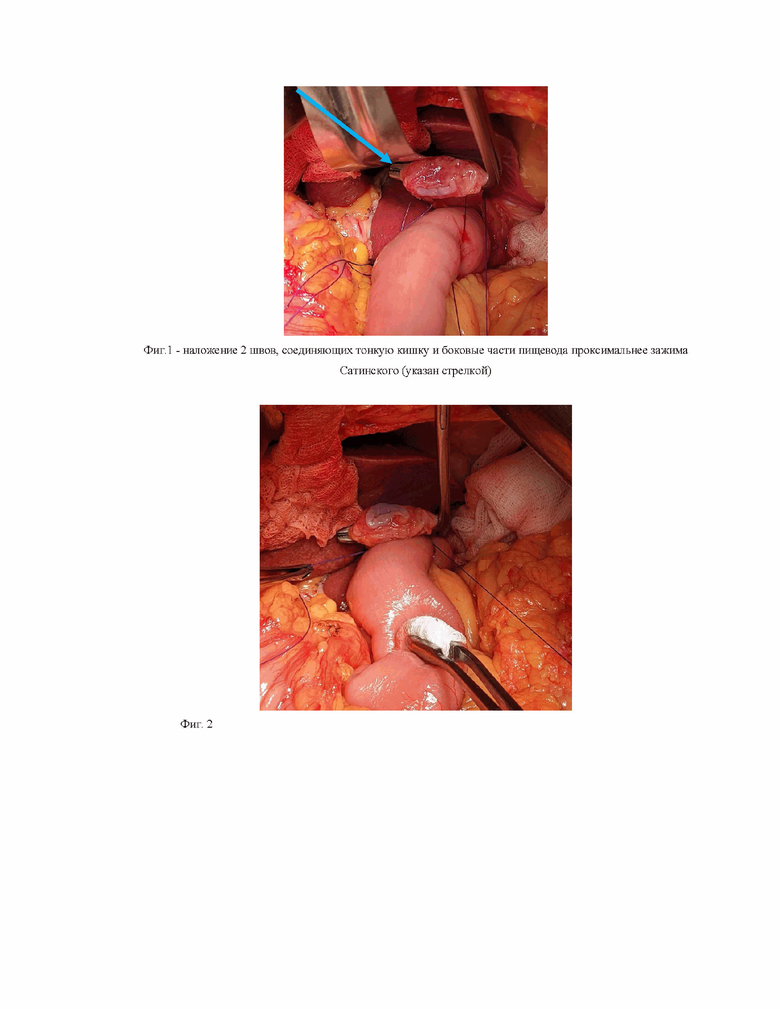
На расстоянии 2-3 см заглушенной части тонкой кишки накладываются 2 шва, соединяющие тонкую кишку и боковые части пищевода проксимальнее зажима Сатинского (фиг.1). После затягивания нитей (фиг. 2).
В 3-4 мм от линии первого ряда делается рассечение передней (противобрыжеечной) стенки тонкой кишки размером около 5-7 мм (фиг. 3).
Далее формируется второй ряд задней губы анастомоза путем наложения 5 узловых швов через все слои. Вкол иглы осуществляется со стороны слизистой оболочки тонкой кишки, выкол со стороны слизистой оболочки пищевода. Первый вкол по краям кишки осуществляется за латеральный «угол» отверстия. Таким образом, все узлы располагаются в просвете кишки (фиг. 4).
Далее после затягивая всех нитей второго ряда задней губы анастомоза формируются два шва, которые являются «переходными» между задней и передней стенкой анастомоза. Вкол иглы осуществляется со стороны слизистой тонкой кишки, выкол также со стороны слизистой пищевода (фиг. 5).
После затягивания этих двух «переходных» узлов начинается формирование передней стенки анастомоза. Каждый вкол осуществляется со стороны серозной оболочки тонкой кишки, игла выкалывается у самого края слизистой кишки, чтобы исключить транспозицию слизистой в «стык» пищевода и кишки. Далее вкол иглы осуществляется со стороны слизистой оболочки пищевода в 2-3 мм от края, и движением вверх слизистая пищевода сдвигается проксимальнее по пищеводу, и далее осуществляется выкол со стороны адвентиции (фиг. 6). Обычно достаточно 3-4 швов. Швы сразу не затягиваются, а берутся на держалку. Перед затягиванием осуществляется заведение за анастомоз на 3-4 см назоинтестинального зонда, 24-26 Fr. После чего нити на зонде затягиваются.
После этого начинается инвагинация области анастомоза путем салазоочных П-образных швов. Первый стежок формируется со стороны серозы тонкой кишки параллельно оси тонкой кишки, второй стежок перпендикулярно оси пищевода, и третий стежок снова делается параллельно оси тонкой кишки. Нити по очереди затягиваются, если имеются технические сложности с эффективным затягиваем, целесообразно для погружения, слегка осуществляя давление на анастомоз, помочь погрузиться линии анастомоза под салазочный П-образный шов (фиг. 7),
После проверки на герметичность назоинтестинальный зонд удаляется.
Предлагаемый вариант позволяет обеспечить простой в исполнении, герметичный и тем самым безопасный анастомоз.
Изобретение поясняется подробным описанием, клиническими примерами и иллюстрациями.
По данной методике формирование анастомоза выполнено у 80 пациентов за 2018-2023 год, ни у одного пациента не зарегистрирована несостоятельность анастомоза. У всех пациентов было выполнено с целью исключения субклинической несостоятельности компьютерная томография с пероральным контрастированием.
Клинический пример 1.
Больной А, 59 лет. В 10.2020 году госпитализирован в хирургическое торакальное отделение ГУЗ ОКОД г. Ульяновска, с диагнозом: рак кардиального отдела желудка cT3N0M0 ПВ стадии, состояние после диагностической лапароскопии, 4 курсов XT по схеме FLOT. В плановом порядке 19.10.2020: лапаротомия, гастрэктомия с резекцией абдоминального сегмента пищевода, лимфодиссекция D2.
При контрольном осмотре на 7 сутки, признаков несостоятельности нет по данным контрольного рентгенологического исследования, анастомоз выше диафрагмы, без признаков несостоятельности. На 10 сутки после операции пациент выписан с выздоровлением.
Дополнительно для демонстрации функциональных результатов, пациенту выполнена рентгенографии пищевода с BaSo4 Per os через 3 месяца после операции, при исследовании контраст свободно проходим по пищеводу, пищевод не расширен, анастомоз проходим, при глубоком вдохе рефлюкса бариевой взвести в пищевод не происходит. Фиг. 8. Фотоиллюстрация (рентгенография): стрелкой отмечен анастомоз.
Возможное использование в клинической практике заявляемого способа позволяет снизить риск несостоятельности дигестивного анастомоза после гастрэктомии и резекции пищевода, и обеспечивает удовлетворительные функциональные результаты в отдаленный период. Таким образом, заявленный способ позволяет:
• Выполнить безопасный дигестивный анастомоз после гастрэктомии и резекции пищевода
• Предотвратить формирование рефлюкса из просвета кишки в пищевод
Список литературы:
1. Олексенко В.В., Ефетов С.В., Захаров В.А., Щербаков Г.В. Профилактика рефлюкс-эзофагита после гастрэктомии. Хирургия. Журнал им. Н.И. Пирогова. 2015;(3):42-47.
2. Давыдов, М.И. Энциклопедия хирургии рака желудка / М.И. Давыдов, И.Н. Туркин, М.М. Давыдов. - М.: ЭКСМО, 2011.-536 с.
3. Черноусов А.Ф. Хирургия рака желудка /А.Ф. Черноусое, С.А. Поликарпов, Ф.А. Черноусов. М.: Москва, 2004. 560 с.
4. Ранние осложнения после гастрэктомии с однорядным эзофагоэнтероанастомозом / Ф.Ш. Ахметзянов, P.P. Гайнаншин, Ф.Ф. Ахметзянова [и др.] // Вестник современной клинической медицины. -2020.-Т. 13,вып.3. - С.7-14. DOI: 10.20969/VSKM.2020.13(3).7-14.
5. Результаты лечения больных с несостоятельностью пищеводно-тонкокишечного анастомоза после открытых и лапароскопических гастрэктомий / И. Е. Седаков, О. В. Совпель, И. В. Румянцева [и др.] // Новообразование.-2019.-Т. 11, №4(27). - С.128-131.
6. Aurello Р, Magistri Р, D'Angelo F, Valabrega S, Sirimarco D, Tiemo SM, Nava AK, Ramacciato G. Treatment of esophagojejunal anastomosis leakage: a systematic review from the last two decades. Am Surg. 2015 May;81(5):450-3.
7. Makuuchi R, Irino T, Tanizawa Y, Bando E, Kawamura T, Terashima M. Esophagojejunal anastomotic leakage following gastrectomy for gastric cancer. Surg Today. 2019 Mar;49(3): 187-196. doi: 10.1007/s00595-018-1726-8.
8. Kim SH, Son SY, Park YS, Ann SH, Park DJ, Kim HH. Risk Factors for Anastomotic Leakage: A Retrospective Cohort Study in a Single Gastric Surgical Unit. J Gastric Cancer. 2015 Sep; 15(3): 167-75. doi: 10.5230/jgc.2015.15.3.167
9. Цацаниди K.H. Пищеводно-кишечные и пищево дно-желудочные анастомозы / K.H. Цацаниди, А.В. Богданов М.: Медицина, 1969. 170 с.



Изобретение относится к медицине, а именно к абдоминальной хирургии, гастроэнтерологии. Формируют Ру-петлю длиной 60 см и межкишечный анастомоз «бок в бок». При отсечении желудка от пищевода накладывают зажим Сатинского на пищевод. Пересекают циркулярно адвентицию и мышечный слой пищевода, после его сокращения отсекают одним движением подслизисто-слизистый слой. Ру-петлю проводят через мезоколон в бессосудистой зоне. Накладывают 2 шва, соединяя тощую кишку и боковые части пищевода. Проксимальнее зажима рассекают переднюю стенку тощей кишки. Формируют второй ряд швов задней губы анастомоза путем наложения узловых швов через все слои так, чтобы узлы были расположены в просвете кишки. Формируют два переходных шва между задней и передней губой анастомоза. Формируют переднюю губу анастомоза, вкол осуществляют со стороны серозной оболочки тощей кишки, иглу выкалывают у края слизистой кишки, далее вкол иглы осуществляют со стороны слизистой оболочки пищевода, а выкол - со стороны адвентиции. Накладывают салазочные П-образные швы и инвагинируют область анастомоза. Способ позволяет снизить риск несостоятельности дигестивного анастомоза после гастрэктомии и резекции пищевода, обеспечивает удовлетворительные функциональные результаты в отдаленный период, предотвращает формирование рефлюкса из просвета кишки в пищевод. 8 ил., 1 пр.
Способ формирования дигестивного анастомоза после гастрэктомии и резекции пищевода, отличающийся тем, что петлю тощей кишки пересекают в 20-25 см от связки Трейца, формируют Ру-петлю длиной 60 см и межкишечный анастомоз «бок в бок»; при отсечении желудка от пищевода накладывают зажим Сатинского на пищевод, пересекают циркулярно адвентицию и мышечный слой пищевода, далее после его сокращения отсекают одним движением подслизисто-слизистый слой, Ру-петлю проводят через мезоколон в бессосудистой зоне; нитью на атравматической игле накладывают 2 шва, соединяя тощую кишку и боковые части пищевода, проксимальнее зажима в 3-4 мм от линии первого ряда швов переднюю стенку тощей кишки рассекают на протяжении 5-7 см; формируют второй ряд швов задней губы анастомоза путем наложения 5 узловых швов через все слои так, чтобы узлы были расположены в просвете кишки; затем формируют два переходных шва между задней и передней губой анастомоза; формируют переднюю губу анастомоза, вкол осуществляют со стороны серозной оболочки тощей кишки, иглу выкалывают у края слизистой кишки, далее вкол иглы осуществляют со стороны слизистой оболочки пищевода, а выкол - со стороны адвентиции, заводят назоинтестинальный зонд за анастомоз на 3-4 см и затягивают нити, накладывают салазочные П-образные швы и инвагинируют область анастомоза, проверяют на герметичность и удаляют назоинтестинальный зонд.
| СПОСОБ ЭЗОФАГОЕЮНОСТОМИИ ПРИ ГАСТРЭКТОМИИ И РЕЗЕКЦИИ ПИЩЕВОДА | 1998 |
|
RU2180192C2 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РЕФЛЮКС-ЭЗОФАГИТА ПРИ ОПЕРАЦИИ РЕКОНСТРУКТИВНОЙ ЕЮНОГАСТРОПЛАСТИКИ ПОСЛЕ ГАСТРЭКТОМИИ | 1999 |
|
RU2148958C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭРИТРЕНА | 1915 |
|
SU1102A1 |
| JP 3150576 U, 21.05.2009 | |||
| Зубков Р.А | |||
| и др | |||
| Лапароскопическая гастрэктомия с еюногастропластикой | |||
| Сибирский онкологический журнал, 2016, 15 (4), с.70-74 | |||
| XING J | |||
| et al | |||
| Приспособление с иглой для прочистки кухонь типа "Примус" | 1923 |
|
SU40A1 |
Авторы
Даты
2025-03-13—Публикация
2024-04-22—Подача