Изобретение относится к медицине, а именно к хирургии, и может быть использовано для лечения злокачественных новообразований желудка.
Несомненным прогрессом абдоминальной хирургии и онкологии следует считать повсеместное снижение послеоперационной летальности и осложнений после гастрэктомии. Тем не менее, актуальность проблемы остается высокой ввиду неудовлетворительного качества жизни оперированных больных, развития у них патологических синдромов, связанных с утратой важных морфо-функциональных структур и развитием эвакуаторных нарушений. Из большого многообразия существующих методов формирования пищеводно-кишечных соустий большинством авторов в настоящее время используются муфтообразные, инвагинационные и резервуарные анастомозы. Особенностью муфтообразного пищеводно-кишечного анастомоза является то, что линию шва герметизируют подготовленным для этой цели участком тощей кишки. Указанный технический прием, выполняемый в различных модификациях, позволяет сформировать соустье в виде муфты, обладающее повышенной механической прочностью за счет увеличения площади соприкосновения стенок соединяемых органов. Авторы, располагающие большим опытом выполнения гастрэктомии, отмечают удовлетворительные функциональные свойства муфтообразного пищеводно-тонкокишечного анастомоза у большинства оперированных больных. Однако признаки рефлюкс-эзофагита и демпинг-синдрома после таких операций отмечали соответственно в 2,3% и 31,5% наблюдений [Бондарь Г.В., Думанский Ю.В., Попович А.Ю., Бондарь В.Г. Рак желудка - проблемы и возможности восстановительной хирургии. Журнал АМН Украины 1999; 3: 589-595].
Широкое применение в клинической практике нашли инвагинационные пищеводно-кишечные анастомозы, конструкция которых предусматривает наличие инвагината, создаваемого путем погружения проксимального и дистального соединяемых отрезков в просвет дистального отрезка. При таком сопоставлении соединяемых поверхностей значительно увеличивается площадь соприкосновения и существенно уменьшается нагрузка на линию швов. Сформированный инвагинат выполняет функцию клапана, обладающего антирефлюксными свойствами. Однако наличие пищеводно-тонкокишечного клапана с антирефлюксными свойствами не исключает возникновения функциональных нарушений со стороны инвагинационных анастомозов, при которых рефлюкс-эзофагит и демпинг-синдром наблюдали соответственно у 25,6 - 30,2% и 31,4 - 66,8%, и стриктуру анастомоза - у 10% больных [Жерлов Г.К., Дамбаев Г.Ц., Рыжов А.И., Клоков С.С. Функциональные результаты гастрэктомии, проксимальной резекции желудка у больных раком желудка. В кн.: Органосохраняющие и реконструктивные операции в онкологии. Томск 1991; 58-60].
Наиболее благоприятные функциональные результаты после гастрэктомии получены при выполнении гастропластических операций, предполагающих формирование резервуарных пищеводно-кишечных анастомозов [Жерлов Г.К., Ефименко Н.А., Беляев Л.Б., Кошель А.П., Зыков Д.В., Васильченко М.И., Юдин Е.В. Пути улучшения качества жизни пациентов после гастрэктомии и субтотальной дистальной резекции желудка. Клин. Мед. 2000; 9: 66-68]. После них рефлюкс-эзофагит наблюдается значительно реже, лишь у 3,1-6%, демпинг-синдром - у 3,1-3,6%, агастральная астения - у 3,6% больных, что подчеркивает высокий реабилитационный эффект таких операций [Клименков А.А., Губина Г.И., Бондарь В.Г., Попович А.Ю. Опыт использования муфтообразного пищеводно-кишечного анастомоза при гастрэктомии по поводу рака. Хирургия 1989; 5: 109-112; Патютко Ю.И., Хубиев А.И., Поляков М.И., Кирсанов А.И. Функциональные результаты гастрэктомии, произведенных по поводу рака, в зависимости от метода операции и формирования пищеводно-кишечного анастомоза. Вестн. Хир.. 1989; 11: 23-26].
Исходя из этих данных, исследования, направленные на повышение надежности и функциональности пищеводно-кишечного анастомоза, а также разработку наиболее физиологически обоснованной хирургической технологии восстановления пищеварительного тракта, сохраняют свою высокую актуальность.
Известен способ формирования муфтообразного пищеводно-кишечного анастомоза по В.Г.Бондарю [Бондарь В.Г. Результаты хирургического лечения рака желудка. Клин. хир. 1997; 9-10: 62-64]. После мобилизации желудка из Т-образной петли тощей кишки формируют муфту, которую фиксируют к ножкам диафрагмы с одновременным проведением культи пищевода через канал в муфте. Далее, между пищеводом и стенками муфты накладывают ряд узловых серозно-мышечных швов. Вскрывают просвет отводящей петли в косом направлении на ширину анастомоза и формируют пищеводно-кишечный анастомоз конец в бок узловым швом из рассасывающегося материала. Линия швов герметизируется вторым рядом серозно-серозных швов с использованием приводящего сегмента муфты. Операцию заканчивают наложением межкишечного анастомоза Брауна между приводящим и отводящим отделами тонкой кишки.
При всех достоинствах данной методики и в первую очередь высокой прочности и герметичности данного анастомоза все же следует признать ряд недостатков, с которыми соглашаются сами авторы [Бондарь Г.В., Думанский Ю.В., Попович А.Ю., Бондарь В.Г. Рак желудка - проблемы и возможности восстановительной хирургии. Журнал АМН Украины 1999; 3: 589-595]. Арефлюксные свойства анастомоза не всегда убедительны даже при его безупречном техническом исполнении, что связано с конструктивными особенностями анастомоза. Муфта из тонкой кишки, охватывающая абдоминальный сегмент пищевода, является лишь приближенным подобием сфинктера и единственным препятствием для рефлюкса. Поэтому рефлюкс может реализоваться в условиях возрастающего градиента давления в пищеводе и тонкой кишке, когда антирефлюксных свойств муфты оказывается недостаточно. Другим недостатком методики В.Г.Бондаря является выключение 12-перстной кишки из процесса пищеварения.
Известен способ Шелешко П.В. (1990; Кафедра онкологии Полтавского медицинского стоматологического института). Суть метода заключается в формировании резервуара-двустволки путем изоперистальтического вставления отводящего от пищеводно-кишечного анастомоза сегмента тонкой кишки между пищеводом и 12-перстной кишкой и наложением межкишечного анастомоза между приводящим отделом и приводящей петлей тонкой кишки. Операцию осуществляют следующим образом. После удаления желудка пищевод удерживают изогнутым зажимом. Формируют Т-образную петлю из тощей кишки по аналогии с методикой В.Г.Бондаря. Далее тремя швами Т-образную петлю подшивают к пищеводу у самой диафрагмы и одиночными капроновыми швами, формируют анастомоз между пищеводом и отводящей кишкой. Затем стенку кишки выше этих швов подшивают к пищеводу, а ниже к отводящей петле, по середине края Т-образной петли сшивают между собой. Отводящую петлю подводят к 12-перстной кишке и пересекают. Без натяжения тканей формируют анастомоз между 12-перстной кишкой и проксимальным концом отводящей кишки. Торцевой конец дистальной части отводящей петли ушивают наглухо, брыжейку рассекают вдоль одного из радиальных сосудов. Ушитую кишку несколько низводят и формируют резервуар-двустволку. Для этого ушитую часть отводящей кишки у связки Трейтца сшивают серозно-серозными швами по противобрыжеечному краю с приводящей кишкой на протяжении 16-17 см. Сшитые кишечные петли рассекают электроножом и ушивают непрерывным слизисто-серозным капроновым швом, сверху накладывают ряд серо-серозных швов. Операцию заканчивают ушиванием верхней части «резервуара-двустволки» в окне брыжейки поперечно-ободочной кишки.
Данная методика имеет ряд неоспоримых преимуществ по сравнению с методикой В.Г.Бондаря, поскольку предполагает включение 12-перстной кишки в процесс пищеварения и формирование тонкокишечного резервуара, что позволяет обеспечить более физиологический пассаж кишечного содержимого. Однако при формировании резервуара наносится существенная травма тонкой кишки рассечением ее на протяжении до 17 см. Кроме того, формирование пищеводно-кишечного анастомоза также не устраняет кишечно-пищеводный рефлюкс.
Известен способ формирования арефлюксного пищеводно-кишечного анастомоза, предложенный Гринбергом А.А. и Каном В.И., взятый в качестве прототипа [Гринберг А.А., Кан В.И., Лахтина В.П., Джитава И.Г. Способ инвагинационного арефлюксного пищеводно-кишечного анастомоза. Хирургия, 1994; 4: 55-57].
После мобилизации желудка с сальниками и отсечения от 12-перстной кишки ее культю погружают двумя полукисетными и узловыми швами. На пищевод накладывают зажим Сатинского, заводя его сзади наперед в сагиттальном направлении под углом 60 град. К его продольной оси (Фиг.1.а). Пищевод пересекают под зажимом, желудок с большим сальником и связочным аппаратом удаляют. Находят начальный отдел тощей кишки и пересекают ее аппаратом НЖКА на расстоянии 20-25 см от связки Трейтца. Предварительно для удлинения орального отрезка тощей кишки рассекают в радиальном направлении брюшинные листки брыжейки и пересекают один радиальный сосуд, сохраняя сосудистую дугу.
Закрыв оральный конец пересеченной кишки двумя полукисетными и узловыми швами, формируют Y-образный энтеро-энтероанастомоз по Ру на расстоянии 40-50 см. Последний переводят через отверстие в бессосудистом участке брыжейки поперечно-ободочной кишки в верхний отдел брюшной полости. Сгибают конец отключенной кишки и сшивают по брыжеечному краю серо-серозными швами в виде буквы Т (фрагмент методики В.Г.Бондаря). Длина вертикальной части по брыжеечному краю 6-8 см, ширина горизонтальной части 5-6 см (Фиг.1.б). В косом направлении рассекают электроножом передние стенки сшитых между собой колен кишки. Длина разреза 3 см. Верхняя граница разреза начинается под горизонтальной частью Т и на расстоянии от средней линии 2,5 см, нижняя заканчивается в 1 см от средней линии. Производя этот этап операции, обращают внимание на тщательный гемостаз. Накладывают по два шва с каждой стороны между боковой поверхностью пищевода над зажимом и одним из колен кишки. На кишке серозно-мышечный шов производят между срединной линией и внутренним краем разреза. Расстояние между швами 2 см. Фиксируют пищевод этими швами к Т-образно сшитой кишке (Фиг.1.в.). Снимают зажим Сатинского и вшивают отдельными швами пищевод по всей окружности во внутренние края разрезов. Для этого используют атравматические иглы с нитью №3/0 викрил, пролон или капрон №3. Пищевод и кишку прошивают через все слои (Фиг.1.г.). Переднюю стенку анастомоза начинают формировать снизу, вшивая наружные края разрезов однорядными швами. Имеющийся избыток кишки из горизонтальной части Т используют для формирования кольца муфты вокруг пищевода (Фиг.1.д.).
Недостатками способа являются нефизиологичное пищеварение вследствие выключения 12-перстной кишки из пищеварения и возможность развития демпинг-синдрома и агастральной астении.
Для повышения арефлюксных свойств пищеводно-кишечного анастомоза и уменьшения частоты и тяжести постгастрэктомических расстройств предлагается Т-образную петлю формировать на ушитой отводящей тощей кишке на расстоянии 50-60 см от уровня пересечения, затем пищеводно-тонкокишечный анастомоз формируют, рассекая приводящий и отводящий отделы кишки прилежащей муфты длиной, равной двум ее диаметрам, сшивая узловыми швами по окружности конец пищевода с краями вскрытых прилежащих петель муфты в верхнем отделе, после чего создают клапан, ушивая сверху края рассеченных отделов тонкой кишки на величину диаметра пищеводного отверстия, далее накладывают непрерывный слизисто-серозный шов тонкой кишки ниже сформированного пищеводно-кишечного анастомоза, формируют резервуар в виде кольцевидной приводящей петли тонкой кишки путем наложения межкишечного анастомоза бок в бок между перемещенным ушитым концом приводящего отдела тонкой кишки и просветом отводящей и приводящей петель тонкой кишки ниже сформированного клапана, образованный резервуар анастомозируют в 12-перстную кишку путем наложения дуодено-еюнального анастомоза конец в бок.
Изобретение поясняется чертежами, где на Фиг.2-7 представлены этапы операции и цифрами обозначены:
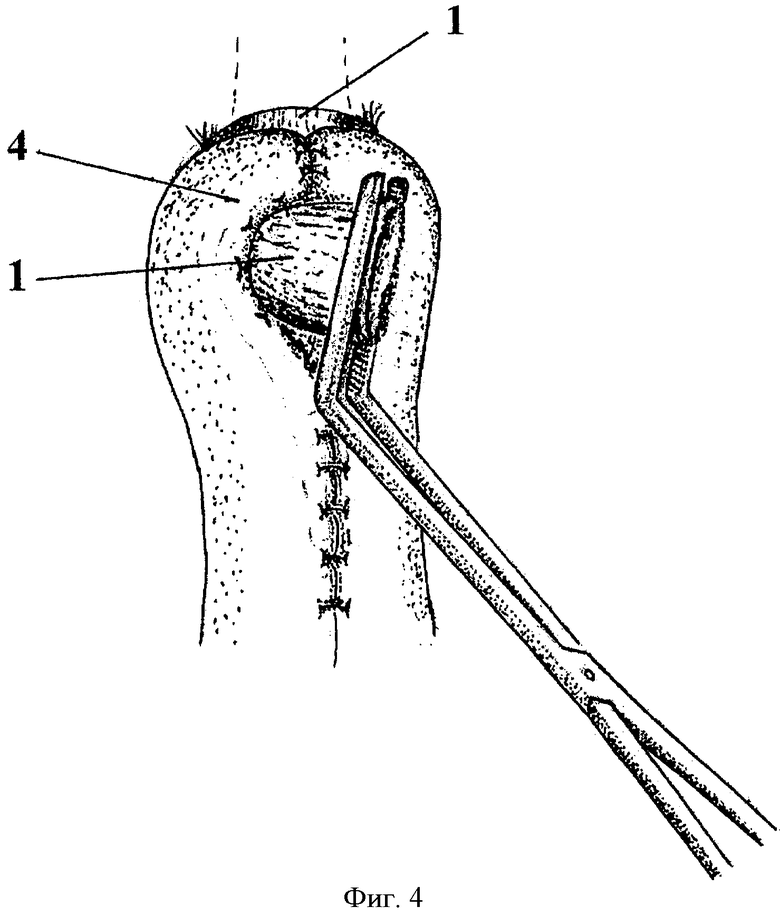
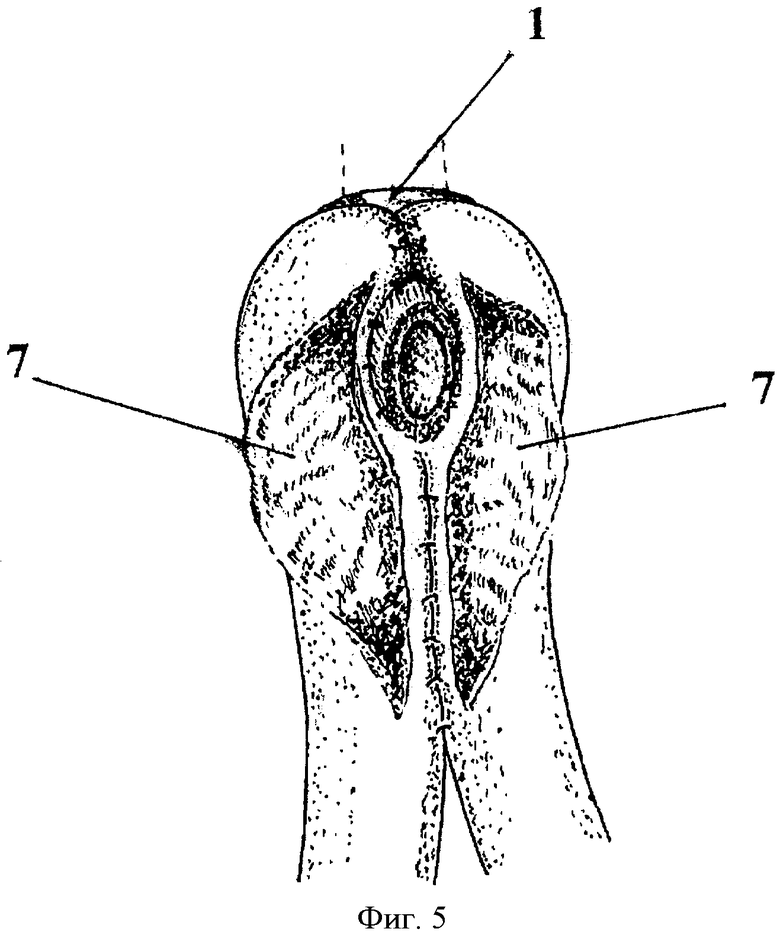
1. Культя пищевода
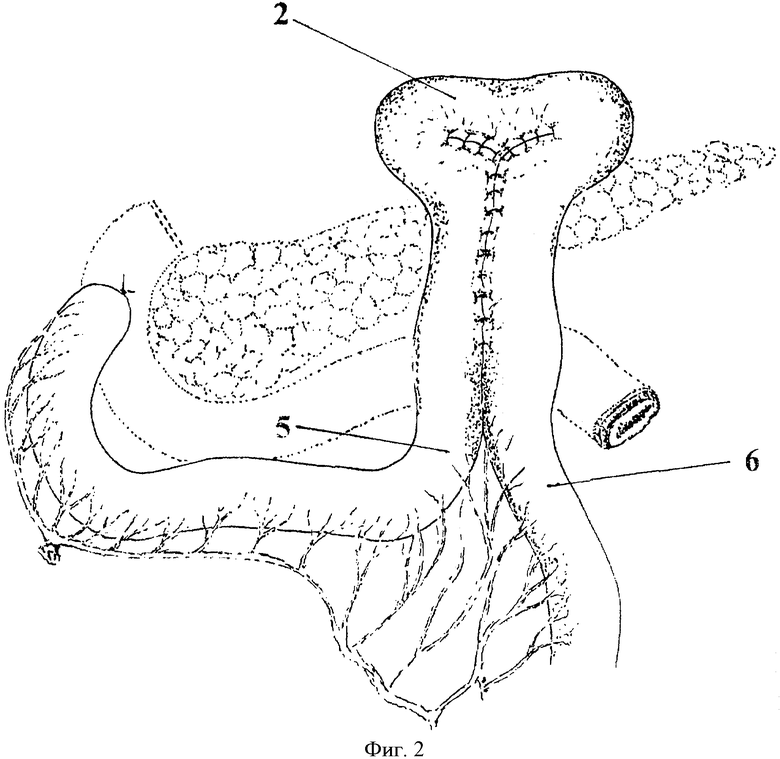
2. Т-образная петля тонкой кишки (горизонтальная часть)
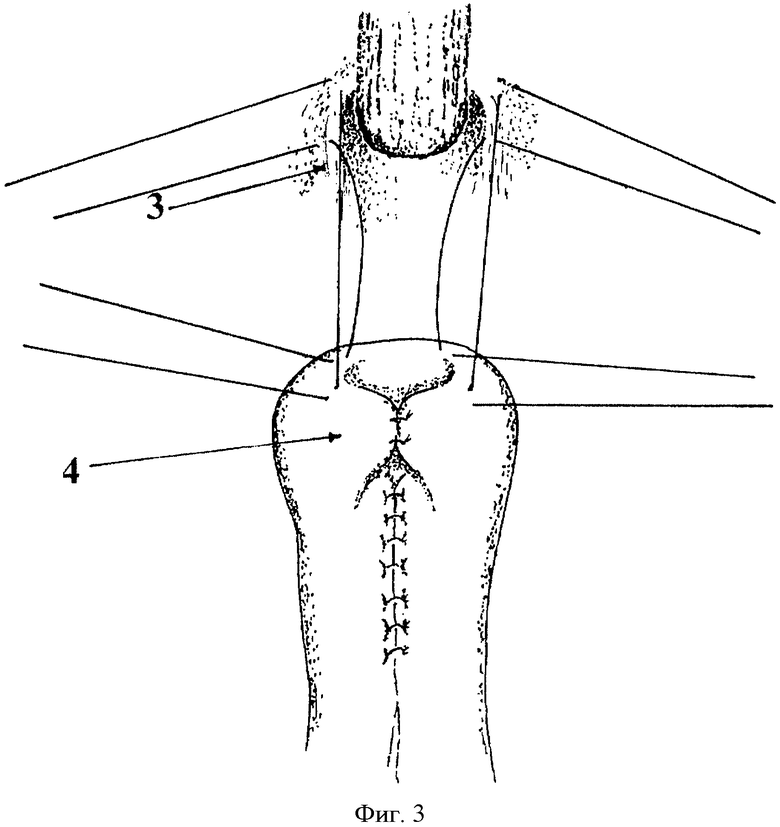
3. Диафрагмальные ножки
4. Сформированная муфта из тонкой кишки
5. Приводящий отдел тонкой кишки (вертикальная часть Т-образной петли)
6. Отводящий отдел тонкой кишки (вертикальная часть Т-образной петли)
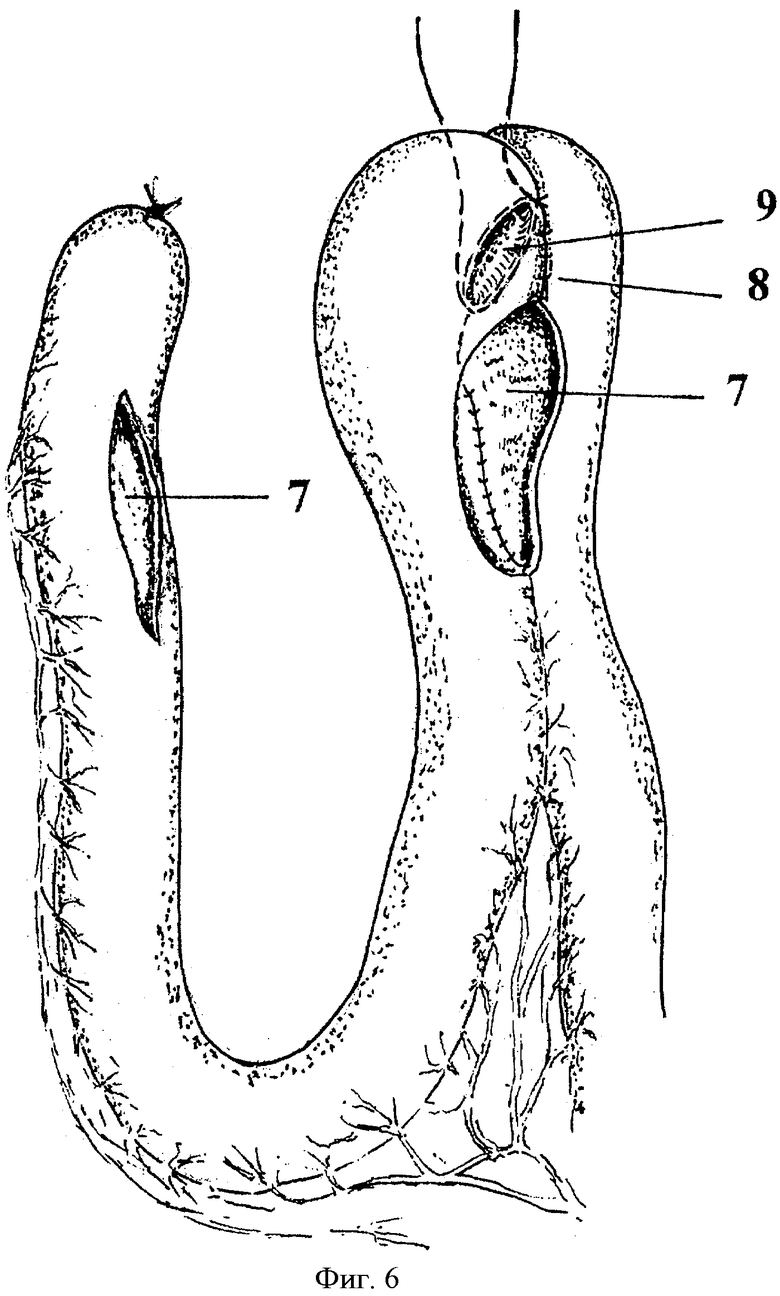
7. Энтеротомия
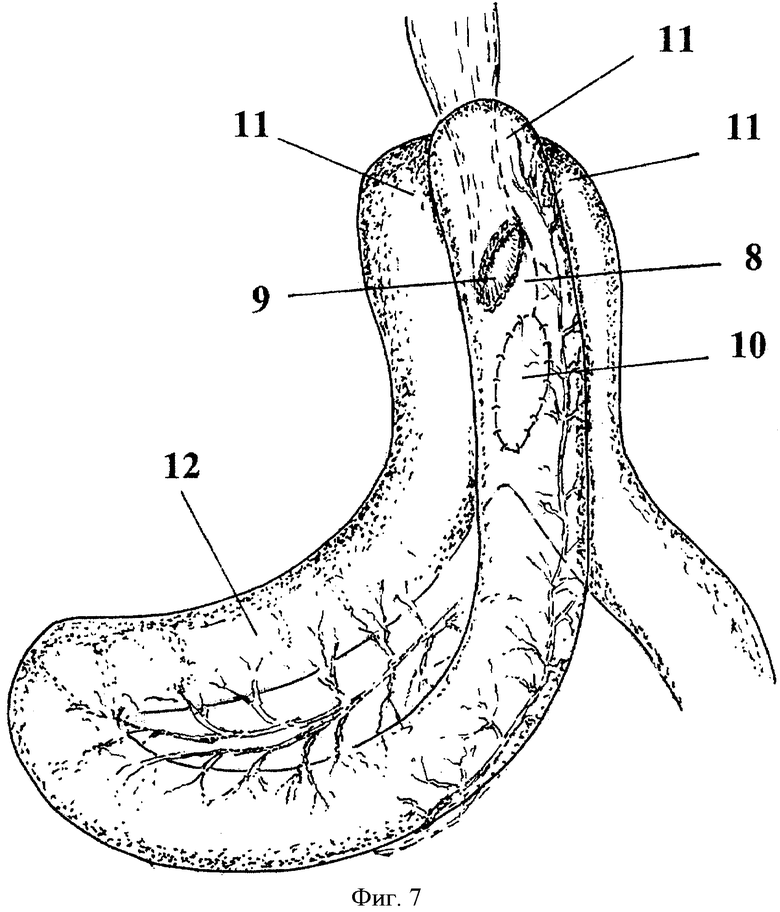
8. Арефлюксный клапан
9. Сформированный пищеводно-кишечный анастомоз
10. Сформированный межкишечный анастомоз
11. Аналог «газового пузыря»
12. Тонкокишечный резервуар
Способ осуществляется следующим образом.
После мобилизации желудка с сальниками связочным аппаратом начальная петля тощей кишки пересекается в 10 см от связки Трейтца, проксимальный конец кишки временно остается на жоме, а дистальный конец окончательно ушивается двумя рядами швов. С целью мобилизации дистального сегмента пересеченной кишки вскрывают листки брюшины брыжейки вдоль радиальных сосудов, пересекают и лигируют 1-2 радиальных сосуда с сохранением сосудистой дуги. Далее, на расстоянии 50-60 см от ушитого конца кишки формируется Т-образная петля наложением узловых швов по брыжеечному краю (Фиг.2), таким образом, чтобы длина вертикальной части петли 5 и 6 составляла 8-10см, горизонтальной части 2 - 5-6 см (Фиг.2). Сшивая спереди наиболее выступающие края горизонтальной части петли 2 (Фиг.2) двумя узловыми швами, формируют муфту 4 (Фиг.3). Накладывают превентивные салазочные швы-держалки в количестве 4-х между верхним краем муфты и ножками диафрагмы по 2 с каждой стороны с захватом мышечного слоя пищевода (Фиг.3). Через подготовленный канал в муфте проводят Г-образный зажим и захватывают пищевод в сагиттальной плоскости. Желудок отсекают от пищевода. Подтягивая пищевод инструментом, муфту нанизывают на пищевод, затягивают и завязывают ранее наложенные швы-держалки. Для фиксации пищевода в муфте накладывают узловые серозно-мышечные швы по 3-4 с каждой стороны между мышечным слоем пищевода выше зажима на 1-1,5 см и прилегающими стенками муфты (Фиг.4). Параллельно наложенным швам в косом сходящемся книзу направлении электроножом вскрывается просвет приводящей и отводящей петли тонкой кишки на протяжении 5 см. Иссекают раздавленный инструментом сегмент пищевода. У верхнего края вскрытых просветов края пищевода по окружности сшивают с прилежащими краями кишки узловыми швами из рассасывающегося монофиламентного материала (Фиг.5).
Далее формируют антирефлюксный клапан: сшивают края вскрытых отделов кишечной муфты, начиная с верхнего края пищеводно-кишечного соустья на протяжении 1,5 см, в результате просвет пищеводно-кишечного анастомоза спереди прикрывается ушитым участком кишечной стенки, выполняющим функцию клапана. Затем накладывают непрерывный слизисто-серозный шов тонкой кишки от нижнего края пищеводно-кишечного анастомоза до нижнего конца разреза вскрытых петель кишки. Далее вскрывается электроножом просвет перемещенной и отключенной тонкой кишки по противобрыжеечному краю дистальнее от ушитого конца на 4-5 см на протяжении 3-4 см (Фиг.6). Вскрытые просветы тонкой кишки обращают друг к другу таким образом, чтобы ушитый конец перемещенной кишки располагался на уровне пищеводного отверстия диафрагмы, после чего накладывают анастомоз, сшивая непрерывным слизисто-серозным швом обращенные друг к другу края вскрытых петель тонкой кишки. Линию швов в области сформированного клапана герметизируют вторым рядом узловых серо-серозных швов с захватом ушитого конца перемещенной петли. Аналогичным образом герметизируют линию швов межкишечного анастомоза (Фиг.7).
В результате выполнения данных технических приемов приводящий сегмент тонкой кишки оказывается закольцованным на пищеводно-кишечном анастомозе и межкишечном анастомозе, разнесенных по уровню на высоту клапана, и выполняет функцию резервуара, начальный объем которого составляет 280-300 мл. Следующим этапом является включение резервуара в 12-перстную кишку наложением дуодено-еюнального анастомоза конец в бок двухрядным швом. Операция заканчивается формированием межкишечного анастомоза между отводящим концом тощей кишки от нижнегоризонтальной части дуоденум и отводящей от пищеводно-кишечного анастомоза петлей тонкой кишки конец в бок.
Техническим результатом заявленного способа является улучшение физиологичности анастомоза, уменьшение риска развития рефлюксной болезни, демпинг-синдрома и агастральной астении.
Примеры конкретного выполнения
Пример 1
Больной Д. 68 лет, находился на лечении в хирургическом отделении ГУЗ «Областная больница №3» с 09.10.08 по 27.10.08 г. с диагнозом: Инфильтративно-язвенный рак тела желудка II Аст. pT2N0M0, осложненный профузным кровотечением, геморрагическим шоком 3 ст, ДВСК-синдромом.
Из анамнеза установлено, что заболел 03.10.08 г., когда появились боли в эпигастральной и загрудинной областях. 08.10.08 г. отмечено падение АД и диагностировано желудочно-кишечное кровотечение. Больной доставлен в хирургический стационар, где в результате обследования установлен диагноз: инфильтративно-язвенный рак верхней трети тела желудка, состоявшееся желудочное кровотечение. После предоперационной подготовки больной оперирован в экстренном порядке 09.10.08 г. При ревизии органов брюшной полости метастазов в печени не обнаружено. Желчный пузырь размерами 8-4-3 см содержит гомогенную желчь. Тонкая и толстая кишка заполнены старой темной кровью, в желудке определяется небольшое количество старой крови со сгустками объемом не более 100-150 мл. После эвакуации желудочного содержимого на задней стенке субкардиального отдела желудка обнаружена инфильтративная опухоль размерами до 5-6 см в виде инфильтрированной утолщенной до 0,8 см стенки с неровным рельефом слизистой. При ревизии зон лимфооттока признаков метастатического поражения лимфатических узлов не обнаружено. Констатирован операбельный опухолевый процесс pT2N0M0. Принято решение выполнить радикальную гастрэктомию с сальниками и лимфодиссекцией Д2 с наложением арефлюксного пищеводно-тонкокишечного анастомоза с формированием резервуара и включением его в 12-перстную кишку, наложением межкишечного анастомоза, санации и дренирования брюшной полости.
Желудок с сальниками и связочным аппаратом мобилизован от 12-перстной кишки до пищевода с пересечением и лигированием кровоснабжающих его сосудов и лимфодиссекцией Д2. Выполнена стволовая ваготомия. Мобилизован абдоминальный сегмент пищевода. Желудок отсечен от пищевода. Наложен муфтообразный арефлюксный пищеводно-тонкокишечный анастомоз с формированием кольцевидного резервуара из приводящей петли тонкой кишки. Препарат одним блоком отсечен от 12-перстной кишки. Сформированный резервуар включен в 12-перстную кишку путем наложения дуодено-еюнального анастомоза. Отводящие отделы тонкой кишки от нижнегоризонтальной части 12-перстной кишки анастомозированы с отводящей петлей кишки от пищеводно-тонкокишечного анастомоза конец в бок по Ру. Брюшная полость дренирована в обоих подреберьях трубчатыми и перчаточными дренажами. В 12-перстную кишку через сформированный резервуар установлен декомпрессивный назо-интестинальный зонд. Лапаротомная рана ушита послойно наглухо.
Препарат: Удаленный желудок с сальниками, серозный покров не изменен. На слизистой оболочке верхней трети желудка на задней стенке инфильтративная опухоль в виде площадки фиксированной слизистой до 5-6 см с плотной бугристой поверхностью, на которой видны 4 тромбированных сосуда до 1-1,5 мм в диаметре. В клетчатке метастазов не обнаружено. Морфологическая структура опухоли соответствовала умеренно-дифференцированной аденокарциноме желудка, метастазов в лимфоузлах не обнаружено.
Послеоперационный период протекал без осложнений. Назо-интестинальный декомпрессивный зонд удален на 5 сутки. Выполнена контрольная рентгенография пищевода и резервуара. Функция сформированного резервуара удовлетворительная, задержка контраста в нем наблюдалась до 2 часов, дисфагии и признаков рефлюкса в положении Тренделенбурга не отмечено. При эндоскопическом исследовании пищевода и тонкой кишки анастомоз сомкнут, свободно проходим, признаков кишечно-пищеводного рефлюкса не выявлено. Больной в удовлетворительном состоянии выписан по месту жительства на 18 сутки после операции.
Пример 2
Больная К. 73 лет, находилась на лечении в хирургическом отделении ГУЗ «Областная больница №3» с 05.09.07 г. по 09.10.07 г. с диагнозом: Рак тела желудка, блюдцеобразная форма, III ст. рТ3N1М0, осложненный состоявшимся желудочным кровотечением. Сопутствующие заболевания: Атеросклероз аорты, мозговых сосудов. Фибромы яичников. Распространенный остеохондроз позвоночника.
В процессе предоперационного обследования опухолевый процесс подтвержден гистологическим исследованием гастробиопсийного материала от 07.09.07г - умеренно-дифференцированная аденокарцинома. При клиническом исследовании визуальных данных за запущенный опухолевый процесс не обнаружено. При гинекологическом исследовании выявлено увеличение придатков, которое подтверждено данными УЗИ от 13.09.07 г. После предоперационной подготовки 18.09.07 г. больная оперирована. При ревизии брюшной полости в теле желудка обнаружена большая блюдцеобразная опухоль, расположенная преимущественно на малой кривизне и задней стенке размерами 8-7 см, прорастающая все слои стенки желудка с выходом на серозную оболочку в виде разрастаний опухолевой ткани. При ревизии зон лимфооттока обнаружены метастазы в перигастральных лимфатических узлах, по ходу левой желудочной, селезеночной артерии до 1,5 см в диаметре в количестве трех. При ревизии малого таза обнаружены увеличенные до 4-5 см плотные бугристые яичники белого цвета весьма подозрительные по принадлежности к метастазам Крукенберга. Признаков асцита и опухолевой диссеминации по брюшине не обнаружено, процесс расценен операбельным, выполнена гастрэктомия с сальниками, лимфодиссекцией Д2 с формированием арефлюксного пищеводно-кишечного анастомоза, тонкокишечного резервуара с включением его в 12-перстную кишку и двусторонняя овариоэктомия. Гистологическая структура опухоли желудка соответствовала блюдцеобразной форме низкодифференцированного аденогенного рака с выраженным инфильтративным ростом, с прорастанием всех слоев стенки желудка, выходом в окружающую клетчатку, распространенным канцероматозом сосудов. Операционный разрез прошел в пределах здоровых тканей. В двух лимфатических узлах обнаружены рост железистого рака с субтотальным замещением лимфоидной ткани. При исследовании удаленных яичников данных за метастаз Крукенберга в пределах исследованного материала не обнаружено, картина соответствует фибромам яичников.
Послеоперационный период протекал без осложнений. Раны зажили первичным натяжением. При оценке непосредственных функциональных результатов симптомов пищеводно-кишечного рефлюкса и демпинг-синдрома не зарегистрировано. При ФЭС от 05.10.07г = Слизистая пищевода обычная, анастомоз на уровне 40 см от резцов. В зоне анастомоза видны лигатуры и три входа в тонкую кишку диаметром до 1,5 см. Тонкая кишка осмотрена за анастомозами на 8-10см, содержит мутную жидкость с глыбками слизи, реакция тонкой кишки на бародавление через эндоскоп вялая. Контактной геморрагии не наблюдается. Заключение: тотально удаленный желудок, анастомоз пищевода с тонкокишечным резервуаром. Оценка резервуарной функции проводилась клиническим и рентгенологическим тестированием, одномоментный прием 250 мл жидкости не приводил к изменениям в субъективных ощущениях. При рентгеноскопии пищевода и тонкой кишки с сульфатом бария определяются контрастированные петли тонкой кишки. Через 2 часа от начала исследования контраст прослеживается как в проксимальных отделах (резервуаре), так и в дистальных отделах кишки. Дополнительных затеков контраста не выявлено. Больная в удовлетворительном состоянии выписана по месту жительства.
По описанной методике оперированы 3 больных в возрасте 67-74 лет, двум из которых выполнен расширенный объем: гастрэктомия с двусторонней овариоэктомией и гастрэктомия с резекцией сигмовидной кишки. Осложнений в послеоперационном периоде не отмечено, все больные выписаны в сроки на 14-18 сутки после операции. Функциональные результаты оценивались клиническими тестами, эндоскопическим и рентгенологическим исследованием пищевода с сульфатом бария в положении Тренделенбурга, энтерографией с серией снимков через 20, 60, 120 минут. Симптомов рефлюкса и демпинг-синдрома ни в одном случае не отмечено, на рентгенограммах тонкой кишки в положении Тренделенбурга затека контраста в пищевод нет, на сериях энтерограмм отмечается постепенная эвакуация контраста из сформированного резервуара в дистальные отделы тонкой кишки, причем на 120 минуте в верхних отделах еще сохраняется до 10% контраста. Обращает внимание у больных довольно быстрая динамика нарастания веса, при потере веса 6-8 кг в раннем послеоперационном периоде все больные восстановили свой первоначальный вес через 1-1,5 месяца после операции.
Таким образом, заявляемый способ формирования арефлюксного пищеводно-тонкокишечного анастомоза можно рекомендовать при хирургическом лечении злокачественных новообразований желудка, а также при ряде хирургических заболеваний желудка, в лечении которых невозможно соблюсти органосохраняющий принцип.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВЫПОЛНЕНИЯ ГАСТРЭКТОМИИ | 2015 |
|
RU2577234C1 |
| СПОСОБ ПЕРВИЧНОЙ ЕЮНОГАСТРОПЛАСТИКИ ПОСЛЕ ГАСТРЭКТОМИИ | 1999 |
|
RU2189789C2 |
| СПОСОБ РЕКОНСТРУКЦИИ ПИЩЕВАРИТЕЛЬНОГО ТРАКТА ПОСЛЕ ПАНКРЕАТОДУОДЕНАЛЬНОЙ РЕЗЕКЦИИ И ЭКСТИРПАЦИИ ЖЕЛУДКА С ВОССТАНОВЛЕНИЕМ ФИЗИОЛОГИЧЕСКОЙ И АНАТОМИЧЕСКОЙ ЦЕЛОСТНОСТИ | 2016 |
|
RU2636881C1 |
| СПОСОБ ФОРМИРОВАНИЯ ИСКУССТВЕННОГО ЖЕЛУДКА | 2010 |
|
RU2445018C2 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РЕФЛЮКС-ЭЗОФАГИТА ПРИ ОПЕРАЦИИ РЕКОНСТРУКТИВНОЙ ЕЮНОГАСТРОПЛАСТИКИ ПОСЛЕ ГАСТРЭКТОМИИ | 1999 |
|
RU2148958C1 |
| СПОСОБ РЕДУОДЕНИЗАЦИИ С ФОРМИРОВАНИЕМ АНТИРЕФЛЮКСНОГО КЛАПАНА ПРИ БОЛЕЗНЯХ ОПЕРИРОВАННОГО ЖЕЛУДКА ПОСЛЕ ГАСТРЭКТОМИИ В ПЕТЛЕВОЙ РЕКОНСТРУКЦИИ ПО БРАУНУ | 2023 |
|
RU2801772C1 |
| СПОСОБ РЕДУОДЕНИЗАЦИИ С СОЗДАНИЕМ КИШЕЧНОГО РЕЗЕРВУАРА ПРИ БОЛЕЗНЯХ ОПЕРИРОВАННОГО ЖЕЛУДКА ПОСЛЕ ГАСТРЭКТОМИИ В ПЕТЛЕВОЙ РЕКОНСТРУКЦИИ ПО БРАУНУ | 2023 |
|
RU2801773C1 |
| СПОСОБ ТОНКОКИШЕЧНОЙ ГАСТРОПЛАСТИКИ ПОСЛЕ ГАСТРЭКТОМИИ | 2003 |
|
RU2262896C2 |
| СПОСОБ ЭЗОФАГОЕЮНОСТОМИИ ПРИ ГАСТРЭКТОМИИ И РЕЗЕКЦИИ ПИЩЕВОДА | 1998 |
|
RU2180192C2 |
| СПОСОБ ФОРМИРОВАНИЯ АРЕФЛЮКСНОГО ПИЩЕВОДНО-КИШЕЧНОГО АНАСТОМОЗА ПОСЛЕ ГАСТРЭКТОМИИ | 2006 |
|
RU2327426C1 |

Изобретение относится к хирургии и может быть применимо для формирования арефлюксного пищеводно-тонкокишечного анастомоза. Формируют Т-образную петлю на ушитой отводящей тощей кишке на расстоянии 50-60 см от уровня пересечения. Формируют пищеводно-тонкокишечный анастомоз, рассекая приводящий и отводящий отделы кишки прилежащей муфты длиной, равной двум ее диаметрам, сшивая конец пищевода с прилежащими краями вскрытых петель в верхнем отделе узловыми швами. Создают клапан, ушивая сверху края рассеченных отделов тонкой кишки на величину диаметра пищеводного отверстия. Накладывают слизисто-серозный непрерывный шов тонкой кишки ниже сформированного пищеводно-кишечного анастомоза. Формируют резервуар в виде кольцевидной приводящей петли тонкой кишки путем наложения межкишечного анастомоза бок в бок между перемещенным ушитым концом приводящего отдела тонкой кишки и просветом отводящей и приводящей петель тонкой кишки ниже сформированного клапана. Образованный резервуар анастомозируют в 12-перстную кишку путем наложения дуодено-еюнального анастомоза конец в бок. Способ позволяет улучшить физиологичность пищеварения, предотвратить развитие демпинг-синдрома. 7 ил.
Способ формирования арефлюксного пищеводно-тонкокишечного анастомоза, включающий рассечение тощей кишки, формирование Т-образной петли тонкой кишки с последующим созданием из нее тонкокишечной муфты, наложение пищеводно-тонкокишечного анастомоза, формирование межкишечного анастомоза конец в бок между отводящими отделами тонкой кишки, отличающийся тем, что Т-образную петлю формируют на ушитой отводящей тощей кишке на расстоянии 50-60 см от уровня пересечения, пищеводно-тонкокишечный анастомоз формируют, рассекая приводящий и отводящий отделы кишки прилежащей муфты длиной, равной двум ее диаметрам, сшивая конец пищевода с прилежащими краями вскрытых петель в верхнем отделе узловыми швами, после чего создают клапан, ушивая сверху края рассеченных отделов тонкой кишки на величину диаметра пищеводного отверстия, далее накладывают слизисто-серозный непрерывный шов тонкой кишки ниже сформированного пищеводно-кишечного анастомоза, формируют резервуар в виде кольцевидной приводящей петли тонкой кишки путем наложения межкишечного анастомоза бок в бок между перемещенным ушитым концом приводящего отдела тонкой кишки и просветом отводящей и приводящей петель тонкой кишки ниже сформированного клапана, образованный резервуар анастомозируют в 12-перстную кишку путем наложения дуодено-еюнального анастомоза конец в бок.
| ГРИНБЕРГ А.А | |||
| и др | |||
| Способ инвагинационного арефлюксного пищеводно-кишечного анастомоза | |||
| - Хирургия, 1994, №4, с.55-57 | |||
| СПОСОБ ЭНТЕРОЦИСТОПЛАСТИКИ | 2000 |
|
RU2163093C1 |
| US 2008312559 A1, 18.12.2008 | |||
| REA T | |||
| Study of the antireflux action of the Roux-en-Y jejunal loop in reconstruction after gastrectomy and nutritional status in the follow-up | |||
| Ann Ital Chir | |||
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
Авторы
Даты
2011-12-27—Публикация
2009-02-09—Подача