Область техники
Изобретение относится к области медицины, а именно к кардиологии и сердечно-сосудистой хирургии, и может быть использовано при персонализированном определении показаний к интервенционному лечению больных фибрилляцией предсердий (ФП).
Уровень техники
Известен способ диагностики и прогнозирования сердечно-сосудистых заболеваний и явлений (RU 2018130866 А 04.03.2020), учитывающий клинические характеристики пациентов с заболеваниями сердечно-сосудистой системы путем определения по меньшей мере двух биомаркеров в биологическом образце, полученном от субъекта, и определения статуса по меньшей мере одной клинической переменной для субъекта. Затем на основании полученных данных вычисляют прогностическую оценку результатов лечения, на основании которой решают вопрос о проведении интервенционного вмешательства. При этом в качестве биомаркеров определяют: адипонектин, аполипопротеин А-II, аполипопротеин C-I, декорин, интерлейкин-8, молекулы повреждения почек-1, матриксную металлопротеиназу-9, мидкин, миоглобин, N-концевой прогормон натрийуретического белка головного мозга (NT-proBNP), остеопонтин, связанного с легочным сурфактантом белка D, фактор стволовых клеток, тканевой ингибитор металлопротеиназ-1 (ТИМП-1), тропонин и молекула адгезии эндотелия сосудов. А в качестве клинической переменной определяют: возраст, аортокоронарного шунтирования в анамнезе, наличие сахарного диабета II типа, гемодиализ в анамнезе, инфаркт миокарда в анамнезе, эндоваскулярное коронарное вмешательство, например, имплантация коронарного стента и/или коронарная баллонная ангиопластика, а также пол пациента.
Недостатками данного способа является то, что: при определении клинической значимости заболевания не учитываются морфофункциональные особенности сердечно-сосудистой системы, а именно: систолическая и диастолическая функция (ДФ) сердца, а также варианты впадения легочных вен (ЛВ) в левое предсердие (ЛП) не учитываются.
Известен способ дооперационного прогнозирования рецидива фибрилляции предсердий после проведения процедуры радиочастотной абляции (RU 2556533 С1 10.07.2015), учитывающий клинические характеристики пациентов для дооперационного прогнозирования рецидива фибрилляции предсердий после проведения процедуры радиочастотной абляции путем определения возраста пациента в годах, диаметра левого предсердия, оценки проводимой антиаритмической терапии, степени недостаточности аортального и митрального клапанов. С использованием полученных данных рассчитывают риск неэффективности интервенционного вмешательства, что позволяет определить показания для интервенционного лечения пациентов с ФП.
Недостатками данного способа является то, что: при определении клинической значимости заболевания не учитываются морфофункциональные особенности сердечно-сосудистой системы, а именно: систолическая и диастолическая функция сердца, а также варианты впадения ЛВ в ЛП не учитываются.
Кроме того известен способ отбора пациентов с длительно персистирующей формой фибрилляции предсердий на проведение эффективного катетерного лечения (RU 2749552 С1 15.06.2022) отбора пациентов с длительно персистирующей формой фибрилляции предсердий для проведения эффективного интервенционного лечения, при котором у пациентов с длительно персистирующей формой ФП до проведения катетерного лечения проводят забор периферической крови с целью количественного определения в сыворотке крови уровня стимулирующего фактора роста 2 (ST 2) посредством твердофазного иммуноферментного анализа. На основании полученных данных прогнозируют эффективность проведения интервенционного вмешательства.
Способ позволяет уточнить показания к проведению интервенционного лечения пациентов с ФП на основании определения уровня стимулирующего фактора роста 2.
Недостатками данного способа является то, что: при определении клинической значимости заболевания не учитываются морфофункциональные особенности сердечно-сосудистой системы, а именно: систолическая и ДФ сердца, а также варианты впадения ЛВ в ЛП не учитываются.
Наиболее близким аналогом настоящего изобретения является способ оценки клинической значимости фибрилляции предсердий при определении показаний к интервенционному лечению фибрилляции предсердий, раскрытый в патенте RU 2791191 С1 03.03.2023. В ходе выполнения способа осуществляют мультиспиральную компьютерную томографию сердца с контрастированием (МСКТ) и трансторакальную эхокардиографию (ЭХОКГ) с оценкой систолической и диастолической функций сердца. Последовательно оценивают систолическую функцию сердца, диастолическую функцию сердца и тип впадения легочных вен в левое предсердие. С учетом проведенного предоперационного обследования определяют клиническую значимость фибрилляции предсердий путем выполнения последовательности действий, а именно: если систолическая функция сердца нарушена, то считают фибрилляцию предсердий клинически значимой; если систолическая функция сердца не нарушена, то оценивают диастолическую функцию сердца; если диастолическая функция сердца нарушена, то выполняют МСКТ и оценивают тип впадения легочных вен в левое предсердие. Если определяют Тип 1, Тип 2 или Тип 4, то оценивают фибрилляцию предсердий как клинически значимую, если определяют Тип 3, Тип 5 или Тип 6, то оценивают фибрилляцию предсердий как клинически незначимую. Способ позволяет персонализировать оценку клинической значимости ФП, позволяющую уточнить показания к интервенционному лечению ФП у бессимптомных пациентов за счет поэтапного анализа морфофункциональных особенностей сердечно-сосудистой системы.
Недостатком известного алгоритма является отсутствие возможности проведения оценки клинической значимости фибрилляции предсердий при определении показаний к интервенционному лечению фибрилляции предсердий в случае невозможности оценки диастолической дисфункции по данным ЭХОКГ.
Технической проблемой, на решение которой направлено настоящее изобретение является оптимизация протокола отбора больных ФП для интервенционного лечения, с учетом систолической и диастолической дисфункции сердца.
Раскрытие изобретения
Техническим результатом, достигаемым при реализации разработанного способа, является персонализация оценки клинической значимости ФП, позволяющая уточнить показания к интервенционному лечению больных ФП, на основе поэтапного анализа морфо-функциональных особенностей сердечно-сосудистой системы, при невозможности определения диастолической функции сердца по данным трансторакальной эхокардиографии. Соблюдают следующую последовательность действий: Блок 1:
оценивают систолическую функцию сердца по данным трансторакальной эхокардиографии; если систолическая функция сердца нарушена, то считают фибрилляцию предсердий клинически значимой и проведение интервенционного лечения больному показанным;
если систолическая функция сердца не нарушена, то оценивают диастолическую функцию сердца по данным трансторакальной эхокардиографии;
если диастолическая функция сердца не нарушена, то оценивают фибрилляцию предсердий как клинически незначимую и считают, что интервенционное лечение больному не показано;
если диастолическая функция сердца нарушена, то переходят к блоку 3 алгоритма;
если диастолическую функцию сердца по данным трансторакальной эхокардиографии оценить не удается, то оценивают риск нарушения диастолической функции сердца в соответствии с номограммой, приведенной на фигуре 1;
если при помощи номограммы, приведенной на фигуре 1, определяют средний риск нарушения диастолической функции сердца, то считают, что диастолическая функция сердца не нарушена и считают, что интервенционное лечение больному не показано;
если при помощи номограммы, приведенной на фигуре 1, определяют высокий и очень высокий риск нарушения диастолической функции сердца, то считают, что диастолическая функция сердца нарушена и переходят к блоку 2.
Блок 2:
проводят неинвазивное электрофизиологическое картирование сердца с определением роторной активности в предсердиях, состоящее из последовательных этапов, а именно:
регистрируют многоканальную поверхностную электрокардиограмму;
выполняют мультиспиральную компьютерную томографию сердца с контрастированием;
синхронизируют многоканальную поверхностную электрокардиограмму и мультиспиральную компьютерную томограмму сердца с получением воксельной и полигональной моделей предсердий;
выбирают фрагмент многоканальной поверхностной электрокардиограммы для анализа с максимальным интервалом RR с последующей обработкой электрической активности предсердий:
- выбирают и удаляются все QRS комплексы на отведениях многоканальной поверхностной электрокардиограммы;
- устанавливают глобальную полосу фильтрации выбранного участка электрокардиограммы в диапазоне от 3 Гц до 9 Гц;
- выбирают максимальный T-q интервал на многоканальной поверхностной электрокардиограмме;
- выполняют анализ роторной активности на изопотенциальной фазовой карте;
- осуществляют анализ роторной активности на карте плотности фазовых сингулярностей;
если определить роторную активность в предсердиях не удается, то считают, что выполнение интервенционного лечения не целесообразно.
если определить роторную активность в предсердиях удается, то считают, что в этом случае проведение интервенционного лечения целесообразно и переходят к блоку 3 алгоритма.
Блок 3:
выполняют мультиспиральную компьютерную томографию сердца с контрастированием и оценивают тип впадения легочных вен в левое предсердие:
- тип 1 - типичная анатомия: наличие четырех раздельных устьев легочных вен;
- тип 2 - рассыпной тип: наличие трех и более ипсилатеральных устьев легочных вен;
- тип 3 - ствол левых легочных вен: левая верхняя и нижняя легочные вены сливаются в один ствол до впадения в левое предсердие, правые легочные вены впадают в левое предсердие двумя раздельными устьями;
- тип 4 - смешанный тип: сочетание ствола легочных вен с одной стороны и рассыпного типа с другой;
- тип 5 - ствол контралатеральных легочных вен: слияние контралатеральных легочных вен в один ствол до впадения в левое предсердие;
- тип 6 - ствол правых легочных вен: правые легочные вены сливаются в общий ствол до впадения в левое предсердие;
если определяют тип 1, тип 2 или тип 4, то оценивают фибрилляцию предсердий как клинически значимую и считают, что проведение интервенционного лечения больному показано;
если определяют тип 3, тип 5 или тип 6, то оценивают фибрилляцию предсердий как клинически незначимую и считают, что интервенционное лечение больному не показано.
Краткое описание чертежей
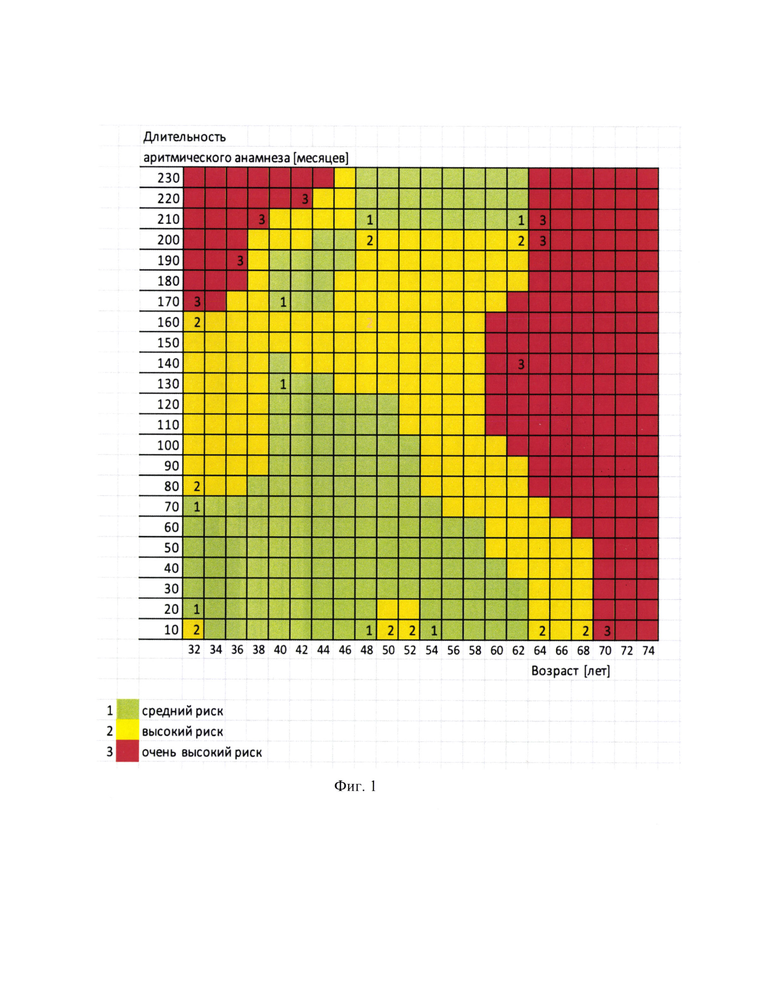
Фиг. 1. Представлена разработанная номограмма прогноза риска развития диастолической дисфункции левого желудочка у пациентов с фибрилляцией предсердий в зависимости от длительности аритмического анамнеза и возраста пациента. Зоны риска: 1-3.
Фиг. 2. Этапный анализ многоканальной электрокардиограммы
Осуществление способа.
Способ определения показаний к проведению интервенционного лечения при фибрилляции предсердий у бессимптомных пациентов с учетом клинических, функциональных и электрофизиологических данных осуществляют последователь по блокам: 1, 2 и 3.
Блок 1 включает последовательную оценку систолическую и диастолическую функции (ДФ) сердца. С учетом проведенного предоперационного обследования определяют клиническую значимость фибрилляции предсердий путем выполнения последовательности действий, а именно: если систолическая функция сердца нарушена, то считают фибрилляцию предсердий клинически значимой; если систолическая функция сердца не нарушена, то оценивают ДФ сердца; если ДФ сердца не нарушена, то считают, что ФП клинически не значима; если ДФ сердца нарушена, то переходят к Блоку 3, в ходе которого выполняют МСКТ и оценивают тип впадения легочных вен в левое предсердие по следующей классификации:
тип 1 - типичная анатомия: наличие четырех раздельных устьев легочных вен;
тип 2 - рассыпной тип: наличие трех и более ипсилатеральных устьев легочных вен;
тип 3 - ствол левых легочных вен: левая верхняя и нижняя легочные вены сливаются в один ствол до впадения в левое предсердие, правые легочные вены впадают в левое предсердие двумя раздельными устьями;
тип 4 - смешанный тип: сочетание ствол легочных вен с одной стороны и рассыпного типа с другой;
тип 5 - ствол контралатеральных легочных вен: слияние контралатеральных легочных вен в один ствол до впадения в левое предсердие;
тип 6 - ствол правых легочных вен: правые легочные вены сливаются в общий ствол до впадения в левое предсердие.
Если определяют Тип 1, Тип 2 или Тип 4, то приходят к заключению, что ФП клинически значима, если определяют Тип 3, Тип 5 или Тип 6, то приходят к заключению, что ФП клинически не значима.
В том случае если в Блоке 1 диастолическую функцию сердца по данным трансторакальной эхокардиографии оценить не удается, то использую номограмму оценки риска диастолической дисфункции.
Указанная номограмма была разработана коллективом авторов, которые определили закономерность между длительностью аритмического анамнеза и возрастом пациента, на основании которой оценивают диастолическую дисфункцию сердца.
При разработке данной номограммы осуществляли отбор факторов для включения в построение прогностической модели «Распознавание образов» (Лапко, А.В. Статистические методы моделирования и принятия решений в развивающихся медико-биологических системах / А.В. Лапко, О.М. Новиков, Л.С.Поликарпов. - Новосибирск: Наука, 1991. - 221 с.) проведена оценка значимости изучаемых параметров.
Анализ показал, что среди всех изучаемых факторов лишь длительность заболевания и возраст пациента позволяют построить математическую модель с точностью прогноза более 70% (Фиг. 1).
В связи с этим для построения математической модели прогнозирования развития ДД ЛЖ у больных с ФП в качестве предикторов были включены: возраст и аритмический анамнез.
Построенная по результатам математического моделирования номограмма позволяет графически отобразить области распределения состояний в многомерном пространстве признаков и выделить три зоны риска развития ДД ЛЖ у больных ФП (далее - риск): 1 - среднего риска, 2 - высокого риска и 3 - очень высокого риска. Зона среднего риска выделилась в трех областях.
Одна из областей среднего риска ограничена пределами возраста от 32 до 62 лет и пределами аритмического анамнеза от 10 до 130 месяцев. В пределах возраста 32-38 лет граница зоны среднего риска не зависит от возраста.
При дальнейшем увеличении возраста, больше 38 лет, возраст является ведущим фактором риска. Но после 44 лет зависимость нахождения в зоне среднего риска в пространстве признаков, продолжительности аритмического анамнеза и возраста обратная, близкая к линейной.
Обращают внимание обнаруженные дополнительные зоны среднего риска: одна, расположенная в интервале значений продолжительности аритмического анамнеза 170-200 месяцев и возраста 40-46 лет, другая в интервале значений продолжительности аритмического анамнеза 210-230 месяцев и возраста 48-62 лет.
Зона высокого риска выделилась в трех областях: наибольшая в интервале возраста 32-68 лет, в которую вклинивается область среднего риска со значениями продолжительности аритмического анамнеза 170-200 месяцев.
Также выделились небольшие зоны высокого риска, в области значений возраста до 34 лет и длительности аритмического анамнеза до 20 месяцев, а также в области значений возраста от 50 до 54 лет и длительности аритмического анамнеза до 30 месяцев.
Зона очень высокого риска выделилась в двух областях: одна зона очень высокого риска расположена в пространстве значений длительности аритмического анамнеза 170 и более месяцев и возраста 32-44 лет, в которой с увеличением возраста увеличиваются предельные значения длительности аритмического анамнеза.
Вторая зона очень высокого риска, наибольшая по площади располагается в области значений возраста 60 лет и старше.
С увеличением возраста от 60 до 70 лет в интервале значений аритмического анамнеза 50-100 месяцев зависимость между признаками, обратная, близкая к линейной: с увеличением возраста уменьшаются значения аритмического анамнеза, определяющие нахождение в зоне очень высокого риска.
В возрасте 70 лет и старше нахождение в зоне очень высокого риска определяется возрастом и не зависит от продолжительности аритмического анамнеза.
Если по нормограмме определяют высокий и очень высокий риск диастолической дисфункции, то считают, что диастолическая функция сердца нарушена и переходят к блоку 2.
Если определяют средний риск диастолической дисфункции считают диастолическая функция сердца не нарушена и интервенционное лечение не показано.
Блок 2
Проводят неинвазивное электрофизиологическое картирование сердца с определением роторной активности в предсердиях, состоящее из последовательных этапов, а именно:
Регистрируют многоканальную поверхностную ЭКГ с регистрацией сигналов от 224 униполярных отведений на фоне исходного ритма с ФП. Для этой задачи используют специальные полоски с 8-ю контактами ЭКГ, которые наклеивают равномерно продольно по всей окружности грудной клетки. Многоканальное ЭКГ записывают в течение 5 минут с использованием полосы пропускания от 0,05 до 500 Гц, частоты дискретизации 1000 выборок/секунду и дополнительного фильтра с частотой среза 50 Гц. Параллельно осуществляют запись стандартной 12-ти канальной ЭКГ. После окончания записи выбирают и экспортируют 5 секундный фрагмент ЭКГ, обязательно содержащий максимально длинный интервал между соседними комплексами QRS (Фиг. 2).
Выполняют МСКТ с контрастированием;
синхронизируют многоканальную поверхностную ЭКГ и МСКТ с получением воксельной и полигональной моделей предсердий;
выбирают фрагмент многоканальной поверхностной ЭКГ для анализа с максимальным интервалом RR с последующей обработкой электрической активности предсердий:
- выбирают и удаляются все QRS комплексы на отведениях многоканальной поверхностной ЭКГ;
- устанавливают глобальную полосу фильтрации выбранного участка электрокардиограммы в диапазоне от 3 Гц до 9 Гц;
- выбирают максимальный T-q интервал на многоканальной поверхностной электрокардиограмме;
- выполняют анализ роторной активности на изопотенциальной фазовой карте;
- осуществляют анализ роторной активности на карте плотности фазовых сингулярностей;
Данная карта одновременно отражает в процентах, как часто наблюдается роторная активность на всей поверхности предсердий. Применение данной карты позволило судить о зоне максимально частого появления роторной активности.
При определении локализации роторной активности в предсердиях удается, то переходят к блоку 3;
Если роторная активность в предсердиях не локализуется, то считают, что выполнение интервенционного лечения не показано.
Клинические примеры:
Клинический пример 1.
Пациент 65 лет женского пола.
Диагноз: пароксизмальная форма ФП. EHRA 2а.
Жалобы активно не предъявляет.
По данным анамнестических электрокардиограмм (ЭКГ) - ФП с частотой активации желудочков сердца - 77-112 в минуту.
По данным ЭХОКГ: фракция выброса ЛЖ - 41%. Систолическая функция расценена как нарушенная. В связи с этим ФП расценена как клинически значимая. Проведена радиочастотная катетерная изоляция ЛВ.
Через 6 месяцев наблюдения - пароксизмы ФП не рецидивируют. По данным трансторакальной ЭХОКГ - систолическая функция сердца нормализована (ФВ ЛЖ - 55%).
Клинический пример 2.
Пациент 38 лет женского пола.
Диагноз: пароксизмальная форма ФП. EHRA 2а.
Жалобы активно не предъявляет.
По данным анамнестических ЭКГ - ФП с частотой активации желудочков сердца - 78-97 в минуту.
По данным ЭХОКГ: фракция выброса ЛЖ - 64%.
Систолическая функция расценена как не нарушенная.
На следующем этапе оценена ДФ сердца. Выявлено нарушение ДФ сердца.
Выполнена МСКТ: рассыпной тип впадения ЛВ в ЛП (тип 2).
ФП расценена как клинически значимая.
Выполнена криобаллонная изоляция ЛВ.
Через 6 месяцев наблюдения - пароксизмы ФП не рецидивируют. По данным трансторакальной ЭХОКГ - нарушений систолической и ДФ сердца нет.
Клинический пример 3.
Пациент 65 лет мужского пола.
Диагноз: пароксизмальная форма ФП. EHRA 2а.
Жалобы активно не предъявляет.
По данным анамнестических ЭКГ - ФП с частотой активации желудочков сердца - 70-97 в минуту.
По данным ЭХОКГ: фракция выброса ЛЖ - 61%.
Систолическая функция расценена как не нарушенная.
На следующем этапе оценена ДФ сердца. Выявлено нарушение ДФ сердца.
Выполнена МСКТ: - ствол правых легочных вен: правые легочные вены сливаются в общий ствол до впадения в ЛП (тип 6).
ФП расценена как клинически не значимая. Принято решение воздержаться от интервенционного лечения нарушений ритма сердца.
Через 6 месяцев наблюдения - пароксизмы ФП не рецидивируют. По данным трансторакальной ЭХОКГ - нарушений систолической и ДФ сердца нет.
Клинический пример 4.
Пациент 58 лет мужского пола.
Диагноз: пароксизмальная форма ФП. EHRA 2а.
Жалобы активно не предъявляет.
По данным анамнестических ЭКГ - ФП с частотой активации желудочков сердца - 60-96 в минуту.
По данным ЭХОКГ: фракция выброса ЛЖ - 62%. Систолическая функция расценена как не нарушенная. По данным ЭХОКГ ДФ оценить не удалось. По номограмме выявлен высокий риск ДФ.
На следующем этапе проведено неинвазивное электрофизиологическое картирование сердца - роторная активность в предсердиях не определяется.
ФП расценена как клинически не значимая. Принято решение воздержаться от интервенционного лечения нарушений ритма сердца.
Через 6 месяцев наблюдения - пароксизмы ФП не рецидивируют. По данным трансторакальной ЭХОКГ - нарушений систолической и ДФ сердца нет.
Клинический пример 5.
Пациент 48 лет женского пола.
Диагноз: пароксизмальная форма ФП. EHRA 2а.
Жалобы активно не предъявляет.
По данным анамнестических ЭКГ - ФП с частотой активации желудочков сердца - 62-94 в минуту.
По данным ЭХОКГ: фракция выброса ЛЖ - 58%. Систолическая функция расценена как не нарушенная. По данным ЭХОКГ ДФ оценить не удалось. По номограмме выявлен средний риск ДФ.
ФП расценена как клинически не значимая. Принято решение воздержаться от интервенционного лечения нарушений ритма сердца.
Через 6 месяцев наблюдения - пароксизмы ФП не рецидивируют. По данным трансторакальной ЭХОКГ - нарушений систолической и ДФ сердца нет.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ оценки клинической значимости фибрилляции предсердий при определении показаний к интервенционному лечению фибрилляции предсердий | 2022 |
|
RU2791191C1 |
| Способ персонализации подхода к интервенционному лечению фибрилляции предсердий | 2022 |
|
RU2791135C1 |
| Способ выбора метода визуализации транссептальной катетеризации левого предсердия | 2022 |
|
RU2791130C1 |
| Способ выбора метода катетерной изоляции легочных вен у пациентов с фибрилляцией предсердий | 2020 |
|
RU2731963C1 |
| СПОСОБ ЛЕЧЕНИЯ ПАРОКСИЗМАЛЬНОЙ ФОРМЫ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ У ПАЦИЕНТОВ С ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТЬЮ ПРИ АРТЕРИАЛЬНОЙ ГИПЕРТОНИИ | 2019 |
|
RU2703517C1 |
| Способ предоперационного прогнозирования риска развития поздних рецидивов фибрилляции предсердий после первичной процедуры эндокардиальной радиочастотной аблации | 2021 |
|
RU2767133C1 |
| СПОСОБ ОДНОВРЕМЕННОЙ ХИРУРГИЧЕСКОЙ КОРРЕКЦИИ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ И ПАТОЛОГИИ АТРИОВЕНТРИКУЛЯРНЫХ КЛАПАНОВ | 2017 |
|
RU2644924C1 |
| СПОСОБ ЛЕЧЕНИЯ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ У ПАЦИЕНТОВ С АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИЕЙ | 2010 |
|
RU2477158C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РЕЦИДИВА ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ В ОТДАЛЕННЫЕ СРОКИ ПОСЛЕ ОПЕРАЦИИ РАДИОЧАСТОТНОЙ АБЛАЦИИ УСТЬЕВ ЛЕГОЧНЫХ ВЕН У БОЛЬНЫХ С ПЕРЕДНЕ-ЗАДНИМ РАЗМЕРОМ ЛЕВОГО ПРЕДСЕРДИЯ НЕ БОЛЕЕ 5,0 СМ | 2017 |
|
RU2644939C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АНАТОМИИ СЕРДЦА И КРУПНЫХ СОСУДОВ | 2013 |
|
RU2539993C2 |

Изобретение относится к области медицины, а именно к кардиологии и сердечно-сосудистой хирургии, и может быть использовано при персонализированном определении показаний к интервенционному лечению больных фибрилляцией предсердий (ФП). Способ осуществляют поэтапно по блокам. Блок 1 включает оценку систолической функции сердца по данным трансторакальной эхокардиографии. Если систолическая функция сердца нарушена, то считают фибрилляцию предсердий клинически значимой и проведение интервенционного лечения больному показанным. Если систолическая функция сердца не нарушена, то оценивают диастолическую функцию сердца по данным трансторакальной эхокардиографии. Если диастолическая функция сердца не нарушена, то оценивают фибрилляцию предсердий как клинически незначимую и считают, что интервенционное лечение больному не показано. Если диастолическая функция сердца нарушена, то переходят к блоку 3 алгоритма. Если диастолическую функцию сердца по данным трансторакальной эхокардиографии оценить не удается, то используют номограмму оценки риска диастолической дисфункции с учетом возраста больного в годах и длительности аритмического анамнеза в месяцах, как указано на фиг. 1. Если определяют высокий и очень высокий риск диастолической дисфункции, то считают, что диастолическая функция сердца нарушена и переходят к блоку 2. Если определяют средний риск диастолической дисфункции, считают, что диастолическая функция сердца не нарушена и интервенционное лечение не показано. Блок 2 включает проведение неинвазивного электрофизиологического картирования сердца с локализацией роторной активности в предсердиях, состоящее из последовательных этапов. Осуществляют регистрацию многоканальной поверхностной электрокардиограммы (ЭХО КГ). Выполняют мультиспиральную компьютерную томографию сердца с контрастированием (МСКТ); синхронизируют ЭХО КГ и МСКТ с получением воксельной и полигональной моделей предсердий. Затем выбирают фрагмент электрокардиограммы для анализа. Осуществляют глобальную полосовую фильтрацию от 3 до 9 Гц выбранного участка электрокардиограммы. Выполняют расчет карт активации с восстановлением нефильтрованного сигнала в стандартном отведении. Выбирают участок с максимальной паузой между соседними комплексами QRS - интервал T-q. Осуществляют выбор фазовой изопотенциальной карты. Выбирают левую и правую границы «окна интереса», где визуализируют электрическую активность только предсердий. Выполняют анализ роторной активности на изопотенциальной фазовой карте. Осуществляют анализ роторной активности на карте плотности фазовых сингулярностей. При определении локализации роторной активности в предсердиях переходят к блоку 3. Если роторная активность в предсердиях не локализуется, то считают, что выполнение интервенционного лечения не показано. Блок 3 включает осуществление МСКТ сердца с контрастированием, при этом оценивают тип впадения легочных вен в левое предсердие: тип 1 - типичная анатомия: наличие четырех раздельных устьев легочных вен; тип 2 - рассыпной тип: наличие трех и более ипсилатеральных устьев легочных вен; тип 3 - ствол левых легочных вен: левая верхняя и нижняя легочные вены сливаются в один ствол до впадения в левое предсердие, правые легочные вены впадают в левое предсердие двумя раздельными устьями; тип 4 - смешанный тип: сочетание ствола легочных вен с одной стороны и рассыпного типа с другой; тип 5 - ствол контралатеральных легочных вен: слияние контралатеральных легочных вен в один ствол до впадения в левое предсердие; тип 6 - ствол правых легочных вен: правые легочные вены сливаются в общий ствол до впадения в левое предсердие. Если определяют тип 1, тип 2 или тип 4, то оценивают фибрилляцию предсердий как клинически значимую и считают, что проведение интервенционного лечения больному показано. Если определяют тип 3, тип 5 или тип 6, то оценивают фибрилляцию предсердий как клинически незначимую и считают, что интервенционное лечение больному не показано. Способ позволяет осуществить персонализированную оценку клинической значимости ФП, уточнить показания к интервенционному лечению больных ФП, на основе поэтапного анализа морфо-функциональных особенностей сердечно-сосудистой системы, при невозможности определения диастолической функции сердца по данным трансторакальной эхокардиографии. 2 ил., 5 пр.
Способ определения показаний к проведению интервенционного лечения больных с непароксизмальными формами фибрилляции предсердий с учетом клинических, функциональных и электрофизиологических данных, отличающийся тем, что соблюдают последовательность действий, а именно:
блок 1:
оценивают систолическую функцию сердца по данным трансторакальной эхокардиографии; если систолическая функция сердца нарушена, то считают фибрилляцию предсердий клинически значимой и проведение интервенционного лечения больному показанным;
если систолическая функция сердца не нарушена, то оценивают диастолическую функцию сердца по данным трансторакальной эхокардиографии;
если диастолическая функция сердца не нарушена, то оценивают фибрилляцию предсердий как клинически незначимую и считают, что интервенционное лечение больному не показано;
если диастолическая функция сердца нарушена, то переходят к блоку 3 алгоритма;
если диастолическую функцию сердца по данным трансторакальной эхокардиографии оценить не удается, то оценивают риск нарушения диастолической функции сердца в соответствии с номограммой, приведенной на фигуре 1;
если при помощи номограммы, приведенной на фигуре 1, определяют средний риск нарушения диастолической функции сердца, то считают, что диастолическая функция сердца не нарушена, и считают, что интервенционное лечение больному не показано;
если при помощи номограммы, приведенной на фигуре 1, определяют высокий и очень высокий риск нарушения диастолической функции сердца, то считают, что диастолическая функция сердца нарушена и переходят к блоку 2;
блок 2:
проводят неинвазивное электрофизиологическое картирование сердца с определением роторной активности в предсердиях, состоящее из последовательных этапов, а именно:
регистрируют многоканальную поверхностную электрокардиограмму;
выполняют мультиспиральную компьютерную томографию сердца с контрастированием;
синхронизируют многоканальную поверхностную электрокардиограмму и мультиспиральную компьютерную томограмму сердца с получением воксельной и полигональной моделей предсердий;
выбирают фрагмент многоканальной поверхностной электрокардиограммы для анализа с максимальным интервалом RR с последующей обработкой электрической активности предсердий:
- выбирают и удаляют все QRS комплексы на отведениях многоканальной поверхностной электрокардиограммы;
- устанавливают глобальную полосу фильтрации выбранного участка электрокардиограммы в диапазоне от 3 до 9 Гц;
- выбирают максимальный T-q интервал на многоканальной поверхностной электрокардиограмме;
- выполняют анализ роторной активности на изопотенциальной фазовой карте;
- осуществляют анализ роторной активности на карте плотности фазовых сингулярностей;
если определить роторную активность в предсердиях не удается, то считают, что выполнение интервенционного лечения нецелесообразно;
если определить роторную активность в предсердиях удается, то считают, что в этом случае проведение интервенционного лечения целесообразно и переходят к блоку 3 алгоритма;
блок 3:
выполняют мультиспиральную компьютерную томографию сердца с контрастированием и оценивают тип впадения легочных вен в левое предсердие:
- тип 1 - типичная анатомия: наличие четырех раздельных устьев легочных вен;
- тип 2 - рассыпной тип: наличие трех и более ипсилатеральных устьев легочных вен;
- тип 3 - ствол левых легочных вен: левая верхняя и нижняя легочные вены сливаются в один ствол до впадения в левое предсердие, правые легочные вены впадают в левое предсердие двумя раздельными устьями;
- тип 4 - смешанный тип: сочетание ствола легочных вен с одной стороны и рассыпного типа с другой;
- тип 5 - ствол контралатеральных легочных вен: слияние контралатеральных легочных вен в один ствол до впадения в левое предсердие;
- тип 6 - ствол правых легочных вен: правые легочные вены сливаются в общий ствол до впадения в левое предсердие;
если определяют тип 1, тип 2 или тип 4, то оценивают фибрилляцию предсердий как клинически значимую и считают, что проведение интервенционного лечения больному показано;
если определяют тип 3, тип 5 или тип 6, то оценивают фибрилляцию предсердий как клинически незначимую и считают, что интервенционное лечение больному не показано.
| Хамнагадаев И | |||
| А., ПЕРСОНАЛИЗИРОВАННЫЙ ПОДХОД К ИНТЕРВЕНЦИОННОМУ ЛЕЧЕНИЮ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ, АВТОРЕФЕРАТ, Москва 2024 | |||
| Способ отбора пациентов с длительно персистирующей формой фибрилляции предсердий на проведение эффективного катетерного лечения | 2020 |
|
RU2749552C1 |
| Способ персонализации подхода к интервенционному лечению фибрилляции предсердий | 2022 |
|
RU2791135C1 |
| СПОСОБ ЛЕЧЕНИЯ ПАРОКСИЗМАЛЬНОЙ ФОРМЫ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ У ПАЦИЕНТОВ С ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТЬЮ ПРИ АРТЕРИАЛЬНОЙ ГИПЕРТОНИИ | 2019 |
|
RU2703517C1 |
| V | |||
| Laurent et al, Incidence and predictive factors of atrial fibrillation after ablation of typical atrial flutter, J | |||
| Interv | |||
| Card | |||
Авторы
Даты
2025-04-01—Публикация
2024-12-27—Подача