Изобретение относится к области медицины, а именно к кардиологии и сердечно-сосудистой хирургии, и может быть использовано для персонализации подхода к выбору метода визуализации транссептальной катетеризации левого предсердия в ходе интервенционного лечения фибрилляций предсердий (ФП).
ФП в настоящее время является одной из распространенных аритмий, которая диагностируется у 0,4% населения земного шара и ассоциирована с высоким риском инвалидизации и смертности вследствие кардиогенных тромбоэмболий, а также развития и декомпенсации хронической сердечной недостаточности (Wilke T., Groth A., Mueller S., Pfannkuche M., Verheyen, et al. Incidence and prevalence of atrial fibrillation: an analysis based on 8.3 million patients. Europace. 2013; 15(4): 486-493. doi: 10.1093/europace/eus333; Camm A., Lip G., De Caterina R., et al. ESC Committee for Practice Guidelines (CPG). 2012 focused update of the ESC Guidelines for the management of atrial fibrillation: an update of the 2010 ESC Guidelines for the management of atrial fibrillation. Developed with the special contribution of the European Heart Rhythm Association. European Heart Journal, 33(21), 2719-2747. doi: 10.1093/eurheartj/ehs253; Calkins H., Kuck K.H., Cappato R., et al. 2012 HRS/EHRA/ECAS expert consensus statement on catheter and surgical ablation of atrial fibrillation: recommendations for patient selection, procedural techniques, patient management and follow-up, definitions, endpoints, and research trial design. Heart Rhythm. 2012; 9(4): 632-696. doi: 10.1016/j.hrthm.2011.12.016). Одной из ведущих причин возникновения ФП может быть эктопическая активность в легочных венах (ЛВ). Их электрическая изоляция от миокарда левого предсердия (ЛП) позволяет снизить вероятность развития ФП (Haissaguerre M., Jaïs P., Shah D., et al. Spontaneous initiation of atrial fibrillation by ectopic beats originating in the pulmonary veins. New England Journal of Medicine. 1998; 339 (10): 659-666. doi: 10.1056/NEJM199809033391003).
Для достижения данного результата в большинстве случаев применяются малоинвазивные хирургические технологии: криобаллонная и радиочастотная изоляция легочных вен (ЛВ). Ключевым этапом данного хирургического лечения является транссептальная катетеризация ЛП, которая заключается в выполнении пункции межпредсердной перегородки в области овальной ямки транссептальной иглой, по которой в левое предсердие проводится интродьюсер для установки инструментов в ЛП (Thakur R., Natale A. Transseptal catheterization and interventions. - Cardiotext Publishing, 2010). Среди жизнеугрожающих осложнений транссептальной катетеризации ЛП являются перфорация аорты, правого предсердия, ЛП, ЛВ и левого желудочка. Основным проявлением данных осложнений является тампонада сердца, частота развития которой может достигать 6%. Для устранения данных осложнений требуется выполнение дренирования перикарда, а в ряде случаев и выполнение экстренной операции в условиях искусственного кровообращения. (Ellis E. R. et al. Trends in utilization and complications of catheter ablation for atrial fibrillation in Medicare beneficiaries //Heart rhythm. - 2009. - Т. 6. - №. 9. - С. 1267-1273; Cappato R. et al. Worldwide survey on the methods, efficacy, and safety of catheter ablation for human atrial fibrillation // Circulation. - 2005. - Т. 111. - №. 9. - С. 1100-1105; Cappato R. et al. Updated worldwide survey on the methods, efficacy, and safety of catheter ablation for human atrial fibrillation //Circulation: Arrhythmia and Electrophysiology. - 2010. - Т. 3. - №. 1. - С. 32-38; HSU L. I. F. et al. Incidence and prevention of cardiac tamponade complicating ablation for atrial fibrillation //Pacing and Clinical Electrophysiology. - 2005. - Т. 28. - С. S106-S109). С целью предотвращения данных осложнений в дополнение к флюороскопическому контролю могут применяться дополнительные методы визуализации, такие как: транспищеводная или внутрисердечная эхокардиография (Thakur R., Natale A. Transseptal catheterization and interventions. - Cardiotext Publishing, 2010.). Несмотря на то, что дополнительные методы визуализации могут значительно снизить или полностью исключить возможность развития данных осложнений, их применение ограничено стоимостью расходных материалов и дополнительного оборудования. Алгоритмы, позволяющие персонализировано подойти к выбору метода визуализации в настоящее время не разработаны.
Известен способ (RU 2724191 C1, опубликовано 22.06.2020), описывающий способ визуализации сердца, в котором проводят мультиспиральную компьютерную томографию (МСКТ), с получением 3D изображения сердца, получают интраоперационно электроанатомическую модель камеры сердца с помощью системы навигационного картирования и совмещают эти изображения. Совмещение изображений проводят по выбранным точкам и корректируют положение изображений по анатомическим ориентирам: бифуркация правых, левых легочных вен, крыша левого предсердия, основание ушка левого предсердия. Способ позволяет получать точную компьютерную модель камеры сердца, обеспечивая повышение точности и эффективности проведения интервенционного лечения при нарушениях ритма сердца
Недостатками данного способа является то, что в ходе предоперационной подготовки не обеспечивается персонализация подхода к выбору метода визуализации транссептальной катетеризации ЛП при интервенционном лечении ФП с учетом данных МСКТ сердца.
Известен способ (RU 2723225 C1 опубликовано 09.06.2020), в котором описывается способ визуализации сердца при проведении хирургического лечения нарушений ритма сердца, при котором проводят электрофизиологическое картирование, МСКТ грудной клетки, регистрацию электрокардиограмм, что обеспечивает визуализацию результатов реконструкции распределения электрического поля сердца в режиме реального времени, определение очага аритмии.
Недостатками данного способа является то, что в ходе предоперационной подготовки не обеспечивается персонализация подхода к выбору метода визуализации транссептальной катетеризации ЛП при интервенционном лечении ФП с учетом данных МСКТ сердца.
Известен способ (US 7877128 B2, опубликовано 25.01.2011) предоперационного планирования, включающий предоперационное моделирование катетеризации левого предсердия, получение изображения сердца, оценку анатомии сердца с использованием трехмерной ультразвуковой визуализации, МСКТ сердца, электроанатомического картирования и выполнение операции на сердце на основе полученных данных.
Недостатками данного способа является то, что в ходе предоперационной подготовки не обеспечивается персонализация подхода к выбору метода визуализации транссептальной катетеризации ЛП при интервенционном лечении ФП с учетом данных МСКТ сердца.
Известен способ (КАШТАНОВА Н.Ю. Методики томографической визуализации ушка левого предсердия при планировании интервенционного лечения фибрилляции предсердий. Медицинская визуализация, 2020; 24 (3): 88-106 [доступен онлайн: Методики томографической визуализации ушка левого предсердия при планировании интервенционного лечения фибрилляции предсердий], раскрывающий обоснование важности визуализации ушка левого предсердия для уточнения наличия тромбов методом томографической визуализации перед процедурой интервенционного лечения фибрилляции предсердий, так как это позволяет в течение одного исследования получить детальную информацию об анатомии, функции интересующих структур, исключить тромбоз ушка ЛП и также предположить эффективность операции на основании распространенности фиброза миокарда (стр. 100).
Недостатками данного способа является то, что: в ходе предоперационной подготовки не обеспечивается персонализация подхода к выбору метода визуализации транссептальной катетеризации ЛП при интервенционном лечении ФП с учетом данных МСКТ сердца.
Известен способ (D'SILVA A. Advances in Imaging for Atrial Fibrillation Ablation. Radiology Research and Practice Volume 2011, 1-10, [доступно онлайн: Advances in Imaging for Atrial Fibrillation Ablation]), в котором описываются варианты визуализации левого предсердия, моделирование катетеризации левого предсердия путем электроанатомического картирования сердца, использование предоперационного МСКТ и интеграции полученных данных.
Недостатками данного способа является то, что: в ходе предоперационной подготовки не обеспечивается персонализация подхода к выбору метода визуализации транссептальной катетеризации ЛП при интервенционном лечении ФП с учетом данных МСКТ сердца.
Наиболее близким аналогом разработанного нами способа является способ (THAI W. Preprocedural Imaging for Patients with Atrial Fibrillation and Heart Failure. Curr Cardiol Rep, 2012, 14(5), 584-592 [доступен онлайн: (Preprocedural Imaging for Patients with Atrial Fibrillation and Heart Failure.]), в котором описывается использование МСКТ, магнитно-резонансной томографии сердца и методов электроанатомического картирования в качестве методик визуализации ЛВ и ЛП перед процедурой интервенционного лечения ФП. Причем выбор той или иной методики визуализации осуществляют, исходя из возможности и опыта специалистов и доступного оборудования. При визуализации оценивают количество, характер ветвления ЛВ, особенности их анатомического строения и аномалии. Также оценивают строение, размеры ЛП, наличие в нем тромбов и взаимосвязь с окружающими анатомическими структурами. Предоперационная визуализация сердца у пациентов с ФП обеспечивает получение важной анатомической и функциональной информации, облегчает выбор показаний для хирургического лечения, улучшает клинические результаты.
Недостатками данного способа является то, что в ходе предоперационной подготовки не обеспечивается персонализация подхода к выбору метода визуализации транссептальной катетеризации ЛП при интервенционном лечении ФП с учетом данных МСКТ сердца.
Технической проблемой, на решение которой направлено, настоящее изобретение, является оптимизация протокола выбора способа визуализации транссептальной катетеризации ЛП в ходе интервенционного лечения фибрилляции предсердий.
Раскрытие изобретения
Техническим результатом, достигаемым при реализации разработанного способа, является снижение количества жизнеугрожающих осложнений и сокращение времени транссептальной катетеризации ЛП за счет персонализации метода визуализации транссептальной катетеризации ЛП, что позволяет определить оптимальную методику визуализации в ходе интервенционного лечения фибрилляции предсердий и избежать необходимости репозиционирования транссептальной иглы в правом предсердии.
Указанные аспекты технического результата достигаются благодаря следующей совокупности существенных признаков:
Выполняют МСКТ сердца с контрастированием и последующим предоперационным моделированием при выполнении транссептальной катетеризации ЛП по данным МСКТ путем выполнения последовательности действий, а именно: визуализируют устье коронарного синуса и определяют его скелетотопию по отношению к грудным позвонкам; определяют ход коронарного синуса по отношению к первому разветвлению левого главного бронха; при помощи комплексного анализа данных МСКТ моделируют ультразвуковое изображение, получаемое при транспищеводной эхокардиографии, межпредсердной перегородки и овальной ямки в бикавальной проекции и по короткой оси на уровне синусов Вальсальвы; определяют взаимоотношение первого разветвления левого главного бронха по отношению к коллектору левых легочных вен; с учетом проведенного предоперационного моделирования определяют метод интраоперационной визуализации для транссептальной катетеризации левого предсердия при интервенционном лечении фибрилляции предсердий путем определения количества баллов, а именно: устье коронарного синуса не деформировано и его катетеризация диагностическим электродом возможна: да - 4 балла; нет - 0 баллов; ось, соединяющая центр овальной ямки и центр коллектора левых легочных вен параллельна ходу коронарного синуса: да - 1 балл; нет - 0 баллов; ось, соединяющая центр овальной ямки и центр коллектора левых легочных вен, и ось, соединяющая центр овальной ямки и первое разветвление левого главного бронха, лежат в плоскости параллельной ходу коронарного синуса: да - 1 балл; нет - 0 баллов; центр овальной ямки можно визуализировать при одновременном моделировании транспищеводного ультразвукового изображения межпредсердной перегородки и овальной ямки в бикавальной проекции и проекции по короткой оси на уровне синусов Вальсальвы: да - 6 балла; нет - 4 балла; набранные балы суммируют: если набрано 12 баллов, то для транссептальной катетеризации левого предсердия выбирают рентгеноскопический контроль; если набрано 9-11 баллов, то для транссептальной катетеризации левого предсердия выбирают транспищеводный эхокардиографический контроль; если набрано менее 9 баллов, то для транссептальной катетеризации левого предсердия выбирают внутрисердечную эхокардиографию.
Краткое описание чертежей.
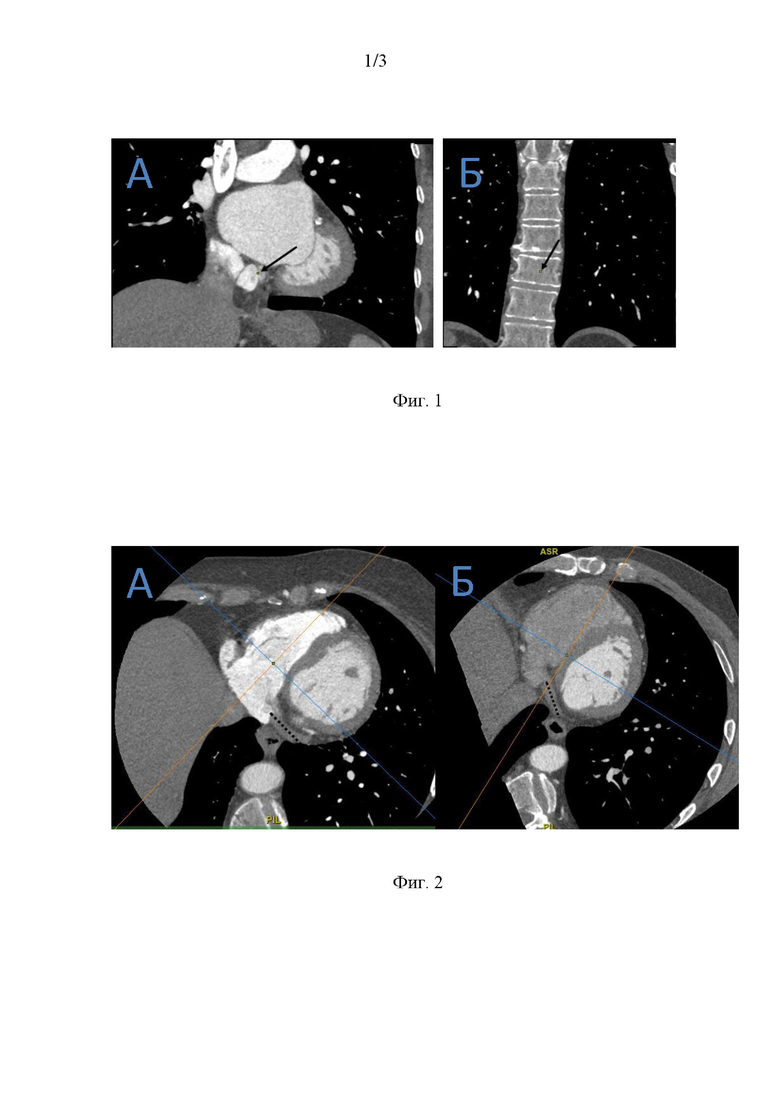
На фиг. 1 представлена оценка формы устья коронарного синуса (А) и его скелетотопия (Б) по данным мультиспиральной компьютерной томографии в корональной проекции. Устье коронарного синуса отмечено стрелкой.
На фиг. 2 представлена оценка хода коронарного синуса по отношению к первому разветвлению левого главного бронха по данным мультиспиральной компьютерной томографии в косой проекции.
Примечание:
А - ось, соединяющая центр овальной ямки и центр коллектора левых легочных вен, и ось, соединяющая центр овальной ямки и первое разветвление левого главного бронха (синяя линия), лежит в плоскости параллельной ходу коронарного синуса (пунктирная линия);
Б - ось, соединяющая центр овальной ямки и центр коллектора левых легочных вен, и ось, соединяющая центр овальной ямки и первое разветвление левого главного бронха (синяя линия), не лежит в плоскости параллельной ходу коронарного синуса (пунктирная линия).
На фиг. 3 представлено моделирование транспищеводного ультразвукового изображения межпредсердной перегородки и овальной ямки в бикавальной позиции по данным мультиспиральной компьютерной томографии в косой проекции.
Примечание:
А - центр овальной ямки удается визуализировать;
Б - центр овальной ямки визуализировать не удается.
На фиг. 4 представлено моделирование транспищеводного ультразвукового изображения межпредсердной перегородки и овальной ямки по короткой оси на уровне синусов Вальсальвы по данным мультиспиральной компьютерной томографии в косой проекции.
Примечание:
А - центр овальной ямки удается визуализировать;
Б - центр овальной ямки визуализировать не удается.
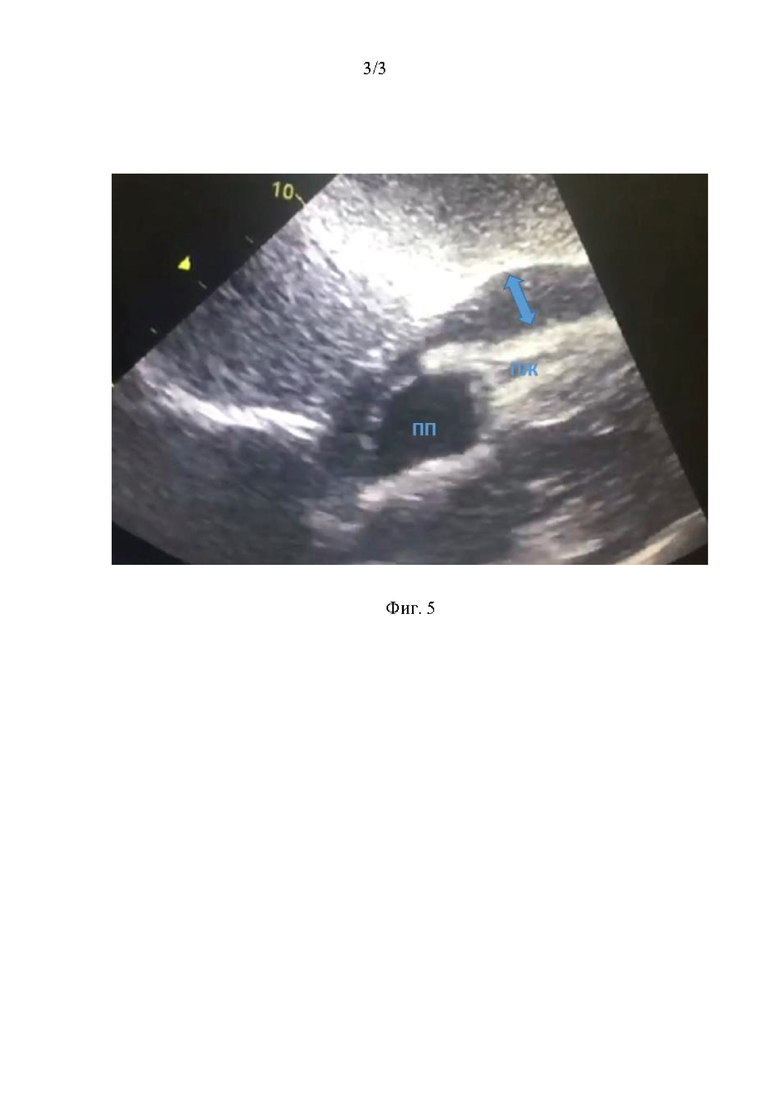
На фиг. 5 представлена тампонада сердца. Трансторакальная эхокардиография (субкостальная позиция).
Примечание:
ПП - правое предсердие;
ПЖ - правый желудочек (коллабирован); синей стрелкой обозначена сепарация листков перикарда (кровь в перикарде).
Для разработки способа, изучены результаты интервенционного лечения ФП у 156 пациентов. Пациенты разделены на две группы.
Группа 1 - выбор подхода к визуализации транссептальной катетеризации левого предсердия при интервенционном лечении ФП проводился без учета данных МСКТ.
Группа 2 - выбор подхода к визуализации транссептальной катетеризации левого предсердия при интервенционном лечении ФП проводился по предлагаемому способу.
Пациенты групп 1 и 2 были сопоставимы по возрасту и полу, сопутствующим и фоновым заболеваниям, тяжести клинических проявлений, а также риска развития кардиогенных тромбоэмболий. При сравнении групп 1 и 2 по данным параметрам статистически значимых различий выявлено не было. Так в группе 1 возраст пациентов колебался в диапазоне 29-77 лет, медиана возраста составили 61,5 лет (IQR 52-67) лет, группу 2 составили пациенты в возрасте 32-74 года, медиана возраста также составила 61,5 (IQR 55-65) лет. В обеих группах большую часть составляли пациенты мужского пола. Максимальная продолжительность как аримтического анамнеза, так и приема антиаритмической терапии в группе 1 достигала 240 месяцев, а в группе 2 - 360 месяцев. При оценке индекса массы тела установлено, что большая часть пациентов страдала ожирением. В группе 1 у 58 (74,36%) пациентов диагностировано ожирение, а в группе 2 - у 48 (61,54%) больных. Реже у пациентов была избыточная масса тела и была выявлена в группе 1 у 15 (19,23%) пациентов, а в группе 2 - у 21 (26,92%) больного. Нормальная масса тела встречалась реже всего и была выявлена в группе 1 у 5 (6,41%) пациентов и у 9 (11,54%) в группе 2. Дефицит массы тела не был выявлено ни в одном случае.
При оценке формы ФП установлено, что в группе 1 чаще всего диагностировалась пароксизмальная форма ФП и была выявлена у 58 (74,36%) пациентов, а в группе 2 - 59 (75,64%). Персистирующая форма ФП выявлялась реже и была диагностирована в группе 1 у 20 (25,64%) пациентов, а в группе 2 - у 19 (24,36%) больных. Артериальная гипертония явилась одним из часто встречающихся фоновых состояний и была выявлена боле чем в половине случаев в группах 1 и 2 (n=62; 79,49% и n=68; 87,18% соответственно). Такое сопутствующее заболевание как сахарный диабет 2 типа был диагностирован редко и был выявлен в группе 1 у 7 (9,21%) пациентов, а в группе 2 - у 13 (16,88%) больных. Реже диагностировалась у пациентов ишемическая болезнь сердца и была выявлена в группе 1 у 5 (6,41%) пациентов, а в группе 2 - у 4 (5,13%) больных. Также редко встречалась хроническая обструктивная болезнь легких и была выявлена в группе 1 у 3 (3,85%) пациентов, а в группе 2 - у 5 (6,41%) больных. Наличие хронической сердечной недостаточности было выявлено в группе 1 у 16 (20,51%) пациентов, а в группе 2 - у 13 (16,67%) больных.
Клиническая характеристика пациентов в группах 1 и 2 приведена в таблице 1.
Мужской пол - 48 (51,1%)
Персистирующая форма - 17 (18,1%)
При анализе данных МСКТ оценивалась форма и скелетотопия устья коронарного синуса (фиг. 1), ход коронарного синуса по отношения первому разветвлению левого главного бронха (фиг. 2). Выполнялось моделирование проекций, получаемых при транспищеводной эхокардиографии. Определялась возможность визуализировать центр овальной ямки в бикавальной проекции (фиг. 3) и в проекции по короткой оси (фиг. 4).
Учитывалось количество кровотечений в полость перикарда после транссептальной катетеризации ЛП.
Выявлено, что в группе 1 количество кровотечений в полость перикарда после транссептальной катетеризации ЛП развилось в 4-х случаях (фиг. 5). Во всех случаях потребовалось дренирование перикарда. Кровопотеря колебалась от 200-800 мл.
В группе 2 кровотечение в полость перикарда выявлено не было ни в одном случае.
При оценке времени, которое было необходимо для транссептальной катетеризации выявлено, что в группе 1 время, которое было затрачено на выполнение транссептальной катетеризации ЛП было статистически значимо больше, чем таковое в группе 2, что было обусловлено необходимостью репозиционирования транссептальной иглы в правом предсердии для достижения оптимальной позиции на фоне неудовлетворительной визуализации. Выявлено, что вероятность успешной транссептальной катетеризации ЛП с первой попытки было выше с группе 2. Последний факт объясняется тем, что в группе 2 выбор метода визуализации был основан на индивидуальный анатомических особенностях пациента, что позволяло персонифицировать протокол транссептальной катетеризации ЛП.
Клинический пример 1
Пациент 58 лет мужского пола.
Диагноз: пароксизмальная форма ФП. EHRA 2b.
Жалобы на приступы сердцебиения, ограничивающие повседневную физическую активность.
По данным анамнестических электрокардиограмм (ЭКГ) - ФП с частотой активации желудочков сердца - 85-98 в минуту.
Определены показания к интервенционному лечению ФП.
По данным МСКТ устье коронарного синуса не деформировано и его катетеризация диагностическим электродом возможна (4 балла); ось, соединяющая центр овальной ямки и центр коллектора левых легочных вен параллельна ходу коронарного синуса (1 балл); ось, соединяющая центр овальной ямки и центр коллектора левых легочных вен, и ось, соединяющая центр овальной ямки и первое разветвление левого главного бронха, лежат в плоскости параллельной ходу коронарного синуса (1 балл); центр овальной ямки можно визуализируется при одновременном моделировании транспищеводного ультразвукового изображения межпредсердной перегородки и овальной ямки в бикавальной проекции и проекции по короткой оси на уровне синусов Вальсальвы (6 баллов). Набрано 12 баллов. В связи с этим, для транссептальной катетеризации левого предсердия выбирали рентгеноскопический контроль. Во время оперативного вмешательства транссептальная игла успешно позиционирована в области овальной ямки по стандартным флюороскопическим ориентирам. Транссептальная катетеризация ЛП выполнена с первой попытки. Кровотечения в полость перикарда отмечено не было.
Клинический пример 2
Пациент 38 лет мужского пола.
Диагноз: пароксизмальная форма ФП. EHRA 2b.
Жалобы на приступы сердцебиения, ограничивающие повседневную физическую активность.
По данным анамнестических электрокардиограмм (ЭКГ) - ФП с частотой активации желудочков сердца - 74-105 в минуту.
Определены показания к интервенционному лечению ФП.
По данным МСКТ устье коронарного синуса не деформировано и его катетеризация диагностическим электродом возможна (4 балла); ось, соединяющая центр овальной ямки и центр коллектора левых легочных вен не параллельна ходу коронарного синуса (0 баллов); ось, соединяющая центр овальной ямки и центр коллектора левых легочных вен, и ось, соединяющая центр овальной ямки и первое разветвление левого главного бронха, не лежат в плоскости параллельной ходу коронарного синуса (0 баллов); центр овальной ямки визуализируется при одновременном моделировании транспищеводного ультразвукового изображения межпредсердной перегородки и овальной ямки в бикавальной проекции и проекции по короткой оси на уровне синусов Вальсальвы (6 баллов). Набрано 10 баллов. В связи с этим, для транссептальной катетеризации левого предсердия выбирали транспищеводный эхокардиографический контроль. Во время оперативного вмешательства транссептальная игла успешно позиционирована в области овальной ямки под контролем транспищеводной эхокардиографии. Транссептальная катетеризация ЛП выполнена с первой попытки. Кровотечения в полость перикарда отмечено не было.
Клинический пример 3
Пациентка 59 лет женского пола.
Диагноз: пароксизмальная форма ФП. EHRA 2b.
Жалобы на приступы сердцебиения, ограничивающие повседневную физическую активность.
По данным анамнестических (ЭКГ) - ФП с частотой активации желудочков сердца - 50-98 в минуту.
Определены показания к интервенционному лечению ФП.
По данным МСКТ устье коронарного синуса не деформировано и его катетеризация диагностическим электродом возможна (4 балла); ось, соединяющая центр овальной ямки и центр коллектора левых легочных вен не параллельна ходу коронарного синуса (0 баллов); ось, соединяющая центр овальной ямки и центр коллектора левых легочных вен, и ось, соединяющая центр овальной ямки и первое разветвление левого главного бронха, не лежит в плоскости параллельной ходу коронарного синуса (0 баллов); центр овальной ямки не возможно визуализировать при одновременном моделировании транспищеводного ультразвукового изображения межпредсердной перегородки и овальной ямки в бикавальной проекции и проекции по короткой оси на уровне синусов Вальсальвы (4 балла). Набрано 8 баллов. В связи с этим для транссептальной катетеризации левого предсердия выбирали внутрисердечную эхокардиографию. Во время оперативного вмешательства транссептальная игла успешно позиционирована в области овальной ямки под контролем внутрисердечной эхокардиографии. Транссептальная катетеризация ЛП выполнена с первой попытки. Кровотечения в полость перикарда отмечено не было.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ персонализации подхода к интервенционному лечению фибрилляции предсердий | 2022 |
|
RU2791135C1 |
| СПОСОБ ИНТЕРВЕНЦИОННОГО ЛЕЧЕНИЯ ПАРОКСИЗМАЛЬНОЙ ФОРМЫ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ | 2007 |
|
RU2364370C1 |
| Способ транссептальной пункции при криобаллонной аблации устьев легочных вен | 2019 |
|
RU2724491C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АНАТОМИИ СЕРДЦА И КРУПНЫХ СОСУДОВ | 2013 |
|
RU2539993C2 |
| СПОСОБ МОБИЛИЗАЦИИ СЕРДЦА ПРИ ХИРУРГИЧЕСКОМ ЛЕЧЕНИИ ГИПЕРТРОФИЧЕСКОЙ ОБСТРУКТИВНОЙ КАРДИОМИОПАТИИ, ОСЛОЖНЕННОЙ ПОСТОЯННОЙ ФОРМОЙ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ | 2012 |
|
RU2511088C1 |
| Способ оценки клинической значимости фибрилляции предсердий при определении показаний к интервенционному лечению фибрилляции предсердий | 2022 |
|
RU2791191C1 |
| СПОСОБ МОДИФИЦИРОВАННОЙ ФРАГМЕНТАЦИИ ПРЕДСЕРДИЙ ПРИ КОРРЕКЦИИ ПРИОБРЕТЕННЫХ ПОРОКОВ СЕРДЦА, ОСЛОЖНЕННЫХ ФИБРИЛЛЯЦИЕЙ ПРЕДСЕРДИЙ | 2010 |
|
RU2476166C2 |
| СПОСОБ БИАТРЕАЛЬНОЙ КРИОАБЛАЦИИ С ХИРУРГИЧЕСКОЙ ОККЛЮЗИЕЙ УШКА ЛЕВОГО ПРЕДСЕРДИЯ ПОЛНОСТЬЮ ТОРАКОСКОПИЧЕСКИМ МЕТОДОМ ПРИ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ | 2024 |
|
RU2826346C1 |
| Способ изоляции ствола левой легочной вены, превышающего диаметр криобаллона | 2020 |
|
RU2757444C1 |
| СПОСОБ МОБИЛИЗАЦИИ СЕРДЦА ПРИ ХИРУРГИЧЕСКОМ ЛЕЧЕНИИ ГИПЕРТРОФИЧЕСКОЙ ОБСТРУКТИВНОЙ КАРДИОМИОПАТИИ ТРАНСАОРТАЛЬНЫМ ДОСТУПОМ | 2012 |
|
RU2511246C2 |

Изобретение относится к медицине, а именно к кардиологии и сердечно-сосудистой хирургии, и может быть использовано для выбора метода визуализации при выполнении транссептальной катетеризации левого предсердия (ЛП). Проводят предоперационное моделирование по данным мультиспиральной компьютерной томографии сердца с контрастированием. Визуализируют устье коронарного синуса. Определяют ход коронарного синуса по отношению к первому разветвлению левого главного бронха. Моделируют ультразвуковое изображение межпредсердной перегородки и овальной ямки в бикавальной проекции и по короткой оси на уровне синусов Вальсальвы. Определяют положение центра овальной ямки по двум проекциям: бикавальная проекция и проекция по короткой оси на уровне синусов Вальсальвы по отношению к грудным позвонкам. Определяют взаимоотношение первого разветвления левого главного бронха по отношению к коллектору левых легочных вен. Выявленные признаки оценивают в баллах. Устье коронарного синуса не деформировано, и катетеризация коронарного синуса диагностическим электродом возможна: да – 4 балла; нет – 0 баллов. Ось, соединяющая центр овальной ямки и центр коллектора левых легочных вен, параллельна ходу коронарного синуса: да – 1 балл; нет – 0 баллов. Ось, соединяющая центр овальной ямки и центр коллектора левых легочных вен, и ось, соединяющая центр овальной ямки и первое разветвление левого главного бронха, лежат в плоскости, параллельной ходу коронарного синуса: да – 1 балл; нет – 0 баллов. Центр овальной ямки можно визуализировать при одновременном моделировании транспищеводного ультразвукового изображения межпредсердной перегородки и овальной ямки в бикавальной проекции и проекции по короткой оси на уровне синусов Вальсальвы: да – 6 баллов; нет – 4 балла. Если набрано 12 баллов, то при выполнении транссептальной катетеризации левого предсердия осуществляют рентгеноскопический контроль. Если набрано 9-11 баллов, то при выполнении транссептальной катетеризации левого предсердия осуществляют транспищеводный эхокардиографический контроль. Если набрано менее 9 баллов, то при выполнении транссептальной катетеризации левого предсердия осуществляют внутрисердечную эхокардиографию. Способ обеспечивает снижение количества жизнеугрожающих осложнений и сокращение времени транссептальной катетеризации ЛП, позволяет определить оптимальную методику визуализации в ходе интервенционного лечения фибрилляции предсердий и избежать необходимости репозиционирования транссептальной иглы в правом предсердии, проводить персонализацию метода визуализации транссептальной катетеризации ЛП за счет оценки комплекса наиболее значимых признаков при проведении предоперационного моделирования по данным мультиспиральной компьютерной томографии сердца с контрастированием. 5 ил., 1 табл., 3 пр.
Способ выбора метода визуализации при выполнении транссептальной катетеризации левого предсердия, включающий предоперационное моделирование по данным мультиспиральной компьютерной томографии сердца с контрастированием, а именно:
визуализируют устье коронарного синуса;
определяют ход коронарного синуса по отношению к первому разветвлению левого главного бронха;
моделируют ультразвуковое изображение межпредсердной перегородки и овальной ямки в бикавальной проекции и по короткой оси на уровне синусов Вальсальвы;
определяют положение центра овальной ямки по двум проекциям: бикавальная проекция и проекция по короткой оси на уровне синусов Вальсальвы по отношению к грудным позвонкам;
определяют взаимоотношение первого разветвления левого главного бронха по отношению к коллектору левых легочных вен;
выявленные признаки оценивают в баллах: устье коронарного синуса не деформировано, и катетеризация коронарного синуса диагностическим электродом возможна: да – 4 балла; нет – 0 баллов;
ось, соединяющая центр овальной ямки и центр коллектора левых легочных вен, параллельна ходу коронарного синуса: да – 1 балл; нет – 0 баллов;
ось, соединяющая центр овальной ямки и центр коллектора левых легочных вен, и ось, соединяющая центр овальной ямки и первое разветвление левого главного бронха, лежат в плоскости, параллельной ходу коронарного синуса: да – 1 балл; нет – 0 баллов;
центр овальной ямки можно визуализировать при одновременном моделировании транспищеводного ультразвукового изображения межпредсердной перегородки и овальной ямки в бикавальной проекции и проекции по короткой оси на уровне синусов Вальсальвы: да – 6 баллов; нет – 4 балла,
и если набрано 12 баллов, то при выполнении транссептальной катетеризации левого предсердия осуществляют рентгеноскопический контроль;
если набрано 9-11 баллов, то при выполнении транссептальной катетеризации левого предсердия осуществляют транспищеводный эхокардиографический контроль;
если набрано менее 9 баллов, то при выполнении транссептальной катетеризации левого предсердия осуществляют внутрисердечную эхокардиографию.
| СПОСОБ ТРЕХМЕРНОГО КАРТИРОВАНИЯ КАМЕР СЕРДЦА С ИСПОЛЬЗОВАНИЕМ НАВИГАЦИОННОЙ СИСТЕМЫ "АСТРОКАРД" ДЛЯ ЛЕЧЕНИЯ ПАЦИЕНТОВ С НАРУШЕНИЕМ РИТМА СЕРДЦА | 2019 |
|
RU2724191C1 |
| СПОСОБ И УСТРОЙСТВО ДЛЯ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ БОЛЬНЫХ СО СЛОЖНЫМИ НАРУШЕНИЯМИ РИТМА СЕРДЦА | 2019 |
|
RU2723225C1 |
| US 7877128 B2, 25.01.2011 | |||
| КАШТАНОВА Н.Ю | |||
| Методики томографической визуализации ушка левого предсердия при планировании интервенционного лечения фибрилляции предсердий | |||
| Медицинская визуализация, 2020; 24 (3): 88-106 | |||
| THAI W | |||
| Preprocedural Imaging for Patients with Atrial Fibrillation and Heart | |||
Авторы
Даты
2023-03-02—Публикация
2022-12-23—Подача