Изобретение относится к области анализа медицинских данных и предназначено для поддержки врачебных решений при постановке диагноза о наличии или отсутствии у пациента болезни Альцгеймера с высокой достоверностью.
Известно, что нейродегенеративные заболевания, такие как болезнь Альцгеймера (БА), трудно поддаются точной диагностике, особенно на ранних стадиях заболевания. Исследования последних 20 лет отмечают, что все больше людей подвержены болезням, связанным с головным мозгом, в том числе и БА. По данным 2020 года во всем мире насчитывается около 50 млн человек во всем мире, страдающих БА, в 2015 году было около 33,9 млн человек, в 2008 году число больных было менее 30 млн человек. Данные цифры указывают на стремительную прогрессивность данной болезни. Как показывают исследования распространенность данной болезни, как ожидается, утроится в течение следующих 40 лет (Gaugler J., James B., Marin A., Alzheimer's Association. 2019 Alzheimer's disease facts and figures // Alzheimer's & dementia. - 2019. - Т. 15. - №. 3. - С. 321-387). Не смотря на возможность выявления людей, генетически подверженных развитию БА, чаще всего предварительный диагноз ставится уже на стадии, когда нарушения когнитивных способностей человека становятся очевидными для клинических специалистов.
На данный момент существуют различные методики выявления БА, которые справляются с постановкой диагноза, однако появляется всё больше исследований и доказательств того, что БА может начаться задолго до возможности проведения какой-либо из существующих методов диагностики. Прогрессирование БА происходит постепенно, стадии её развития делят на 4 категории:
- предеменция;
- ранняя деменция;
- умеренная деменция;
- тяжелая деменция (Парфенов В.А., Захаров В.В., Преображенская И.С. Когнитивные расстройства. М.: Ремедиум, 2014).
Из-за отсутствия в настоящее время доступной терапии для предотвращения БА раннее выявление заболевания по-прежнему имеет первостепенное значение для отсрочки начала заболевания.
Известен способ диагностирования болезни Альцгеймера с помощью тестирования ДНК исследуемого индивида с целью определения полиморфизма rs 908832 в гене АВСА2 (RU 2380423 , опубл. 27.01.20210).
Один из главных недостатков данного способа состоит в том, что полиморфизм rs 908832 не является полностью предсказуемым для этой болезни, т.к. наличие или отсутствие данного полиморфизма не может с достоверностью показать развивается ли у индивида БА или нет. Другим недостатком такого прогноза является его ограниченность. Тестирование только одного полиморфизма не учитывает ряд других генетических и не генетических факторов, которые могут влиять на развитие заболевания. БА имеет сложную мультифакторную природу, и несколько геномных вариаций могут быть вовлечены в ее развитие. Кроме того, тестирование ДНК для определения полиморфизма rs 908832 в гене АВСА2 требует дорогостоящего и сложного генетического анализа, что делает его недоступным для широкого применения в клинической практике. Это ограничивает его эффективность при попытке определить риск развития БА на популяционном уровне или в общей медицинской практике.
Известен способ выявления БА с помощью исследования коры головного мозга. (RU 2169366 , опубл. 20.06.2001).
В данном способе диагностики исследуют биоптаты теменной, височной и лобной коры головного мозга, окрашивают их азотнокислым серебром, в препаратах определяют ядрышки нейронов, в которых отсутствуют аргентофильные гранулы (Ag-гранулы), и при их количестве не менее 20% диагностируют БА.
Основным недостатком данного способа является необходимость взятия образца ткани пациента, что может являться рискованным и отталкивающим фактором для пациента. Также проведение исследования требует высокой квалификации и опыта в области нейропатологии, такое исследование может быть проведено только специализированными медицинскими центрами, что требует значительных финансовых затрат.
Также известен способ комплексной лучевой диагностики доклинических и клинических стадий БА (RU 2315559, опубл. 27.01.2008), согласно которому проводится компьютерная томография головного мозга, после чего с помощью определенных расчетов определяют объемы массы правой и левой височных долей головного мозга, затем в условиях рентгеноперационной пациенту проводят по классической методике полипроекционную ангиографию головного мозга. При наличии уменьшения объема ткани височных долей головного мозга, а также крупного петлеобразования, множественных артерио-венозных шунтов в периферических отделах передних и средних мозговых артерий, питающих лобно-теменные отделы коры головного мозга, а также в передних ворсинчатых артериях, питающих височные отделы головного мозга, сочетающихся с редукцией капиллярного кровотока в этих отделах и образованием «капиллярных кратеров» и гиповаскулярных зон, наличием редукции венозных синусов в лобных отделах с образованием дополнительных аномальных венозных ветвей и развитием венозного застоя в лобно-теменных отделах головного мозга свидетельствуют о развитии болезни Альцгеймера.
Главный недостаток данного способа заключается в необходимости проведения двух исследований: компьютерная томография и ангиография головного мозга, что может быть затруднительно с учетом загруженности оборудования. Также для проведения ангиографии головного мозга требуется введение катетера в крупную артерию, что может вызвать некоторые риски, включая кровотечения, инфекции и аллергические реакции на использованный в данном способе контрастное вещество (Омнипак 350). В данной работе авторы также указывают, что в каждом из исследований требуется детальное рассмотрение снимков и достаточно много расчетов определенных параметров, производимых врачом, что повышает вероятность погрешности и недостаточной точности способа.
Известен способ диагностики БА на основе определения относительного содержания химически модифицированных форм металлсвязывающего домена бета-амилоида в биологических жидкостях (RU 2548759 , опубл. 20.04.2015), который является способом лабораторной диагностики БА посредством применения модифицированных по металлсвязывающему домену 1-16 форм бета-амилоида человека в качестве биомаркеров патогенеза БА. Способ характеризуется тем, что из денатурированного образца биологической жидкости, а именно крови, мочи, цереброспинальной жидкости, последовательно выделяют общую пептидную фракцию, затем фракцию бета-амилоида и, наконец, после направленного протеолиза фракцию фрагментов 1-16 бета-амилоида с ее последующим анализом. При обнаружении в образце биологической жидкости, модифицированной по металлсвязывающему домену формы бета-амилоида, изомеризованной по аспарагиновой кислоте в положении 7, при ее относительном содержании более 5% от общего количества фракции 1-16 бета-амилоида и/или при обнаружении модифицированной по металлсвязывающему домену формы бета-амилоида, фосфорилированной по серину в положении 8, диагностируют наличие БА.
Однако данный способ диагностики требует проведения сложных и высокотехнологичных анализов, которые могут быть дорогими и недоступными для всех медицинских учреждений. Также уровень модифицированных форм металлсвязывающего домена бета-амилоида может меняться со временем или быть подвержен влиянию других факторов, таких как возраст, пол, наличие других заболеваний и так далее, что может повлиять на точность и надежность диагностики.
Известен способ диагностирования болезни Альцгеймера с помощью определения количества митогенетически экспрессируемых маркеров поверхности клетки (RU 2426130, опубл. 10.08.2011).
Данный способ основан на определении количества митогенетически экспрессируемых маркеров поверхности клетки, предпочтительно CD69, периферически доступных клеток, например, клеток кожи или лимфоцитов.
Одним из недостатков способа является недостаточная специфичность и чувствительность метода. Присутствие или отсутствие этих маркеров может быть обусловлено не только болезнью Альцгеймера, но и другими патологическими состояниями или возрастными изменениями. Также, использование периферически доступных клеток в качестве исследуемого материала может привести к ошибкам интерпретации данных, так как состояние клеток в периферической крови или коже может не отражать состояние клеток, находящихся в нервной системе, где происходит развитие болезни Альцгеймера. Кроме того, данный способ может быть трудоемким и дорогостоящим, требующим специального оборудования и экспертизы для проведения анализа, и интерпретации результатов.
Известен способ выявления БА с помощью определения в крови маркеров системного воспаления. (RU 2781612 , опубл. 14.10.2022).
В данном способе определяют в крови маркеры системного воспаления, устанавливают выраженность системного воспаления, если уровень IgG ниже 10,0 г/л, определяют повышенный риск развития болезни Альцгеймера у лиц с aMCI. Если уровень IgG выше 10,0 г/л, определяют низкий риск развития болезни Альцгеймера у лиц с aMCI. Способ обеспечивает прогнозирование развития болезни Альцгеймера у лиц с aMCI за счет определения степени иммуновоспалительных нарушений путем выявления в крови больного уровня маркеров гуморального иммунитета, цитокинов и хемокинов, белков острой фазы.
Данный способ имеет множество недостатков. Основной из них так же, как и в предыдущем способе заключается в неспецифичности маркеров, то есть маркеры системного воспаления, такие как С-реактивный белок (СРБ), интерлейкины IL-1β, IL-8 и фактор некроза опухоли TNFα, являются неспецифичными для болезни Альцгеймера. Это означает, что их повышенный уровень может быть связан с другими состояниями и заболеваниями, включая инфекции, рак, ревматоидный артрит и сердечно-сосудистые заболевания. Поэтому интерпретация результатов анализа крови на маркеры системного воспаления требует специальных знаний и опыта. Полученные данные должны быть анализированы в контексте других клинических симптомов и результатов исследований, в следствие чего исключение других потенциальных причин повышенного уровня маркеров может занимать достаточно продолжительное время. Так же данный способ является достаточно дорогостоящим, так как анализ крови на маркеры системного воспаления требует специального оборудования и квалифицированного медицинского персонала, что сокращает доступность и возможность применения данного способа в широкой практике.
Также известен способ прогнозирования вероятности развития болезни Альцгеймера (RU 2663451, опубл. 06.08.2018), согласно которому проводят измерение в плазме крови человека энзиматической активности лейкоцитарной эластазы (ЛЭ) и функциональной активности α1-протеиназного ингибитора (α1-ПИ), в следствии чего и определяют вероятность развития болезни Альцгеймера.
Главный недостаток данного способа заключается в недостаточной достоверности результатов, так как уровень функциональной активности α1-протеиназного ингибитора может изменяться не только при болезни Альцгеймера, но и при других патологических состояниях, и энзиматическая активность лейкоцитарной эластазы может изменяться при различных воспалительных или инфекционных состояниях что может привести к ложноотрицательным результатам. Так же на данный момент нет единого стандарта для измерения энзиматической активности лейкоцитарной эластазы и функциональной активности α1-протеиназного ингибитора, что может привести к неправильной интерпретации результатов.
Известен способ диагностики болезни Альцгеймера на основе определения относительного содержания химически модифицированных форм металл-связывающего домена бета-амилоида в биологических жидкостях (RU 2794040 , опубл. 11.04.2023).
Данный способ обеспечивает возможность оценки риска развития болезни Альцгеймера с высокой чувствительностью и специфичностью для широкомасштабного клинического анализа плазмы крови возрастных пациентов, как в качестве самостоятельного исследования, так и в качестве основы для создания целевых методов, за счет мультиплексного целевого (таргетного) количественного хромато-масс-спектрометрического анализа панели 22-х изотопно-меченных белков плазмы крови.
Недостаток данного способа заключается в том, что панель из двадцати двух белков может требовать большого объема исследований и данных для тщательного обучения классификатора. Необходимость большого количества биологических образцов может затруднить реализацию этого метода в клинической практике. Так же обученный классификатор может иметь ограниченную точность. Вероятность неправильной классификации или ложноположительных/ложноотрицательных результатов может быть высокой, что может привести к неправильному диагнозу или ненужным дополнительным тестам и процедурам.
Несмотря на то, что рассмотренные способы имеют ряд своих преимуществ, они в целом не учитывают возможность более позднего обнаружения заболевания, а также некоторые из них являются достаточно дорогостоящими для пациента. Таким образом остро встает проблема в необходимости создания усовершенствованного способа быстрого и достаточного точного обследования пациентов с обеспечением выявления БА на различных этапах: на доклинической фазе, на этапе постановки предварительного диагноза и на этапе постановки окончательного диагноза, когда развитие БА ещё можно замедлить или предотвратить.
Известен способ диагностики болезни Альцгеймера с помощью «корня принятия решений», основанного на данных о магнитной восприимчивости четырех вен головного мозга (RU 2819148, опубл. 14.05.2024).
Одним из недостатков данного способа является то, что «корень принятия решений» имеет недостаточно высокую точность из-за своей сложности и неоднозначности в интерпретации результатов, т.к. известный способ учитывает только четыре параметра, что снижает достоверность прогнозирования болезни Альцгеймера.
Технический результат заключается в повышении достоверности диагностирования болезни Альцгеймера у пациента.
Указанный технический результат достигается тем, что способ диагностики болезни Альцгеймера включает проведение исследования головного мозга пациента методом магнитно-резонансной томографии с введением контрастного вещества, определение величин магнитной восприимчивости базальных вен в левом L_BV и правом R_BV полушариях головного мозга, вен таламуса левого L_TV и правого R_TV полушарий головного мозга по полученным томографическим снимкам, определение диапазонов полученных величин магнитной восприимчивости в соответствии с интервалами их категориальных значений и осуществление кодирования полученных величин в категориальные значения магнитной восприимчивости базальных вен, вен таламуса и внутренних мозговых вен L_BV*, R_BV*, L_TV*, R_TV*, соответственно; с помощью дискретных функциональных зависимостей переменных категориальных значений магнитной восприимчивости в матричной форме определяют значение «корня принятия решений». Согласно изобретению дополнительно определяют величины магнитной восприимчивости внутренних мозговых вен левого L_ICV и правого R_ICV полушарий головного мозга, определяют диапазоны полученных величин магнитной восприимчивости в соответствии с интервалами их категориальных значений и осуществляют кодирование полученных величин в категориальные значения магнитной восприимчивости указанных внутренних мозговых вен L_ICV*, R_ICV*,соответственно; строят предварительно обученное «дерево решений», представляющее собой разветвляющийся алгоритм действий, соответствующий блок-схеме, построенной на основе данных с применением теоретико-информационного критерия, включающего информационную энтропию для разбиения данных в очередном узле дерева, на основе результатов исследования головного мозга группы пациентов с болезнью Альцгеймера и контрольной группы пациентов, полученных методом магнитно-резонансной томографии с введением контрастного вещества, причем обученное «дерево решений» выполняют со спецификацией, включающей стратегию разбиения данных на каждом узле с минимальным количеством выборок в узле, при котором разделение узла дерева не происходит, при этом узел «дерева решений» представляет собой условие, а лист -прогноз; в память ЭВМ загружают алгоритм «дерева решений»; с помощью клавиатуры ЭВМ вводят входные данные переменных категориальных значений магнитной восприимчивости; алгоритм обученного «дерева решений» обрабатывает полученные данные и на мониторе ЭВМ показывает одно из значений переменных значений CON или AD, где значение AD означает, что пациент относится к группе больных, а значение CON означает, что пациент не болен.
«Деревья решения» предоставляют более структурированный и понятный анализ данных, что позволяет более точно с высокой долей достоверности определить наличие или отсутствие признаков болезни. В способе-прототипе использование «корня принятия решений» менее эффективно в сравнении с методом «деревьев решения» в предлагаемом способе из-за своей сложности и неоднозначности в интерпретации результатов. Кроме того, «деревья решений» учитывают большее количество параметров (6 вместо 4), что также повышает достоверность прогнозирования вероятности развития болезни Альцгеймера на ранних стадиях ее развития.
Вышеперечисленные операции позволяют в конечном счете получить качественно обученное «дерево решений», которое принимает одно из значений CON или AD, соответствующих постановке диагноза, с использованием значений магнитной восприимчивости шести вен головного мозга, наиболее важных для диагностирования болезни Альцгеймера на любой стадии заболевания.
Окончательное решение в постановке диагноза принимает врач, поскольку достоверность заявляемого способа составляет не менее 89%.
Изобретение проиллюстрировано следующими фигурами.
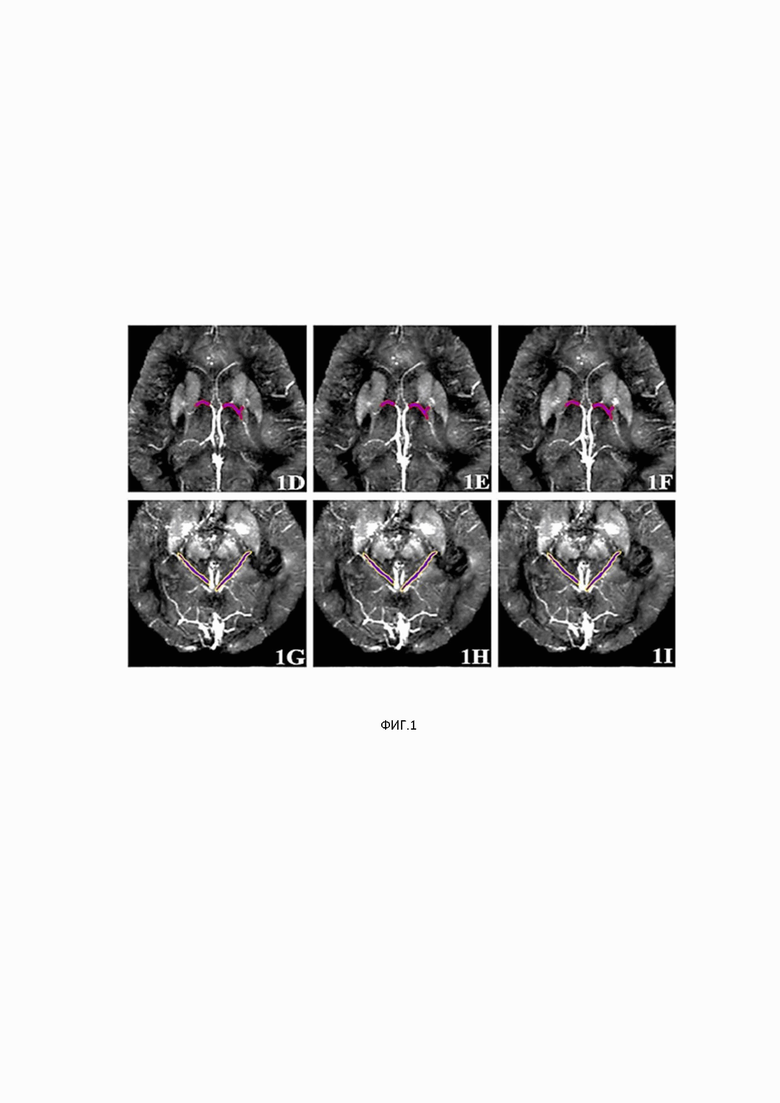
На фиг. 1 представлены томографические снимки вен головного мозга, где показаны три непрерывных среза с выделением вен таламуса, базальных вен и внутренних мозговых вен.
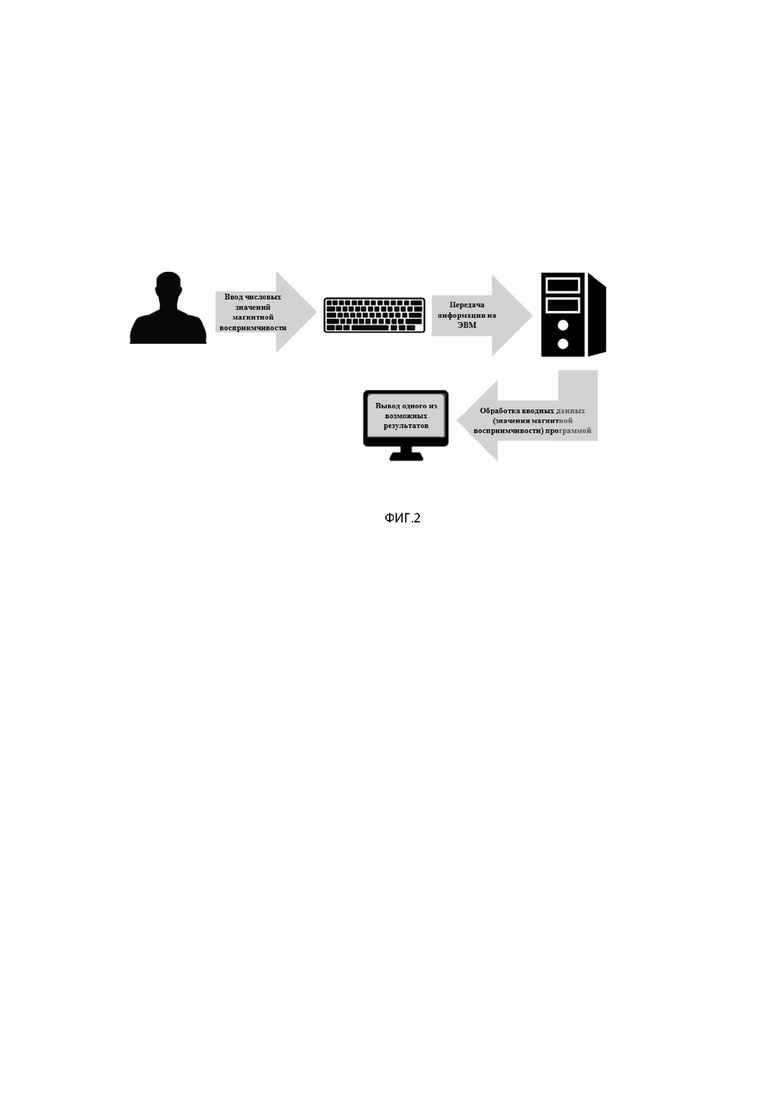
На фиг. 2 представлен порядок работы при диагностике болезни Альцгеймера согласно заявленному способу. Врач производит ввод числовых значений магнитной восприимчивости на клавиатуре ЭВМ, после чего программа осуществляет обработку введенных в соответствии с обученным «деревом решений», после чего получают результат на устройстве вывода информации.
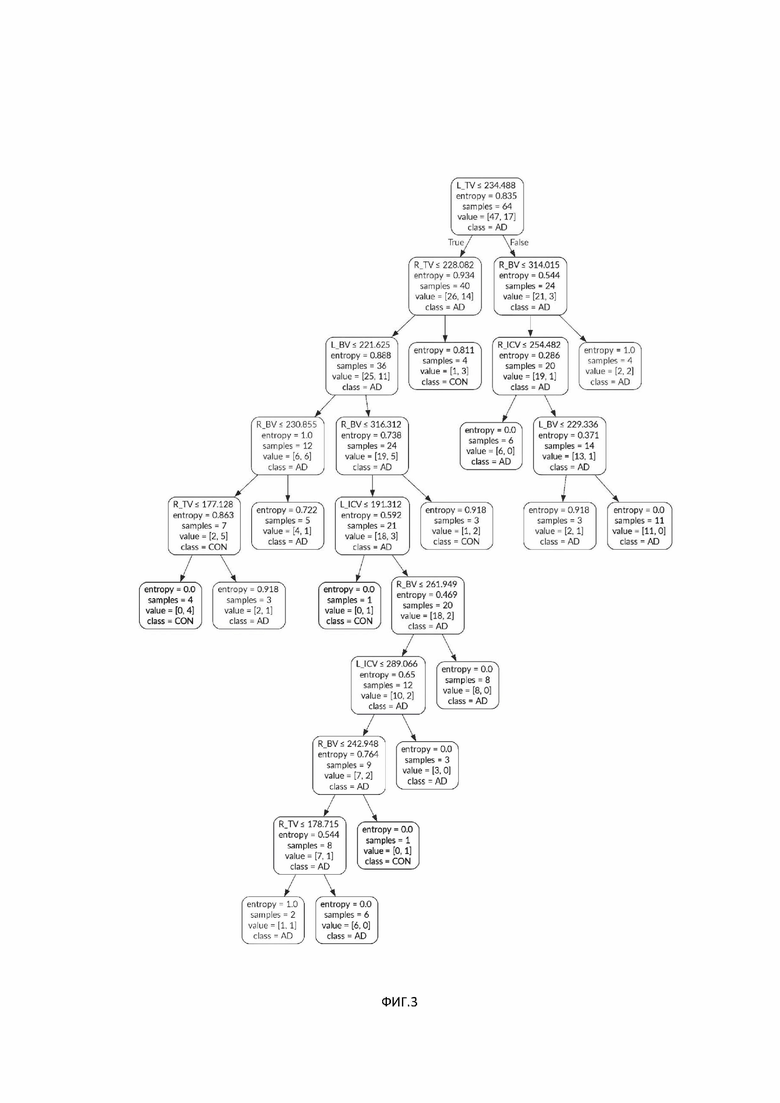
На фиг. 3 представлена блок-схема «дерева решений» при осуществлении способа на примере диагностики болезни Альцгеймера для конкретного пациента.
Заявляемый способ осуществляется следующим образом. Первым шагом пациенту проводят исследование МРТ с введением контрастного вещества.
При этом концентрация контрастного вещества в крови повышается, что увеличивает сигнал МРТ в активированных участках мозга. На основании томографических снимков (фиг. 1) количественно определяют величины магнитной восприимчивости следующих вен головного мозга: базальных вен левого и правого полушарий (L_BV и R_BV, соответственно), вен таламуса левого и правого полушарий (L_TV, R_TV, соответственно) и внутренних мозговых вен левого и правого полушарий (L_ICV, R_ICV, соответственно).
Далее полученные значения магнитной восприимчивости с помощью клавиатуры заносят в ЭВМ, где с помощью программы, т.е. обученного «дерева решений» осуществляют обработку введенных данных. «Дерево решений» представляет собой алгоритм действий ( блок-схема) внутри специальной программы для ЭВМ.
Алгоритм работы «дерева решений» заключается в принятии серии решений на основе данных входной выборки, чтобы классифицировать и предсказать значение целевой переменной. Каждый узел «дерева решений» представляет собой условие, а каждый лист - прогноз.
Обработка введенных значений магнитной восприимчивости начинается с корневого узда дерева решений, который представляет собой значение входных данных. Далее к входным данным применяется условие, в соответствии с которым происходит переход к одному из дочерних узлов, после чего данный шаг повторяется для каждого узла, пока не будет достигнут конечный листовой узел со значением целевой переменной. То есть «дерево решений» последовательно проходит от корня к листу, применяя заданные условия на каждом внутреннем узле для определения «правильного» листа.
В качестве переменных использованы категориальные значения магнитной восприимчивости вен таламуса, базальных вен и внутренних мозговых вен в левом и правом полушариях. Функция принимает два возможных значения: AD (от англ. Alzheimer's Disease), что интерпретируется - пациент относится к группе больных, CON - пациент не болен.
Далее врач ставит диагноз в зависимости от полученного значения переменной, т.е. в случае, если в конечном узле получено значение CON, то пациент не болен, если полученная переменная соответствует значению AD, то пациент болен болезнью Альцгеймера.
Пример
Пациент N прошел МРТ исследование. В кровь пациента было введено одно из используемых в России контрастных веществ, содержащих гадолиний - Оптимарк (OptiMARK), Магневист (Bayer) или Омнискан (GE Healhcare).
Томографические снимки представлены на фиг. 1. Значения магнитной восприимчивости следующих вен головного мозга: левой и правой базальных вен (L_BV и R_BV, соответственно), левой и правой вен таламуса (L_TV, R_TV, соответственно), левой и правой внутренних мозговых вен (L_ICV, R_ICV, соответственно) были рассчитаны по методике (Liu, Y.; Dong, J.; Song, Q.; Zhang, N.; Wang, W.; Gao, B.; Tian, S.; Dong, C.; Liang, Z.; Xie, L.; et al. Correlation between cerebral venous oxygen level and cognitive status in patients with Alzheimer's disease using quantitative susceptibility mapping. Front. Neurosci. 2021, 14, 570848).
Полученные величины магнитной восприимчивости имели следующие значения: L_BV* - 279, R_BV* - 288, L_TV* - 140, R_TV* - 138, L_ICV* - 255, R_ICV* - 263.
После чего врач вводил полученные данные в программу, которая в свою очередь анализировала введенные данные и проводила их по алгоритму («дереву решений»), представленному на фиг. 3, проходя следующие этапы:
1) Введенные данные поступают в корневой узел, где к ним применяется условие: L_TV <234,488. Так как значение L_TV* = 140 соответствует поставленному условию, то есть является «правдивым», происходит переход по левой ветке «true» на внутренний узел.
2) В следующем узле применяется условие R_TV <228,082, которому введенное значение R_TV* = 138 соответствует, следовательно, происходит переход по левой ветке к следующему внутреннему узлу.
3) Далее в новом узле применяется условие L_BV <221,625. Введенное значение L_BV* = 279 не соответствует данному условию, поэтому происходит переход по правой или же «ложной» ветке «false».
4) В следующем узле применяется условие R_BV <316,312. Введенное значение R_BV* = 288 соответствует узловому условию, следовательно, переход в следующий узел происходит по левой ветке «true».
5) В новом узле применяется условие L_ICV <191,312, которому введенные данные L_ICV* = 255 не удовлетворяют, поэтому переход в следующий узел происходит по правой ветке.
6) В следующем узле применяется условие R_BV <261,949. Так как R_BV* = 288, то условие не соблюдается и переход осуществляется по правой ветке.
7) Далее происходит переход в крайний узел, который в данном примере является конечным. Таким образом, придя в конечный узел, получен результат AD.
После чего врачу на устройство вывода информации (монитор) выходит полученный результат, соответствующий значению AD, что означает наличие у пациента болезни Альцгеймера.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДИАГНОСТИКИ БОЛЕЗНИ АЛЬЦГЕЙМЕРА | 2023 |
|
RU2819148C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ПОСТИНСУЛЬТНОЙ ДЕМЕНЦИИ | 2008 |
|
RU2392861C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ УМЕРЕННЫХ КОГНИТИВНЫХ РАССТРОЙСТВ | 2015 |
|
RU2588314C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ПОСТИНСУЛЬТНОЙ ДЕМЕНЦИИ | 2009 |
|
RU2425642C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЛЕВО-ПРАВОПОЛУШАРНОЙ ДИХОТОМИИ У ЗДОРОВЫХ ЛИЦ | 2023 |
|
RU2805362C1 |
| СРЕДСТВА ДИАГНОСТИКИ НЕЙРОДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЙ | 2008 |
|
RU2494669C2 |
| СПОСОБ ДИАГНОСТИКИ КОРСАКОВСКОГО СИНДРОМА У БОЛЬНЫХ С ОПУХОЛЯМИ БАЗАЛЬНО-ДИЭНЦЕФАЛЬНОЙ ЛОКАЛИЗАЦИИ ПО ДАННЫМ ЭЛЕКТРОЭНЦЕФАЛОГРАФИЧЕСКОГО ИССЛЕДОВАНИЯ | 2012 |
|
RU2493771C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВОЗМОЖНОСТИ ДЕКОМПЕНСАЦИИ ДИСЦИРКУЛЯТОРНОЙ ЭНЦЕФАЛОПАТИИ ПОСЛЕ ИНСУЛЬТА ГОЛОВНОГО МОЗГА | 2004 |
|
RU2292845C2 |
| СПОСОБ КОМПЛЕКСНОЙ ЛУЧЕВОЙ ДИАГНОСТИКИ ДОКЛИНИЧЕСКИХ И КЛИНИЧЕСКИХ СТАДИЙ БОЛЕЗНИ АЛЬЦГЕЙМЕРА | 2006 |
|
RU2315559C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ БОЛЕЗНИ АЛЬЦГЕЙМЕРА, СОСУДИСТОЙ И СМЕШАННОЙ ДЕМЕНЦИИ | 2015 |
|
RU2578188C1 |
Изобретение относится к области анализа медицинских данных и предназначено для поддержки врачебных решений при постановке диагноза о наличии или отсутствии у пациента болезни Альцгеймера с высокой достоверностью. Предложенный способ диагностики болезни Альцгеймера включает проведение исследования головного мозга пациента методом магнитно-резонансной томографии с введением контрастного вещества, определение величин магнитной восприимчивости базальных вен в левом L_BV и правом R_BV полушариях головного мозга, вен таламуса левого L_TV и правого R_TV полушарий головного мозга, по полученным томографическим снимкам, определение диапазонов полученных величин магнитной восприимчивости в соответствии с интервалами их категориальных значений и осуществление кодирования полученных величин в категориальные значения магнитной восприимчивости базальных вен и вен таламуса L_BV*, R_BV*, L_TV*, R_TV*, соответственно, далее с помощью дискретных функциональных зависимостей переменных категориальных значений магнитной восприимчивости в матричной форме определяют значение «корня принятия решений». Дополнительно определяют величины магнитной восприимчивости внутренних мозговых вен левого L_ICV и правого R_ICV полушарий головного мозга, определяют диапазоны полученных величин магнитной восприимчивости в соответствии с интервалами их категориальных значений и осуществляют кодирование полученных величин в категориальные значения магнитной восприимчивости указанных внутренних мозговых вен L_ICV*, R_ICV*, соответственно, затем строят предварительно обученное «дерево решений», представляющее собой разветвляющийся алгоритм действий, соответствующий блок-схеме, построенной на основе данных с применением теоретико-информационного критерия, в которой узел «дерева решений» представляет собой условие, а лист - прогноз, далее в память ЭВМ загружают указанный алгоритм «дерева решений», с помощью клавиатуры ЭВМ вставляют входные данные переменных категориальных значений магнитной восприимчивости, алгоритм обученного «дерева решений» обрабатывает полученные данные и на мониторе ЭВМ показывает одно из значений переменных значений CON или AD. Изобретение обеспечивает повышение достоверности диагностирования болезни Альцгеймера у пациента. 3 ил.
Способ диагностики болезни Альцгеймера, включающий проведение исследования головного мозга пациента методом магнитно-резонансной томографии с введением контрастного вещества, определение величин магнитной восприимчивости базальных вен в левом L_BV и правом R_BV полушариях головного мозга, вен таламуса левого L_TV и правого R_TV полушарий головного мозга по полученным томографическим снимкам, определение диапазонов полученных величин магнитной восприимчивости в соответствии с интервалами их категориальных значений и осуществление кодирования полученных величин в категориальные значения магнитной восприимчивости базальных вен, вен таламуса и внутренних мозговых вен L_BV*, R_BV*, L_TV*, R_TV*, соответственно; с помощью дискретных функциональных зависимостей переменных категориальных значений магнитной восприимчивости в матричной форме определяют значение «корня принятия решений»,
отличающийся тем, что
дополнительно определяют величины магнитной восприимчивости внутренних мозговых вен левого L_ICV и правого R_ICV полушарий головного мозга, определяют диапазоны полученных величин магнитной восприимчивости в соответствии с интервалами их категориальных значений и осуществляют кодирование полученных величин в категориальные значения магнитной восприимчивости указанных внутренних мозговых вен L_ICV*, R_ICV*, соответственно; строят предварительно обученное «дерево решений», представляющее собой разветвляющийся алгоритм действий, соответствующий блок-схеме, построенной на основе данных с применением теоретико-информационного критерия, включающего информационную энтропию для разбиения данных в очередном узле дерева, на основе результатов исследования головного мозга группы пациентов с болезнью Альцгеймера и контрольной группы пациентов, полученных методом магнитно-резонансной томографии с введением контрастного вещества, причем обученное «дерево решений» выполняют со спецификацией, включающей стратегию разбиения данных на каждом узле с минимальным количеством выборок в узле, при котором разделение узла дерева не происходит, при этом узел «дерева решений» представляет собой условие, а лист - прогноз; в память ЭВМ загружают алгоритм «дерева решений»; с помощью клавиатуры ЭВМ вводят входные данные переменных категориальных значений магнитной восприимчивости; алгоритм обученного «дерева решений» обрабатывает полученные данные и на мониторе ЭВМ показывает одно из значений переменных значений CON или AD, где значение AD означает, что пациент относится к группе больных, а значение CON означает, что пациент не болен.
| СПОСОБ ДИАГНОСТИКИ БОЛЕЗНИ АЛЬЦГЕЙМЕРА | 2023 |
|
RU2819148C1 |
| WO 2018064715 A1, 12.04.2018 | |||
| US 10746822 B2, 18.08.2020 | |||
| КОЖЕМЯКИН Л | |||
| В | |||
| и др | |||
| Применение корней принятия решений для определения взаимосвязи между магнитной восприимчивостью вен головного мозга и наличием болезни Альцгеймера | |||
| Управление большими системами: труды XVIII Всероссийской школы-конференции молодых ученых, | |||
Авторы
Даты
2025-04-07—Публикация
2024-08-26—Подача