2. Сочетав мембраны ионоселектив- ного электрода для определения активности перренат-ионов, содержащий электродно-активное вещество на основе ионного ассоциата перренат-ионов с органическим катионом и органический растворитель, отличающийс я тем, что, с целью повышения селективности и воспроизводимости, 8 качестве электродно-активного вещества использован ионный ассоциат перренат-ионов .с 2 ,,6-трифенилпириллием, а в качестве растворителя использована смесь поливинилхлорида и диоктилфталата при следующем соотношении компонентов мембраны, вес.: Электродно-активное вещество5-7 Поливинипхлорид 31-33 Диоктилфталат 60-б5



| название | год | авторы | номер документа |
|---|---|---|---|
| СОСТАВ МЕМБРАНЫ ИОНОСЕЛЕКТИВНОГО ЭЛЕКТРОДА ДЛЯ ОПРЕДЕЛЕНИЯ АКТИВНОСТИ ПЕРРЕНАТ-ИОНОВ | 1994 |
|
RU2083979C1 |
| Состав мембраны ионоселективного электрода для определения перренат-ионов | 1983 |
|
SU1075136A1 |
| Состав мембраны ионоселективного электрода для определения меди (1) | 1981 |
|
SU989441A1 |
| Состав мембраны ионоселективного электрода для определения активности ионов серебра в цианидных растворах | 1980 |
|
SU966579A1 |
| Состав мембраны ионоселективного электрода для определения активности ионов палладия в цианидных растворах | 1982 |
|
SU1092403A1 |
| МЕМБРАНА ИОНОСЕЛЕКТИВНОГО ЭЛЕКТРОДА ДЛЯ ОПРЕДЕЛЕНИЯ ИОННЫХ ПОВЕРХНОСТНО-АКТИВНЫХ ВЕЩЕСТВ В СТОЧНЫХ ВОДАХ И СИНТЕТИЧЕСКИХ МОЮЩИХ СРЕДСТВАХ | 2013 |
|
RU2531130C1 |
| СОСТАВ ПЛЕНОЧНОЙ ИОНОСЕЛЕКТИВНОЙ МЕМБРАНЫ ДЛЯ ОПРЕДЕЛЕНИЯ СУММАРНОЙ АКТИВНОСТИ ИОНОВ КАЛЬЦИЯ И МАГНИЯ | 1993 |
|
RU2056632C1 |
| ИОНОСЕЛЕКТИВНАЯ МЕМБРАНА ДЛЯ ОПРЕДЕЛЕНИЯ ИОННЫХ ПОВЕРХНОСТНО-АКТИВНЫХ ВЕЩЕСТВ | 2013 |
|
RU2546045C1 |
| Мембрана ионоселективного электрода для определения серебра на основе жидкого ионообменника | 1978 |
|
SU693808A1 |
| Состав мембраны ионоселективного электрода для определения нитрит-ионов | 1981 |
|
SU1132209A1 |
1. Состав мембраны ионоселективного электрода для определения активности перренат-ионов, содержащий электродно-активное вещество на основе ионного ассоциата перренат-ионов с органическим катионом и органический растворитель, отличающийся тем, что, с целью повышения селективности и воспроизводимости, в качестве электродно-активного вещества использован ионный ассоциат перренат-ионов с 2,+,6-трифенилпирриллием с концентрацией 10 , а вкачестве растворителя использована смесь дихлорэтана и хлороформа при соотношении компонентов растворителя о6.%: Дихлорэтан10-90 Хлороформ80-20 . -pffeO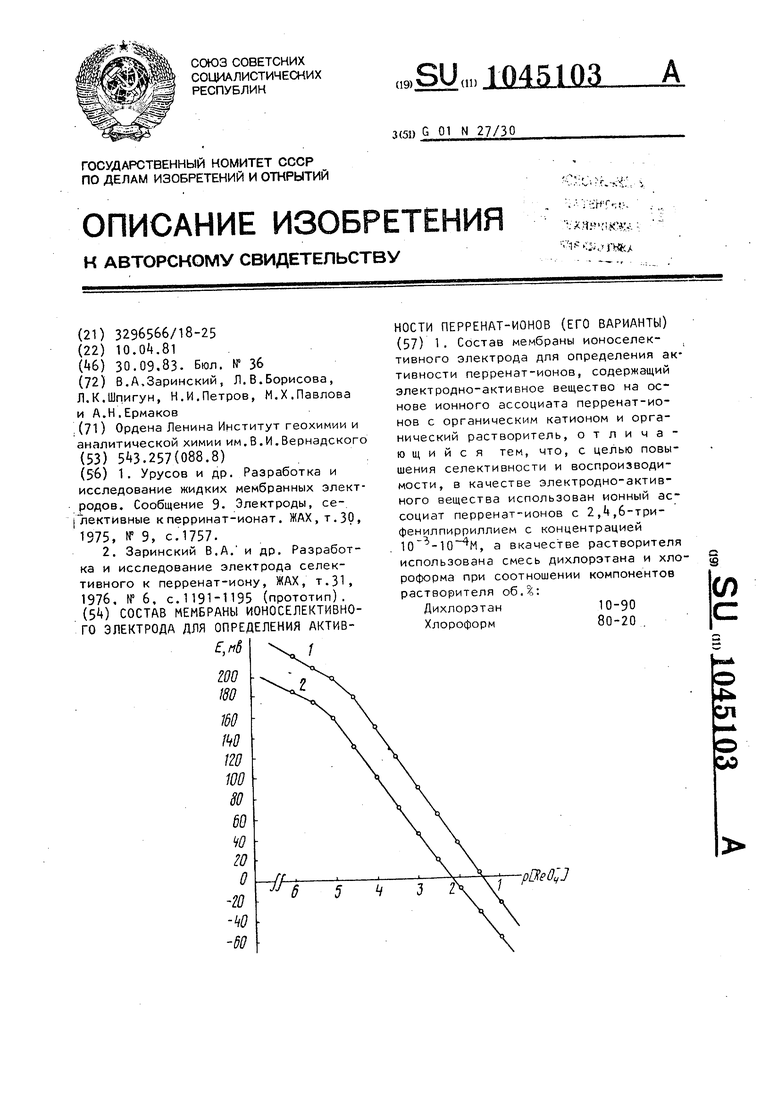

1 Изобретение относится к потенциометрическим методам анализа и контроля концентрации ионов в водных растворах и может быть использовано в химической, металлургической промышленности, в оптической химии и в практике научных исследований.
Известиь мембраны, состоящие из соединений перренат-ионов, с бриллиатовой зеленью в органическом растворе, обладающие перренатной функцией в диапазоне концентраций 10 -ТО М при рН 5,0-7,2, которые характери- зуются довольно низкой селективность по oтнouJeнию к перренат-ионам, особенно в присутствии ионов CIO.-SCN и N0 l .
Наиболее близким к предлагаемому . является состав мембраны ионоселективного электрода для определения перренат-ионов, содержащий электроднактивное вещество на основе ионного ассоциата перренат-иона с органическим катионом и органическим растворителем. Мембрана электрода состоит из раствора ионообменкика в органическом растворителе, в качестве которого используют 1 М раствор ионного ассоциата перренат-иона с катио ном тетрафениларсония состава I (С, Н ). в нитробензоле. Электрод на основе этого соединения сохраняет электродную функцию в диапазоне 10-10 М; обнаруживает независимость потенциала (при постоянной ионной силе) в широком интерЕ(але концентрации ионов водорода (от 1,5М t-l/)SO,: до 5 М ) , характеризуется коэффициентами селективности, раЁ:ным 3, 8, 7,10-5; 10о 1 О соответственно в присутствии
«i50д , WO , VO,,; и ионов любых катионов., однако потенциал этого электрода в большей или меньшей степени зaвиcиt от присутствия С10, CNS, I, Вг, С, СП. Время установления равновесного потенциала для разбавленных растворов 3-5 мин, а для концентрированных 1-2 мин, в сложных по составу растворах это время значительно увеличивается.
Воспроизводимость значений потенциалов этого электрода для растворов одной и той же концентрации +7. мВС2Х
Существенным недостатком ионообменника является также его токсичность и сложность синтеза.
Цель изобретения - повышение селективности и воспроизводимости.
Поставленная цель достигается тем, что в составе мембраны ионоселективного электрода для. определения активности перренат-ионов, содержащем электродно-активное вещество на основе ионного ассоциата перренат-ионов с органическим катионом и органический растворитель, в качестве электродно-активного вещества использован ионный ассоциат перренат-ионов с 2,+,6-трифенилпириллием с концентрацией 10 -10 М, а в качестве растворителя использована смесь дихлорэтана и хлороформа при соотношении компонентов растворителя, обД:
Дихлорэтан10-90
Хлороформ - 80-20
Поставленная цель достигается таке тем, что в составе мембраны ионоселективного электрода для определеия активности перренат-ионов, содеращем электродно-активное вещество на основе ионного ассоциата перренат3ИОНОВ с органическим катионом и орга нический растворитель, в качестве электродно-активного вещества исполь ован ионный ассоциат перренат-ионов с 2,А,6-трифенилпириллием, а в качес ве растворителя использована смесь поливинилхлорида идиоктилфталата при следующем соотношений компонентов мембраны, вес.: Электродно-активнов вещество5-7 Поливинилхлорид 31-33 Диоктафталат60-б5 Жидкую мембрану готовят экстракционным, методом. В делительную воронку помещают 10 мл 0,01 М водного раствора перрената аммония и добавляют 10 мл 0,001 М раствора сульфата 2,,6-трифенилпиррилия в смеси хлороформ 1,2-дихлорэтан. После 5 мин перемешивания фазыразделяют, органический раствор фильтруют через бумажный фильтр и используют в -дальнейшем бе предварительного контроля концентра ции. Предлагаемый рабочий состав ор ганической фазь - 0,001 М раствора U(CfoH).,.. Пленочную мембрану готовят следующим образом. 60 мг перрената 2,,6-трифенилвериллия (ПТФП) растворяют в 6 мл смеси диоктилфталата мг (ДОФ) и 1,2-дихлорэтэна. Полученный раствор постепенно приливают к 0 мг поливинилхлорида (ПВХ) , предварительно растворенного в 2 мл 1,2-дихлорэтан После тщательного перемешивания маг нитной мешалкой ро получения однород ной вязкой смеси последнюю выливают в чашку Петри (внутренний диаметр 33 мм) и оставляют открытой на воздухе до получения прозрачной эласти ной пленки. Оптимальный состав мемб ранной -смеси, вес.;: ПВХ:ДОФ:ПТФП 33,3:62,7:5,0, Изучение электрохимического пове дения мембран проводят путем измерения ЭДС гальванической цепи с переносом„ ,„ „. 10 MNH.ReOA К, I .Ag(AgCl, | Мембрана 1Исследуемый „(н,.) 50 КС 1, 1 j Ад раствор Общее омическое сопротивление цепи, включающей жидкую и пленочную мембр ны, соответствено равно 700 кОм и 10 МОм. 34 Нижний предел обнаружения рения с помощью предлагаемого электрода составляет , в то время как линейная область функционирования электрода порядка 10 . Предлагаемые пределы содержания компонентов в мембранах являются оптимальными, поскольку в случае жидкой мембраны электрода при концентрации ионообменника меньше ЮМ значительно ухудшаются кинетические свойства мембран и наблюдается дрейф потенциала вследствие увеличения их электрического сопротивления; при концентрации ионообменника больше 10 М в фаз.е мембраны наблюдается увеличение нижнего предела обнаружения перренат-ионов. Применение смешанного растворителя с концентрацией в указанных пределах продиктовано тем, что применяемый ионообменник хорошо растворяется в хлороформе а 1,2-дихлорэтан, диэлектрическая проницаемость которого 10,36, уменьшает электрическое сопротивление ионоселективной мембраны и тем самым улучшает ее рабочие характеристики, в случае пленочной мембраны содержание ионообменника лимитируется растворимостью в диоктилфталате. Указанные количества диоктилфтала (60-б5) обеспечивают наилучшую совместимость ПВХи иснообменника, а также придают пленке требуемую эластичность; при добавлении указанного количества ПВХ () получают пленки оптимальной толщины 0,3-0,5 мм (более тонкие пленки обладают малой механической прочностью, а более толстые имеют худшие рабочие характерис-тики; . Для регистрации ЭДС используют цифровой вольтметр Ш 1513, показания которого автоматически регистрируют с помощью цифропечатающего устройства Р 5033К, состоящего из транскриптора Ф 5033 и электроуправляемой пишущей машины ЭУМ-23Д. На чертеже представлены калибровочные графики, полученные для случая жидкой (кривая 1) и пленочной (кривая 2) мембран при температуре (22+1)4. Как видно из чертежа, электрохимическое поведение мембран на основе перрената. 2,,6-трифенил, периллия характеризуется широкими диапазонами функционирования 1 10 .
Крутизна электродной функции соотт ветственно равна для жидкой и пленочной мембран (59±1) мВ/рГКеОф и 57,5±0,5) мВ/р ReO. Перренатная функция мембран выполняется в облас- 5 ти концентрации водородных ионов от 1 М H. до 5 М .
Электроды с этими мембранами характеризуются высокой стабильностью
10 в работе и хорошими кинематическими свойствами.
Время установления равновесного потенциала для-концентрированных растворов перренат-ионоа составляет
30 с 1 мин, а для разбавленных м.ин. Мембранный потенциал оста
э н и е. R-0,95, лоб, ионная сила водных растворов (Ц 0,1, температура 22+1 С.
Состав мембраны: 1 -10 М раствор 30не оказывает влияния на мембранный
перрената 2,Д,6 трифенилпериллия впотенциал {при условии постоянства
смеси хлороформ - 1,2-дихлорэтан 1:1.ионной силы раствора). Существенного
Как следует из данных табл.1,различия в селективности мембран с
электрод с мембраной на основе перре-различным содержанием описанного выше
ната 2,А,6-трифенилпериллия обладает ассоциата в мембране, а также с растзначительной селективностью к перре-.ворителями различной природы замечено
наг-ионам в присутствии хлоридов,не было.
фосфатов, сульфатор и целого ряда дру- Для проверки функционирования перрегих анионов. --натного электрода с вышеописанной
Присутствие ионов меди (||).желе- 40мембраной проведены прямые потенциоза {).никеля(Г|), кобальта(I1),метрические измерения содержания рения
ци:нка(1), кадмия(М), ртути (I), тал-в ряде модельных растворов различного
ЛИЯ (1 ) и других катионов практическиспг.тавд I табл.2 и 3).
Результаты потенциометрического определения Re в модельных растворах (Re-Mo-Vf) методом добавок
03
ется постоянным в течение рабочего дня с точностью ±0,5 мВ.
Чувствительность мембрано-активного материала к изменению концентрации перренат-ионов в растворе в присутствии посторонних анионов оценивают путем расчета потенциометрических коэффициентов селективности, значения которых приведены в табл.1. Установлено также, что присутствии меди (11), железа (М), никеля (11), кобальта (М), цинка (I i), кадмия (I ) ртути (|1), таллия (|) и других катионов практически не оказывает влияния на потенциал электродной системы (при условии постоянства ионной силы раствора) коэффициенты селективности
Таблица 1
Таблица 2
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Урусов и др | |||
| Разработка и исследование жидких мембранных элект родов | |||
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Электроды, се|лективные кперринат-ионат | |||
| ЖАХ, т.30 1975,№ 9, с.1757 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Заринский В.А | |||
| и др | |||
| Разработка и исследование электрода селективного к перренат-иону, ЖАХ, т.31, 1976,№ 6, с.1191-1195 (прототип) | |||
| . | |||
Авторы
Даты
1983-09-30—Публикация
1981-04-10—Подача