Настоящее изобретение относится к технологии получения карбонатов щелочных металлов из хлоридов соответствующих металлов, аммиака и углекислоты нутем обменной реакции
2МеС1- -(МН4)2СОз 2ЫН4С1+МеСОз в водном растворе с использованием ионитов.
Известный способ получения растворов карбонатов щелочных металлов предусматривает наибольшую и равную степень превращения раствора и ионита из одной формы в другую. Б таком процессе неполностью используется производительность аппаратуры и емкость иопита из-за малой движущей силы диффузионного нроцесса ионообмена.
Кроме того, известный способ не позволяет получить чистые соли ввиду большой степени перехода хлорида щелочного металла в хлористый аммоний.
С целью иптепсификации процесса и обеспечения чистоты получаемого продукта предложен способ получения карбонатов щелочных металлов из водных растворов хлоридов этих металлов и раствора карбоната аммония путем катионообмеипой реакции в батарее ионообменных колонн с одновременным проведением прямого и обратного процесса По этому способу растворы на ионит подают в таком количестве, чтобы степень перехода одной формы катионнта в другую не превышала бОо/о, а отношение общего количества катионов в растворах к емкости катионнта было не более 1,5. Предусмотрено также регенерировать хлорид щелочного металла из хлористого аммония маточной жидкости эквивалентным количеством содового раствора, а промывку ионита в батарее при переключении колонны с одного цикла на другой осуществлять концентрированным раствором солей.
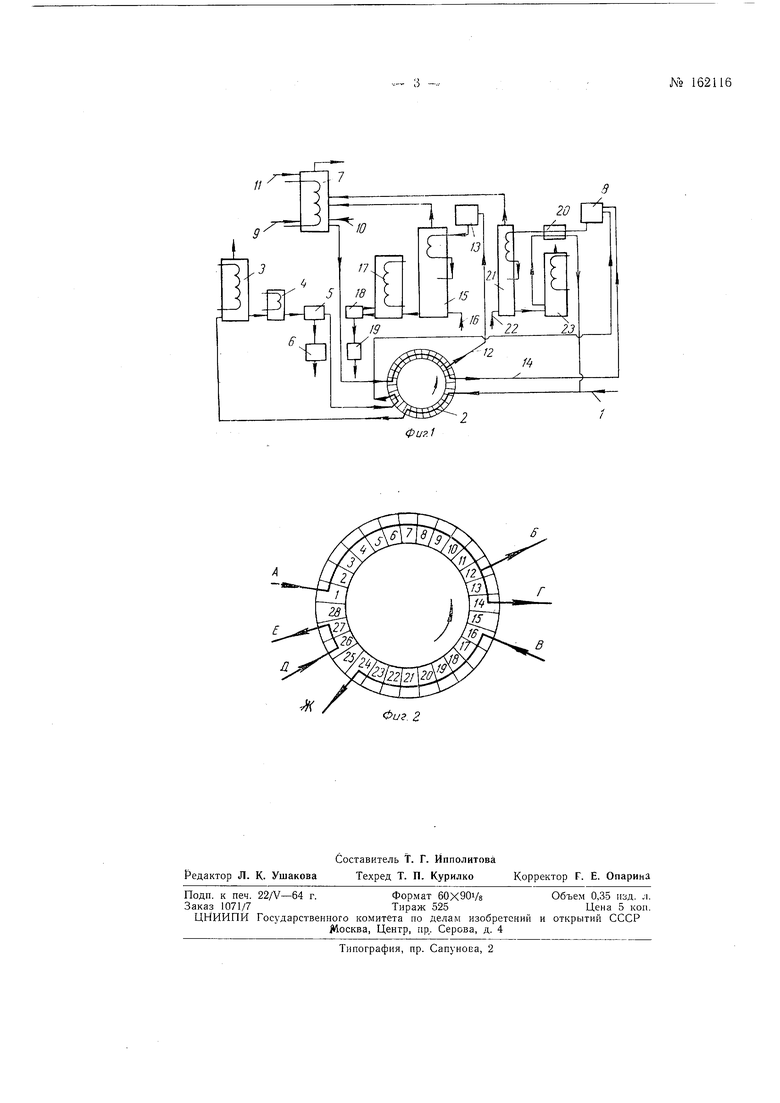
На фиг. I изображена схема, ноясняющал предлагаемый способ; на фиг. 2 - условно показана батарея ионообменных колонн.
Насыщенный раствор хлористого натрия по трубопроводу / поступает в батарею 2 ионообменных колонн и проходит через ту часть их, которая содержит катионит преимущественно в аммонийной форме. При этом большая часть находящихся в растворе ионов натрия замещается на ионы аммония. Полученный смешанный раствор NH4C1 и NaCl упаривают в выпарном аппарате 3 до достил-сения насыщения по хлористому натрию, носле чего подают в кристаллизатор 4, где раствор охлаждается до достаточно низкой температуры. Выкристаллизовавшийся твердый хлористый аммоний отделяют от маточной жидкости на центрифуге 5 и высушивают в сушилке 6. Маточную жидкость после отделения хлористого аммония на центрифуге 5 подают в батарею 2 ионообменных колонн и используют для промывки двух очередных иопообменных колонн от карбоната аммония, после чего она поступает в сборник 8.
Аммиак и углекислоту, используемые для получения раствора карбоната аммония, вводят в абсорбционную колонну 7 по трубопроводам 9 и }0. Колонна орошается сверху водой, поступающей по трубопроводу /), она снабжена впутренним охлаждением.
Раствор карбоната аммония из абсорбционной колонны 7 подают в ту часть ионообменных колонн батареи 2, которая содержит катионит преимуществеппо в натриевой форме. При этом большая часть находящихся в растворе ионов аммония замешается на ионы натрия. Часть полученного содового раствора, содержашего некоторое количество карбоната аммония, отбирают из батареи 2 и по трубопроводу }2 направляют в сборник 13. Оставшуюся часть содового раствора используют для промывки двух очередных ионообменных колонн от хлористого натрия, после чего по трубопроводу 14 раствор поступает в сборник 8.
Содовый раствор, поступивший в сборник J3, переходит в дистилляционную колоппу 15, обогреваемую паром, подаваемым по трубопроводу 16. В колонне раствор освобождается от примеси углекислого аммония. Выделяющиеся аммиак и углекислоту подают в абсорбционную колонну 7, а горячий содовый раствор упаривают в выпарном аппарате 17.
Выделившийся осадок твердого кристаллогидрата углекислого натрия отделяют от маточной жидкости на центрифуге 18, высушивают в сушилке 19 и подают на упаковку.
В сборнике 8 смешивают растворы NH4C1, NaGl и раствор NagCOs, использоваппые для промывки очередных ионообменных колонн, в такой пропорции, чтобы в результате взаимодействия по реакции
2NH4Cl+NaoCO3 2NaCl+(NH4)2C03
весь хлористый аммоний перешел в хлористый натрий.
Из сборника 8 раствор NaCl и (NH4)2CO.;i поступает в теплообменник 20, а затем в дистилляционную колонну 21, обогреваемую паром, подаваемым по трубопроводу 22, где освобол дается от карбопата аммония. Выделяющиеся аммиак и углекислоту подают в абсорбционную колонну 7, а горячий раствор хлористого натрия упаривают в выпарном аппарате 23 до насыщения, но без выделения твердой соли. Горячий насыщенный раствор хлористого натрия, выходящий из выпарного аппарата 23, проходит через теплообменник 20, после чего возвращается в цикл производства - поступает в батарею 2 ионообменных колонн.
В батарее ионообменных колонн (см. фиг. 2) процессы прямого (получение раствора Ыа2СОз) и обратного (получение раствора NH4C1) ионообмена происходят одновременно таким образом, что через каждую из колонн проходят циклически все стадии обоих процессов, каждая колонна своевременно опорожняется и промывается периодически поступающими извне растворами.
Внутри каждой части батареи ионообменных колонн жидкость переходит последовательно из одной колонны в другую. Так, на фиг. 2 изображен момент, когда колонны /- 12 работают в прямом процессе (АБ), 16- 24 - в обратном (ВЖ), 13-14 промываются содовым раствором (Г), 26-27 - нашатырным лчаточником (ДЕ, колонны 15, 25 и 28- опорожняются.
После очередного переключения в прямом процессе будут работать колонны 2-1, в обратном 17-25; колонны 14-15 будут промываться содовым раствором, а 27-28 - нашатырным маточником. Колонны 16, 26 ц 1 будут опорожняться.
Технологическая схема получения карбонатов других щелочных металлов из их хлористых солей не отличается от описанной схемы нолучения углекислого натрия, изображенной на фиг. 1.
Предмет изобретения
Способ получения карбонатов щелочных металлов из водных растворов хлоридов этих металлов и раствора карбоната аммония путем катионообменной реакции в батарее ионообменных колонн с одновременным проведением прямого и обратного процесса, отличаюшийся тем, что, с целью получения чистого продукта и интенсификации процесса, растворы, проходящие через ионит, подают в таком количестве, чтобы степень перехода одной формы катионита в другую не превышала 60%, а отношение общего количества катионов в растворах к емкости катионита было не более 1,5.
//

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ УЛЬТРАЧИСТОГО КАРБОНАТА ЛИТИЯ ИЗ ТЕХНИЧЕСКОГО КАРБОНАТА ЛИТИЯ И УСТАНОВКА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2013 |
|
RU2564806C2 |
| СПОСОБ ОБЕССОЛИВАНИЯ ВОДЫ | 1991 |
|
RU2072326C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАЛЬЦИНИРОВАННОЙ СОДЫ АММИАЧНЫМ МЕТОДОМ | 2007 |
|
RU2381177C2 |
| СПОСОБ ОБЕССОЛИВАНИЯ ВОДЫ | 1991 |
|
RU2072325C1 |
| Способ получения литиевого концентрата из литиеносных природных рассолов и его переработки в хлорид лития или карбонат лития | 2017 |
|
RU2659968C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРИСТОГО АММОНИЯ | 2012 |
|
RU2495824C2 |
| Способ получения моногидрата гидроксида лития из рассолов и установка для его осуществления | 2016 |
|
RU2656452C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИТИЕВОГО КОНЦЕНТРАТА ИЗ ЛИТИЕНОСНЫХ ПРИРОДНЫХ РАССОЛОВ И ЕГО ПЕРЕРАБОТКИ | 2012 |
|
RU2516538C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПАРАВОЛЬФРАМАТА АММОНИЯ | 2015 |
|
RU2600045C1 |
| СПОСОБ ПОЛУЧЕНИЯ СВИНЦА | 2014 |
|
RU2555261C1 |

. 2
Авторы
Даты
1964-01-01—Публикация