Изобретение относится к HOBBIM производным пиридина, конкретно к (4транс-алкилциклогексил)-фенил -5-(4-транс-алкилциклогексил)-пиридинам общей формулы I
ОнОУ
С ц пП2п4;
-cjf
7т+1
где п - целые числа 2, 3, 5; m - целые числа 3, 5, .
которые могут быть использованы как компоненты жидкокристаллического материала, а также к жидкокристаллическому материалу для электрооптических устройств.
Цель изобретения - изыскание новых соединений в ряду производных пиридина, обладающих жидкокристаллическими свойствами, и жидкокристаллический материал с использованием этих соединений, которые обеспечивают снижение нижнего предела интервала нематической фазы.
Изобретение иллюстрируется следующими примерами.
П р и м е р 1, Получение 2- 4-{4-транспентилциклогексйл)-фенил -5-{4-транс-прО пилциклогексил)-пиридина (1вб)..
1.1,транс.-1-Пропил-4-циклогексилуксусный альдегид (Мб).
К смеси 0,05 моль металлического магния в 20 мл абсолютного тетрагидрофурана медленно прибавляют по каплем при кипении 0,05 моль транс-1-пропил-4-бромметилциклогексанй (1116). После 3астворения магния полученный раствор прибавляют по каплям к охлажденному до -40°С раствору 0,045 моль N-мeтил-N-фopмил-2-aминoпиридина в 50 мл абсолютного тетрагидрофурана. Реакционную смесь перемешивают при -20°С 20 мин и выливают в 150 мл 5%ной.соляной кислоты, предварительно охлажденной до 0°С. Экстрагируют эфиром, экстракт промывают насыщенным водным раствором хлористого натрия, водой, сушат над сульфатом натрия (добавив гидрохинон). Эфир отгоняют, остаток перегоняют в вакууме, т.кип. 69-71°С(1 мм рт.ст,). Получают транс-1-пропил-4-циклогексилуксусный альдегид с выходом 65%.
ИК-спектр: vco 1720 см Спектр ПМР (CCI4, д. М.Д.): т 0,85 (J 6 Гц, СНз), м 0,97-1,85 (СН2, СН), дд 2,22 (J 6 Гц и J 2 Гц, СН2СО), т 9,65 (J 2 Гц. СНО).
Аналогично получают соединения Па, Ив: транс-1-этил-4-циклогексилуксусный альдегид (На), выход 70%, т.кип. 62°С (1 мм рт.ст.); транс-1-пентил-4-циклогексилуксусный альдегид (Ив), выход 72%, т.кип. 9395°С (1 мм рт.ст.).
1.2.(4-транс-Пропилциклогексил)этиленил}-пиперидин (IV6).
Смешивают 0,078 моль безводного сульфата натрия с 0,086 моль пиперидина и при температуре в атмосфере азота прикапывают 0,039 моль соединения 116. Перемешивают реакционную массу 3 сут при комнатной температуре, осадок отфильтровывают, промывают гексаном, объединяют фильтраты и перегоняют в вакууме, т.кип.
118-120°С (1 мм рт.ст.). Выделяют 1-|уЗ-(4транс-пропилциклогексил)-этиленил -пипе ридин с выходом 75%.
Найдено,%: 6,13. Cj6H29N. ВычислеHO,%:N5,95.
Спектр ПМР (ССМ, (5, М.Д.): т 0,85 (J 6 Гц, СНз), м 0,97-1.85 (СН2, СН), м 2,52-2,76 (CH2N), дд 4,10 (J 7 Гц и J 14 Гц. СН С), д 5,60д 14Гц, ).;:
0 Аналогично получают соединения IVa, IV в: 1 (4-транс-этилциклогексил)-этиленил -пиридин (IVa), выхбд 75%, т.кип. 110113°С (1 мм рт.ст.). I Майдено,%: N 6,19. C15H27N, Вычислено,%: N 6,33; (A5 транс-пентилциклогексил)-этиленил)-пири- дин (IV в)-выход 50%, т.кип. 153-155°С(1 мм рт.ст.). Найдено , %: N 5,52. CieHisN. Вычислено, %: N5,31.
1.3.1-(3-Димети 1аминопропионил)-4-(40 транс-пентилциклогексил)-бензол (V в).
Смесь 0,13 моль 4-(4-транс-пентияциклогексил -ацетофенона (V|B), 0,22 моль параформа и 0,13 моль гидрохлорида диметиламина, 0,25 мл концентрированной
5 соляной кислоты, 15 мл абсолютного этилового спирта кипятят при 78-82°С 8-10 ч, охлаждают, разбавляют 100 мл абсолютного ацетона. Выпавший рсадок 1-(3-диметиламинопропионил)-4-(4-транс-пентилциклоге0 ксил)-фенилгидрохлорида (Vile) отфильтровывают, растворяют в 200 мл воды, подщелачивают водным раствором гидроокиси натрия, экстрагируют хлористым метиленом. Органический слой сушат над Na2S04,
5 отгоняют растворитель.
Получают 1-(3-диметиламинопропионил)-4-(4-транс-пентилциклогексил)-бензол (VB), выход 75%. Аналогично получают соединения Va, V6. Соединения Va-Vs, не анализируя, направляют на следующую стадию.
1.4.Йодметилат 1-(3-диметиламинопропионил)-4-(4-транспентилциклогексил)-бен- зoлa().
Растворяют-0,11 моль соединения V в 110 мл безводного хлористого метилена и прибавляют при 10°С 0,18 моль йодметана, оставляют на 2 сут в темноте. Осадок соединения Villa отфильтровывают, промывают безводным CH2CI2 и высушивают на воздухе. Получают Йодметилат 1-(3-диметиламинопропионил)-4-(4-транс-циклогексил)-бен зола (Villa), выход 98%. Аналогично получают соединения Villa, VIII6. Соединения Villa, и VIII6, не анализируя, направляют на следующую стадию.
1.5.1-Акрилоил-4-(4-:транс-пентилциклогексил)-:бензол (ККв).
Суспендируют 0,056 моль соединения VIИв в смеси 110 мл воды и 180 мл хлористого метилена. Прибавляют к суспензии при интенсивном перемешивании в течение 15 мин раствор 3,2 г КОН в 32 мл воды, реакционную смесь перемешивают еще 10 мин, происходит полное растворение осадка. Органический слой отделяют, водный экстрагируют 20 мл CH2CI2. Органические экстракты объединяют, промывают водой, добавляют гидрохинон, сушат над Na2S04, фильтруют через Si02 (h 3 см), отгоняют растворитель в вакууме..
Получают 1-акрил оил-4-(4-транс-пентилциклогексил)-бензол (1Хв).
Спектр ПМР (CCU): б, м.д.); т 0,86 (СНз), м 1,0-2,0 (СН2 и СН), м 2,65-2,78 (Аг-СН), дд 5,73 (J 2 Гц и J 10 Гц. С СН2). ДД 6,29 (J 2 Гц и J 17 Гц, С СН2), ДД 7,08 (J 10 Гц и J 17 Гц, СОСН), д 7,14 (J 8 Гц. 3-Н. 5-Н), д 7,75 {J 8 Гц, 2-Н, 6-Н).
Аналогично получают соединения 1Ха, 1X6. Соединения 1Ха-1Хв во избежание разложения не перекристаллизовывают и направляют на следующую стадию.
1.6. (4-транс-Пентилциклогексил)фенил -5-(4-транспропилциклогексил)-пир - идин(1вб).
Смешивают при 0-10°С 0,0375 моль соединения 1Хв с 0,034 моль соединения IV6 и 15 мл абсолютного этанола. Смесь выдерживают при комнатной jeMnepaType 2 ч, охлаждают до 0°С, осадок отфильтровывают и промывают 10 мл абсолютного этанола (предварительно охладив его до 0°С). Растворяют полученный пиран Хвб в 90 мл диоксана, прибавляютО,14 моль гидрохлорида гидроксиламина, 10 мл воды и 5 мл концентрированной соляной кислоты. Реакционную смесь перемешивают и кипятят при. 97-101°С 8 ч. Отгоняют 2/3 объема растворителя, к остатку прибавляют 150 мл воды и при 25-30°С подщелачивают до рН примерно 8 водным раствором едкого натра. Выпавший осадок отфильтровывают, промывают водой, сушат на воздухе, растворяют в бензоле и фильтруют через слой L 5/40 (h 3 см). Из фильтрата отгоняют растворитель. Остаток перекристаллизовывают из ацетона или CCU. Вы еляЮт 0,24 моль2- 4-(4-транс-пентилциклогексил)фенил -5-(4-тра НС-пропил циклогекСил)-пиридина (1вб), выход 70%.
Спектр ПМР (CCI4, б, М.Д.): т 1,03.(J б Гц,. СНз). м 1,10-2,05(СН2, СН). м 2,23-2,63 (СЙАг), ДД 7,08 (J 9 Гц, З-Н, 5-Н), дд 7,29 (J 8 Гц и J 2 Гц, 4-Н), д 7,48 (J 8 Гц, 3-Н), д 7,71 (J 9 Гц, 2-Н, 6 -Н), д 8,34 (J 2 Гц, 6-Н).
Аналогично получены другие (4 транс-ал кил циклогексил)-фенил -5-{4-транс-алкилциклогексил)-пиридины (I). Температуры фазовых переходов, элементный ана5 ЛИЗ и выход соединений (I) представлены в табл.1.
Соединения I являются транс-изомерами. Спектры ПМР С соединений I записаны на Фурье-спектрометре WP-80 в режиме
0 полной спиновой разрядки от протонов. Сигналы углерода циклогексановых колес 33,5 и 34,5 м.д. имеют удвоенную интенсивность. Характер этих сигналов соответствует транс-расположению заместителей в
5 обоих циклогексановых кольцах,
Сравнительные данные по температурам фазовых переходов для известных соединений - 4-{4-транс-алкилциклогексил)-4 -(4-тра НС-ал кил циклогексил)-бисфенилов
0 (XI) и предлагаемых соединений I представлены в табл.2.
П р и м е р 2. Получение жидкокристаллического материала (ЖКМ). 0,2 г (20 мас.%) 4-(транс-4-н-пропилциклогексил)-бензонит5 рила, 0,16 г (16 мас.%) 4-(транс-4-н-бутилциклогексил)-бензонитрила, 0,22 г (22 мас.%) 4-(транс-4-н-пентилциклогексил)бензонитрила, 0,25 г (25 мае. %) 4-(транс-4-нп;ентилциклогексил)-4-этилбифенила, 0,07 г
0 (7 мас.%) 4-(транс-4-н-Пропилциклогексил)этилбензола, 0,1 г (10 мас.%) (4-транспентилциклогексил)-фенил -5-(4-транс-про пилциклогексил)-пиридина помещают в сосуд, нагревают до , тщательно перемешивают и получают готовый к употреблению жидкокристаллический материал с интервалом нематической фазы от -20 до 85.,8°С.
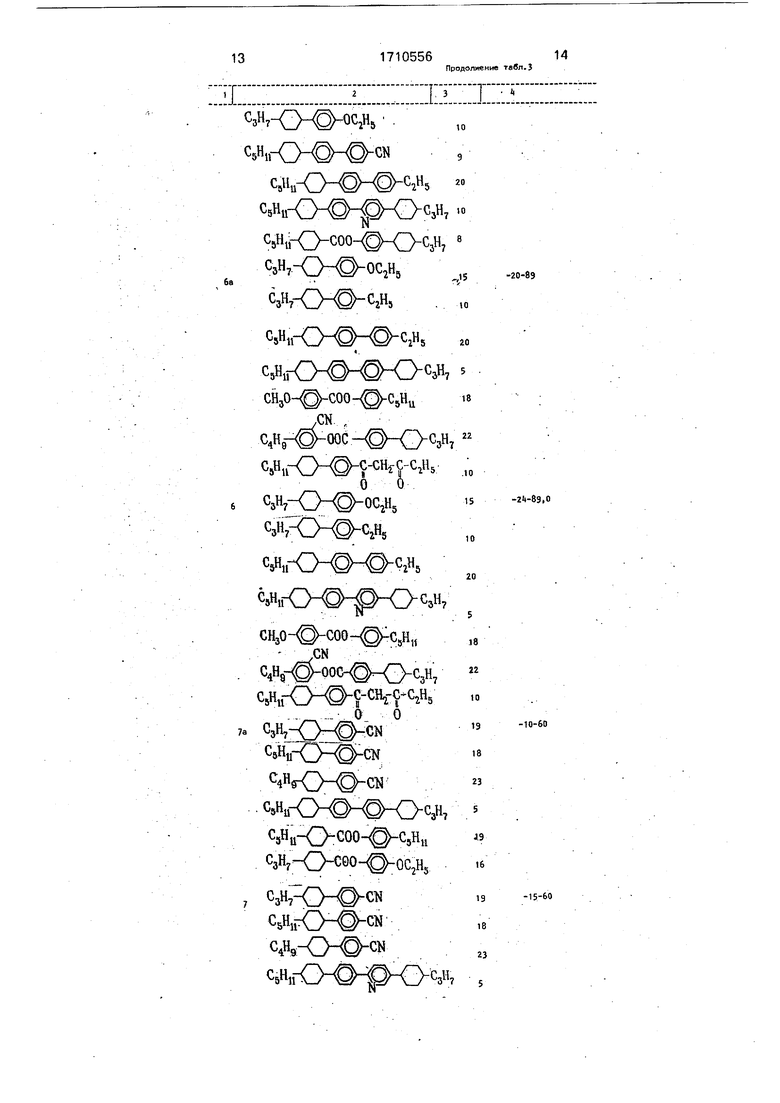
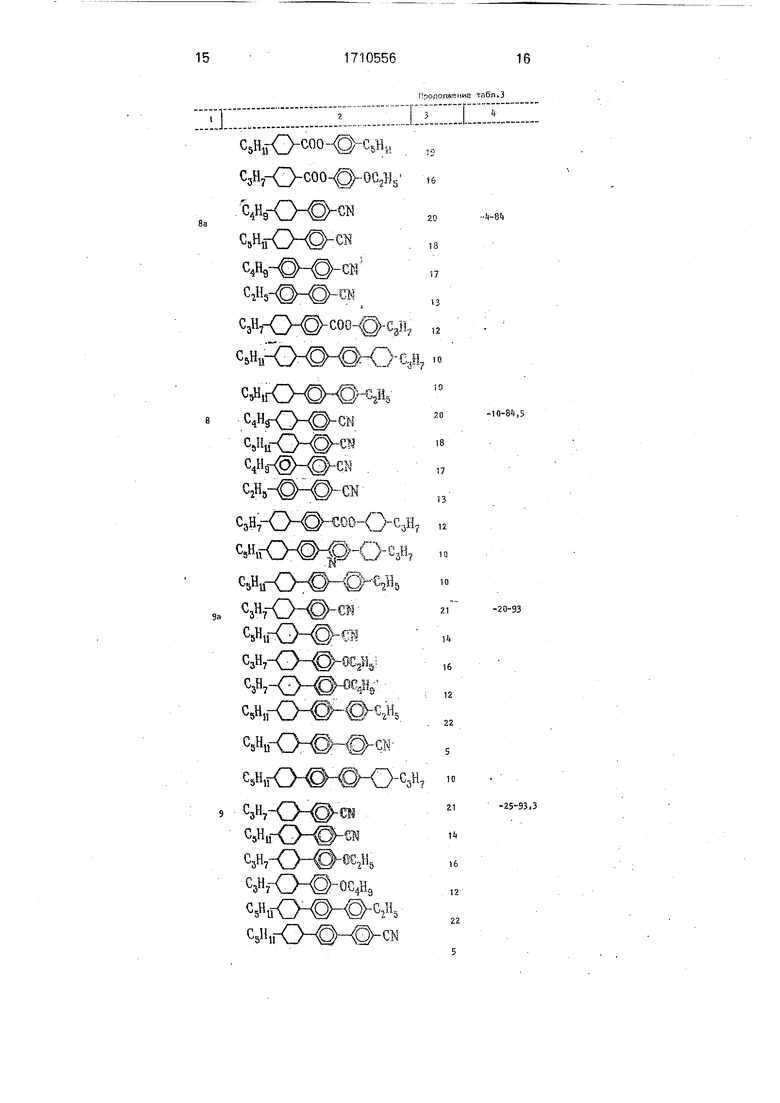
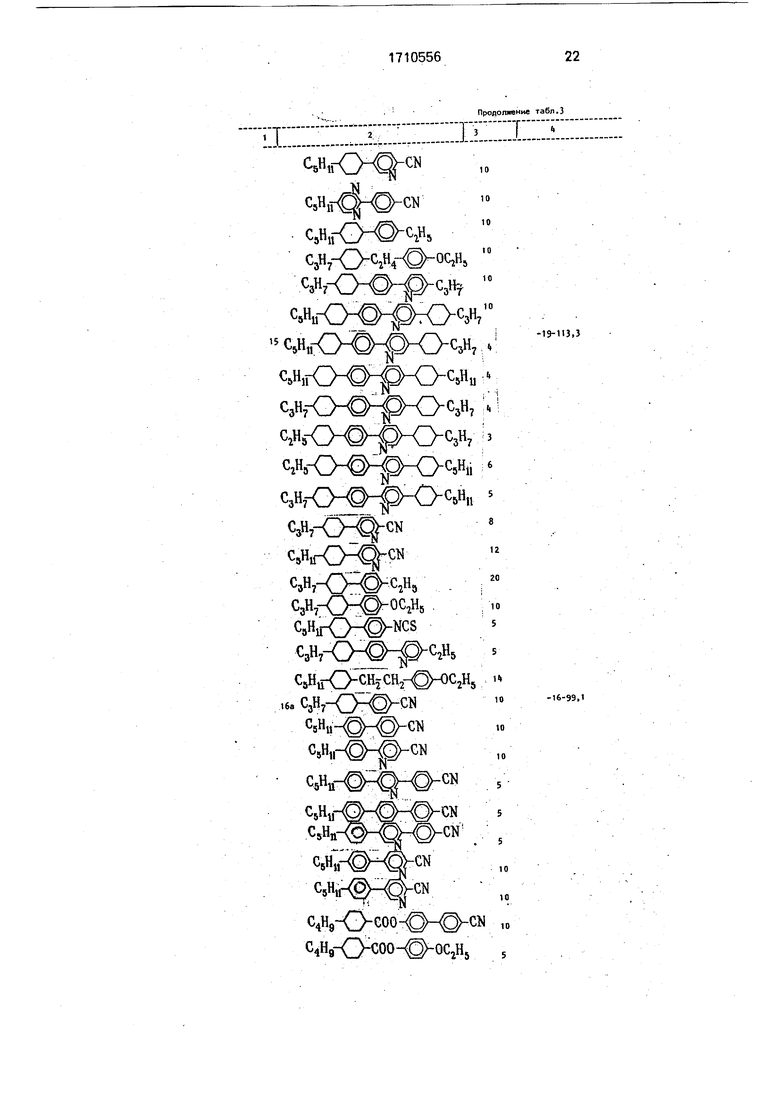
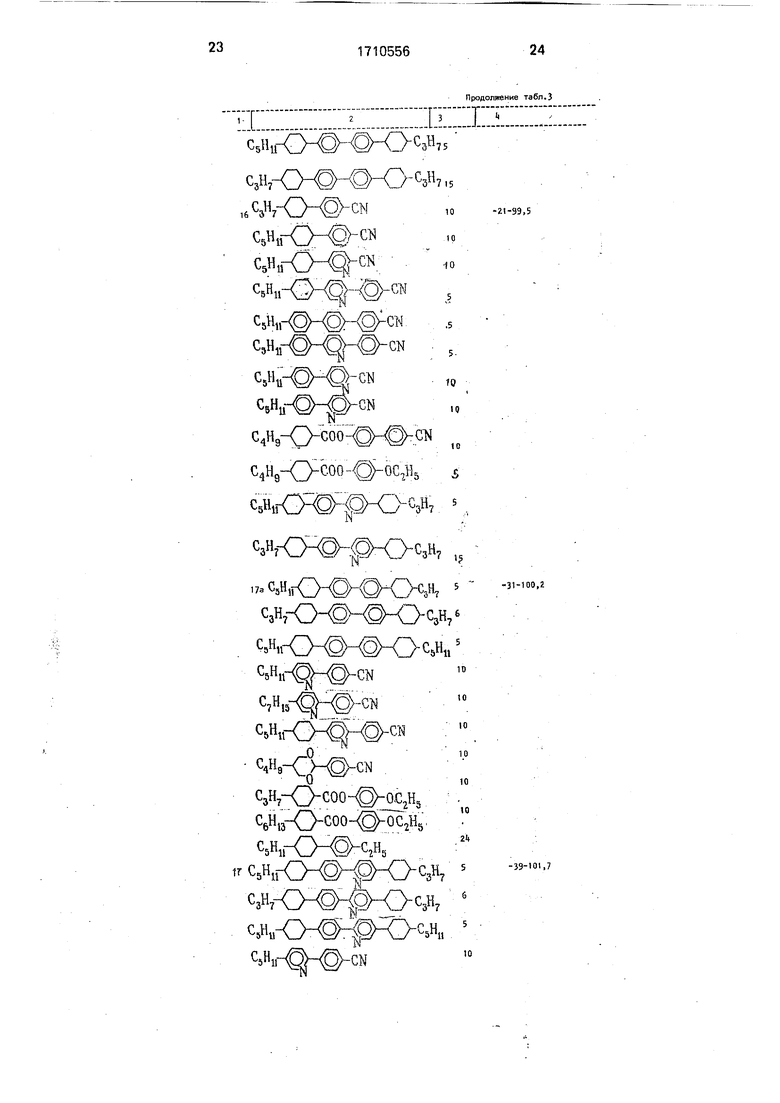
Аналогично получают другие ЖКМ по примерам 3-19. Составы ЖКМ, интервалы
0 нематической фазы ЖКМ по примерам 2-19 приведены в табл.3. Там же для сравнения приведены составы по известным компонентам, интервалы нематической фазы для ЖКМ, в которых соединения I заменены равным количеством известных соединений XI (примеры 2а - 19а).
Примеры 18 и 19 - сравнительные, из которых видно, что при повышении содержания соединений I (больше 26%)
0 повышается нижний предел интервала нематической фазы (примеры 19а и 19). Снижение содержания соединений Г (меньше 5%) не оказывает влияния на значение нижнего предела интервала нематической фазы
5 (примеры 18а и 18)..
Таким образом, предлагаемый жидкокристаллический материал имеет меньшее значение нижнего предела интервала нематической фазы (-39 -10°С), чем известный жидкокристаллический материал (-31 -4°С).
Кроме того, предлагаемый ЖКМ обладает низкой кинематической Вязкостью (v 19 - 26 при ), что позволяет использовать его в электрбоптических индикаторных устройствах наружного применения, где требуется быстродействие при отрицательных температурах.
Формула изобретения
1,(4-транс-АлкилциклоГёксил)-фенил}5-(4-тpaнc-aлкилциклoгeкcил пиpидины общей формулы I
СпНа..1 ,
где п - целые числа 2, 3, 5;
m - целые числа 3, 5,
в качестве компонентов жидкокристаллического материала для электрооптических устройств.
2.Жидкокристаллический материал для электрооптическихустройств, состоящий из жидкокристаллических веществ, выбранных из классов: производных бифенила, циклогексана, диоксана, пиримидина, азоксибензолов, эфиров бензойных кислот, эфиров циклогексанкарбоновых кислот, оснований Шиффа, дикетонов, алкилфенил- и алкилциклогексилцианпиридинов, ал кил-, алкилфенил- и алкилциклогексилцианфенилпиридинов, алкилциклогексилфенилалкилпиридинов, отличающийся тем. что. с целью снижения нижнего предела интервала иематической фазы, материал дополнительно содержит от одного до шести
(4-транс-алкилциклогексил)-фенил}-5-( 4-транс-алкилциклогексил)-пиридинов общей формулы )
Cn%:iOQ-OO «2-i
N
где п - целые числа 2, 3. 5;
m - целые числа 3,5,
при следующем соотношении компонентов, мас.%:
2- 4-{4-транс-Алкилцйклогексил)-фенил -5-(4-трансалкилциклогексил)-пиридины формулы I5,0-26,0
Жидкокристаллические веществаОстальное









| название | год | авторы | номер документа |
|---|---|---|---|
| 2-[4-(4-Транс-алкил-3-метилциклогексил)фенил]-5-алкилпиридины в качестве компонентов жидкокристаллического материала и жидкокристаллический материал для электрооптических устройств | 1988 |
|
SU1749218A1 |
| Жидкокристаллический материал для электрооптических устройств | 1987 |
|
SU1749229A1 |
| 2-[4-(4-Транс-алкил-3-метилциклогексил)-фенил]5-(4-транс-алкилциклогексил)пиридины в качестве компонентов жидкокристаллического материала и жидкокристаллический материал для электрооптических устройств | 1988 |
|
SU1781214A1 |
| 4-Транс-н-алкенилфениловые эфиры 4Ъ-транс-н-алкилциклогексанкарбоновой кислоты в качестве компонентов жидкокристаллического материала для электрооптических устройств и жидкокристаллический материал для электрооптических устройств | 1987 |
|
SU1527235A1 |
| Гетероциклические соединения, содержащие окси-группу, в качестве компонентов жидкокристаллического материала и жидкокристаллический материал для электрооптических устройств | 1988 |
|
SU1775399A1 |
| Жидкокристаллический материал для электрооптических устройств | 1985 |
|
SU1302684A1 |
| Производные пиридина в качестве компонентов жидкокристаллического материала для электрооптических устройств | 1988 |
|
SU1749219A1 |
| ПРОИЗВОДНЫЕ ХЛОРДИФТОРМЕТОКСИФЕНИЛА И ЖИДКОКРИСТАЛЛИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЭЛЕКТРООПТИЧЕСКИХ УСТРОЙСТВ НА ИХ ОСНОВЕ | 1993 |
|
RU2070191C1 |
| Производные 5-(4-транс-алкилциклогексил)пиридинов в качестве компонентов жидкокристаллического материала и жидкокристаллический материал для электрооптических устройств | 1988 |
|
SU1754714A1 |
| 6-Алкил-2-(4-цианофенил)-5,6,7,8-тетрагидрохинолины в качестве компонентов жидкокристаллического материала для электрооптических устройств и жидкокристаллический материал для электрооптических устройств | 1987 |
|
SU1749221A1 |
Изобретение касается жидкокристаллических веществ, в частности 2-[4г
Темпе1 атуры фазовых переходов, данные элементного анализа и выход (|-транс-элкилциклогексил -111енил2-5-(-транс-алкилциклогексил)-пивндин9В
«-О- Оф-О-«
т а 6 л и ц а I
Сравнительные данные по температурам фазовых переходов предлагаемых соединений I и известных соединений XI
Состав ЖКН и интервалы нематической фазы RKH
CjH,
му-&р
а
СзНу-О- ОД
b-cii АНпнСн5-вкс,н,
CsHu
Сг«5- 0СзйгО-р-ек
ТаблицаЗ
-20-85.8
16 22 Z5-7
to
-10-66
162217 27
CgH., ,)0
-Й-66,5
16
22
/ -
CsHjjс5н„-ОнО-р-О,
7CHjO
CHjO-Q-coo
C Hgto
-25-8V
10
5
-31.0-Bii.l
10
10
20
--N-KJH
23
12
JCN:
ООС-ОкО-СаНт сДо
-10-8
«rQ-GOo
СзНг-О- С,Нд
10
8 13
-(г-в.з
to го
Qiu
С5Ни-О- Э-вК СзНт СэН ;-ОсооСНзО
-coo.CN C Hg- -OOCS H CgH,
C5HirO- D-c-c%c- c Hg
7e СзН7-О10-:ск
C5Hu-O- 5-CN
- I
СзНц u-Ocoo-0-C5H,i
СзНунЭ-сео
СЛ
5Н„-О - К СзН,
ii:::::i
10
9 20
OC,Hg
-20-89
.,15
to
p U 22
tgH
C-CHj-C-C Hj
.10 00
-2lt-89,0
15
ID 20
5
13
22
10
-10-60
13
18
23
5
J.9
16
-15-60
19 18 23
;I::::::Z:::: ::::I:I:L:::
C5HiT CQO-0-C,H, СзН7Ч СОО- Оь-ОС,11д ,е
5HfiO S -CK
-Qi
-Ш СОО
О- -О-СЛ
-С СэНт-О-О ОО-О-СзН,
сАг оьрч: сан.
С Ни-Он СШ
СзНг-О- ОС:,, С,Н,,11,С5Н, CsHirO O CN 5 11
C5 irO-O- c i
)6л.З
продолжение т: Ц
..)-8)
ЗН 12
iO
-10-81, 5
20
-20-93
-25-93,3
СаНгСнОф-О-СзН
сдаоид --О-СзН7,
C3HfO- Q OC2H5
СбНцсдаоо- ЭК сл
10
СаН7-О-©-ОС,Нд
Продолжение табл.3
IJZZI
7 10
-10-59
,8
1Z.
-16-59,3
IS
21
18
12
c Hu-Q-0-eN
СзН7-СмОьс,Н5
СаНгО ОС Нэ
5НгС - ВмОи:,Н5
-ZO-85
23
17
16
12
ОЧТ
, 28
СНз-ОСЛ-С -ООС-0-ОС-СбН15 22
с НйОО соо-ОСзН, « ,H, п
. С}
13а
C5HirQ- Qbcii; C.H«-(O-C
)НО))
CbHtiOO-p-Oc ii
tl.a 3 7С5Н„о хОмО -с 1
СзН„-о- д-с
СэНн-нОнОьС
С5Нц- чЩ -с 1
-N
,
Продолжение
ijii
-11-70,3
9
-7-88
21,6 32,1. 22,5 13,5 10,0
-11-88,2
21,6
32,Ji 22,5
13,5
10,0
-16-86,)
10
1C
10
10
10
10
10
10
СзН7-Ос,н,,н, зН.
, -о
1-.
СвН,
10
10
-21-86,6
10 10 10 10
:::z:::;::i;:i::zzr
,
зН.-ОО-р-СзНсл- а --р7 сзнг
С НсО-О-рЮ-СзН. .r 0 -pK C5flu
СзНг -О р-О-сА :
С Г 0 - рК СзН/1з
сгНбООьр-оэд: 6
СзНгО-О -р-О-СьНи ед-O- CN C,
СзН7Ч :Р-ос и
C5HrO-C - cs СзН,,н,
CsHrO )2Hi
i6e СзН7-О-; 0 -С«
C5H,,HOHpbG J CsH - QHOhClJ
с Нд- О-еоо iHg-Q-coo
Продолжение табл.З
10
DVcN
10 10
to
h
10
-19-113,J
20
c,H,
10
14 10
-16-99,1
10
10
10
т
10
С5Пи- €Ь-бК С,Н,/
сА-ОО-ОК /-СзН7„
CsHuO- CN ,0
) 5 C5Hn- gMQh QbCN, ,5 C5Hii- b q 0-C I .
C5Hir -p-CN
c4H9- coo- o- g -c j
C4H9- C-00-0-OC,ll55
cSiiOV-pKD-c HT. , Сзн,-см0., ,
слгО-О -О-С зН. .
cлЧ x0 чg -O-CьHt,
0 -CN
с.и,
- C4H9-CHD-CN
010
зНт-О-СОО-О-ОС Нз
СбНйЧЗ-соо- ос н.
С,Н,
СзН7Ч ;фК СзН,
.Hn
10
. to
10
10
inllo
10
to
C4Hg- Hg) ,
CjH -O-eoo бНй-О-соо
CsHy
CsHit-CH N
18а CvH«4 - C J
c5H,
СЛ
«CoHtf ««-O-P-CNCsHjj- -Q-CN
csHu-x Q}
ЛИэ-О аО-О-Сз
CjHjj
С5Н1гО-%р- СэИ7 CN
CaHr-O-S OC H
Продбпжение табл.3
:: :::::::::::::L:::::::::iL::-i7
193 ед-Op-ci ,0 -э-107
CsHu-O-O-CN
зНтЧЗ СООнО-ОСзНу 7 СзН7-О-0-ОС,Н5 23
.з С5Н,,,
5НйК х5- -О-€зН,,
1Эед -р-С1 ;,0
f
10
-СОО- § -ОСзН7 17
C.,3 С5Н,
СА-О-€ К СА
Продолжение табл.,Н523
| W.H.de Jeu, R | |||
| Eldenschlnk | |||
| Smectic behawior and molecular structure; On the mesomorphism of a series of hydrocarbons | |||
| - J | |||
| Chem | |||
| Phys., 78 | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| УСТРОЙСТВО ДЛЯ ЭЛЕКТРИЧЕСКОГО ОСАЖДЕНИЯ ВЗВЕШЕННЫХ В ГАЗАХ ЧАСТИЦ | 1925 |
|
SU4637A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
Авторы
Даты
1992-02-07—Публикация
1987-04-07—Подача