Изобретение отиосится к усовершенствованному способу получения кетонов тетрагидрофуранового ряда формулы
L(CH2-CH2)-C-Il
Ч X
О
о
где R - алкил или арил и п -- целое чнсло от О до 2, которые могут быть использованы в качестве полупродуктов в органическом синтезе, а также в качестве специфических растворителей высокомолекулярных соединений.
Известен способ получения кетонов тетрагидрофуранового ряда гидрированием в жидкой фазе соответствующих ненасыщенных фурановых кетонов в присутствии палладий-алюминиевого катализатора при повыщенном давлении водорода и постепенном повышении температуры от 20 до 100°С.
Недостатками известного способа являются: длительность процесса (5 час), большой расход катализатора {5%-ный палладий-алюминиевый катализатор берут в количестве 10% от веса гидрируемого вещества), необходимость периодически его активировать и довольно высокая температура процесса.
Целью иастоянгего изобретения является
упрощение технологии процесса и повьпиение иы.хода целевого продукта.
Предлагают способ получения кетонов тетрагидрофуранового ряда, заключающийся в
iOM, что соответствующий ненасыщенный или насыщенный кетон фураиового ряда подвергают жидкофазному гидрированию при повыiHoiHOM давлении водорода в присутствии руте1;иевы. пли родиевых катализаторов, с выде.TGiHieM целевого продукта обычными приемалИ1.
Реакцию проводят при постоянном давлении недорода в интервале 10-150 атм при температуре 20-бО С.
Повыщение температуры вьнпе 60°С нежелательно, т. к. это обычно приводит к дальнейи гему гидрированию карбонильной группы и получению в качестве продуктов реакции, главным образом, тетрагндрофурановых спиртов. Гидрированию подвергают растворы ненасы неннь х или насыщенных фурановых кетонов в спиртах, диоксане, эфире, циклогексане и т. н. нли ведут процесс без растворителя. Предлагаемый способ позволяет значительно сократить время процесса (реакция протекает в течение 10-90 мин). Большая активность катализаторов на основе рутения и родия, их высокая избирательность при восстановлении двойных связей в боковой цепи и в
фура новом цикле по сравнению с кетогруппон
позволяют получать тетрагидрофурановые кетоны с более высоким выходом (80-90%). В отличие от платиновых и палладиевых рутениевые и родиевые катализаторы менее склонны к отравлению.
Катализаторами могут быть как свободные металлы (черни) или их окиси, так и металлы на носителях (окись алюминия, силикагель, уголь и др.).
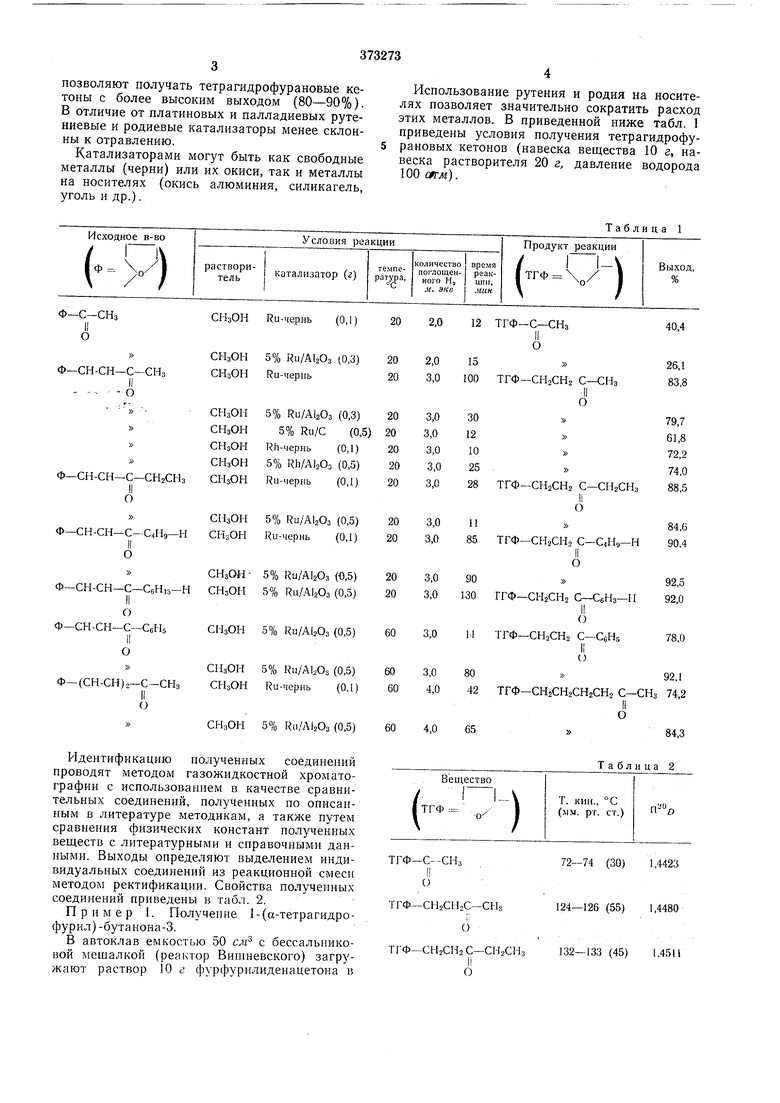
Использование рутения и родия на носителях позволяет значительно сократить расход этих металлов. В приведенной ниже табл. 1 приведены условия получения тетрагидрофурановых кетонов (навеска вещества 10 г, навеска растворителя 20 г, давление водорода 100 атм).
Таблица 1

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ГИДРИРОВАНИЯ α, β-НЕНАСЫЩЕННЫХ КЕТОНОВ | 2013 |
|
RU2529033C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТЕТРАГИДРОФУРАНОВЫХ СОЕДИНЕНИЙ | 1962 |
|
SU151347A1 |
| Способ получения -или изомеров -аминокислот | 1971 |
|
SU640659A3 |
| СПОСОБ ГИДРИРОВАНИЯ АЛЬФА, БЕТА-НЕНАСЫЩЕННЫХ КЕТОНОВ | 2013 |
|
RU2529032C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФЕНИЛАМИДА 5-(4-ФТОРФЕНИЛ)-1-[2-(2R,4R)-4-ГИДРОКСИ-6-ОКСОТЕТРАГИДРОПИРАН-2-ИЛ)ЭТИЛ]-2-ИЗОПРОПИЛ-4-ФЕНИЛ-1H-ПИРРОЛ-3-КАРБОНОВОЙ КИСЛОТЫ | 2003 |
|
RU2279430C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ОКТЕНА | 2002 |
|
RU2279420C2 |
| Способ получения производных 6- метилканамицина а и в | 1975 |
|
SU581873A3 |
| Способ получения циклогексана | 1977 |
|
SU662538A1 |
| РУТЕНИЕВЫЙ КАТАЛИЗАТОР СЕЛЕКТИВНОГО ГИДРИРОВАНИЯ НЕНАСЫЩЕННЫХ ПОЛИМЕРОВ И СПОСОБ ГИДРИРОВАНИЯ НЕНАСЫЩЕННЫХ ПОЛИМЕРОВ | 2010 |
|
RU2482915C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТРЕТИЧНЫХ АМИНОВ | 2012 |
|
RU2499793C1 |

СНзОН Ru-чернь (0,1)20
Ф-С-СНз II О
5% Ки/АЬОз tO,3)20
СЫзОМ
-СН-СН-С-СНз СНзОН
Ru-чернь20
11 - - О
-СНзОИ
5% Яи/АШз (0,3)20
5% RU/C (0,5)20
СНзОН
СНзОН
Rh-чернь (0,1)20
5% Rh/AI,03 (0,5)20
СНзОН
-СН-СН-С-СНгСНз СНзОН
Ru-чернь (0,1)20
II О
5% Ru/Al2O3 (0,5)20
СНзОН
Ru-чернь (0,1)20
-СН-СН-C-CiHg-Н СНзОН
II о
5% Ru/AlaOs (0,5)20
СНзОИ
5% Ru/Al2O3 (0,5)20
-СН-СН-с-СбН1з-Н СНзОН
О
СНзОН 5% Ru/Al2O3 (0,5) 60 Ф-СН-СН-С-CeHs
О
5% Ru/АЬОз (0,5) 60
СНзОН
(СН-СН) 2--С-СНз СНзОН Ru-чернь (0,1) 60
II о
5% Ru/Ai2O3 (0,5) 60
СНзОН
Идентификацию полученных соединений проводят методом газожидкостной хроматографии с использованием в качестве сравнительных соединений, полученных по описанным в литературе методикам, а также путем сравнения физических констант полученных веществ с литературными и справочными данными. Выходы определяют выделением индивидуальных соединений из реакционной смеси методом ректификации. Свойства полученных соединений приведены в табл. 2.
Пример 1. Получение 1-(а-тетрагидрофурил)-бутанона-3.
В автоклав емкостью 50 см с бессальникоиой мещалкой (реактор Вишневского) загружают раствор 10 г фурфурилиденацетона в
12 ТГФ-С-СНз40,4
II О
,1
100 ТГФ-СНгСНз С-СНз83,8
II О
,7
,8
,2
,0
28 ТГФ-СНгСНа С-СНгСНз 88,5
11 О
,6
85 ТГФ-СНаСНо С-С4Н9-Н90.4
11 О
,5
130 ТГФ-СНгСНа С-СеНз-Н 92,0
II (J
М ТГФ-CHaCHs С-CcHj78,0
II О
,1
42 ТГФ-CHsCHsCHsCHj С-СНз 74,2
II О
,3
Таблица 2
72-74 (30) 1,4423
С--СНз
II
С) 124-126 (55) 1,4480 СН2СН2С-СНз
о (45) 1,4511
СН2СН2 С-СН2СНз
|г
о
Авторы
Даты
1973-01-01—Публикация