где fij-L-{-) - Г-амино- -гидрокскбуткрил, L -(-)- -амино- -гидрок ипропионил или L-(-)- 8 -амино- - 30
-гидроксИвалерил, а Rj, - гидроксильная или с№«1ногруппа.
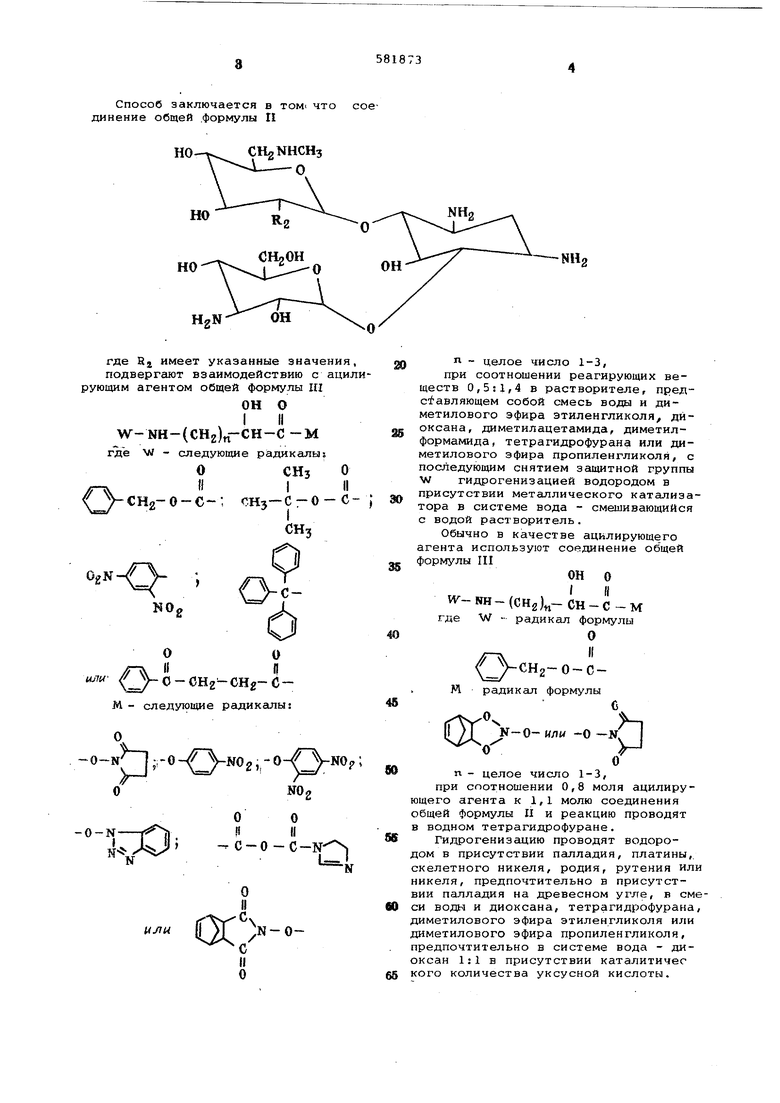
Способ заключается в том что соединение общей .формулы II
СН КНСНз
о
где Rj имеет указанные значения, подвергают взаимодействию с ацилирующим агентом общей формулы Ш
ОН О
I II
W-NH-(CH2)n-СН-С -М
где А/ - следующие радикалы
снз о
О
и
I II снз-с-о- с- I
п - целое число 1-3,
при соотношении реагирующих веществ 0,5:1,4 в растворителе, представляющем собой смесь воды и диметилового эфира этиленгликоля, диоксана, диметилацетамида, диметилформамида, тетрагидрофурана или диметилового эфира пропиленгликоля, с последующим снятием защитной группы W гидрогенизацией водородом в присутствии метсшлического катализатора в системе вода - смешивающийся с водой растворитель.
Обычно в качестве ацилирующего агента используют соединение общей формулы III
ОН О
(CH2)-CH-C-M
где W - радикал формулы
О
о о
/Г If и
. - следующие радикалы
О
i, 3
/Г N02
II 0 -C-N
l
;N-Oили
-CHg-O-CМ
радикал формулы
|Г ГЧ 0-«Л« -О-Np
п - целое число 1-3,
при спотношении 0,8 моля ацилирующего агента к 1,1 молю соединения общей формулы 11 и реакцию проводят в водном тетрагидрофуране.
Гидрогенизацию проводят водородом в присутствии Псшладия, платины,, скелетного никеля, родия, рутения или никеля, предпочтительно в присутствии палладия на древесном угле, в смеси воды и диоксана, тетрагидрофурана, диметилового эфира этиленгликоля или диметилового эфира пропиленгликоля, предпочтительно в системе вода - дноксан 1:1 в присутствии каталитичес
кого количества уксусной кислоты. Пример. 1-N-(L)-{T -ами но- t. -гидроксибутирил)-6 - N-метил канамицин А, К раствору 750 мг б- N -метилкана мицина А в 30 мл 60%-ного водного те трагидрофурана добавляют 525 мг гидроксисукцинимидного эфира Н -карбобенэокси- L - Г -амипо- о«. -гидроксимасляной кислоты. Реакционную смес гидрируют ночь при комнатной температуре при атмосферном давлении в присутствии 500 мг 10%-ного палладия на древесном угле. Реакционную смесь фильтруют, сушат под уменьшенным дав лением. Остаток растБГЬряют в небольшом количестве воды и адсорбируют в колонке с Амберлитом CG-50 ( NHJ , 70 мл). Колонку промывают водой и последовательно вымывают 850 мл 0,1 н. NHi,OH {20 мл фракции 1-43) , 1450 мл 0,2 и. МНцОН (20 МП фракции 44-115) и, наконец, 100 мл 0,5 н. NHi,OH (20мл фракции 116-215) . Фракции 152-161, обнаруживавшие биоактивность и нингидриновую реакцию при Rj 0,17 в TLC (силикагель, CHCEj - CHjOH28% NHi,OH - НгО 1:4:2:1), объединяют выпаривают под уменьшенным давлением лиофилизируют и получают 149 мг (16%) целевого продукта с т.пл. 187-189°С (раэл. ); ИК-спектр ( КВг ) : Ic 0. 1650 Вычислено,%: С 39,42 Н 7,03 N 9,23 Сг5Н„Ы50„2Н,,0 Найдено,%: С 39,26; 39,00; Н 6,69 6,54; N9,69, 9,20. Для удаления следов изомера II типа N -ацилированный изомер продукт подвергают хроматографированию в колонке с ионообменной -смолой Амберлит Cij-50 тетрааминомедного типа (ТАСи ). Для этого продукт (73г) растворяют в небольшом количестве воды и хроматографируют в колонке Амберлитом CG-50 (3 мл). Колонку про fJвaют 20 мл воды и затем элюируют 100 мл 0,2 н. ЫНцОН и затем 0,1 н. ЫНцОН . Элюат собирают фракциями по 7 мл, которые испытывают нингидриновой реакцией и на биоактивность (бактерии Sobtitis РС1-219 и Pseudomo nas aerufinosa) и Ttc на силикагеле (S -100, нингидрин) . Фракции 21-24 обнаруживавшие положительную нингидриновую реакцию и биоактивность (про тив штам,а Р. aeruginosa) г объединяют, выпаривают в вакууме и получают 30 м синего порошка. Этот синий остаток растворяют в небольшом количестве во ды, хроматографируют в колонке с CG-50 ( NHj , 3 мл) и элюируют 20 мл 0,2 н. МНцОИ и 200 мл 0,5 н. NH,OH. Элюат собирают фракциями по 7 мл. Фракции, дававшие положительную нингидриновую реакцию, объединяют, выпаривают в вакууме, сушат при температуре ниже 0°С и получают 20 мг чистого целевого продукта с т.пл. 187189 С (раэл.). Приме р2. l-N-(L)-ft-амино- л -гидроксипропионил)-6- N -метилканамицин А. Смесь 218 г (0,912 ммоля) N -карбобензокси - 1 - изосерина, 163 мг (0,912 ммоля) N -гидрокси-5-норборнен-2-, 3-дикарбоксимида ( OHNB ) и 188 мг (0,912 ммоля) дициклогексилкарбодиимида ( DCC) в 10 мл тетрагидрофурана оставляют стоять на ночь при и затем фильтруют. Фильтрат добавляют к раствору 441 мг (0,892ммоля) 6- N -метилканамицина А в 20 мл 50%-ного водного тетрагидрофурана и смесь перемешивают 5 ч при комнатной температуре и концентрируют затем под уменьшенным давлением до 2 мл. Концентрат адсорбируют в колонке с Амберлитом CQ-50 ( NHJ , 26 мл), которую прокывают 40 МП воды и элюируют 500 ь« 0,1 н. NH|,OH . Элюат собирают фракциями по 10 мл. Фракции 11-16 объединяют, выпаривают в вакууме и получают 231 мг N г-ацилированного продукта. Из элюата раствором 0,3 н. ИНг,ОН извлекают 175 мг (40%) исходного производного канамицина. К раствору ацилпроизводного в 20мл 50%-ного водного этилового спирта добавляют 130 мг палладиевого (10%-ного) .катализатора на древесном угле и смесь гидрируют при обычном давлении и комнатной температуре. Затем катализатор отфильтровывают и фильт рат выпаривают для удаления органического растворителя, полученный водный раствор подвергают хроматографн- |рованию в колонке с CG-50 ( ЫНц , 25 мл). Колонку последовательно элюируют 40 мл водя, 240 мл 0,1 н.ЫНцОН| 500 мл, 0,2 н. ЫНцОН , 300 МП 0,4 Н. и элюат собирают фракциями по 10 мл. Биоактивные фракции объединяют, выпаривают в вакууме и получают 127 мг неочищенного продукт|1, который опять хроматографируют в колонке с Амберлитом CG-50 ;(тетраминомедного типа 4 мл) и 200мл 0,3 н. ЫНцОН , 300 мл 0,5 H.NHj,QH и 300 мл 1 н. КН.„Ои . Элюат собирают фракциями по 10 мл. Результаты приведены в табл.1.
Т а
лица






Неактивная
it
Неактивная, вероятно изомер
Целевой продукт
Фракции 50-54 объединяют/ выпаривают досуха и получают 35 мг (6,8%) целевого биоактивного продукта с т.пл 178-185 С, с О 1630 CM-i.
Примерз. l-N-(L)-{ -амино- -гидроксивалерил)-б- N -метилканамицин А.
Смесь 94 мг (0,353 ммоля) N -карбобензокси- L - J -аминогидроксивалериановой кислоты, 64,3 мг (0,353 ммоля) HONB и 74,5 мг (0,353 ммоля) DC С в 5 МП сухого тетрагидрофурана оставляют стоять на ночь при 4°С и
фильтруют. Фильтрат добавляют к раствору 175 мг (0,35 ммоля) 6- N -метилканамицина А в 10 мл 50%-ного водного тетрагидрофурана и смесь перемешивают при комнатной температуре 5 ч. Реакционную смесь затем гидрируют при комНеактивная Смесь двух компонентов
Целевой продукт
Фракции 10-14 объединяют, выпаривают досуха и получают 24 мг (-11%) желаемого биоактивного продукта с т.1Л. 167-174°С (раэл.); М 0, 1620см
Пример7. l-N-(L)-f-амино- о4 -гидроксибутирил)-б -N -метилканамицин В.
Смесь 253 мг (1 ммоль) N -карбобензокси 1- f-arviHHo-oi.-гидроксимасляяой кислоты, 115 мг (1ммоль) N -гиЯГ-Оксисукцинимида и 206 мг (1 ммоль) DC С перемешивают 3 ч при 5°С и фильтнатной температуре в присутствии палладия (10%-ный, на древесном угле). Катализатор отфильтровывают и фильтрат выпаривают для удаления тетрагидрофурана. Полученный водный концент зат хроматографируют в колонке с Амберлитом (типа NH 20 мл) при последовательном элюировании водой (50 мл), 0,1 и. «НцОН (250 мл), 0,2 н КНцОН (450 мл) и 0,5 н. (400м Элюат собирают фракциями по 10 мл. Биоактивные фракции объединяют, выпаривают досуха и получают 40 мг неочищенного продукта, который опять xpoмaтoгpaфиpy т в колонке с Амберлитом СО-50 |(тетраминомедного1 типа, 1,5 мл) и элюируют Ю мл воды и ЮОмп 0,5 н. NHijOH . Элюат собирают фракциями по 5 мл.
Результаты приведены в табл. 2.
Таблица 2
руют для удаления осадка, выделивш гося при реакции. Полученный раствор активного сложного эфира добавляют к раствору 497 мг (1 ммоль) 6- N -метилканамицина В в 10 м.п воды и смесь перемешивают ночь при комнатной температуре. Реакционную смесь фильтруют и выпаривают в вакууме. Остаток растворяют в 5 МП воды и адсорбируют в колонке с Амберлитом СО-50 (смола типа ЫНц , 45 мл) и элюируют последовательно 200 мл воды, 1500 мл
0,05 и. аммиака и 500 мп 0,3 н..аммиака. Элгаант собирают фракциями по 10 мл. Промежуточное производное содержится во фракциях 58-72, злюироBaHiJHx 0,5 н. аммиаком, а из фракций элюированных 0,3 н. аммиаком, извлекают 163 мг (33%) исходного продукта Раствор промежуточного производного в 20 мл 50%-ного тетрагидрофурана гидрируют ночь под обычным давлением в присутствии 30 мг 10%-ного паллади на древесном угле. Реакционную смесь фильтруют и кбнцентрируют до 4 мл. Концентрат адсорбируют в колонке с Амберлитом CG-50 ( NH ц , Ю мп) , ко торую промывают 150 мл воды и элюируют последовательно 350 мп 0,5 н. ЫНцОН , 300 мл 0,1 н. , 150 мл 0,3 н. и 500 мл 0,5 н.МН(,ОН. Элюат собирают фракциями по 15 мл. Фракции 67 и 68, обнаруживавшие биоактивное пятно при RJ 0,22 наТиС
(силикагелевая пластинка, CHCt-CHjOH28% ЫНцОН-НгО : 4:2: 1) , объединяют и снова хроматографируют в колонке с Амберлитом CG-50 {нижняя часть, ННц - типа, 1 мл, верхняя часть те1траминомедного типа,2 мл). Колонку элюируют 100 МП 0,5 н. ЫНцОН и затем 50 мл 1 н. МНцОН и злюат собирают фракциями по 5 МП. Фракции 15-3 объединяют, выпаривают в вакууме и получают 29,4 мг (5%) желаемого биоактивного продукта с т.пл. 188-192C
(разл.); ИК-спектр (КВг): с
О 1640 .
Вычислено,%: С 41,55; Н 6,97; N 11,63
C jH eNeOn
Найдено,%: С 41,52; Н 6,72; N 10,95
Примера. l-N-(L)-j -амино- oi -гидроксипропионил)-6- N -метилканамицин В.
Перемешиваемую -тмесь из 120 мг (0,5 ммоля) N -карбобензокси-1-изосерина, 58 мг (0,5 ммоля) HOSu и 103 мг (0,5 ммоля) DC С в ТГФ оставCH2NHCH3
-О
HgN
ляют на ночь при 5С. Смесь фильтруют, фильтрат добавляют к раствору 248 мг (0,5 ммо.пя) б- N -метклканамицина В в 5 ьш вод411 и перемешивают ночь. После удаления ТГФ водный раствор адсорбируют в колонке на Амберпите CG-50 (ЫНц типа, 10 MI). Элюирование производят 300 мл 0,5 н. МНцОН , затем 300 мп 0,1 н. и собирают фракции по 10 мл. Желаемое промежуточное производное получают после выпаривания фракций 18-31 и элюирования 0,5 н. КН(,ОН , а из фракций, элюированных 0,1 н. аммиаком, получают 69 мг (28%) исходного б- N -метилканамицина В.
Раствор промежуточного производного в 10 мл воды гидрируют в течение ночи в присутствии 20 мг 10%-ного (талладиевого катализатора, затем реакционную смесь фильтруют и концентрируют до 5 мл. Концентрат хроматографируют в колонке с Амберлитом C(i-50 ( NHq , 8 мл) с элюированием последовательно 280 мл 0,05 H,NHi,OH , 340 мл 0,1 н. и 200 мл 0,2 н. КНцОН . Биоактивный компонент (35мг) получают из фракций, элюированных 0,2 н. КНцОН . Продукт, все еще показываюищй от двух до трех положительных пятен, очищают повторной кроматографией в колонке с Амберлитом C(i-50 (нижняя часть ЫНц , 1 мл, верхняя часть тетраминомедного типа, 2 мл) с элюированием последовательно 60 мл 0,3 н. МНцОН , 110 мл 0,5 н.ЫНцОН и 100 мл 1 н. NlipH,
Х елаемый продукт получают из фракций 40-50, элюированных 1,0 н.ЫНцОН.
Выход 8,1 мг (3%); т.пл. 190-198С (разл.); ИК-спектр ( КВг ): 1630 см
Формула изобретения
5Нр
NH- R
где RI .L -(-)- Г -амино- « -гидроксибутирил, U (-}- fi -амнно- X -гидроксипропионил или L. -(-).- U -амино- -гидроксивалерил, а RjCHgNHCHj
НО
HpN
гидроксильная или аминогруппа, отличающийся тем, что соединениеобщей формулы П -О
где R имеет приведенные значения, п вергают взаимодействию с ацилиующим агентом общей формулы III
ОН О I и . W -NH- (CHgItT С Н - С - М
где W - следующие радикалы;
, Г
CHg-O-G-,; СНз-С-О-С
или
М - следуюцрие радикалы: О
0-N
И
О
« -
-C-0-C-N J
или
П - целое число 1-3, - при соотношении реагирующих веществ 0,5; 1,4 в растворителе, представляющем собой смесь воды и диметилового эфира этиленгликоля, диоксана, диметилацетамида, диметилформамида, тетрагидрофурана или диметилового эфира пропиленгликоля, с последующим снятием защитной группы W гидрогенизацией водородом в присутствии металлического катализатора в системе вода - смешивающийся с водой растворитель.
ОН О I Я
W-NH-(CH2) где - радикал формулы
О
II
- Л- г-о-сМ - радикал формулы
ул« - о -
П- целое число 1-3, при соотнесении 0,8 моля ацилирующего агента к 1,1 молю соединения общей формулы П и процесс осуществляют в водном тетрагидрофуране.

Авторы
Даты
1977-11-25—Публикация
1975-12-09—Подача