рироваиием олефиновой связи в присутствии оптически активного координашюнно- го металлического комплексного катализатора гидрирования. Такая реакция иллюс рируется следующим уравнением II Где {Ь -заместитель представляет собой фенил, - симметричный атом, В дачестве примера {Ь -заместителя могут быть приведены такие группы, как водород, алкил, замещенный алкил, арил, арапкил, амино-, бензнламино-, дибенаил- амино-, нитро-, карбоксил- и карбоксильная эфирная группа и аналогичные, fb -Заместитель может выбираться из большо го числа групп и ограничивается только оС-аминокислотой, которая яеляется целевым конечным продуктом. Примерами Oi -аминокислот, антипо ды которых могут быть получены в соответствии с процессом изобретения, явля ются аланин, п хлорфенилаланин, триптофен, фенилаланин, 3-(3 4« диоксифенил)-аланин, 5-окситриптофав, лизин, гисти- дин, тирозин, леМин, ггаотаминовая кис лота и валив. Ацильная группа может быть замещеН ной или незамещенной ашльной группой, в качестве примеров ее могут быть приведены такие группы, как ацетил, бензо- ил, формил, пропионил, бутнрия, толуил, нитробензоил, или другие ацильиые раэновидности, используемые в качестве бло кирующих групп в пететидиом синтезе. Фосфиновый или арсшовый лига.нд мо.суг бьлть, например формулы где А представляет собой фосфор или мь шьяк; R, R и R - каждый незавиСИМО водород; алкил влй апкСксаш, имеющих по крайней мере оовк атом 5Т71ерода и максяамум 12 атсадов урлерода замешенный алкил с заместителями, представ лаюшими собой амиво, карбокил-, ари1 нитро и алкоксвгрзгппы, имеющие макс мум 4 углеродных атома, арил, арилоксв фенил, замешенный фенил с заместителя- MHji представляющими собой алкоксил или алкил, оксил, арнлоксвл, амино и ннтро руппЫ| причем количество заместителей оставляет менее 3; циклоалкил, имеющий, о крайней мере 3 углеродных атома, заещенный циклоалкил; пиррил, тиенил} фурил; гшридип, пиперидил или 3-холетерил. Оптическая активность металлического координационного комплекса согласно изобретению свойственна фос4шновому или арсиновому лиганду. Оптическая активность может быть результатом или наличием трех различных групп у атома фосфора или атома мыщьяка или наличия оптически активной группы, примыкающей к атому фосфора или мышьяка. В координационном металлическом комплексе вышеприведенной формулы один ли ганд ( L ) должен быть оптически актив ным для осуществления реакции. Если оптическая активность лиганда является следствием наличия оптически активной группы, примыкающей к атому фосфора или мыщьяка, должна иметься только Одна такая группа, а другие две могут быть Одними и теми же или неактив ными. В данном случае только одна из групп I , R или К должна быть оптически активной, остальные две группы могут быть идентичными или неактивными. Используются катализаторь, совершающие координационные металлические ком. плексы приведенных формул. показыва- ет асимиетрию н, следовательно, оптическую активность, она также обозначает асимметричный атом или дисимметрнчную группу. Например, R показывает, что фосфор или мьгщьяк асимметричны. От сутствие звездочки показывает отсутст ше оптической активности. ()з; CIDM X A R RR),j(); an)MX{A R R R)fAR5R6R7)g (iV)MX()3} (V) MA()(). {VI)()( OfinMXjCA R5 R RMj , )№4s(A R5RbR7) ). aX)MJ,() (X)№ X9{AR R { M,; ai)Mx,() л nrfc - (АЙ ajM),(), 9 1 (XW)MX2fA R R)(); ift«5i 6s (XV)M-XjfAR R R7)gj (XVl)M X.j(AR n6R7HAR R( где M, X, A, R R и R имеют указанные ранее значения. Способ предпочтительно осуществляют в присутствии оптически активного фос- финового или арсинового лиганда, где ли- гаид находится в соотношении от 1,5 до 2,5, предпочтительно 2, эквивалентов лиганда на 1 моль металла Предпочтительно иметь оптически активный катализатор в твердой форме для удобства обращения и хранения. Реакцию гидрирования обычно проводят в растворителе, таком как бензол, этанол, циклогексен, и в смесях указанных растворителей. Может использоваться почти любой ароматический или нась щенный алкановый или циклоалкановый растворитель, который является неактивным в условиях реакции гидрирования. Также могут использоваться растворители нитробензол, предпочтительно метанол Катализатор добавляется к растворите лю или сам по себе, или в виде его компонентов, которые затем образуют катализатор. Когда катализатор добавляется в виде его компонентов, он может добавляться как до, так и ьместе с добавлением |i -замещенной оС- циламидоак- риловой кислоты. Компонентами ля приготовления катализатора на месте являются растворимое металлическое соединение и оптически активные фосфиновый или арсиновый лиганд. Катализатор может добавляться в любом каталитическом аффективном количест ве и обычно в пределах от O.OOOl до 5 вес.% содержащегося металла, в расчете на содержание ft-замещенной оС-адил амидоакриловой кислоты и/или ее солей. Необходимо 1федпринимать меры для избежания контакта катализатора или реак ционной массы с окисляющими вещества1ли В частности, принимается предосторож ность с целью избежать контакта с кисло родом. Предпочитается выполнять подготовку к реакции гидрирования и фактическую реакцию в газах других по сравн .нию с Hg) которые являются инертными и по отнощению к реагентам и катализаторам, таких как азот или двуокись уплерода. Асимметрическое гидрирование усиливается при наличии основания в реакционной массе. Хотя асимметрическое гидрирование может выполняться в реакционной массе, свободной от основания,и даже может проводиться в кислых условиях {в кислой среде), оно усиливается .при прибавлении небольшого количества, не более, чем одного эквивалента, основного вещества на моль акриловой кислоты. Основаниами, которые могут использоваться, являются третичные, такие как триэтиламин, МаОИ, и почти любое друч гое основное вещество, которое буппт образовывать соли с карбоновыми кислотами. Реакционные температуры могут быть в пределах от -2О до . Более высокие температуры могут использоваться, но они могут увеличивать побочные реакции. Целевой продукт вьщеляют известными методами. Пример 1, В аппарат гидрирова- .НИН, снабженный прибором, измеряюншм давление, средствак5и измере тя темпера туры и нагревающими устройствами, загружается 25 частей с -бензамидо-4- -окси-3-метокснкоричной кислоты, 186 частей метанола и 64 части 5%-ной гидроокиси натрия. Ванна тщательно очищается от каких-либо следов воздуха и окончательно устанавливается давление 50 фунтов на кв. дюйм водорода и температуры 25°С. Раствор катализатора приготавливают растворением О,ОО59 родиевого 1,5-цик- логексадненхлорнда -1,5-гексадивн-Ct 2 в 2 мл бензола в атмосфере азота. Затем добавляют 0,О139 г (н-)-метилфенил-о- низилфосф1ша в 1,3 мл бензола. Затем водород пропускают через смесь в течение 5 мин. Полученный в результате раствор катализатора затем нагнетают в автоклав. Гидрирование начинается немедленно и заверщаегся по истечении 3-4 ч при 25°С и давлении 50 фунт на кв.дюйм, Испытание получившегося в результате раствора показало оптическую чистоту 56,4%, соответству ощую 78 (22 L ) Д смеси натриевой соли N-бензолил-3-(4-ок- си-3-метоксифенил)-«ланина. N -Бензоил- замещенная аминокислота может получаться с 95% выходом упариванием метанола и нейгрализакией натриевой соли соляной кислотой. 1олученный в результате L антипод Может превращаться в L -ДОРА (диок- сифенилаланин простым гидролизом для удаления блокирующих групп, бензоила и метила в положении 3 заместителя у фенила. Пример 2. В Однолитровый автоклав загружается 25 г I, -бензамидо- -4-окс -3-метоксикоричной кислоты.
ЗОО мл метанола и О,6 мл 5%-ного водного раствора МаОН.
Перемешивается при 25 С под давлением 4О фунт на кв.дюйм чистрго водорода. Затем приблизительно 1 мл (О,О1% Rtl и 0,О5% фосфина) раствора катализатора добавляется через отверстие без снижения давления Раствор катализатора припуГавливается растворением под Ng О,005О г ( )-1,5-гекседиен-(С) в 0,33 мл растш)ра метилфени о-йнизило- сфина с удельным вращением о13 « + 42 (метанол) в бензоле, содержащи О,Ь41 г/мл и разбавленный до объема в 1 мл метанолом.
Скорость перемешивания 14ОО об/мин сохраняется в реакционной массе и водород начинает адсорбироваться после 2-5минутноро индукционного периода и гидрирование заканчивается через 2 ч.
Метанол упаривают и кислоту растворяют в Одном моле водного раствора NaOH. Нейтральный катализатор экстрагируют бензолом и осаждают отдельно для регенерации. Свободную аминокислоту затем осаждают добавлением к концентрированной неб со свободным затраливанием (кристаллизации).; получают 24 г N-бeнзoиJ -3-(4-oкcи-3-мeтoкcифенил)-вланина, содержащего 73% L - антипода и 27% 33 - антипода. L -антипод может превращаться в {, -диоксифе- нилаланин гидролизом.
Примеры 3-17. Другие оггг чески активные L -аминокислоты полу. чают по способу примеров 1 и 2. Гидрируется олефиновое соединение, фосфиновый лиганд используют в родиевом катализаторе. Оптическая чистота приведена в таблице.


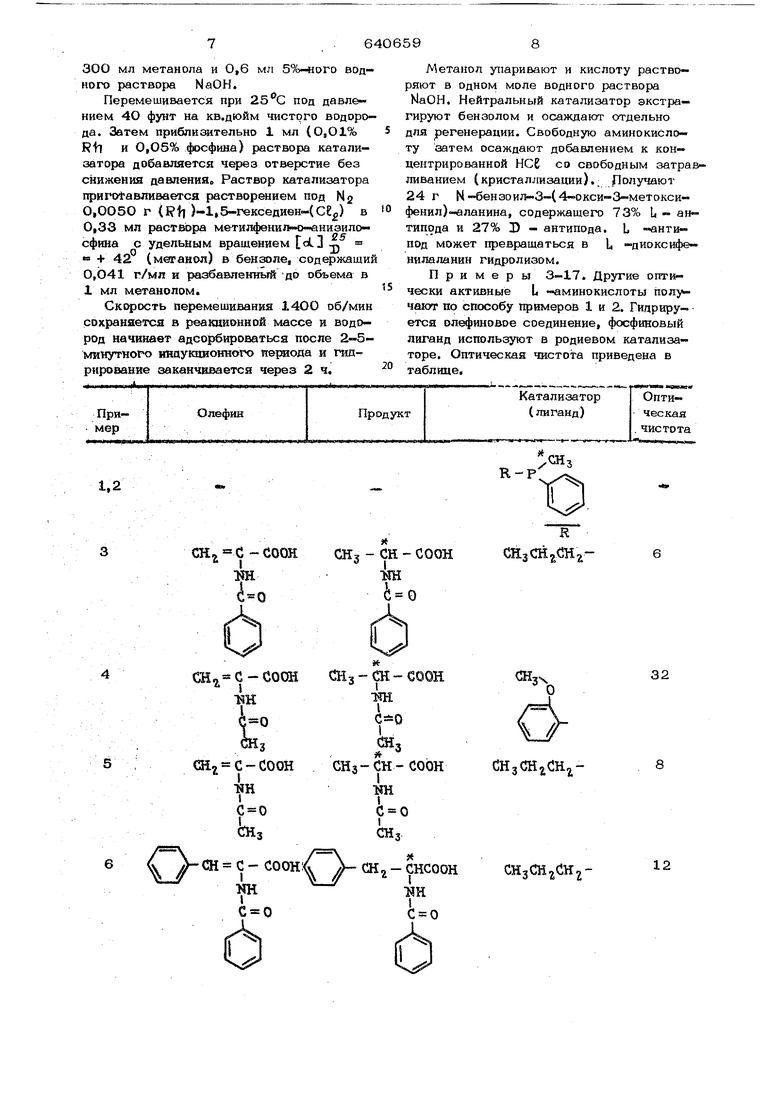

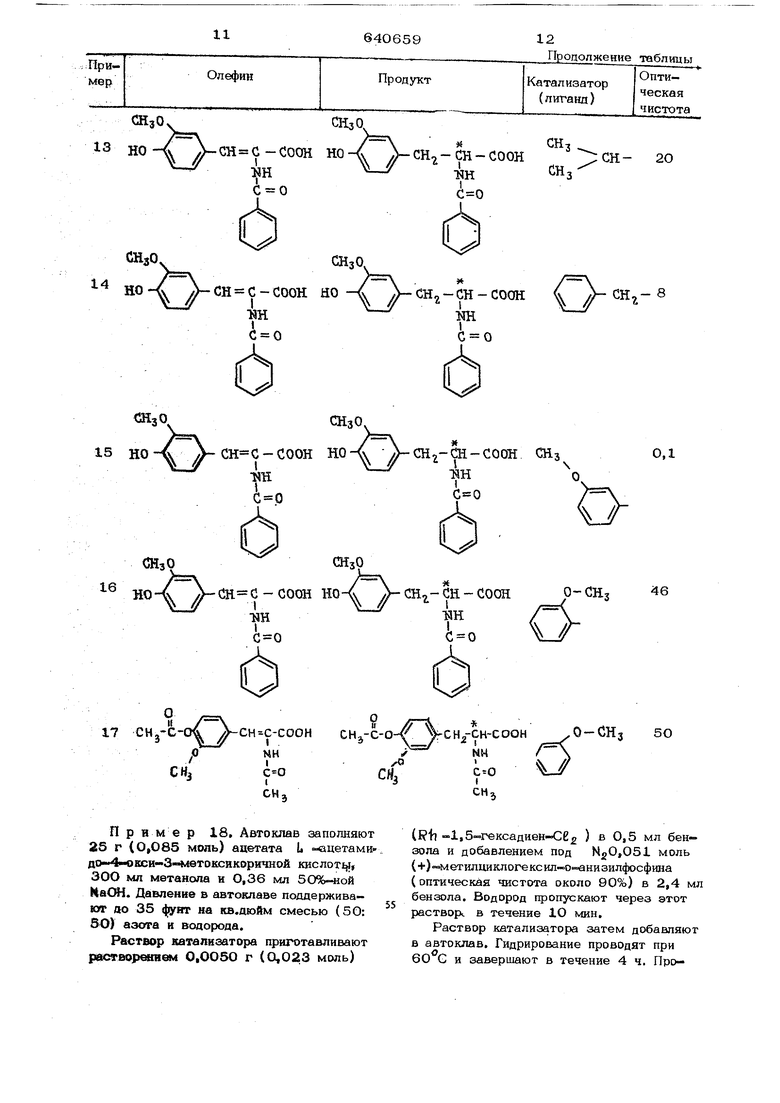


1,2
С - СООН
СНз - СН - СООН
ад
сош
С-СООН
СНз-СН-СООН
I н
СНз
R СНзСН Шг6
32
8
Uo
сн с-соон; У-сн -снсоон
с о
12
СНдСН СНо
с о
/Ьсн-с-соон ; -сНг-сн соон тт
I
сн.
р-СНз
45
NH
СНз
-соон н
cacjCH-iCHjсн -сн -соон
JCR
28
CHjCH сн 2
сн с-соон:
СНзО
сн с-соон
но I
NH
32
( у- сн;- - сн - соон 3 -Уолвстерил Д
СНзО
СНзО,
СН С-СООН ЙО НН i 0
у-СН -СН-СООН
Ж
с о СНзО, СН С-СООН НО-(СНзО
0,1 CH-COOH СЕз н ° ио-4 -сн с-соон но- иснг
П р и м е р 18, Автоклав заполняют 25 г ( моль) ацетата 1 -ацетамидО 4-«8СИ«3«4 еТОКСЯКОр Г ШОЙ КИСЛОТ1,}
ЗОО мл метанола н 0,36 мл 5О%-ной KaCHi. Давление в автоклаве поддерживают ао 35 фуят на кв.аюйм смесью (50: 50) азота и водорода.
Раствор катализатора приготавливают раствореиием 0,ОО5О г (0,023 моль) CHj-C-O
(Rfl -.1,5-гексадиен-Се2 ° зола и добавлением под ,051 моль (ф)метш1циклогексш1-0 внизилфосфина (оптическая чистота около 90%) в 2,4 мл бензола. ВодОрод пропускают через этот риствор в течение 1О клин.
Раствор катализатора затем добавляют в автоклав. Гидрирование проводят при и завершают в течение 4 ч. Про0-СНз бсн-сош да, - 0-СНз 50 CHjfCH-COOH дукт, полученный упариванием растворителя, представляет собой ацетат N «вце тил-3-(4-окси-3 -метоксифенил)- ланина, который имеет удельное вращение oLj- +38,(соль Na в воде). Чистый ацетат М ацетил 3-(4-окси -3- метоксифенил) Ь-аланина, также, как и натриевая соль в воде, имеет удельное вращение CLJ ,+54,О . Таким образом, оптическая чистота по лученного в результате гидрирования про дукта 7О,7%| т.е. лучше, чем 85% U -антипода и 15% 1Э -антипода. Используя сходную методику по отношению к (-)метилциклогексил о анизил- фосфину (оптическая чистота около 80%), в результате получают продукт гидрирования, содержащий преобладающее количество 13-антипода (оптическая чистота смеси реакционного продукта 65%). Таким образом, при соответствующем подборе одного из двух (+) или () подов фосфина могут получать вещество в большом количестве Пример 19. Применялась методи ка, сходная с методикой примера 18, с использованием ()-метилциклогекснл-о-аниаилфоофина в качестве оптически а к- тивного лиганда и сС -бензамид 4 °окси«-3-метоксикоричной кислоты в качестве |5 замещенной d -ациламидоакриловой кислоты. Полученный в результате гиорирования продукт N -бензоил-3-(4-окси-3-мето№сифенил)-аланин, содержит большое количество D -антипода (оптическая чистота смеси реакшюнного продукта около 65%). Формула изобретения 1. Способ получения d - или Е-изомеров об -аминокислот гидрированием производных амнноакрнловой кислоты или ее соли в присутствии катализатора с последующим выделением целевого продукта иэ вестным способом, отличающий- с я тем, что, с целью упрощения технологического процесса и получения соответ ствующего антипода, в качестве катализатора гидр1фова шя используют оптически активный коороинационный металлический комплекс обшей формулы ,или м%ц де М - родий, рутений, иридий или ос- ИЙ5 М - палладий или платина; X - водород, фтор, хлор, бром или йоп; L - фосфин, или арсии, причем по крайней мере одна из L -групп является оптически активной; И - целое число от 1 до 3. 2, Способ по п. 1, от л ичаю ши йс я тем, что процесс провопят в присут ствии основания. Приоритет по пунктам: 11.05.70по п. 1. 03.ОЗ.71.по п. 2.
Авторы
Даты
1978-12-30—Публикация
1971-05-10—Подача