Изобретение относится к способам, определения концентрации азотной кислоты в мн гокомпонентных водных растворах. Известен многопараметрический способ определения состава многокомпонентных водных растворов. Способ состоит в одновременном измере нии стольких независимых физических параметров раствора, сколько компонентов растворено в контролируемой жидкости. По величинам измеренных параметров вычисляют значения неизвестных концентраций ком понентов с помощью предварительно полученных систем управлений, графических номограмм или таблиц. Недостатками многопараметрического способа контроля является трудность вычисления результатов измерения, сложность аппаратурного оформления и необходимость иметь высокоточные измерители физических параметров. Наиболее существенным недостатком многопараметрического способа в случае применения его для измерения кон- ентрации азотной кислоты в многокомпонентных водных растворах является то, что для измерения концентрашг/, одного .-нента необходимо проведение большого чг.с- ла промежуточных измерительных ..), количество которых зависит от чюпа ргкт;:-.. ренных компонентов. Целые опясываекюго изобротенил яв:Ш ется уменьшение числа определявsji-ix -ы; ;vreTpOB при определении концентргцяи азотной кислоты в хгногокомпонентных водчых растворах, содерх ащих кроме азотной кислоты Т - 1 азотнокислых солей, где 71 2 Достигается это измерением двух физических параметров раствора, графические зависимости между которыми в поле номо граммы при изменении концентрации каждой из солей одинаковы и не совпадают о графической зависимостью между ними при изменении концентрации азотной ктелоты. В качестве одного из napaNieTpoB уделькую электропроводность раствора, как наиболее чувствительный к изменениям кониен центрации азотной кислоты параметр, а в качестве второго-параметр, мало зависящий от концентрации азотной кислоты , но в
значительной степени зависящий от концентрации солей , н.-шример, вязкость.
Предлагаемый способ опр депения концентроиия азотной кислоты в многокомпояеигных водных растворах, содержаи их
азотнокислые соли, использованием построенной J 0 v oгpflм fы сводится к следующим операцирм:
одновременно по двум приборам., измеряют удельную электропроводность и вяз кость конфопируемого раствора}
отсчитывают величину концентрации азотной кислоты по полученным значениям уденой электропроводности и вязкости с помощью номограммы,
Оказывается,такая номограмма позволяе определять еще оану важную концентрационную характеристику контролируемого раствора - содержание ионов N0,, тай: как подны заряд всех ионов в единице объема раствора пропорционален содержаггию ионов МО.
Ион Оо оказывает определяющее влияние в процессах экстракции, как высалива- тель. Контроль его содержания в технологических продуктах в настоящее время ведетсп расчетным путем по результатам лабораторного анализа всех солей и азотной кислоты.
Для проверки описанного готовят четы- рехкомпонентные растворы азотная кис- лота - нитрат алюминия - нитрат натриявода,
Концентрации компонентов выбирают в пределах: азотная кислота - 8 О 4-12 О г/л, нитраты алюминия и натрия - 15От 250 г/л Интервалы варьирования концентрации азотной кислоты 20 г/п, нитратов алюминия и натрия 5О г/п. При температуре + 2ООС измеряют удельную электропроводность и вязкость растворов. Удельную электропроводность измеряют лабораторным кондуктометром КЛБ -1 с контактной электролитической ячейкой вязкость - лабораторным Капиллярным вискозиметром СЬтвальда,
Злектролитическ Ю ячейку калибруют по Стандартному раствору хлористого калия, вискозиметр - по дистиллированной воде. Погрешность измерения удельной элетропроводности + 1,5 %, .вязкости +3%.
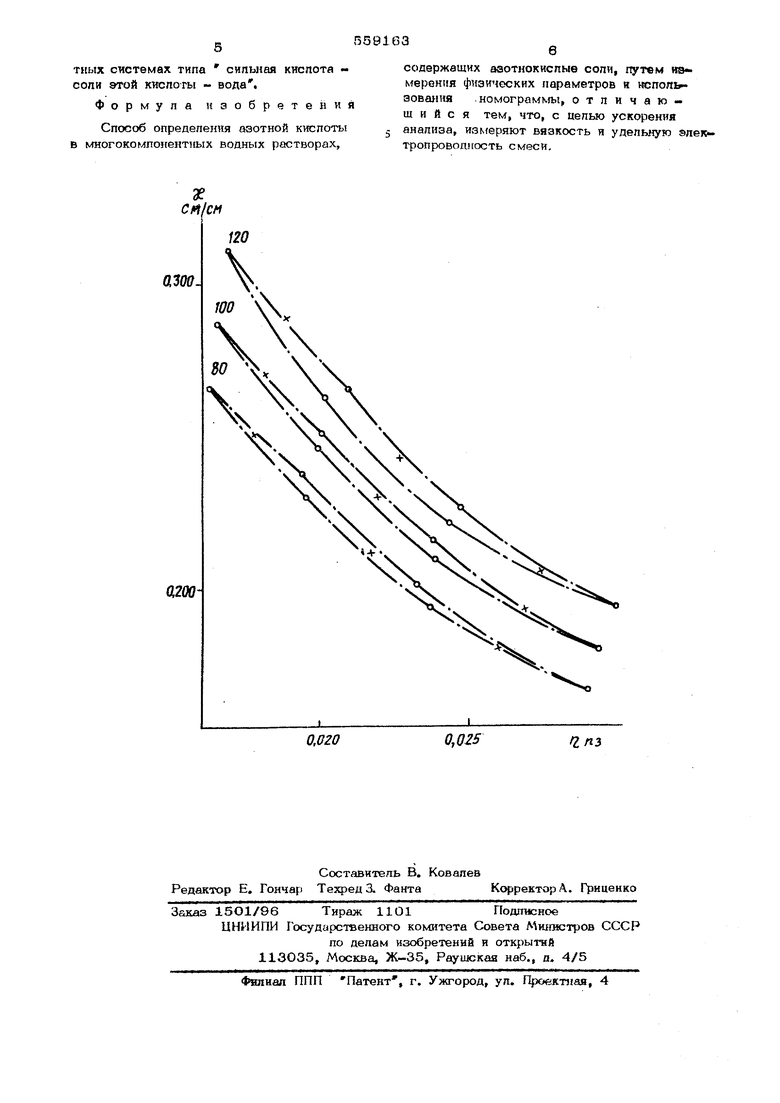
По данным измерений строят номограмму X - Т (удельная электропроводность-
вязкость), приведенную на чертеже . Штрихпунктирной линией ограничены области точек равной концентрат и азотной кислоты (80,1 ОС и 120 г/л) при изменении концентраций нитратов алюминия и натрия в пределах от 150 . до 250 г/л (по каждой соли), ЛУ:НИИ одинаковых точеклш ми изменения концентрации {штрата
апюК№ния, ()азличных точек - изменение концентраш и нитрата натрия.
Неопределенность линий равных концентраций азотной кислоты (см. чертеж), обусловленная произвольным изменением концентрации нитратов алюминия и натр1ш от 15О до 250 г/л, не превышает 5 г/л Это значит, что методическая погрешность определения концентрации азотной кислоты предлагаемым методом, на уровне 100 г/л при тех же условиях не превысит +5 г/п.
Методическая погрешность определения концентрации ионов МО не превысит + 2О г/л на уровне 4ОО г/л при произвольном изменении концентрации нитратов алюминия и натртш в пределах от 150 до 250 г/л. Таким образом, предположение о справедливости закона Вальдена для солей в концентрированных многокомпонентных растворах электролитов подтвердилось (в формуле закона Вальдена вместо эквивалентной электпропроводности нужно 1тредлагать относительное Изменение удельной электропроводнсстги, а вместо вязкости - оносительное изменение вязкости).
Имеется принципиальная возможность построения номограммы - Т| для избирательного определения концентрации азотной кислоты и ионов NO в водных растворах с произвольным числом и в произвольном концентрационном сочетании азотнокислых солей. Чем больше растворенных азотнокислых солей, тем более эффективным окажется применение предлагаемого способа определения концентрации азотной кислоты.
Предлагаемый способ проверен в лабораторных условиях на 6 имитационных растворах, приготовленных дополнительно. Концентрации азотнокислых солей алюминия и натрия варьировали в пределах от 150 до 25 О г/л, значения концентрации азотной кислоты выбирали 80, 10О и 120 г/л. Методика приготовления растворов и измерения удельной электропроводности и вязкости аналопгчны изложенным..
По измеренным значениям удельной эпетропроводности и вязкости определяют точки на номограмме удельная электропроводность - вязкость , описывающие составы контролируемых растворов. По линиям равных, концентраций азотной кислоты и нитрата - иона, проходящих через найденные точки номограммы, определяли концентрации компонентов. При этом максимальная погрешность определения концентрации азотной кислоты не превышала +10 г
а нитрат - иона + 30 г/л.
Предлагаем1 1й способ может быть исползован в других подобных многокомпонен- тных системах типа сильная кислота соли этой киспогы - вода . Формула нэобрете 1и Способ определенутя азотной кислоты в многокомпонентных водных растворах.
зе
CfftlCM 3 содержащих ааотнокиспыв сопи, путем ив иерения физических параметров и нсполызования .HOMorpaMNfbi, отличающийся тем, что, с цепью ускорения анализа, HasfspHroT вязкость и удельную электропроводность смеси.
am.
0,200

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРЕСС-ПОРОШКОВ НА ОСНОВЕ ДИОКСИДА ЦИРКОНИЯ ДЛЯ ИЗГОТОВЛЕНИЯ КЕРАМИКИ | 2023 |
|
RU2825401C1 |
| СПОСОБ ПЕРЕРАБОТКИ ЛЕГИРОВАННОГО МЕТАЛЛИЧЕСКОГО ПЛУТОНИЯ | 2000 |
|
RU2200133C2 |
| Способ электрохимического получения порошков оксида алюминия | 2017 |
|
RU2664135C1 |
| Способ приготовления оксидных катализаторов | 2021 |
|
RU2781406C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ГИДРООБЛАГОРАЖИВАНИЯ НЕФТЯНЫХ ФРАКЦИЙ | 2002 |
|
RU2216404C1 |
| Способ получения удобрения для гидропоники | 1982 |
|
SU1060603A1 |
| СПОСОБ КОМПЛЕКСНОЙ ПЕРЕРАБОТКИ НИКЕЛЬ-КОБАЛЬТОВОГО СЫРЬЯ | 2009 |
|
RU2393251C1 |
| СПОСОБ ЭЛЕКТРОХИМИЧЕСКОГО ОСАЖДЕНИЯ АКТИНИДОВ | 2012 |
|
RU2493295C1 |
| СПОСОБ ОБРАБОТКИ КОНТУРОВ ВОДООХЛАЖДАЕМЫХ РЕАКТОРОВ | 1999 |
|
RU2169957C2 |
| СПОСОБ ВЫДЕЛЕНИЯ ТЕХНЕЦИЯ ИЗ АЗОТНОКИСЛОГО РАСТВОРА | 1998 |
|
RU2194802C2 |


0,020
0,025
Чпз
Авторы
Даты
1977-05-25—Публикация
1974-03-18—Подача