1
Изобретение относится к способам изготовления биологических препа(ратов для вакцинации сельскохозяйственных животных и. может быть использовано в биологической промышленности для получения авирулентной, безвредной и высокоиммуногенной противояндурной вакцины.
Известны способы изготовления противоящурдой гидроокисьалюминЕевой формо-лвакцины из афтозного, культурального и лаиинизированного вируса 1. Известная технология изготовления противоящурной вакцины из лапииизированного вируса включает следующие операции: приготовление вируссодержащей суспензии, сорбцию вируса на гидроокись алюминия с последующей инактивацией формалином и теплом. В качестве дополнительного адъюванта применяется санопин. Противоящурная вакцина из ланинизированного вируса, изготовленная указанным способом, отличается слабой иммуногенностью и в большинстве случаев создает у привитых животных недостаточно нанряженный иммунитет. Многочисленные попытки усовершенствовать вакцину не увенчались успехом.
Известен также способ изготовления противояшурной ГОА-формолвакцины из ланинизнрованного вируса, используемый биологической промышленностью СССР и являющийся наиболее близким по технической сущности к предлагаемому способу 2. Вируссодержащую суспензию готовят из тушек 2-3 дневных крольчат на 1/15М фосфатном буфере в отношении 1 : 10. После размола и экс5 трагировання в суспензию добавляют 5% хлороформа, который тщательно эмульгируют в суспензии с помощью коллоидных мельниц. Хлороформ и денатурированные белки удаляют .сепарированпем или центрифугированием. Затем вирус ящура двукратно концентрируют сорбцией на гидроокиси алюминия. Суспензию гидроокиси алюминия готовят «а дистиллированной воде. Процесс концентрации вируса ящура на гидроокиси алюминия контролируют проверкой сорбции вируса и комплементсвязывающего антигена. Концентрация считается полной при сорбции вируса не менее 99% и комплементсвязывающего антигена не менее 90%. После этого постепенно добавляют 5%-ный раствор формалина при постоянном перемешивании. Инактивацию вируса ведут прц 25-26°С в течение 48 ч. После окончания инактивации в реактор добавляют под давлением глицерин, 10%-ный раствор
хинозола и 10%-ный раствор сапонина. Все .компоненты перемешивают в течение 30 мин, рП вакцины устанавливают в пределах 7,6- 7,8 путем добавления (1 или 5%-ного) раствора химически чистой соляной кислоты. Вакцину охлаждают до 4-б°С. Основным педостатком противоящурной вакцины из лапинизировЗНиого вируса и в особенности типа О, изготовленной на 1/I5M фосфатном буфере, является то, что оиа обладает весьма низ1кой иммуыогенной активностью, не создает продолжительности иммунитета у сельскохозяйственных животных и при многократном применении вызывает большие трудности.
С целью повышения иммупогенной активности противояшуриой ГОА-формолвакцины из лапииизцрованного вируса, предлагают в известном сиособе изготовления противояи1уриой ГОА-формолвакцииы из лапинизированного вируса, включаюшем операции культивирования вируса, приготовление вируосодержаш,ей суспензии, ее экстрагироваиия и эмульгирования, очистки вируса, добавлеиия гидроокиси алюминия для сорбции вируса и его инактивации, вируссодержащую суспензию готовить ца солевом изотоническом растворе, наиример, Хеикса, Эрла, Тироде или Дульбекко с добавлением 0,5% гидролизата лактальбумина или казеииа. При этом гидроокись алюминия добавляют к вирусу после очистки, предварительио приготовленную па солевом изотоническом растворе Хеикса.
Противоящурная ГОА-формол1вакцииа, получеииая предлагаемым способом, превышает в 2-4 раза по активности вакципу, приготовленную известиым снособом. Высокая иммуногенность вакцины, иолученной предлагаемым способом, по мнению авторов изобретения обусловлена тем, что в процессе инактивации сохраняются антигенные и иммуиогепиые свойства вируса за счет стабилизации его солями кальция, магния и аминокислот гидролизатов, находящихся в солевых изотопических растворах. Кроме того, вакциаа, иолучецная предлагаемым способом, не обладает
Иммуногенная активность ГОА-формолвакцины, изготовленной на различных растворах
реактогенностыо и легко рассасывается на месте введения.
Для изготовления ГОА-формолвакцины использовали лапинизированный вирус яш,ура типа О, штамм 194,3-10 пассажей, адаптированный к крольчатам двух-трехдневного возраста. Было изготовлено и испытано 15 экспериментальных образцов вакцины из лапинизировалного вируса типа О, из которых 12 на солевых изотонических растворах Хенкса, Эрла, Тироде, Дульбекко с 0,5%-ным гидролизатом лактальбумина фирмы «Дифко (по 3 образца), и 3 серии в качестве контроля на фосфатно-буферном растворе. Ави арулентность всей серий вакцины контролировали на мышатах-сосунах, иммупогенность - путем определения 50% иммунизирующих доз (ИмДао) вакцины для взрослых белых мышей. При этом мышам вакцину вводили в области снины в цельном виде и в разведени-ях 1:2, 1 : 4, и 1:8, доза 0,8 мл. Каждой дозой вакцины прививали по 20 мышей, а в качестве контроля оставляли такое же количество певакцинироваиных животных. Через 21 день после вакцинации привитых и. контрольных мышей заражали подкожно в дозе 10000 ЛДбо/мл индикаторным П1таммом вируса, адаптированным к этому виду животных. Учет результатов проводили в течение 10 дней по количеству выживших мышей к общему числу привитых животиых, 50%-ную иммунизирующую дозу вакцины рассчитывали но методу Кербера-Ашмарина.
В результате ироведенных опытов установлено, что все серии вакцины были авирулентными и безвредными. Данные контроля иммуногенности вакцины на взрослых белых мышах представлены в табл. 1.
Таблица 1


| название | год | авторы | номер документа |
|---|---|---|---|
| ВАКЦИНА ПРОТИВ ЯЩУРА ТИПА О И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 2001 |
|
RU2212895C2 |
| ВАКЦИНА ПРОТИВ ЯЩУРА ТИПА А И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 1999 |
|
RU2143921C1 |
| ВАКЦИНА ПРОТИВ ЯЩУРА ТИПА АЗИЯ-1 И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 2002 |
|
RU2220744C1 |
| Вакцина инактивированная сорбированная против ящура типа А | 2017 |
|
RU2681815C1 |
| ВАКЦИНА ИНАКТИВИРОВАННАЯ СОРБИРОВАННАЯ ПРОТИВ ЯЩУРА ТИПА А | 2014 |
|
RU2562547C1 |
| ВАКЦИНА ИНАКТИВИРОВАННАЯ СОРБИРОВАННАЯ ПРОТИВ ЯЩУРА ТИПА А | 2014 |
|
RU2563345C1 |
| ВАКЦИНА ИНАКТИВИРОВАННАЯ СОРБИРОВАННАЯ ПРОТИВ ЯЩУРА ТИПА А | 2004 |
|
RU2294760C2 |
| ШТАММ О №2102/Забайкальский/2010 ВИРУСА ЯЩУРА Aphtae epizooticae ТИПА О ДЛЯ КОНТРОЛЯ АНТИГЕННОЙ И ИММУНОГЕННОЙ АКТИВНОСТИ ПРОТИВОЯЩУРНЫХ ВАКЦИН И ДЛЯ ИЗГОТОВЛЕНИЯ БИОПРЕПАРАТОВ ДЛЯ ДИАГНОСТИКИ И СПЕЦИФИЧЕСКОЙ ПРОФИЛАКТИКИ ЯЩУРА ТИПА О | 2014 |
|
RU2563522C1 |
| Вакцина инактивированная эмульсионная против ящура типа О | 2017 |
|
RU2682876C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ПРОТИВОВИРУСНЫХ ВАКЦИН | 1980 |
|
SU991634A1 |

Из таблицы 1 следует, что ГАО-формолвакцина из лапинизированного вируса О-194, изготовленная на фосфатном буфере (контрольная), отличается низкой иммуногенностью, средняя ИмДбо трех серий составляет 0,48+0,07 мл. Активность ГОА-формолвакцины из лапинизированного вируса О-194, изготовленной на растворах Хенкса, Эрла, Ти.роде, Дульбекко с 0,5%-ным гидролизатором лактальбумина повышается от 3 до 4 раз, по сравнению с контрольной. Различие статически достоверное (,01). В то же время не отмечено существенных различий в активности вакцин, изготовленных на любом из изотонических солевых растворов с гидролизатом лактальбумина.
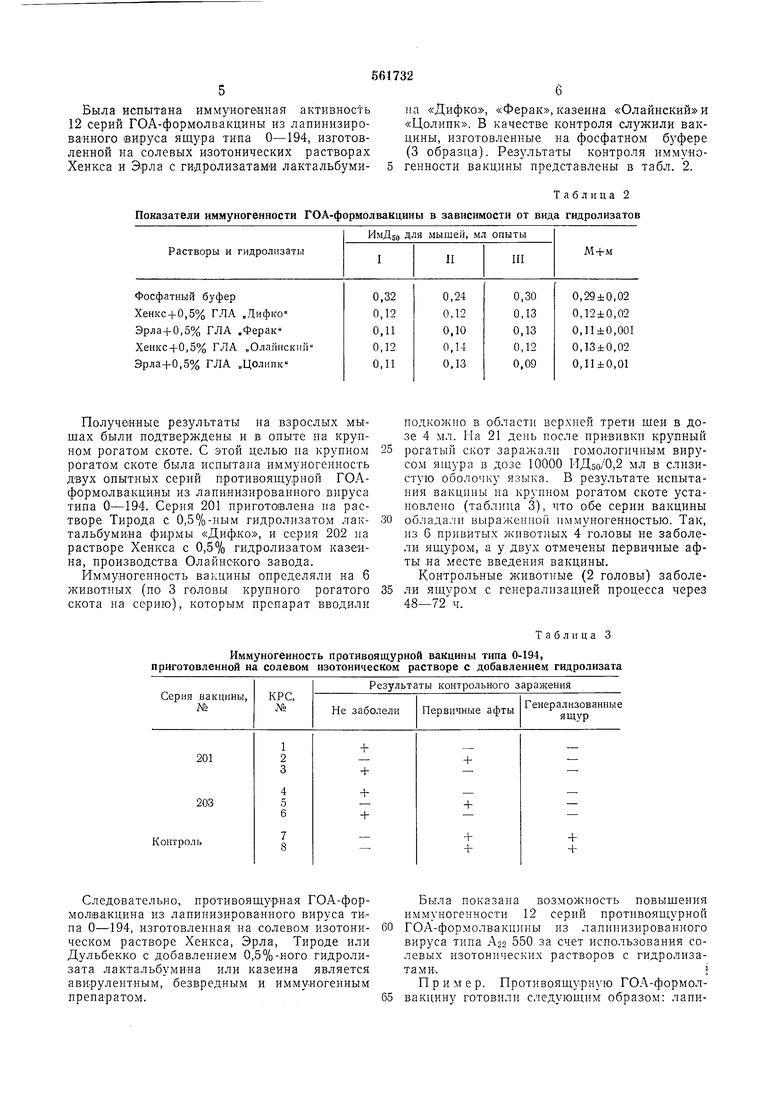
Была испытана иммуногенная активносФь 12 серий ГОА-формолвакцины из лапинизироваиного вируса ящура типа 0-194, изготовленной на солевых изотонических растворах Хенкса и Эрла с гидролизатамй лактальбумиПоказатели иммуногенности ГОА-формолваКцины
Получанные результаты на взрослых мышах были подтверждены и в опыте на крупном рогатом скоте. С этой целью на крупном рогатом скоте была испытана иммуногенность двух онытных серий противоящурной ГОАформолвакцины из лапинизированного вируса типа О-194. Серия 201 приготовлена па растворе Тирода с 0,5%-ным гидролизатом лактальбумина фирмы «Диф:ко, и серия 202 на растворе Хенкса с 0,5% гидролизатом казеина, производства Олайнского завода.
Иммуногенность вакцины оиределяли на б животных (по 3 головы крупного рогатого скота на серию), которым препарат вводили
Иммуногенность противоящурной вакцины типа 0-194, приготовленной на солевом изотоническом растворе с добавлением гидролизата
Следовательно, противоящурная ГОЛ-формолвакцина из лапинизированного вируса типа О-194, изготовленная на солевом изотоннческом растворе Хенкса, Эрла, Тироде или Дульбекко с добавлением 0,5%-ного гидролизата лактальбумина или казеина является авирулентным, безвредным и иммуногенным препаратом.
на «Дифко, «Ферак, казеина «Олайнский и «Цолиик. В качестве контроля служили вакцины, изготовленные на фосфатном бзфере (3 образца). Результаты контроля иммуногенности вакцины представлены в табл. 2.
подкожно в области верхней трети шеи в дозе 4 мл. На 21 день после прививки крупный рогатый скот заражали гомологичным вирусом ящура в дозе 10000 ИД5о/0,2 мл в слизистую оболочку языка. В результате испытания вакцнны на крупном рогатом скоте установлено (таблица 3), что обе серии вакцины обладали выраженной иммуногенностью. Так, из 6 привитых животных 4 головы не заболели ящуром, а у двух отмечены первичные афты на месте введения вакцины.
Контрольные животные (2 головы) заболели ящуром с генерализацией процесса через 48-72 ч.
Таблица 3
Была показана возмолсность повышения иммуногенности 12 серий противоящурной ГОЛ-формолвакцины из лапинизированного вируса тина А22 550 за счет использования солевых изотонических растворов с гидролизата ми.i
Пример. Противоящурную ГОА-формолвакцнну готовили следующим образом: ланиТаблица 2 в зависимости от вида гидролизатов
низйрованный вирус производственного штамма измельчали на мясорубке с последующи} размолом на размельчителе тканей РТ-1 или РТ-2, а при изготовлении производственных серий на коллоидных мельницах типа IV-8 и IV-10 с добавление м солевых изотонических растворов Хенкса, Эрла, Тироде или Дульбекко с 0,5%-щым гидролизатом лактальбумина или казеи.на (рН 7,4-7,8) в соотношении 1 : 10. Затем в суспензию вносили антибиотики (пенициллин и стрептомицин по 200 кд/мл). После экстрагирования ;в течение 1-2 ч в суспензию добавляли 5-10% хлороформа и смесь эмульгировали на размельчителе тканей или коллоидной мельнице с последующим центрифугированием (сепарированием). В очищенную суспензию добавляли мертиолат 1 :20000.
Затем к зара«ее пригатовле«ной 3%-ной гидроокиси алюминия на солевом растворе Хенкса добавляли вируссодержащую суспензию и проводили сорбцию вируса (с периодическим встряхиванием - перемешиванием компон-енто1в) в течение 20-30 мин (1-2 ч), рН смеси (ГОА-суспензия) соста1вляла 7,4- 7,8; температура 4-6°С. По окончании сорбции вируса на гидроокись алюминия температуру смеси доводили до 25-26°С и с помощью гликоколового буфера устанавливали. рН, равный 8,6-8,8.
По достижении указанной температуры и рН смеси при постоянном помешивании к общему объему добавляли 0,05% пятидесятипроцентного раствора формалина (с поправкой на количество формальдегида) и проводили инактивацию вируса в течение 48 ч. После инактивации рН препарата с помошью 5N раствора соляной кислоты (х. ч.) устанавливали в пределах 7,6-7,8 и охлаждали до температуры 4-6°С. При указанной температуре производили отстой инактивированного препарата жидкости в количестве 50% от общего объема. К оставшемуся объему концентрированного препарата добавляли 10% глицерина, 0,5% десятипроцентного раствора сапонина и хинозола. Все компоненты перемешивали в течение 20-30 мин и готовую вакцину хранили при температуре 4-6°С и рН 7,4-7,8.
Пропись вакдйнЫ на 1110 Л следующая, л: 10%-ная вируссодержащая суспензия14003%-ная гидроокись алюминия 600 После удаления надосадочяой жидкости в количестве 1000 л, к оставщемуся объему 1000 л концентрированного препар ата добавляли, л:
Глицерин100
10%-вый сапонин5
10%-ный хинозол5
Вакцина представляет собой однородную жидкость серовато-зеленого цвета, при хранении которой на дне флакона образуется рыхлый осадок, при встряхивании легко разбивается и вновь превращается в однородную, равномерную взвесь.
Формула изобретения
ее экстрагирование и эмульгирование,, очистку вируса, добавление гидроокиси алюминия для сорбции вируса и инактивацию его, отличающийся тем, что, с целью повышения иммуногенности и уменьшения ее реактогенности, вируссодержашую суспензию готовят на солевом изотоническом растворе, например Хенкса, Эрла, Тироде или Дульбекко с добавлением 0,5%-«ого гидролизата лактальбумина или .казеина.
Источники информации, принятые во внимание при экспертизе

Авторы
Даты
1977-06-15—Публикация
1975-07-04—Подача