Изобретение относится к применению лекарственных средств для стимуляции умственной деятельности и диагностики старческого слабоумия. Было обнаружено, что гипофизарные гормоны гипоталамуса, т.е. фактор высвобождения гормона роста и соматостатин, оказывают влияние на умственную деятельность. А именно, каждый из обоих гормонов оказывает существенное влияние на двигательную активность и повышает способность обучаться. Если пациент страдает невропсихиатрическими заболеваниями, эти гормоны могут вызвать, по крайней мере, частичный возврат к нормальному состоянию. Если же пациент не страдает невропсихиатрическими заболеваниями, например для здоровых индивидуумов, эти гормоны могут вызвать повышение умственных способностей. Например, наблюдались заметные изменения в результатах психометрических тестов, таких как короткая память и внимание, а также на ЕЕG (электроэнцефалограммное картрирование). Кроме того, так как эти гормоны влияют на улучшение состояния пациентов, страдающих старческим слабоумием типа Алцгеймера, их можно использовать для диагностики этого заболевания, особенно на ранних стадиях.
В частности было обнаружено, что реакция гормона роста, вызванная фактором высвобождения гормона роста, может быть использована как полезный симптом для распознавания ранних стадий старческого слабоумия по Алцгеймеру.
Целью изобретения является повышение эффективности стимуляции умственной деятельности и повышение точности идентификации форм заболевания старческим слабоумием, поддающихся лечению.
Эта цель достигается тем, что в способе стимуляции умственной деятельности путем введения лекарственных средств вводят соматостатин или фактор выделения гормона роста, или их физиологически активные фрагменты, или их смесь в дозе 1-50 мкг/кг. При этом внутривенно препарат вводят в дозе 1,0-10,0 мкг/кг, а подкожно - в дозе 5,0-50,0 мкг/кг.
В способе диагностики старческого слабоумия путем проведения обследования согласно изобретению цель достигается тем, что осуществляют психофизиологические тесты, регистрируют результаты их выполнения до и после введения соматостатина, или фактора выделения гормона роста, или его физиологически активного фрагмента, или их смеси в дозе 1,0-50,0 мкг/кг и при выявлении динамики полученных показателей диагностируют старческое слабоумие, поддающееся лечению.
В предлагаемом способе можно использовать различные коммерчески доступные формы соматостина или фактора выделения гормона роста. Биологически активные фрагменты можно заместить для всех или для части используемых соматостина или фактора выделения гормона роста. Соматостин обычно характеризуют как фактор, ингибирующий высвобождение гормона роста. Предпочтительно, чтобы в нем был использован фрагмент 1-14, т.е. SS-14. В способе можно использовать различные коммерческие продукты, содержащие полезные формы SS. Можно также использовать смеси.
Фактор, высвобождающий гормон роста, обычно описывают как стимуляторный фактор гипоталамуса, высвобождающий гормон роста, который участвует в нейрорегуляции секреции гормона роста. Предпочтительными для использования являются сегменты или фрагменты, обозначаемые как 1-44 и 1-29. В способе можно использовать различные коммерческие продукты, содержащие их полезные формы. Возможно использование смесей.
Фармацевтические препараты, используемые в соответствии с предлагаемым способом, должны содержать один или более из этих гормонов вместе с обычными фармацевтически приемлемыми носителями.
Длительность приема композиций, содержащих гормоны, может сильно варьироваться. В зависимости от желательного действия предпочтителен ежедневный прием. Можно также принимать препарат каждые 6-12 ч. Время приема определяется лечащим врачом.
П р и м е р 1. Для выяснения факта, дают ли SS и GRF на центральном уровне тот же самый антагонистический эффект, который они давали на питуитарном уровне, изучалось действие этих нейропептидов на некоторые параметры поведения с использованием OU CEM-86тм (Osaka University Computerized Electronic Mаze). Система состоит из следующих компонентов: программируемая электронная платформа (консоль) (РЕР) (620-620 мм), снабженная 48 фоточувствительными сенсорами (ОРХ-Т30), программируемая панель (РР) (модель ВЕСМ-0062) для стимуляции; шоковый генератор (SGS) модель BSG-1065 (для подачи непрерывного или переменного электрического тока на PEP; Контрольная станция (CS), (ВЕС-16-Dio Computer Control Station BCS-1105; Bio Medica, LTD, Osaka), которая обрабатывает вход/выход на интерфейсе в автоматически компьютеризованные параметры поведения; компьютерная система (NEC PC-9801 VM2) с объемом памяти Мбайт (RAM) для обработки данных и проведения экспериментов.
Крысам-самцам штамма Вистар (175-200 г) количество животных 5-8 крыс в группе) вводили интрацеребровентрикулярно инъекции GRF1-44 и SS-14 в дозах 0,1-10 мкг. Затем крыс изучали в OUCEM в двух различных тестах (например, в открытой зоне и в лабиринте).
Животных помещали на РЕР на 30 мин и автоматически записывали двигательную активность (LA) как полное количество перемещений (1/0), включая движения в положении на четырех лапах (4F) и в положении на двух лапах (2F), активность хождения, подпрыгивания и приподнимания на задние лапы, тогда как горизонтальные линейные перемещения (4F) представлены как импульсы в минуту (р/м) или см2/мин.
Интрацеребровентрикулярное введение SS (1 мкг) вызывает количественное и качественное изменение при значительном повышении LA (31,16±6,90 р/мин от 20,88 ± 2,82 р/мин, т = 3,08; р < 0,02), тогда как GRF (1 мкг) вызывает гиперкинетический синдром, характеризующийся обязательными движениями при LA 47,60 + 5,35 рм ( т = 4,21, р < 0,005) (контроль 1122 ± 248 см2/мин; GRF = 1713,6 ± 69,5 см2/мин, т = =18,73, р < 0,005). Эти изменения зависят от дозы /SS: ED50 1,83 нмоль; Емакс = 6,10 нмоль; GRF1-44:ED50 = 99,1 пмоль; Емакс = =1,98 нмоль, GRF1-29:ED50= 297 пмоль, Емакс = 5,95 нмоль.
П р и м е р 2. В этом примере продемонстрировано действие интрацеребровентрикулярного введения SS и GRF на двигательную активность и обучение в лабиринте. Используя лабиринт, где крысы должны были обучаться выходу из шоковой зоны для того, чтобы избежать электрошока 1,5 мА, SS (1 мкг, интрацеребровентрикулярно) существенно снижает LA (17,12 ± ±5,42 от 6,01 + 1,45 р/м, т = 4,42, р < 0,004, а GRF повышает LA в зависимости от дозы (26,66±3,15 р/м, т = 3,40, р < 0,01 при 1 мкг и 90,2 ± 8,4 р/м, т = 17,51, р < 0,05 при 5 мкг. Количество вводов (1/0), вызванное SS составило 103,5 + 29,5 (контроль = 216,25 ± ±55,19, т = 8,49, р < 0,005) в нейтральной зоне (NA) и 77,14 ± 13,5 1/0 в шоковой зоне (SA) (контроль 298 ± 40, т = 1,26 н. с.), GRF вызывает 459,35 ±32,5 (1/0) в NA (т = 18,13, р < 0,005) и 340,5 %+ 63,5 (1/0) (т = 9,07, р < <0,005). Отношение NA/SA (N/S) для контроля, SS- и GRF-обработанных крыс составил 0,72, 1,33 и 1,35 соответственно.
Результаты показывают, что GRF и SS оказывают антагонистическое действие на LA в новых условиях, как для теста в открытой зоне, так и в лабиринте. Если считать показатель N/S как показатель обучения, то оказывается, что как SS, так и GRF повышают умственные способности в дозах приблизительно 6,10 х 10-10 моль и 1,98 х 10-10 моль соответственно.
Однако, так как GRF вызывал гиперкинетический синдром, в котором 1/0 отношение, также как время нахождения в SA было значительно выше, чем в контрольной группе, следует считать, что SS более эффективно, чем GRF, улучшает обучение. Двигательная активность, вызванная GRF (гиперкинетический синдром), составляет серьезный недостаток для животных при дифференциации и разделении поведения в лабиринте.
П р и м е р 3. Двадцать пациентов (женщин) с первичным дегенеративным слабоумием (типа Алцхеймера) в возрасте 67 - 84 лет разделили на две терапевтические группы с GRF (1-29) NH2. Всем пациенткам вводили этот препарат в течение 8 дн по одной из следующих схем: I) 250 мкг подкожно дважды в день; II) 50 мкг внутривенно дважды в день.
Терапевтическое лечение начинали спустя 15 дней после прекращения приема психотропных препаратов.
Изменения в пациентах оценивали, используя тест ММS Фольштейна и тест шкалы Кричтона (Chrichton) в течение 12 ч, 24 ч и 7 дн после начала GRF. Статическую оценку проводили, используя тест Фридмана с уровнем риска р < 0,01 (существенные разницы).
Обе группы демонстрируют повышение как в опытных, так и в клинических тестах, причем выше в группе с внутривенным GRF-введением, чем в группе с подкожным введением. Эффект начинается спустя 12 ч после введения и остается заметным более, чем 7 дн после введения препарата.
Более низкие оценки по шкале Кричтона наблюдались для I группы, что вероятно связано с тем фактом, что так как введение в каждой из групп зависело от трудности внутривенной инъекции, в ту группу, которой препарат вводили подкожно, вошли более сложные клинические случаи.
Во время введения GRF сестры, работавшие с пациентами, сообщали об улучшении в состоянии пациенток в плане сфинктерного контроля и общей психомоторной деятельности. Улучшение исчезало и возобновлялась ситуация до лечения, если введение GRF прекращали.
После окончания введения GRF проводили оценку для тех же групп в тесте ММS-Фольштейна и тесте о шкале Кричтона как для оценки воспроизводимости тестов, так и для установления факта исключения действия GRF, подтверждая тем самым заметное действие GRF (1-29) NH2 на этих пациентов. Коэффициенты вариации составили 12% для теста ММS-Фольштейна и 2,7% для тестовой шкалы Кричтона.
П р и м е р 4. 5 здоровых добровольцев обоего пола в возрасте 18-25 лет были подвергнуты следующему слепому опыту.
Пациентов подвергли следующим процедурам:
1. Базовая линия: регистрация EEG (электроэнцефалограммы), психометрическое тестирование (короткая память), оценка Р-300 потенциала по аудиометрическому тестированию.
2. То же, после введения плацебо (физиологический раствор).
3. То же, после введения GRF.
Между каждыми фазами 1-3 проходила по крайней мере одна неделя. Каждый пациент прошел все 3 фазы.
Дозировка: GRF 125 мкг внутривенно (прибл. 1,5-2,5 мкг/кг); физиологический раствор: тот же объем, что использовался для разбавления GRF.
Тест на запоминание (короткая память).
Тест на запоминание сводится к запоминанию списка нейтральных слов. Испытатель читает эти слова, а затем разделительная фаза включает выполнение некоторых арифметических задач. Затем испытуемого просят повторить все слова из списка, которые он/она сможет вспомнить.
В каждом случае слова были другие во избежание заучивания.
Тест на внимание.
Целью этого теста является изучение наведенного потенциала Р-300, который как известно связан с объемом внимания, необходимым для слежения за явлением и его запоминанием.
Для этого теста выбрали в качестве стимула слуховой стимул, так как известно, что аудиометрическое тестирование этого потенциала надежно и легкоосуществимо. После стимулирования (в данном случае звука) механизмы, участвующие в этом процессе слушания, сами по себе проявляют некоторую биоэлектрическую активность, непосредственно связанную с самим стимулом. Процесс восприятия более сложен, чем просто "слушание", и даже после того, как звук прекращается, биоэлектрическая активность, связанная с ним, может наблюдаться, например в виде "эхо". Это "эхо" и является наведенным потенциалом. Р-300 представляет собой положительную волну, которую можно наблюдать спустя 300 мс после первого пика, связанного со стимулом, и известно, что оно связано с процессом сознания, а именно со связанным с ним вниманием.
Субъект слышит несколько сигналов с частотой либо 1000, либо 2000 Гц, в произвольном порядке. Затем его спрашивают, сколько он слышал сигналов высокой частоты (2000 Гц).
Запись ЕЕG.
Запись энцефалограммы начинают спустя 10 мин после инъекции и проводят до конца тестирования (20-30 мин).
Немедленно после завершения первой группы тестов, т.е. спустя 30-40 мин после инъекции, процедуру повторяют с новыми словами и звуковыми сигналами, одновременно записывая ЕЕG.
Длительность испытания.
Каждая серия длится около часа, считая с момента инъекции.
ЕЕG картрирование.
Его проводят на PATHFINDER устройстве.
Первое скринирование карт для каждой частотной полосы (альфа, бета 1, бета 2, дельта и тета) проводят так же, как для Р-300.
Изменения определяют как любые отклонения по амплитуде (потенциалу) или по топографическому распределению полос и сравнивают от индивидуума к индивидууму, причем сравнивают картины, полученные после инъекции препарата от базовой линии, записанной для инъекции плацебо.
Наблюдаемые улучшения характеристик для психометрических тестов коррелируют с импрессивными модификациями на ЕЕG, как по амплитуде, так и по топографическому распределению.
Результаты анализов сфокусированы на наиболее заметных изменениях в поведении и/или ЕЕG. После предварительного Фурье-преобразования, карты перестраивают для тех частотных полос, которые демонстрируют наиболее очевидные изменения, т.е. альфа, бета-2 и Р-300.
Результаты психометрических тестов (память).
Число слов, которые запомнили 5 субъектов, подвергнутых испытаниям, было следующим (среднее ± сд): Базовое значение 8,4±1,34 Плацебо 12,4±3,13 GRF (10 мин после инъекции) 14,0±3,0
GRF (30-40 мин после инъекции) 16,2±2,38
Субъект от субъекта по результатам распределялись следующим образом: 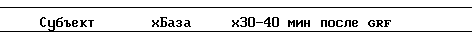
1 9 15
2 7 16
3 10 19
4 7 18
5 9 13
Таким образом, GRF повышает способность к запоминанию. Важность этого наблюдения существенно возрастает за счет наблюдавшейся корреляции с картами ЕЕG, что показано далее.
Анализ биоэлектрической активности.
Альфа волны. Наблюдается чистое возрастание энергии.
Далее для нормальных субъектов во время отдыха пик альфа активности расположен главным образом в правой затылочной доле вблизи средней линии мозга. Спустя 30-40 мин после GRF наблюдается отчетливое распространение альфа активности по всему мозгу, что предполагает общую стимуляцию мозговой активности, что возможно связано с неспецифической стимуляцией активирующей ретикуляpной системы.
Бета-2 волны. В нормальных условиях основная активность бета-2 волн сосредоточена главным образом в левой теменно-затылочной области (parieto-occipital).
Карта, спустя 30-40 мин после введения GRF, демонстрирует следующие изменения: общее распространение активности бета-2 на весь мозг; возрастание интенсивности исходного левого parieto-occipital фокуса (интенсивность более чем в два раза превосходит исходное значение) и расширение этого фокуса; появление нового фокуса, расположенного в правом краю лобной доли.
Левая parieto-occipital доля, как известно, связана с памятью, так что повышение электрической активности в этой области коррелирует с результатами теста на поведение.
С другой стороны, возникновение нового фокуса активности бета-2 во фронтальной доле (площадь интегрирования) интерпретируется как доказательство того факта, что субъект создает некоторые логические ассоциации для того, чтобы связать нейтральные слова друг с другом в предложения.
Р-300 активность. Наблюдается чистое повышение энергии Р-300 спустя 30-40 мин после введения GRF. Р-300 является потенциалом наведения, который как известно связан с вниманием. Это интерпретируется как способность субъекта "обращать более интенсивное внимание на стимул" после введения GRF, чем в условиях записи базовой линии.
Изобретение относится к медицине, а именно к неврологии. Способ позволяет повысить терапевтическую эффективность лечения старческого слабоумия и идентифицировать его формы. Для этого вводят соматостатин, или фактор выделения гормона роста, или их физиологически активные фрагменты, или их смесь в дозе 1 - 50 мкг/кг. Для диагностики предъявляют психофизиологические тесты до и после введения указанной дозировки препарата и при выявлении динамики полученных показателей, диагностируют старческое слабоумие, поддающееся лечению. 2 с. и 2 з.п. ф-лы.
Приоритет по пунктам:
26.01.88 - по пп.1 - 3;
13.06.88 - по п.4.
| Штернберг Э.Я | |||
| Геронтологическая психиатрия | |||
| Шеститрубный элемент пароперегревателя в жаровых трубках | 1918 |
|
SU1977A1 |
Авторы
Даты
1994-12-15—Публикация
1989-01-25—Подача