ОБЛАСТЬ ТЕХНИКИ
Данное изобретение относится к области терапевтических применений эритропоэтина и, более конкретно, к лечению субъектов рекомбинантным эритропоэтином, полученным с использованием ApaI фрагмента ДНК генома человека, в том числе рекомбинантным эритропоэтином, экспрессируемым в трансформированных клетках почки детеныша хомячка, который производит меньшие побочные действия, чем другие рекомбинантные эритропоэтины человека, в том числе получаемые из клеток яичника Китайского хомячка.
Эритропоэтин (ЕРО) является важным фармацевтическим средством для применения в различных способах терапии, где желательной является стимуляции пролиферации эритроцитов (RBC). Исторически развитие применения рекомбинантного ЕРО (rHu EPO) рассматривалось как развитие его применения исключительно в качестве фактора против анемии, известного как фактор роста для стимуляции дифференцированных стволовых клеток в костном мозге для стимуляции продуцирования ретикулоцитов (т.е. пролиферации молодых пост-стволовых клеток). Обычно, для целей лечения анемии использовали ЕРО, и сначала надеялись, что он будет применим для любого состояния анемии, где существует недостаточность эндогенного гормона, где происходит потеря крови или где пациент имеет симптомы анемии или имеет пониженную чувствительность костного мозга к эндогенному гормону. Примеры состояний, изначально считающихся потенциально излечимыми эритропоэтином, включают в себя анемию при злокачественном заболевании (т.е. любом типе рака твердого органа или гематологического рака, в том числе лейкозе, лимфоме и множественной миеломе); анемию, происходящую вследствие лечения химиотерапией/облучением злокачественного заболевания; анемию хронического заболевания, в том числе, например, аутоиммунных заболеваний, таких как ревматоидный артрит и гепатит, анемию у пациентов со СПИДом, в частности, получающих азидотимидин (AZT) в качестве лечения; анемию недоношенных новорожденных; анемию, связанную с почечной недостаточностью; анемию при талассемии; аутоиммунную гемолитическую анемию; апластическую анемию и анемию, связанную с хирургией (например, для улучшения предоперационного взятия крови для аутотрансфузии с целью стимуляции увеличения уровней гемоглобина (гемоглобина) для противодействия существенной потере крови или для увеличения эритропоэза у субъектов, подвергающихся пересадке (трансплантации) костного мозга).
Эритропоэтины, используемые для таких способов терапии, являются гликозилированными белками, получаемыми экспрессией из рекомбинантных последовательностей геномной ДНК эритропоэтина человека или кДНК-последовательностей в линиях клеток млекопитающих. Как описано более подробно далее, имеются по меньшей мере три формы рекомбинантного эритропоэтина человека, используемые в данной области, Эпоэтин Альфа, Эпоэтин Бета и Эпоэтин Омега.
Недавно было установлено, что препараты рекомбинантного эритропоэтина существенно различаются в зависимости от точной последовательности ДНК, используемой для экспрессии, или от используемой линии клеток хозяина и/или от структурных и биологических свойств продуцируемого ими эритропоэтина. Различные структурные и биологические свойства включают в себя такие признаки, как различающиеся картины гликозилирования, различные изоформы (анализируемые изоэлектрическим фокусированием (IEF) и ОФ-ВЭЖХ-анализом), различные молекулярные размеры/массы, различие антигенных свойств, различие фармакокинетических свойств, различие скоростей ответов на дозу, различные биологические эффекты, различия в связывании рецепторов и т.п.
Один из типов эритропоэтина, обычно используемый в терапии, продуцируется экспрессией в клетках яичника Китайского хомячка (СНО) с использованием большого фрагмента геномного клона гена эритропоэтина человека, как описано, например, в патентах США с номерами 4703008 и 5955422, выданных Lin, включенных здесь в качестве ссылки. Этот тип эритропоэтина включает в себя эпоэтины, названные Эпоэтин Альфа (геномная ДНК) или Бета (кДНК). Эпоэтин Альфа является коммерчески доступным под товарными названиями EPREX, PROCRIT или EPOGEN. EPOGEN выходит в виде единственного пика при ОФ-ВЭЖХ и имеет немного изоформ согласно IEF-анализу изоформ. При использовании различных способов сообщалось, что Эпоэтины Альфа и Бета имеют среднюю молекулярную массу, оцениваемую в диапазоне 30,4-41 кД. Эта приближенная оценка варьируется в зависимости от сообщения или способа, используемого для анализа (см. USPDI, под EPOGEN; J. Chromatog. B 687:189, 1996; J. Am. Soc. Nephrol. 10:2392, 1989). Сравнение с расположением рядом, показанное здесь, с использованием анализа электрофорезом на ДСН-полиакриламидном геле со стандартами молекулярных масс приближенно определяет, что Эпоэтин Альфа и Эпоэтин Бета имеют среднюю молекулярную массу приблизительно 41 кД, тогда как Эпоэтин Омега имеет молекулярную массу приблизительно 39 кД. Эпоэтин Бета доступен под товарным названием RECORMON и является почти идентичным Эпоэтину Альфа, но содержит дополнительные минорные изоформы, кроме больших изоформ, сходных с Эпоэтином Альфа.
Одним из наиболее существенных биологических побочных действий препаратов Эпоэтина Альфа или Бета является рутинное увеличение кровяного давления, которое приводит быстро к гипертензии при первоначальном введении дозы и может продолжаться в виде непрерывного осложнения/побочного явления во время пролонгированных периодов поддерживающего лечения. Другие побочные явления включают в себя припадок, головные боли, тромбоз, задержку эффективности, подобные гриппу симптомы, и многие пациенты жалуются и сообщают о неожиданных и нежелательных уровнях увеличенной боли в месте инъекции, в том числе при введении i.v. или s.c., и увеличенной боли в теле, связанной с лечением Эпоэтином Альфа. BMJ 303:288, 1991; Am. J. Nephrol. 12:68, 1992; Pharm. Week B1 13:55, 1992; Nephrol. Dial. Transplant 13:817, 1998; Clin. Nephrol. 49:41, 1998. Кроме того, увеличение образования тромбоцитов является обычным событием при применении Эпоэтинов Альфа и Бета, которое требует разжижающих кровь агентов в качестве рутинного аспекта терапии и которое может в значительной степени способствовать повышенному риску свертывания или тромбоза, особенно у пациента с нарушенными кровеносными сосудами. Кроме того, как показано более подробно далее, некоторые субъекты испытывают другие побочные эффекты, такие как хроническая боль или хроническая усталость. Кроме того, другие субъекты не отвечают на лечение Эпоэтином Альфа или Бета, так что реакция на лечение отсутствует (неотвечающие субъекты) или ограничивается по характеру некоторыми патологическими состояниями или состояниями, вызываемыми химиотерапевтическими агентами, облучением или другими нарушениями, которые подавляют пролиферацию клеток. Многие нежелательные побочные последствия применения rHu EPO в виде Альфа и Бета являются зависимыми от дозы, причем более высокие дозы, как сообщается, способствуют возникновению более частых или более тяжелых побочных реакций, и гипертензия или увеличения кровяного давления являются одними из них.
К сожалению, некоторые из нежелательных побочных эффектов Эпоэтинов Альфа или Бета означают, что субъектам, проявляющим такие состояния, как предсуществующая гипертензия, или субъектам с нарушенными кровеносными сосудами лечение Эпоэтинами Альфа и Бета является противопоказанным и должно подвергаться тщательному мониторингу. Гипертензия может быть связана с другими состояниями, такими как патологическое сердечное состояние, рак, дисфункция печени или аутоиммунные заболевания, такие как ревматоидный артрит, что увеличивает риск лечения пациентов, имеющих эти состояния, Эпоэтином Альфа или Бета. Даже в случаях, когда известно, что пациент имеет манифестирующиеся состояния, такие как сосудистые рестрикции или сосудистое заболевание, такие как сужение артерий, профессионалы-медики должны пытаться избегать увеличения кровяного давления или других неблагоприятных событий, даже у полностью "здорового" или почти "здорового" пациента. Далее, пациент может быть "здоровым" в том смысле, что он не страдает от гипертензии (например, иметь кровяное давление не выше 90), но может "вступить" в гипертензию после введения рекомбинантного эритропоэтина человека (rHu EPO). Например, увеличение на 20 пунктов кровяного давления могло бы перевести "здорового" пациента в "гипертензивное" состояние. Пациенты, требующие более высоких доз rHu EPO, находятся перед более высоким риском неблагоприятного события, и некоторые пациенты при гемодиализе или некоторые пациенты, имеющие связанную с онкологией анемию, должны принимать гораздо большие дозы, требующиеся для получения желаемого увеличения пролиферации RBC, показателей гемотокрита или гемоглобина. Кроме того, потенциал в отношении нежелательных побочных эффектов обычно мешает применению этих эпоэтинов для более слабых или симптоматических целей, таких как ослабление усталости, ослабление васкулярной боли, разумное увеличение физических упражнений, например, у солдат, или улучшение познавательной функции у пациентов, в остальном здоровых, таких как пожилые люди, для которых эритропоэтин в ином случае является благоприятным, но риск неблагоприятных побочных действий может перевесить пользу. Эти проблемы с другими эпоэтинами способствуют, по меньшей мере отчасти, частоте и высоким дозам Эпоэтинов Альфа и Бета, обычно требующимся для достижения терапевтической или физиологической пользы. Обычно, частота введения дозы в случае Эпоэтина Альфа или Бета составляет три раза или большее число раз в неделю, причем типичная доза равна 200 или более МЕ/кг в неделю (см. для Эпоэтина Альфа, Drugs 38:863, 1989; Drugs 49:232, 1985; Drugs 51:289, 1996; J. Bone Joint Surg. 78:-A:62, 1996; Lancet 344:367, 1994; Transfusion 36:822, 1996; Nephrol. Dial. Transplant 2:85, 1999; Neth. J. Med. 54:10, 1999; для сравнения с Эпоэтином Бета см. Clin. Pharmacol. Ther. 50:702, 1991).
Таким образом, существует потребность в способах лечения, использующих эритропоэтин, который не имеет случаев одного или нескольких неблагоприятных побочных действий или снижает случаи одного или нескольких неблагоприятных действий эритропоэтина, продуцируемого клетками СНО, и который был бы полезен в способах лечения пациентов, имеющих состояния, которые могли бы препятствовать лечению эпоэтинами Альфа или Бета. Кроме того, существует потребность в лечении субъектов, которые являются нечувствительными к лечению эпоэтинами Альфа или Бета или на которых неблагоприятно влияет лечение эпоэтинами Альфа или Бета. Далее, существует потребность в эритропоэтине, который является активным в достижении ответной реакции у пациентов, которые являются супрессированными при патологических состояниях такой обработкой, как химиотерапия и облучение, или которые не отвечают или имеют неадекватную реакцию на другие эпоэтины.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Данное изобретение удовлетворяет эту потребность обеспечением лечения пациентов Эпоэтином Омега, описанным в патенте США №5688697 и заявках на патент США с регистрационными номерами 08/238 255 и 08/466 412, включенных здесь в качестве ссылки. Он доступен коммерчески под товарными названиями Elanex Erythropoietin, EPOMEGA, EPOMAX, HEMAX, REPOTIN или Hi Potency EPO cytokine related factor (HP-EPO-CRF) (высокоэффективный ЕРО-цитокин-родственный фактор), доступными из Elanex Pharmaceutical, Bothell Washington. Этот улучшенный и легко доступный Эпоэтин Омега получают из клеток почек детенышей хомячка (например, клеток ВНК-21) экспрессией из рестрикционного ApaI фрагмента гена эритропоэтина человека. Здесь показано, что Эпоэтин Омега имеет значительно большую эффективность, более высокую концентрацию в сыворотке на протяжении времени клиренса (в 2,5 раза более высокую в сравнении с Эпоэтином Альфа), более высокую биодоступность, требует более низких доз как в начальном лечении (приблизительно 75 - приблизительно 120 МЕ/кг в неделю), так и в поддержании (приблизительно 20 - приблизительно 75 МЕ/кг в неделю) и является эффективным в субъектах, нечувствительных к лечению другими эпоэтинами. Кроме того, описано, что Эпоэтин Омега оказывает действия на пациентов, которые не связаны с гипоксией или анемией или увеличением числа эритроцитов или гемоглобина. Другими словами, Эпоэтин Омега оказывает прямое действие на другие механизмы в организме по еще не вполне понятным причинам, но в путях, которые были идентифицированы из клинических наблюдений, таких как уменьшение или устранение боли в теле, снижение тошноты, увеличение бодрости или "энергичности", повышение в смысле хорошего самочувствия и/или улучшенного "настроения", усиление функции печени при нарушениях, включающих в себя печеночную недостаточность или повреждение печени, и многие другие регистрируемые благоприятные эффекты.
Здесь обеспечено изобретение, заключающееся в том, что Эпоэтин Омега удивительным образом отличается от эпоэтинов Альфа и Бета по типу и тяжести неблагоприятных побочных эффектов, вызываемых Эпоэтином Альфа или Бета, что делает его применимым, в частности, для лечения определенных патологических состояний, таких как онкология/рак, особенно вместе с химиотерапией или облучением. Одним из наиболее важных неблагоприятных побочных эффектов, отсутствующим у Эпоэтина Омега, но присутствующим в случае других эпоэтинов, является увеличенное кровяное давление и сопутствующий риск гипертензии. Это делает Эпоэтин Омега особенно полезным в лечении пациентов с имеющейся гипертензией (или с риском возникновения гипертензивного или пограничного гипертензивного состояния), заболеванием сердца, сосудистой недостаточностью или пациентов с увеличенным риском тромботических осложнений. Кроме того, здесь описано, что Эпоэтин Омега является более эффективным, чем другие эпоэтины, т.е. требует меньшей дозы для обеспечения терапевтической пользы. Описано также, что Эпоэтин Омега действует без латентного периода, т.е. немедленно производит терапевтическую пользу без временного лага, в противоположность другим эпоэтинам, которые обычно требуют, по меньшей мере, две недели для получения измеримой реакции при обычной анемии, такой как анемия пациентов с гемодиализом, и можно ожидать применения в течение четырех или более недель до какого-либо клинически значимого ответа, если он появляется. Кроме того, показано, что он является более биодоступным, чем другие эпоэтины, т.е. остается в плазме на более высоком уровне концентрации по сравнению с той же самой дозой других эпоэтинов, и остается эффективным в субъекте в течение продолжительного периода. Далее, описано отсутствие образования антител против ЕРО у пациентов, лечившихся Эпоэтином Омега. Эти новые свойства, отдельно или в сочетании, делают возможным применения Эпоэтина Омега в пониженных дозах и с уменьшенной частотой и делают возможным его применение для лечения субъектов, на которых неблагоприятно действует применение эпоэтинов Альфа или БЕТА, и/или субъектов, нечувствительных к этим другим эпоэтинам.
В одном аспекте обеспечены способы лечения или предупреждения анемического состояния у субъекта, предусматривающие введение терапевтического количества Эпоэтина Омега, где количество выбрано для обеспечения терапевтической пользы на протяжении периода лечения без возникновения или обострения неблагоприятного побочного эффекта, выбранного из группы, состоящей из увеличенного кровяного давления или гипертензии. В одном варианте кровяное давление включает в себя диастолическое или систолическое измерения, которые не увеличиваются более чем на 10 мм рт.ст., во время периода лечения. В другом варианте диастолическое или систолическое измерение не увеличивается более чем на 1 мм рт.ст. на единицу увеличения гемоглобина (г/дл). Еще в одном варианте риск развития гипертензии в популяции субъектов, лечившихся Эпоэтином Омега, составляет менее 15% по сравнению с субъектами, получавшими плацебо.
Анемическое состояние может быть анемией любого типа, в том числе, но не только, почечной анемией, анемией злокачественного состояния, анемией, связанной с химиотерапией, анемией, связанной с хроническим заболеванием, анемией в случае СПИДа, анемией при преждевременных родах, анемией талассемии, анемией аутоиммунного гемолитического заболевания или апластической анемией. Кроме того, этот способ применим для лечения или предупреждения анемического состояния, связанного с операционной процедурой. В одном варианте способ предусматривает введение Эпоэтина Омега перед взятием крови, используемой для обратного переливания (реинфузии) крови (известного также как переливание аутологичной крови). В другом варианте способ предусматривает введение Эпоэтина Омега в предоперационной стадии, тогда как в еще одном варианте Эпоэтин Омега вводят в послеоперационной стадии. Еще в одном варианте эта операционная процедура является пересадкой (трансплантацией) костного мозга.
В другом аспекте обеспечен способ лечения или предупреждения анемического состояния у субъекта, который не отвечает на лечение терапевтическим количеством Эпоэтина Альфа или Бета, или это лечение действует на пациента неблагоприятным образом. Этот способ также предусматривает введение терапевтического количества Эпоэтина Омега, причем количество Эпоэтина Омега выбрано таким образом, что оно обеспечивает терапевтическую пользу во время периода лечения. Обычно, дозы 50-150 МЕ/кг могут вводиться с частотой один-три раза в неделю.
В любом аспекте время, необходимое для периода лечения, варьируется в зависимости от типа и тяжести анемии, или оно будет варьироваться в соответствии с желаемой терапевтической пользой, которая включает в себя, но не ограничивается ими, увеличение числа эритроцитов (RBC), увеличение гематокритного числа (HCT), увеличение гемоглобина. Типичное лечение включает в себя значительно более низкие дозы Эпоэтина Омега и/или менее частое введение доз для достижения терапевтического ответа, чем получаемые с использованием Эпоэтина Альфа или Бета, или которые не могут быть получены вообще при любом сообщенном введении доз других эпоэтинов, например, при химиотерапии/лучевой терапии пациентов с раком/онкологией. Оно также включает в себя признак быстрой и измеримой реакции без латентного периода, так что проводящие лечение профессионалы-медики могут ожидать ответа из лабораторных анализов крови в пределах недели или более быстро, по сравнению с 2-5 неделями с другими эпоэтинами. Это, в свою очередь, позволяет немедленное изменение дозирования для получения результата у пациента, и позволяет быстро определить отвечаемость пациента на Эпоэтин Омега, когда может быть показано крутое или быстрое обращение ответной реакции. Быстрая реакция применима, в частности, для пациентов во время химиотерапии или лучевой терапии, которые нуждаются в немедленной реакции для продолжения спасающего жизнь способа лечения и не могут быть освобождены от этого лечения, что дает, таким образом, преимущество, заключающееся в отсутствии необходимости обременительного переливания крови. Это делает возможным пролонгированное лечение химиотерапевтическими агентами и/или облучением для разрушения или ингибирования рака, когда в противном случае прекращение обработки может позволить раку расти или становиться более устойчивым к химиотерапевтическому лечению в результате прерывания лечения или снижения дозы или частоты этой обработки. Кроме того, это делает возможным относительное немедленное улучшение качества жизни пациента, который имеет анемию, и позволяет организму человека иметь позицию здоровой крови для борьбы с заболеванием, таким как рак, что позволяет организму лучшим образом использовать его природную систему преодоления как лечения, так и рака.
В родственном аспекте описано улучшение в здоровье проходящего лечение пациента вообще, в том числе пациентов, проходящих химиотерапию, которым вводят Эпоэтин Омега, причем это улучшение в отношении к жизни имеет тенденцию ослаблять ощущаемую пациентом тяжесть и отрицательную сторону химио/лучевой терапии. Это обеспечивает улучшенную установку рассудка пациента на то, чтобы выдержать химио/лучевую терапию, и готовность повторно пройти химио/лучевую терапию снова при любом рецидиве рака. Фактически немедленное ощущение улучшения самочувствия или улучшения в отношении к жизни позволили по меньшей мере одному пациенту вести нормальный образ жизни, даже при прохождении химиотерапии, независимо от изменения в реакции гемоглобина или RBC. В другом родственном аспекте лечение Эпоэтином Омега обеспечивает также уменьшение или устранение тошноты в случае пациентов, проходящих курс химиотерапии/облучения, даже до такой степени, что пациент отказывался от обычных медикаментов против тошноты, обычно прописываемых для проходящего химиотерапию пациента.
В других аспектах обеспечены способы лечения или предупреждения анемии, связанной с несколькими состояниями, в том числе состояниями сердечной или сосудистой недостаточности пациента, дисфункцией печени, гепатитом, аутоиммунным заболеванием или злокачественным заболеванием (т.е. раком). Эти способы предусматривают лечение субъектов без увеличения риска или увеличения вредных побочных действий, в том числе, но не только, увеличенного кровяного давления или гипертензии. Эти способы предусматривают также лечение субъекта, который является нечувствительным или испытывает неблагоприятное действие при лечении Эпоэтином Альфа или Бета. В контексте лечения состояний, связанных с раком, эти способы применимы для лечения анемических состояний, вызываемых во всех способах или в части способов раковой терапии. Эти варианты включают в себя анемические состояния, вызываемые или усиливаемые химиотерапией или лучевой терапией. Эти способы включают в себя введение Эпоэтина Омега до, во время или после завершения раковой терапии. В другом аспекте обеспечен способ лечения субъекта более низкими дозами Эпоэтина Омега, такими как 12000 МЕ в неделю или менее, и/или дозой, вводимой только один раз в неделю, сравнимой с 100000 МЕ - 200000 МЕ в неделю Эпоэтина Альфа, которую обычно вводят два или более раз в неделю. Существует также обычно более высокий риск неблагоприятных реакций, встречающихся при введении более высоких доз эпоэтинов, так как многие неблагоприятные реакции могут быть связанными с дозой в виде абсолютной дозы в МЕ Эпоэтина, вводимого в типичной схеме введения лекарственного средства.
В другом аспекте обеспечена композиция или обеспечен набор для лечения субъекта, который включает в себя терапевтическое количество Эпоэтина Омега, приготовленного для лечения субъекта без индуцирования или обострения вредного побочного эффекта, такого как гипертензия или увеличение кровяного давления. Этот аспект включают в себя композиции или наборы для лечения субъекта, нечувствительного к лечению Эпоэтином Альфа или Бета, или имеющего неблагоприятные побочные эффекты при использовании Эпоэтина Альфа или Бета. Композиция или набор могут необязательно включать в себя инструкции для введения терапевтического количества Эпоэтина Омега для достижения терапевтической пользы. Эти инструкции могут включать в себя коррекции терапевтического количества Эпоэтина Омега посредством сравнительной ссылки на количество Эпоэтина Альфа или Бета, используемое в других способах лечения.
Далее, описан неожиданный результат, заключающийся в том, что Эпоэтин Омега вызывает прямое и, по-видимому, немедленное и непрерывное уменьшение боли в теле, связанной с различными состояниями, в том числе состояниями онкологии, фибромиалгии, синдрома хронической усталости, RA (ревматоидного артрита), гепатита, и в том числе ухудшенными/патологическими состояниями, а также в случае ракового пациента, подвергнутого химиотерапии. Еще более неожиданно, уменьшение телесной боли происходит независимо от значимой реакции стимуляции эритропоэза, такой как увеличение числа эритроцитов (RBC), гематокритного числа или уровней гемоглобина. Уменьшение боли возникает в пределах минут после введения дозы и может продолжаться в течение нескольких дней.
Описано также улучшение в качестве жизни, бодрости и ощущении благополучия в пределах менее чем неделя, или в пределах одной-двух недель введения Эпоэтина Омега пациенту с печеночной недостаточностью, страдающему запущенным гепатитом, приближающимся к терминальному состоянию. Эти измеряемые улучшения происходили независимо от увеличения гемоглобина или числа RBC; и, кроме того, было улучшение в различных параметрах функции печени, измеренных типичными лабораторными тестами, в том числе по активности трансаминазы глутаминовой кислоты - щавелево-уксусной кислоты в сыворотке (sgot), и другими. Улучшение в ощущении благополучия позволило прикованному к постели пациенту, страдающему от терминального гепатита, вернуться к обычному стилю жизни на период почти двух лет.
Эти и другие аспекты преимуществ способов лечения с использованием Эпоэтина Омега, обеспеченных здесь, будут очевидными специалисту с квалификацией в данной области в свете следующего подробного описания.
Фигура 1 изображает окрашенный Кумасси гель изоэлектрического фокусирования, который иллюстрирует различные изоформы, содержащиеся в препаратах проб эпоэтинов Альфа, Бета и Омега, которые происходят, отчасти, из различных углеводных заместителей.
Фигура 2 изображает окрашенный серебром гель изоэлектрического фокусирования, который иллюстрирует различные изоформы, содержащиеся в препаратах проб Эпоэтина Альфа в сравнении с Эпоэтином Бета, и то, как они отличаются от Эпоэтина Омега.
Фигура 3 изображает ДСН-полиакриламидный гель, который иллюстрирует различные молекулярные массы в препаратах проб Эпоэтина Альфа, Бета и Омега.
Фигура 4 иллюстрирует результаты клинических испытаний, показывающие появление нескольких неблагоприятных побочных эффектов у пациентов, получавших Эпоэтин Омега, в сравнении с пациентами, получавшими Эпоэтин Альфа.
Фигура 5 иллюстрирует сравнение Эпоэтина Омега с Эпоэтином Альфа по увеличению среднего систолического ВР (кровяного давления) над линией фона после s.c. введения (30 на группу).
Фигура 6 иллюстрирует действия Эпоэтина Омега на кровяное давление. Фигура 6А показывает сравнение действия Эпоэтина Омега с действием Эпоэтина Альфа на среднее систолическое ВР (А) и диастолическое ВР (В) относительно действия на увеличение гемоглобина. Фигура 6С показывает слабое, но линейное уменьшение как диастолического, так и систолического давления на протяжении периода лечения. Фигура 6D показывает увеличение гемоглобина на протяжении периода лечения, уменьшение дозы Эпоэтина Омега на протяжении периода лечения и уменьшение артериального кровяного давления во время того же самого периода.
Фигура 7 показывает отсутствие значимого увеличения в тромбоцитах у субъектов, получавших Эпоэтин Омега.
Фигура 8 иллюстрирует различия в требованиях поддерживающей дозы для лечения анемии Эпоэтином Омега по сравнению с пациентами, получавшими Эпоэтин Альфа.
Фигура 9 иллюстрирует зависимость средняя концентрация эритропоэтина в плазме-время для 18 субъектов, получавших единую дозу s.c. 50 МЕ/кг Эпоэтина Омега по сравнению с Эпоэтином Альфа. Фигура 9А показывает сравнительные концентрации в сыворотке rHu EPO, сравнение Эпоэтина Омега (верхняя линия) с Эпоэтином Альфа (нижняя линия), иллюстрирующее, что на протяжении времени концентрации в сыворотке у пациентов in vivo в 2,5 раз больше по площади для Эпоэтина Омега, чем для Эпоэтина Альфа. Фигура 9В показывает сравнительные концентрации в сыворотке rHu EPO Альфа и Бета, иллюстрирующие, что уровни в сыворотке Альфа и Бета являются почти идентичными.
Фигура 10 иллюстрирует абсолютные еженедельные дозы и средние концентрации эритропоэтина в плазме у пациентов, получавших Эпоэтин Омега (А) или Эпоэтин Альфа (В).
Фигура 11 иллюстрирует сравнение боли, испытываемой пациентами, получавшими s.c. инъекцию Эпоэтина Омега или Эпоэтина Альфа. Боль выражена в виде средних еженедельных баллов визуальной шкалы аналогов для боли в месте инъекции. (30 на группу).
Фигура 12 иллюстрирует быструю ответную реакцию в получении увеличения уровней гемоглобина, показанную в виде среднего из 379 пациентов, которым вводили Эпоэтин Омега i.v. инъекцией, или среднего из 450 пациентов, которым вводили Эпоэтин Омега s.c. инъекцией. Столбики ошибок обозначают SEM (среднюю квадратичную ошибку).
Фигура 13 иллюстрирует средние еженедельные дозы титрования и поддержания для пациентов, получавших Эпоэтин Омега i.v. инъекцией (А) или s.c. инъекцией (В).
Фигура 14 показывает результаты клинического испытания, иллюстрирующие, что средние величины гемоглобина непрерывно увеличиваются на протяжении 11 недель лечения Эпоэтином Омега.
Фигура 15 иллюстрирует быстрый ответ в получении увеличения уровней гемоглобина с использованием единой еженедельной дозы Эпоэтина (А) и процент субъектов, достигающих целевого уровня гемоглобина на протяжении времени (В). Фигура 15С иллюстрирует быстрое и линейное увеличение гемоглобина в течение первых 7 недель периода лечения из 24 недель в популяции пациентов, получавших среднюю дозу приблизительно 3×25-3×33 МЕ/кг в неделю, и показывает постепенное снижение общей средней еженедельной дозы, требуемой на протяжении периода лечения.
Фигура 16 иллюстрирует сравнение уровней ответа гемоглобина у пациентов, получавших Эпоэтин Омега или Эпоэтин Альфа s.c. инъекцией (30 на группу), показывающее средние величины гемоглобина (А) и среднюю абсолютную еженедельную дозу, требуемую для поддержания (В).
Фигура 17 иллюстрирует сравнение уровней ответа гемоглобина у получавших Эпоэтин Омега или Эпоэтин Альфа пациентов в зависимости от фона гемоглобина (А) и отношение среднее увеличение гемоглобина/средняя еженедельная доза (В).
Фигура 18 иллюстрирует результаты тройного перекресного испытания, показывающие, что субъект, нечувствительный к Эпоэтину Альфа, является высокочувствительным к Эпоэтину Омега. 18А показывает начальную положительную реакцию на Эпоэтин Омега, вводимый дважды в неделю, в первой фазе; 18В показывает отсутствие реакции на Эпоэтин Альфа, вводимый дважды в неделю, во второй фазе; 18С показывает реакцию на Эпоэтин Омега, вводимый один раз в неделю, в третьей фазе. Верхние панели показывают общие недельные дозы, средние панели показывают уровень гемоглобина и нижние панели показывают действия на кровяное давление.
Фигура 19 показывает применение Эпоэтина Омега в предоперационной процедуре для предупреждения анемии при взятии крови для последующего переливания. А и В показывают уровни гемоглобина для индивидуумов в группе, получавшей лечение, и в группе контроля, соответственно. С и D показывают средние линейные скорости снижения гемоглобина до конечной выписки и до момента хирургии, соответственно.
Фигуры 20А и В иллюстрируют среднее число RBC и ретикулоцитов, соответственно, для получавших Эпоэтин Омега и контрольных пациентов, из которых берут кровь для последующего переливания в предоперационной процедуре. С показывает средний общий уровень железа в сыворотке (TSI) для получавших Эпоэтин Омега и контрольных пациентов до конечной выписки.
Фигура 21 иллюстрирует применение Эпоэтина Омега для лечения анемии, связанной с химиотерапией. 21А показывает варьирование уровней гемоглобина на протяжении периода химиотерапии. 21В показывает схему введения Эпоэтина Омега и лечения химиотерапией, которая приводит к уровням гемоглобина, показанным в 21А.
Фигура 22 иллюстрирует сравнение диапазонов доз, требуемых для лечения анемии, связанной с получающими химиотерапию пациентами, участвующими в предварительном восьминедельном исследовании лечения Эпоэтином Омега по сравнению с подобным лечением Эпоэтином Альфа.
Фигура 23 иллюстрирует сравнение увеличения гемоглобина у получающих Эпоэтин Омега проходящих химиотерапию пациентов, участвующих в предварительном восьминедельном исследовании лечения Эпоэтином Омега по сравнению с подобным лечением Эпоэтином Альфа.
Фигура 24 иллюстрирует эффективность Эпоэтина Омега в лечении анемии преждевременных родов (т.е. анемии у недоношенных новорожденных) при исследовании 23 новорожденных. 24А показывает, что группа получавших Эпоэтин Омега новорожденных требовала меньшего числа переливаний крови, чем необработанная контрольная группа. 24В-D показывает, соответственно, увеличение числа RBC (В), гематокритного числа (С) и уровня гемоглобина (D) в получавшей Эпоэтин группе по сравнению с контрольной группой.
Фигура 25 иллюстрирует сравнительную эффективность доз, требуемых для лечения пациентов с гемодиализом на протяжении периода 12 недель Эпоэтином Омега по сравнению с Эпоэтином Альфа.
Фигура 26 иллюстрирует распределение требований поддерживающей дозы в популяции пациентов с гемодиализом, получавших Эпоэтин Альфа.
ПОДРОБНОЕ ОПИСАНИЕ
Перед подробным изложением данного изобретения для его лучшего понимания приводятся следующие определения.
"Симптом, связанный" с заболеванием или состоянием, является симптомом, который появляется одновременно с данным заболеванием или состоянием или как результат лечения заболевания или состояния. Связь заболевания или состояния со связанным с ним симптомом может быть или не быть причинной связью. Более конкретно, симптом может быть независимым от заболевания или состояния или может быть зависимым от заболевания или состояния, так как он непосредственно обусловлен заболеванием или состоянием, непосредственно обусловлен действием этого заболевания или состояния или обусловлен первичным лечением заболевания или состояния.
"Неблагоприятно воздействующая" или "неблагоприятный побочный эффект" является нежелательными биологической реакцией, физиологическим состоянием, биологическим измерением или риском их увеличения, которые могут происходить после введения фармацевтического агента, в частности, rHu EPO, субъекту.
"Противопоказанное состояние" является первым состоянием или симптомом, для которого применение терапии для лечения второго состояния, связанного с первым, могло бы представлять большую опасность или большее увеличение диапазона неблагоприятного действия, чем в том случае, если бы это первое состояние не было связано с ним.
"Лечение или предупреждение анемического состояния" означает введение терапевтического агента, который является эффективным в предупреждении, уменьшении, ослаблении или устранении анемического состояния. В одном аспекте это лечение применяют к предсуществующему анемическому состоянию, определяемому мерой анемии, например RBC, гемоглобином, гематокритным числом или другой мерой. В другом аспекте предупреждение анемического состояния означает лечение для уменьшения или предупреждения анемического состояния, появление которого статистически ожидается у индивидуума как результат лечебной процедуры или медицинского состояния, часто связанных с анемией.
"Сердечное состояние" означает патологическое состояние сердца, в том числе, но не только, застойную сердечную недостаточность, хроническую сердечную недостаточность, ишемию миокарда и инфаркт миокарда.
"Терапевтическая польза" является положительным результатом лечения симптома и может включать в себя, например, благоприятное изменение клинического показателя, такого как число эритроцитов (RBC), число тромбоцитов, гематокритное число (НСТ), уровень гемоглобина (гемоглобин), а также субъективные показатели, такие как уменьшенная боль, уменьшенная усталость, повышенная бодрость или улучшение ощущения благополучия.
"Период лечения" является, минимально, временем между первым введением терапевтического агента и обнаружением терапевтической пользы этого терапевтического агента. Период лечения может быть продлен на определенный или неопределенный период за пределы этого минимального времени.
"Без индуцирования или обострения неблагоприятного эффекта" означает отсутствие индуцирования неблагоприятного побочного эффекта, отсутствие ухудшения существующего неблагоприятного эффекта, отсутствие увеличения риска появления неблагоприятного эффекта, превышающего более чем на 15% риск, встречаемый в отсутствие лечения субъекта. Риск может быть определен сравнением частоты встречаемости в популяции одинаковых субъектов, получающих Эпоэтин Омега, с пациентами, получавшими плацебо. В отношении гипертензии, этот риск является меньшим, чем приблизительно 15%, если у пациента с "нормальным уровнем" кровяного давления кровяное давление будет измеряться как приблизительно 140/80-85 мм рт.ст. или более. В отношении кровяного давления увеличение диастолического или систолического давления менее чем на 10 мм рт.ст. по сравнению с измерением перед лечением не является значимым.
"Нормальный уровень" является величиной в диапазоне величин биологических или клинических измерений, который считается клиницистом статистически нормальным в популяции здоровых субъектов. Перечень нормальных уровней может быть найден в многочисленных ссылках, например, Harrison's Principles of Internal Medicine. Специалисту с обычной квалификацией в данной области будет понятно, что "нормальный уровень" будет меняться в зависимости от таких факторов, как возраст, вес, пол, и может изменяться в зависимости от новых развитий данной области.
"МЕ", или "международная единица" является стандартизованным измерением количества указанного биологического эффекта лекарственного или природно встречающегося материала. В частности, МЕ для эритропоэтина обозначает стандартное измерение из анализа in vivo экс-гипоксической имеющей полицитемию (эритроцитоз) мыши, которое стандартизовано с использованием Международного ссылочного препарата эритропоэтина Всемирной Организации Здравоохранения. Количество материала, требующегося для обеспечения одной МЕ для конкретного материала, будет меняться в зависимости от источника, состояния, качества, чистоты и/или типа этого материала. Взаимосвязь между МЕ и другими единицами, такими как определенные радиоиммунными тестами, может быть дополнительно понята со ссылкой на работу Storring et al., Brit. J. Haematol. 100:79, 1998, включенную здесь в качестве ссылки.
Структурные свойства эпоэтинов
Как упоминалось выше, эритропоэтины, полученные из различных ДНК (геномных или кДНК) и/или из различных клеточных линий, имеют различные картины гликозилирования и другие признаки, приводящие к гликопротеинам с различающимися биологическими активностями. В случае Эпоэтина Омега, фракций широкого пика, отобранных на конечной изоэлектрической стадии очистки, результаты анализа in vivo с использованием полицитемической мыши обычно показывают диапазон от приблизительно 40000 до 65000 МЕ/мг. Фракции более узко выбранного пика имеют активность in vivo в диапазоне 90000 МЕ - 120000 МЕ на мг. Для Эпоэтина Альфа активность in vivo фармацевтических препаратов обычно находится в диапазоне приблизительно 110000 МЕ на мг. Фармацевтические препараты испытывают в процессе гарантии качества/контроля качества с использованием анализа с применением полицитемической мыши перед разрешением использования для человека. Например, в условиях анализа с применением экс-гипоксической имеющий полицитемию мыши (см. Nature (1961/191:1069-1087/, величины в диапазоне от приблизительно 40000 до 65000 Е/мг наблюдаются для Эпоэтина Омега. Результаты радиоиммуноанализа показывают биологическую активность in vitro в диапазоне приблизительно 200000 - приблизительно 240000 Е/мг для Эпоэтина Омега. Сообщалось, что очищенный ЕРО мочи имеет активность in vivo от приблизительно 45000 МЕ до приблизительно 75000 или более МЕ на мг. Кроме того, имеются, вероятно, соответствующие различия во вторичной или третичной структурах рекомбинантных эритропоэтинов (т.е. в структуре/укладке белка), а также установленные различия в углеводном составе и прочности связывания углеводов, а также стабильности различных гликопротеинов, даже в том случае, когда первичная последовательность белков может быть идентичной. Каждая известная форма рекомбинантного эритропоэтина представляет собой гликопротеин, имеющий мириады сложных углеводных цепей, которые включают в себя сахара, которые являются N-связанными с аминокислотными остатками и/или О-связанными с гидроксиостатками. Однако количественное содержание, число, положение, прочность связи, структура и состав этих углеводных связей различаются между различными рекомбинантными эритропоэтинами и между эритропоэтином мочи человека. Структура и состав углеводных остатков Эпоэтина Омега были описаны, например, в статьях Nimtz et al., Eur. J. Biochem. 213:39, (1993); Tsuda et al., Eur. J. Biochem. 188:405, (1990) и Sytkowski et al., Biochem. Biophys. Res. Comm. 176:698, (1988), каждая из которых включена здесь в качестве ссылки в ее полном виде.
Sytkowski, et al., сообщает результаты электрофореза в додецилсульфат натрия/полиакриламидном геле (электрофореза в ДСН/ПААГ) Эпоэтина Омега, который приближенно определяет, что этот гликопротеин имеет среднюю молекулярную массу (приблизительно 35 кД), которая сравнима со средней молекулярной массой, обнаруженной для гликопротеина эритропоэтина человека в моче (34-39 кД; см., например, Miyake, T. et al., in J. Biol. Chem. (1977) 252:5558-5564). Дополнительные исследования в условиях изоэлектрического фокусирования показывают, что Эпоэтин Омега состоит из множественных изоформ (т.е., согласно IEF, приблизительно 6-8 изоформ во фракциях широкого пика и приблизительно 6 изоформ во фракциях узкого пика), что указывает на различающиеся типы и количества гликозилирования и, в частности, различные количества сиалилирования. В случае обоих Эпоэтинов Альфа и Бета имеются, по-видимому, всего 2-4 изоформы, как измерено посредством сравнительного IEF.
Nimtz, et al. наблюдал, что Эпоэтин Омега имеет содержание О-связанного олигосахарида меньше 1 моль на моль гликопротеина. Фактически, содержание О-связанного олигосахарида Эпоэтина Омега может быть существенно меньшим, чем 1 моль на моль гликопротеина, и, хотя степень О-гликозилирования может меняться от партии к партии, обычно она равна приблизительно 0,6 - приблизительно 0,7 моль на моль гликопротеина. Дополнительные исследования физико-химических свойств Эпоэтина Омега показывают, что фосфорилированная олигоманнозидная часть молекулы присутствует в сайте N-гликозилирования Asn-24. (См. статью Nimtz et al., in FEBS Letters (1995) 365:203-208, также включенную здесь в качестве ссылки). Считается, что Эпоэтин Омега имеет три сайта N-гликозилирования при аминокислотных остатках Asn-24, Asn-38 и Asn-83, и, кроме того, считается, что он имеет сайт О-гликозилирования при аминокислотном остатке Ser-126. И, в противоположность эритропоэтину мочи человека или Эпоэтину Альфа или Бета, Эпоэтин Омега, который экспрессируется из ApaI-фрагмента геномной ДНК эритропоэтина человека, трансформированной в клетки-хозяева ВНК, сохраняет всю его биологическую активность in vivo даже после подвергания условиям, которые приводят к существенному, если не полному, N-дегликозилированию. (См. работу Sytkowski, A.J. et al., in Biochem. Biophys. Res. Commun. (1991) 176(2):698-704, также включенную здесь в качестве ссылки). Эпоэтин Омега является уникальным в этом отношении, так как сообщается, что другие Эпоэтины теряют in vivo активность при N-дегликозилировании. Таким образом, описанные здесь способы могут быть выполнены с любым рекомбинантным эритропоэтином, проявляющим эти и другие структурные и/или функциональные характеристики Эпоэтина Омега.
Фигуры 1-3 изображают анализы при помощи гель-электрофореза, которые визуально иллюстрируют структурные различия между эпоэтинами Альфа, Бета и Омега. Фигура 1 изображает окрашенный Кумасси гель изоэлектрического фокусирования, который показывает различные изоформы, содержащиеся в препаратах проб эпоэтинов Альфа, Бета и Омега. Эти структурные различия происходят, отчасти, из различных углеводных компонентов. Эпоэтины Альфа и Бета имеют сходные составы с четырьмя легко детектируемыми изоформами при pI 3,7, 3,8, 3,9 и 4,1. Из них основными составляющими изоформами для обоих эпоэтинов Альфа и Бета являются изоформы с pI 3,8 и 3,9. Эпоэтин Омега имеет изоформы при 3,8, 3,9 и 4,1, однако Эпоэтин Омега содержит также менее кислые изоформы при pI 4,3, 4,5 и 4,6. Кроме того, основными компонентами-изоформами Эпоэтина Омега являются изоформы с pI 3,9, 4,1, 4,3 и 4,5.
Фигура 2 показывает более чувствительный, окрашенный серебром гель изоэлектрического фокусирования, который дополнительно выявляет, что Эпоэтин Бета имеет минорные изоформы при pI 4,2 и 4,6. Фигура 3 показывает окрашенный серебром ДСН-полиакриламидный гель, который иллюстрирует пример одной приближенной оценки различных молекулярных масс в препаратах проб эпоэтинов Альфа, Бета и Омега. В этом анализе средняя молекулярная масса для собрания изоформ Эпоэтин Омега была приближенно определена при 39 кД, независимо от того, был ли этот препарат разбавленным, например, приготовленным для терапевтического применения (дорожки 4 и 5), или происходил из объемного концентрата (дорожки 8, 11 и 12). В противоположность этому, для эпоэтинов Альфа и Бета собранные изоформы были приближенно определены как имеющие молекулярные массы 41 для разбавленных препаратов (дорожки 6 и 7) или 42 кД для концентрированных препаратов (дорожки 9 и 10). Эти оценки основаны на одном анализе, однако другие анализы будут показывать другие приближенные оценки в молекулярных массах или изоформах. Способ оценки будет влиять на анализ, но любой тщательный анализ будет показывать различие между молекулярными массами Эпоэтина Омега и Эпоэтином Альфа или Бета. Без связывания себя с теорией, авторы изобретения считают, что одним из объяснений различия в молекулярных массах для разбавленных и концентрированных форм эпоэтинов Альфа и Бета является то, что эти эритропоэтины являются более чувствительными к протеолизу или гидролизу углеводов, чем Эпоэтин Омега.
Антигенные реакции
Кроме чувствительности к протеолизу или гидролизу, антигенность рекомбинантного лекарственного средства, такого как эритропоэтин, может влиять на его эффективность, реактивность в зависимости от дозы и/или биодоступность на протяжении времени. О присутствии нейтрализующих IgG-антител против ЕРО сообщалось у некоторых подвергаемых гемодиализу анемических субъектов, которые не отвечали на введение Эпоэтина Альфа или Эпоэтина Бета. См., например, New England J. Med., 1996, 335:523; и Pharmacol. Res. 41:313, 2000, включенные здесь в качестве ссылки. В противоположность этому, Эпоэтин Омега является, по-видимому, менее антигенным, так как, по меньшей мере, три клинических испытания (называемые здесь ECU, испытания в Бразилии и Аргентине, описанные более подробно далее) показали, что, хотя все пациенты были подвергнуты скринингу на нейтрализующие антитела, никакие антитела не были обнаружены. Опять без связывания с теорией, авторы считают, что распределение гликозилирования Эпоэтина Омега приводит, возможно, к молекуле, которая более сходна с природно встречающимся эритропоэтином человека, или к молекуле, которая является структурно отличающейся, но просто менее антигенной, чем эндогенный ЕРО, найденный в сыворотке человека. Кроме того, возможно, что различия в третичной структуре могут способствовать различиям в антигенности. В любом случае данные по антигенности указывают на то, что менее вероятно то, что Эпоэтин Омега узнается системой иммунологического надзора человека, в сравнении с другими rHu EPO. В недавно опубликованном исследовании сообщалось, что получавшие Эпоэтин Альфа пациенты имеют антитела против rHu EPO, появляющиеся у приблизительно 66% находящихся на этой терапии пациентов. В противоположность этому, менее чем 1% пациентов, получавших Эпоэтин Омега, в нескольких исследованиях обнаружили присутствие антител против rHu EPO. Опять без связывания с теорией, авторы считают, что более высокая антигенность Эпоэтина Альфа может быть, по меньшей мере, частичной причиной сообщенных увеличивающихся доз (необходимости "ползучего" изменения доз) и/или более низкой величины Площади под Кривой (AUC) доступного rHu EPO у пациентов, подвергающихся продолжительному лечению Эпоэтином Альфа. Недавно опубликованное сообщение из Италии показывает, что более 60% пациентов, получавших Эпоэтин Альфа или Бета, обнаруживают присутствие антител к рекомбинантым ЕРО. (Castelli G., et al., Detection Of Anti-Erythropoietin Antibodies In Haemodialysis Patients Treated With Recombinant Human Erythropoietin, Pharmacol. Res. 2000 Mar. 41(3):313-8, включено здесь в качестве ссылки).
Далее, отмечается, что экспрессия ЕРО из ApaI-фрагмента в культивируемых клетках (ВНК или COS) продуцирует миллионы единиц на литр культуральной среды, что свидетельствует об очень быстрой скорости трансляции перед посттрансляционным гликозилированием. В противоположность этому, скорости продуцирования для систем, экспрессирующих Эпоэтин Альфа или Бета, находятся обычно в диапазоне 1400 МЕ на литр культуральной жидкости. Авторы считают, что в случае Эпоэтина Омега использование геномного ApaI-фрагмента дает мРНК, которая более эффективно транслируется в клетке, что, вероятно, дает трехмерную структуру предгликозилированного белка, приводящую к белку, который отличается от других rHu EPO или ЕРО мочи, несмотря на ту же самую аминокислотную последовательность. В настоящее время установлено, что рецепторы различных цитокинов являются высокочувствительными к белковым структурам более высокого порядка факторов передачи сигнала/цитокинов, которые способны активировать рецептор. Таким образом, различия в клинических или лекарственных эффектах Эпоэтина Омега могут быть связаны не только с различиями в структуре углеводов, но могут быть связаны с другими структурными факторами, такими как вторичная или третичная структура белка.
Типичные неблагоприятные эффекты
Различия в структуре разных эпоэтинов способствуют различным терапевтическим свойствам и различным рискам и величинам неблагоприятных побочных эффектов. Как упоминалось выше, здесь обеспечены способы применения Эпоэтина Омега для лечения или предупреждения анемического состояния без значимого увеличения риска неблагоприятного побочного эффекта, в частности, увеличенного кровяного давления или гипертензии. Эти способы применимы для лечения или предупреждения анемии у пациентов, имеющих предсуществующее состояние высокого кровяного давления, и/или для лечения пациентов, имеющих связанные состояния, такие как рак, состояние сердечной недостаточности, аутоиммунное заболевание, дисфункция печени, цирроз, склероз печени, гепатит или почечная дисфункция, без значимого продуцирования или обострения неблагоприятного побочного эффекта. Другие вредные побочные эффекты могут включать в себя тромбоз, увеличение тромбоцитов, тошноту или боль в месте инъекции, происходящие из данного способа лечения.
Фигура 4 показывает, что возникновение в процентах наиболее часто сообщаемых вредных побочных эффектов у пациентов, получающих Эпоэтин Омега, является значимо более низким, чем у пациентов, получающих Эпоэтин Альфа. Особенно важным для данного изобретения является появление гипертензии. Гипертензия обостряется увеличениями кровяного давления, что является одним из рисков, связанных со всеми способами лечения эритропоэтинами. Усталость часто связана с анемией или с таким состоянием, как дисфункция печени или рак, или с первичным лечением таких заболеваний. Тошнота является обычным симптомом определенных первичных терапевтических способов лечения, таких как химиотерапия и лучевая терапия.
Гипертензия и кровяное давление
Гипертензия, которая может проявляться в виде ухудшения предсуществующего состояния и/или заново развившейся гипертензии, является наиболее частым неблагоприятным побочным эффектом у анемических подвергающихся гемодиализу пациентов, получающих Эпоэтин Альфа, и встречается у 25-35% и 40-60% пациентов, соответственно. Обычно стойкое увеличение на 20 пунктов кровяного давления может ожидаться в большинстве случаев при лечении Эпоэтином Альфа. Обычно лечение любым эритропоэтином имеет тенденцию производить некоторое прогипертензивное действие. В соответствии с существующими результатами в данной области Эпоэтин Альфа и Бета стимулируют секрецию эндотелина 1, одного из наиболее важных эндогенных вазоконстрикторов, из васкулярных эндотелиальных клеток, он ингибирует продуцирование и высвобождение NO из васкулярного эндотелия, который является важным сосудорасширяющим медиатором (вазодилататором). Эпоэтин Альфа/Бета действует на систему реннин-ангиотензин-альдостерон, которая является гуморальной системой, регулирующей кровяное давление через интраваскулярный объем (альдостерон) и сосудистый тонус (ангиотензин II). Он увеличивает симпатический тонус и отвечаемость кровеносных сосудов на него. Он улучшает уровни гемоглобина, приводя к обращению вазодилатации в периферических тканях, которая происходит в качестве механизма локальной адаптации к низкому гемоглобину. Все эти эффекты являются более выраженными, более частыми или и теми, и другими у субъектов, которые имеют пониженную почечную функцию или уже являются более гипертензивными, чем "нормальными". В противоположность этому, гипертензия встречается всего лишь у 12,7% пациентов, получающих Эпоэтин Омега, согласно данному описанию (независимо от способа введения), как показано в клинических испытаниях, описанных более подробно далее. Далее, очевидно, что появление гипертензии или увеличение кровяного давления Эпоэтином Омега является по существу одинаковым с плацебо (по существу не встречающимся), что предполагает, что не следует ожидать причинного увеличения вследствие Эпоэтина Омега.
Таким образом, обеспеченные здесь способы включают в себя лечение Эпоэтином Омега, в котором риск развития гипертензии меньше приблизительно 15%. В зависимости от тяжести подвергаемого лечению состояния, а также от дозы и продолжительности лечения этот риск составляет менее чем приблизительно 10%, или менее чем приблизительно 5%. В другом варианте увеличение диастолического кровяного давления лечением Эпоэтином Омега составляет менее чем приблизительно 5 - приблизительно 10 мм рт.ст. и обычно менее чем приблизительно 7 мм рт.ст. на протяжении периода лечения. В другом варианте среднее ожидаемое увеличение диастолического кровяного давления для популяции субъектов, получавших Эпоэтин Омега, равно менее чем приблизительно 5,0 мм рт.ст. В другом варианте увеличение диастолического или систолического кровяного давления составляет менее 1,0 мм рт.ст., и более типично менее чем 0,8 мм рт.ст. на стандартное увеличение гемоглобина (г/дл). В сходном аспекте увеличение диастолического кровяного давления составляет менее чем 0,5 мм рт.ст. на стандартное увеличение гемоглобина. Эти преимущества обеспечиваются введением терапевтического количества Эпоэтина Омега в дозе приблизительно 5 - приблизительно 150 МЕ/кг или более типично приблизительно 25 - приблизительно 75 МЕ/кг один-три раза в неделю, как описано более подробно далее.
В испытании, сравнивающем эффекты Эпоэтина Омега с эффектами Эпоэтина Альфа, увеличение кровяного давления (ВР) над величинами фона, результаты показали, что увеличение ВР было более выраженным у пациентов, получавших Эпоэтин Альфа. Средняя величина увеличения систолического ВР над фоном была постоянно более высокой, чем у пациентов, получавших Эпоэтин Омега. Кроме того, несмотря на колебания, средняя величина увеличения систолического ВР над уровнем фона повышалась линейно во время испытания у пациентов, получавших Эпоэтин Альфа, но не у пациентов, получавших Эпоэтин Омега. Фигура 5 показывает, что площадь под кривой зависимости среднего увеличения над фоном от времени у пациентов, получавших Эпоэтин Альфа, была в 2 раза больше, чем в случае пациентов, получавших Эпоэтин Омега. Сходное различие было зарегистрировано для среднего увеличения диастолического кровяного давления (ВР), но оно было менее выраженным.
Фигура 6А и В показывает, что этот признак становится более важным при рассмотрении его с одновременным и значительно более выраженным действием Эпоэтина Омега на уровни гемоглобина. Более конкретно, отношение нежелательного увеличения кровяного давления к желательному увеличению гемоглобина является более благоприятным с Эпоэтином Омега, чем Эпоэтином Альфа. Во время первых 4 недель испытания (с фиксированными дозами) отношение среднее увеличение систолического ВР/среднее увеличение гемоглобина у Эпоэтин Альфа-пациентов было между 2,5 и 6,5, а отношение среднее увеличение диастолического ВР/среднее увеличение гемоглобина было между 1 и 2,75. Это указывает на то, что, в среднем, для каждой единицы увеличения гемоглобина над линией фона, Эпоэтин Альфа индуцировал повышение ВР на 1-6,5 единиц (мм рт.ст.). У Эпоэтин Омега-пациентов, в среднем, систолическое ВР увеличивалось на 0,2-0,8 мм рт. ст., а диастолическое ВР увеличивалось менее чем на 0,5 мм рт.ст., для каждой единицы увеличения гемоглобина. Во время этих первых недель данного испытания эти отношения у Эпоэтин Альфа-пациентов были в 4-12 раз более высокими, чем отношения у Эпоэтин Омега-пациентов. Таким образом, относительно действия на гемоглобин, Эпоэтин Омега оказывал заметно меньшее действие на кровяное давление, чем Эпоэтин Альфа.
Это различие между действиями эпоэтинов Альфа и Омега на систолическое и диастолическое кровяное давление относительно действий на гемоглобин было наиболее заметным во время первых 8 недель испытания, т.е. периода, когда увеличение гемоглобина было наиболее выраженным. Общее различие между этими двумя лекарственными средствами иллюстрируется также тем фактом, что площади под кривыми отношение/время для Эпоэтин Альфа-пациентов были в 4,5 и 2,3 раза большими, чем для Эпоэтин Омега-пациентов (для систолического и диастолического кровяного давления, соответственно). Кроме того, при тщательном мониторинге и коррекции доз Эпоэтина Омега в течение продолжительного периода времени как диастолическое, так и систолическое кровяное давление может даже показать слабое, но линейное снижение на протяжении времени, как иллюстрируется на фигуре 6С. Фигура 6D дополнительно показывает, что, хотя средний уровень гемоглобина увеличивается на протяжении периода лечения, среднее артериальное кровяное давление уменьшается во время того же самого периода, вместе с уменьшением средней дозы Эпоэтина Омега, требующейся для получения терапевтической пользы.
Поскольку сообщенное появление гипертензии у получавших Эпоэтин Альфа или Бета пациентов является по меньшей мере в 2 раза более высоким, чем появление, наблюдаемое у получавших Эпоэтин Омега пациентов, определенным является то, что риск появления гипертензии у получающих Эпоэтин Омега пациентов является более низким для получающих Эпоэтин Омега субъектов. Вышеупомянутые результаты испытаний показали, что действие Эпоэтина Альфа на кровяное давление было более выраженным, чем действие Эпоэтина Омега, в абсолютном количестве увеличения ВР над линией фона на протяжении всего периода обработки. Кроме того, для каждого г/дл увеличения гемоглобина Эпоэтин Альфа вызывал увеличение ВР до более чем в 12 раз высокой величины (в мм рт.ст.), чем Эпоэтин Омега. Таким образом, хотя точный увеличенный риск повышения ВР для каждого отдельного пациента является неопределенным, ясно, что риск гипертензии и/или увеличения величины кровяного давления (ВР) является более низким с Эпоэтином Омега, чем с Эпоэтином Альфа.
Отсутствие или снижение риска в отношении гипертензии или увеличения кровяного давления является важным для всех пациентов, но особенно для пациентов, для которых нельзя ожидать какой-либо реакции при использовании Эпоэтина Альфа или Бета. Например, пациенты, проходящие химиотерапию/лучевую терапию, которые должны подвергнуться лечению Эпоэтином Альфа или Бета, представляют для профессионала-медика вероятность малой пользы или отсутствия терапевтической пользы вследствие высоких доз (с сопутствующими высокими расходами) и вероятность ожидания по меньшей мере 4 недели (и иногда более, чем 6 недель) какой-то реакции, если она вообще наступит. Это приводит к увеличенному риску побочных реакций с малой вероятностью ожидания какого-либо увеличения RBC, гематокритного числа или гемоглобина. Кроме того, если такие терапевтические преимущества могут возникать, среднее ожидание равно приблизительно 10% увеличению над уровнями фона, например, увеличению в уровне гемоглобина от приблизительно 8,0 до приблизительно 8,8 г/дл гемоглобина, что существенно ниже желаемой целевой величины 12 г/дл или более.
Повышенный риск гипертензии или увеличения кровяного давления является важным неблагоприятным побочным эффектом лечения эритропоэтинами для пациентов, страдающих от связанных с сердцем проблем, таких как хроническая болезнь сердца. Это также верно, когда пациенты страдают от связанных с сосудами проблем, таких как артериальный склероз, где появление высокого кровяного давления может способствовать увеличению риска тяжелых побочных эффектов, таких как удар, CVA (инсульт), инфаркт миокарда или смерть. Это еще более осложняется у пациентов, имеющих высокий риск тромбоза вследствие других факторов риска, связанных с процессами коагуляции/антикоагуляции, таких как число тромбоцитов, агрегация тромбоцитов, протромбиновое время, тромбиновое время, уровни фибрина/фибриногена, уровни деградации фибриногена, уровни антитромбина 3 и т.д. Эти факторы действуют вместе с образованием комплексной системы, регулирующей коагуляцию и явления блокирования/рестрикции сосудов. Эритропоэтин обладает центральным терапевтическим действием по стимуляции эритропоэза, которое способствует увеличению вязкости крови и, следовательно, может приводить к повышению шанса коагулируемости, поскольку эритроциты имеют тенденцию занимать центральную часть кровотока и, следовательно, имеют тенденцию "отталкивания" тромбоцитов в сторону, приводя потенциально к большей вероятности контактирования с эндотелиальными клетками в "турбулентном потоке", что приводит к запуску агрегации тромбоцитов и внутрисосудистого свертывания.
Предыдущие способы лечения Эпоэтином Альфа, обсуждаемым, например, под названием EPOGEN в Physicians Desk Reference, 53 Ed. (1999), показали, что увеличенная смертность наблюдалась среди пациентов, получавших дозы Эпоэтина Альфа, достаточные для получения более высокого гематокрита 42%, чем среди пациентов, получавших дозы, достаточные для получения более низкого гематокрита 30%. Кроме того, встречаемость инфарктов миокарда, удара, сосудистых тромозов и других тромботических событий была также повышенной. В родственном исследовании частота смерти среди пациентов, подвергнутых хирургическому вмешательству для шунтирования коронарной артерии и получавших Эпоэтин Альфа, была 7 на 126 пациентов против отсутствия смертей среди 56 пациентов, получавших плацебо. Четыре смерти из 7 наступили после лечения Эпоэтином Альфа, и каждая из этих четырех смертей была связана с тромботическими событиями.
Кроме того, проводили исследование на пациентах с сосудистыми нарушениями (пациентах с клинически очевидным сердечным заболеванием, т.е. с хронической сердечной недостаточностью или ишемической сердечной недостаточностью) с Эпоэтином Альфа, чтобы довести их до гематокритного числа 42% или более. Это испытание было остановлено исследователями спустя всего лишь приблизительно 6 недель из-за результатов, которые показали смерть 35% пациентов, нацеленных на гематокрит 42%, и также смерть 29% пациентов, нацеленных на гематокрит 30%. Таким образом, из 1265 пациентов, в группе с гематокритом 42% была 221 смерть из 634 пациентов; и в группе с гематокритом 30% умерли 185 из 631 пациента. Кроме того, васкулярный тромбоз при применении шунта (шунта для диализа scribner) сообщался у 39% и 29% для группы, нацеленной на высокий гематокрит, и группы, нацеленной на низкий гематокрит, соответственно. Далее, другие тромботические события возникали в 22% и 18% случаев, соответственно. Наконец, из тех пациентов, которые не имели смертельного сердечного приступа, 3,1% и 2,3%, соответственно, обнаружили не имеющий летального исхода инфаркт миокарда (сердечный приступ). Эти результаты, полученные с Эпоэтином Альфа, суммированы ниже:
Нежелательные эффекты при лечении пациентов, имеющих патологические сердечные состояния, Эпоэтином Альфа
См. Amgen web-сайт в www.amgen.com в отношении полной предписывающей информации для врачей и Source Breaking news release Juni 25, 1996.
Хотя до сих пор еще не было проведено подобное клиническое испытание пациентов с сердечным заболеванием, нацеленных на конкретные гематокритные числа, с Эпоэтином Омега, к настоящему времени имелись тысячи пациентов в нескольких клинических исследованиях, некоторые из которых имели сосудистые нарушения или страдали от сердечных заболеваний, которые достигали высоких гематокритных чисел, и не было сообщений о сердечных приступах или тромботических событиях ни в одном случае. В родственном аспекте, с использованием Эпоэтина Омега постоянно сообщалось отсутствие значимого увеличения числа тромбоцитов. Фактически имеются многочисленные случаи, в том числе пациенты, описанные ниже в примерах 2 и 4, которые имели хроническую сердечную недостаточность и хорошо переносили Эпоэтин Омега без неблагоприятных событий тромбоза или сердечного приступа или смерти.
Связь тромботических событий с лечением эритропоэтинами может быть понята, частично, на основании исследований пациентов, подвергающихся гемодиализу (ГД), которые получали эритропоэтины. Вследствие применения шунтов эти пациенты обычно получали гепарин или другое лекарство, даже, в том числе, аспирин, для поддержания пролонгированного протромбинового времени для предотвращения тромбоза в A-V-шунте и свертывания в диализаторе. Тромбоз в А-V-шунте и свертывание в диализаторе (или свертывание в другом ГД-оборудовании) являются нередкими у ГД-пациентов и в основном обусловлены плохим мониторингом и неточной коррекцией доз гепарина, хотя увеличение тенденции тромбоза может способствовать соответствующему увеличению риска тромбоза в шунте.
Эти общие характеристики возникновения тромбоза в шунте применимы, по-видимому, также и к Эпоэтину Омега. Связанный с шунтами тромбоз встречался у 10,3% получавших i.v. и 7,8% получавших s.c. инъекции Эпоэтина Омега пациентов в одном многоцентровом испытании (379 i.v.- и 450 s.c.-инъецированных пациентов), что сравнимо с сообщениями для других эпоэтинов. Тромбообразование или сгустки в диализаторе не сообщались в двух других испытаниях. Один случай свертывания в диализаторе сообщался в сравнительном испытании в сравнении с Эпоэтином Альфа. Если объединить всех s.c.-инъецированных пациентов из этих испытаний, то тромбы в A-V-шунте и/или диализаторе встречались у 36/530 или 6,8% этих пациентов (на протяжении 11-16-26 недель).
Случаи тромбоза являются вторым наиболее частым нежелательным эффектом у анемических ГД-пациентов, получающих Эпоэтин Альфа или Бета, и сообщалось их появление у 7%-18% пациентов, получавших Эпоэтин Альфа или Бета. Сообщалось, что определенный процент пациентов имеют значимо измененные лабораторные тесты, указывающие на увеличенную тенденцию в отношении свертывания (число тромбоцитов и/или адгезия тромбоцитов, протромбиновое время и т.д.). Исследования in vitro, на моделях животных, здоровых волонтерах, ГД- или других пациентах, страдающих от почечной анемии, и "непочечных" пациентах, получавших рекомбинантные эпоэтины (Альфа и Бета), показали, что лечения этими эритропоэтинами могут иметь большое разнообразие действий на параметры коагуляции, такие как образование или агрегация тромбоцитов, время кровотечения, уровни антитромбина, уровни фибриногена и т.д., хотя каждый из этих эффектов встречается непостоянно и редко.
Однако фигура 7 показывает, что лечение пациентов Эпоэтином Омега не обнаруживает какого-либо значимого увеличения уровня числа тромбоцитов крови. Числа тромбоцитов остаются в нормальном диапазоне на протяжении всего типичного протокола лечения. Без связывания с теорией, авторы изобретения считают, что отсутствие встречаемости увеличения числа тромбоцитов может способствовать общему более низкому риску тромботических событий у пациентов, получающих Эпоэтин Омега, чем получающих эпоэтины Альфа или Бета. Это позволяет использовать Эпоэтин Омега в лечении анемических состояний, связанных с сердечными заболеваниями, без значимого увеличения риска нежелательного тромботического события. Это является важным показанием для использования Эпоэтина Омега без индуцирования нежелательных тромботических событий у пациентов, имеющих риск тромбообразования, который не связан с применением шунтов. В таких случаях было бы важным для профессионала-медика иметь доступный для применения ЕРО, который НЕ увеличивает число тромбоцитов и, следовательно, не представляет явно увеличенного риска тромбоза или рестрикции сосудов в получающем ЕРО пациенте (иного, чем естественный и предвидимый риск большего числа эритроцитов и, следовательно, увеличенной вязкости крови).
Лечение пациентов с раком
Лечение пациентов, имеющих злокачественные заболевания, Эпоэтином Омега вносит вклад в общий прогноз этого заболевания в силу различных причин. Во-первых, со злокачественным заболеванием могут быть связаны усталость, тошнота, телесная боль и анемия. Эта связь может быть либо независимым или вторичным патологическим состоянием, состоянием, вызываемым раком, либо состоянием, которое происходит из первичной терапии в отношении рака, такой как химиотерапия или лучевая терапия. Лечение и улучшение в случае анемии, связанной с раком, в общем, усиливает природные механизмы защитных сил организма, усиливает способность организма функционировать на "нормальном" уровне для борьбы с заболеванием и аксигенации ткани, увеличивает переносимость первичного лечения (химиотерапии/облучения и связанных с ними медикаментов), что делает возможным пролонгированное и полное применение показанного первичного лечения и/или более высоких доз, и снижает риск появления вредных побочных эффектов этого лечения. Во-вторых, лечение Эпоэтином Омега позволяет ослаблять усталость, уменьшать/устранять тошноту и/или ослаблять боль. В-третьих, вышеуказанная польза, в свою очередь, обеспечивает пациенту более "нормальную" жизнь и улучшение в настроении и ощущении благополучия (т.е. лечение депрессии, отчаяния/безнадежности или плохого настроения, связанных с раком/лечением рака), что является положительным видом на будущее, который дополнительно способствует прогнозу лечения.
Кроме того, хорошо переносимая схема лечения с меньшим страданием от этого лечения будет действовать как положительный фактор для пациентов, решающих принять дополнительные схемы лечения с химиотерапией или лучевой терапией, или решающих принять дополнительные раунды лечения в случае рецидива рака, когда предписывается дополнительный курс лечения. Пациент, который получил улучшение или имел меньше "страданий" во время лечения рака, более склонен согласиться на курс повторного лечения или альтернативного лечения, чем отказаться от лечения при рецидиве рака, чтобы не страдать снова от самого лечения. Отмечается, что нижеследующее относится к лечению рака без Эпоэтина Омега: 76% усталость, 54% тошнота, 23% депрессия, 20% боль. Таким образом, когда Эпоэтин Омега действует в случае анемии рака и действует, уменьшая боль и тошноту, независимо от увеличения гемоглобина, Эпоэтин Омега способствует ценной и очень необходимой терапии в отношении онкологии.
Анемия, связанная со злокачественным заболеванием, очень сходна с анемией хронической болезни. Ее называют иногда неосложненной гипопролиферативной анемией злокачественного заболевания, которая обычно является хронической, умеренной, нормохромной, нормоцитарной анемией с нормальными уровнями MCV (среднего объема эритроцитов), MCH (среднего содержания гемоглобина в эритроците) и MCHC (средней концентрации гемоглобина в эритроците), с уровнями гемоглобина 8-10 г/дл и ретикулоцитопенией и пониженным железом и TSI сыворотки, с нормальным или повышенным ферритином. Нормальные предшественники и нормальные или увеличенные запасы железа обнаруживаются в костном мозге. Эта анемия может быть многофакторной, но первично гипопролиферативной анемией. Имеется отсутствие эритропоэтина без физического повреждения почек, и уровни эритропоэтина являются низкими по сравнению с гемоглобином, т.е. нет линейного обратного отношения гемоглобина к эритропоэтину. Раковые пациенты нуждаются в более выраженной гипоксии для индукции продуцирования эндогенного эритропоэтина. Таким образом, существует ярко выраженная потребность в замещении и восполнении эндогенного эритропоэтина.
Без связывания себя теорией, авторы считают, что часть объяснения для хронической анемии, связанной со злокачественным заболеванием, включает в себя продуцирование или отсутствие продуцирования различных цитокинов и применение цитотоксических агентов, например, цисплатины или другие химиотерапевтические агенты, при первичном лечении рака. Кроме того, может быть изменен метаболизм железа, т.е. запасы железа не могут утилизироваться наиболее эффективным образом. Реактивность костного мозга на эритропоэтин часто может быть притупленной без поражения костного мозга раком, а скорее как результат действия комплекса различные цитокины/цитотоксины/облучение. Длительность жизни RBC является несколько более короткой даже без гемолиза или других путей индукции истощения RBC вследствие действия цитокинов в активации макрофагов. В любой момент хроническая злокачественная анемия может быть осложнена несколькими факторами. Они включают в себя (а) инфекцию и/или другое воспалительное заболевание, (b) аутоиммунную гемолитическую анемию, которая индуцируется некоторыми опухолями и некоторыми цитостатическими/цитотоксическими агентами, такими как метотрексат, обычно используемый в химиотерапии, (с) микроангиопатический гемолиз, который может быть индуцирован некоторыми опухолями, (d) кровотечение и (е) гиперспленизм, который очень часто имеет место в случае твердых опухолей, и (f) супрессию костного мозга цитостатическими агентами/облучением или опухолевой тканью.
Как показано на фигуре 4, Эпоэтин Омега обычно производит значимо меньше случаев вредных побочных эффектов, чем Эпоэтин Альфа, даже в диапазонах доз приблизительно 150 МЕ/кг в неделю. Эффективность более низких доз и уменьшенные вредные побочные эффекты также позволяют использовать более частые дозы, например, до 7 или более раз в неделю. Лечение анемического состояния, связанного с раком, эпоэтинами Альфа или Бета обычно требовало бы дозы приблизительно 450-3500 или более МЕ на кг в неделю. В противоположность этому, лечение с использованием Эпоэтина Омега является эффективным при дозах, которые являются значимо более низкими при выражении в международных единицах. Лечение Эпоэтином Омега может быть начато до, после или во время первичного лечения с использованием раковой терапии, например химиотерапии или лучевой терапии. Данные, показанные на фигурах 22 и 23, были получены на пациентах, начинающих терапию Эпоэтином Омега уже после достижения анемического гемоглобина 6,5, который увеличивался до нормальных уровней гемоглобина (12 или выше) за восемь недель. Доктор может лечить пациента, который имеет тяжелую анемию, и ожидать ответной реакции от применения Эпоэтина Омега в пределах недели, а не ожидать 4-6 недель, прежде чем какая-либо реакция может ожидаться для Эпоэтина Альфа. В наилучшей ситуации лечение Эпоэтином Омега начинают до начала раковой терапии или одновременно (в пределах 3 недель) с раковой терапией и лечение может успешно продолжаться во время и после раковой терапии. Далее описаны типичные диапазоны доз для лечения Эпоэтином Омега.
Дозы
Каждый из способов лечения с использованием Эпоэтина Омега в соответствии с данным изобретением использует более низкую дозу, чем доза, требующаяся при использовании Эпоэтина Альфа или Эпоэтина Бета. Более низкие дозы являются эффективными как во время начального периода титрования (запуска), в котором исходная доза для увеличения гемоглобина оптимизируется в отношении индивидуума, так и во время периода поддержания, в котором доза корректируется для продолжительной и непрерывной терапии. В широких вариантах способы лечения используют Эпоэтин Омега, вводимый в дозе приблизительно 5 - приблизительно 150 МЕ/кг, один-три раза в неделю, или приблизительно 25 - приблизительно 150 МЕ/кг в неделю. В одном варианте осуществления Эпоэтин Омега вводят в дозе приблизительно 10 - приблизительно 100 МЕ/кг в неделю или приблизительно 10 - приблизительно 75 МЕ/кг один-два раза в неделю. В другом варианте осуществления Эпоэтин Омега вводят в дозе около 25 - около 60 МЕ/кг или около 25 - около 35 МЕ/кг, два раза в неделю. Еще в одном варианте осуществления Эпоэтин Омега вводят в дозе около 50 - около 150 МЕ/кг или около 75 - около 100 МЕ/кг, один раз в неделю.
Эти дозы Эпоэтина Омега меньше, чем в типичных способах лечения, использующих Эпоэтины Альфа или Бета, как по величине дозы, так и по частоте введения. Более конкретно, Эпоэтины Альфа и Бета обычно вводят 3-7 раз в неделю в дозах, начинающихся при 150->450 МЕ/кг на дозу или от 450->3000 МЕ/кг в неделю (титруемых в виде 6 доз или предоставляемых почти каждый день). В противоположность этому, здесь обеспечены более низкие дозы Эпоэтина Омега и более низкая частота введения 1-3 раза в неделю, к чему давно стремились после того, как введение доз один раз в неделю оказалось эффективным при использовании Эпоэтина Омега. Типичный период терапевтического лечения включает в себя период титрования, в котором Эпоэтин Омега вводят при начальной дозе около 50 - около 150 МЕ/кг в неделю и корректируют во время периода титрования для достижения желаемой терапевтической пользы. В этом случае не является необычным, что пациент достигает уровней гемоглобина 15 или выше вплоть до 19 без вредных побочных реакций. Один пример намечает в качестве терапевтической пользы во время периода титрования получение уровня гемоглобина приблизительно 10 - приблизительно 12 или более г/дл. Типичное лечение сопровождается также периодом поддержания, с титрованием для поддержания желаемой величины гемоглобина. В одном варианте осуществления Эпоэтин Омега вводят в дозе около 20-60 МЕ/кг в неделю во время периода поддержания.
Примерное сравнение требований доз при использовании Эпоэтина Альфа/Бета по сравнению с Эпоэтином Омега для лечения анемии у подвергнутых гемодиализу пациентов является следующим:
Для сравнения, фигура 26 иллюстрирует примерное распределение требований поддерживающей дозы в популяции пациентов с гемодиализом, получавших Эпоэтин Альфа.
При лечении анемии, связанной с онкологией (т.е. связанной с химиотерапией или лучевой терапией), где пациентов лечат rHu EPO в попытке предотвращения необходимости переливания крови, сравнение требующихся доз является следующим:
В этом сравнении следует отметить, что лечение Эпоэтином Альфа было эффективным в повышении гемоглобина до достаточного уровня, чтобы избежать переливания крови, у менее чем 40% пациентов, тогда как все пациенты, получавшие Эпоэтин Омега, повышали уровни гемоглобина до уровней, достаточных для избежания необходимости переливания крови.
Фигура 22 визуально иллюстрирует сравнение между требованиями введения высоких и низких доз Эпоэтина Омега и Альфа при лечении анемии у проходящих химиотерапию пациентов, которых лечили на протяжении периода восьми недель Эпоэтином Омега, по сравнению с подобными исследованиями лечения пациентов, проходящих химиотерапию, Эпоэтином Альфа. Показанные количества доз скорректированы в отношении среднего веса пациента 70 кг. Эпоэтины вводили при частоте две дозы в неделю. Получавшие Эпоэтин Омега пациенты требовали общую недельную дозу между приблизительно 4000 и 12000 МЕ по сравнению с общей недельной дозой 40000-100000 МЕ или более для получавших Эпоэтин Альфа пациентов. В этом примере примечательным является то, что Эпоэтин Омега достигает желаемого уровня или поддерживает желаемый уровень гемоглобина, тогда как Альфа/Бета показывают 60% не отвечающих на лечение пациентов при фактически любой дозе. При коррекции относительно среднего веса пациента 70 кг доза на одно введение была приблизительно 28-86 МЕ/кг для Эпоэтина Омега по сравнению с приблизительно 285-571 МЕ/кг для Эпоэтина Альфа. Таким образом, Эпоэтин Омега является в приблизительно 6,6-10 раз более эффективным в схеме введения доз, чем Эпоэтин Альфа, в расчете единица/единица при лечении анемии, связанной с химиотерапией. Кроме того, Фигура 23 иллюстрирует, что Эпоэтин Омега был значительно более эффективным в повышении уровней гемоглобина, чем Эпоэтин Альфа, в том смысле, что Эпоэтин Омега действовал на анемию. В конце 8 недели, получавшие Эпоэтин Омега пациенты достигали увеличенного уровня гемоглобина от средней исходной величины приблизительно 6,5 г/дл до желаемой величины 12 г/дл. В противоположность этому, получавшие Эпоэтин Альфа пациенты в среднем достигали только умеренного увеличения от приблизительно 9,0 до 9,5 г/дл на протяжении того же самого периода. Поскольку биологические фармацевтические вещества, такие как эритропоэтины, обычно продаются на основе единиц, более высокая эффективность Эпоэтина Омега практически переводится в существенные сбережения расходов для терапии с использованием эритропоэтинов. Например, во время подачи этой заявки 100000 МЕ в неделю Эпоэтина Альфа переводится в 1000 долларов США при 10 долларах за 1000 МЕ, в сравнении с 4000 МЕ - 12000 МЕ Эпоэтина Омега, по конкурентной цене 40-120 долларов США в неделю. На протяжении 8 недель терапии Эпоэтин Омега при 8000 МЕ в неделю стоил бы 80 долларов в неделю × 8 недель, или 640 долларов США; по сравнению с 100000 или более МЕ Эпоэтина Альфа (например, 25 флаконов по 4000 в неделю) или 1000 в неделю, или 8000 долларов США на протяжении 8 недель применения.
Введение доз может быть скорректировано в соответствии с подлежащим лечению состоянием и реакцией субъекта. В лечении усталости или боли более низкую начальную дозу 5-50 МЕ/кг в неделю или более часто 20-60 МЕ/кг вводят один раз или два раза в неделю в течение начального периода титрования 1-4 недель. Во время этого периода титрования субъекта оценивают на уменьшение боли или усталости. Если субъект жалуется на продолжающиеся симптомы, дозу корректируют в направлении увеличения в виде приращений, которые обычно увеличиваются на 1/2 начальной дозы. Альтернативно, начальную дозу вводят дважды в неделю. Напротив, если субъект сообщает об уменьшении боли или усталости, доза может быть скорректирована в направлении уменьшения на примерно 10 МЕ/кг для получения минимальной дозы, которая является эффективной для периода поддержания без увеличения риска вредных побочных эффектов.
Для лечения обычной возникающей при диализе анемии средняя доза периода титрования для Эпоэтина Альфа находится обычно в диапазоне около 150-450 МЕ/кг в неделю с разделением на три дозы в неделю, со средней дозой около 200 МЕ/кг или более на дозу. Подобным образом, типичная поддерживающая доза для Эпоэтина Альфа составляет 225 МЕ/кг в неделю, с разделением на две или три дозы, причем 25% пациентов требуют более 600 МЕ/кг в неделю. В противоположность этому, средняя доза при титровании для Эпоэтина Омега равна приблизительно 32 МЕ/кг два-три раза в неделю и средняя поддерживающая доза равна 23 МЕ/кг два-три раза или 40-100 МЕ/кг в неделю, при разделении на один, два или три раза в неделю; и средняя поддерживающая доза Эпоэтина Омега для пациентов с диализом равна 20-70 МЕ/кг в неделю, при разделении на одну, две или три дозы в неделю. Это иллюстрируется, например, на фигуре 8, которая показывает требования высокой, низкой и средней дозы для Эпоэтина Альфа по сравнению с Эпоэтином Омега для лечения анемии во время периода поддержания для пациентов с диализом. Типичная доза периода поддержания для Эпоэтина Омега, применяемая после достижения желаемой величины гемоглобина, равна приблизительно 1/2-1/3 количества, используемого во время периода титрования. Эта доза может быть уменьшена до меньшей частоты дозы, чем с Эпоэтином Альфа или Бета, отчасти благодаря более длительной биодоступности и увеличенной эффективности Эпоэтина Омега. Увеличение дозы во время фазы поддержания редко требуется для Эпоэтина Омега. Эти дозы должны быть скорректированы в небольшие количества, обычно около 5 - около 25 МЕ/кг в неделю. Типичная недельная доза Эпоэтина Омега для 60-70% пациентов с гемодиализом была приблизительно 40 - приблизительно 60 МЕ/кг в неделю. Приблизительно 45% пациентов могли поддерживать желаемый уровень гемоглобина без какого-либо лекарственного средства вообще в течение одной или двух или даже трех недель. Таким образом, с Эпоэтином Омега инъекции один раз в неделю приблизительно 50-150 или 40-100 МЕ/кг могут быть также использованы для большого числа пациентов. Поскольку нежелание получать инъекции/укалывания иглами является нормальным состоянием для пациентов с гемодиализом или с хроническим заболеванием, эта низкая частота фактического введения является большим преимуществом, особенно если доза должна вводиться подкожным путем (s.c.) (более болезненным из-за игл и нервов, расположенных в коже), для получения еще более низкой общей недельной дозы. Это отличается существенно от любого известного способа лечения с использованием Эпоэтина Альфа или Бета, где частота доз один раз в неделю является неэффективной, так что даже такие высокие дозы, как 200 МЕ/кг, являются недостаточными для поддержания уровней гемоглобина в желаемом диапазоне. Применение гораздо более низких доз Эпоэтина Омега и меньшей частоты инъекций/введения приводит к нескольким сопутствующим преимуществам, в том числе более низкой общей стоимости терапии, пониженному риску связанных с дозой ЕРО побочных эффектов и меньшей вероятности - отсутствию вероятности требований "ползучих" доз, чем обнаруживаемые пациентами, получающими Эпоэтин Альфа или Бета.
Другим важным признаком обеспеченных здесь способов лечения Эпоэтином Омега является отсутствие лаг-периода в достижении реакции по сравнению с использованием других эпоэтинов, что означает фактически немедленную реакцию или отсутствие латентного периода. Например, фигуры 15С, 16 и 17 иллюстрируют, что уровни гемоглобина увеличиваются после первой недели введения Эпоэтина Омега. Это контрастирует с Эпоэтином Альфа, который обычно не обнаруживает увеличения гемоглобина до периода по меньшей мере второй недели лечения в случае анемии у пациентов с диализом и 4 недель или более в случае попытки лечения Эпоэтином Альфа/Бета анемии при онкологии. Таким образом, дозы титрования и поддержания для Эпоэтина Омега могут быть установлены более быстро и с большей определенностью, чем для эпоэтинов Альфа или Бета.
Кроме того, более низкие и менее частые дозы, требующиеся для Эпоэтина Омега, способствуют более низкой встречаемости или более низкому риску или размеру вредных побочных эффектов, таких как увеличенное кровяное давление, гипертензия, стимуляция/увеличение количества тромбоцитов, телесная боль, боль в месте инъекции или тромбоз, по сравнению с другими эпоэтинами. Кроме того, более низкие дозы и более высокая биодоступность, сопряженные с, по существу, отсутствием или с низким риском какого-либо вредного события, позволяют вводить Эпоэтин Омега для лечения слабых симптоматических состояний, таких как усталость или телесная боль. Эти состояния могут лечиться независимо от того, связаны ли или не связаны они с анемией, или связаны ли или не связаны они с застойной сердечной недостаточностью, раком, аутоиммунным заболеванием или дисфункцией печени или другим хроническим заболеванием.
Клинические испытания лечения анемии, связанной с заболеванием
Традиционно, анемия почечного заболевания конечной стадии является главным показанием для применения рекомбинантного эритропоэтина (эритропоэтинов) человека. Это связано в основном с тем, что эндогенный ЕРО образуется в почках. В состоянии почечного заболеваниия, либо пре-ESRD (предтерминальной почечной недостаточности), либо ESRD (терминальной почечной недостаточности), почка замедляет или прекращает продуцирование ЕРО, что делает гормональную (эритропоэтиновую) заместительную терапию способом лечения, который необходим для лечения анемии. Эффективность и безопасность Эпоэтина Омега в этом показании исследовали в нескольких испытаниях с участием взрослых пациентов с гемодиализом (ГД). Хотя описанные здесь результаты относятся к анемии, связанной с почечным заболеванием, низкие дозы, быстрые реакции и низкая частота встречаемости побочных эффектов указывают на то, что Эпоэтин Омега является полезным для лечения анемии, связанной с другими состояниями, в частности, состояниями, которые могут быть противопоказанными для Эпоэтинов Альфа и Бета вследствие высоких доз, более медленных ответных реакций и более тяжелых побочных эффектов.
Однодозовое, односторонне-слепое, перекрестное испытание, сравнивающее s.c. Эпоэтин Омега с Эпоэтином Альфа, исследующее 18 регулярно диализуемых анемических пациентов (13М/5Ж, возраст 33-75, 51,8±10,8 лет), показало, что Эпоэтин Омега имеет более высокую относительную биодоступность, чем Эпоэтин Альфа. Пациентов распределяли методом случайной выборки на группы для получения s.c. 50 МЕ/кг либо Эпоэтина Альфа (n=9), либо Эпоэтина Омега (n=9). После 7-дневного периода вымывания Эпоэтин Альфа-пациентов переключали на Эпоэтин Омега и vice versa с теми же самыми дозами. Величины фона эритропоэтина определяли непосредственно перед введением каждого лекарственного средства. Эритропоэтин в плазме измеряли с использованием коммерчески доступного набора ЕРО-ELISA (Boehringer Mannheim, cat. no. 1693417, моноклональное антитело против ЕРО, "CHO Epoetin", калиброванное против стандарта WHO IRP (международного эталонного препарата Всемирной организации здравоохранения).
Как средняя Смакс, так и средняя площадь под концентрационной кривой (AUC0-120) были значительно более высокими после инъекции Эпоэтина Омега, чем после инъекции Эпоэтина Альфа. Как показано в таблице I и графически изображено на фигуре 9, средние уровни эритропоэтина в плазме в случае Эпоэтина Омега были более высокими и сохранялись на протяжении более продолжительного периода времени, чем в случае Эпоэтина Альфа. Более конкретно, t1/2β имел большую продолжительность после инъекции Эпоэтина Омега. В данных по отдельным пациентам для 16 из 18 пациентов Смакс и AUC после инъекции Эпоэтина Омега были более высокими, чем после инъекции Эпоэтина Альфа. t1/2β также увеличивался у 12 из 18 пациентов после инъекции Эпоэтина Омега.
Фармакокинетические данные по Эпоэтину Омега и Эпоэтину Альфа после единственной s.c.-инъекции (50 МЕ/кг).
AUC и полупериод выведения из организма рассчитывали из концентраций в плазме, скорректированных на величины фона. Величины представляют X±SID.
Приведенные выше данные иллюстрируют более высокую относительную биодоступность Эпоэтина Омега после s.c.-инъекции (на основании сравнений AUC). Данные Смакс и кривая зависимости концентрации в плазме от времени, вместе с наблюдением, что фазы выведения этих двух лекарственных средств не были настолько драматически различными, предполагают, что различие обусловлено различиями в абсорбции (всасывании) между этими двумя типами эритропоэтинов. На основании этого и других доступных данных было приближенно определено, что полупериод абсорбции (t1/2α) для Эпоэтина Омега (оцениваемый по характеру кинетики первого порядка) был приблизительно 5 часов, а средний полупериод абсорбции (t1/2α) для Эпоэтина Альфа был приблизительно на 60% более длительным. Эти данные показывают, что единственная доза равного количества (МЕ/кг) Эпоэтина Омега и Эпоэтина Альфа приводит к приблизительно в 1,72 раза более высокому уровню эритропоэтина в плазме с использованием Эпоэтина Омега. Далее, Эпоэтин Омега выводится из плазмы более медленно, как иллюстрируется средним отношением 1,41 в величине полупериода конечного выведения. Это способствует заметно более высокой биодоступности Эпоэтина Омега, иллюстрируемой отношением 2,43 в величине AUC для Эпоэтина Омега в сравнении с Эпоэтином Альфа.
Фигура 10 показывает, что при коррекции доз этих двух эритропоэтинов для поддержания терапевтической реакции в течение периода поддержания 12 недель после начальной дозы 2×50 МЕ/кг в неделю s.c., которая была фиксированной в течение первых 4 недель, средняя концентрация в плазме остается более высокой для Эпоэтина Омега (фигура 10А), чем для Эпоэтина Альфа (фигура 10В), приводя к необходимости более низких доз Эпоэтина Омега на протяжении периода поддержания. Более конкретно, фигура 10 показывает, что (средние) дозы Эпоэтина Омега непрерывно уменьшались во время испытания, тогда как концентрации эритропоэтина в плазме повышались. В противоположность этому, после первого периода фиксированного дозирования дозы Эпоэтина Альфа должны были увеличиваться, а концентрации эритропоэтина в плазме увеличивались незначительно. Результатом этого является то, что дозы Эпоэтина Омега были постоянно более низкими, чем дозы Эпоэтина Альфа, а концентрации эритропоэтина в плазме были постоянно более высокими у пациентов, получивших Эпоэтин Омега.
Это различие Эпоэтина Омега в сравнении с Эпоэтином Альфа в эффекте доза/концентрация в плазме было наиболее заметным во время первых 4 недель лечения. Хотя использовали идентичные дозы (т.е. 2×50 МЕ/кг), не было повышения концентраций эритропоэтина в плазме у Эпоэтин Альфа-пациентов, тогда как было значимое почти 2-кратное повышение концентраций эритропоэтина в плазме у Эпоэтин Омега-пациентов. Тот факт, что концентрация в плазме продолжала увеличиваться, несмотря на снижение доз Эпоэтина Омега, свидетельствует о лучшем накоплении Эпоэтина Омега, чем Эпоэтина Альфа, в ходе терапевтического лечения. Обычно является предпочтительным, чтобы дозы вводились s.c.-инъекцией, а не i.v.-инъекцией, так как s.c.-введение склонно удлинять время, в течение которого эритропоэтин остается на уровне выше уровней фона, однако, авторы считают, что эти различия в накоплении и доступности между Эпоэтином Омега и Эпоэтином Альфа будут наблюдаться также для i.v.-введения.
Приведенные выше данные (и другие данные, не представленные здесь) показывают, что Эпоэтин Омега лучше всасывается, чем Эпоэтин Альфа, так как получена более высокая Смакс (таблица I), и полупериод абсорбции, по-видимому, является значимо более коротким. Сравнение этих данных с исследованием с Эпоэтином Бета, например, опубликованным в работе в Drugs, 1995; 49:232, включенной здесь в качестве ссылки, показывает, что полупериод существования в организме Эпоэтина Омега является в 2-3 раза более низким, чем для Эпоэтина Бета.
Время клиренса для Эпоэтина Омега также значительно отличается от времени клиренса других эпоэтинов, например, время клиренса для Эпоэтина Омега является более продолжительным по сравнению с Эпоэтином Альфа. Более конкретно, скорость клиренса приблизительно 0,26±0,12 мЕ/мин/мл наблюдали для Эпоэтина Омега по сравнению со скоростью клиренса 0,68±0,31 мЕ/мин/мл для Эпоэтина Альфа, как сообщается Storring et al. Время клиренса, как и абсорбция, является, по-видимому, также независимым от дозы.
В начальных испытаниях Эпоэтин Омега вводили внутривенно. Однако, как обсуждалось выше, предпочтительным является введение эритропоэтина s.c.-путем. Однако, как суммировано в таблице II, открытые, не имеющие контроля i.v.-испытания, оцениваемые с использованием более 100 пациентов, ясно показали, что Эпоэтин Омега эффективно стимулировал эритропоэз у субъектов, имеющих анемию, связанную с терминальной стадией почечного заболевания. Введение очень низких доз Эпоэтина Омега оказывало удивительные действия как на гемоглобин, так и на НСТ (гематокрит), которые были на низких фоновых уровнях, хотя параметры метаболизма железа могли не быть идеальными. Индивидуальные данные из двух испытаний (испытания в Бразилии и испытания в Аргентине) обнаружили, что ни один пациент, включенный в испытание, не получал более 230 МЕ/кг в неделю. Кроме действий на гематологические параметры, испытание в Аргентине и третья серия испытаний в Индии показали, что 4 недели лечения Эпоэтином Омега эффективно увеличивали работоспособность и переносимость физической нагрузки пациентами, что демонстрировалось увеличенной работоспособностью и потреблением кислорода.
Фигура 11 показывает, что случаи боли в месте s.c.-инъекции с использованием шкалы визуальных аналогов (VAS) были значительно меньшими для получавших Эпоэтин Омега пациентов, чем получавших Эпоэтин Альфа пациентов. Средний недельный балл VAS из недель 1-14 испытания был значимо более высоким в Эпоэтин Альфа-группе, чем в Эпоэтин Омега-группе. Различие между этими лекарственными средствами иллюстрируется также тем фактом, что площадь под кривой зависимости средних значений средних недельных баллов VAS от времени была в 1,7 раз большей в Эпоэтин Альфа-группе, чем в Эпоэтин Омега-группе. Эти данные предполагают, что Эпоэтин Омега лучше переносился, чем Эпоэтин Альфа, в отношении локальной боли после s.c.-инъекции.
Четвертое открытое, не имеющее контроля Европейское испытание включало в себя более 1000 ГД-пациентов. В целом, оценивали 829 пациентов в течение 26 недель. Из этих пациентов 379 получали Эпоэтин Омега i.v.-инъекцией и 450 получали Эпоэтин Омега s.c.-инъекцией.
В контролируемом исследовании с использованием начальной дозы 3×40 МЕ/кг в неделю, либо i.v., либо s.c., как гемоглобин, так и гематокрит быстро повышались, приводя к раннему снижению дозы всего лишь после двух недель лечения большинства пациентов. Таким образом, для основной части этого испытания использовали начальные дозы 3×30 МЕ/кг в неделю i.v. или s.c. Включенные в это испытание пациенты имели гемоглобин ≤9,0 г/дл, НСТ ≤27% и все стандартные критерии включения/исключения для испытаний эффективности/безопасности rHu EPO.

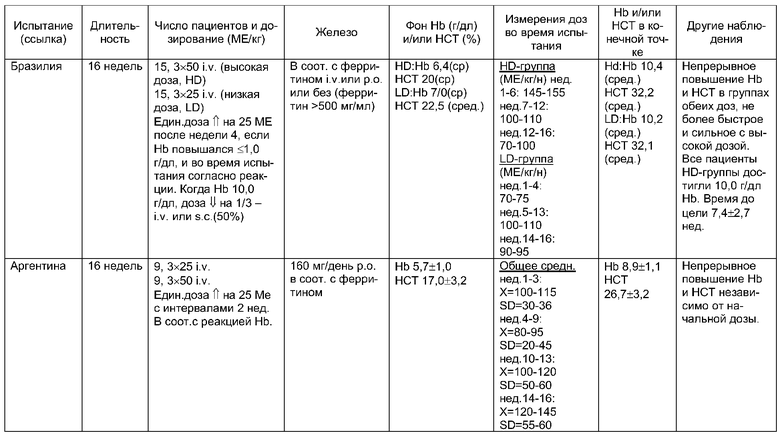
Основной целью этого испытания было увеличение и поддержание гемоглобина при 10,0-12,0 г/дл или по меньшей мере индуцирования повышения гемоглобина ≥2,0 г/дл, НСТ >6% на протяжении первых 12 недель испытания. Введение доз было разделено на два периода: период титрования (необходимый для достижения этой цели) и период поддержания (необходимый для сохранения гемоглобина и НСТ в пределах намеченных величин с как можно меньшей вариабельностью). Коррекции доз выполняли каждые две недели в соответствии с реакцией гемоглобина и переносимостью (одноразовую дозу повышали или понижали на 5-20 МЕ/кг). Железо добавляли перорально или внутривенно, в зависимости от статуса железа таким образом, чтобы поддерживать ферритин >150 мкг/л и насыщение трансферрина >20%. Следует отметить, что в этом испытании пациентов подвергали скринингу на присутствие антител против ЕРО, и только два пациента среди 1000 обнаружили присутствие антител. Таким образом, частота встречаемости образования антител при использовании Эпоэтина Омега равна, по-видимому, менее 0,2%.
Фигуры 12 и 13 иллюстрируют изменения в гемоглобине как следствие этого испытания. Изменения НСТ следовали той же самой картине, т.е. имели ту же самую динамику и (относительное) увеличение во время этого испытания. Быстрое повышение гемоглобина наблюдали в обеих группах обработки, но обычно реакция была лучше в группе с s.c.-инъекцией. В противоположность известным реакциям при лечении эпоэтинами Альфа и Бета, не наблюдали латентного периода в реакции на Эпоэтин Омега. Повышение гемоглобина было значимым после первой недели в s.c.-группе и после второй недели лечения в i.v.-группе. Средние величины гемоглобина увеличивались непрерывно на протяжении этого испытания в обеих группах. Увеличение (достигаемое в виде наклона и максимальных средних значений) было более высоким в s.c.-группе. Подробнее, во время первых 4 недель испытания средний гемоглобин в i.v.-группе увеличивался в среднем на 0,4 г/дл на протяжении 2 недель (R=0,98), тогда как наклон в s.c.-группе показал увеличение 0,8 г/дл на протяжении 2 недель (R=0,98). Последующие увеличения среднего гемоглобина замедлялись вследствие уменьшения доз. Во время первых 11 недель средний гемоглобин в i.v.-группе повышался в среднем на 0,3 г/дл на протяжении каждого 2-недельного периода (R=0,97), тогда как наклон увеличения среднего гемоглобина в s.c.-группе показал увеличение 0,4 г/дл/2 недели. Как показано на фигуре 13, это меньшее различие между i.v. и s.c. было обусловлено большими снижениями доз в группе s.c.
Дозы "титрования" были обычно низкими в обеих группах. Однако они были последовательно более низкими в s.c.-группе, чем в i.v.-группе. Максимальная недельная доза "титрования" в i.v.-группе была 106±15 МЕ/кг (неделя 26) и общая средняя недельная доза "титрования" была 96±4 МЕ/кг. В s.c.-группе максимальная недельная доза "титрования" была 95±2 МЕ/кг. Общая средняя недельная доза "титрования" в s.c.-группе была 78±3 МЕ/кг.
Что касается коррекций доз, общие тенденции в изменении доз во время этого испытания отражали терапевтическую реакцию. В i.v.-группе средняя недельная доза "титрования" уменьшалась непрерывно во время первых 7-10 недель испытания, свидетельствуя о быстром и значимом увеличении гемоглобина (требующем снижений доз). Однако, начиная с недели 10, доза "титрования" в i.v.-группе постепенно увеличивалась. Эта тенденция указывает на то, что некоторые пациенты слабо отвечали на лечение и требовали большего времени и большего количества Эпоэтина Омега для достижения цели. Доля пациентов, находящихся все еще на режиме "титрования" на неделе 26, была приблизительно 10%. В противоположность этому, средняя недельная доза "титрования" в s.c.-группе непрерывно уменьшалась во время всего испытания (с некоторыми колебаниями между неделями 7 и 14), что свидетельствовало о лучшей реакции в этой группе. Доля пациентов на режиме "титрования" на неделе 26 в s.c.-группе была <5%.
Изменения недельных доз (фигура 13) указывают на то, что некоторые пациенты достигали целевого значения гемоглобина и, следовательно, начинали введение доз поддержания на неделе 2 в i.v.-группе и неделе 3 в s.c.-группе (возможно, вследствие несколько более низкого фона гемоглобина в s.c.-группе). В общем, в любом конкретном моменте времени во время данного испытания большая доля s.c.-инъецированных, чем i.v.-инъецированных пациентов, находилась на режиме "поддерживающего" введения доз.
Дозы "поддержания" были более низкими, чем дозы титрования, в обеих группах. Средние недельные дозы "поддержания" в i.v.-группе варьировались от <40 МЕ/кг до приблизительно 70 МЕ/кг и общая средняя доза "поддержания" была 70±4 МЕ/кг в неделю. В s.c.-группе средние недельные дозы "поддержания" были между 30 МЕ/кг и 50 МЕ/кг. Общая средняя доза "поддержания" была 49±3 МЕ/кг в неделю (фигура 13). Таким образом, в общем можно утверждать, что доза поддержания Эпоэтина Омега обычно равна приблизительно 30 - приблизительно 70 МЕ на кг в неделю, причем средняя величина находится в диапазоне приблизительно 45 - приблизительно 70 МЕ на кг в неделю. В противоположность этому, типичная доза поддержания Эпоэтина Альфа равна приблизительно 150 - приблизительно 600 МЕ на кг в неделю, причем сообщенная средняя доза в США равна приблизительно 200 - приблизительно 225 МЕ на кг в неделю. Таким образом, можно утверждать, что "средняя" доза Эпоэтина Омега равна приблизительно 55 МЕ на кг в неделю по сравнению со "средней" дозой для поддержания 225 МЕ на кг в неделю для Эпоэтина Альфа. Таким образом, Эпоэтин Омега является на приблизительно 400% более эффективным, чем Эпоэтин Альфа, в достижении одного и того же поддержания гемоглобина/гематокрита у пациента с гемодиализом. Эта разительно более высокая эффективность является совершенно неожиданной при условии, что в медицине обычно различие от 10 до 25% в эффективности класса лекарства рассматривается как достаточно высоко различающееся и делающее новое соединение "отличающимся" и "превосходящим" сравниваемое соединение.
Три другие дополнительные открытые испытания подтвердили эффективность s.c.-вводимого Эпоэтина Омега для анемических ГД-пациентов. Первым было испытание в Словении, которое включало в себя 27 взрослых с гемоглобином ≤8,5 г/дл и НСТ ≤27% на протяжении 11 недель. Вторым было испытание в Македонии, которое включало в себя 22 взрослых с гемоглобином <8,5 г/дл и НСТ <27%. Оба испытания оценивались на протяжении 16 недель. Остальные критерии включения/исключения были стандартными для испытаний rHu EPO. Железо добавляли i.v., в зависимости от ферритина в сыворотке и насыщения трансферрина. В обоих испытаниях начальная доза была 3×30 МЕ/кг в неделю s.c. Дозы корректировали постепенно (одноразовую дозу повышали или понижали на 5-20 МЕ/кг) с 2-недельными интервалами в соответствии с реакцией гемоглобина. Задачей было достижение и поддержание гемоглобина 10,0-12,0 г/дл и НСТ 30-35%. Основные результаты суммированы на фигуре 14 и фигуре 15. Хотя показаны только изменения в гемоглобине, изменения НСТ показывали ту же самую картину.
Фигура 14 показывает результаты испытания в Словении, иллюстрирующие, что средняя величина гемоглобина непрерывно увеличивалась на протяжении 11 недель. Наклон (R=0,98) показал среднее увеличение гемоглобина 0,52 г/дл на протяжении каждого 2-недельного периода. Во время этого периода средняя доза значимо не изменялась. Первые 3 пациента (11,1%) достигали цели в конце недели 3. В конце 6-й недели 54% пациентов достигали цели. После недели 10 только 3 пациента все еще были ниже желаемой цели. Два из них достигали увеличения гемоглобина ≥2,0 г/дл против фона и только один был "слабо отвечающим" (этот пациент не отвечал также на предыдущее лечение Эпоэтином Альфа). Четыре других "слабо отвечающих" на Эпоэтин Альфа пациента реагировали очень хорошо на Эпоэтин Омега (не отличались от остальных пациентов этой группы).
Фигура 15 показывает результаты испытания в Македонии, иллюстрирующие, что средняя величина гемоглобина также быстро и линейно увеличивалась на протяжении первых 10 недель испытания (R=0,98). Этот наклон указывает на увеличение 1,05 г/дл/2 недели на протяжении этого времени. Дозы были очень сходными во время первых 8 недель и затем снижались. Первые 3 пациента (13,6%) достигали целевого уровня гемоглобина к концу недели 3. Половина этих пациентов была "в пределах" целевого диапазона гемоглобина к концу недели 7 и только 5 пациентов (22,7%) были ниже целевого уровня после недели 8 лечения. Только 1 пациент был ниже целевого уровня после недели 10. Все 5 пациентов, которые требовали более 8 недель для достижения цели, имели TSI постоянно <20%. Последний пациент, достигший цели (в конце недели 15), достиг желаемого уровня гемоглобина, только после того, как его TSI повысился выше 20%.
Третьим было открытое испытание в Польше, которое включало в себя 29 пациентов, получавших Эпоэтин Омега на протяжении 24 недель. Фигура 15В иллюстрирует результаты этого испытания, показывающие быстрое увеличение среднего гемоглобина без латентного периода (верхняя панель). Это увеличение было особенно быстрым и линейным во время первых 7 недель (средняя панель) с одновременным снижением требуемой средней недельной дозы Эпоэтина Омега на протяжении периода лечения (нижняя панель). Начальная доза титрования была 3×25 МЕ/кг в неделю и дозы выражены в виде общих недельных количеств. В этом испытании максимальной используемой средней дозой была доза приблизительно 6900 МЕ в неделю, соответствующая дозе около 100 МЕ/кг в неделю или 3×33 МЕ/кг в неделю.
Проводили еще одно испытание, которое было односторонне-слепым, рандомизированным, перекрестным испытанием с двумя 16-недельными параллельными периодами лечения (и 8-недельным "вымыванием" между ними), сравнивающим Эпоэтин Омега и Эпоэтин Альфа. Это испытание включало в себя взрослых ГД-пациентов (возраст 18-80 лет) с гемоглобином <8,5 г/дл и НСТ <27%. Другие критерии включения/исключения были стандартными для клинических испытаний rHu EPO. Пациентов относили к группам, получавшим Эпоэтин Омега или Эпоэтин Альфа в течение 16 недель (30 пациентов в каждой группе) (фаза 1). После "вымывания" Эпоэтин Омега-пациентов переключали на Эпоэтин Альфа и vice versa для последующего 16-недельного периода лечения (фаза 2). Обе фазы этого испытания завершали, но здесь обсуждается только первая фаза. Начальная доза представляла собой s.c.-инъекцию 2×50 МЕ/кг в неделю любого из лекарственных средств. Дозы фиксировали в течение первых 4 недель лечения. После этого дозы корректировали (одноразовую дозу повышали или понижали на 25 МЕ/кг) в соответствии с реакцией гемоглобина и переносимостью. Железо добавляли i.v. для поддержания TSI>30% и ферритина сыворотки >500 нг/л. Целью было доведение уровней гемоглобина до диапазона 10,0-12,0 г/дл и сохранение их в этом диапазоне.
Фигуры 16 и 17 иллюстрируют преимущества Эпоэтина Омега над Эпоэтином Альфа в реакции гемоглобина в зависимости от дозы на протяжении времени. Оба лекарственных средства индуцировали увеличение гемоглобина, но, как показано, между ними было явное различие. Фигура 16 показывает, что уровни гемоглобина были постоянно более высокими (за исключением фона) у Эпоэтин Омега-пациентов. Изменения в гемоглобине были более быстрыми и заметными. Средний гемоглобин повышался во время самой первой недели, тогда как в этом периоде не было действия Эпоэтина Альфа. Во время первых 4 недель (фиксированная доза 2×50 МЕ/кг в неделю) средний гемоглобин у Эпоэтин Омега-пациентов увеличивался на 0,47 г/дл в неделю (в среднем) и на 0,2 г/дл в неделю у Эпоэтин Альфа-пациентов. После этого средний гемоглобин у Эпоэтин Омега-пациентов продолжал быстро увеличиваться (среднее недельное увеличение во время первых 11 недель 0,32 г/дл), хотя средняя доза линейно уменьшалась. Гемоглобин увеличивался также у Эпоэтин Альфа-пациентов, но медленнее (среднее недельное увеличение среднего гемоглобина во время первых 11 недель 0,25 г/дл). Однако доза Эпоэтина Альфа была значительно более высокой в это время - между неделями 5 и 12 средняя недельная доза Эпоэтина Альфа была в 1,2-1,8 раз более высокой, чем доза Эпоэтина Омега.
Значимо более высокие средние уровни гемоглобина достигались в Эпоэтин Омега-группе, и желаемый уровень достигался значительно быстрее (к концу недели 7 против недели 12 в Эпоэтин Альфа-группе). Средний гемоглобин успешно поддерживался выше нижней целевой границы у Эпоэтин Омега-пациентов на протяжении всего испытания. Начиная с недели 13, средняя недельная доза повышалась опять до начальных величин, отражая приращения доз у некоторых пациентов, которые не отвечали на лечение так же заметно, как остальная часть группы. Однако максимальная средняя недельная доза в Эпоэтин Омега-группе не превышала минимальных средних недельных доз в Эпоэтин Альфа-группе. Общая используемая кумулятиная доза Эпоэтина Омега была на приблизительно 1/3 ниже, чем доза Эпоэтина Альфа, т.е. общее количество МЕ, необходимое для лечения 2 пациентов Эпоэтином Альфа, было равно количеству МЕ, требующемуся для лечения 3 пациентов Эпоэтином Омега.
Различия во взаимосвязи доза-эффект между этими двумя лекарственными средствами были даже еще более выраженными при иллюстрации увеличением гемоглобина над фоном и, в частности, в виде отношения увеличение гемоглобина/недельная доза, как показано на фигуре 17. В конце недели 4 (интервала фиксированных доз) это отношение было в 4 раза более высоким у Эпоэтин Омега-пациентов, чем у Эпоэтин Альфа-пациентов, и оно было постоянно значительно более высоким (приблизительно в 1,5-3,5 раза). Площадь под кривой зависимости этого отношения от времени была в 2,3 раза более высокой в Эпоэтин Омега-группе, чем в Эпоэтин Альфа-группе.
Эта фаза испытания продемонстрировала более высокую дозу и преимущества действия Эпоэтина Омега по сравнению с Эпоэтином Альфа. Те же самые преимущества Эпоэтина Омега наблюдали в фазе переключения этого испытания, т.е. где пациенты, которые прежде лечились Эпоэтином Альфа, переключаются на Эпоэтин Омега и vice versa.
Анемия младенцев при преждевременных родах
Эффективность и безопасность Эпоэтина Омега при анемии преждевременных родов исследовали в одном рандомизированном, открытом, имеющем контроль испытании. Основной целью было определение, уменьшает ли введение Эпоэтина Омега необходимость трансфузий эритроцитарной массы. Младенцы в возрасте при рождении <31 недели и с весом при рождении <1500 г допускались для включения в это испытание. Младенцы с основными врожденными пороками, внутричерепным кровотечением, гемолизом, геморрагической полицитемией (венозный Hct≥0,6) и артериальной гипертензией исключались. Пятьдесят недоношенных новорожденных методом случайной выборки относили либо в группу Эпоэтина Омега, либо в контрольную группу. В каждой группе были 2 не учитываемых младенца вследствие повторяющихся инфекций.
Если вес тела при рождении был >1000 г, лечение начинали в постнатальном возрасте >1 недели, в противном случае лечение начинали в 30 недельном гестационном возрасте и продолжали 4 недели, т.е. пока возраст не становился равным 34 неделям гестационного возраста. Лечение включало в себя 3×100 МЕ/кг в неделю Эпоэтина Омега, вводимых s.c., первоначально с 3,0 мг/кг/день трехвалентного железа в пище, затем модифицируемого в соответствии с железом и ферритином в сыворотке (во избежание токсичности железа), витамином Е при 0,5 мг/день перорально, поглощение энергии 460-505 кДж/кг/день. Трансфузии эритроцитарной массы проводили, если требовалось (Hct <35% или 30%, или 20%, в зависимости от уровня вспомогательного дыхания (искусственной вентиляции легких) и клинических симптомов анемии)). Контрольная группа получала такую же обработку, за исключением Эпоэтина Омега. Пациентов внимательно наблюдали в течение 4 недель после лечения и затем наблюдали до 1 года скорректированного возраста. При более длительном последующем наблюдении пациентов оценивали на психомоторное, неврологическое и соматическое развитие.
Фигура 24 иллюстрирует результаты этого исследования. Все получавшие лечение пациенты отвечали хорошо на лечение и не было необходимости введения приращения дозы. Не было различий между группами в отношении поглощения железа, энергии и витамина Е. В фазе предварительного лечения младенцы получали одинаковую трансфузию. Однако только 1 младенец (4,3%) в группе Эпоэтина Омега нуждался в трансфузии PRC (1 единица) во время фазы лечения по сравнению с 8 младенцами (34,8%) в контрольной группе (фигура 24А). Ни один из получавших Эпоэтин Омега пациентов не нуждался в трансфузии при одном месяце последующего наблюдения по сравнению с 5 младенцами (21,7%) в контрольной группе. В целом, во время этих 8 недель только 1 младенец получал 1 единицу PRC в Эпоэтин Омега-группе по сравнению с 13 младенцами в контрольной группе (56,5%) (фигура III-12). Уровни ретикулоцитов были постоянно значительно более высокими в получавшей Эпоэтин Омега-группе (фигура 24В). Площадь под кривой ретикулоциты/время была в 1,45 раз большей у получавших Эпоэтин Омега, чем у контрольных пациентов, и в 8,3 раза большей, если вычитали количество ретикулоцитов, являющееся фоном (в начале лечения). Далее, снижение гемоглобина и Hct (гематокрита) было заметно более выраженным в контрольной группе, чем у Эпоэтин Омега-пациентов. Средние величины гемоглобина и Hct в Эпоэтин Омега-группе были значимо более высокими и постоянно держались выше более нижних желаемых уровней в фазе лечения, чем в контрольной группе (фигура 24С и D). Уровни эритропоэтина в сыворотке были значимо более высокими у получавших Эпоэтин Омега пациентов, чем у контрольных пациентов, в конце периода лечения. Ферритин в сыворотке уменьшался в обеих группах, но это снижение было более ярко выраженным у получавших Эпоэтин Омега младенцев, возможно, вследствие значительно более стимулируемого эритропоэза.
За исключением действия Эпоэтина Омега на эритропоэз, не было различия в другом клиническом или лабораторном тесте между младенцами в этих двух группах обработки. Не наблюдали различий в отношении соматического, неврологического и психомоторного развития до 1 года скорректированного возраста. Анемия новорожденных при преждевременных родах является временной, устойчивой к железу и/или витаминам, многофакторной, но прежде всего гипопролиферативной анемией вследствие абсолютной или относительной недостаточности эритропоэтина и гипореактивности в отношении (низкого) эндогенного эритропоэтина.
В сравнении с испытаниями, включающими в себя тысячи недоношенных младенцев, как Эпоэтин Альфа, так и Эпоэтин Бета также эффективно корректируют анемию недоношенных младенцев, но они требуют существенно более высоких доз, чем Эпоэтин Омега. Что касается эффективной дозы, таблица III иллюстрирует диапазон доз, которые применяли в испытаниях в этом показании с использованием Эпоэтина Альфа или Бета. Доза, используемая в случае Эпоэтина Омега, является более низкой, чем дозы либо Эпоэтина Альфа, либо Эпоэтина Бета, перечисленные в таблице III, которые, как сообщалось, являются более эффективными, чем плацебо. Фигура 24 иллюстрирует высокую и низкую дозы Эпоэтина Альфа, требующиеся для того, чтобы он был эффективным, по сравнению с Эпоэтином Омега. Дозы 300 МЕ/кг в неделю Эпоэтина Омега на протяжении четырех недель (8 недель наблюдения) почти полностью устраняли необходимость трансфузий (только 1 младенец получал 1 единицу). Несомненно, Эпоэтин Омега стимулировал эритропоэз, как показано измерениями ретикулоцитов, гемоглобина и Hct. Эти данные являются сильным доказательством того, что Эпоэтин Омега является более эффективным, чем другие Эпоэтины, для лечения анемии недоношенных младенцев.
Дозы Эпоэтина Альфа и Бета (s.c.), эффективные при анемии недоношенных младенцев
Заключение по данным клинических испытаний
Результаты сравнительных клинических испытаний, обсуждаемых выше, показывают, что имеются несколько преимуществ вводимого s.c. Эпоэтина Омега над Эпоэтином Альфа. В общем, Эпоэтин Омега является более эффективным (более сильнодействующим) в коррекции анемии. Более конкретно, с использованием Эпоэтина Омега увеличение гемоглобина является явно более быстрым, и оно начинается во время первой недели лечения, т.е. не существует "временного лага" между началом обработки и появлением ответной реакции. Более короткое время требуется для достижения желаемых величин гемоглобина. Кроме того, если лекарственные средства вводят в дозах в соответствии с их терапевтической реакцией и переносимостью, с Эпоэтином Омега достигаются более высокие максимальные уровни гемоглобина, чем с Эпоэтином Альфа. Кроме того, значимо лучшие действия на гемоглобин, динамику и абсолютную величину увеличения гемоглобина достигаются со значительно более низкими стандартными дозами Эпоэтина Омега, чем Эпоэтина Альфа или Бета. В целом, что касается коррекции анемии, пациенты требовали приблизительно на одну треть меньше (МЕ/кг) для достижения лучших результатов. Далее, Эпоэтин Омега обладает меньшим действием на кровяное давление и гипертензию, чем Эпоэтины Альфа или Бета.
Таким образом, Эпоэтин Омега значительно отличается по его фармакологическим характеристикам от других эпоэтинов. Кроме того, преимущества такого фармацевтического вещества, как Эпоэтин, характеризуются не только типом проявляемого положительного действия (т.е. увеличения RBC, гематокрита, гемоглобина или поглощения железа), но также присущей ему эффективностью, которая приводит к более низкой биологической нагрузке на организм пациента, и/или соответствующим отсутствием или снижением вредных побочных действий, который могут угрожать жизни пациента или иным образом делать невозможным применение этого фармацевтического средства. Это особенно очевидно в случае гипертензии, которая неблагоприятным образом влияет на риск возникновения тяжелых последствий, таких как инфаркт миокарда или инсульт.
Следующие примеры приводятся для дополнительной иллюстрации аспектов способов данного изобретения, эффектов и преимуществ лечения симптомов у пациентов с использованием Эпоэтина Омега.
ПРИМЕР 1
ПРОЦЕДУРА ВВЕДЕНИЯ ДОЗ ЭПОЭТИНА ОМЕГА ПРИ ЛЕЧЕНИИ АНЕМИИ, СВЯЗАННОЙ С ЗАБОЛЕВАНИЕМ
Следующий протокол представляет типичную процедуру титрования и поддержания для введения терапевтического количества Эпоэтина Омега, которое является эффективным в лечении симптома анемии, связанного с заболеванием, без существенного продуцирования или обострения вредного побочного эффекта.
Эпоэтин Омега обычно готовят в дозах 2000 или 4000 МЕ/мл с фармацевтически приемлемым носителем или разбавителем для подкожной (s.c.) или внутривенной (i.v.) инъекции. Пример носителя или разбавителя в объеме 1 мл может включать в себя: хлорид натрия (NaCl) 8,18 мг, одноосновный фосфат натрия (NaH2PO4×Н2О) 1,56 мг, гидроксид натрия (NaOH) до рН 7,2 и человеческий сывороточный альбумин 1,0 мг.
Начальная доза титрования 50-100 МЕ/кг в неделю (например, 2×30 МЕ/кг в неделю) инициируется и корректируется постепенно, с 2-недельными интервалами, в соответствии с реакцией гемоглобина и переносимостью. Например, отсутствие повышения или небольшое снижение в количестве гемоглобина на протяжении любого 2-недельного периода будет требовать приращения дозы (отдельной дозы, повышаемой максимально на приблизительно 20 - приблизительно 25 МЕ/кг). Слабое увеличение (<0,5 г/дл/каждый 2-недельный период) будет также требовать приращения дозы (но в меньшем количестве). Умеренное увеличение (0,5-1,5 г/дл за 2 недели) не будет требовать коррекций доз, тогда как сильное увеличение гемоглобина (>1,5 г/дл за 2 недели) может потребовать убывания дозы (отдельную дозу снижают максимально на приблизительно 20-25 МЕ/кг).
Процедура введения доз поддержания начинается с дозы на приблизительно на 1/4-1/3 более низкой, чем последняя доза титрования. Эта доза может быть дополнительно уменьшена (с понижением отдельной дозы максимально на 20 МЕ/кг) после продолжительных периодов постоянных уровней гемоглобина или в том случае, если наблюдаются явные тенденции в направлении верхней желаемой границы (увеличение >0,5 г/дл на протяжении каждого 2-недельного периода). Доза должна быть увеличена, если гемоглобин уменьшается ниже нижней желаемой границы (относительно предыдущего уровня), или, если наблюдается явная тенденция снижения, но все еще в пределах желаемого диапазона (снижение гемоглобина >0,5 г/дл на протяжении каждого 2-недельного периода), следует повысить отдельную дозу максимально до 20 МЕ/кг в неделю.
Лечение Эпоэтином Омега следует временно прекращать, если гемоглобин увеличивается слишком быстро (≥4,0 г/дл в каждом 2-недельном периоде) или, если его уровень превышает верхнюю желаемую границу. После этого введение Эпоэтина Омега должно быть возобновлено с дозами, более низкими, вплоть до 50%.
При переключении на Эпоэтин Омега после лечения другими эритропоэтинами должно учитываться более эффективное действие Эпоэтина Омега. Если лечение Эпоэтином Омега должно начинаться сразу же после лечения Эпоэтином Альфа или Бета, дозы должны быть скорректированы, соответственно, в сторону понижения. Например, если Эпоэтин Омега должен вводиться во время поддержания после дозы титрования 3×150 МЕ/кг в неделю Эпоэтина Альфа, введение Эпоэтина Омега должно начинаться при максимуме 60-100 МЕ/кг в неделю s.c., с разделенными на 2 недельными инъекциями. Препарат, содержащий Эпоэтин Омега, может быть включен в набор, содержащий инструкции в этом отношении. Инструкции могут включать, например, ссылочную таблицу, которая сравнивает дозу Эпоэтина Альфа с дозой Эпоэтина Омега для конкретного ряда состояний.
ПРИМЕР 2
ЛЕЧЕНИЕ АНЕМИИ, СВЯЗАННОЙ С ГИПЕРТЕНЗИЕЙ,
ЗАБОЛЕВАНИЕМ СЕРДЦА И РАКОМ
Мужчина 71 года весом 128 фунтов обнаружил застойную сердечную недостаточность, ишемическую (коронарную) болезнь сердца и генерализованный артериосклероз. Кроме того, этот субъект страдает от аденокарциномы легкого и ободочной кишки, имеет железодефицитную анемию и страдает от хронической усталости, наряду с другими симптомами. Рассматриваемый пациент имеет историю сахарного диабета и инфаркта миокарда. Первичное лечение как рака легкого, так и рака ободочной кишки включает в себя резекцию. Пациент является гипертензивным, и проходил лечение ЛАЗИКСОМ и ЛИЗИНОПРИЛОМ по поводу его кровяного давления. При поступлении субъект имел гемоглобин 12,9, гематокритное число 39,6% и число тромбоцитов 213К.
В ходе раковой терапии субъекту вводили Эпоэтин Омега в дозе около 3×2000 МЕ в неделю, что соответствует приблизительно 100 МЕ/кг в неделю при 33 МЕ/кг на одно введение. Не было значимого увеличения в кровяном давлении, не было тромботических событий и ухудшения функции сердца. Реакция этого субъекта показывает, что даже для пациента, имеющего состояния, связанные с раком, которые противопоказаны для лечения Эпоэтином Альфа, т.е. гипертензию, хроническую сердечную недостаточность, коронарную болезнь сердца, применение Эпоэтина Омега не обостряло предсуществующую гипертензию и не производило никаких тромботических осложнений.
ПРИМЕР 3
ЛЕЧЕНИЕ СУБЪЕКТОВ, ИМЕЮЩИХ АНЕМИЧЕСКИЕ СОСТОЯНИЯ,
СВЯЗАННЫЕ С РАКОМ
1. Усталость при раке молочной железы и костном раке
Субъект, жалующийся на хроническую усталость, является женщиной 85 лет весом 125 фунтов с продолжительной историей метастатического рака молочной железы с метастазами в кости, и правое плевральное пространство лечилось в отношении рака с использованием химиотерапевтических лекарственных средств АРЕДИА и АРИМЕДЕКС. Последующее лечение ОКСИКОНТИНОМ приводит к усталости и сомнамбулизму. Кроме того, субъект получает системную лучевую терапию низкого уровня в форме инъекции МАТАСТРОНА (стронция-89). Перед этими лечениями женщина получала первичное лечение карциномы молочной железы наружным облучением вместе с химиотерапевтическими агентами ЦИТОКСАНОМ, АДРИАМИЦИНОМ и МЕГАЦЕ. Эта пациентка страдает от одышки, боли, слабости и усталости, которые обостряются предыдущими способами лечения. Она имела также симптомы одышки и анемии, которые могут быть обусловлены химиотерапией и/или основным заболеванием.
Результаты гематологии показывают, среди прочих показателей, RBC 3,68, гемоглобин 10,6, НСТ 31,9% и тромбоциты при 279 К/мкл. Пациентка начала терапию Эпоэтином Омега приблизительно в 1992 году. Ей вводили 4000 МЕ Эпоэтина Омега (80 МЕ/кг) два-три раза в неделю, наряду с другими терапиями, направленными на подавление распространения рака и удаление жидкостей из плеврального пространства. Спустя несколько месяцев пациентка имела нормальные RBC 5,3 М/мкл (норма равна 4,04-5,48 для женщин), гемоглобин 14,1 г/дл (норма равна 12,2-16,2 для женщин), НСТ 46,37% (норма 37,7-47,9 для женщин) и число тромбоцитов крови 228 К/мкл (норма 142-424). В пределах 2 недель после начала терапии пациентка была визуально более бодрой, не имела больше жалоб на хроническую усталость и имела ослабление одышки. Кроме того, она утверждала постоянно, что ее боль уменьшилась после начала терапии с Эпоэтином Омега. Ее поддерживали на Эпоэтине Омега при дозе от одного до трех флаконов Эпоэтина Омега до времени ее смерти, обусловленной раком, приблизительно через 7 лет после начала лечения Эпоэтином Омега.
2. Анемия, связанная с раком молочной железы
Женщина 40 лет весом 164 фунта не имеет предыдущей истории серьезного заболевания и демонстрирует воспалительную карциному правой молочной железы. Первичное лечение включало химиотерапевтические средства метотрексат, ВИНКРИСТИН, АДРИАМИЦИН и 5-ФУ, вводимые i.v. через портативный катетер, и представляет собой очень агрессивную программу химиотерапии, в том числе максимальное и одновременное введение химиотерапевтических средств. Спустя десять дней после начала терапии пациентка имеет низкий гемоглобин 11,4, низкий НСТ 33,7% и число тромбоцитов 239 К. После этого возникновения анемии пациентка начала лечение Эпоэтином Омега при 150 МЕ/кг в неделю. Дальнейшее лечение продолжалось с использованием режима химиотерапии Marty Abeloff, который включает в себя дополнительно 5-ФУ с последующим введением ЛЕКОВРИНА и ЦИТОТАКСАНА после метотрексата. Женщина получала также колониестимулирующий фактор GM-CSF для увеличения числа лейкоцитов, но он привел к другим вредным побочным эффектам, связанным с комбинированными курсами лечения GM-CSF и химиотерапии.
После месяца вышеуказанного лечения пациентка имеет RBC 3,2, гемоглобин 11,6, гематокрит 35,0 и число тромбоцитов 152К. Во время периода лечения около 3 месяцев пациентка не страдала от гипертензии, а скорее поддерживала стабильное кровяное давление около 110-115/70-75 мм рт.ст. Во время этого 3-месячного периода лечения пациентка показывает увеличение НСТ, которое повышается с 36,5% до 40% или более, и показывает увеличение гемоглобина 11,4, 12,1, и в конце концов достижение уровня гемоглобина 17-19 постоянно в течение последующих месяцев. После продолжающегося лечения дозы Эпоэтина Омега снижали до всего лишь 4000 МЕ каждую третью неделю, пациентка вернулась к нормальным RBC 4,62 М/мкл, гемоглобину 13,4 г/дл, НСТ 41,4%.
Хотя эта пациентка была первоначально кандидатом на развитие анемии злокачественного заболевания, частично из-за агрессивной/одновременной химиотерапии, одновременное лечение Эпоэтином Омега предотвратило развитие в субъекте ожидаемой анемии и фактически поддерживало субъекта при уровнях гемоглобина 17-19, которые выше нормальных уровней. Пациентка также рутинно показывала нормальный уровень НСТ, RBC и гемоглобина на протяжении всего периода лечения. Кроме того, она демонстрировала отсутствие ожидаемой усталости и обычно проявляла улучшенное ощущение благополучия, чем это ожидалось для субъекта, получающего такие курсы лечения.
Действительно, пациентка сообщала, что не было потери аппетита, а был скорее нормальный аппетит; сообщала об отсутствии значительной тошноты и отказывалась от предписываемого обычного лекарства против тошноты. Пациентка сообщала также об исчезновении или снижении телесной боли, связанной с инъекцией Эпоэтина Омега. Эта пациентка позвонила автору изобретения после начального введения доз, чтобы сообщить, что она боится, что ей доставили болеутоляющее средство вместо ЕРО (когда пациентке предоставили действительно именно Эпоэтин Омега). Пациентка сообщила, что боль в ее теле исчезла в пределах получаса после инъекции. Пациентка страдала также от аутоиммунного нарушения системной красной волчанки с артритом и синдромом хронической усталости, сопровождающимся фибромиалгией, который, как сообщила пациентка, симптоматически ослаблялся или устранялся инъекциями Эпоэтина Омега. Действительно, пациентка сообщила, что после начала терапии Эпоэтином Омега она чувствовала себя лучше, имела больше энергии, лучшее настроение и чувство благополучия, чем она имела в любое время на протяжении нескольких предыдущих лет, несмотря на появление агрессивного рака и программы агрессивной химиотерапии, в которую она вступила и которую поддерживала. Несмотря на агрессивную химиотерапию и облучение она постоянно имела энергию и желание совершать прогулки, путешествовать по реке, работать в ее дворе, вести домашнее хозяйство для всей ее семьи, в том числе готовить пищу. Доза вводимого этой женщине Эпоэтина Омега была 4000-8000 МЕ в неделю, и эта доза была намного ниже любой дозы Эпоэтина Альфа, предписываемой для возможного лечения анемии, связанной с химиотерапией. Эта пациентка проходила лечение в то же самое время у того же самого доктора, что и пациентка в клинике, которая получала Эпоэтин Альфа в 6 дозах 4000 МЕ в день, 6 дней в неделю или 36 доз 4000 МЕ в неделю; эта параллельная пациентка имела гемоглобин 10-11. Эта пациентка была единственной пациенткой из 16 пациентов в ее программе, которая не должна была приостанавливать химиотерапию. В данный мемент она не имеет активного рака, как показано медицинскими тестами.
3. Анемия, связанная с мезотелиомным раком
Субъект мужского пола 63 лет весом 170 фунтов был диагностирован как имеющий мезотелиому pleurae lateris dextri (боковой правой плевры). Субъект имел в анамнезе артериальную гипертензию, псориаз и сахарный диабет типа II. В момент поступления субъект имел нормальные RBC 4,93, нормальный НСТ 41%, нормальный гемоглобин 14,2 и нормальное число тромбоцитов 348К и кровяное давление 150/85. Первичное лечение для рака включало химиотерапию цисплатиной. В результате химиотерапии RBC уменьшились до 4,46, гемоглобин понизился до 11,0, НСТ снизился до 36% и тромбоциты снизились до 296. Эпоэтин Омега вводили в дозе около 50 МЕ/кг дважды в неделю на протяжении периода двух недель. Пациент получал также дозу железа перорально при приблизительно 300 мг/день на протяжении лечения Эпоэтином Омега.
В ходе одновременной химиотерапии гемоглобин субъекта поддерживался в нормальном диапазоне около 12-14 г/дл, несмотря на ожидаемую анемию, связанную с химиотерапией с применением цисплатины. Дозу Эпоэтина Омега снижали до 2×25 МЕ/кг два раза в неделю. Кровяное давление пациента поддерживалось при около 150/90 и даже уменьшалось до 140/80 во время короткого периода. В более поздний период дозу химиотерапии удваивали, что приводило к небольшому снижению гемоглобина до 11,8 г/дл, после чего Эпоэтин Омега снова повышали до дозы 2×50 МЕ/кг два раза в неделю. Фигура 21А показывает уровень гемоглобина на протяжении курса химиотерапии, а фигура 21В показывает схему введения Эпоэтина Омега относительно химиотерапии с применением цисплатины. Эти результаты показывают, что низкие дозы Эпоэтина Омега при низких частотах введения являются эффективными в предупреждении анемии, обычно ожидаемой в результате жесткой химиотерапии, такой как химиотерапия с использованием цисплатины, которая, как известно, подавляет дифференцировку эритроидов в эритроциты в виде части ее побочных эффектов.
4. Анемия рака с химиотерапией/одной недельной дозой Эпоэтина Омега
Три пациента в Индии, имеющие раки, являющиеся твердыми опухолями, имели снижение гемоглобина до приблизительно 6,5-8 г/дл, вызываемое, по меньшей мере, частично химиотерапией с использованием цисплатины. После применения один раз в неделю дозы 12000 МЕ Эпоэтина Омега гемоглобин каждого пациента повышался на протяжении периода пяти-шести недель до величины около 12 или более г/дл желаемого уровня гемоглобина. Таким образом, показано, что введение один раз в неделю дозы Эпоэтина Омега является эффективным в лечении анемии онкологии, в частности анемии, связанной с химиотерапией, и более конкретно, с химиотерапией на основе цисплатины. Кроме того, схема введения с низкими дозами была эффективной на протяжении продолжительного периода поддержания, а не просто "уменьшающей" необходимость переливаний крови, лечение Эпоэтином Омега было достаточным для повышения уровней гемоглобина до нормального уровня и поддержания этого уровня в течение всего курса химиотерапии.
ПРИМЕР 4
ЛЕЧЕНИЕ СУБЪЕКТА, ИМЕЮЩЕГО ДИСФУНКЦИЮ ПЕЧЕНИ/ГЕПАТИТ С
Пациентом была женщина 61 года весом 200 фунтов, с 15-летней историей прогрессивно ухудшающейся хронической инфекции гепатита С. Она была прикована к постели, в кислородной палатке, имела печеночную недостаточность терминальной стадии и жаловалась на тошноту, головокружение, задержку жидкости, боль в области живота, диарею и хроническую усталость. Она была не способна принимать пищу или переносить пищу в течение нескольких недель. Она также имеет гипертензию. Принимаемые ею лекарства включают в себя САЛСАЛАТ, НАДОЛОЛ, ПРЕМАРИН, АЛЬДАКТОН, ЭНТЕКС и ПРИЛОСЕК. Пациентка начинает курс лечения Эпоэтином Омега, вводимым при 2000 МЕ (около 22 МЕ/кг) один раз каждые четыре дня. Железо, при приблизительно 300 мг/день также обеспечивается в виде пероральной добавки, а кровяное давление снижают с использованием ЛАЗИКСА и/или ПРЕМАРИНА. Пациентка была почти в терминальном состоянии, прикованной к постели, на кислороде, и лечащие ее врачи предсказывали возможность прожить менее 7-21 дней, причем нарушение/недостаточность печени оценивались приближенно как 90% или более. Эта пациентка страдала также от хронической сердечной недостаточности.
После начала терапии Эпоэтином Омега в пределах 2 дней она могла опять разговаривать, что она была не способна делать в течение нескольких дней перед этим. В пределах 3-4 дней от начала терапии она перестала нуждаться в предоставлении кислорода. В пределах 4-7 дней она встала с постели и вернулась к более нормальной жизни. Пациентка постоянно сообщала, что в течение получаса после инъекции Эпоэтина Омега интенсивная боль, которая была хронической, исчезала из ее тела. Фактически, отсутствие боли длилось около 2-4 дней, и боль опять исчезала после инъекции Эпоэтина Омега.
Во время периода около 7 месяцев лечения Эпоэтином Омега эта пациентка не обнаруживала типа анемии, ожидаемого для ее состояния, т.е. анемии хронического воспалительного заболевания. В противоположность этому, она обнаруживала нормальные RBC 4,11, нормальный гемоглобин 13,4, нормальный НСТ 38,2% и низкое число тромбоцитов 112. Во время лечения Эпоэтином Омега предсуществующая гипертензия, обнаруживаемая пациенткой, поддерживалась на относительно постоянном уровне. В пределах первых двух недель - одного месяца лечения пациентка сообщила о существенном увеличении энергии, возврате к по существу нормальной активности, и имела существенно уменьшенную боль в теле, утверждая, что она не испытывает боли. В пределах 7-14 дней начальной обработки Эпоэтином Омега и со спорным незначимым увеличением гемоглобина пациентка отказалась от дальнейшего лечения кислородом и перестала быть прикованной к постели. В пределах 21-30 дней она вернулась к нормальному стилю жизни, в конце концов смогла провести в качестве хозяйки свадьбу для 200 человек, вернуться к ее хобби - регулярной работе в саду и вернуться ко всем намерениям и целям, к полностью нормальной и активной жизни для пациента ее возраста. Далее, лабораторные анализы подтвердили, что эта пациентка улучшила функцию печени, независимо от повышения ее гемоглобина или RBC. Кроме того, она была способна путешествовать по Соединенным Штатам Америки на автофургоне для осмотра достопримечательностей и посещения родственников и для посещения трассы для автогонок с ремонтной бригадой, которая работала для ее мужа в команде, участвующей в автогонках.
После приблизительно 22 месяцев непрерывного лечения Эпоэтином Омега пациентка поступила в больницу по поводу симптомов, связанных со склерозом печени, вызванным дальнейшим ухудшением функции печени. Заболевание, такое как гепатит, которое является вирусным по природе, продолжает действовать губительным образом на пациентку. Во время поступления она еще обнаруживала нормальные уровни RBC, гемоглобина и НСТ по существу без изменения числа тромбоцитов с того времени, когда эти величины определялись в последний раз. Пациентка прекратила применение Эпоэтина Омега во время нахождения в больнице, где применялись другие терапии для ухудшающегося состояния печени. На протяжении короткого периода времени число RBC упало до 2,99, гемоглобин упал до 10,3, НСТ упал до 29,9 и число тромбоцитов упало со 109 до 93. Пациентка опять жаловалась на повышенную усталость и слабость и этот курс лечения стал терминальным во время этого пребывания в больнице.
ПРИМЕР 5
ЛЕЧЕНИЕ СУБЪЕКТА С НЕЖЕЛАТЕЛЬНЫМ ДЕЙСТВИЕМ ВАСКУЛЯРНОЙ БОЛИ, СВЯЗАННОЙ С ЭПОЭТИНАМИ АЛЬФА И БЕТА, НО НЕ С ЭПОЭТИНОМ ОМЕГА
Женщина 55 лет, имеющая терминальную почечную недостаточность, происходящую из хронического пиелонефрита, страдает от хронической анемии с величинами гемоглобина около 7 г/дл. Пациентка перенесла ранее неудачную трансплантацию почки. После этого ее лечили стандартной дозой 4000 МЕ Эпоэтина Бета три раза в неделю. Хотя гемоглобин пациентки повышался до почти нормальной величины 10 г/дл на протяжении трехмесячного периода лечения, она начала страдать от различных связанных с сосудами жалоб (опухание, покраснение, зуд, спонтанная боль и давящая боль в нижних конечностях, верхних конечностях и локте). Лечение Эпоэтином Бета было прервано и спустя 14 дней эти симтомы улучшились. При возобновлении лечения Эпоэтином Бета пациентка опять жаловалась на те же самые симптомы, требуя прекращения применения Эпоэтина Бета. Прекращение применения Эпоэтина Бета опять сопровождалось ослаблением этих симптомов, однако гемоглобин пациентки упал ниже нормальных уровней.
Приблизительно спустя один месяц после прекращенного применения Эпоэтина Бета пациентке ввели Эпоэтин Альфа в той же самой дозе 3×4000 МЕ в неделю. Пациентка обнаружила улучшение в гемоглобине до 10 г%, но опять испытывала те же самые васкулитные симптомы в пределах 16 дней, требуя прекращения применения Эпоэтина Альфа.
Приблизительно спустя два с половиной месяца после прекращения применения Эпоэтина Альфа пациентке ввели ту же самую дозу 3×4000 МЕ в неделю Эпоэтина Омега. В пределах четырех недель гемоглобин пациентки улучшился до нормальной величины 14,7% и она не испытывала каких-либо вредных побочных эффектов васкулитной боли. После второй трансплантации почки, которая опять была неудачной, пациентка поддерживалась на дозе 3×2000 МЕ Эпоэтина Омега в течение нескольких лет для поддержания стабильного уровня гемоглобина в диапазоне 10-10,6% без каких-либо вредных побочных эффектов. Таким образом, эта пациентка не испытывала вредных побочных эффектов при использовании той же самой дозы Эпоэтина Омега, которую использовали с Эпоэтином Альфа или Бета. Кроме того, доза Эпоэтина Омега могла быть снижена до половины количества, необходимого для получения эквивалентных полезных результатов гемоглобина, получаемых с использованием других препаратов Эпоэтина.
ПРИМЕР 6
ЛЕЧЕНИЕ СУБЪЕКТА ЭПОЭТИНОМ ОМЕГА, КОТОРЫЙ ЯВЛЯЕТСЯ НЕЧУВСТВИТЕЛЬНЫМ К ЭПОЭТИНУ АЛЬФА
Мужчина в возрасте 46 лет страдает от семейного гломерулонефрита и дисплазии коленной чашечки (неполного синдрома Ногтей-коленной чашечки). Почечная гистология с 13-летнего возраста показывала гломерулярное повышенное содержание паренхимных клеток, утолщение базальной капсулы, интерстициальный фиброз, частичную атрофию канальцев и 10-20% гломерулярное гиалиновое перерождение. Была диагностирована почечная недостаточность, и первый диализ проводили в 1993 году. Пациент страдал от гиперлипопротеинемии IIB, артериальной гипертензии, гипертрофии левого желудочка, пониженной диастолической релаксации, перикардиального фиброза, анемии и Lopomata cutis. Пациент имел также один случай слабой сердечной недостаточности.
Вышеописанный пациент участвовал в перекрестном испытании с "вымыванием", в котором сравнивали лечение Эпоэтином Омега с лечением Эпоэтином Альфа хронической анемии, связанной с почечной недостаточностью и гемодиализом. Пациентов рандомизировали для получения Эпоэтина Омега или Эпоэтина Альфа в первой фазе в течение 16-20 недель, с последующим периодом "вымывания", в котором лекарственные средства не вводили в течение некоторого периода, пока уровни гемоглобина не возвращались к анемическим состояниям, существующим перед испытанием, и в это время во второй фазе пациент получал другой эпоэтин из Эпоэтина Омега или Эпоэтина Альфа, который ему не вводили в первой фазе. Это сопровождалось вторым периодом вымывания. В третьей фазе субъекта возвращали к отличающейся или подобной дозе лекарственного средства, используемого в первой фазе. Таким образом, каждый пациент служил в качестве его собственного внутреннего контроля. Начальная доза для любого из эпоэтинов была 2×50 МЕ/кг в неделю. Дозы фиксировали во время первых 4 недель периода титрования и затем увеличивали на 25 МЕ/кг, уменьшали на такое же количество или оставляли неизмененными в зависимости от коррекции, необходимой для поддержания гемоглобина в желаемом диапазоне 10-12 г/дл.
Вышеуказанный пациент начал лечение Эпоэтином Омега в первой фазе. Как показано на фигуре 18А, реакция на Эпоэтин Омега была исключительно хорошей, гемоглобин повышался от низкого фона 7,4 и достигал желаемого уровня в пределах 4 недель (18А, средняя панель). Дозу снижали до 2×25 МЕ/кг в неделю для 6 следующих недель, затем опять корректировали до нуля Эпоэтина Омега в течение конечного периода 4 недель (18А, верхняя панель, величины выражены в виде общего числа МЕ в неделю для этого индивидуума с весом 80 кг). Тем не менее, несмотря на снижение Эпоэтина Омега до нуля во время последнего месяца первой фазы, пациент поддерживал уровни гемоглобина в желаемом диапазоне в течение этой фазы испытания. Как показано в нижней панели фигуры 18А, систолическое кровяное давление, которое было границей для гипертензии, т.е. при 140-160 мм рт.ст., было неизмененным или фактически снижалось во время этого периода лечения Эпоэтином Омега.
После первого периода вымывания в течение нескольких месяцев гемоглобин пациента возвращался до 7,4 г/дл, и вторую фазу начинали с использованием той же самой дозы, но Эпоэтина Альфа, как показано на фигуре 18В (верхняя панель). Этот пациент не был чувствительным к Эпоэтину Альфа, как иллюстрируется отсутствием достижения желаемого уровня гемоглобина (18В, средняя панель) в течение всей продолжительности этого испытания, которое включало в себя увеличение доз Эпоэтина Альфа до 2×75 МЕ/кг в течение 5 недель с последующим вторым увеличением до 2×100 МЕ/кг и затем, наконец, до 2×125 МЕ/кг в неделю в последние две недели испытания. Пациент не только не реагировал, но и, в сильном контрасте с лечением Эпоэтином Омега, систолическое кровяное давление этого пациента повышалось существенно выше нормального до увеличения на 30 мм рт.ст. во время периода лечения, что приводило пациента в гипертензивное состояние в течение нескольких периодов во время этого лечения.
После второго периода вымывания пациента опять лечили Эпоэтином Омега в фиксированной дозе 1×100 МЕ/кг один раз в неделю, как показано на фигуре 18С (верхняя панель). Наблюдали немедленное и стойкое повышение уровня гемоглобина, которое было линейным на протяжении 12-недельного периода лечения, достигая почти нормального уровня приблизительно 10 г/дл, как показано на фигуре 18С, средняя панель. Опять в сильном контрасте с эффектами Эпоэтина Альфа, систолическое кровяное давление пациента фактически скорее снижалось, а не увеличивалось, как показано на фигуре 18С, нижняя панель. Эти результаты показывают, что некоторые пациенты, которые не реагируют на Эпоэтин Альфа, могут фактически удивительным образом отвечать на Эпоэтин Омега. Это показывает также, что Эпоэтин Альфа может существенно способствовать увеличению кровяного давления, даже давая низкую реакцию или при отсутствии реакции увеличения уровней гемоглобина. Далее, эти данные ясно указывают на то, что Эпоэтин Омега имеет непосредственную терапевтическую пользу, даже при введении в виде инъекций один раз в неделю при уровне доз, не дающих хорошей реакции с Эпоэтином Альфа.
ПРИМЕР 7
ПРИМЕНЕНИЕ ЭПОЭТИНА ОМЕГА В ОПЕРАЦИОННОЙ ПРОЦЕДУРЕ ДЛЯ ПРЕДУПРЕЖДЕНИЯ АНЕМИИ И ОБЕСПЕЧЕНИЯ ТРАНСФУЗИИ АУТОЛОГИЧНОЙ КРОВИ
Эпоэтин Омега использовали для лечения неанемических пациентов, подвергающихся селективной ортопедической хирургии в рандомизированном открытом (с известными группами) испытании с контролем. Пациентов лечили Эпоэтином Омега при 2×50 МЕ/кг в неделю в течение четырех недель s.c. перед хирургическим вмешательством и дополнительно вводили 2×100 мг железа в неделю i.v. Контрольных пациентов лечили только железом в течение того же самого периода. Целью было обеспечение получения 3 единиц донорской крови (3×500 мл) во время предоперационной процедуры и предупреждение того, чтобы пациент стал анемичным перед хирургическим вмешательством (т.е. для предотвращения снижения гемоглобина до <10 г/дл). Взятие крови было возможным только в том случае, если гемоглобин был ≥11,0 г/дл. Хирургия планировалась в конце недели 4 этого испытания. Кровь брали по понедельникам и точки измерения на гематологические параметры были по понедельникам и вторникам предоперационно, 2-3 дня после хирургии и снова спустя 14 дней после хирургии (при выписке). Полученную кровь использовали для аутологичной трансфузии во время хирургического вмешательства.
Фигуры 19А и В показывают величины гемоглобина индивидуумов во время испытания для получавшей Эпоэтин Омега и контрольной групп, соответственно. Некоторые из контрольных пациентов имели гемоглобин менее 11,0 г/дл, и, следовательно, были не способны отдавать планируемое количество крови. В противоположность этому, все получавшие Эпоэтин Омега пациенты были способны отдавать всю кровь, которая планировалась. Далее, несколько из контрольных пациентов были анемическими перед хирургией (но ни один из получавших Эпоэтин Омега пациентов) и некоторые становились зависимыми от переливания крови, т.е. имели гемоглобин ≤9,0. Кроме того, скорость снижения гемоглобина была существенно более высокой в контроле по сравнению с получавшими лечение пациентами. Фигуры 19С и D показывают, что, хотя гемоглобин снижался линейно на протяжении этого испытания в обеих группах, как в периоде, приводящем к хирургии (фигура 19D), так и во всем периоде, включающем постоперационный период (фигура 19С), скорость снижения гемоглобина была заметно более крутой в контрольной группе. Фигуры 20С и D показывают число RBC и ретикулоцитов, соответственно, для среднего из получавших Эпоэтин Омега пациентов по сравнению с контрольной группой и показывают значимое превосходство для группы лечения над контрольной группой. Фигура 20D показывает, что для среднего всех пациентов, получавших лечение, или пациентов в контрольной группе общий уровень железа в сыворотке (TSI) получавших лечение пациентов был значимо более низким, чем в контрольной группе, что свидетельствует о явном увеличении эритропоэза, даже хотя основное условие, обычно ожидаемое для применения других эпоэтинов, не удовлетворялось, т.е. более высокие уровни TSI. Эти эффекты наблюдали с использованием дозы Эпоэтина Омега, которая была значительно более низкой, чем доза, требуемая для лечения другими эпоэтинами.
Предыдущее описание и примеры приводятся в качестве иллюстрации и не предназначены для ограничения объема данного изобретения. Специалисту с обычной квалификацией в данной области будет вполне понятно, что данное изобретение может осуществляться разными путями, которые исходят из данного изобретения без отклонения от идеи и объема данного изобретения, ограничиваемого только прилагаемой формулой изобретения.
ПРИМЕР 8
ПРИМЕНЕНИЕ ЭПОЭТИНА ОМЕГА ДЛЯ ЛЕЧЕНИЯ АНЕМИИ ХИМИОТЕРАПИИ/ЛУЧЕВОЙ ТЕРАПИИ, КОГДА ЭПОЭТИН АЛЬФА НЕ ФУНКЦИОНИРУЕТ
Пациентку, страдающую от злокачественного рака молочной железы, метастазировавшего в лимфатические узлы, лечили CMF (метотрексатом), 5ФУ и НАВАЛБИНОМ в качестве химиотерапии вместе с суточными дозами НЕЙПОГЕНА и тремя недельными дозами Эпоэтина Альфа. НЕЙПОГЕН был успешным в поддержании низкого-нормального числа лейкоцитов, но Эпоэтин Альфа не мог поддерживать достаточное число RBC, которое падало до "диапазона паники" 2,06, и были необходимы трансфузии. Пациентку переключали на Эпоэтин Омега, инъецируемый s.c. два-три раза в неделю в дозе около 60 МЕ/кг на одно введение. Спустя один месяц пациентка имела достаточную силу, чтобы подвергаться наружному облучению легких в течение периода 9 недель. Пациентка продолжала получать Эпоэтин Омега во время и после курса облучения и во время последующего лечения МУТАМИЦИНОМ. Во время курса облучения и после этого уровни RBC, НСТ и гемоглобина оставались в низком-нормальном диапазоне. Пациентка сообщала об ощущении нормальной бодрости и улучшении отношения к будущему из-за лечения Эпоэтином Омега перед лучевой терапией, и сообщала также, что это улучшенное отношение является причиной ее решения продолжать лучевую терапию и последующую химиотерапию. Действительно, пациентка вновь стала играть в теннис и могла играть два сета в теннис в занятии в один и тот же день. Спустя шесть месяцев после начала лучевой терапии и последующей химиотерапии оценки RBC пациентки были нормальными, и не было данных об опухолевых маркерах или опухолевой ткани согласно КАТ-скану (компьютерной аксиальной томографии). Пациентка продолжала химиотерапию один раз в две недели и продолжала получать Эпоэтин Омега в дозе около 60 МЕ/кг три-пять раз в неделю в течение по меньшей мере трех месяцев после КАТ-сканирования и поддерживала нормальные числа RBC и продолжала сообщать о позитивном психическом самочувствии, хорошем настроении, которые она имела и связывала с применением Эпоэтина Омега во время пролонгированной раковой терапии.
ПРИМЕР 9
ПРИМЕНЕНИЕ ЭПОЭТИНА ОМЕГА ДЛЯ ЗДОРОВОГО СУБЪЕКТА
Мужчина 51 года является администратором фармацевтической компании, страдал в течение более десяти лет от CFS, хронической фибромиалгии и мышечной боли, в том числе васкулярной боли, обычно более тяжелой в бедрах и нижних конечностях и в руках, особенно предплечьях. Этот субъект имел все время нормальный гемоглобин и нормальное число RBC. Отражая Японскую философию служащего компании, использующего, по меньшей мере, один раз изготовляемое компанией лекарство, он сам вводил Эпоэтин Омега s.c. на кг веса (40 МЕ/кг). Во время менее чем 5 минут, после введения генерализованная боль в мышцах и ткани субъекта, в том числе в ногах и руках, полностью исчезала. Такое явление было спонтанным и немедленным и, следовательно, не было связано с каким-либо увеличением гемоглобина или числа эритроцитов. Это устранение боли, как сообщалось, длилось в течение 4-6 дней и постепенно прекращалось после дня 4, пока это болезненное состояние не возвращалось в день 8. В 12 или большем числе случаев этот пациент сам вводил Эпоэтин Омега в отдельной дозе 4000 МЕ с повторяющимися успешными результатами значительного или полного устранения боли тела/мышц/ткани. Также этот пациент сообщает о сходных улучшениях в "настроении" и чувстве "благополучия". Кроме того, этот пациент был погранично гипертензивным в течение 20 лет с нижним кровяным систолическим давлением в диапазоне от 95 до 105. После введения Эпоэтина Омега не было никакого увеличения кровяного давления, которое наблюдалось ежедневно. Это сообщение согласовалось с сообщением пациентки в примере 3, которая сообщила при начальном применении, что она подумала, что ей дали "болеутоляющий укол" "по ошибке", так как ее телесная боль, происходящая из хронического заболевания и рака, утихла в течение минут после введения Эпоэтина Омега. В том случае она продолжала на протяжении месяцев лечение Эпоэтином Омега с сообщениями рутинного уменьшения или устранения телесной боли при введении Эпоэтина Омега.
Неожиданно было обнаружено также, что эритропоэтины, в частности Эпоэтин Омега и родственные формы, как описано выше и заявлено в прилагаемой формуле изобретения, пригодны для лечения и/или предупреждения типичных форм "джет-лэга" (нарушения суточного ритма организма в связи с перелетом через несколько часовых поясов (на реактивном самолете), например, после трансатлантического или пересекающего Тихий Океан полетов. Симптомами джет-лэга являются утомление, усталость, отсутствие концентрации и другие нарушения автономной нервной системы, связанные с джет-лэгом (дисритмия). Нормально, симптомы джет-лэга длятся в течение 3-7 дней, перед тем как организм адаптируется к отличающейся временной зоне, с которой он столкнулся.
Введение обычно 25-30 МЕ эритропоэтина на кг веса тела заранее или после появления симптомов джет-лэга подавляет или в значительной степени устраняет такие симптомы. Введение в пределах 48 часов после прибытия в место назначения дает наилучшие результаты. Обычно достаточными являются одно-три введения с интервалом 24-72 часа. Конечно, эритропоэтины являются также активными против других форм дисритмии.
Еще одной областью активности эритропоэтинов, в частности, Эпоэтина Омега и его родственных форм, является лечение хронических сердечных состояний, таких как хроническая сердечная недостаточность или сердечная недостаточность. Неожиданно, Эпоэтин Омега показал гораздо большую активность и меньше побочных эффектов, чем Эпоэтин Альфа.
Эритропоэтины широко использовались для лечения пациентов с почечной недостаточностью. Почечная недостаточность часто сопровождается сердечной недостаточностью и является одной из ведущих причин смерти для таких пациентов. То же самое относится к недиализным диабетическим пациентам. По-видимому, центральную роль играет определенный тип гипертензии.
Известно, что Эпоэтин Альфа, вследствие его тенденции увеличивать кровяное давление, противопоказан гипертензивным пациентам. Теперь было обнаружено, что введение Эпоэтина Омега в диапазоне доз 10-200 МЕ на кг веса тела в значительной степени уменьшает симптомы, такие как усталость, одышка, задержка воды, пациентов, страдающих от застойной сердечной недостаточности, позволяя им вернуться к нормальной или почти нормальной жизни. Все получавшие это лечение пациенты подтверждали большое улучшение, как их состояний, так и самочувствия. Во всех случаях значительно или очень сильно увеличивалась способность к физической нагрузке.
Активность Эпоэтина Омега против хронической сердечной недостаточности не ограничивается случаями, в которых пациент страдает от почечной недостаточности, диабета и/или анемии. По-видимому, это лекарственное средство является активным со многими различными формами хронической сердечной недостаточности и со всеми классами. Было показано, что возможным является долгосрочное лечение, и оно не имеет побочных эффектов, которые были обнаружены с Эпоэтином Альфа.
Формами хронической сердечной недостаточности, которые могут лечиться Эпоэтином Омега, являются, например, рецидивирующая острая сердечная недостаточность, ишемическая сердечная недостаточность, латентная сердечная недостаточность, первичная сердечная недостаточность и относительная сердечная недостаточность, а также формы сердечной недостаточности, связанные с другими заболеваниями и/или терапией заболеваний.
ПРИМЕР 10
ПРИМЕНЕНИЕ ЭПОЭТИНА ОМЕГА ДЛЯ ЛЕЧЕНИЯ ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ
Пациент - женщина 82 лет находилась в больнице с застойной сердечной недостаточностью IV степени, связанной с клапанной кардиомиопатией с 4+ регургитацией митрального клапана. Ее лечили с использованием полной программы медикации с предполагаемой очень органиченной жизнью. В то время она имела гемоглобин в диапазоне 10-11.
Спустя полгода пациентка развила значительное падение гемоглобина до диапазона 8,3-8,7, которое ухудшило и дестабилизировало ее легочно-сердечный статус.
После лечения 4000 МЕ Эпоэтина Омега, вводимого три раза в неделю, ее гемоглобин отвечал увеличением до максимума 13,8. Для поддержания лекарственной терапии для этой пациентки дозу уменьшали до 2000 МЕ три раза в неделю, и ее гемоглобин установился при 11.
Параллельно повышению гемоглобина до нормальных диапазонов сердечный шум пациентки по существу исчез, ее способность к физической нагрузке очень сильно увеличилась, и она была способна вернуться к нормальной жизни с регулярной лекарственной терапией с использованием Эпоэтина Омега. Состояние пациентки было улучшенным и более стабильным, чем при обычной лекарственной терапии для застойной сердечной недостаточности.
Приведенные выше примеры даются только в качестве иллюстрации и не предназначены для ограничения объема данного изобретения, который ограничивается только прилагаемой формулой изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАКОКИНЕТИЧЕСКОЕ И ФАРМАКОДИНАМИЧЕСКОЕ МОДЕЛИРОВАНИЕ ВВЕДЕНИЯ ЭРИТРОПОЭТИНА | 2000 |
|
RU2248215C2 |
| КОМПОЗИЦИИ ФОРБОЛОВЫХ ЭФИРОВ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ ДЛЯ ЛЕЧЕНИЯ ИЛИ УМЕНЬШЕНИЯ ПРОДОЛЖИТЕЛЬНОСТИ ЦИТОПЕНИИ | 2015 |
|
RU2730998C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ Эритропоэтина | 2000 |
|
RU2225221C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ АНЕМИИ | 2014 |
|
RU2705206C2 |
| ИСПОЛЬЗОВАНИЕ ЛХАТ ДЛЯ ЛЕЧЕНИЯ АНЕМИИ И ДИСФУНКЦИИ КРАСНЫХ КРОВЯНЫХ КЛЕТОК | 2010 |
|
RU2576838C2 |
| КОМБИНИРОВАННОЕ ПРИМЕНЕНИЕ ЛОВУШЕК GDF И АКТИВАТОРОВ РЕЦЕПТОРОВ ЭРИТРОПОЭТИНА ДЛЯ ПОВЫШЕНИЯ СОДЕРЖАНИЯ ЭРИТРОЦИТОВ | 2010 |
|
RU2592670C2 |
| Способ коррекции анемии у зависимых от трансфузий эритроцитов больных бета-талассемией | 2023 |
|
RU2820878C1 |
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ 15-HEPE, ДЛЯ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ ГЕМАТОЛОГИЧЕСКИХ НАРУШЕНИЙ И/ИЛИ СВЯЗАННЫХ ЗАБОЛЕВАНИЙ | 2020 |
|
RU2833560C1 |
| ПРИМЕНЕНИЕ СТАБИЛИЗАТОРОВ HIF-АЛЬФА ДЛЯ УСИЛЕНИЯ ЭРИТРОПОЭЗА | 2004 |
|
RU2414214C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ И/ИЛИ ПРЕДОТВРАЩЕНИЯ СЕРДЕЧНО-СОСУДИСТОГО ЗАБОЛЕВАНИЯ | 2011 |
|
RU2606853C2 |
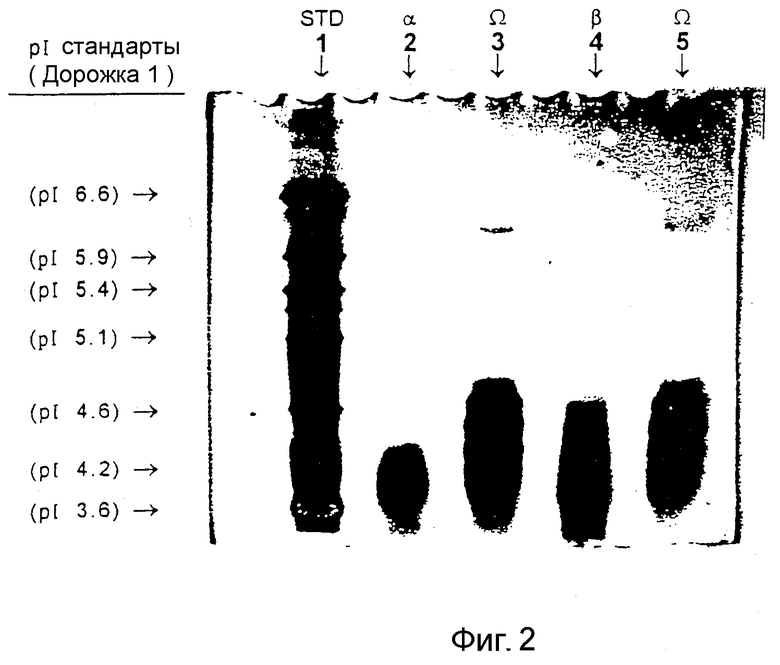
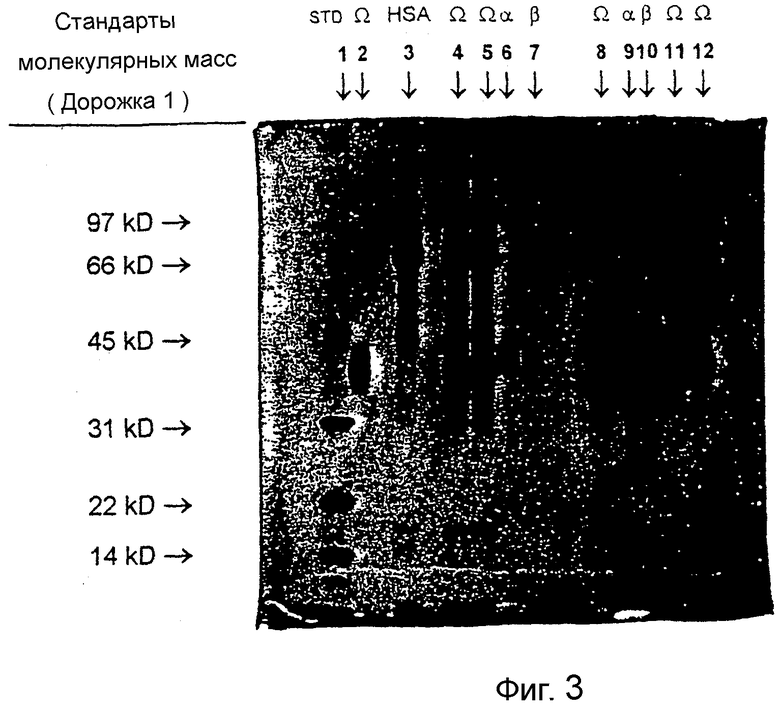
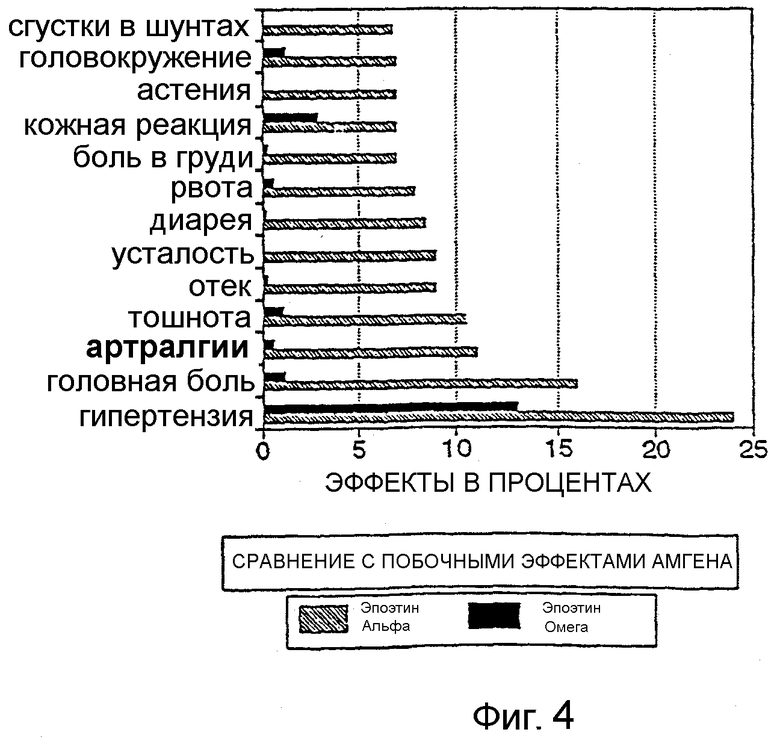
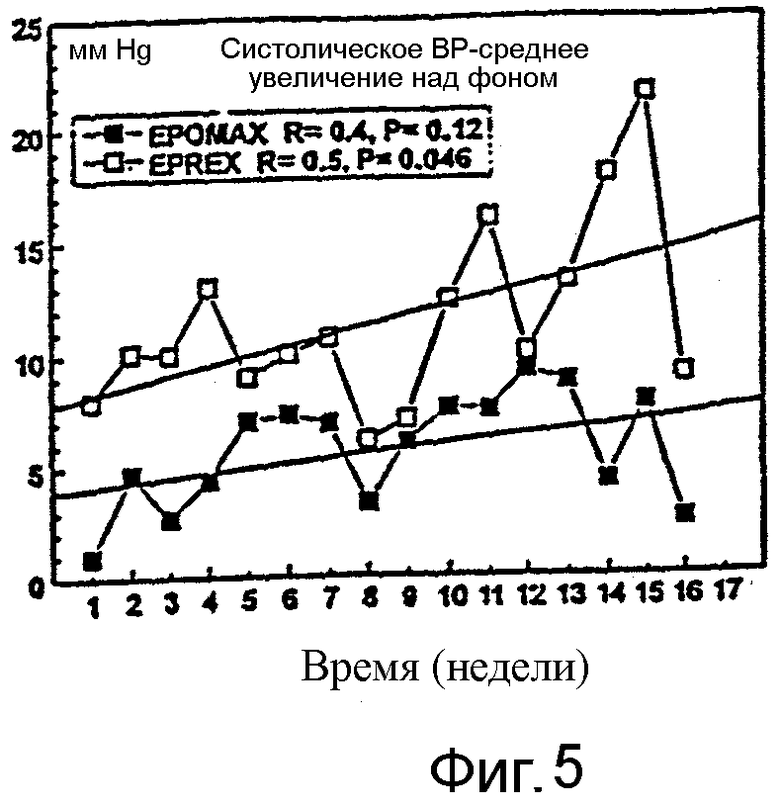
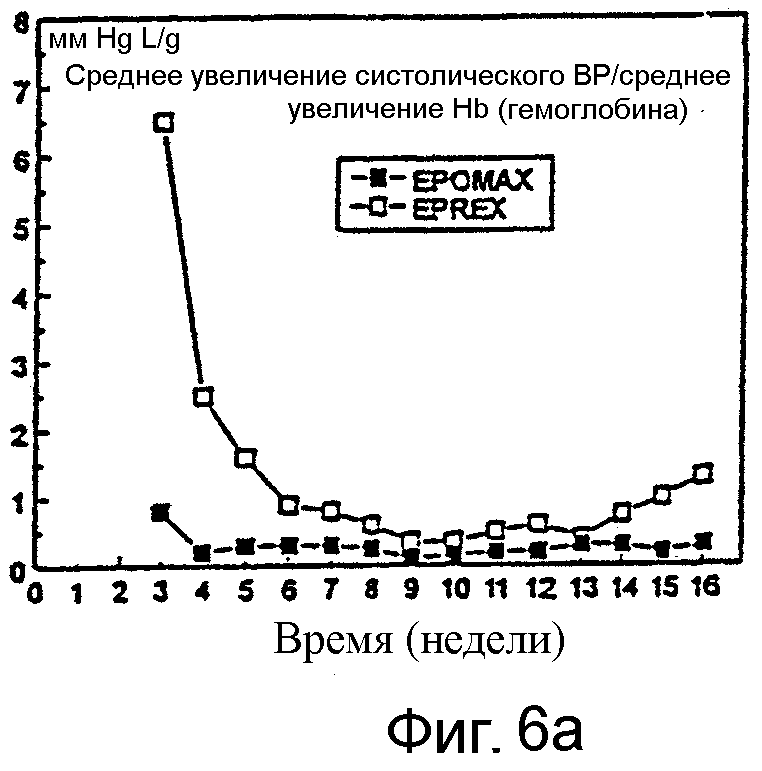
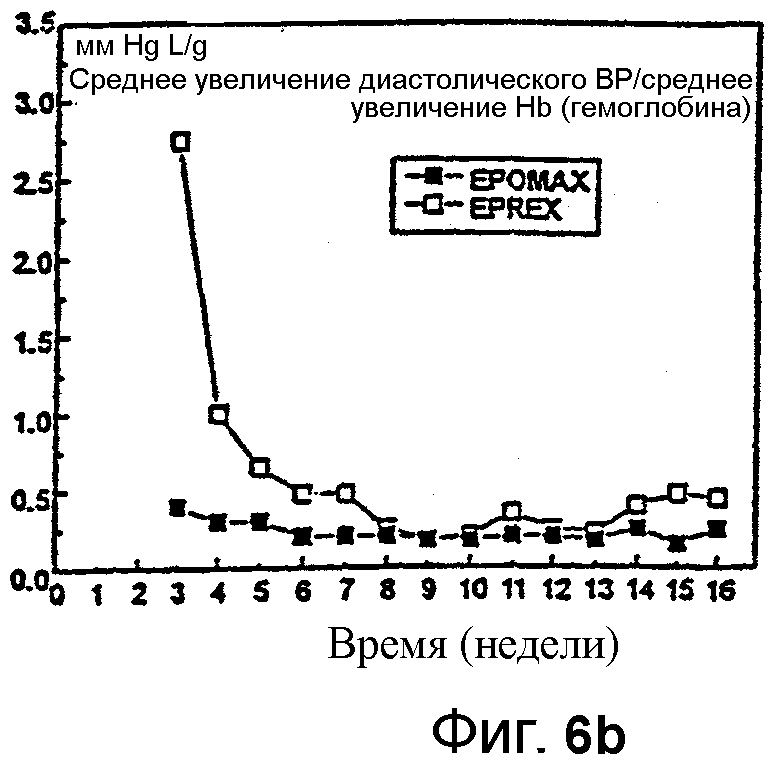
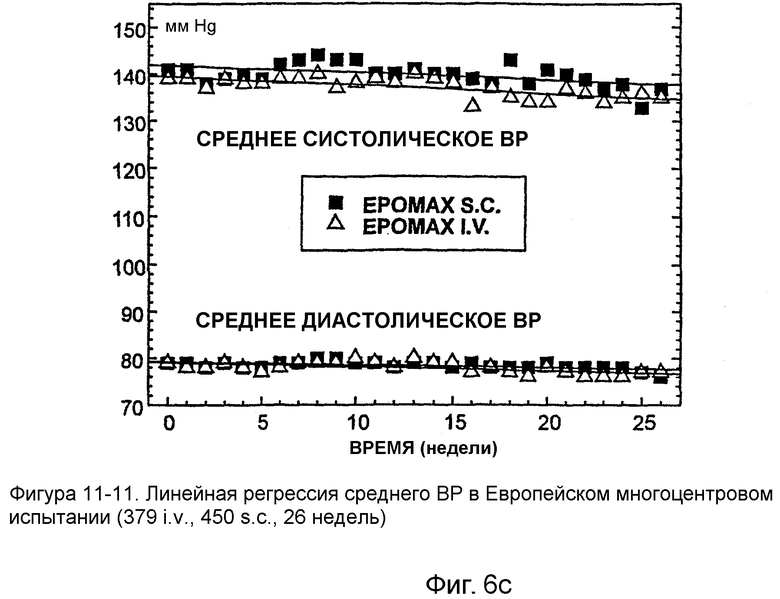
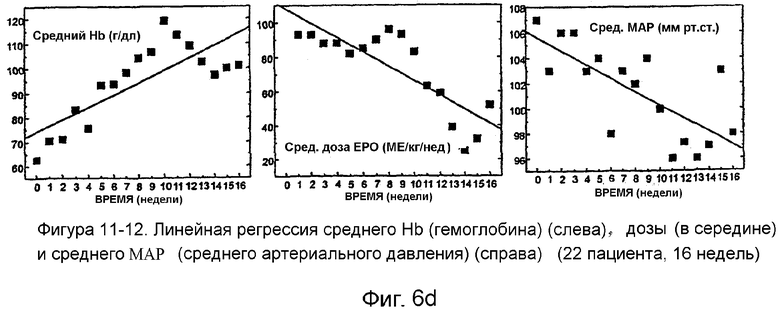
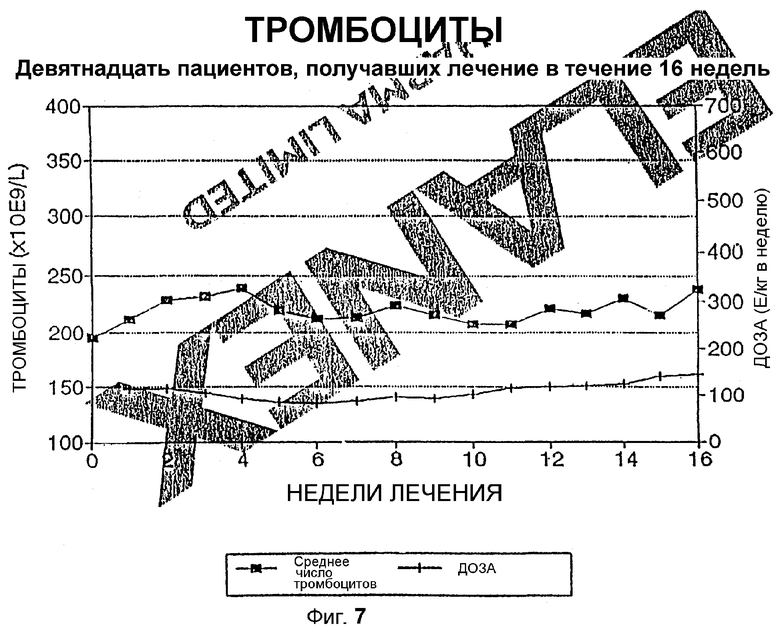
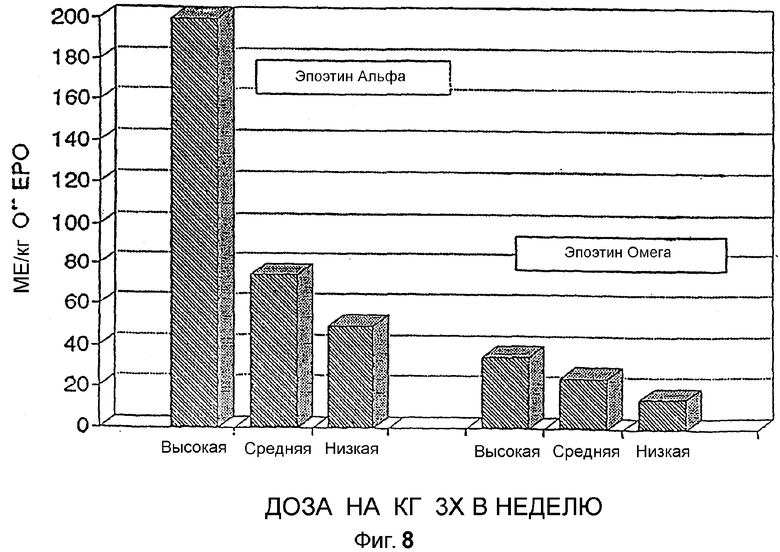
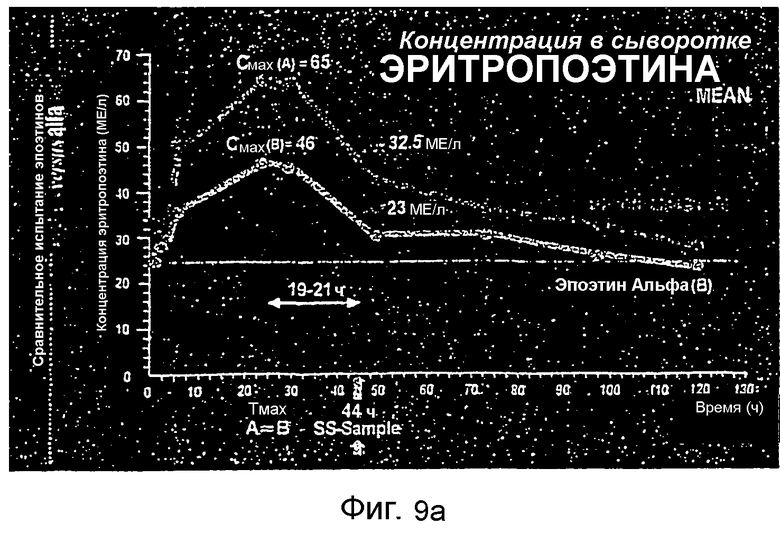
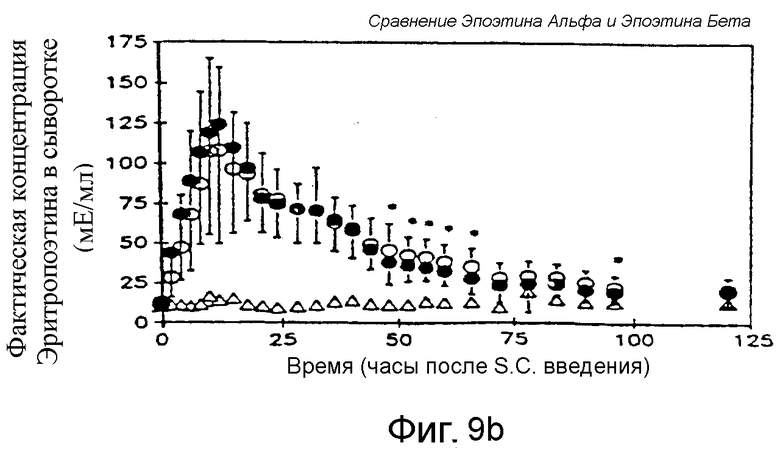
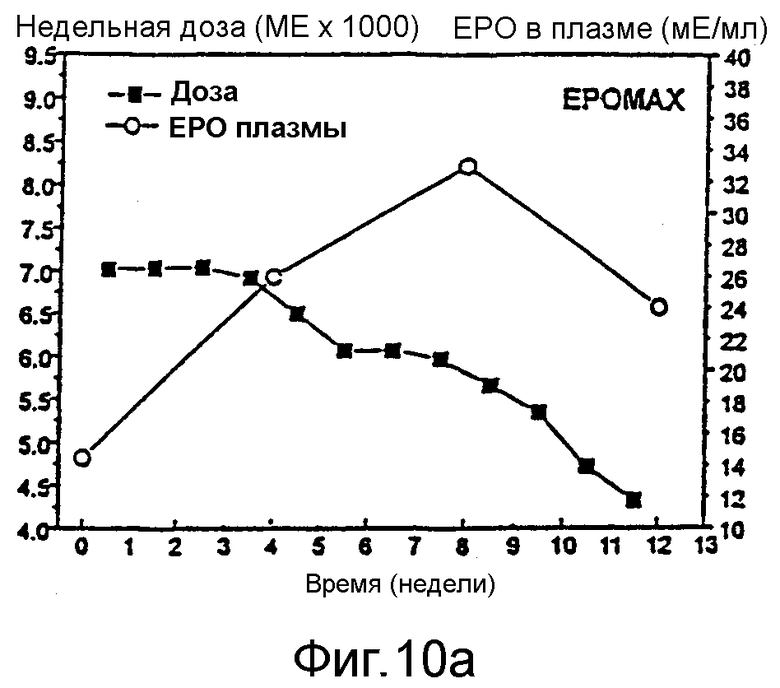
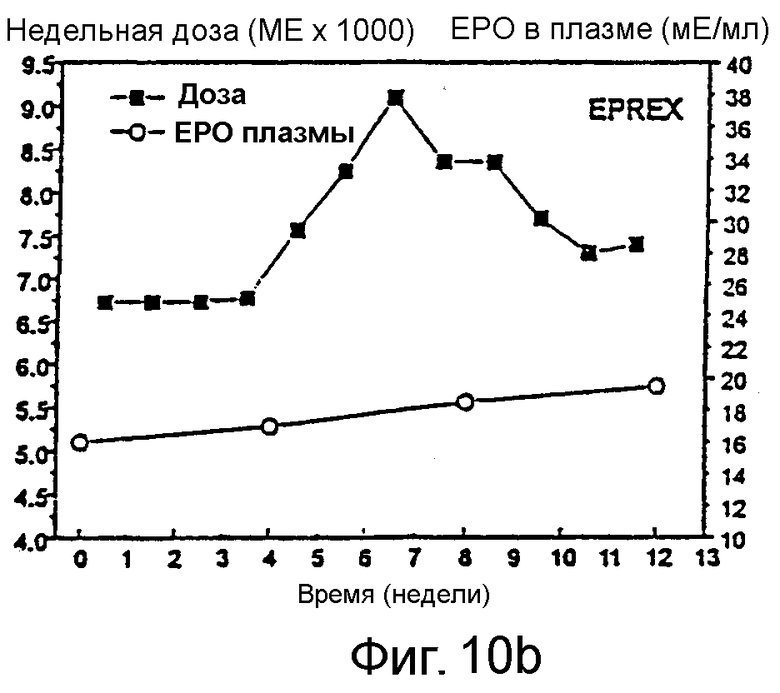
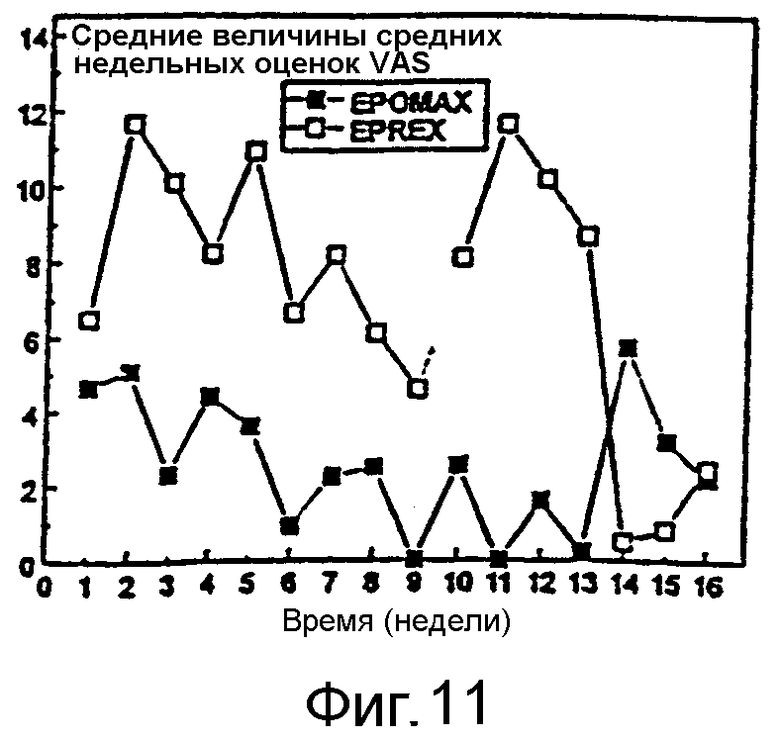
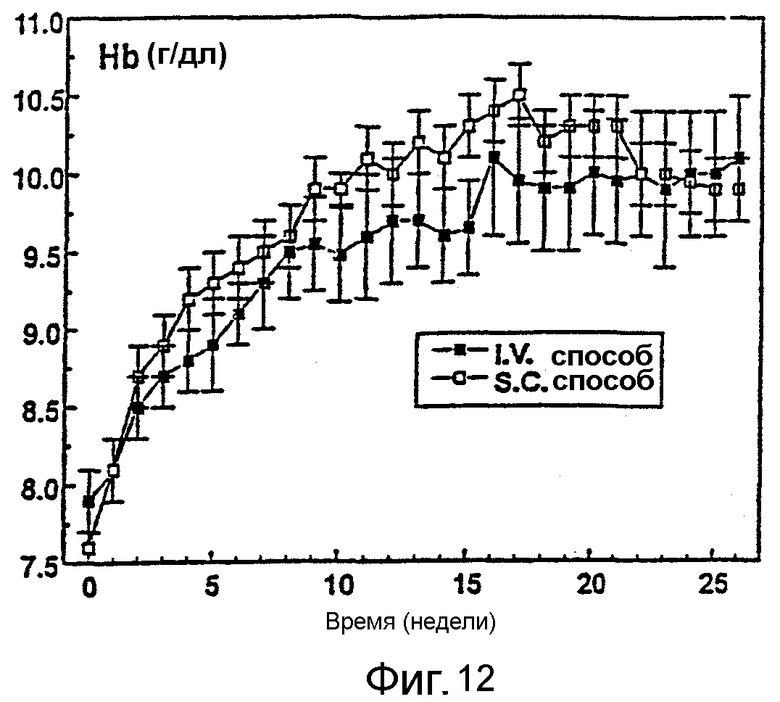
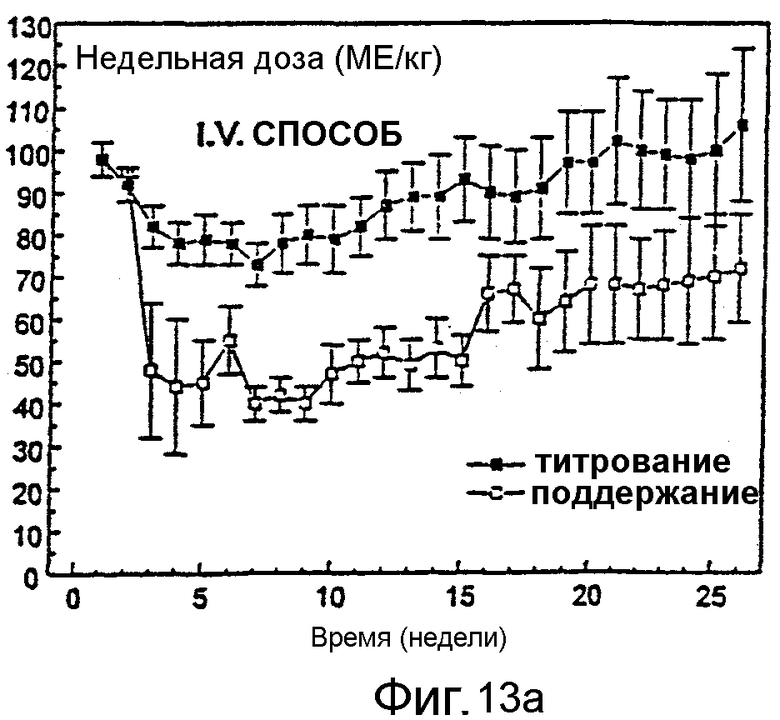
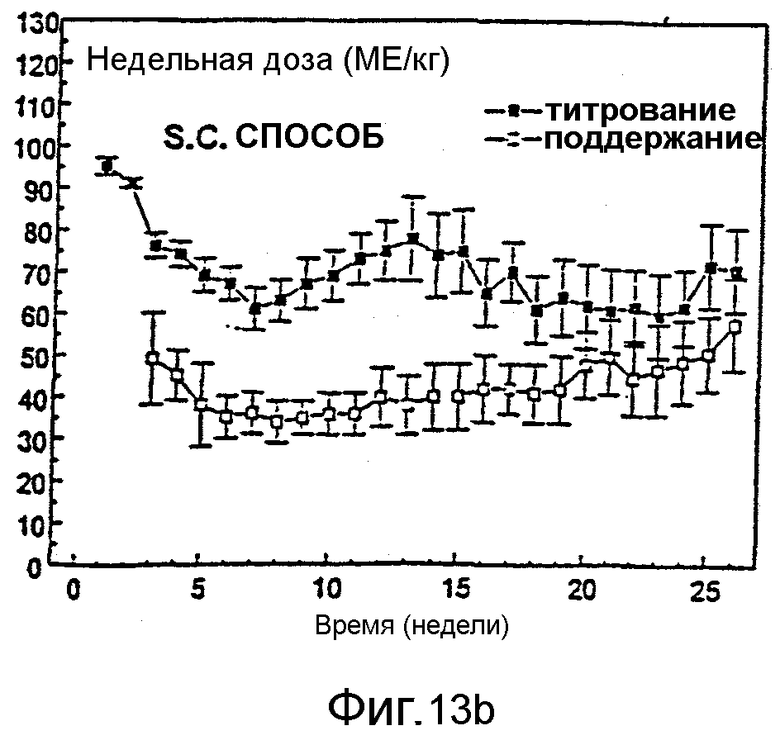
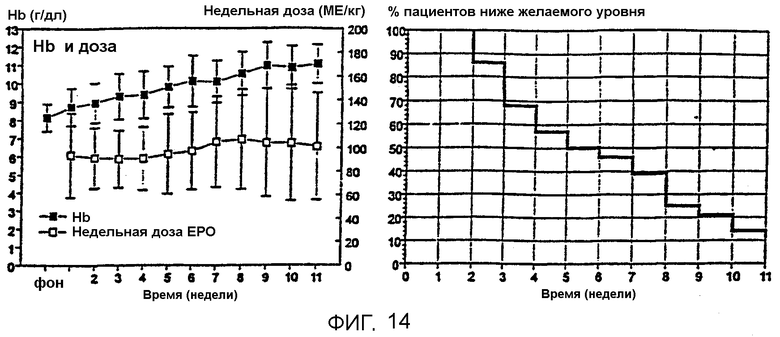
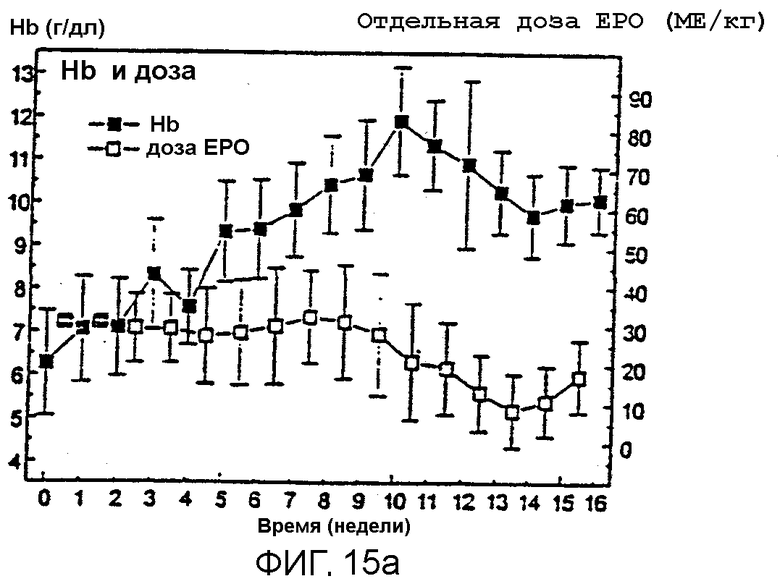
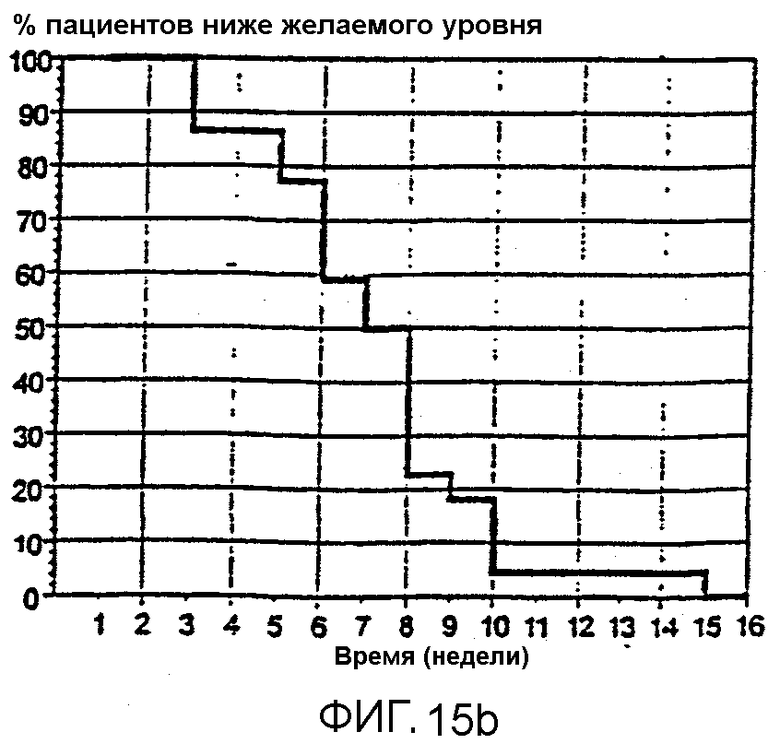
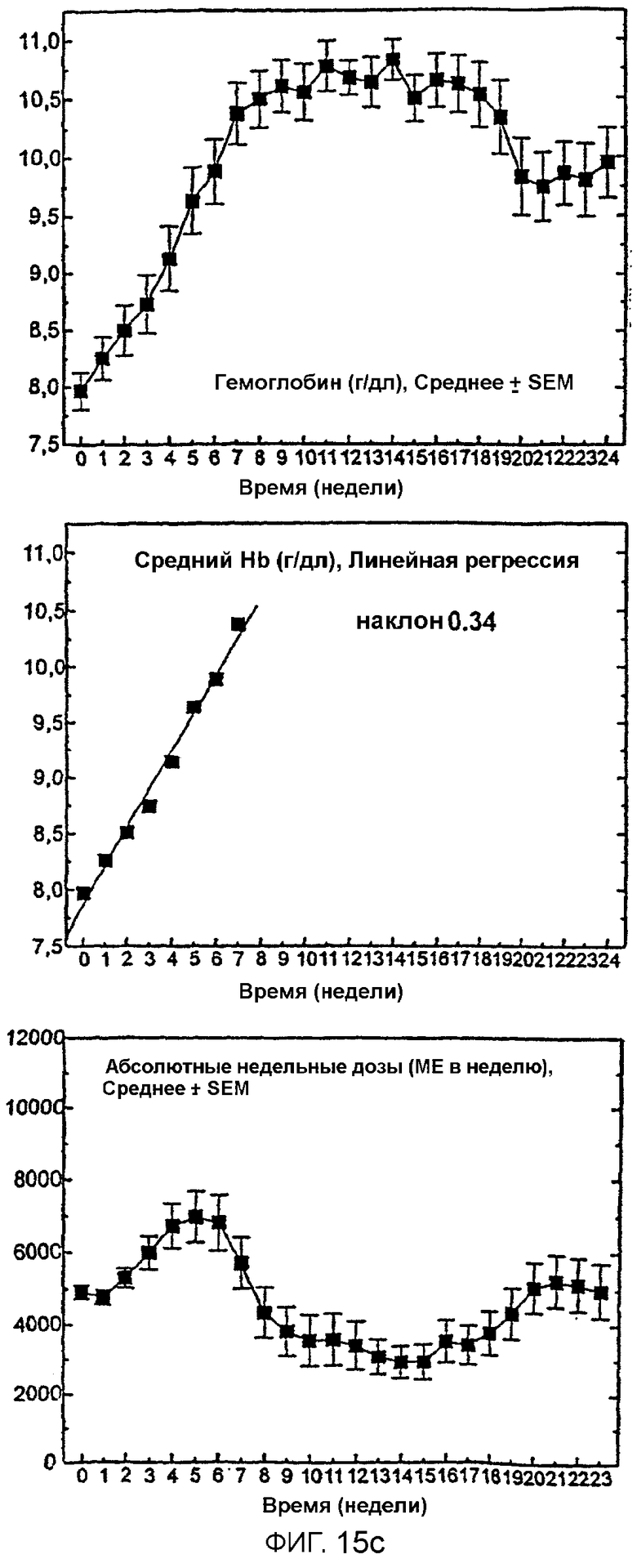
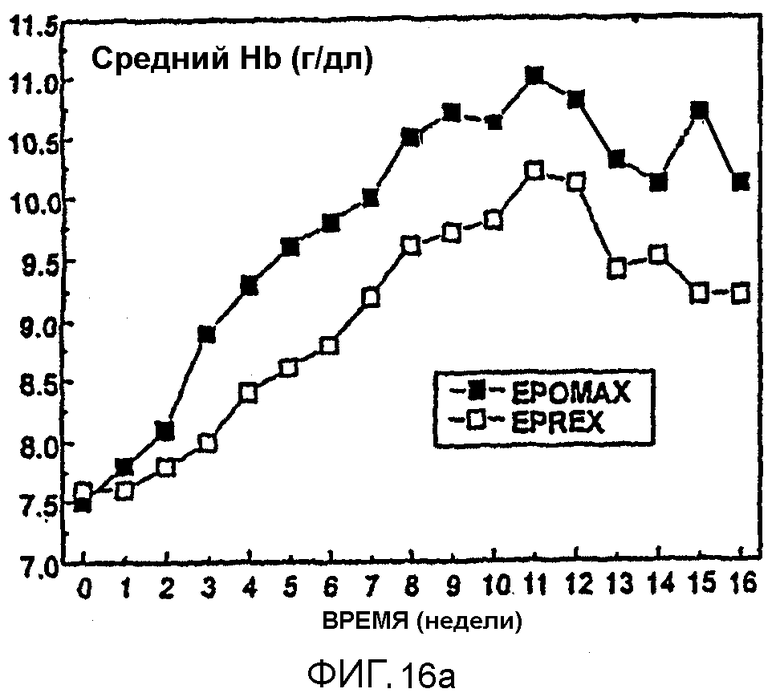
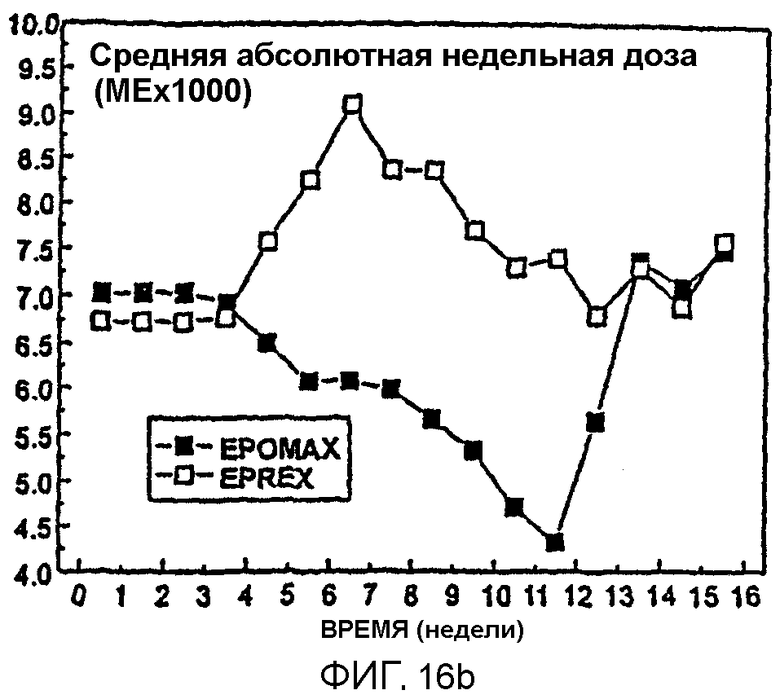
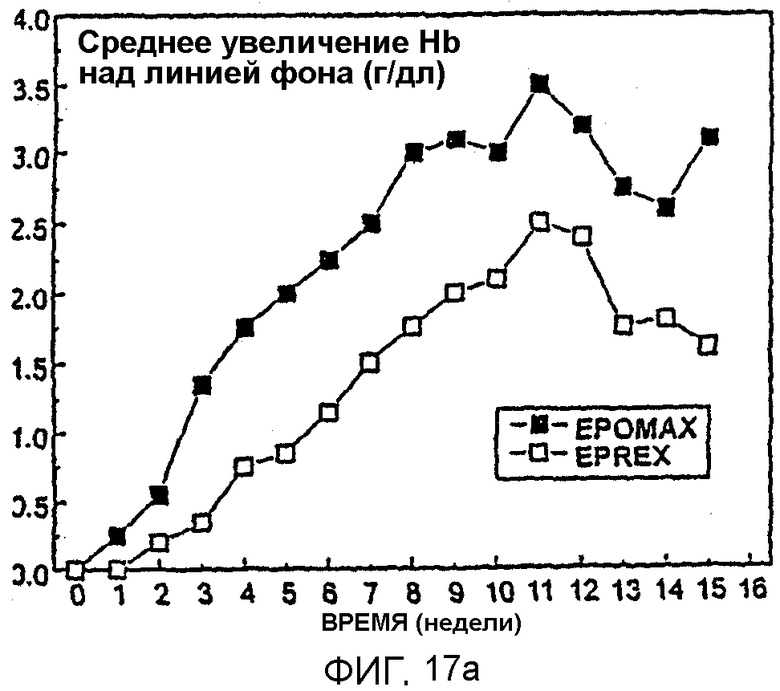
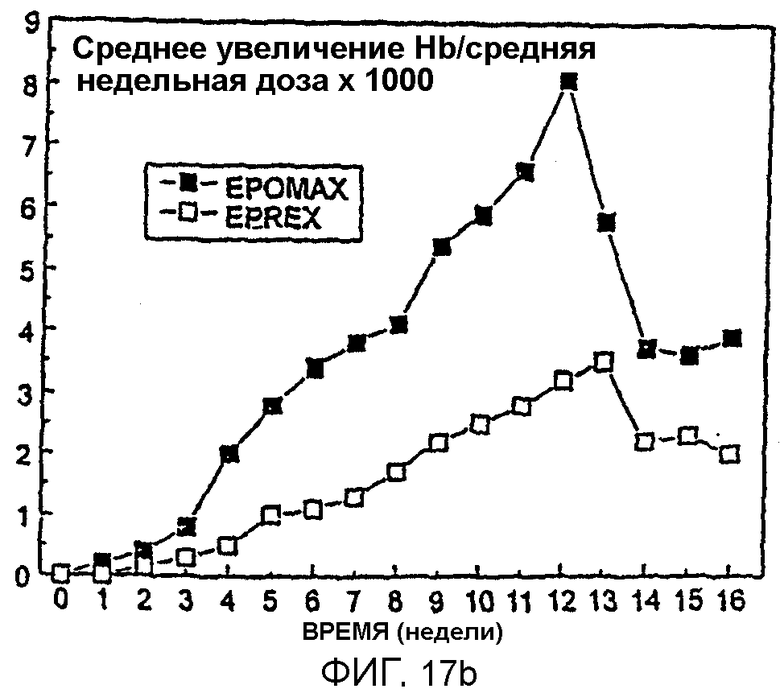
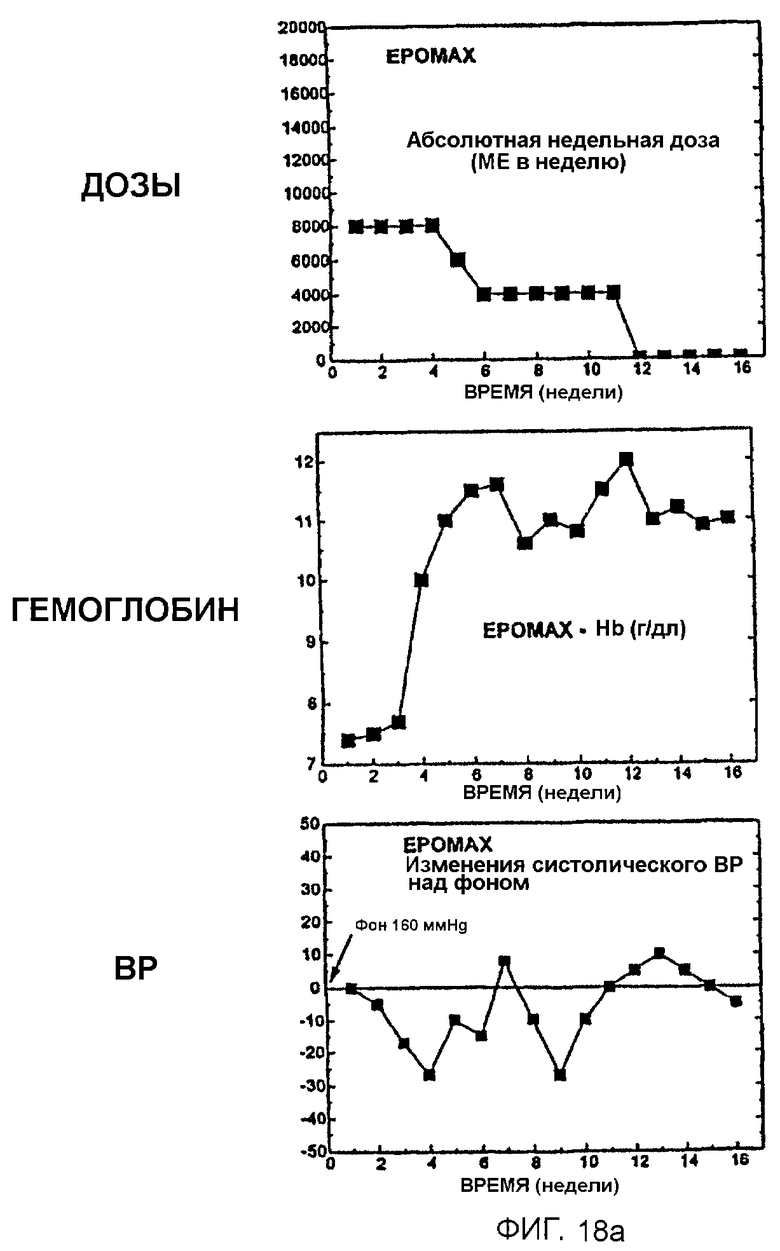
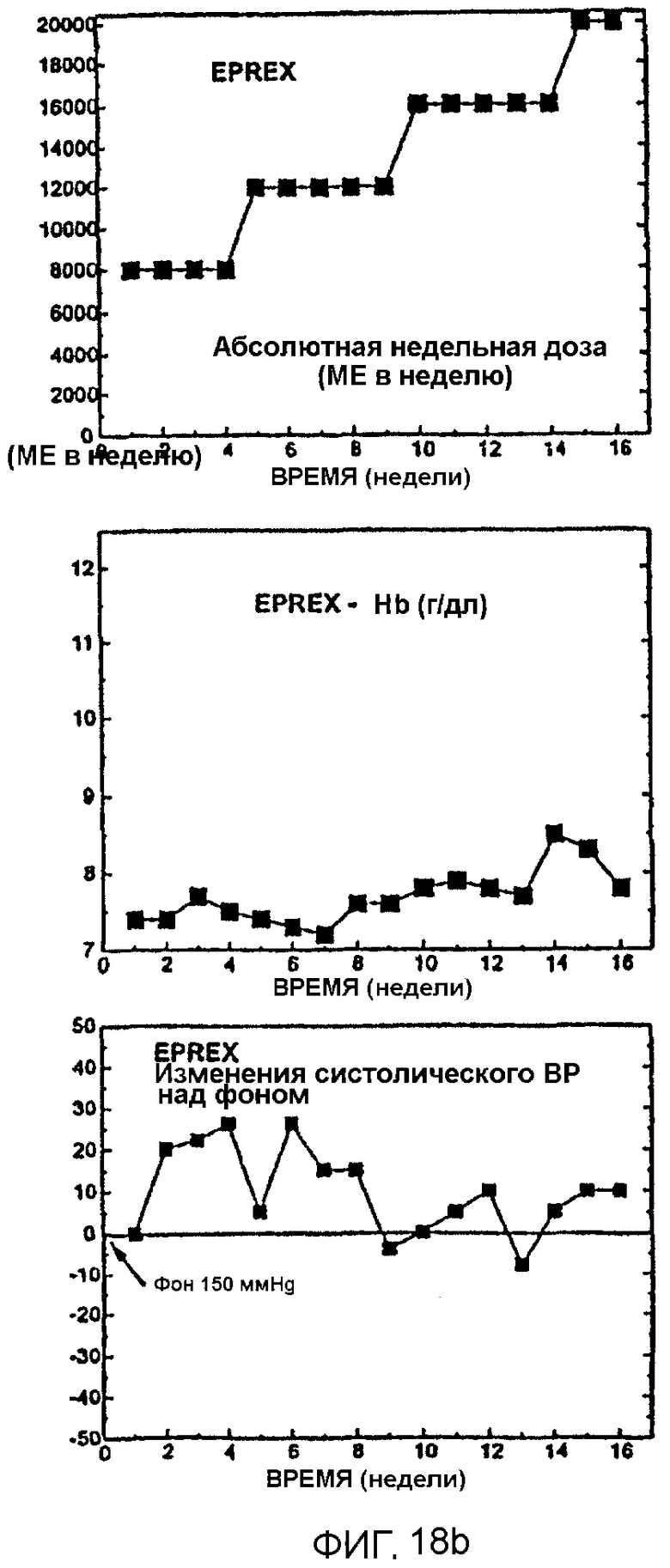
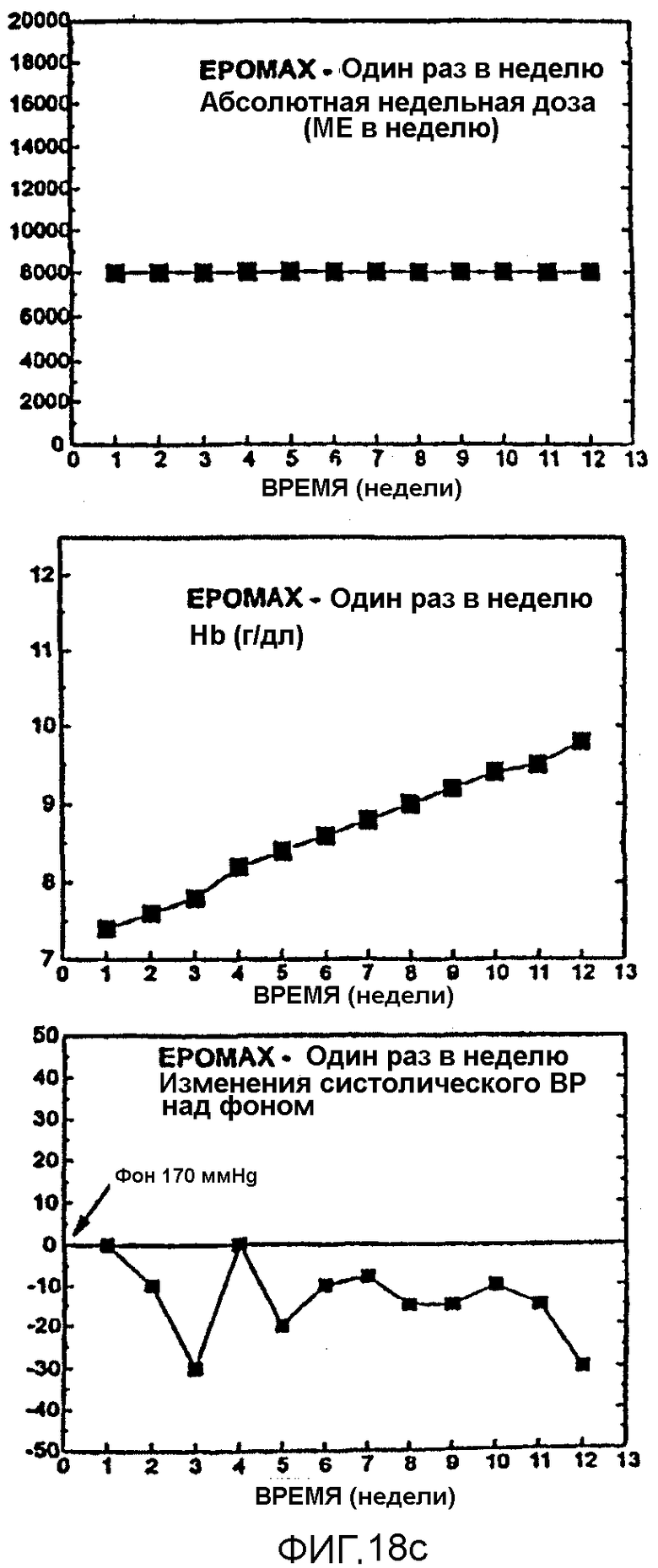
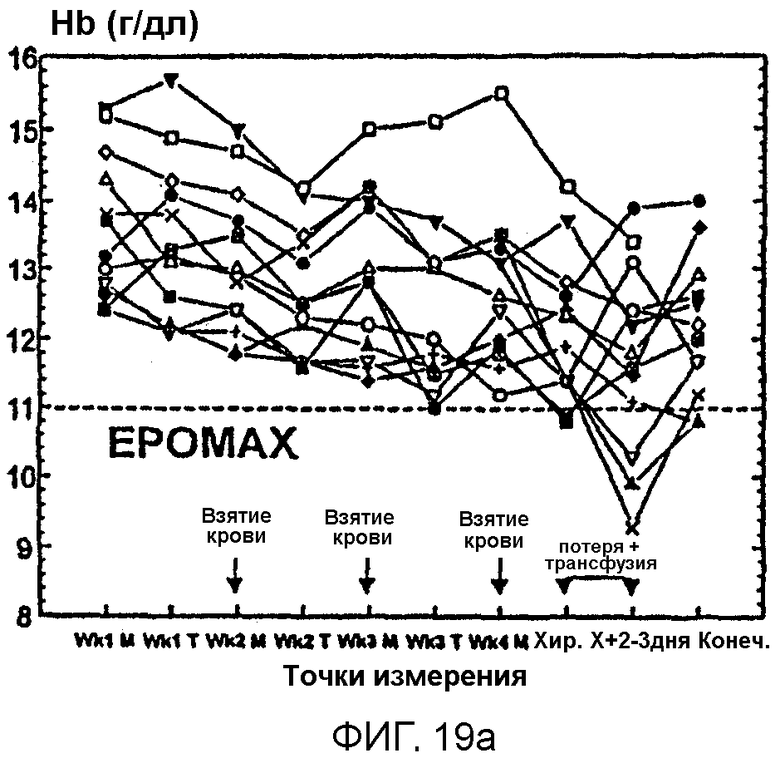
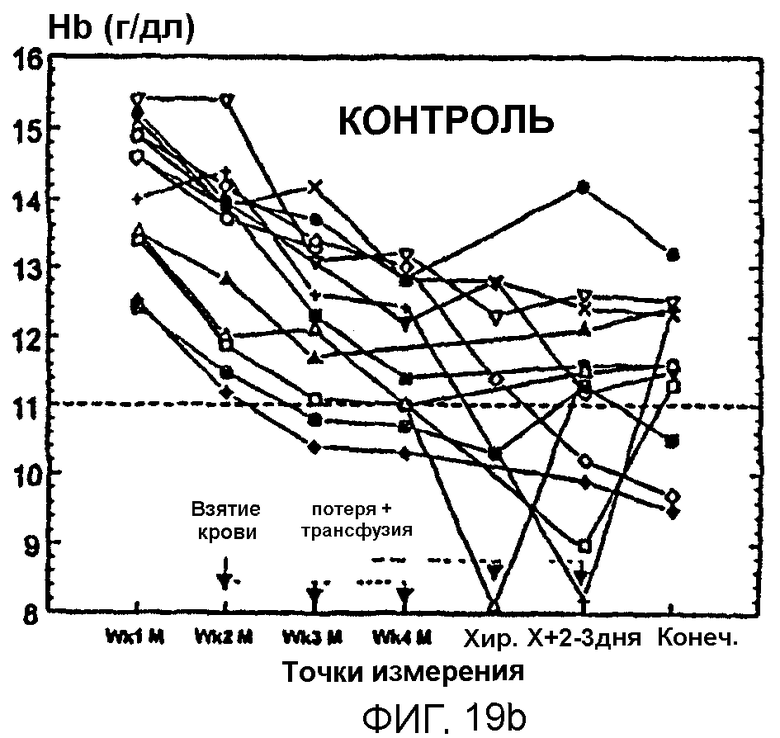
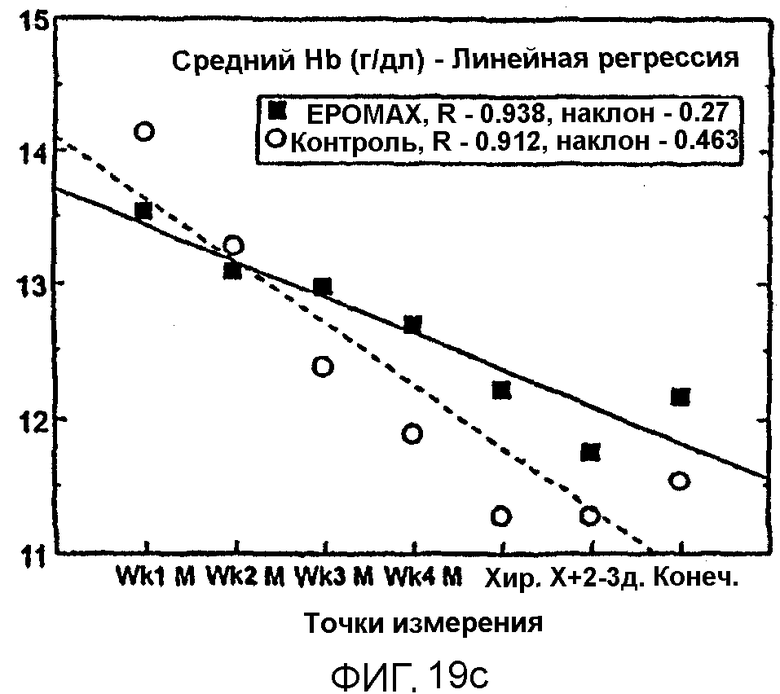
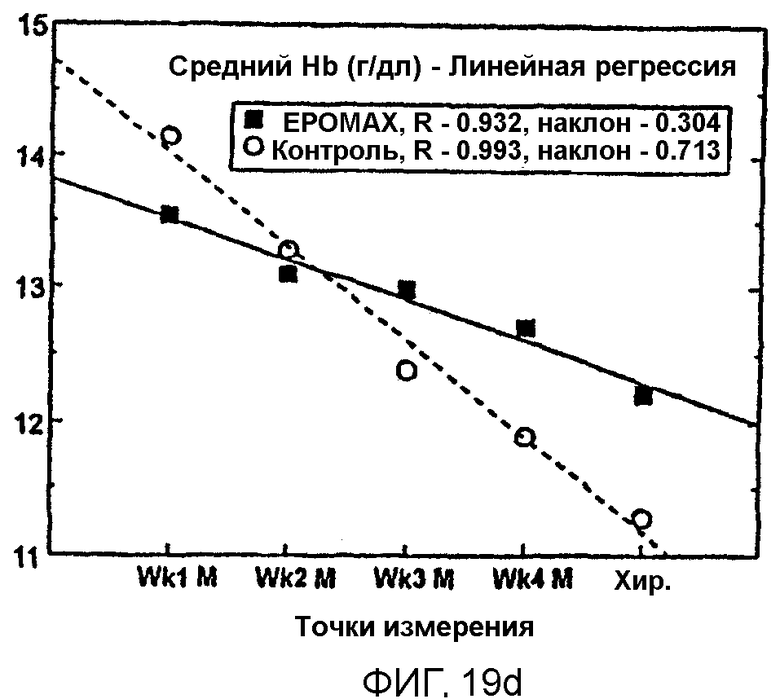
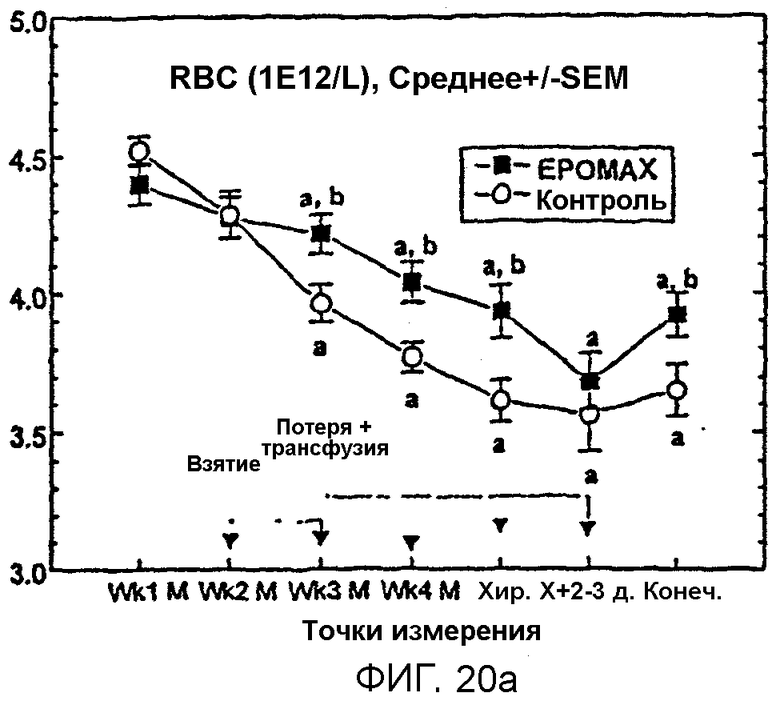
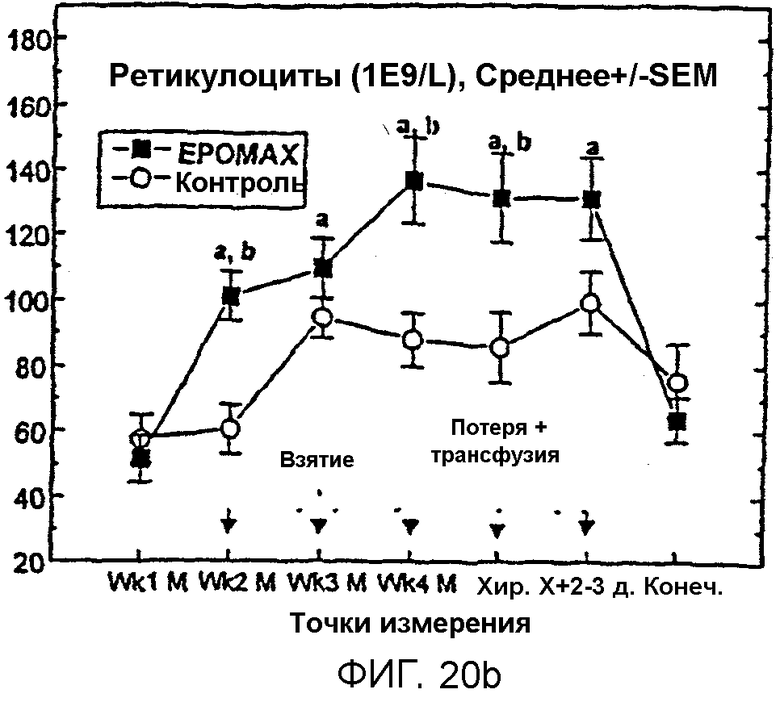
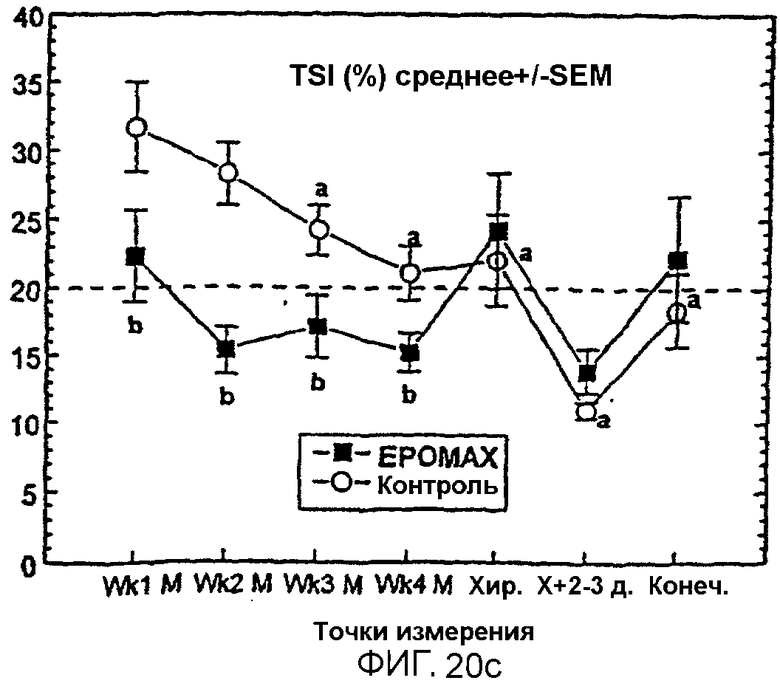
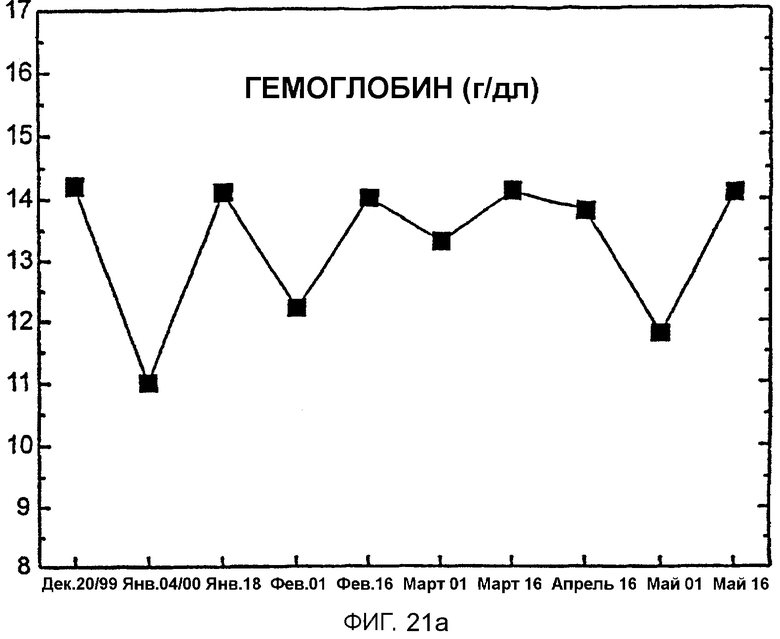
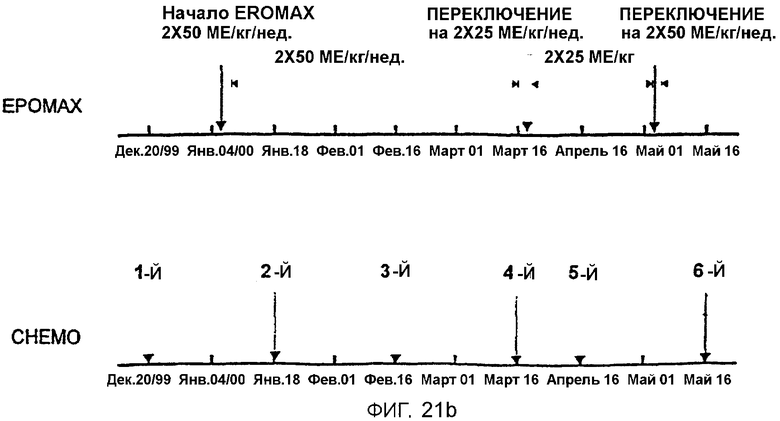
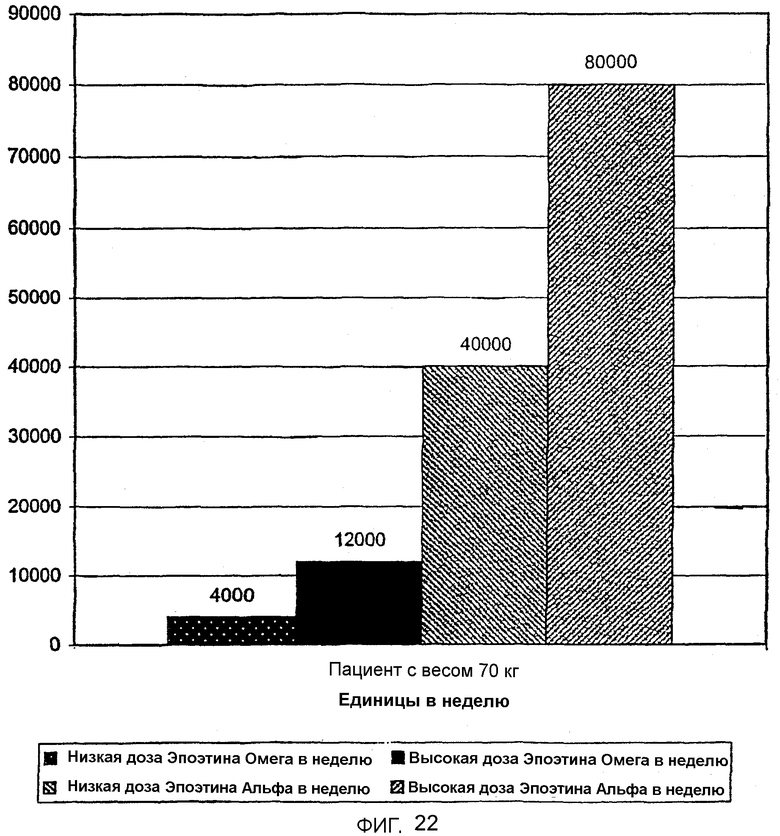
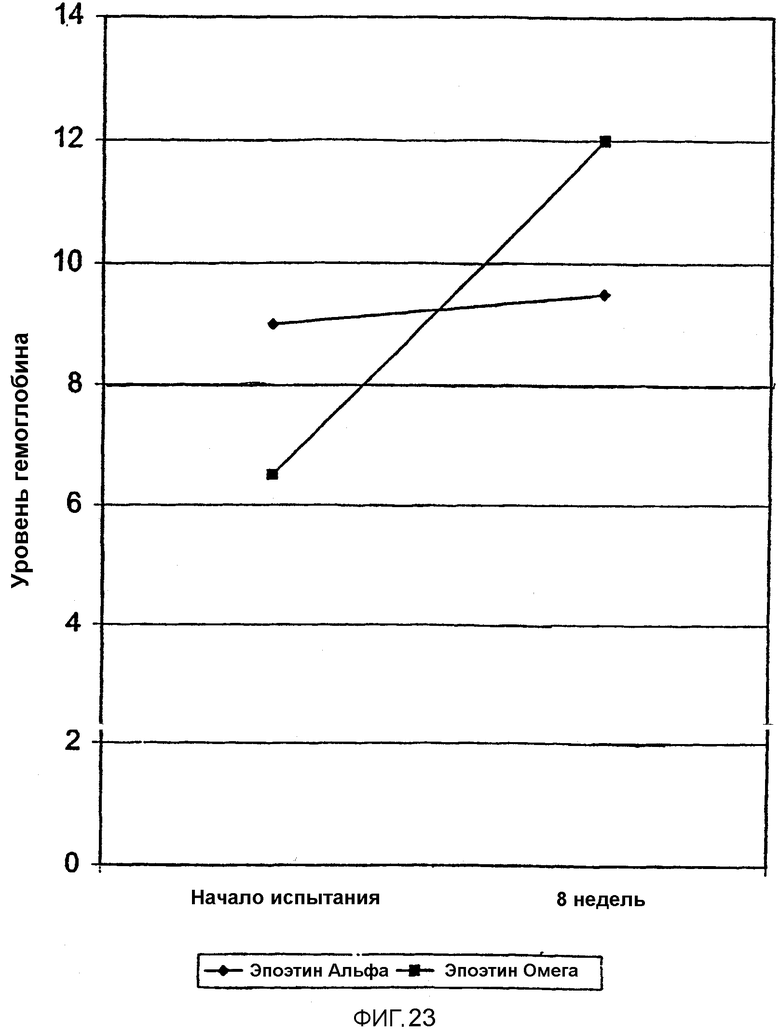
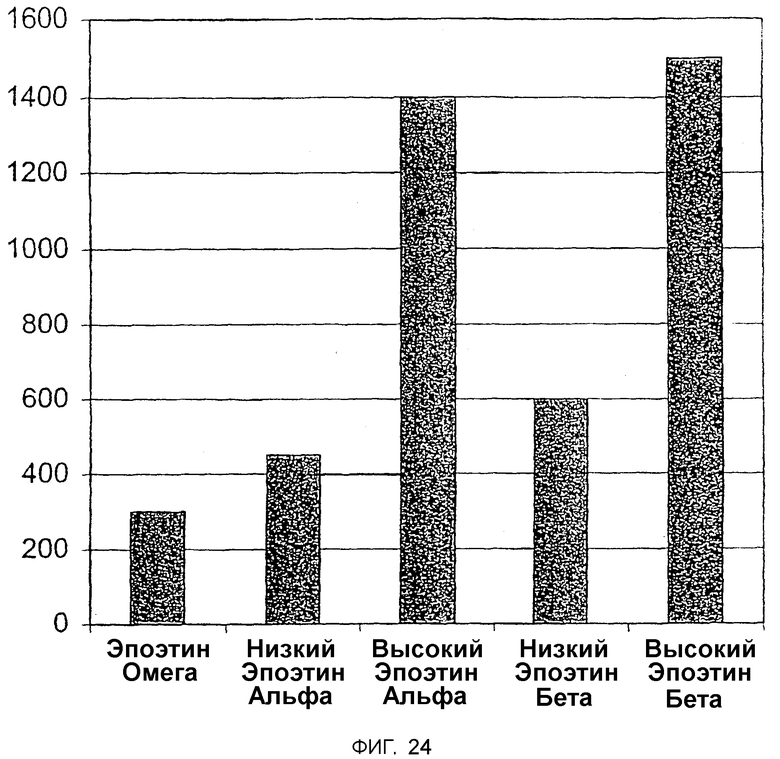
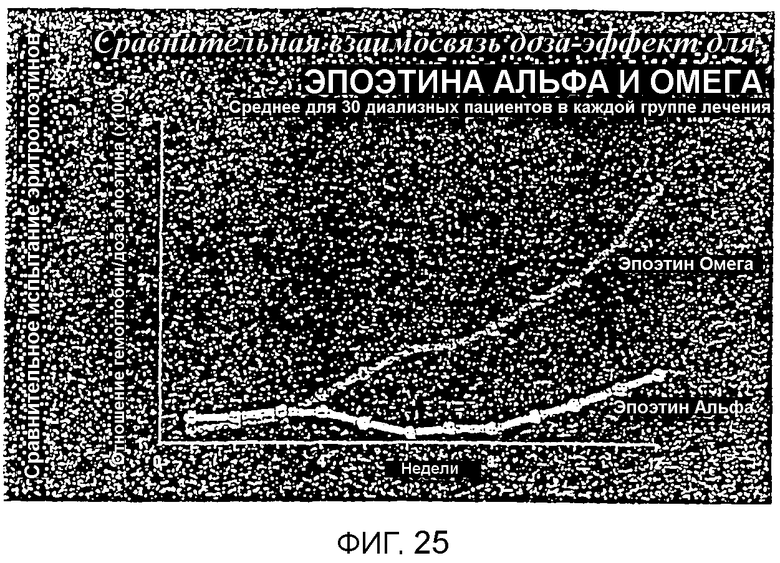
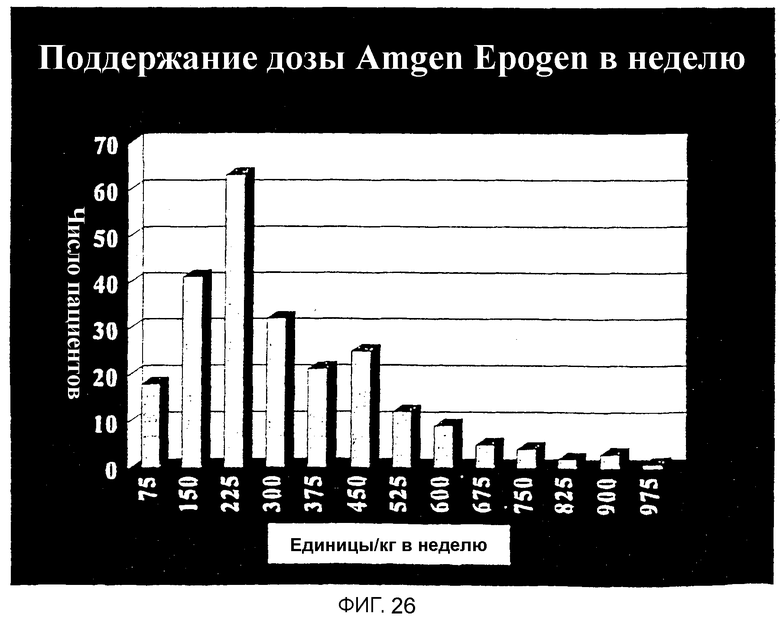
Изобретение относится к медицине, в частности к терапии, гематологии и касается лечения анемии различного происхождения. Для этого предложено применение рекомбинантного Эпоэтина Омега (ЭО) для получения лекарственного средства для лечения анемии у пациентов, которые нечувствительны к действию Эпоэтина Альфа или Бета, или у которых возникают неблагоприятные побочные эффекты при введении этих эпоэтинов. Изобретение обеспечивает эффективное лечение анемии без побочного действия. 2 н. и 13 з.п. ф-лы, 4 табл., 26 фиг.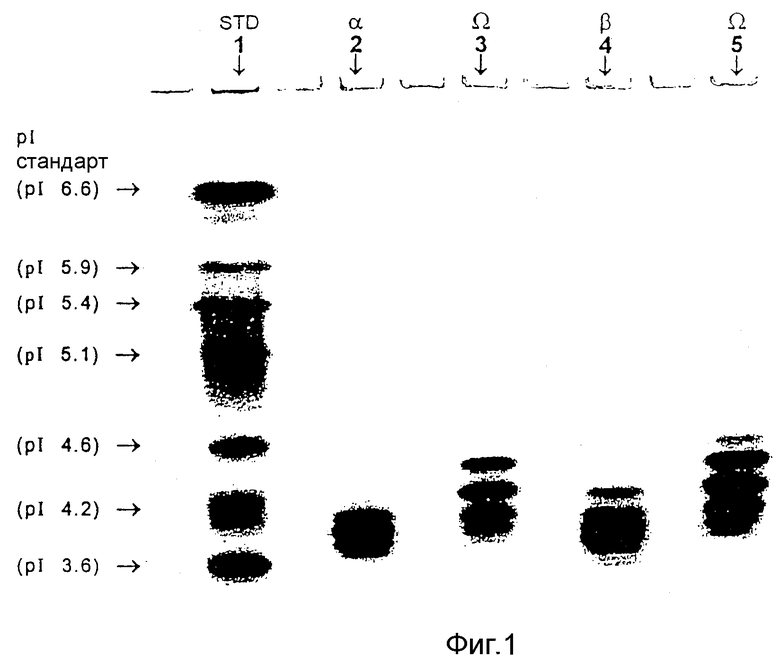
| СТАБИЛИЗИРОВАННЫЙ ВОДНЫЙ РАСТВОР ЭРИТРОПОЭТИНА | 1998 |
|
RU2128517C1 |
| RU 98106841 A1, 20.07.2000 | |||
| RU 97119627 A, 27.08.1999 | |||
| RU 95115239 A1, 27.03.1997 | |||
| ВАГОНЕТКА ДЛЯ ОДНОРЕЛЬСОВЫХ ВОЗДУШНЫХ ЖЕЛЕЗНЫХ ДОРОГ | 1927 |
|
SU24893A1 |
| Справочник терапевта | |||
| Под ред | |||
| проф | |||
| Б.И.Шулутко, СПб, Ренкор, 1996, с.335, 338-339, 341 | |||
| LUDWIG H | |||
| Epoetin in cancer-related anaemia | |||
| Nephrology Dialysis Transplantation, 1999, Feb., vol.14, ho Suppi 2, pp.85-92. | |||
Авторы
Даты
2006-08-27—Публикация
2001-08-09—Подача