Изобретение относится к медицине, а именно к отоларингологии, и может быть использовано как средство, улучшающее герметизацию склеиваемых биоповерхностей и репарационные процессы при микрохирургических вмешательствах на ухе.
В последнее время возник большой интерес к использованию биологических полимеров, в частности фибрина, в качестве композиций в различных областях хирургии. Фибриновый клей в отличие от синтетических - цианакрилатов и полиуретанов не оказывает повреждающего действия на склеиваемые поверхности и рассасывается в сравнительно короткие сроки (Durham L.H. Watt W., Juny M.V. et all." A method for preparation of fibrin glue/ J.Laryngol Otol. - 1987. - V.101.- N 11. - p. 1182-1186). За рубежом различные фирмы выпускают специальные наборы фибринового клея ("Tissucol, Tissel") Romeo G. Applications of Tissucol in larynx, traches and neck surgery/Rev. Laryngol.- 1989. - V. 110. - N 1. - P.121-122. Основным компонентом этих наборов является фибриноген, получаемый из донорской плазмы крови человека. Недостатком таких препаратов является потенциальная возможность передачи с ними инфекционного гепатита В, СПИДа и других заболеваний. Этот недостаток может быть устранен путем получения фибриногена из аутогенной плазмы крови больного (Everberg G. , Henrichsem J. Autologous tissue seal in myringoplasty/Laryngoscope - 1987. - V.97. - N 3. - P.370-371).
Прототипом предлагаемого состава является фибриновый клей, полученный из аутогенной крови по методу (Tolnay S., Benyo J., Dobo I/Autolog szovetragaszto alkalmasasa beteganyagynkon/Ful-orr-gegegyogyaszat. - 1987. - V. 33. - P 208-212). В его состав входит фибриноген, тромбин и 40 мМ СaCl2. Для получения фибриногена в качестве осадителя использовали насыщенный раствор сульфата аммония, который добавляли к плазме крови больных в соотношении 1:3 (0,25 насыщения), смесь центрифугировали 10 мин, 3000 об/мин, осадок, содержащий фибриноген, растворяли в 40 мМ растворе CaCl2.
К недостаткам прототипа относится:
- использование больших объемов крови (100 мл), что ограничивает применение клея у детей и больных с нарушенной системой свертывания и фибринолиза;
- отсутствие данных о чистоте и выходе фибриногена в полученных препаратах, что затрудняет их стандартизацию;
- отсутствие в препарате антипротеолитических и антифибринолитических веществ, способствующих предохранению фибринового клея от лизиса протеинизами крови и тканей. Известно, что расщепление фибринового клея может привести к разобщению склеенных поверхностей (С.Н.Хечинашвили, IX съезд отоларингологов СССР. Тез. докладов. Кишинев, 1988. - С. 237-244);
- отсутствие в составе клея антибактериальных и иммуностимулирующих средств, что может обуславливать развитие воспалительных реакций и замедление репарационных процессов.
Цель изобретения - улучшить репарационные процессы и герметизацию склеиваемых биоповерхностей, предупредить развитие воспаления в них при микрохирургических операциях на ухе.
Указанная цель достигается путем дополнительного введения в состав фибринового клея ингибиторов фибринолиза и протеолиза, антибиотика и лизоцима при следующем соотношении указанных компонентов: фибрина - 0,01-0,013 г, ε - АКК - 0,02-0,04 г, трасилола 200-400 КИЕ, лизоцима 0,02-0,04, карбенициллина - 0,02-0,04 г.
Фибриновый клей является физиологическим средством для соединения тканей, имитируя биологический процесс свертывания крови. Он способствует склеиванию и восстановлению целостности хрящей, слизистой оболочки, оказывает гемостатический эффект, ускоряет заживление ран, герметизирует ткани, что объясняется его способностью связываться с коллагеном, фибронектином, находящимися на поверхности фибробластов (Siedentop K.H., Harris D.M., Loewy A. Experimental use of fibrin tissue adhesive in middle ear surgery//Laryngoscope. - 1983. - V.93. - N 10. - P.1310-1313).
Для получения фибринового клея смешивают фибриноген, тромбин и CaCl2. Фибриноген получают из небольших количеств плазмы крови человека (10 мл) при помощи полиэтиленгликоля - 1000 (ПЭГ-1000), который добавляют к плазме с таким расчетом, чтобы его конечная концентрация составила 10%. После центрифугирования смеси при 3000 об./мин полученный осадок фибриногена растворяют в различных объемах (0,25-0,5 мл) 0,06 М цитрата натрия в зависимости от исходного уровня фибриногена в плазме крови. Концентрацию фибриногена определяют спектрофотометрическим методом (В.А.Белицер, Т.В.Варецкая, Ю.П. Бутылин и соавт. Определение содержания фибриногена в плазме//Лаб.дело. - 1983. - N 4. - С.38-42). Характеристика препаратов фибриногена, полученных из аутогенной плазмы крови человека в сравнении с прототипом, приведена в табл.1.
Согласно полученным данным, чистота выделенного из плазмы крови человека фибриногена при помощи ПЭГ-1000 составляет в среднем 48%, что значительно превышает аналогичный показатель в прототипе (19%).
Для получения геля фибрина к раствору фибриногена прибавляли равный объем 3% -ного раствора тромбина, содержащего 0,44% CaCl2. С целью предохранения клея от лизиса протеазами крови к нему добавляют синтетический ингибитор фибринолиза - ε- аминокапроновую кислоту ( ε -АКК) - 0,02-0,04 г и природный ингибитор протеолиза - полифункциональный ингибитор Кунитца - трасилол - 200-400 КИЕ. Первый угнетает превращение плазминогена в плазмин, второй инактивирует как ферменты фибринолиза, так и протеиназы, освобождающиеся из тканей, в особенности после хирургических вмешательств (К.Н.Веремеенко, О.П.Голобородько, А.И.Кизим. Протеолиз в норме и при патологии. - 1988. - Изд. "Здоров"я. - К. - 200 с).
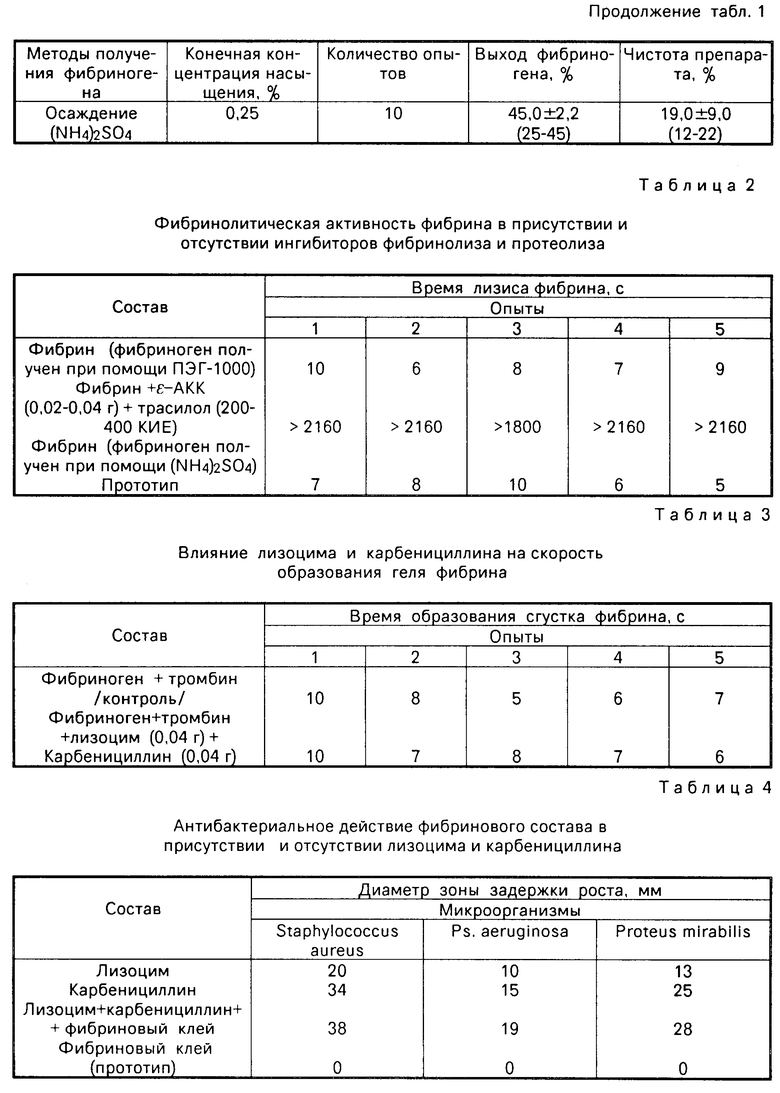
В специальной серии опытов изучали влияние ингибиторов фибринолиза и протеолиза на активность плазмина, который образуется из плазминогена, связанного с фибриногеном фибринового клея и выявляемого после добавления к нему 25-50 ед. стрептокиназы (см. табл.2).
Приведенные результаты указывают на то, что добавление к фибрину ε -АКК и трасилола придает сгусткам фибрина устойчивость к действию протеолитических ферментов крови, время их лизиса удлиняется более чем в 200-300 раз.
Для обоснования совместимости включенных в состав клея антибиотиков и лизоцима были проведены биохимические исследования по выяснению их влияния на способность фибриногена превращаться в фибрин под действием тромбина (см.табл.3).
Согласно данным табл.3, лизоцим и карбенициллин в концентрации 0,04 г не влияют на образование сгустка фибрина. Время свертывания фибриногена в присутствии этих веществ и в их отсутствии на отличается, что свидетельствует о сохранении фибриногеном и тромбином своих свойств в составе смеси.
Результаты микробиологических исследований антибактериальных свойств состава приведены в табл. 4.
Как видно из полученных результатов, диаметр зоны задержки роста различных микроорганизмов, вызываемый предлагаемым составом, не отличается от таковой свободного антибиотика. Эти данные свидетельствуют о том, что вносимые в состав карбенициллин (0,025-0,1 мг) и лизоцим (2 мг) находятся в активном состоянии, т.е. проявляют свое антимикробное действие в отношении испытуемых тест-культур. Сам фибриновый клей, полученный по методу, предложенному в прототипе, не обладает антимикробным эффектом. Как показали специальные исследования, антибактериальное действие предлагаемого состава сохраняется на протяжении 10 дней.
Методика предложенного состава осуществляется следующим образом. В один 1 мл шприц набирали 0,3 мл подогретого до 37оС раствора фибриногена, 0,1 мл ε -ААК (0,02-0,04 г), 0,1 мл трасилола (200-400 КИЕ), в другой шприц - 0,2 мл тромбина, 0,1 мл 0,44% раствора CaCl2, 0,1 мл лизоцима (0,02-0,04 г), 0,1 мл карбенициллина (0,02-0,04 г). Оба раствора подавались одновременно на склеиваемые поверхности. Через 30" в месте склеивания образуется гель фибрина, который уплотняется через 30-60 мин.
Адгезивные свойства применяемого состава были проверены в опытах in vitro по склеиванию кость-фасция височной мышцы, фасция-фасция (см.табл.5). Прочность соединения биопластических материалов с помощью предлагаемого состава проводили путем определения силы разрыва (г) склеиваемых поверхностей.
Данные табл. 5 показывают, что предлагаемый состав обладает более выраженными адгезионными свойствами, чем таковой в прототипе: склеиваемые биоповерхности в первом случае выдерживали максимальную нагрузку 80 г, во втором - 25 г.
| название | год | авторы | номер документа |
|---|---|---|---|
| Гемостатическая губка и способ ее получения | 2016 |
|
RU2628809C1 |
| Способ изготовления аутологичного фибрина с регулируемым содержанием фибриногена без использования экзогенного тромбина | 2020 |
|
RU2758260C1 |
| Губка гемостатическая и способ ее получения | 2016 |
|
RU2618896C1 |
| ТЕКСТИЛЬНЫЙ МАТЕРИАЛ ДЛЯ ОСТАНОВКИ КРОВОТЕЧЕНИЙ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2007 |
|
RU2380117C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОМБИНИРОВАННОГО БИОМАТЕРИАЛА С ПРОТИВОСПАЕЧНЫМ ЭФФЕКТОМ | 2003 |
|
RU2224549C1 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРИМОГО ФИБРИНОГЕНА EX VIVO | 2014 |
|
RU2571288C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКООБРАЗНОГО БИОМАТЕРИАЛА ДЛЯ ЭНДОСКОПИЧЕСКОГО УКРЫТИЯ РАНЕВЫХ ПОВЕРХНОСТЕЙ | 2003 |
|
RU2243777C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pET15/N-Dest+ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ, ШТАММ Escherichia coli BL21(DE3)Gold, ТРАНСФОРМИРОВАННЫЙ РЕКОМБИНАНТНОЙ ДНК pET15/N-Dest+, И СПОСОБ ЕГО ПОЛУЧЕНИЯ, СПОСОБ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОГО БИФУНКЦИОНАЛЬНОГО ФЕРМЕНТА - ДЕСТАБИЛАЗЫ МЕДИЦИНСКОЙ ПИЯВКИ | 2015 |
|
RU2658429C2 |
| СПОСОБ СОЗДАНИЯ БИОРЕЗОРБИРУЕМОГО КЛЕТОЧНОГО СКАФФОЛДА НА ОСНОВЕ ФИБРИНА ПЛАЗМЫ КРОВИ | 2017 |
|
RU2653434C1 |
| СПОСОБ ПОЛУЧЕНИЯ МАТЕРИАЛА ДЛЯ УКРЫТИЯ РАНЕВОЙ ПОВЕРХНОСТИ ПЕЧЕНИ | 1998 |
|
RU2139735C1 |


Изобретение относится к медицине, а именно к отоларингологии. Цель - предупреждение развития воспаления в склеиваемых биоповерхностях. Сущность состоит в том, что состав для соединения биопластических материалов содержит фибриновый клей, Ε -аминокапроновую кислоту, трасилол, лизоцим и карбенициллин взятые в определенных количественных соотношениях. 5 табл.
СОСТАВ ДЛЯ СОЕДИНЕНИЯ БИОПЛАСТИЧЕСКИХ МАТЕРИАЛОВ В ОТОХИРУРГИИ, содержащий фибриновый клей, отличающийся тем, что, с целью предупреждения развития воспаления в склеиваемых биоповерхностях, он дополнительно содержит ε -аминокапроновую кислоту, трасилол, лизоцим и карбенициллин при следующем соотношении компонентов, г:
Фибриновый клей - 0,01 - 0,013
e -Аминокапроновая кислота - 0,02 - 0,04
Трасилол, КИЕ - 200 - 400
Карбенициллин - 0,02 - 0,04
Лизоцим - 0,02 - 0,04
Авторы
Даты
1995-03-10—Публикация
1989-07-13—Подача