Изобретение относится к способу получения нового водосвязывающего дисперсных алюмосиликатных систем неустановленной структуры координационного соединения хлорида железа со смесью предельных (жирных) первичных аминов (ЖА) общей формулы RNH2, где R-C17-C20-алкил, которое помогает более эффективно устранять избыточную влажность грунта и тем самым уменьшать его пучение при промерзании по сравнению с известными водосвязывающими.
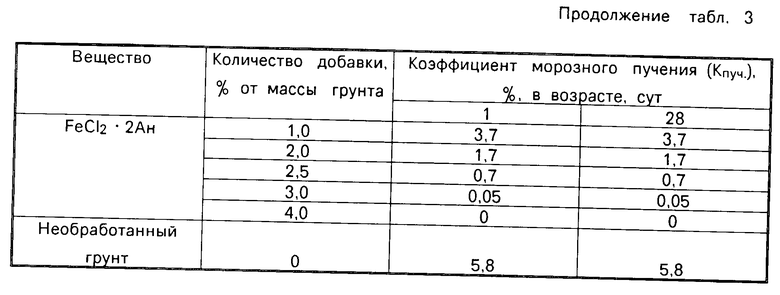
Для уменьшения морозного пучения грунта в настоящее время используется портландцемент [1] Основным недостатком использования портландцемента является отсутствие эффекта уменьшения морозного пучения сразу после обработки грунта и необходимость для проявления этого эффекта длительного периода (28 сут), определяемого сроком твердения вяжущего. Для получения эффекта уменьшения морозного пучения (Кпуч=0,9-0%) требуется большой расход дефицитного вяжущего-8-12% от массы грунта (см. табл. 3, чертеж).
В настоящее время известно водосвязывающее дисперсных алюмосиликатных систем, уменьшающее морозное пучение грунта, которое представляет собой координационное соединение хлорида железа с анилином FeCl2˙2Ан, где Ан анилин [2] Способ получения FeCl2 ˙2Ан заключается в смешивании кубовых остатков после дистилляции анилина с отходом титанового производства, содержащим FeCl2, в молярном соотношении 1:5.
Известное водосвязывающее имеет недостаток. Координационное соединение FeCl2˙2Ан не обеспечивает в достаточной степени связывание влаги грунта и не создает с ним прочные структурные связи. В связи с этим для получения эффекта уменьшения морозного пучения (Кпуч.=0,7-0,05%) требуется вводить в грунт FeCl2˙2Ан в количестве 2,5-3,0% от массы грунта (см. табл. 3, чертеж).
Цель изобретения синтез нового водосвязывающего дисперсных алюмосиликатных систем неустановленной структуры координационного соединения хлорида железа со смесью предельных (жирных) первичных аминов (ЖА) общей формулы RNH2, где R C17-C20-алкил, с улучшенными качественными характеристиками по сравнению с известными водосвязывающими.
Цель достигается тем, что хлорид железа обрабатывают расплавленной смесью предельных (жирных) первичных аминов (ЖА) общей формулы RNH2, где R C17-C20-алкил, при их молярном соотношении (2,1-2,3):(1,0-1,2). Образующийся осадок отделяют от фильтрата на пористом фильтре (типа воронки Бюхнера), промывают этиловым спиртом, водой и высушивают на воздухе.
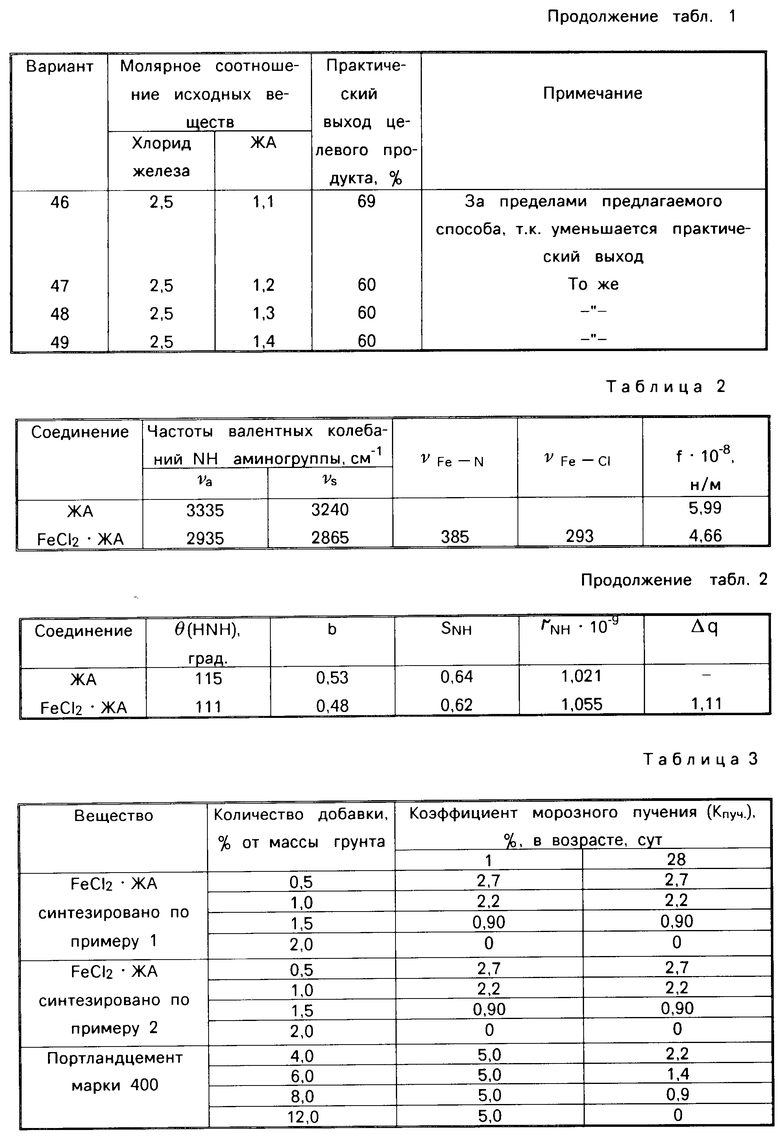
При использовании полученного продукта для уменьшения морозного пучения глинистого грунта требуется меньшее его количество по сравнению с известными водосвязывающими дисперсных алюмосиликатных систем. Так, введение 1,5-2,0% вещества от массы грунта переводит глинистый грунт в непучинистый. Для получения подобного эффекта требуется 2,5-3,0% FeCl2˙2Ан и 8-12% портландцемента марки 400 от массы грунта (табл. 3, чертеж).
Примеры способов получения координационного соединения хлорида железа с ЖА.
П р и м е р 1. 0,46 кг хлорида железа (отходы производства) обрабатывают 1,75 кг расплавленного ЖА (отходы производства). Образующийся осадок отделяют от фильтрата на пористом фильтре (типа воронки Бюхнера), промывают этиловым спиртом, водой и высушивают на воздухе. Получают 1 кг координационного соединения хлорида железа и ЖА FeCl2 ˙ЖА с практическим выходом 87% Температура разложения полученного продукта 136оС.
Хлорид железа используется в виде твердого отхода титанового производства марки ХТТ-2 по ТУ 48-10-27-84 Березниковского титано-магниевого комбината (г. Березники Пермской области), который образуется при хлорировании титанового сырья. Отход содержит, FeCl287,3-76,4; MgCl2 1,6-3,1; CaCl2 3,5-6,2; FeCl3 0,3-0,7; Al2O3 1,3-3,5; SiO2 4,4-7,0; TiO2 1,6-3,1.
Смесь предельных (жирных) первичных аминов (ЖА) общей формулы RNH2, где R -C17-C20-алкил, используется в виде отходов производства ПО "Азот" (г. Березники Пермской области) по ТУ 113-03-3-12-89, который образуется при выделении флотационного реагента ЖА высокой чистоты. Отход содержит 56% аминов, остальное углеводороды.
П р и м е р 2. 0,38 кг хлорида железа обрабатывают 1,10 кг расплавленного ЖА. Образующийся осадок отделяют от фильтрата на пористом фильтре (типа воронки Бюхнера), промывают этиловым спиртом, водой и высушивают на воздухе. Получают 1 кг координационного соединения хлорида железа и ЖА FeCl2 ˙ЖА с практическим выходом 87% Температура разложения полученного продукта 136оС. Хлорид железа и ЖА использованы в виде готовых препаратов. Смесь предельных (жирных) первичных аминов (ЖА) общей формулы RNH2, где R C17-C20-алкил, использовалась в виде готового продажного препарата, выпускаемого ПО "Азот" (г. Березники Пермской области) по ТУ 6-02-740-79, как флотационный реагент, который содержит первичных аминов 89,3% остальное углеводороды.
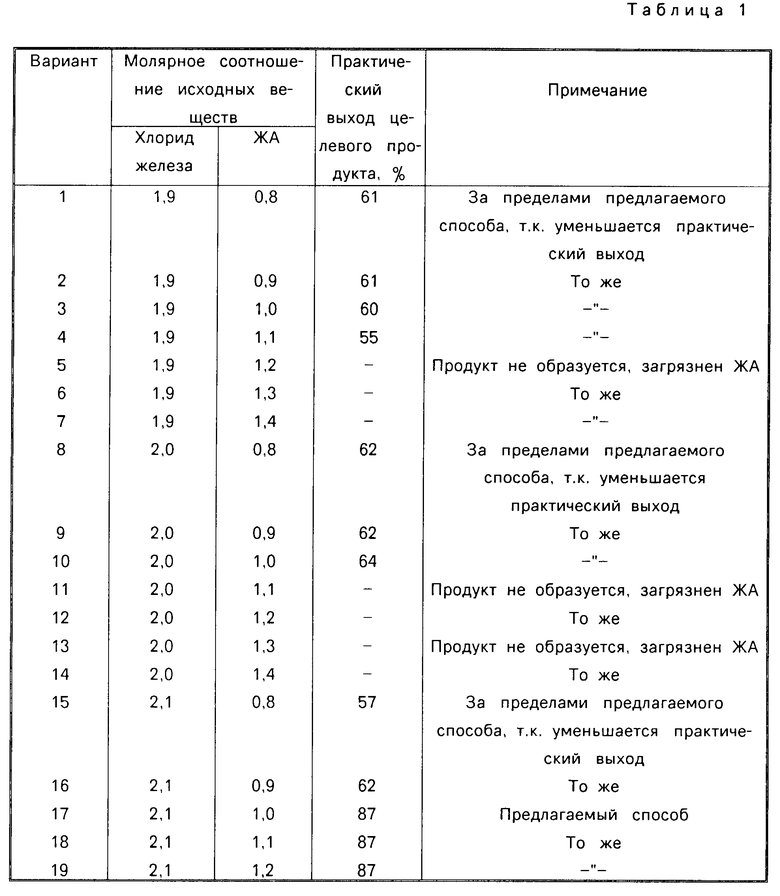
Обоснование выбранного молярного соотношения хлорида железа и ЖА приведено в табл. 1. Из табл. 1 видно, что молярное соотношение хлорида железа и ЖА должно быть (2,1-2,3):(1,0-1,2) (варианты 17-19, 24-26, 31-33), так как при таком молярном соотношении наблюдается наибольший практический выход целевого продукта, который имеет ИК-спектр с четким положением соответствующих полос поглощения. Поскольку отсутствуют результаты элементного анализа целевого продукта, ИК-спектроскопия была использована для его идентификации. Отнесение полос поглощения в ИК-спектре FeCl2 ˙ЖА приводится ниже. При уменьшении молярного количества хлорида железа до 1,9-2,0 (варианты 1-14) или увеличении молярного количества хлорида железа до 2,4-2,5 (варианты 36-49), а также уменьшении молярного количества ЖА до 0,8-0,9 (варианты 1, 2,8, 9, 15, 16, 22, 23, 29, 30, 36, 37, 43, 44) или увеличении молярного количества ЖА до 1,3-1,4 (варианты 6, 7, 13, 14, 20, 21, 27, 28, 34, 35, 41, 42, 48, 49) образуется продукт с уменьшенным практическим выходом и недостаточно четким ИК-спектром, т. е. за пределами предлагаемого способа (варианты 1-4, 8-10, 15, 16, 22, 23, 29, 30, 34-49), либо вообще не образуется продукт (варианты 5-7, 11-14, 20, 21, 27, 28). Таким образом, из табл. 1 следует, что молярное соотношение хлорида железа и ЖА должно быть (2,1-2,3):(1,0-1,2).
Соединение хлорида железа с ЖА представляет собой мелкокристаллический продукт темно-коричневого цвета, жирный на ощупь, практически не растворяется в воде. Взвесь FeCl2˙ ЖА в воде имеет рН около 7.
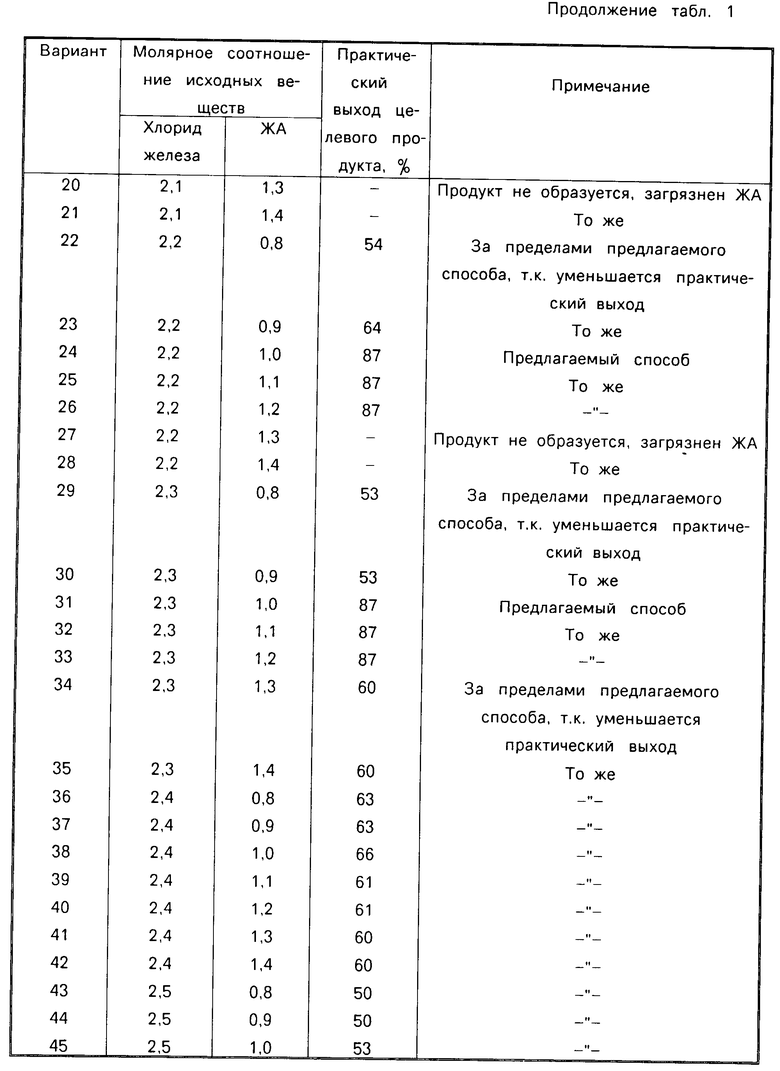
Поскольку FeCl2 ˙ЖА представляет вещество неустановленной структуры и элементный анализ в данном случае проводиться не может, то для идентификации целевого продукта, характеристики химической природы связи использовался метод ИК-спектроскопии в области 4000-150 см-1. Измерение ИК-спектров производилось на спектрометре UR-20 и FIS-21 фирмы Хитачи. Отнесение полос поглощения в ИК-спектрах свободного ЖА и FeCl2˙ ЖА приведено в табл. 2.
Из табл. 2 видно, что взаимодействие аминогрупп ЖА с катионом железа акцептором электронных пар приводит к резкому понижению частот симметричных (νs) и антисимметричных (νa) валентных колебаний NH аминогрупп. В табл. 2 содержатся результаты расчетов, характеризующих изменение состояния аминогрупп ЖА в результате координации, выполненные с использованием приведенных значений частот валентных колебаний NH. Расчет силовых постоянных fNH связи NH, валентных углов θ (HNH) и длин связей r NH аминогрупп ЖА выполнен по методу Линнета [3] Величины коэффициентов гибридизации b и интегралов перекрывания Is орбитали атома водорода с гибридной орбиталью атома азота SNH выполнены по методике, изложенной в работе [4] Причиной уменьшения величин fNH, θ (HNH), SNH, b и увеличения r NH в случае FeCl2 ˙ЖА по сравнению с ЖА является возникновение дополнительного положительного заряда на атомах азота аминогрупп ЖА в результате оттягивания его неподеленной электронной пары катионом цинка, играющим роль электрон-акцептора. Оценка величины дополнительного положительного заряда Δq на атоме азота в FeCl2˙ ЖА произведена по уравнению Линнета [3]
Правомерность примененного эмпирического подхода с использованием приближенной валентно-силовой схемы для анализа колебательных спектров свободных и координационных аминов подтверждается данными работами [5] В ИК-спектре FeCl2˙ ЖА имеются полосы поглощения, отвечающие согласно литературным данным [6] валентному колебанию Fe-N и валентному колебанию Fe-Cl (см. табл. 2). В соответствии с литературными данными положение полос поглощения Fe-Cl отвечает тетраэдрическому строению комплекса FeCl2˙ЖА с валентным углом α(ClFeCl)=111oC.
ИК-спектры целевого продукта, полученного из готовых продажных препаратов и из отходов производства, идентичны. На основании ИК-спектроскопического изучения целевого продукта следует, что он представляет собой координационное соединение хлорида железа с ЖА FeCl2˙ ЖА.
Координационное соединение FeCl2 ˙ЖА может быть использовано в качестве водосвязывающего дисперсных алюмосиликатных систем (табл. 3). Указанное практическое использование FeCl2˙ЖА является новым. В литературе нет сведений об использовании FeCl2 ˙ЖА для рассматриваемого практического применения. Основная сложность при укреплении дисперсных алюмосиликатных систем, к которым, в частности, относятся высоковлажные глинистые грунты, заключается в устранении избыточной липкости, препятствующей использованию большинства землеройных, грунтосмесительных и транспортных машин. Образующиеся в процесс рыхления комья высоковлажного глинистого грунта слипаются и прилипают к рабочим органам и ходовой части машин. Поэтому высоковлажный грунт очень трудно перемешивать с вяжущими компонентами и еще труднeе его уплотнять. В связи с этим перед введением вяжущего, в частности цемента, необходимо предварительно устранить избыточную влажность грунта, что способствует уменьшению его морозного пучения.
Механизм взаимодействия координационных соединений первичных аминов (аминокомплексов) с глинистыми грунтами повышенной влажности можно представить следующим образом. Взаимодействию минеральных частиц глинистых грунтов с аминокомплексами предшествует определенная их ориентация. Аминокомплексы проникают к поверхности глинистых минералов, частично оттесняя связанную воду. На это указывает некоторое снижение гидрофильности глинистых пород в присутствии аминокомплексов. Аминокомплексы притягиваются и удерживаются на поверхности раздела в ориентированном состоянии полярной группой (аминогруппой) к полярному сорбенту (глинистым частицам), неполярной углеводородной (инактивной) во внешнюю среду (поровый раствор). Группы NH2 дают прочные водородные связи с соседними электроотрицательными атомами. В связи с этим взаимодействие между электроотрицательными ионами кислорода поверхности кристаллической структуры глинистых минералов и реагентами представляется происходящим через водород полярных групп, например R.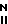 -H.O
-H.O  (поверхность минерала), где R углеводородный радикал. В случае аминокомплексов аминогруппа с помощью одного водорода участвует в водородной связи с атомами кислорода, находящимися на поверхности минерала:
(поверхность минерала), где R углеводородный радикал. В случае аминокомплексов аминогруппа с помощью одного водорода участвует в водородной связи с атомами кислорода, находящимися на поверхности минерала:

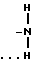
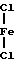
 -
-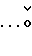
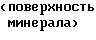
Известны факты, указывающие на то, что лиганды, координированные к центральному атому, в комплексных соединениях в связях с металлом используют не всю свою электронную плотность. Согласно квантово-химическим расчетам, на координированных лигандах сохраняется часть отрицательного заряда, что проявляется, в частности, в существовании координационных полимеров. Таким образом, имеются возможности участия координированных лигандов в дополнительных взаимодействиях, наиболее существенные из которых водородные связи. Показано, что аминокомплексы одновременно переводят часть свободной воды в связанное состояние за счет водородной связи по следующей схеме:
-
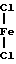
 +
+ 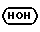 __→
__→ 
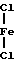
Этот вывод подтверждается литературными данными, согласно которым участие первичных аминов в водородной связи в качестве акцептора протонов приводит к росту максимума деформационных NH колебаний. К деформационным NH колебаниям аминогруппы аминокомплекса в ИК-спектрах принадлежит полоса около 1600 см-1. В ИК-спектре суспензии FeCl2 ˙ЖА H2O глинистый грунт наблюдается увеличение максимума полосы поглощения (1600 см-1) деформационного NH колебания аминогруппы FeCl2˙ ЖА, что служит подтверждением образования водородной связи между азотом аминогруппы комплекса и водородом молекулы воды. Изменение поверхностных сил глинистых частиц под воздействием аминокомплекса FeCl2˙ЖА сказывается на водоудерживающей способности глинистых грунтов вследствие создания новых структурных связей. Координационное соединение FeCl2 ˙ЖА, обладающее высокой водосвязывающей способностью, в небольшом количестве понижает морозное пучение глинистого грунта.
Влияние на морозное пучение глинистого грунта координационного соединения FeCl2 ˙ЖА сравнивалось с влиянием на морозное пучение FeCl2˙ 2Ан и портландцемента марки 400.
Для исследования использовался глинистый грунт, отобранный в Красносельском районе г. Санкт-Петербурга. Глинистый грунт представляет собой гидрослюдистый суглинок желтовато-коричневого цвета, пластичный, с небольшими серыми пятнами, вероятно, пятнами оглоения, с включениями щебня, дресвы, корешков растений, с гнездами ожелезения. Рентгенографическое исследование глинистого грунта показало, что он представлен гидрослюдой (преобладает), хлоритом (в подчиненном количестве), каолинитом (следы). Естественная влажность грунта W=15-16% плотность изменяется от 2,06 до 2,11 г/см3, число пластичности 0,12. При испытаниях относительная влажность глинистого грунта составила 0,8.
Изучение влияния на морозное пучение глинистого грунта координационных соединений FeCl2˙2Ан, FeCl2 ˙ЖА и портландцемента марки 400 проводилось по методике [1]
Глинистый грунт обрабатывали различным количеством координационных соединений FeCl2˙2Ан, FeCl2˙ЖА и портландцемента с последующим перемешиванием до образования нелипкой, сыпучей, однородной, удобообрабатываемой массы. Полученную смесь уплотняли на гидравлическом прессе в специальных формах-цилиндрах с диаметром 100 мм и высотой 80 мм, состоящих из наборных колец, при давлении уплотнения 15 МПа в течение 3 мин. Приготовленные образцы выдерживали в течение 1 и 28 сут в формах в воздушно-влажной среде, затем насыщали водой до состояния полного водонасыщения (в течение 3 сут) и испытывали на морозоустойчивость по методике [1] с определением коэффициента морозного пучения, представляющего собой отношение (% ) деформации морозного пучения (величины морозного поднятия) к высоте образца.
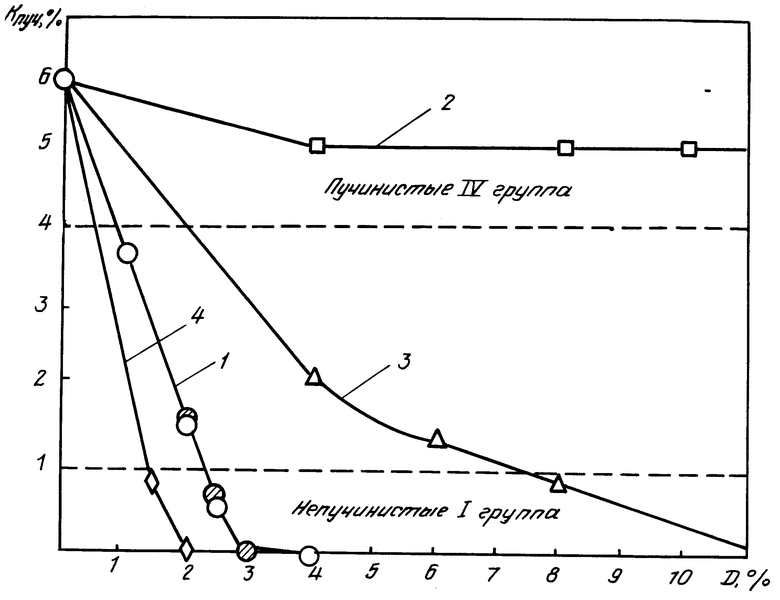
Испытания показали (табл. 3, чертеж), что глинистый грунт, относящийся в необработанном виде по степени пучинистости (Кпуч.=5,8%) к пучинистым грунтам (IV группа), в результате обработки FeCl2˙ЖА в количестве 1,5-2,0% от массы породы характеризуется коэффициентом морозного пучения, меньшим 1,0% (чертеж), что переводит его в группу непучинистых грунтов (I группа). Причем введение в глинистый грунт FeCl2˙ЖА в количестве 2% предотвращает морозное пучение (Кпуч.=0%). Результаты изучения влияния на морозное пучение глинистого грунта координационного соединения FeCl2˙ ЖА, синтезированного из отходов производства (по примеру 1) и из готовых препаратов (по примеру 2) одинаковые. Для получения подобного эффекта уменьшения морозного пучения глинистого грунта при использовании координационного соединения FeCl2˙ 2Ан требуется значительно большее его количество 2,5-3,0% Для получения подобного эффекта при использовании портландцемента марки 400 требуется еще большее его количество 8-12% причем эффект (Кпуч=0,9-0%) проявляется только после 28-суточного срока, необходимого для твердения цемента. В 1-суточном возрасте, т.е. сразу после обработки грунта цементом, уменьшение морозного пучения практически не наблюдается (Кпуч=5,0%). Оптимальное количество FeCl2 ˙ЖА, необходимое для предотвращения морозного пучения глинистого грунта, определялось следующим образом: нижний предел из того условия, что уменьшение морозного пучения при использовании FeCl2˙ЖА было эффективнее, чем при использовании FeCl2 ˙2Ан, не менее чем на 20% верхний предел по количеству FeCl2˙ ЖА, вызывающему полное отсутствие морозного пучения. Эти пределы FeCl2 ˙ЖА составляют 1,5-2,0% от массы грунта.
С целью улучшения качественных характеристик водосвязывающего дисперсных алюмосиликатных систем предлагается координационное соединение FeCl2˙ЖА. Как следует из данных табл. 3 и чертежа, для предотвращения морозного пучения глинистого грунта требуется меньшее количество FeCl2˙ ЖА по сравнению с FeCl2˙2Ан и портландцементом марки 400. Следовательно, FeCl2 ˙ЖА обладает более высокой водосвязывающей способностью по сравнению с FeCl2˙2Ан и портландцементом марки 400. Координационное соединение FeCl2˙ ЖА может использоваться как материал длительного складского хранения, транспортироваться без специальных мер затаривания. Синтез координационного соединения FeCl2˙ЖА осуществляется с использованием отходов химических производств, в связи с чем оно может быть рекомендовано для широкого внедрения в качестве водосвязывающего дисперсных алюмосиликатных систем. Одновременно решаются некоторые вопросы охраны окружающей среды, так как утилизируются отходы химических производств.
На чертеже показан характер изменения коэффициента морозного пучения (Кпуч.) глинистого грунта в зависимости от вида вещества (Д%), где даны следующие обозначения: 1 координационное соединение FeCl2˙2Ан (1 или 28 суток выдерживания образцов), 2 портландцемент (1 сут выдерживания образцов), 3 портландцемент (28 сут выдерживания образцов), 4 координационное соединение FeCl2 ˙ЖА (1 или 28 сут выдерживания образцов), пунктиром показано отнесение грунтов к соответствующей группе по Кпуч.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ВОДОСВЯЗУЮЩЕГО ДИСПЕРСНЫХ АЛЮМОСИЛИКАТНЫХ СИСТЕМ | 1993 |
|
RU2041877C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДОСВЯЗЫВАЮЩЕГО ДИСПЕРСНЫХ АЛЮМОСИЛИКАТНЫХ СИСТЕМ | 1993 |
|
RU2041880C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДОСВЯЗЫВАЮЩЕГО ДИСПЕРСНЫХ АЛЮМОСИЛИКАТНЫХ СИСТЕМ | 1993 |
|
RU2041883C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДОСВЯЗЫВАЮЩЕГО ДИСПЕРСНЫХ АЛЮМОСИЛИКАТНЫХ СИСТЕМ | 1993 |
|
RU2041882C1 |
| Способ укрепления глинистого грунта | 1988 |
|
SU1553607A1 |
| Асфальтобетонная смесь | 1987 |
|
SU1511237A1 |
| СМЕСЬ ДЛЯ ОБЕЗВРЕЖИВАНИЯ И ЛИТИФИКАЦИИ БЫТОВЫХ И ПРОМЫШЛЕННЫХ ОТХОДОВ, А ТАКЖЕ ДОННЫХ ОСАДКОВ | 1999 |
|
RU2162068C1 |
| Геокомпозиты на основе техногенных грунтов антропогенного генезиса и способ их получения | 2020 |
|
RU2759620C1 |
| СПОСОБ ОБРАБОТКИ ПОДЗЕМНЫХ ПЛАСТОВ | 2010 |
|
RU2564298C2 |
| СОЕДИНЕНИЯ И КОМПОЗИЦИИ С ПОЛИГЛИЦЕРИНОМ | 2011 |
|
RU2592275C2 |
Изобретение относится к области химической промышленности, в частности к способу получения нового водосвязывающего дисперсных алюмосиликатных систем. Цель изобретения синтез нового водосвязывающего неустановленной структуры дисперсных алюмосиликатных систем координационного соединения хлорида железа со смесью предельных (жирных) первичных аминов (ЖА) общей формулы RNH2, где R -C17-C20 -алкил, с улучшенными качественными характеристиками по сравнению с известными водосвязывающими. Способ осуществляется путем обработки хлорида железа расплавленной смесью предельных (жирных) первичных аминов (ЖА) общей формулы RNH2, где R -C17-C20 -алкил, при молярном соотношении хлорида железа и ЖА, равном (2,1-2,3) (1,0-1,2). 1 ил. 3 табл.
СПОСОБ ПОЛУЧЕНИЯ ВОДОСВЯЗЫВАЮЩЕГО ДИСПЕРСНЫХ АЛЮМОСИЛИКАТНЫХ СИСТЕМ путем взаимодействия соли железа с аминосодержащим компонентом, отличающийся тем, что в качестве аминосодержащего компонента используют расплавленную смесь предельных первичных аминов общей формулы
RNH2,
где R C17 C20-алкил,
при молярном соотношении соли железа и амина (2,1 2,3) (1,0 1,2).
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Журнал органической химии, 1988, N 9, с.2109. | |||
Авторы
Даты
1995-08-20—Публикация
1993-03-01—Подача