Изобретение относится к биотехнологии и медицинской технологии и предназначено для получения биологических и медицинских препаратов, в состав которых входят жидкие перфторорганические соединения (ПФОС), в частности кровезаменителей на основе эмульсий ПФОС, которые в процессе использования вводятся в организм внутривенно.
ПФОС являются главным компонентом газопереносящих кровезаменителей на основе ПФОС. Как известно, ПФОС химически инертны, однако они хорошо физически растворяют газы, в частности кислород и двуокись углерода. Поэтому они могут являться переносчиками газов. Но ПФОС не растворяются в воде и их приходится эмульгировать при изготовлении кровезаменителей и перфузионных сред. Одной из основных проблем кислородпереносящих эмульсий ПФОС, предназначенных для введения в организм, является наличие в ПФОС вредных примесей, микроорганизмов и их продуктов жизнедеятельности, что увеличивает токсичность и пирогенность эмульсий ПФОС. Поэтому ПФОС необходимо очищать от пирогенов и стерилизовать перед эмульгированием.
В практике работы с препаратами для внутривенного введения известно, что растворы лекарственных веществ иногда проявляют пирогенные свойства. Это происходит, как правило, из-за бактериального загрязнения, обусловленного в основном недостаточно строгим соблюдением правил асептики при подготовке аппаратуры и реагентов, а также при приготовлении растворов для испытаний или лекарственной формы.
Как известно, пирогены это продукты жизнедеятельности микроорганизмов, соединения полисахаридной или полипептидной природы, продуцируемые не только патогенными микроорганизмами, но и сапрофитами, всегда имеющимися в воздухе. Пирогенные вещества проходят через фильтры с размерами пор 1-5 мкм. Они термоустойчивы и сохраняются после стерилизации. При парентеральном введении уже при концентрации 0,01 мкг на 1 мл раствора пирогенные вещества могут вызывать у человека и животных пирогенную реакцию (повышение температуры тела на 2-3оС, цианоз, одышка, рвота и др.).
Известен способ очистки жидких пер- фторорганических соединений, включающий приведение в контакт с сорбентом, с последующим отделением от сорбента и автоклавированием.
Недостатками способа являются недостаточно высокая производительность и высокий расход сорбента.
Цель изобретения увеличение производительности процесса апирогенной очистки и экономия сорбента.
Указанная цель обеспечивается тем, что предложен способ очистки жидких перфторорганических соединений, в котором сначала сорбент этиловый спирт, взятый в объемном соотношении с очищаемым жидким ПФОС от 0,4:1 до 1:1, перемешивается с помощью электромеханического смесительного устройства в течение 1-5 мин при скорости вращения вала смесительного устройства 50-3000 об/мин, а затем после отделения слоя ПФОС его перемешивают с апирогенной водой, взятой в объемном соотношении с очищаемым жидким ПФОС 1:1, с помощью электромеханического смесительного устройства в течение 1-5 мин при скорости вращения вала смесительного устройства 50-3000 об/мин. После этого производится отстой смеси в течение 5-15 мин и отделение нижнего слоя очищаемого жидкого ПФОС.
Этиловый спирт является не только сорбентом, очищающим ПФОС от спирторастворимых вредных примесей, но и стерилизующим агентом, уничтожающим микроорганизмы. Этиловый спирт и водорастворимые вредные примеси затем отмываются апирогенной водой.
Наличие вредных примесей в ПФОС можно обнаружить различными методами, например с помощью изменения оптического поглощения в УФ-части спектра.
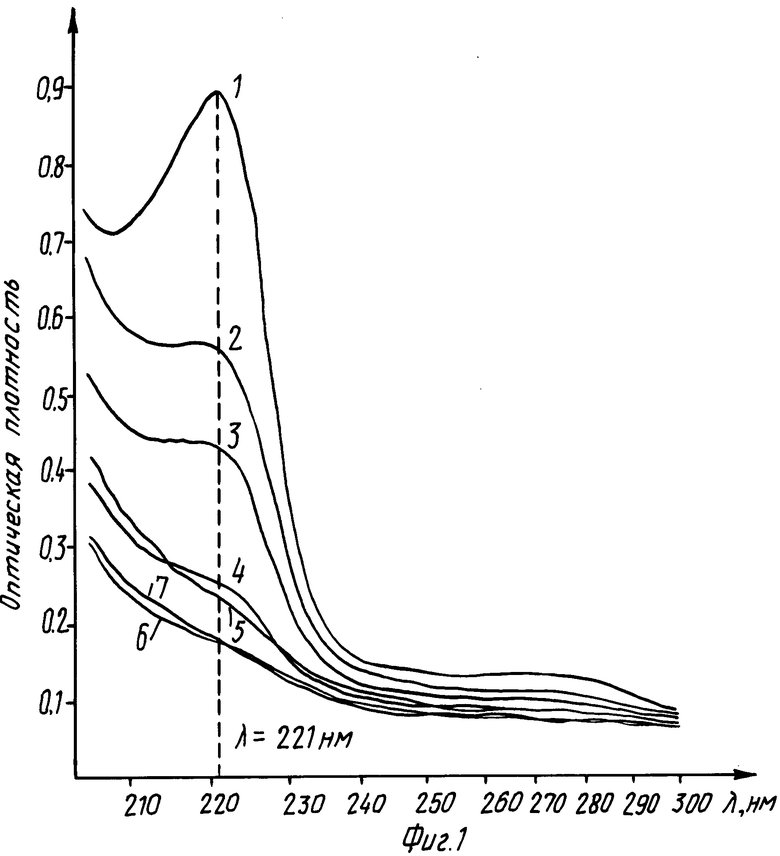
На фиг. 1 приведены спектрограммы оптической плотности образцов ПФОС на участке УФ-спектра 200-300 нм, очищенных с помощью различного количества этилового спирта; на фиг.2 кривая зависимости степени очистки ПФОС от количества спирта, взятого в процентах от объема ПФОС, определенная для длины волны 221 нм.
Кривые оптической плотности ПФОС, очищенного спиртом (см.фиг.1), обозначены в зависимости от различного количества спирта, взятого в процентах от объема ПФОС:
1 количество спирта равно 0% от объема ПФОС;
2 количество спирта равно 5% от объема ПФОС (спирт/ПФД=1:20);
3 количество спирта равно 15% от объема ПФОС (спирт/ПФД=3:20);
4 количество спирта равно 25% от объема ПФОС (спирт/ПФД=1:4);
5 количество спирта равно 50% от объема ПФОС (спирт/ПФД=1:2)
6 количество спирта равно 75% от объема ПФОС (спирт/ПФД=3:4);
7 количество спирта равно 100% от объема ПФОС (спирт/ПФД=1:1).
На кривых хорошо заметен пик поглощения на длине волны 221 нм, который принадлежит пирогенам, находящимся в ПФОС. С увеличением количества спирта удаляется все возрастающее количество пирогенов, что выражается в уменьшении пика поглощения на длине волны 221 нм. Из анализа этих кривых видно, что степень очистки ПФОС прямо зависит от количества спирта.
За 100% очистки взята степень очистки при количестве спирта, равном 100% от объема ПФОС (соотношение спирт/ПФОС 1:1). Степень очистки ПФОС при построении кривой (см.фиг.2) вычислялась по формуле
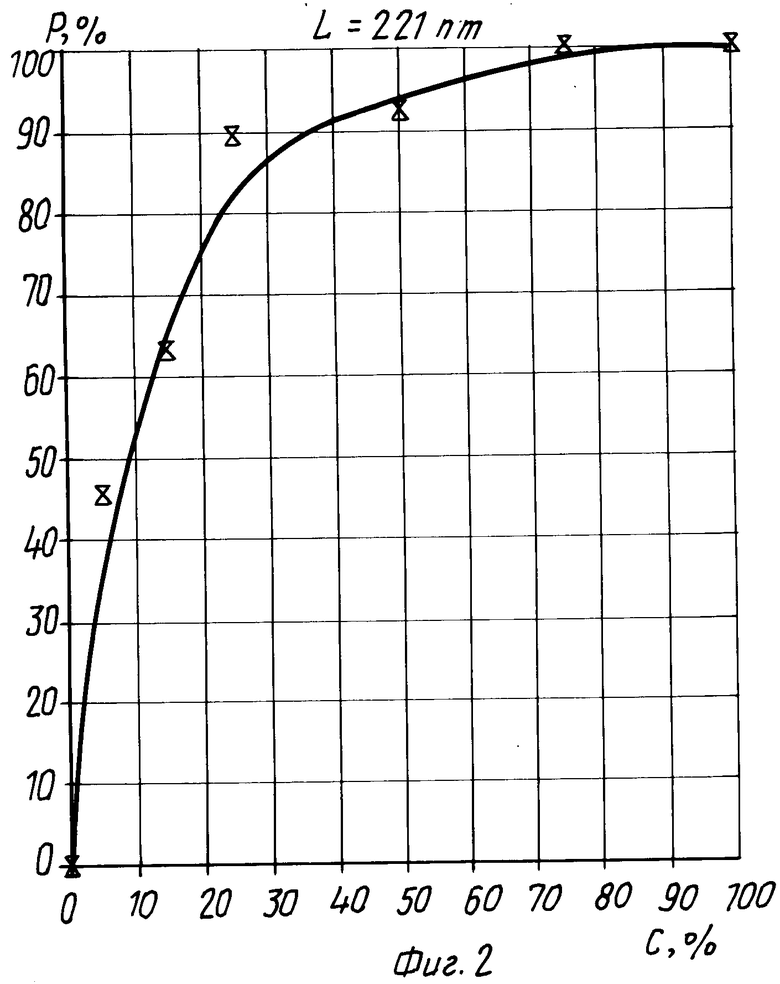
Pi= 1- 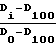 · 100% 100% где Рi степень очистки ПФОС в процентах;
· 100% 100% где Рi степень очистки ПФОС в процентах;
Di оптическая плотность на длине волны 221 нм i-го образца;
Dо оптическая плотность на длине волны 221 нм неочищенного образца (0% спирта);
D100 оптическая плотность на длине волны 221 нм образца очищенного 100% спирта.
Из фиг.2 видно, что степень очистки ПФОС нелинейно зависит от количества этилового спирта и становится выше уровня в 90% при количестве спирта, взятого более 40% от количества ПФОС, а 100% уровень очистки достигается уже при количестве спирта более 75% Отсюда следует, что апирогенная очистка ПФОС достигается при количестве этилового спирта более 40% от количества ПФОС.
На основании проведенных экспериментов установлено, что степень очистки не зависит от времени перемешивания и слабо зависит от интенсивности перемешивания (скорости вращения вала электромеханического смесительного устройства).
П р и м е р 1. В чистую и стерильную емкость электромеханического смесительного устройства объемом 10 л заливают 5 л перфтордекалина (ПФД). Туда же наливают 4,5 л этилового спирта-ректификата, т.е. получается соотношение ПФОС к спирту, равное 1:0,9. Затем включают электромеханическое смесительное устройство со скоростью вращения вала 3000 об/мин и перемешивают ПФОС со спиртом в течение 5 мин. Затем дают отстояться ПФОС в течение 10-15 мин для удаления газов из ПФОС и оседания частиц ПФОС из спирта и наблюдают границу раздела фаз между спиртом и перфтордекалином. После этого ПФД, который находится внизу, отделяют от спирта. Затем к ПФОС, находящемуся в емкости смесительного устройства, приливают 4,5 л апирогенной воды, т.е. соотношение ПФОС и воды 1:1, и перемешивают с помощью электромеханического смесительного устройства 5 мин при скорости вращения вала 3000 об/мин. Затем дают отстояться ПФОС 10-15 мин для удаления газов из ПФОС и оседания частиц ПФОС из воды и наблюдают границу раздела фаз между водой и перфтордекалином. Очищенный перфтордекалин отделяют от апирогенной воды и разливают по флаконам, закупоривают под закатку и автоклавируют при 120оС 25 мин.
П р и м е р 2. В чистую и стерильную емкость электромеханического смесительного устройства объемом 10 л заливают 0,5 л перфтортрибутиламина (ПФТБА). Туда же наливают 0,2 л этилового спирта-ректификата, т.е. соотношение ПФОС к спирту 1:0,4. Затем включают электромеханическое смесительное устройство со скоростью вращения вала 50 об/мин и перемешивают ПФОС со спиртом в течение 1 мин. Затем дают отстояться ПФОС в течение 5 мин для удаления газов из ПФОС и оседания частиц ПФОС из спирта и наблюдают границу раздела фаз между спиртом и перфтордекалином. После этого ПФД, который находится внизу, отделяют от спирта. Затем к ПФОС, находящемуся в емкости смесительного устройства, приливают 0,5 л апирогенной воды, т.е. соотношение ПФОС и воды 1: 1, и перемешивают с помощью электромеханического смесительного устройства в течение 1 мин при скорости вращения вала 50 об/мин. Затем дают отстояться ПФОС в течение 5 мин для удаления газов из ПФОС и оседания частиц ПФОС из воды и наблюдают границу раздела фаз между водой и перфтордекалином. Очищенный перфтордекалин отделяют от апирогенной воды и разливают по флаконам, закупоривают под закатку и автоклавируют при 120оС в течение 25 мин.
П р и м е р 3. Условия осуществления способа те же, что в примерах 1 и 2, но для очистки берут 5 л препарата перфторпараметилциклогексилпиперидина, 3,5 л спирта соотношение ПФОС/спирт 1:0,7 и 5 л апирогенной воды соотношение ПФОС/воды 1: 1. Скорость вращения вала электромеханического смесительного устройства в течение 3 мин 1000 об/мин.После перемешивания со спиртом и после перемешивания с апирогенной водой производится отстаивание в течение 10 мин.
Процесс легко поддается масштабированию и автоматизации.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ очистки жидких перфторорганических соединений | 2022 |
|
RU2806825C1 |
| ЭМУЛЬСИЯ ПЕРФТОРОРГАНИЧЕСКИХ СОЕДИНЕНИЙ С ГАЗОТРАНСПОРТНЫМИ СВОЙСТВАМИ, ПОВЕРХНОСТНО-АКТИВНОЕ ВЕЩЕСТВО ДЛЯ ЭТОЙ ЭМУЛЬСИИ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2002 |
|
RU2305543C2 |
| ЭМУЛЬСИЯ ПЕРФТОРОРГАНИЧЕСКИХ СОЕДИНЕНИЙ С ГАЗОТРАНСПОРТНЫМИ СВОЙСТВАМИ | 2003 |
|
RU2240108C1 |
| ЭМУЛЬСИЯ ПЕРФТОРОРГАНИЧЕСКИХ СОЕДИНЕНИЙ С ГАЗОТРАНСПОРТНЫМИ СВОЙСТВАМИ | 1993 |
|
RU2088217C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРФТОРУГЛЕРОДНЫХ ЭМУЛЬСИЙ ДЛЯ МЕДИЦИНСКИХ ЦЕЛЕЙ | 1994 |
|
RU2070033C1 |
| ЭМУЛЬСИЯ ПЕРФТОРОРГАНИЧЕСКИХ СОЕДИНЕНИЙ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ, СПОСОБ ЕЕ ПРИГОТОВЛЕНИЯ И СПОСОБ ЕЕ ПРИМЕНЕНИЯ | 2006 |
|
RU2393849C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ СТЕРИЛЬНОЙ ЭМУЛЬСИИ ПЕРФТОРОРГАНИЧЕСКИХ СОЕДИНЕНИЙ И ПОЛИЭЛЕКТРОЛИТОВ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2022 |
|
RU2811867C1 |
| ЭМУЛЬСИЯ ПЕРФТОРОРГАНИЧЕСКИХ СОЕДИНЕНИЙ С ГАЗОТРАНСПОРТНЫМИ СВОЙСТВАМИ | 2011 |
|
RU2469714C1 |
| ВЫСОКОДИСПЕРСНАЯ ЭМУЛЬСИЯ НА ОСНОВЕ ПЕРФТОРОРГАНИЧЕСКИХ СОЕДИНЕНИЙ С ГАЗОТРАНСПОРТНЫМИ СВОЙСТВАМИ | 2016 |
|
RU2631608C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ СТЕРИЛЬНОЙ ЭМУЛЬСИИ ПЕРФТОРОРГАНИЧЕСКИХ СОЕДИНЕНИЙ И ПОЛИЭЛЕКТРОЛИТОВ | 2023 |
|
RU2828256C1 |
Использование: в производстве перфторорганических веществ, в частности в способе очистки жидких перфторорганических соединений (ПФОС) для синтеза био- и медпрепаратов, например кровезаменителей. Сущность изобретения: способ предусматривает следующую последовательность операций: этанол и ПФОС (объемное соотношение (0,4 1) (1 1) перемешивают с помощью электромеханического смесительного устройства 1 5 мин при скорости вращения вала смесительного устройства 50 300 об/мин, отделяют слой ПФОС, перемешивают отделенный слой ПФОС с апирогенной водой (объемное соотношение 1 1) с помощью электромеханического смесительного устройства в течение 1 5 мин при скорости вращения вала смесительного устройства 50 300 об/мин. Далее проводят отстой смеси 5 15 мн и отделяют нижний очищенный жидкий продукт ПФОС. Степень очистки выше 90% при количестве спирта, взятого в количестве выше 40% от количества ПФОС. 2 ил.
СПОСОБ ОЧИСТКИ ЖИДКИХ ПЕРФТОРОРГАНИЧЕСКИХ СОЕДИНЕНИЙ, включающий приведение в контакт с сорбентом с последующим отделением от сорбента и автоклавированием, отличающийся тем, что в качестве сорбента используют сначала этиловый спирт, взятый в объемном соотношении с очищаемой жидкостью от 0,4:1 до 1: 1, который перемешивают с помощью электромеханического смесительного устройства в течение 1-5 мин при скорости вращения вала смесительного устройства от 50 до 3000 об/мин, и затем после отделения слоя перфторорганического соединения в качестве сорбента используют апирогенную воду, взятую в объемном соотношении с очищаемой жидкостью 1:1, которую перемешивают с помощью электромеханического смесительного устройства в течение 1-5 мин при скорости вращения вала 50-3000 об./мин, после чего производят отстой смеси в течение 10-15 мин, а отделение целевого продукта осуществляют из нижнего слоя.
| Александрова А.Е., Богомольный В.Я., Васильев А.В | |||
| и др | |||
| Хим.фарм.журнал, 1982, т.16, N 7, с.846-851. |
Авторы
Даты
1995-09-10—Публикация
1993-05-25—Подача