Изобретение относится к энергетике, прямому преобразованию химической энергии в электрическую и может быть использовано в электрохимии для измерения составов сред в качестве измерительного преобразователя концентрации окислителя или восстановителя в среде.
Аналогом изобретения в термоэмиссионной части является термоэмиссионный преобразователь (ТЭП) с микрозазором между эмиттером и коллектором [1] Реализация в ТЭП зазора не менее 10 мкм создает условия прохождения эмиттированных электронов через тонкое "облако электронов", удерживаемых у катода положительным зарядом катода, образовавшимся в результате термоэмиссии электронов из катода. Промышленного применения ТЭП с микрозазором не получили из-за трудности создания и поддержания микрозазора в условиях высокой температуры, неизбежных термомеханических процессов. Основным достоинством ТЭП является перенос тока с эмиттера к коллектору без электрических потерь. Основным недостатком ТЭП является трудность создания и поддержания микрозазора между электродами.
Наиболее близким к заявляемому устройству является электрохимический элемент (ЭХЭ) с высокотемпературным твердым электролитом с преобразованием химической энергии реагентов в электроэнергию или термоэлектрохимический (ТЭХЭ), преобразовывающий тепло в электроэнергию с циклом Карно [2] В ЭХЭ пористый катод и пористый анод плотно соединены с ионопроводящим электролитом, который не должен иметь электронной значимой проводимости и не должен допускать смешения окислителя и восстановителя, то есть не иметь сквозной пористости. Электроды ЭХЭ должны обладать достаточной электропроводностью, пропускать реагенты, обладать каталитическими свойствами. В современных высокотемпературных ЭХЭ толщина электродов и электролита составляет около 0,1 мм, что требует применения несущей пористой основы. Несколько слоев из разных материалов с многими регламентированными параметрами создают высокие требования к технологии и условиям эксплуатации.
Основным достоинством ЭХЭ является гарантия отсутствия механического касания анода с катодом (слой электролита). Однако диффузия материалов из состава электродов в электролит ограничивает уменьшение толщины электролита из-за появления электронной проводимости. Основным недостатком ЭХЭ являются трудности технологии плотного соединения разнородных пористых и плотных слоев элемента при соблюдении нескольких видов совместимости, проблемы надежности ЭХЭ и батареи ЭХЭ с учетом межэлементной коммутации.
Известен способ эксплуатации ЭХЭ, заключающийся в подаче реагентов на поверхности электродов и удалении продуктов реакции [3] Недостатком известного способа является то, что он предоставляет недостаточные возможности для создания различных конструктивных вариантов ЭХЭ, например, с модуляцией реагентов с высокой частотой для получения переменного тока.
Задача изобретения создание электрохимического элемента и способа его эксплуатации с более полным использованием преимуществ ТЭП и ЭХЭ при устранении их недостатков.
Для решения этой задачи предлагается в электрохимическом элементе, состоящем из катода и анода, разделенных электролитом, электролит выполнить со сквозной пористостью более 5, но менее 100% В частности, электролит может быть выполнен из дискретных тел. Предлагается изготовить, как минимум, один из электролитов газоплотным. ЭХЭ может быть снабжен дистанционаторами, выполненными из электролита. Поверхность катода может быть выполнена из материала с работой выхода электрона меньшей, чем работа выхода электрона из материала поверхности анода. Катод и анод могут быть конструктивно выполнены на общей подложке, а подложка изготовлена из эластичного материала.
Для решения поставленной задачи в способе эксплуатации ЭХЭ, заключающемся в подаче реагентов на поверхности электродов и удалении продуктов реакции, предлагается подавать реагенты и отводить продукты реакции по межэлектродному зазору, который предложено поддерживать меньше толщины слоя прикатодных ионов реагента. Реагенты могут быть подаваемы периодически, причем сначала подают окислитель, а затем восстановитель. Предлагается также температуру катода поддерживать выше температуры анода.
На фиг. 1 представлен термоэмиссионный электрод и эмиттированные электроны; на фиг. 2 термоэмиссионный электрод со связанным в анионах окислителем; на фиг.3 ТЭЭХЭ с ионным проводником; на фиг.4 ТЭЭХЭ без ионного проводника; на фиг.5 схема батареи ТЭЭХЭ.
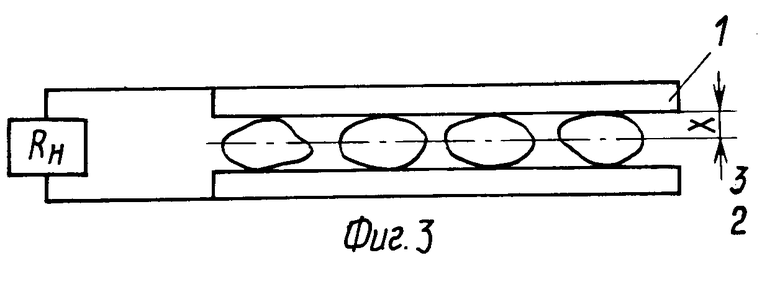
Термоэмиссия электронов из эмиттера 1 (фиг. 1) создает двойной электрический слой у поверхности эмиттера: в эмиттере положительный заряд, у поверхности эмиттера -"связанный" отрицательный заряд в виде "облака электронов" при значимой толщине "облака" около 10 мкм [1] Такой связанный отрицательно заряженный слой электронов у поверхности эмиттеров создает потенциальный, полевой барьер для прохождения отрицательно заряженных частиц от электрода. Применительно к ТЭЭХЭ (термоэмиссионный электрохимический элемент) этот слой-барьер будет удерживать отрицательно заряженные частицы (электроны и ионы). На фиг.1 показан эмиттер-катод, окруженный "облаком" электронов со значимой толщиной 10 мкм. На фиг.2 показан эмиттер-катод 1, окруженный "облаком ионов" кислорода, которые связаны как и эмиттированные электроны равенством положительного заряда в эмиттере с общим зарядом ионов кислорода. Толщина "облака ионов" кислорода X будет отличаться от толщины 10 мкм для электронов, будет зависеть от температуры, динамики движения ионов. Если для некоторого стационарного состояния (фиг. 3) подача кислорода не избыточна относительно числа эмиттированных электронов, то весь кислород будет удерживаться возле эмиттера положительным зарядом эмиттера, то есть независимо от электролита, его плотности-герметичности. Между эмиттером-катодом 1 и анодом 2 (фиг.3) расположены гранулы 3 проводника ионов кислорода, которые в верхней части находятся в облаке кислорода, а в нижней части контактируют с пористым (каталитическим) анодом 2.
Устройство работает, а способ осуществляют следующим образом.
К аноду 2 подводится восстановитель в количестве не большем потребного для соединения с кислородом, который в виде ионов под действием разницы концентрации ионов в областях катода 1 и анода 2 движется к аноду в ионном проводнике. Ионы кислорода могут достигать при соответственном расстоянии между анодом 2 и катодом 1 анода, минуя электролит. Ионы кислорода имеют заполненную валентную оболочку и не могут вступать в реакцию с восстановителем вне контакта с анодом или катодом, на которые можно отдать излишние электроны. Ионы проводимости по ионному проводнику подходят к каталитическому аноду 2 (фиг.3), где отдают в ходе окисления восстановителя избыточные электроны аноду, откуда через полезную нагрузку электроны возвращаются на катод, эмиттеруют, что завершает цикл движения электронов.
Температура катода и анода может быть равной, так как преобразуется не тепловая, а химическая энергия. Анод в общем решении не несет задач эмиссии, создавая поля ионов и может быть выполнен из материала с малой термоэмиссией. Наличие слоя эмиттированных электронов на аноде для восстановителя не существенно, так как он избыточен (валентен) по отдаче электронов не существенно и для ЭДС, которую определяет соотношение концентрации ионов проводимости.
В изобретении (фиг.3) у ионного проводника снята функция разделения окислителя и восстановителя за счет использования пристеночного связанного заряда эмиттера (электрического поля) при условии правильного дозирования окислителя. Заметим, что восстановитель не может реагировать с ионом окислителя, если проводником электронов не отводить избыточные электроны. То есть окислительно-восстановительная химреакция номинально возможна только в зоне анода (ионы кислорода +проводник+восстановитель), на поверхности электролита (боковой) без электронного проводника реакции невозможна. На катоде реакция возможна. Продукты химреакции могут отводится традиционно для ЭХЭ в полость подачи восстановителя и (или) через межэлектродное пространство, не занятое ионным проводником.
Возможность использовать пространство между катодом и анодом за счет устранения электролита дает принципиально отличные от прототипа важные схемные решения:
можно выполнить герметичным катод и окислитель подать через межэлектродное пространство;
можно выполнить герметичным анод и восстановитель подать через межэлектродное пространство;
можно выполнить герметичным анод и катод, подать смесь окислителя и восстановителя совместно при условии, что эта смесь не реагирует в объеме при заданной концентрации, но реагирует на каталитическом аноде.
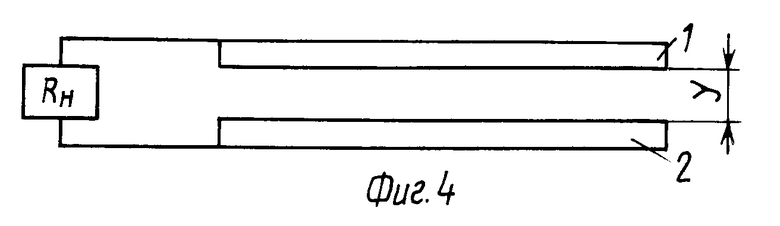
можно использовать межэлектродное пространство для удаления продуктов реакции. Отказ от пористых проницаемых электродов создает условия для быстрого ввода и удаления реагентов, что позволит генерировать пульсирующий ток, например, с частотой 50 Гц и трансформировать ток на высокое напряжение. Возможно расширить область концентрированных соотношений реагентов, если подавать вначале окислитель, ионизировать его присоединением электронов, а затем подавать восстановитель для завершения токообразующей реакции на аноде. На фиг.4 показана схема ТЭЭХЭ без электролита. Если размер Y, толщина слоя ионов окислителя (фиг.4) превышает расстояние между анодом 2 и катодом 1, то окислительно-восстановительная реакция на каталитическом аноде при соответственном балансу дозировании реагентов пройдет без участия ионного проводника. Роль ионного проводника в такой схеме исполняет пристеночное "облако ионов" окислителя возле катода и электрическое поле.
Поскольку между анодом и катодом ТЭЭХЭ в предлагаемой конструкции освобождается полость, возможно ее использование для транспортировки реагентов и продуктов реакции. Рассмотрим вариант решения, когда полость имеет давление газов меньше, чем давление цепной химической реакции подаваемых окислителя и восстановителя. При таком решении существенно повышается надежность ТЭЭХЭ:
невозможно смешение окислителя и восстановителя при их высоком давлении, то есть исключено излишнее объемное энерговыделение (в том числе взрыв);
возможно установление давления реагентов, при котором их реакция в газовой фазе не идет, реакция идет только на каталитических элементах;
возможно изготовление анода 2, катода 1 герметичными, когда смесь реагентов подводится и отводится по межэлектродной полости.
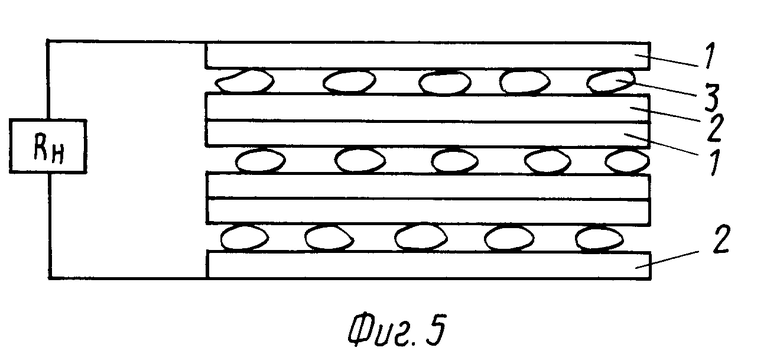
Согласно [3] предел воспламенения водорода в воздухе соответствует 4 - 75% в кислороде 4 95% объемных. Выбор состава позволяет подать смесь, которая будет реагировать основной массой только на электродах ТЭЭХЭ. Такое решение позволяет компоновать ТЭЭХЭ в батарею с последовательным соединением элементов, где анод и катод объединены в единый блок. На фиг.5 показана компоновка батареи с блоками анодов 2 и катодов 1. Катод-анодные блоки, концевые катоды и аноды батареи дистанционированы изоляторами.
Изобретение имеет преимущества перед аналогами с плотным (сплошным) электролитом:
повышается надежность ЭХЭ (электрогенерирующий элемент) из-за снятия требования по герметичности электролита;
радикально упрощается технология изготовления, в частности без электролита;
становятся реальными плотноупакованные плоские ЭХЭ [2] которые радикально ограничены термомеханикой электролита;
возможно отводить продукты химреакции по межэлектродному пространству, свободному от электролита;
при использовании ЭХЭ в качестве измерительного преобразователя исключение электролита исключает "дрейф" характеристик электролита. Пример осуществления показан для ТЭЭХЭ по схеме фиг.3. Пористый катод 1 нагрет до температуры, достаточной для значимой термоэмиссии электронов. По закону постоянства электрического заряда в катоде 1 после эмиссии электронов остается положительный заряд, удерживающий электроны эмиссии возле поверхности катода. Подается кислород на пористый каталитический катод 1. Температура и катализатор (например, тончайший слой платины или каталитической керамики) разрушают молекулу кислорода. Атомы кислорода могут превратиться в ион в "тройной точке" контакта электролит+атом кислорода+электронное облако катода 1. Концентрация ионов кислорода в анионном проводнике-электролите 3 со стороны катода повышается. Некоторый возможный избыток атомов кислорода в "облаке эмиттированных электронов" толщиной X (порядка 10 мкм) ионизируется и в качестве ионов удерживается у катода 1. Ионы кислорода в электрическом поле возле катода являются динамическим резервом восстановления высокой концентрации ионов кислорода в электролите возле катода. Восстановитель подается через пористый каталитический анод 2. В "тройной точке" контакта электролит+восстановитель (например водород)+электропроводный анод 2 проходит окисление восстановителя-топлива. Избыточные электроны, принесенные анионом, заряжают отрицательно (избыток электронов) анод и могут быть поданы через полезную нагрузку внешней электроцепью на катод, где уменьшится положительный заряд, что приведет к термоэмиссии электронов в катоде, увеличение числа ионов кислорода (цикл).
Эмиссия электронов анодом не ионизирует восстановитель. В зависимости от удельной подачи восстановителя часть его электронейтральных атомов (молекул) подается к катоду, где сгорают непосредственно на поверхности катода, чем обеспечивается необходимый приток тепла для обеспечения энергозатрат на эмиссию электронов. При взаимодействии (смешении) ионов кислорода и восстановителя окислительно-восстановительная химреакция (то есть горение) возможно только в контакте с электронопроводным электродом (катодом и анодом). В отличие от ЭХЭ с герметичным слоем электролита ТЭЭХЭ требует подвода тепла к катоду, что возможно внешним подогревом, но более системно-конструктивно достигается сжиганием реагентов на самом катоде. Для сжигания с тепловыделением между электродами в самом элементе требуется проницаемость мембраны электролита для реагентов не в ионном состоянии. Таким образом, для ТЭЭХЭ с внутренним тепловыделением непригоден газогерметичный ЭХЭ.
Второй пример осуществления приведен для схемы ТЭЭХЭ с межэлектродным тепловыделением по фиг.4. Окислитель подводится к горячему пористому каталитическому катоду 1. Окислитель присоединяет свободные эмиттированные электроны, и ионы окислителя образуют "облако ионов", связанных положительным зарядом катода. Катод 1 располагают эквидистантно аноду 2 на расстоянии "Y", меньшем толщины "облака ионов". Через анод 2 каталитический газопроницаемый подают восстановитель. Электрохимический потенциал окислительно-восстановительной реакции реализуется на аноде с передачей электронопроводному аноду эмиссионного электрона, перенесенного анионом с катода. Электроны с анода через полезную нагрузку возвращаются для эмиссии на катод. Для подвода тепла эмиссии расход окислителя должен превышать потребность его ионизации электронами эмиссии. Восстановитель подают в соответственном количестве. Отметим нежелательность высокой термоэмиссии с анода, что достижимо подбором материалов и (или) переносом тепловыделения на катод. Зазор между анодом и катодом может служить трактом удаления продуктов реакции.
Поскольку скорости ионов в газе и возможном прямопролетном режиме превышают скорости ионов в твердом теле в тысячи раз, можно ожидать соответствующего увеличения мощности ТЭЭХЭ в импульсе. В стационарном режиме будет ограничение по подводу тепла к катоду-эмиттеру, эмиссионное ограничение. Эмиссионный ток может быть до 50 150 А/см2. Отметим возможности работы ТЭЭХЭ в импульсном режиме с заданной частотой. В ракетной технике разработаны высококачественные клапаны с высоким ресурсом и надежностью для подачи реагентов, которые могут обеспечить порционное дозирование реагентов с частотой, достаточной для успешной трансформации тока ТЭЭХЭ.
Приведем пример осуществления по ТЭЭХЭ без электролита по фиг.5 с подачей смеси реагентов в межэлектродный промежуток. Исходное состояние: батарея ТЭЭХЭ нагрета до 1000oC; зазор между катодом эмиттером 1 и анодом 2 менее 10 мкм; подается смесь кислорода и водорода при давлении, исключающем цепную химическую реакцию в объеме смеси. Эмиттер катод с работой выхода электронов около 2 эВ эмиттировал электроны, которые "перекрыли" зазор 10 мкм. Поступающий в смеси кислород имеет сродство к электронам и ионизируется. После ионизации соединение кислорода с водородом возможно только на электродах. Отрицательный приэлектродный заряд тем больше, чем больше плотность термоэмиссии электронов. При равной температуре катода и анода на аноде следует обеспечить материал с большей, чем на катоде, работой выхода электронов. Поэтому подавляющая часть кислорода в виде ионов и водорода встретятся у анода, где произойдет реакция (катализированная анодом) с выделением кислородом избыточных электронов на аноде. Эти избыточные электроны были эмиттированы катодом. После химреакции электроны через нагрузку возвратятся на катод, чем замыкается цикл.
Заметим, что возможно осуществить процесс электрохимической генерации электроэнергии при одинаковых работах выхода катода и анода, если температуру анода держать ниже температуры катода. Если смесь в межэлектродный зазор подавать порциями, то будет генерироваться пульсирующий (переменный) ток.
При поддержании перепада температуры возможно осуществление ТЭЭХЭ с однокомпонентным реагентом, например с натрием. Приведем пример для схемы по фиг.3. В этой схеме 3-шранулы электролита из натрий-бета-глинозема диаметром больше 10 мкм. В зоне катода 1 осуществляется контакт электролитных ионов натрия и эмиттированных электронов, натрий восстанавливается и в виде пара идет на анод 2, где конденсируется, отдает электрон аноду, в виде иона диффундирует по глинозему в область катода, обедненную ионами натрия. Цикл замкнут. Преобразователь этого типа ограничен по КПД тепловым циклом (тепловая машина).
Изобретение предлагает схемные решения, которые могут быть реализованы в результате фундаментальных НИР и ОКР. Приведем некоторые оценки потенциала реализации изобретения:
огромный задел по ЭХЭ с твердым электролитом на уровень температур 1000oC;
большой задел по термоэмиссии;
созданы материалы типа пирографита, способные работать при температурах до 2500o 3000oC, что обеспечит достаточную термоэмиссию;
созданы жаростойкие покрытия для высоких температур, композиты;
создан арсенал высокочастотных клапанов для дозирования реагентов.
Описанное выше устройство высокотемпературного ТЭЭХЭ, способ его действия могут с успехом применяться для электрохимических реакций. При подводе электрической мощности к элементу от внешнего источника расширяются возможности регулирования эмиссии, электронных и ионных потоков.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭЛЕКТРОХИМИЧЕСКИЙ ЭЛЕМЕНТ С ТВЕРДЫМ ЭЛЕКТРОЛИТОМ | 2008 |
|
RU2380794C1 |
| ЭЛЕКТРОХИМИЧЕСКИЙ ЭЛЕМЕНТ С ТВЕРДЫМ ЭЛЕКТРОЛИТОМ | 1993 |
|
RU2037918C1 |
| ТЕРМОЭМИССИОННЫЙ ПРЕОБРАЗОВАТЕЛЬ | 1996 |
|
RU2096859C1 |
| ТВЕРДООКСИДНЫЙ ТОПЛИВНЫЙ ЭЛЕМЕНТ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2000 |
|
RU2197039C2 |
| ТВЕРДООКСИДНЫЙ ТОПЛИВНЫЙ ЭЛЕМЕНТ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 1997 |
|
RU2128384C1 |
| ВЫСОКОАКТИВНАЯ МНОГОСЛОЙНАЯ ТОНКОПЛЕНОЧНАЯ КЕРАМИЧЕСКАЯ СТРУКТУРА АКТИВНОЙ ЧАСТИ ЭЛЕМЕНТОВ ТВЕРДООКСИДНЫХ УСТРОЙСТВ | 2016 |
|
RU2662227C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭЛЕКТРИЧЕСКОЙ ЭНЕРГИИ | 2005 |
|
RU2308125C1 |
| ЭЛЕКТРОХИМИЧЕСКИЙ ЭЛЕМЕНТ С ЖИДКИМ АНОДОМ | 2005 |
|
RU2361329C2 |
| БАТАРЕЯ ТОПЛИВНЫХ ЭЛЕМЕНТОВ | 2007 |
|
RU2353025C1 |
| СПОСОБ ОЧИСТКИ СТОЧНЫХ ВОД ОТ НЕФТЕПРОДУКТОВ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2006 |
|
RU2340563C2 |
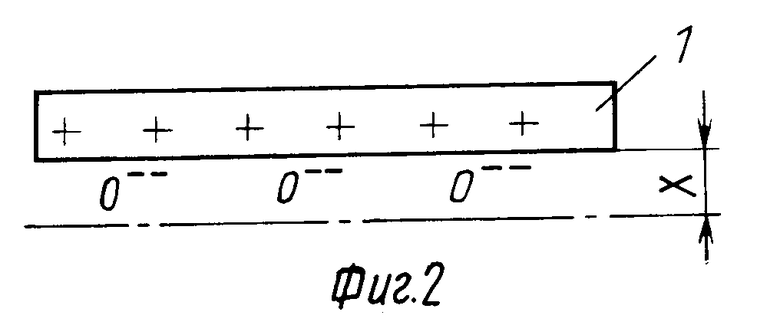
Использование: прямое преобразование химической энергии в электрическую. Сущность изобретения: электрохимический элемент (ЭХЭ) состоит из катода и анода, разделенных электролитом. Отличительной особенностью ЭХЭ является то, что электролит выполнен со сквозной пористостью в пределах более 5 и менее 100%. Возможно изготовление электролита из дискретных тел. Подачу реагентов на поверхность электродов и удаление продуктов реакции осуществляют по межэлектродному зазору. Реагенты могут подавать периодически, сначала окислитель, затем восстановитель. Температуру катода поддерживают выше температуры анода. Смесь реагентов подают при давлении, исключающем цепную химическую реакцию в газовой фазе. 5 ил.
2. Элемент по п.1, отличающийся тем, что электролит выполнен из дискретных тел.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Термоэмиссионные преобразователи и низкотемпературная плазма | |||
| /Под ред | |||
| Мойжес Б.Я., Пикус Г.Е | |||
| - М., 1973, с | |||
| Способ крашения тканей | 1922 |
|
SU62A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Коровин Н.В | |||
| Электрохимическая энергетика | |||
| - М.: Энергоатомиздат, 1991, с.89 и 91 | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Шпильрайн Э.Э., Малышко С.П., Кулешов Г.Г | |||
| Введение в водородную энергетику | |||
| - М.: Энергоатомиздат, 1984, с.21. | |||
Авторы
Даты
1997-07-10—Публикация
1995-09-22—Подача