Изобретение относится к кремнийорганическим соединениям, а именно к области фторсодержащих циклотрисилоксанов общей формулы:
[RfSi(CH3)O]3
где
которые могут использоваться как промежуточные соединения в синтезе фторсилоксановых полимеров, применяемых для изготовления резино-технических изделий, использующихся в кабельной, авиационной, автомобильной и других отраслях промышленности.
Известны 1,3,5-триметил-1,3,5 трис(полифторалкил) циклотрисилоксаны общей формулы: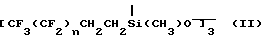
где n 1-10
(пат. ФРГ 3.248.546А1, СА, 101, 172333 F, 1984), получаемые гидролизом соответствующих (полифторалкил)метилдихлорсиланов. По данным (Pierce O.R. Holbrook G.W. Iohannson O.K. Ind. Eng.Chem. 1960, 52, 783-784), полимеры на основе данных циклосилоксанов обладают хорошей маслобензостойкостью - набухание в толуоле за 24 ч при 20 oC составляет 21 25 об. Однако термостойкость таких полимеров невысока, так, по данным авторов настоящей заявки, 13 -я потеря в весе наступает уже при 200 oC.
Известен 1,3,5-триметил-1,3,5 трис(2',2',3',3'-тетрафторциклобутил) циклотрисилоксан (пат. Великобритании 706 201, СА, 51, 14796i, 1957) формулы
получаемый гидролизом соответствующего 2,2,3,3-циклобутилметилдихлорсилана. Однако полимер, полученный на основе данного циклотрисилоксана, обладает недостаточной маслобензостойкостью. Так, по данным авторов настоящей заявки, набухание в толуоле за 24 ч при 20 oC составляет 38 39 об.
Наиболее близким аналогом по своему назначению к предлагаемым соединениям является 1,3,5-триметил-1,3,5-трис(3,3,3 трифторпропил)циклотрислоксан формулы:
(Iarrant P. Dycker G.W. Dunmire R. Butler G.B. JACS, 79, 6536, 1957), получаемый гидролизом соответствующего (3,3,3 - трифторпропил)метилдихлорсилана с выходом 30 Полимер на основе данного циклотрисилоксана обладает хорошей маслобензостойкостью: набухание в толуоле за 24 ч при 20 oC составляет 21 об. (Pierce O.R. Hopbrook G.W. Johannson O.K. Ind. Eng. Chem. 1960, 52, 783-784). Однако по данным (Коршак В.В. Термостойкие полимеры, М. "Наука", 1969, с.78), термостойкость их невысока: 13-я потеря в весе наступает при 270 oC, интервал рабочих температур от -68 oC до +205 oC (там же, с.338).
Целью данного изобретения является синтез доступных фторсодержащих алкилметилциклотрисилоксанов, способных использоваться для получения полимеров, сочетающих высокую термостойкость и хорошую маслобензостойкость.
Поставленная цель достигается синтезом соединений общей формулы I.
Описываемые соединения получают гидролизом соответствующих метил(гексафторалкил)дихлорсиланов двууглекислым натрием в присутствии пиридина при мольном соотношении реагентов 1 1 1 в среде ацетона при 20 - 25 oC. Реакционную массу перемешивают в течение 3 ч, после чего отфильтровывают осадок солей, отгоняют ацетон и вакуумной ректификацией выделяют целевой продукт. Выход составляет 50-60
Состав и структуру полученных соединений подтверждают элементным анализом и методом ЯМР 1H, 19F и 29Si спектроскопии. Все отнесения сделаны на основе (Эмсли Дж. Финей Дж. Сатклифф Л. Спектры ЯМР высокого разрешения, Т.1,2. М. Мир, 1968). Исходные метил(гексафторалкил)дихлорсиланы получают реакцией гидросилилирования соответствующих гексафторолефинов метилдихлорсиланом при мольном соотношении реагентов 1:1,05-1,25 соответственно в присутствии катализатора Спайера при температуре 150 oC.
Пример 1. В колбу емкостью 1 л, снабженную мешалкой, капельной воронкой и термометром, помещают 84 г (1 моль) NaHCO3, 79,1 г (1 моль) пиридина и 420 мл ацетона. К смеси в течение 1 ч при 20 25 oC и перемешивании добавляют 235 мл (319 г, 1 моль) метил-(2,2,3-трифтор-3-трифторметилциклобутил)этилдихлорсилана в 80 мл ацетона. Затем смесь перемешивают еще 3 ч, отфильтровывают от осадка солей, отгоняют ацетон на водяной бане и получают 251 г (95) гидролизата. Циклотрисилоксан выделяют вакуумной ректификацией. Получают 132 г (50) целевого продукта. T кип. 220 oC/2 мм рт.ст. n
Вычислено, Si 10,94; C 36,23; F 43,03; O 6,03; H 3,77.
Найдено, Si 10,95; C 36,15; F 43,11; O 6,10; H- 3,90.
Мол.вес 265.
Спектр ЯМР 19F (в (CD3)2CO, δ м.д.): 73,87 (3F, 3-CF3).
АВ-спектр: dA-100,25, δB-116,67, JAB 228 Гц (2 F, 2-CF2); 170,67 (1F, 3- CF).
Спектр ЯМР 1H (в (CD3)2CO, δ м.д.): 0,45 (3H, Si-CH3), 0,64 (2H, 1-CH2), 1,4 (2H, 2-CH2); 1,65 (1H, 1'-CH), 2,18 (2H, 4'-CH2).
Спектр ЯМР 29Si (в (CD3)2CO с (acac )3Cr, d м.д.) -9,51 и -9,61 (цис- и транс- изомеры).
По данным анализа, выделенное соединение соответствует формуле I-1,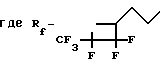
и представляет собой 1,3,5-триметил-1,3,5-трис-(2-(2',2',3'-трифтор-3'-трифторметилциклобутил)этил)циклотрисилоксан.
Пример 2. В колбу емкостью 1 л, снабженную мешалкой, капельной воронкой и термометром, помещают 84 г (1 моль) NaHCO3, 79,1 (1 моль) пиридина и 420 мл ацетона. К смеси в течение 1 ч при 20-25 oC и перемешивании добавляют 235 мл (319 г, 1 моль) метил(2,3,3-трифтор -2- трифторметилциклобутил)этилдихлорсилана в 80 мл ацетона. Затем смесь перемешивают еще 3 ч, отфильтровывают от осадка солей, отгоняют ацетон на водяной бане и получают 251 г (95) гидролизата. Циклотрисилоксан выделяют вакуумной ректификацией. Получают 132 г (50) целевого продукта. Tкип. 220 oC/2 мм рт.ст. n
Вычислено, Si 10,94; C 36,23; F 43,03; O 6,03; H 3,77.
Найдено, Si 10,81; C 36,16; F 43,08; O 6,00; H 3,84.
Мол.вес 265.
Спектр ЯМР 19F (в (CD3)2 CO, δ м.д.): 78,58 (3F, 2-CF3).
AB-спектр dA-105,26, δB-105,72, AB 225,5 Гц (2F, 3-CF2), 193,7 (1F, 2-CF).
Спектр ЯМР 1H (в(CD3)2CO, δ м.д.)
0,44 (3H, Si-CH3), 0,63 (2H, 1-CH2), 1,41 (2H, 2-CH2); 1,66 (1H, 1'-CH), 2,2 (2H,4'-CH2).
Спектр ЯМР 29Si (в (CD3)2CO, Cr(acac)3, d м.д.) -9,54 и 9,63 (цис- и транс- и изомеры).
По данным анализа, выделенное соединение соответствует формуле I-2, где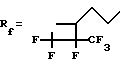
и представляет собой 1,3,5-триметил-1,3,5 - трис-(2-(2',3',3'-трифтор-2'-трифторметилциклобутил)этил)циклотрисилоксан.
Пример 3. В колбу емкостью 1 л, снабженную мешалкой, капельной воронкой и термометром, помещают 84 г (1 моль) NaHCO3, 79,1 г (1 моль) пиридина и 420 мл ацетона. К смеси в течение 1 ч при 20-25 oC и перемешивании добавляют 228 мл (331 г, 1 моль) метил (3,4,4-трифтор-3-трифторметилбицикло[2,2,12,5]гептил)дихлорсилана в 80 мл ацетона. Затем смесь перемешивают еще 3 ч, отфильтровывают от осадка солей, отгоняют ацетон на водяной бане и получают 262 г (95 ) гидролизата. Вакуумной ректификацией выделяют циклотрисилоксан. Получают 166 г (60) целевого продукта. Tкип. 250 oC/2 мм рт.ст. Tпл. 55 oC.
Вычислено, Si 10,47; F 41,16; C 38,98; H 3,61; O 5,78.
Найдено, Si 10,40; F 41,28; C 38,81; H 3,52; O 5,62.
Мол.вес 277.
Спектр ЯМР 19F (в (CD3)2CO, δ м.д.): 76,18 (3F, 3-CF3).
AB-спектр dA-110,08, δB-110,61, JAB 253 Гц (2F,4-CF2), -180,95 (1F, 3-CF).
Спектр ЯМР 1H(в(CD3)2CO, δ, м.д.): 0,9 (3H, Si-CH3), 1,78 (2H, 7-CH2), 2,00(2H, 6-CH2), 2,18 (1H, 1-CH), 2,82 (2H; 2-CH, 5CH).
Спектр ЯМР 29Si (в(CD3)2CO c Cr(acac)3, d м.д.): -10,28 и 10,75 (цис- и транс- изомеры).
По данным анализа, выделение соответствует формуле I-3, где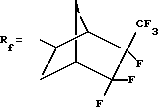
и представляет собой 1,3,5-триметил-1,3,5-трис -(3',4',4'-трифтор-3'-трифторметилбицикло[2.2.12,5] гептил)циклотрисилоксан.
Пример 4. В колбу емкостью 1 л, снаабженную мешалкой, капельной воронкой и термометром, помещают 84 г (1 моль) NaHCO3, 79,1 г (1 моль) пиридина и 420 мл ацетона. К смеси в течение 1 ч при 20-25 oC и перемешивании добавляют 228 мл (331 г, 1 моль) метил-(3,3,4-трифтор-4-трифторметилбицикло[2.2.12,5]гептил) дихлорсилана в 80 мл ацетона. Затем смесь перемешивают еще 3 ч, отфильтровывают от осадка солей, отгоняют ацетон на водяной бане и получают 262 г (95 ) гидролизата. Вакуумной ректификацией выделяют циклотрисилоксан. Получают 166 г (60) целевого продукта. Tкип. 250 oC/2 мм рт. ст. Tпл. 55 oC.
Вычислено, Si 10,47; F 41,16; C 38,98; H 3,61; O 5,78.
Найдено, Si 10,41; F 41,24; C 38,79; H 3,50; O 5,64.
Мол.вес 277.
Спектр ЯМР 19F (в(CD3)2CO, δ м.д.): 75,4 (3F, 4-CF3),
AB-спектр dA-120,9; δB-121,40, JAB 252 Гц,(2F, 3-CF2), 178,4 (1F, 4-CF).
Спектр ЯМР 1H (в(CD3)2CO, δ, м.д.): 0,91 (3H, Si-CH3), 1 1,80 (2H, 7-CH2); 2,05 (2H, 6 CH2), 2,30 (1H, 1-CH), 3,01 (2H; 2-CH, 5-CH).
Спектр ЯМР 29Si (в(CD3)2CO c Cr(acac)3, d м.д.): -10,25 и 10,80 (цис- и транс- изомеры).
По данным анализа, выделенное соединение соответствует формуле I-4, где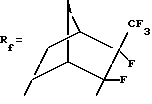
и представляет собой 1,3,5-триметил-1,3,5-трис-(3',3',4'-трифтор-4'-трифторметилбицикло[2.2.1.2,5]гептил) циклотрисилоксан.
Описываемые метил(гексафторалкил)циклотрисилоксаны формулы I были использованы в качестве мономеров для синтеза метил(гексафторалкил)полисилоксанов, содержащих винильную группу.
Полимеры получают полимеризацией соответствующих циклотрисилоксанов силоксанолятом щелочного металла, взятым в количестве 0,004-0,007 мас. в расчете на циклотрисилоксан.
В таблице приведены свойства полученных полимеров, а также полимеров на основе 1,3,5-триметил-1,3,5-трис-(3,3,3- трифторпропил)циклотрисилоксана (IV), 1,3,5-триметил-1,3,5-трис- (полифторалкил)циклотрисилоксана (II) и 1,3,5-триметил-1,3,5-трис (2,2,3,3- тетрафторциклобутил)циклотрисилоксана (III).
Как видно из таблицы, использование метил(гексафторалкил)циклосилоксанов общей формулы I позволяет получить фторсодержащие силоксановые полимеры с высокой термо- и маслобензостойкостью.
Кроме того, способ синтеза заявленных соединений базируется на достаточно простой технологии, не требует затрат дорогостоящих растворителей и позволяет получать целевые продукты с достаточно высокими выходами. Таким образом, предлагаемые соединения являются доступными продуктами и могут быть использованы для промышленного производства фторсилоксановых полимеров.
| название | год | авторы | номер документа |
|---|---|---|---|
| МЕТИЛ(ГЕКСАФТОРАЛКИЛ)ДИХЛОРСИЛАНЫ ДЛЯ ПОЛУЧЕНИЯ ТЕРМО- И МАСЛОБЕНЗОСТОЙКИХ ФТОРСОДЕРЖАЩИХ СИЛОКСАНОВЫХ ПОЛИМЕРОВ | 1995 |
|
RU2101286C1 |
| ПОЛИМЕТИЛ(ГЕКСАФТОРАЛКИЛ)СИЛОКСАНЫ ДЛЯ ТЕРМО- И МАСЛОБЕНЗОСТОЙКИХ МАТЕРИАЛОВ | 1995 |
|
RU2078097C1 |
| ПОЛИДИМЕТИЛМЕТИЛ(ГЕКСАФТОРАЛКИЛ)СИЛОКСАНЫ ДЛЯ ТЕРМО-, МАСЛОБЕНЗОСТОЙКИХ МАТЕРИАЛОВ | 2013 |
|
RU2527968C1 |
| СИЛОКСАНОВЫЕ БЛОКСОПОЛИМЕРЫ, СОДЕРЖАЩИЕ МЕТИЛ (ГЕКСАФТОРАЛКИЛ) СИЛОКСАНОВЫЕ ЗВЕНЬЯ | 2014 |
|
RU2563253C1 |
| ГРЕБНЕОБРАЗНЫЕ ПОЛИМЕТИЛСИЛОКСАНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2010 |
|
RU2440382C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИОРГАНОСИЛОКСАНОВ | 2007 |
|
RU2346960C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИКЛОТРИСИЛОКСАНОВ | 2008 |
|
RU2402577C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФТОРОРГАНОСИЛОКСАНОВЫХ СОПОЛИМЕРОВ | 2011 |
|
RU2455319C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ АЛКИЛСИЛАНА С РАЗНОИМЕННЫМИ ГИДРОЛИЗУЕМЫМИ ГРУППАМИ У АТОМА КРЕМНИЯ | 1996 |
|
RU2129124C1 |
| СПОСОБ ПОЛУЧЕНИЯ МОДИФИЦИРОВАННОГО 1,4-ПОЛИБУТАДИЕНА | 1992 |
|
RU2083592C1 |

Использование: изобретение может быть использовано в промышленности синтетического каучука при производстве фторсодержащих силоксановых полимеров. Цель: создание доступных фторсодержащих алкилметилциклотрисилоксанов, способных использоваться для получения термо- и маслобензостойких силоксановых полимеров. Сущность: предлагаются 1,3,5-триметил-1,3,5-трис(гексафторалкил)циклотрисилоксаны общей формулы
[RfSi(CH3)O]3,
где
полученные гидролизом соответствующих метил(гексафторалкил)дихлорсиланов двууглекислым натрием в присутствии пиридина в среде ацетона при 20-25 oC. Положительный эффект: предлагаемые соединения позволяют получить фторсодержащие силоксановые полимеры, обладающие сочетанием высокой термо- и маслобензостойкости. 1 табл.
[RfSi(CH3)O]3
где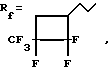
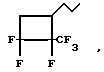
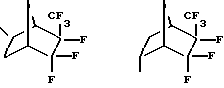
для получения термо- и маслобензостойких фторсодержащих силоксановых полимеров.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Патент ФРГ N 3248546, кл | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| 0 |
|
SU160201A1 | |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
1997-09-10—Публикация
1995-06-27—Подача