Изобретение относится к биологической технологии и может быть использовано в микробиологической, фармацевтической, деревообрабатывающей и нефтехимической промышленности.
Существует проблема утилизации формальдегида из его водных растворов (например, как побочного продукта ряда технологических процессов). Известные биологические технологии его утилизации являются способами очистки промышленных сточных вод от формальдегида.
Известен способ аэробной биологической очистки промышленных сточных вод на очистных сооружениях типа аэротенков путем окисления формальдегида микроорганизмами активного ила [1] Недостатком способа являются низкие (до 1 г/л) предельно допустимые концентрации формальдегида в сточных водах, которые могут быть поданы на очистные сооружения, что ограничивает применимость способа.
В качестве прототипа выбран способ биологической детоксикации формальдегидсодержащих сточных вод в аэрируемом реакторе путем окисления формальдегида микроорганизмами активного ила до муравьиной кислоты и далее до углекислоты [2] согласно которому входные концентрации формальдегида могут достигать 5,3 г/л. Стоки в реактор подаются с соответствующими минеральными добавками. Повышение эффективности в прототипе достигается использованием регуляции подачи стоков в реактор на основе значения pH среды. Реакция окисления формальдегида до муравьиной кислоты в клетках бактерий протекает значительно быстрее реакции окисления муравьиной кислоты до углекислоты, поэтому после добавки формальдегида происходит выделение муравьиной кислоты в среду и соответствующее уменьшение значения pH. Через определенный период наблюдается потребление муравьиной кислоты активным илом и увеличение значения pH. Следующая добавка сточных вод с формальдегидом согласно прототипу производится в тот момент, когда pH достигает уровня исходного значения, равного значению pH перед предыдущей добавкой, при этом исходное значение pH выбирается в нейтральной области (pH 6,5-7,5). Такая регуляция позволяет устранить возможность передозировки формальдегида и поддерживает его концентрацию в реакторе на оптимальном уровне.
К недостаткам этого способа относятся:
а) невысокие входные концентрации формальдегида (до 6 г/л), обусловленные низкой скоростью переработки формальдегида, что не позволяет использовать его вместо дорогостоящих способов обезвреживания концентрированных формальдегидсодержащих стоков, основанных на упаривании и сжигании;
б) недостаточная производительность очистки и отсутствие возможности ее регулирования.
Задачей изобретения является создание способа биологической утилизации формальдегида из его водных растворов с повышенной и управляемой производительностью.
В соответствии с поставленной задачей предлагаемый способ биологической утилизации формальдегида из его водных растворов осуществляют с помощью аэрируемого реактора с микробной популяцией в водно-минеральной среде и со средствами управления температурой и контроля содержания кислорода и кислотности (pH), и включает циклическое введение порций формальдегида при наличии в среде реактора заданного нейтрального значения pH. Способ отличается от прототипа тем, что в нем дополнительно измеряют изменение значения pH в среде реактора после введения указанной порции формальдегида, и на стадии уменьшения pH в реакторе вводят щелочной агент в количестве, обеспечивающем увеличение pH до 90% от диапазона его уменьшения, измеренного в отдельном предварительном цикле, в котором вводят только формальдегид.
Предпочтительно в качестве щелочного агента использовать аммиак, либо иметь аммиак компонентом щелочного агента. Это позволяет улучшить условия утилизации формальдегида за счет использования аммиака в качестве источника азотного питания бактерий.
Предпочтительно в качестве микробной популяции используют штамм метилотрофных бактерий Pseudomonas sp. ВПКМ N В-6798, способных использовать формальдегид в бедной минеральной среде в качестве единственного источника углерода и энергии в концентрации до 8 г/л, и сохраняющих дееспособность при кратковременном восьмикратном увеличении этой концентрации.
Целесообразно измерять период восстановления содержания кислорода и период восстановления нейтрального значения pH в среде реактора под воздействием формальдегида и аммиака. По их соотношению судят о сохранении дееспособности микробной популяции. Это позволяет оптимизировать величину порций формальдегида на уровне ее наибольшей величины.
Изложенная совокупность признаков способа позволяет увеличить порцию вводимого формальдегида до уменьшения pH под ее воздействием ниже 6,0, так как вводимая далее порция щелочного агента поддерживает кислотность реактора в благоприятных пределах. При этом предпочтительно соотношение порций формальдегида и щелочного агента выбрать обеспечивающим изменением pH под их суммарным воздействием в диапазоне благоприятном для жизнедеятельности микробной популяции. При прочих равных условиях это повышает пределы управления производительностью способа.
Целесообразно осуществлять циклическое удаление порций среды из реактора, что позволяет предельно увеличить производительность способа в условиях постоянства объема среды в реакторе. При этом предпочтительно указанное удаление порций среды осуществлять в конце текущего цикла утилизации, когда концентрация формальдегида в среде реактора минимальна.
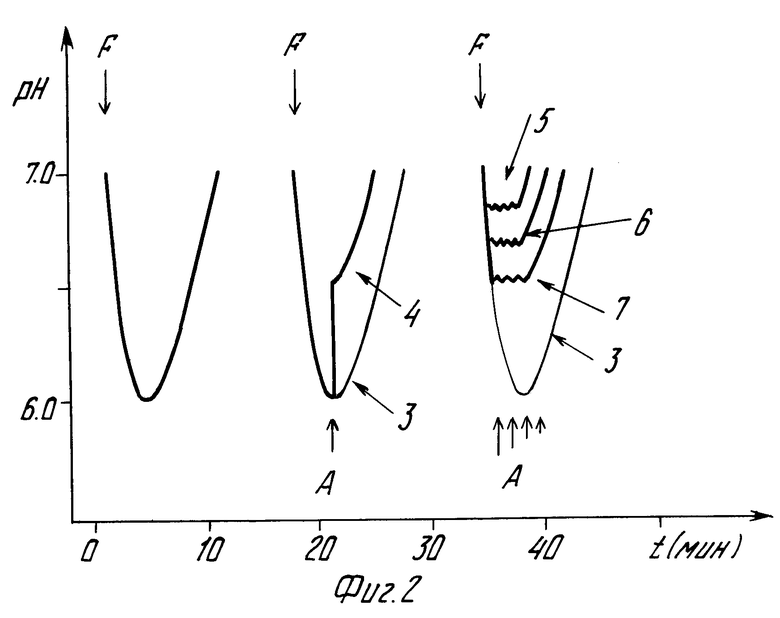
На фиг. 1 приведен временной ход циклического изменения кислотности (pH) среды реактора при увеличивающихся порциях вводимого формальдегида (кривая 1) и временной ход изменения pH при циклическом введении формальдегида и щелочного агента (кривая 2) с указанием стрелками моментов и величины фазы формальдегида в каждом цикле утилизации; на фиг. 2 приведены графики изменения кислотности (pH) среды реактора во времени при введении только порции формальдегида (кривая 3), при последовательности введении формальдегида (стрелка F) и щелочного агента (стрелка А).
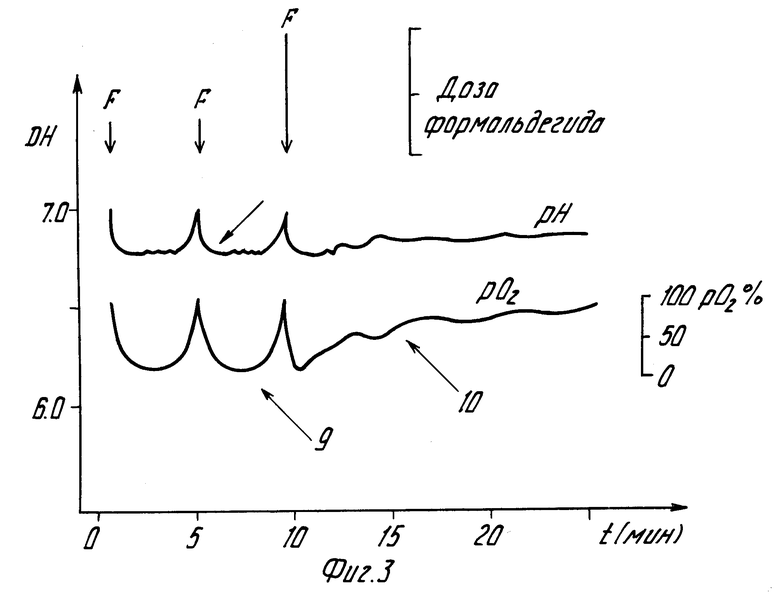
Кривая 4 демонстрирует изменение кислотности при интенсивном (моментальном) вводе порции щелочного агента, а кривая 5, 6, и 7 при плавном вводе порции щелочного агента (кривая 5) и в зависимости от выбора момента начала ввода щелочного агента на стадии падения pH под действием порции формальдегида; на фиг. 3 приведены сопоставленные во времени график измерения периодов восстановления кислотности среды реактора (кривая 8) и график измерения периодов восстановления содержания кислорода (кривая 9) под воздействием введения порций формальдегида и щелочного агента, а также ход изменения содержания кислорода при превышении предельно допустимой дозы формальдегида (кривая 10).
Далее изобретение поясняется на примере утилизации формальдегида из сточных вод в предпочтительном осуществлении предлагаемого способа с помощью общеизвестных технических средств. Это позволяет не приводить схему технологической установки. Концентрация формальдегида в сточных водах в рассматриваемом примере составляла 60 г/л.
Реактор цилиндрической формы емкостью 130 л содержит 100 л культурной среды. Реактор снабжен средством постоянного перемешивания среды, расположенным в его придонной области, и охватывающей водяной рубашкой для обеспечения заданной температуры в среде реактора (около 30 градусов по Цельсию). Реактор снабжен средствами измерения температуры, содержания кислорода и кислотности, а также трубопроводами с дозирующими насосами для раздельной подачи кислорода, минеральных компонентов, водного раствора аммиака и формальдегида и для удаления избытка среды из реактора.
Предварительно, как и при подготовке к осуществлению способа-прототипа, биологическую производительность микробной популяции в среде реактора развивают путем введения последовательного ряда плавно увеличивающихся порций водного раствора формальдегида. При этом контролируют значение pH и при падении значения pH до 6,0 прекращают увеличение этих порций (фиг. 1, кривая 1). При этом достигнута биологическая производительность среды примерно равная производительности способа-прототипа. Однако с учетом того, что в качестве микробной популяции используют штамм метилотрофных бактерий Pseudomonas sp. ВПКМ N B-6798 биологическая производительность средств реактора выше, так как концентрация формальдегида в среде может быть увеличена почти на порядок в сравнении с известными микробными популяциями.
Последующие циклы утилизации формальдегида осуществляют по предлагаемому способу. В предварительном цикле в реактор вводят только порцию формальдегидсодержащих стоков, величину которой контролируют путем непрерывного измерения pH и ограничивают при достижении падения pH в среде реактора до 6,0 (фиг. 1, кривая 1). На этой стадии осуществляется ферментативное окисление формальдегида в муравьиную кислоту. Далее микробная популяция, в качестве которой используют штамм метилотрофных бактерий Pseudomonas sp. ВПКМ N B-6798, активно окисляет муравьиную кислоту с образованием углекислого газа и воды и используют получаемую на всех стадиях окисления формальдегида энергию на синтез дополнительной биомассы. При этом значение pH в среде реактора плавно нарастает. При достижении pH заданного нейтрального значения, выбранного равным 7,0, вводят следующую порцию формальдегидсодержащих сточных вод, величину которой выбирают приблизительно равной порции в предыдущем цикле детоксикации. На стадии падения pH под действием порции формальдегидсодержащих сточных вод, вводимой в текущем цикле, например при pH, равном 6,2, в среду реактора вводят порцию 25% водного раствора аммиака, величину которой также контролируют по изменению pH в среде реактора под суммарным воздействием формальдегида и аммиака.
Возможно несколько режимов ввода порции аммиака: первый интенсивный (одномоментный), при котором значение pH в среде реактора резко нарастает (фиг. 2, кривая 4) и второй плавный, когда значение pH в среде реактора под суммарным воздействием формальдегида и аммиака сохраняется на уровне значения pH, при котором начат ввод водного раствора аммиака (фиг. 2, кривые 5-7). Это достигается использованием насоса перистальтического типа, управляемого сигналом от датчика pH. При этом в первом режиме ввод аммиака прерывают, когда стремительно растущее значение pH под его воздействием достигает выбранного заданного значения, например 6,5. Во втором режиме ввод порции аммиака прерывается автоматически, так как интенсивность ввода аммиака плавно падает до нуля и качественно совпадает с крутизной временной кривой падения pH (кривая 3) и с момента времени t0 (фиг. 2) pH начнет увеличиваться независимо от ввода или прекращения ввода аммиака. Как видно из дальнейшего временного хода кривых 4-7 изменения pH кислотность среды реактора оказывается в более благоприятном диапазоне значений для деятельности бактерий и достигает заданного нейтрального значения значительно раньше, чем при отсутствии аммиака (кривая 3) и, следовательно, следующий (очередной) цикл утилизации формальдегида может быть осуществлен раньше. Кроме того, аммиак служит азотным питанием бактерий. При этом в текущем цикле детоксикации сточных вод измеряют содержание кислорода в среде реактора (кривая 9 на фиг. 3). Под воздействием формальдегида и его интенсивного окисления в муравьиную кислоту содержание кислорода резко падает, затем стабилизируется на уровне равновесия между количеством непрерывно вводимого и потребляемого кислорода и далее нарастает до исходного равновесного значения. Примерно равенство периода начала восстановления содержания кислорода и восстановления кислотности свидетельствует о нормальной для жизнедеятельности микробной популяции величине порции введенного формальдегида. Если же период начала восстановления содержания кислорода значительно короче (0,7 и меньше периода восстановления нейтрального значения кислотности, фиг. 3, кривая 10), то это свидетельствует по меньшей мере об угнетенности микробной популяции, обусловленной избыточностью порции формальдегида, и о необходимости ее уменьшения. Измерение периода начала восстановления содержания кислорода и периода восстановления заданного нейтрального значения pH и сопоставления этих значений позволяет выбрать порцию формальдегида без опасности передозировки.
В следующих циклах детоксикации формальдегида, вводимые в реактор могут быть увеличены настолько, что падение pH под их действием будет ниже 6,0, однако результирующее изменение кислотности под действием вводимого аммиака остается в диапазоне, благоприятном для деятельности микробной популяции (фиг. 1, кривая 2).
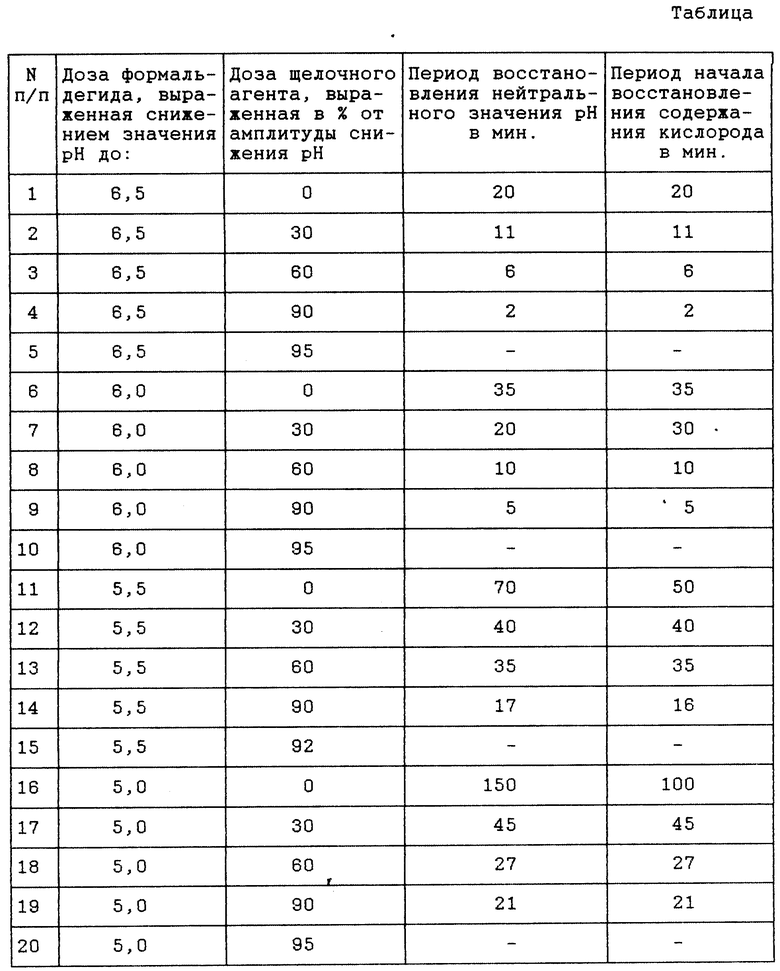
В конце текущего цикла детоксикации, когда pH близко к заданному нейтральному значению, из реактора удаляют порцию среды, которая равна суммарной введенной порции формальдегидсодержащих сточных вод и водного раствора аммиака. Следовательно, объем и другие параметры близки к стационарным, что позволяет оптимизировать производительность детоксикации в каждом цикле. Другие примеры осуществления предлагаемого способа, в которых в пределах цикла утилизации варьировались величина порции вводимого в реактор формальдегида и величина порции щелочного агента, сведены в таблицы.
Как видно из таблицы, при увеличении порции щелочного агента период утилизации формальдегида становится короче, и, следовательно, производительность способа увеличивается. В сравнении со способом-прототипом (примеры 1, 6, 11, 16) период утилизации формальдегида сокращается в 7-10 раз (примеры 4, 9, 14, 19). Вместе с тем, нецелесообразно и неприемлемо превышение дозы щелочного агента, обеспечивающей увеличение pH более 90% от диапазона (амплитуды) уменьшения pH, измеренных в циклах утилизации, когда в реактор вводят только формальдегид (примеры 1, 6, 11, 16), так как при этом оставшиеся 10% регистрируемой амплитуды изменения pH среды попадают в коридор приборных погрешностей для заданного нейтрального значения pH, вследствие чего резко возрастает риск принятия неправильного решения о конце цикла утилизации и необходимости подачи новой порции формальдегида. По этим же причинам невозможно надежное измерение периода восстановления заданного нейтрального значения pH в цикле (примеры 5, 10, 15, 20). Следует также отметить, что циклы утилизации, приведенные в примерах 11, 16 возможны только благодаря использованию штамма метилотрофных бактерий Pseudomonas sp. ВПКМ N B-6798, сохраняющих дееспособность при большей концентрации формальдегида. При этом, однако, период восстановления содержания кислорода в реакторе заметно короче периода восстановления нейтрального значения кислотности, что свидетельствует о некоторой угнетенности микробной популяции. Введение щелочного агента исключает эту проблему.
В качестве щелочного агента могут быть использованы гидроксиды, карбонаты, бикарбонаты щелочных и щелочноземельных металлов и аммония и другие их соли слабых кислот, а также аммиак. Использование аммиака предпочтительно, так как он утилизируется микробной популяцией как источник азота.
Благодаря тому, что дозировка ввода в среду реактора формальдегида и аммиака осуществляется на основе непрерывного измерения кислотности и содержания кислорода, предлагаемый способ удобно автоматизировать с помощью компьютерной техники управления. Программное управление предлагаемым способом детоксикации позволяет достигнуть сочетания высокой производительности и высокой надежности. При этом если циклически удаляемую среду накапливать в дополнительном реакторе, то в этом реакторе микробная популяция ассимилирует остатки формальдегида, а содержимое этого реактора является запасной культуральной средой, которой можно заменить среду основного реактора в случае технологической аварии.
Достигаемая предлагаемым способом производительность позволяет применять его для получения из формальдегида биомассы, которая может быть использована для многих целей. Например:
получение белков и на их основе аминокислот;
выделение РНК и ДНК, АТФ и витаминов, кофакторов типа НАД;
сверхсинтез заданных продуктов в результате внедрения соответствующих плазмид в геном используемого штамма бактерий.
В сравнении с известными способами биологического производства биомассы предлагаемый способ характеризуется простотой и дешевизной технологии и аппаратурного обеспечения, так как формальдегид обладает известным бактерицидным свойством, и его постоянное присутствие позволяет избежать такие дорогостоящих мероприятий, как стерилизации реакторов и коммуникаций, борьба с заражением продукта (биомассы) другими микроорганизмами на стадии между ее производством и переработкой.
| название | год | авторы | номер документа |
|---|---|---|---|
| ШТАММ БАКТЕРИЙ PSEUDOMONAS SPECIES, ИСПОЛЬЗУЕМЫЙ ДЛЯ УТИЛИЗАЦИИ ФОРМАЛЬДЕГИДА И СПОСОБНЫЙ ПРИ ЭТОМ ПОТРЕБЛЯТЬ ФОРМАЛЬДЕГИД В КАЧЕСТВЕ ЕДИНСТВЕННОГО ИСТОЧНИКА УГЛЕРОДА И ЭНЕРГИИ В БЕДНОЙ МИНЕРАЛЬНОЙ СРЕДЕ | 1995 |
|
RU2102474C1 |
| Устройство для контроля и регулирования работы установки для непрерывного культивирования микроорганизмов | 1983 |
|
SU1201304A1 |
| Способ определения полупериода агрегации эритроцитов | 1984 |
|
SU1262376A1 |
| Лабораторный ферментер | 1990 |
|
SU1731805A1 |
| СПОСОБ ДИАГНОСТИКИ ОСТРОЙ ЛУЧЕВОЙ БОЛЕЗНИ | 1986 |
|
SU1519366A1 |
| СПОСОБ ЛЕЧЕНИЯ ЛУЧЕВОЙ БОЛЕЗНИ У ЖИВОТНЫХ | 1991 |
|
RU2077888C1 |
| Пластина геля для электрофореза | 1982 |
|
SU1052983A1 |
| СПОСОБ БИОИНДИКАЦИИ КАЧЕСТВА ВОДЫ | 1991 |
|
RU2006027C1 |
| СПОСОБ ОБНАРУЖЕНИЯ НЕФТЕПРОДУКТОВ В ВОДНЫХ РАСТВОРАХ | 1996 |
|
RU2152613C1 |
| СПОСОБ УНИЧТОЖЕНИЯ ИПРИТА | 1997 |
|
RU2169598C2 |
Использование: биологическая технология для детоксикации формальдегидсодержащих водных стоков и получения биомассы из формальдегида. Сущность способа. В аэрируемый реактор с микробной популяцией в водно-минеральной среде и со средствами управления температурой и контроля содержания кислорода и кислотности циклически вводят порции формальдегида при наличии в среде реактора заданного нейтрального значения кислотности. Для повышения производительности способа на стадии уменьшения кислотности под действием порции формальдегида в среду реактора вводят щелочной агент в количестве, обеспечивающем увеличение кислотности до 90% от диапазона его уменьшения, измеренного в отдельном предварительном цикле утилизации, в котором вводят только порцию формальдегида. Предпочтительно используют в качестве микробной популяции штамм метилотрофных бактерий Pseudomonas sp. ВПКМ N В-6798, а в качестве щелочного агента - аммиак. При этом порции вводимого формальдегида увеличивают до уменьшения кислотности среды под воздействием только формальдегида ниже 6,0 и циклически удаляют порции среды из реактора. 8 з.п. ф-лы, 3 ил., 1 табл.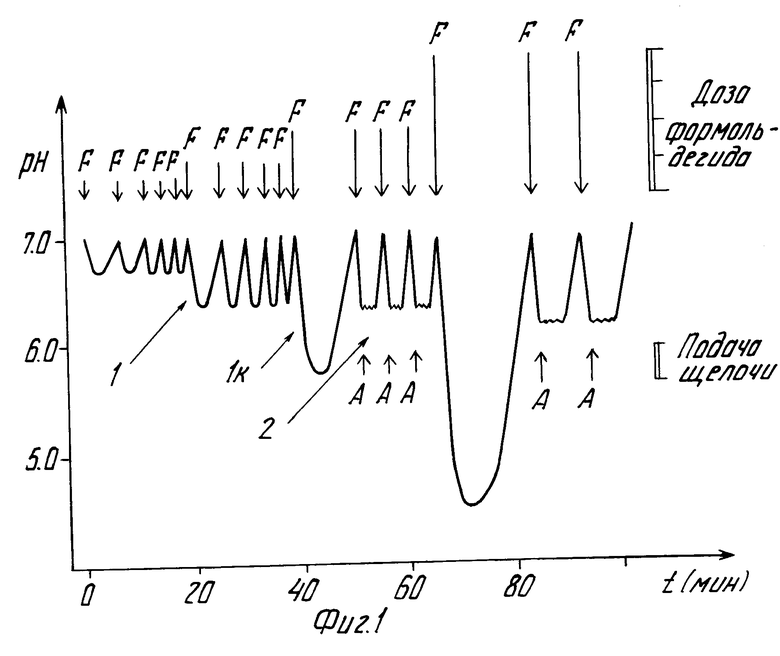
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Поруцкий Г.Ф | |||
| Биохимическая очистка сточных вод органических производств | |||
| - М.: Химия, 1975 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| DD, патент, 216915, кл | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
1997-10-27—Публикация
1995-11-09—Подача