Изобретение относится к способам получения производных пиперидина или к их фармацевтически приемлемым солям, проявляющим антидепрессивную активность, например, к синтезу Брофаромина, исходя из новых производных гидрохинона; к самим производным гидрохинона или их солям, способам их получения; 4-хлоркарбонил-1-бензилоксикарбонилпиперидину или его соли как промежуточному продукту для получения производных пиперидина с антидепрессивной активностью, а также новым N-ациальным производным пиперидина или их солям.
Известен способ получения производных пиперидина, в частности, Брофаромина, формулы: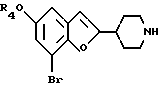
(R4 CH3),
который осуществляют обычно в течение 8 ч по схеме A1 A8, приведенной в конце описания.
Согласно указанной схеме формируют 4-метоксифенол по Reimer-Tiemann (А1) и затем бромируют (А2). Полученный 3-бром-5-метоксисалицилальдегид затем конденсируют с 4-хлорметилпиридином (А3). Полученный 4-(7-бром-5-метоксибензофуран-2-ил)-пиридин-N метилируют до N-метил-1,2,5,6-тетрагидропиридина (А5) и гидрируют до 1-метил-4-(7-бром-5-метоксибензофуран-2-ил)-пиперидина (А6). Последний затем деметилируют путем введения во взаимодействие со сложным эфиром галогенмуравьиной кислоты при образовании соответствующего сложного эфира 4-(7-бром-5-метоксибензофуран-2-ил)-пиперидин-1-карбоновой кислоты (А7), который, наконец, расщепляют до Брофаромина (А8).
Этот способ имеет определенный недостатки. Если исходят из 4-метоксифенола, достигается только общий выход Брофаромина максимально 12,7% от теории. С большими потерями и технически плохо управляемо протекают приводящие к 3-бром-5-метоксисалицилальдегиду стадии А1 и А2 (выход 45% от теории). Последующее превращение его в Брофаромин (стадии А3-А8) дорогостоящее и проходит с большими потерями из-за многостадийности и в связи с тем, что на стадии А6 получается вплоть до 10% нежелательного продукта дебромирования, который можно удалить с трудом путем многократной перекристаллизации (выход 27,4% от теории). Это, прежде всего, из-за того, что выход на стадии циклоконденсации А3 не может превышать 45% от теории. При последующем гидрировании 1-метил-4-(7-бром-5-метоксибензофуран-2-ил)-1,2,5,6-тетрагидропиридина и последующем деметилировании 1-метил-4-(7-бром-5-метоксибензофуран-2-ил)пиперидина (А6-А8) достигается выход продукта только 6% от теории.
Целью изобретения является разработка экологичного и рентабельного способа получения производных формулы XII, предпочтительно Брофаромина, который частично или полностью лишен недостатков известного способа.
Указанный способ, уже исходя из 5-бромсалицилальдегида, в частности, при получении Брофаромина позволяет увеличить выход с 27,4 до 62% от теоретического.
Для осуществления новых способов получения производных пиперидина или их фармакологически приемлемых солей предлагаются новые соединения и способы их получения.
В частности, объектом изобретения являются производные гидрохинона общей формулы I:
где R4 обозначает низший алкил и R1 обозначает либо гидроксильную группу, галоген, группу формулы -P(=O)(R5)(R6)(1a), либо группу формулы P+ (R7)(R8)R9X-(1b), M обозначает метилен, R2 обозначает водород или группу формулы
и R3 обозначает водород или галоген или R1 обозначает гидроксильную группу или низшую алкоксильную группу, М обозначает карбонил, R2 обозначает водород и R3 обозначает галоген, R5 и R6 представляют низшую алкоксильную группу, R7, R8 и R9 обозначают фенильную группу, X- обозначает анион галоидводородной кислоты, Y обозначает группу формулы -(C=O)-(1e) и R10 обозначает низшую алкоксильную группу, при условии, что в соединении I, где R1 обозначает группу 1b, где R7, R8, R9 обозначают соответственно незамещенную фенильную группу и X- обозначает ион бромида, М обозначает метилен, R2 обозначает водород и R4 обозначает метил, R3 не является водородом, и при условии, что в соединении I, где R1 обозначает гидроксильную группу, М обозначает метилен, R2 обозначает водород и R4 обозначает метил или этил, R3 не является водородом в свободном виде или в виде соли.
Соединения формулы I в виде соли представляют собой соответствующие соли с кислотами (для соединений формулы I с по меньшей мере одной основной группой) и соответствующие соли с основаниями (для соединений формулы I с по меньшей мере одной кислотной группой); предпочтительны соответствующие фармацевтически применимые соли. Соли с кислотой образуются, например, с сильными неорганическими кислотами, такими как минеральные кислоты, например, серная кислота, фосфорная кислота или галогеноводородная кислота; с сильными органическими карбоновыми кислотами, такими как низшие алканкарбоновые кислоты, например, уксусная кислота; ненасыщенные дикарбоновые кислоты, например, щавелевая, малоновая, янтарная, малеиновая, фумаровая, фталевая или терефталевая кислота; с такими как оксикарбоновые кислоты, например, аскорбиновая, гликолевая, молочная, яблочная, винная или лимонная кислота, аминокислоты, например, аспарагиновая или глутаминовая кислота, или бензойная кислота; или с органическими сульфокислотами, такими как низшие алкановые сульфокислоты или в случае необходимости замещенные бензолсульфокислоты, например, метил- или п-толуолсульфокислота. Пригодными солями с основаниями являются, например, металлические соли, такие как соли щелочных или щелочноземельных металлов, например, соли натрия, калия или магния; или соли с аммиаком или органическим амином, как морфолин, тиоморфолин, пиперидин, пирролидин, моно-, ди- или три-(низший алкил), например, этил-, трет.-бутил-, диэтил-, диизопропил-, триэтил-, трибутил- или диметилпропиламин; или с моно-, ди- или триокси-(низший алкил)-амином, например, моно-, ди- или триэтаноламин. Соединения формулы I могут быть в виде внутренних солей, например, тогда когда R1 обозначает группу 1b. Непригодные для фармацевтического применения соли могут применяться, например, для выделения, очистки свободных соединений формулы I, а также их фармацевтически применимых солей.
Под понятием "низший", если не указано ничего другого, подразумевают остатки, которые содержат вплоть до 7, прежде всего, вплоть до 4 атомов углерода.
Низший алкил представляет собой C1-C4-алкил, то есть метил, этил, пропил, изопропил, бутил, изобутил, втор.-бутил или трет.-бутил; и далее охватывает C5-C7-алкильные, то есть соответствующие пентильный, гексильный и гептильный остатки.
Низший алкоксил представляет собой C1-C4-алкоксил, то есть метокси, этокси, пропилокси, изопропилокси, бутилокси, изобутилокси, втор.-бутилокси или трет. -бутилокси; далее охватывает C5-C7-алкоксильные, то есть соответствующие пентилокси-, гексилокси- и гептилокси-остатки.
Низшим алкенилокси является, например, аллилокси; фенил-(низший алкенил)-окси обозначает, например, 3-фенилпроп-2-енилокси.
Низший алкилтио представляют собой C1-C4-алкилтио, то есть метилтио, этилтио, пропилтио, изопропилтио, изобутилтио, втор.-бутилтио и трет.-бутилтио; и далее охватывает C5-C7-алкилтио-, то есть соответствующие пентилтио-, гексилтио- и гептилтиоостатки.
Галогеном является в особенности хлор или бром, далее фтор или йод.
N, N-ди-(низший алкил)-амино представляет собой остаток, где оба N-остатка являются одинаковыми или разными и, смотря по обстоятельствам, имеют указанное выше при определении низшего алкила значение, как N,N-диметиламино, N,N-диэтиламино, N,N-диизопропиламино, N-бутил-N-метиламино, N,N-дипентиламино или N-пентил-N-метиламино.
Галоген-(низший алкил) содержит по сравнению с низшим алкилом на одном из своих C-атомов один, два или три одинаковых или разных атомов галогена вместо атомов водорода и представляет собой остаток, где низший алкил имеет указанное выше при определении низшего алкила значение, а галоген имеет указанное выше при определении галогена значение, как трифторметил, трихлорметил, 2,2,2-трифторэтил или 3,3,3-трифторпропил.
(Низший алкан)-сульфонил представляет собой C1-C4- алкансульфонил, как метансульфонил, этансульфонил, пропансульфонил, бутансульфонил или трет.-бутансульфонил, и далее охватывает C5-C7-алкансульфонильные, то есть соответствующие пентансульфонильный, гексансульфонильный или гептансульфонильный остатки.
Галоген-(низший алкан)-сульфонил содержит по сравнению с низшим алкансульфонилом на одном из своих C-атомов один, два или три одинаковых или разных атомов галогена вместо атомов водорода и представляет собой остаток, где (низший алкан)-сульфонил имеет указанное выше при определении (низший алкан)-сульфонила значение, а галоген имеет указанное выше при определении галогена значение, как трифторметансульфонил, трихлорметансульфонил, 2,2,2-трифторэтансульфонил или 3,3,3-трифторпропансульфонил.
Анионами галогеноводородной кислоты (галогенид-ионами) являются в особенности хлорид- или бромид-ион, а также фторид- и иодид ион.
Анионы (низшей)алкансульфокислоты (низший алкансульфонат-ион) имеют значение низшего алкансульфонила, указанные выше, в частности, означают сульфонат-ион, этансульфонат-ион, пропансульфонат-ион, бутансульфонат-ион или трет.-бутансульфонат-ион.
Предпочтительными являются соединения, выбранные из группы:
3-бром-2-окси-5-метоксибензиловый спирт;
[(3-бром-2-окси-5-метоксифенил)метил]трифенилфосфонийхлорид;
[(3-бром-2-окси-5-метоксифенил)метил]трифенилфосфонийбромид;
[(2-окси-5 метоксифенил)метил]трифенилфосфонийхлорид;
[(3-бром-2-[(1-этоксикарбонилпиперид-4-ил)карбонилокси-5- метоксифенил] метил]трифенилфосфонийхлорид;
3-бром-2-окси-5-метоксибензилбромид;
сложный диметиловый эфир [3-бром-2-окси-5-метоксифенил)метил]фосфоновой кислоты;
сложный метиловый эфир 3-бром-2-окси-5-метоксибензойной кислоты.
Особенно среди соединений изобретения предпочтительны указанные в примерах соединения формулы I в свободном виде или в виде соли.
Другим предметом изобретения является способ получения соединений формулы 1: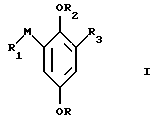
где R4 обозначает низшую алкильную группу, R1 является группой формулы P+(R7)(R8)9X- (1b), M обозначает метилен, R2 обозначает группу формулы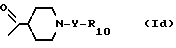
и R3 обозначает галоген, R7, R8 и R9 обозначает фенильную группу, X- обозначает анион галоидводородной кислоты, Y обозначает группу формулы (C=O) (1e) и R10 обозначает низшую алкоксильную группу в свободном виде или в виде соли, заключающий в том, что
а) соединение формулы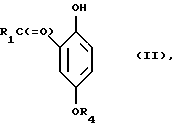
где R1 означает гидроксил или низший алкоксил, а R4 означает низший алкил, или соль этого соединения галогенируют в мета-положении по отношению к группе R1- C(=O)-, причем если R1-C(=O)- группа означает карбоксигруппу, последнюю этерифицируют с получением низшей алкоксикарбонильной группы,
b) в полученном соединении формулы
где X1 обозначает низший алкоксикарбонил, R3 обозначает низшую алкильную группу или соли этого соединения, группу X1 восстанавливают в гидроксиметильную,
c) в полученном соединении формулы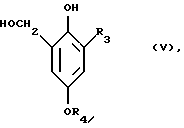
гидроксиметильную группу переводят в галоидметильную,
d) полученное соединение формулы
где X2 обозначает галоген, R3 обозначает галоген и R4 обозначает низшую алкильную группу, подвергают взаимодействию с соединением формулы
или солью этого соединения с кислотой H-X, где X, R7, R8 и R9 имеют значения, указанные в формуле I,
f) полученное соединение формулы
где X4 обозначает группу формулы -P+(R7)(R8)R9X- (1b), M обозначает метилен, R3 обозначает галоген и R4 обозначает низшую алкильную группу, и R7, R8, R9 и X- имеют значения, указанные в формуле I, обрабатывают соединением формулы
или солью этого соединения, где X5 представляет галоген или группу формулы X7-O-, в которой X7 обозначает низшую алкансульфонилгруппу, низшую алкоксикарбонильную группу или группу формулы
и R10 и Y имеют значения, указанные в формуле I, и при необходимости полученное соединение переводят в другое соединение формулы I, отделяют и/или полученное согласно изобретению свободное соединение переводят в соль или полученную согласно изобретению соль переводят в соответствующее свободное соединение.
Объектом изобретения также является другой способ получения гидрохинона формулы I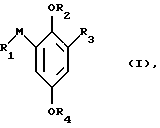
где R4 обозначает низшую алкильную группу, R1 обозначает группу формулы P+(R7)(R8)R9 X- (1b), M обозначает метилен, R2 обозначает группу формулы
и R3 обозначает галоген, R7, R8 и R9 обозначают фенильную группу, X- обозначает анион галоидводородной кислоты, Y обозначает группу формулы (C=O) (1e) и R10 обозначает низшую алкоксильную группу в свободном виде или в виде соли, заключающий в том, что
b) соединение формулы III
где R3 обозначает галоген и R4 обозначает низшую алкильную группу, или соль этого соединения подвергают взаимодействию с параформальдегидом или триоксаном,
c) в полученном соединении формулы
оксиметильную группу переводят в галоидметильную группу,
d) полученное соединение формулы
где X2 обозначает галоген, R3 обозначает галоген и R4 обозначает низшую алкильную группу, подвергают взаимодействия с соединением формулы
или солью этого соединения с кислотой HX, где X, R7, R8 и R9 имеют значения, указанные в формуле I,
f) полученное соединение формулы
где X4 обозначает группу формулы -P+(R7) (R8)R9X- (1b), M обозначает метилен, R3 обозначает галоген и R4 обозначает низшую алкильную группу, и R7, R8, R9 и X- имеют значения, указанные в формуле I, подвергают взаимодействию с соединением формулы
или солью этого соединения, где X5 обозначает галоген или группу формулы X7-O-, в которой X7 обозначает низшую алкансульфонилгруппу, низшую алкоксикарбонильную группу, низшую алканоильную группу или группу формулы
и R10 и Y имеют значения, указанные в формуле I, и при необходимости полученное соединение переводят в другое соединение формулы I, определяют и/или полученное согласно изобретению свободное соединение переводят в соль или полученную согласно изобретению соль переводят в соответствующее свободное соединение.
Объектом изобретения является также способ получения производных гидрохинона формулы I
где R4 обозначает низшую алкильную группу, R1 обозначает группу формулы -P+(R7)(R8)R9 X- (1b), M обозначает метилен, R2 обозначает группу формулы
и R3 обозначает галоген, R7, R8 и R9 обозначают фенильную группу, X- обозначает анион галоидводородной кислоты, Y обозначает группу формулы -(C= O)- (1e) и R10 обозначает низшую алкоксильную группу в свободном виде или в виде соли, заключающийся в том, что
e) соединение формулы
где X4 обозначает группу формулы -P+(R7)(R8)R9X- (1b), M обозначает метилен и R4 обозначает низшую алкильную группу, галогенируют в метаположение по отношению к группе X4-M,
f) полученное соединение формулы
где X4 обозначает группу формулы -P+ (R7)(R8)R9X- (1b), M обозначает метилен, R3 обозначает галоген и R4 обозначает низшую алкильную группу, и R7, R8, R9 и X- имеют значения, указанные в формуле I, подвергают взаимодействию с соединением формулы
или солью этого соединения, где X5 обозначает галоген или группу формулы X7-O-, в которой X7 обозначает низшую алкансульфонильную группу, низшую алкоксикарбонильную группу, низшую алканоильную группу или группу формулы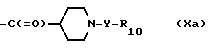
и R10 и Y имеют значения, указанные в формуле I, и при необходимости полученное соединение переводят в другое соединение формулы I, отделяют и/или полученное согласно изобретению свободное соединение переводят в соль, или полученную согласно изобретению соль переводят в соответствующее свободное соединение.
Указанные выше реакции с получением новых исходных веществ, которые соответственно являются промежуточными продуктами, осуществляют по аналогии с реакциями и способами получения известных исходных веществ, являющихся промежуточными продуктами. При этом, когда не упоминают определенные условия, применяются соответствующие обычные вспомогательные средства, такие как катализаторы, конденсирующие средства, а также средства для сольволиза и/или растворители, соответственно разбавители, и реакционные условия, как температура и давление, а также в случае необходимости инертные газы.
Галогенирование соединений формулы II согласно стадии способа а) осуществляют, например, путем обработки элементарным галогеном, в особенности бромом, предпочтительно в органическом растворителе, например, в алифатическом спирте, в особенности в низшем алканоле, таком как метанол, этанол, пропанол, изопропанол. Галогенирование предпочтительно осуществляют при обычной или незначительно пониженной температуре, например, в температурном интервале примерно от 0oC до 30oC, в особенности примерно при 0-20oC. При использовании карбоновых кислот II карбоксильная группа обычно этерифицируется до соответствующей (низший алкокси)-карбонильной группы.
Исходные вещества для стадии способа а) известны.
Взаимодействие соединений формулы III с параформальдегидом или триоксаном согласно стадии способа b) осуществляют, например, в присутствии кислого конденсирующего агента, такого как слабая кислота Льюиса, в особенности в присутствии безводной борной кислоты. Ее получают предпочтительно in situ путем азеотропной дистилляции с растворителем, который образует с водой азеотропную смесь, например, с толуолом. Предпочтительно работают при повышенной температуре, например, в температурном интервале примерно от 60oC до примерно 120oC, в особенности примерно при 80-100oC.
Восстановление формила, карбоксила, соответственно низшего алкоксикарбонила X1 в соединениях формулы IV предпочтительно осуществляют путем обработки комплексным гидридом двух мелких металлов, например, литийалюмогидридом или в особенности натрийборгидридом. Предпочтительно работают в простом эфире, таком как алифатический или циклоалифатический простой эфир, например, в диэтиловом эфире, метоксибутане, тетрагидрофуране или диоксане, или при использовании натрийборгидрида в алифатическом спирте, как в низшем алканоле, например, в метаноле или этаноле, при обычной или предпочтительно слегка пониженной температуре, например, в температурном интервале примерно от 0oC до примерно 40oC, в особенности примерно при 5-20oC.
Исходные вещества формулы III, а также соединения формулы IV, где X1 обозначает формил, известны; исходные вещества формулы IV, где X1 обозначает карбоксил или низший алкоксикарбонил, предпочтительно получают по стадии способа а).
Превращение оксиметила в галогенметил согласно стадии способа c) осуществляют обычным путем, например, обработкой галогенводородной кислотой, как соляная, или в особенности бромводородная кислота, или с предшественником галогенводорода. В качестве таковых используют, например, галогениды аммония, такие как бромид аммония, или для последующего применения на стадии d)
предпочтительно галогениды фосфония, такие как соединения формулы HP+(R7)(R8) R9X-. Предпочтительно работают в органическом растворителе, в таком как алифатическая карбоновая кислота или ее низший алкиловый эфир или нитрил, например, в уксусной кислоте, этилацетате или ацетонитриле. Выбор растворителя этим не ограничивается; можно применять также, например, толуол или бензол.
Исходные вещества формулы V, где R3 обозначает галоген и R4 обозначает метил или этил, известны; другие соединения формулы V можно получать, например, согласно стадии b).
Взаимодействие промежуточных продуктов формулы VI с соединениями VIIc согласно стадии способа d) осуществляют обычным образом.
Взаимодействие соединений формулы VI с соединениями формулы VIIc осуществляется предпочтительно в присутствии органического растворителя или разбавителя, как сложного эфира (низший алкан)-карбоновой кислоты или нитрила (низший алкан)-карбоновой кислоты, как этилацетат или ацетонитрил, в случае необходимости при нагревании, например, в температурном интервале примерно от 30oC до примерно 100oC, предпочтительно примерно при 40-80oC.
В предпочтительном, объединяющем стадии c) и d) способе промежуточный продукт формулы VI получают in situ из соответствующего соединения формулы V путем обработки галогенводородной кислотой, например, хлороводородом, или используют соединение формулы VIIc в виде галогенводородной соли и без выделения вводят во взаимодействие далее.
Галогенирование соединений формулы VIII согласно стадии способа e) осуществляют, например, обработкой элементарным галогеном, в особенности бромом, предпочтительно в органическом растворителе, например, в алифатическом спирте, в особенности в низшем алканоле, таком как метанол, этанол, пропанол, изопропанол.
Взаимодействие соединений формул IX и X согласно стадии f) осуществляют предпочтительно в присутствии основного конденсирующего агента, такого как азотсодержащее органическое основание, как ароматическое азотсодержащее основание, например, пиридин или хинолин, или алифатический амин, в особенности три-(низший алкил)амина, как триэтиламин, предпочтительно в органическом растворителе, например, в сложном эфире низшей алканкарбоновой кислоты или нитриле низшей алканкарбоновой кислоты, как этилацетат или ацетонитрил, в случае необходимости при нагревании, например, в температурном интервале от примерно 20oC до примерно 100oC, предпочтительно при 40-80oC. X5 означает в качестве галогена обычно хлор или бром, в качестве (низшего алкокси)карбонилокси предпочтительно этокси- или трет.-бутоксикарбонилокси.
Получаемые согласно способу соединения обычным образом можно переводить в другие соединения формулы I.
Полученные соли можно превращать в свободные соединения, например, путем обработки основанием, как гидроскид щелочного металла, карбонат металла или гидрокарбонат металла, или аммиак, или другим, указанным выше, солеобразующим основанием; с помощью кислоты, как неорганическая кислота, например, хлороводорода, или другой указанной выше кислоты, образующей соль.
Полученные соли известным образом можно переводить в другие соли: соли с кислотой, например, путем обработки с помощью пригодной соли металла, как соли натрия, бария или серебра, другой кислоты в пригодном растворителе, в котором образующаяся неорганическая соль нерастворима и таким образом выделяется из реакционной массы, и основные соли путем выделения кислоты, образующей соли, переводом основания в другую соль.
Соединения формулы I, включая их соли, можно получать также в виде гидратов или сольватов с используемым для кристаллизации растворителем.
Полученную смесь диастереомеров и рацематов, используя различия в физико-химических свойствах, известным образом можно разделять на чистые диастереомеры, соответственно рацематы, например, путем хроматографии и/или фракционной кристаллизации.
Полученные рацематы далее известными методами можно разделять на оптические антиподы, например, путем перекристаллизации из оптически активного растворителя с помощью микроорганизмов или путем введения во взаимодействие полученной смеси диастереомеров, соответственно рацемата, с оптически активным вспомогательным соединением. Например, соответственно полученные в соединениях формулы I кислотные, основные или функционально изменяемые группы обрабатывают оптически активной кислотой, основанием или оптически активным спиртом, превращая в смеси диастереомерных солей, соответственно функциональных производных, как сложные эфиры, разделяют их на диастереомеры, из которых желательный энантиомер можно выделять обычным образом. Пригодными для этой цели основаниями, кислотами, спиртами являются, например, оптически активные алкалоидные основания, как стрихнин, цинхонин или бруцин, или D- или L-(1-фенил)-этиламин, 3-пипеколин, эфедрин, амфетамин, и обычные синтетически получаемые основания, оптически активные карбоновые или сульфокислоты, как хинная кислота или D- или L-винная кислота, D- или L-ди-о-толуилвинная кислота, D или L-яблочная кислота, D- или L-миндальная кислота, или D- или L-камфорсульфокислота соответственно, оптически активные спирты, как борнеол или D- или L-(1-фенил)-этанол.
Изобретение относится также к тем вариантам осуществления способа, согласно которым исходят из полученного на какой-либо стадии способа в качестве промежуточного продукта соединения и осуществляют отсутствующие стадии или применяют исходное вещество в виде соли или, как правило, получают его при реакционных условиях (in sity).
Соединения формулы I, включая те, в которых R1 обозначает группу 1b, где R7, R8 и R9 обозначают незамещенный фенил и X- обозначает бром, М обозначает метилен, R2 обозначает водород, R4 обозначает метил и R3 обозначает водород, можно применять для получения соединения формулы XI и XII.
Объектом изобретения является 4-хлоркарбонил-1-бензилокси-карбонилпиперидин или его соль в качестве промежуточных продуктов для получения соединений общей формулы: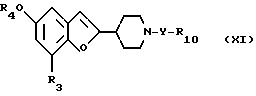
где X6 означает низший алкокси, низший алкенилокси или бензилокси или соединений формулы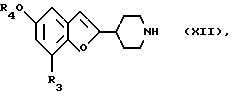
где
R3 обозначает галоген, а R4 обозначает низшую алкильную группу, или их солей.
Объектом настоящего изобретения являются новые производные пиперидина формулы XV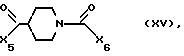
где
X5 обозначает галоген или группу формулы X7-O-, в которой X7 обозначает низшую алкансульфонилгруппу, низшую алкоксикарбонильную группу или группу формулы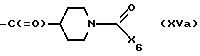
где X6 обозначает низшую алкоксигруппу, низшую алкенилоксигруппу или бензилоксигруппу при условии, что X6 не является бензилоксигруппой, если X5 обозначает хлор, и их соли.
Предпочтительны соединения формулы XV, где X5 обозначает галоген или группу формулы X7-O-, в которой X7 обозначает низшую алкансульфонилгруппу или низшую алкоксикарбонильную группу, и X6 обозначает низшую алкоксигруппу, или их соли.
Наиболее предпочтительны соединения формулы XV, выбранные из группы:
4-хлоркарбонил-1-этоксикарбонилпиперидин,
4-хлоркарбонил-1-аллилоксикарбонилпиперидин,
1-этоксикарбонил-4-метансульфонилоксикарбонилпиперидин,
1-этоксикарбонил-4-изобутилоксикарбонилоксикарбонилпиперидин,
1-этоксикарбонил-4-пивалоилоксикарбонилпиперидин, и
ангидрин 1,1'-бис(этоксикарбонил)пиперидин-4-карбоновой кислоты.
Изобретение также относится к способу получения производных пиперидина формулы
где X5 представляет галоген или группу формулы X7-O-, в которой X7 обозначает низшую алкансульфонилгруппу, низшую алкоксикарбонильную группу формулы
где X6 обозначает низшую алкоксигруппу, низшую алкенилоксигруппу или бензилоксигруппу при условии, что X6 не является бензилоксигруппой, если X5 обозначает хлор, и их солей, заключающемуся в том, что соединение формулы XVIII
где Y и R10 имеют указанные значения, или соль этого соединения подвергают взаимодействию с тионилгалогенидом, низшим алкансульфонилгалогенидом или сложным низшим алкиловым эфиром галогензамещенной муравьиной кислоты, и при необходимости полученное соединение переводят в другое соединение формулы XV, и/или полученное согласно изобретению свободное соединение переводят в соль, или полученную согласно изобретению соль переводят в соответствующее свободное соединение.
При этом галоген обозначает обычно хлор или бром; (низший алкан)-сульфонил обозначает, например, C1-C4- алкансульфонил, как метан- или этансульфонил; низший алканоил-, например, C1-C7-алканоил, как ацетил, пропионил, бутирил или пивалоил; (низший алкокси)-карбонил, например, C1- C4-алкоксикарбонил, как метоксикарбонил, этоксикарбонил, пропилоксикарбонил, изопропилоксикарбонил, бутилоксикарбонил, изобутилоксикарбонил, втор.-бутилоксикарбонил или трет.- бутилоксикарбонил; низший алкокси- означает, например, C1- C4-алкокси, как метокси, этокси, пропилокси, изопропилокси, бутилокси, изобутилокси, втор.-бутилокси или трет.-бутилокси; низший алкенилокси означает в особенности аллилокси и фенил-(низший алкокси)-, предпочтительно бензилокси.
Изобретение, например, относится к таким соединениям формулы XV, где X5 обозначает галоген или группу формулы X7-O-, в которой X7 обозначает (низший алкан)-сульфонил или (низший алкокси)-карбонил, и X6 обозначает низший алкоксил; и к их солям, способу их получения и их применению в качестве промежуточных продуктов.
Соединения формулы XV были синтезированы специально для получения соединений формулы XII.
Согласно изобретению предлагаются способы получения соединений XII, обладающих антидепрессивной активностью.
Первый способ получения производных пиперидина формулы XII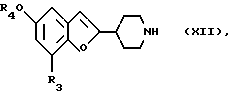
где R3 является галогеном и R4 является низшей алкильной группой, или их фармацевтически приемлемых солей с использованием производного гидрохинона, заключается в том, что
g1) соединение формулы
где R1 обозначает гидроксильную группу или низшую алкоксигруппу и R4 обозначает низшую алкильную группу или соль этого соединения галогенируют путем обработки элементарным галогеном в низшем алканоле в мета-положении по отношению группе R1-C(=O)-, причем если R1-C(=O)- означает карбоксигруппу, последнюю этерифицируют в низшую алкоксикарбонильную группу. В полученном соединении формулы
где X1 обозначает низшую алкоксикарбонильную группу, R3 является галогеном и R4 обозначает низшую алкильную группу или соли этого соединения, восстанавливают группу X1 в гидроксиметил.
Полученное соединение формулы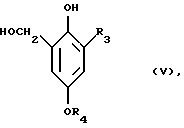
где R3 обозначает галоген и R4 обозначает низшую алкильную группу, обрабатывают в присутствии галоидводородной кислоты формулы HX2 соединением формулы VIIc
где R7, R8 и R9 обозначают фенильную группу, или солью соединения формулы VIIc с галоидводородной кислотой формулы HX2,
h) полученное соединение формулы
подвергают взаимодействию с соединением формулы
или солью этого соединения, где X5 обозначает галоген или группу формулы X7-O-, в которой X7 обозначает низшую алкансульфонилгруппу, или низшую алкоксикарбонильную группу, или группу формулы
и X6 обозначает низшую алкоксигруппу, низшую алкенилоксигруппу или бензилоксигруппу,
i) полученное соединение формулы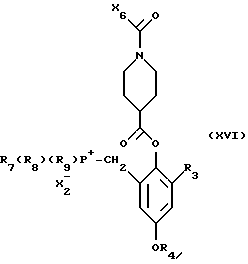
циклизуют в соответствующее соединение формулы
и
j) из этого соединения отщепляют группу формулы -C(=O)-X6 и при необходимости полученное свободное соединение переводят в соль с кислотой или полученную соль с кислотой переводят в свободное соединение или другую соль кислоты.
Объектом изобретения является также способ получения производных пиперидина формулы XII:
где R3 обозначает галоген и R4 обозначает низшую алкильную группу, и их фармацевтически приемлемых солей на основе производного гидрохинона, заключающийся в том, что
g2) соединение формулы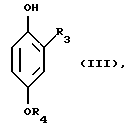
где R3 обозначает галоген и R4 обозначает низшую алкильную группу, или соль этого соединения обрабатывают параформальдегидом или триоксаном и полученное соединение формулы
где R3 обозначает галоген и R4 обозначает низшую алкильную группу, подвергают взаимодействию в присутствии галоидводородной кислоты формулы HX2 с соединением формулы VIIc
где R7, R8 и R9 обозначают фенильную группу, или с солью соединения формулы VIIc и галоидводородной кислоты формулы HX2.
h) полученное соединение формулы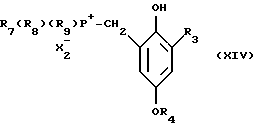
подвергают взаимодействию с соединением формулы
или с солью этого соединения, где X5 обозначает галоген или группу формулы X7-O-, в которой X7 обозначает низшую алкансульфонилгруппу, низшую алкоксикарбонильную группу или группу формулы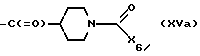
и X6 обозначает низшую алкоксигруппу, низшую алкенилоксигруппу или необязательно замещенную низшей алкильной группой, низшей алкоксигруппой, галогеном или нитрогруппой фенилнизшую алкоксигруппу,
i) полученное соединение формулы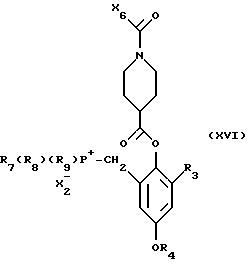
циклизуют в соответствующее соединение формулы
и
j) из этого соединения отщепляют группу формулы -C(=O)-X6 и при необходимости полученное свободное соединение переводят в соль с кислотой или полученную соль с кислотой переводят в свободное соединение или другую соль с кислотой.
Другой способ получения производных пиперидина формулы XII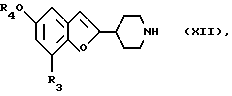
где R3 обозначает галоген и R4 обозначает низшую алкильную группу, и их фармацевтических приемлемых солей на основе производного гидрохинона заключатся в том, что
g3) соединение формулы
где R4 обозначает низшую алкильную группу и где R7, R8 и R9 обозначают фенильную группу, галогенируют путем обработки элементарным галогеном в низшем алканоле в мета-положение по отношению к группе формулы R7(R8)- (R9)P+CH2,
h) полученное соединение формулы
где R3 обозначает галоген, подвергают взаимодействию с соединением формулы
или солью этого соединения, где X5 обозначает галоген или группу формулы X7-O-, в которой X7 обозначает низшую алкансульфонилгруппу, низшую алкоксикарбонильную группу или группу формулы
и X6 обозначает низшую алкоксигруппу, низшую алкенилоксигруппу или необязательно замещенную низшим алкилом, низшим алкоксилом, галогеном или нитрогруппой фенил-низшую алкоксигруппу,
i) полученное соединение формулы
циклизуют в соответствующее соединение формулы
и
j) из этого соединения отщепляют группу формулы -C(=O)-X6 и при необходимости полученное свободное соединение переводят в соль с кислотой или полученную соль с кислотой переводят в свободное соединение или в другую соль с кислотой.
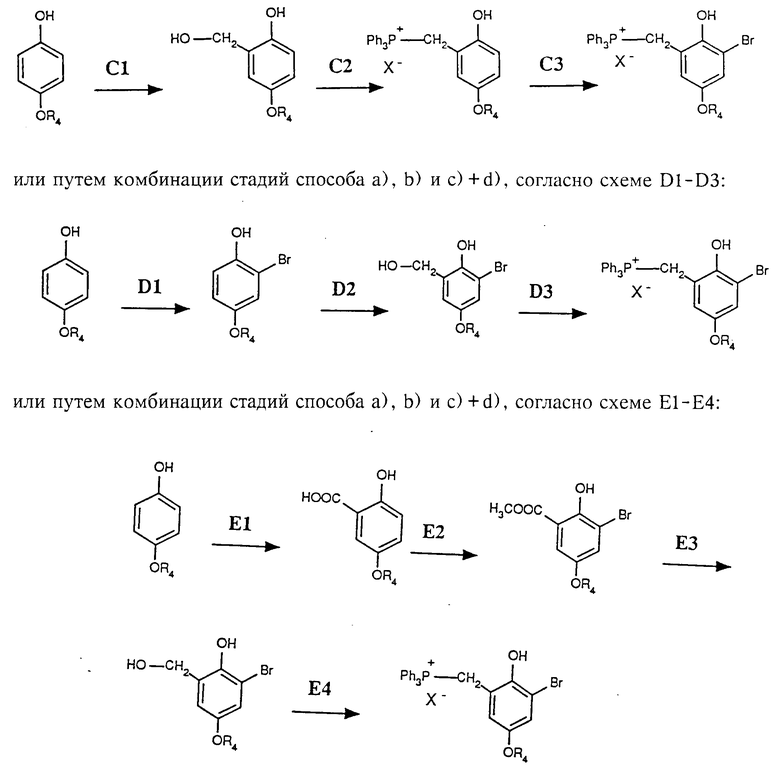
Более подробно способ можно описать схемой B1 B5, приведенной в конце описания.
Возможны также варианты осуществления способов путем комбинации стадий способа b), c)+d) и f) согласно схемам C1-C3, D1 D3, E1 E4, приведенных в конце описания.
При получении (3-бром-2-окси-5-метоксибензил)-фосфонийгалогенида. Это позволяет обходиться без больших потерь, имеющихся при использовании альдегидов, и таким образом повышать выход от 34,5% от теории до 37,9% от теории по схеме (C1-C3), 41,8% от теории (D1-D3), соответственно 50,2% от теории (E1-E4).
Исходя из 4-метоксифенола, согласно изобретению можно легко достигать следующих выходов Брофаромин-гидрохлорида:
схема B1-B5: 27,8% схема C1-C3, B3-B5: 29,0%
схемы D1-D3, B3-B5: 32,0% и схемы E1-E4, B3-B5: 38,4%
Осуществление реакций согласно способу проводят по аналогии с реакциями и образованием исходных веществ, являющихся промежуточными продуктами формул III-IX, обычно, как описано выше в приводимых при получении соединений формулы I вариантах способа a)-e). При этом, если специально не оговорено, применяются обычные, смотря по обстоятельствам, вспомогательные средства, такие как катализаторы, конденсирующие агенты, а также средства для сольволиза и/или растворители, соответственно разбавители, и реакционные условия, такие как температура и давление, а также, в случае необходимости, инертные газы.
Согласно варианту способа ж) проводят обработку соединений формул III, соответственно XIII, с помощью галогена, например, как описано выше в варианте способа a), соответственно d); восстановление соединений формулы IV, а также взаимодействие соединений формулы III с параформальдегидом или триоксаном проводят, как описано выше в варианте способа b), и взаимодействие соединений формул V и VIIc проводят, например, как описано выше в варианте способа d).
Взаимодействие соединений формул XIV и XV согласно варианту способа h) осуществляют, например, аналогично тому, как указано выше для варианта способа f).
Циклизацию согласно варианту способа h) проводят, например, в присутствии основного конденсирующего агента, как карбоната щелочного металла, как карбонат калия, в сложном эфире или нитриле низшей алкановой кислоты, как ацетонитрил, предпочтительно при осаждении образующегося в качестве побочного продукта галогенида фосфония за счет добавки алифатического углеводорода, как C5-C10- алкана, например, гексана, к раствору сырого продукта в аралифатическом углеводороде, как толуол.
Отщепление группы -C(= O)-X6 согласно варианту способа j) можно осуществлять обычным образом, например, путем обработки основанием, в особенности гидроксидом калия в этиленгликоле.
Изобретение также относится к таким вариантам осуществления вышеописанного способа, согласно которым исходят из полученного на любой стадии способа в качестве промежуточного продукта соединения и проводят отсутствующие стадии или применяют исходное вещество в виде соли или в особенности получают в реакционных условиях.
Реагентом, вводящим остаток X5, являются, например, галогенирующие средства, такие как галоидангидриды кислородных кислот серы или фосфора, как тионилхлорид, тионилбромид фосфора или пентахлорид фосфора, или соединения формулы X7-X5 (XIX), где X5 и X7 имеют вышеуказанные значения, как соответствующие (низший алкан)-сульфонилгалогениды [XV; X7 (низший алкан)-сульфонил; X5 галоген] галоидангидриды низших алкановых кислот соответственно, ангидриды низших алкановых кислот [XV; X7 низший алканоил; X5 галоген или -OX7] или низшие алкиловые эфиры галогенмуравьиной кислоты [XV; X5 галоген]
Взаимодействие осуществляется обычно, например, в присутствии основного конденсирующего агента, как третичного органического азотистого основания, как пиридин, или алифатического, или циклоалифатического амина, например, триэтиламин, пиперидин или N-метилморфолин, предпочтительно в аралифатическом или галогеналифатическом углеводороде, как толуол или дихлорметан, и в температурном интервале примерно от -25oC до примерно 50oC, желательно при 0-25oC.
Пример 1. Суспензию 81,8 г 2-бром-4-метоксифенола и 24,9 г борной кислоты в 55 мл толуола кипятят с обратным холодильником с водоотделителем до тех пор, пока не будет более выделяться вода (примерно 12 ч). Затем тонкую светлокоричневую суспензию охлаждают до 90oC и в течение 40 минут порциями смешивают с 13 г параформальдегида. Смесь дополнительно перемешивают 1 ч при 90oC, после последующего охлаждения до 70oC смешивают со 100 мл воды, затем охлаждают до 20oC и с помощью концентрированного раствора гидроксида натрия устанавливают pH 8,5. Суспензию коричневого цвета перемешивают 30 мин и с помощью концентрированной серной кислоты устанавливают pH 2,5. Полученный после отсасывания остаток на фильтре промывают дважды по 50 мл этилацетатом. Объединенные фильтраты хорошо смешивают и органическую фазу отделяют и выпаривают. Остающийся маслянистый остаток хроматографируют на силикагеле с помощью смеси толуола с этилацетатом (4:1) в качестве растворителя. Таким образом полученный 3-бром-2-окси-5-метоксибензиловый спирт имеет Rf- значение 0,3; выход 50% от теории.
Пример 2. Раствор 160 г 3-бром-2-окси-5-метоксибензальдегида в 800 мл этанола при 5-10oC в течение 1 ч порциями смешивают с 18 г бромгидрида натрия. Полученную суспензию доводят до pH 2,5 с помощью серной кислоты (10%-ной) и смесь концентрируют в вакууме до объема 500 мл. Добавляют 200 мл этилацетата, отделяют органическую фазу, водную фазу экстрагируют дважды по 100 мл этилацетатом, объединенные органические фазы промывают водой, сушат их над сульфатом натрия и выпаривают. Полученный маслянистый остаток кристаллизуют из толуола. Таким образом получают 3-бром-2-окси-5- метоксибензиловый спирт в форме бесцветных кристаллов [т.пл. 76oC; ИК-спектр (KBr): 3500, 3280, 2930, 1580, 1470, 1425, 1285, 1235, 1190, 1165, 1125, 1060, 1050, 1040 см-1. 1H-ЯМР (360 МГц, CDCl3): 2,40 (br.s, 1H, CH2OH); 3,75 (s. 3H, OCH3); 4,74 (s. 2H, CH2OH); 6,34 (br.s, 1H, OH); 6,73 (d, 1H); 6,97 (d, 1H) частей на миллион] выход 91% от теории.
Пример 3. В раствор 459 г трифенилфосфана и 387 г 3-бром-2-окси-5-метокси-бензилового спирта в 600 мл этилацетата при 40-60oC в течение 30 мин пропускают 67 г хлорводорода. Затем перемешивают 5 ч при 75oC, причем продукт спустя 30 мин начинает кристаллизоваться. Охлаждают до 0oC, перемешивают следующий час и затем при этой температуре кристаллизат отсасывают. Получают таким образом [(3-бром-2-окси-5-метоксифенил)метил]-трифенилфосфонийхлорид в форме бесцветных кристаллов (т.пл. 257oC (разложение); ИК-спектр (KBr): 3010, 2880, 1605, 1585, 1565, 1440, 1420, 1330, 1260, 1225, 1150 см-1. 1Н-ЯМР (360 МГц, CH3OH- d4); 3,50 (s, 3H, OCH3); 4,84 (d, 2H, CH2P+); 6,49 (dd, 1H); 7,05 (dd, 1H); 7,61-7,77 (m, 12H); 7,88 (m, 3H) частей на миллион; выход 89% от теории.
Пример 4. К раствору 50 г [(2-окси-5-метоксифенил)метил]- трифенилфосфонийбромида в 1 л метанола при 5oC в течение 1,5 ч прикапывают 16 г брома. Затем раствор концентрируют в вакууме при 20oC до объема 130 мл, в течение 2 ч добавляют 250 мл этилацетата, образовавшуюся суспензию желтого цвета перемешивают 2 ч при 0oC, слабо-желтые кристаллы отсасывают и перекристаллизовывают их из метанола. Таким образом получают [(3-бром-2-окси-5-метоксифенил)метил] -трифенилфосфонийбромид в форме бесцветных кристаллов (т.пл. 259oC); ИК-спектр (KBr): 2875, 1585, 1565, 1415, 1325, 1200, 1165, 1150 см-1. 1Н-ЯМР (360 МГц, DMSO-d6):3,43 (s, 3H, OCH3); 5,03 (d, 2H, CH2P+); 6,42 (dd, 1H); 7,08 (dd, 1H); 7,61-7,80 (m, 12H); 7,92 (m, 3H); 9,00 (br.s, 1H, OH) частей на миллион; выход 76% от теории.
Пример 5. В раствор 49,8 г 2-окси-5-метоксибензилового спирта и 115,8 г трифенилфосфина в 150 мл ацетонитрила при 40-60oC в течение 30 мин пропускают 18 г хлорводорода. Затем перемешивают 5 ч при 75oC, причем продукт спустя примерно 30 мин начинает кристаллизоваться. Охлаждают до 0oC, перемешивают следующий час и затем кристаллизат отсасывают при этой температуре. Получают таким образом [(2-окси-5-метоксифенил)метил]-трифенилфосфонийхлорид в форме бесцветных кристаллов (т.пл. 270oC) (разложение); ИК-спектр (KBr): 2990, 1585, 1395, 1295, 1240, 1145, 995 см-1. 1 Н-ЯМР (360 МГц, CH3OH-d4): 3,47 (s, 3H, OCH3); 4,74 (d, 2H, CH2P+); 6,40 (dd, 1H); 6,73 (m, 1H); 7,56- 7,72 (m, 12H); 7,87 (m, 3H) частей на миллион; выход 78% от теории.
Пример 6. К раствору 35 г [(2-окси-5-метоксифенил)метил]- трифенилфосфонийхлорида в 700 мл метанола при 5oC в течение 1,5 ч прикапывают 13 г брома. Раствор концентрируют в вакууме при 20oC до объема 110 мл, в течение 2 ч добавляют 220 мл этилацетата, перемешивают образовавшуюся желтую суспензию в течение 2 ч при 0oC, отсасывают слабо желтые кристаллы и перекристаллизуют их из метанола. Получают смесь бесцветных кристаллов (т.пл. 210oC), которая согласно титру AgNO3 состоит из 22,4 мас. [(3-бром-2-окси-5-метоксифенил)метил] трифенилфосфонийхлорида и 77,6 мас. [(3-бром-2-окси-5-метоксифенил)метил] трифенилфосфонийбромида; выход 76% от теории.
Пример 7. Раствор 578,2 г 4-карбокси-1-этоксикарбонилпиперидина в 1200 мл толуола сначала смешивают с 1,0 г N,N-диметилформамида и затем при 68-70oC в течение 2 ч с 369,0 г тионилхлорида. Перемешивают еще 30 мин при 70oC, затем отгоняют в вакууме толуол и остаток затем в течение примерно 30 мин дегазируют при комнатной температуре в высоком вакууме. Таким образом получают 4-хлоркарбонил-1-этоксикарбонилпиперидин в виде слабо желтого масла [содержание продукта по NaOH и AgNO3-титру: 98% ИК-спектр (пленка): 2969, 2870, 1790, 1695, 1470, 1435, 1300, 1230, 1130, 960, 765 см-1] Продукт перегоняется без разложения при т.кип. 98-98oC (0,08-0,09 торр); выход после дистилляции 94,7% от теории.
Пример 8. Аналогичным образом, как описано в примере 7, исходя из 4-карбокси-1-бензилоксикарбонилпиперидина получают 4-хлоркарбонил-1-бензилоксикарбонилпиперидин.
Пример 9. Аналогичным образом, как описано в примере 7, исходя из 4-карбокси-1-аллилоксикарбонилпиперидина получают 4-хлоркарбонил-1-аллилоксикарбонилпиперидин.
Пример 10. В сухой колбе для сульфирования при 20oC в 150 мл толуола растворяют 24,1 г (120 ммоль) 4-карбокси-1-этоксикарбонилпиперидина. Затем охлаждают до 0oC и в течение 5 мин добавляют 13,8 (120 ммоль) метансульфонилхлорида. После этого в течение 15 мин при 0oC добавляют раствор 12,1 г (120 ммоль) N-метилморфолина в 50 мл толуола, оставляют перемешиваться еще следующие 30 мин при 20oC, фильтруют осадившийся гидрохлорид N-метилморфолина в отсутствии влаги. Образовавшийся желтоватый раствор 1-этоксикарбонил-4- метансульфонилоксикарбонилпиперидина в толуоле без дальнейшей очистки можно использовать для следующей стадии.
Пример 11. Аналогичным образом, как описано в примере 10, путем введения во взаимодействие 4-карбокси-1-этоксикарбонилпиперидина с пивалоилхлоридом получают 1-этоксикарбонил-4- пивалоилоксикарбонилпиперидин.
Пример 12. В сухой колбе для сульфирования при 20oC в 120 мл дихлорметана растворяют 27,7 г (138 ммоль) 4-карбокси-1- этоксикарбонилпиперидина. После охлаждения до -10oC в течение 5 мин добавляют раствор 18,48 г (138 ммоль) изобутилового эфира хлормуравьиной кислоты в 15 мл дихлорметана. После перемешивания в течение 5 мин и охлаждения до -10oC в течение 15 мин добавляют 13,96 г (138 ммоль) триэтиламина, растворенные в 15 мл дихлорметана. Перемешивают еще следующие 30 мин при 0oC и образовавшийся прозрачный, светложелтый раствор 1-этоксикарбонил-4- изобутилоксикарбонилоксикарбонилпиперидина используют на следующей стадии. Для того чтобы исключить смешение растворителей на последующей стадии (см. пример 18), обезвоженный дихлорэтан можно отогнать в вакууме и маслянистый остаток растворить в безводном ацетонитриле.
Пример 13. Аналогичным образом, как описано в примерах 7, 10 или 11, путем введения во взаимодействие 4-карбокси-1- этоксикарбонилпиперидина с 4-хлоркарбонил-1- этоксикарбонилпиперидином получают ангидрид 1,1'-бис(этоксикарбонил)- пиперидин-4-карбоновой кислоты.
Пример 14. В отсутствии воздуха 43,9 г 4-хлоркарбонил-1- этоксикарбонилпиперидина растворяют в 250 мл безводного ацетонитрила (дегазированного) и раствор смешивают с 53,4 г [(3-бром-2-окси-5- метоксифенил)метил]-трифенилфосфонийхлорида. К полученной суспензии при 25-30oC в течение 30 мин прикапывают 20 г пиридина. Смесь кипятят с обратным холодильником в течение 5 ч, затем ее гидролизуют с помощью 100 мл раствора карбоната натрия (15%), отделяют органическую фазу, промывают ее последовательно с помощью 100 мл 1н соляной кислоты и 100 мл воды, выпаривают ее в вакууме и оставшийся маслянистый остаток растворяют в 50 мл дихлорметана. К этому раствору при интенсивном перемешивании при 20oC в течение 30 мин прикапывают 200 мл этилацетата, при этом кристаллизуется продукт. Полученную суспензию кристаллов концентрируют до объема 150 мл на роторном испарителе в слабом вакууме и затем перемешивают 2 ч при 0oC. После отсасывания и высушивания получают [(3-бром-2-[(1- этоксикарбонилпиперидин-4-ил)карбонилокси] -5-метоксифенил)метил]- трифенилфосфонийхлорид (т. пл. 196oC); ИК-спектр (KBr): 3415, 3060, 2855, 2780, 1600, 1565, 1385, 1270, 1190, 1165 см-1; 1Н-ЯМР (360 МГц, CDCl3):1,28 (t, 3H, CO2CH2CH3); 1,45 (m, 2H); 1,75 (m, 2H); 2,58 (m, 1H); 2,87 (m, 2H); 3,47 (s, 3H, OCH3); 4,00 (m, 2H); 4,13 (q, 2H, CO2CH2CH3); 5,37 (br.d, 2H, CH2P+); 6,87 (dd, 1H); 7,07 (dd, 1H); 7,54-7,87 (m, 15H) частей на миллион; выход 66% от теории.
Пример 15. В суспензию 50 г 3-бром-2-окси-5-метоксибензилового спирта в 300 мл безводной уксусной кислоты при комнатной температуре в течение 30 мин пропускают 20 г бромводорода. Перемешивают дополнительно 5 ч при комнатной температуре и образовавшийся раствор выпаривают. Слабокоричневый маслянистый остаток, который при стоянии при комнатной температуре медленно кристаллизуется, кристаллизуют при добавлении небольшого количества активного угля из смеси этилацетат с циклогексаном (5:1). Таким образом получают 3-бром-2-окси-5- метоксибензилбромида [1Н-ЯМР (360 МГц, CDCl3:3,75 (s, 3H, OCH3); 4,53 (s, 2H, CH2Br); 5,45 (s, 1H, OH); 6,85 (d, 1H); 7,00 (d, 1H) частей на миллион]
Пример 16. 20,0 г 3-бром-2-окси-5-метоксибензилбромида смешивают с 8,8 г триметилфосфина и смесь при перемешивании нагревают 3 ч при 140oC (согласно ТСХ полное превращение). Полученное масло с помощью смеси толуола с этилацетатом (4: 1) в качестве растворителя фильтруют через небольшое количество силикогеля. Получают таким образом диметиловый эфир [(3-бром-2-окси-5-метоксифенил)метил] -фосфоновой кислоты [1Н- ЯМР (360 МГц, CDCl3):3,20 (d, 2H, CH2P, 2JP-H= 21 Гц); 3,70 (s, 3H, OCH3); 3,74 (d, 6H, 2•OCH3, 3JP-H=1 Гц); 6,70 (m, 1H); 7,07 (m, 1H) частей на миллион]
Пример 17. В суспензию 20 г размолотого карбоната калия (безводного) в 100 мл ацетонитрила в отсутствии воздуха при 25-30oC в течение 30 мин вносят 50 г [(3-бром-2-[(1- этоксикарбонилпиперид-4- ил)карбонилокси]-5-метоксифенил)метил] трифенилфосфонийхлорида. Смесь перемешивают 2 ч при комнатной температуре, затем смешивают с 80 мл воды и подкисляют концентрированной соляной кислотой до pH=1,0. Органическую фазу отделяют и выпаривают, маслянистый остаток обрабатывают 50 мл толуола и при 20oC в течение 1 ч смешивают со 100 мл гексана, причем основное количество [примерно 90% содержание согласно HPLC (жидкостная хромaтография высокого давления):90% образовавшегося трифенилфосфиноксида выкристаллизуется. Суспензию кристаллов отсасывают и осадок на фильтре промывают дважды по 40 мл смесью гексана с толуолом (3:2). После выпаривания объединенных фильтратов и хроматографии остатка на силикагеле с помощью смеси толуола с этилацетатом (2:1) в качестве растворителя получают 4-(7-бром-5-метоксибензофуран-2-ил)-1-этоксикарбонилпиперидин (т.пл. 85oC); 1Н-ЯМР (360 МГц, CDCl3):1,28 (t, 3H, CO2CH2CH3); 1,69 (m, 2H); 2,09 (m, 2H); 2,95 (m, 3H); 3,80 (s, 3H, OCH3); 4,16 (q, 2H, CO2CH2 CH3); 4,14-4,35 (br.m, 2H); 6,36 (s, 1H); 6,90 (d, 1H); 7,00 (d, 1H) частей на миллион; выход 90 от теории.
Пример 18. К суспензии 105 г [(3-бром-2-окси-5-метоксифенил) метил]-трифенилфосфонийхлорида и 115 г размолотого карбоната калия (безводного) в 250 мл ацетонитрила в отсутствии воздуха при 25-30oC в течение 1,5-2 ч прикапывают 49 г 4-хлоркарбонил-1- этоксикарбонилпиперидина. Перемешивают 30 мин при 25-30oC, затем смешивают с 350 мл воды и подкисляют концентрированной соляной кислотой до pH=1,0. Органическую фазу отделяют и выпаривают. Маслянистый остаток растворяют в 160 мл толуола и в течение 1 ч при 20oC смешивают с 250 мл гексана, при этом выкристаллизуется основное количество (примерно 80% содержание согласно HPLC: 85%) образовавшегося трифенилфосфиноксида. Суспензию кристаллов отсасывают и осадок на фильтре промывают дважды по 40 мл смесью гексана с толуолом (3:2). Объединенные фильтраты выпаривают и маслянистый остаток хроматографируют на силикагеле с помощью смеси толуола с этилацетатом (2:1) в качестве растворителя. Получают таким образом 4-(7-бром-5-метоксибензофуран-2-ил)-1- этоксикарбонилпиперидин, который идентичен продукту, полученному в примере 10. Выход 86% от теории.
Пример 19. К раствору 45,9 г метилового эфира 2-окси-5- метоксибензойной кислоты в 125 мл гептана при 20oC в течение 30-45 мин при перемешивании прикапывают 43,9 г брома. Реакционную смесь затем перемешивают 3-4 ч, после чего разбавляют 100 мл воды, перемешивают следующий час и затем смешивают с 295 мл гептана и 46 мл трет-бутилметилового простого эфира. Затем смесь нагревают до 50-55oC и отделяют водную фазу. Органическую фазу экстрагируют дважды по 114 мл водой и охлаждают до -20oC. Получают таким образом метиловый эфир 3-бром-2-окси-5-метоксибензойной кислоты. Выход 82,5% от теории.
Пример 20. К раствору 8 г боргидрида натрия в 280 мл тетрагидрофурана при 20oC в течение 1 ч при перемешивании прикапывают раствор 57 г метилового эфира 3-бром-2-окси-5- метоксибензойной кислоты в 110 мл тетрогидрофурана. Реакционную смесь перемешивают следующие 2,5 ч и гидролизуют с помощью 105 мл 2н соляной кислоты и устанавливают pH=2,5. Водную фазу отделяют. Органическую фазу экстрагируют трижды по 90 мл раствором хлорида натрия (10%), выпаривают на роторном испарителе, разбавляют 100 мл толуола, концентрируют на роторном испарителе до 100 г, при 60oC в течение 30 мин добавляют к нагретой до 70-80oC суспензии из 55,1 г трифенилфосфина, 8,8 г хлороводорода и 42 мл толуола. Реакционную смесь перемешивают следующие 7 ч и затем охлаждают до 0.-5oC. Образовавшийся кристаллизат фильтруют, промывают 4 раза по 40 мл толуолом и высушивают в высоком вакууме. Получают таким образом [(3-бром-2-окси- 5-метоксифенил)метил]-трифенилфосфонийхлорид, который идентичен продукту, полученному согласно примеру 3; выход 79% от теории.
Пример 21. 7,6 г 4-(7-бром-5-метоксибензофуран-2-ил)-1- этоксикарбонилпиперидина растворяют в 80 мл этиленгликоля. После добавления 19,4 г 86% -ного гидроксида калия образовавшийся мутный раствор при сильном перемешивании нагревают 18 ч при 160oC. Реакционную смесь охлаждают до 100oC, разбавляют 80 мл толуола и охлаждают далее до 20oC. Реакционный раствор экстрагируют дважды по 1000 мл водой и затем четырежды по 200 мл 10%-ным раствором метансульфокислоты в воде. Метансульфоновокислый раствор доводят до pH=12 путем добавления 30%-ного раствора гидроксида натрия и встряхивают с 1000 мл хлороформа, хлороформенный раствор сушат над сульфатом натрия, фильтруют и выпаривают. После кристаллизации из этилацетата получают 4-(7-бром-5-метоксибензофуран-2-ил)-пиперидин с т.пл. 149-152oC. Из основания путем обработки метанольным раствором соляной кислоты и перекристаллизации из смеси метанола с эфиром получают гидрохлорид 4-(7-бром-5-метоксибензофуран-2-ил)-пиперидина с т.пл. 242-243oC.

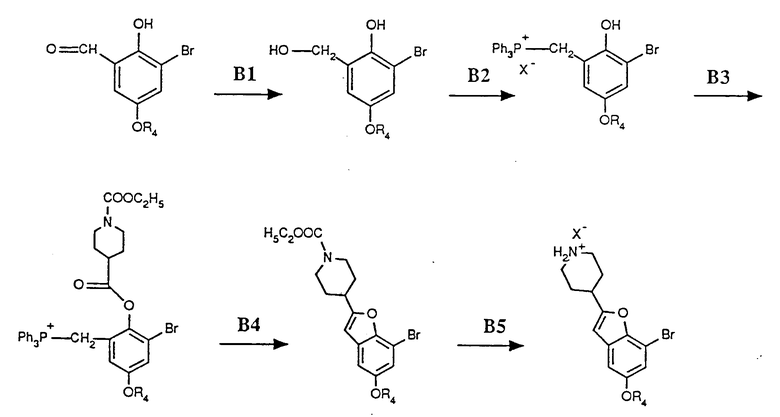
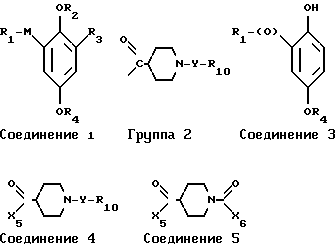
Использование: в медицине как полупродукты для получения антидепрессантов. Сущность: продукты - производные гидрохинона ф-лы I, где R4 - низший алкил и R1 - OH, галоген, -P(O)(R5)(R6) или P+(R7)(R8)R9X-, M - метилен, R2 - H или группа формулы 2, R3 -H, галоген или R1 - OH или низшая алкоксильная группа, М - карбонил, R2 - H и R3 - галоген, R5 и R6 - низшая алкоксильная группа, R7, R8 и R9 - фенил, X- - анион галоидоводородной кислоты, У -группа - C(O), R10 - низшая алкильная группа. Реагент 1 соединение ф-лы 3, которое галогенируют, восстанавливают и подвергают взаимодействию с соединением ф-лы 4. Продукты - производные пиперидина ф-лы 5, где X5 - галоген или группа X7 - O, где X7 - низшие алкансульфонилгруппа или алкаксикарбонилгруппа, X6 - низшие алкоксилгруппа, алкенилоксигруппа, бензилоксигруппа. 10 с. и 16 з.п. ф-лы.
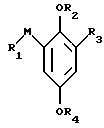
где R4 низший алкил;
R1 либо гидроксильная группа, галоген, группа формулы Iа
-P(=O)(R5)(R6),
либо группа формулы Ib
-P+(R7)(R8)R9X-;
М метилен;
R2 водород или группа формулы Id
R3 водород или галоген
или
R1 гидроксильная группа или низшая алкоксильная группа;
M карбонил;
R2 водород;
R3 галоген;
R5 и R6 низшая алкоксильная группа;
R7 R9 фенильная группа;
X- анион галоидоводородной кислоты;
Y группа формулы Ie
-(C=O)-
R1 0 низшая алкоксильная группа,
при условии, что в соединении I, где R1 группа формулы Ib, R7 R9 обозначают соответственно незамещенную фенильную группу и X- ион бромида, М метилен, R2 водород и R4 - метил, R3 не является водородом, и при условии, что в соединении I, где R1 гидроксильная группа, М метилен, R2 водород и R4 метил или этил, R3 не является водородом,
в свободном виде или в виде соли.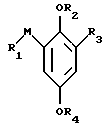
где R4 низшая алкильная группа;
R1 группа формулы Ib
-P+(R7)(R8)R9X-;
М метилен;
R2 группа формулы Id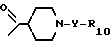
R3 галоген;
R7 R9 фенильная группа;
X- анион галоидоводородной кислоты;
Y группа формулы Ie
-(C=O)-
R1 0 низшая алкоксильная группа,
в свободном виде или в виде соли, отличающийся тем, что а) соединение формулы II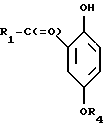
где R1 гидроксил или низший алкоксил;
R4 низший алкил,
или соль этого соединения галогенируют в мета-положение по отношению к группе R1-C(= O)-, причем группа R1-C(=O) должна быть в виде низшей алкоксикарбонильной группы; b) в полученном соединении формулы IV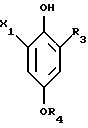
где X1 низший алкоксикарбонил;
R3 галоген;
R4 низшая алкильная группа,
или соли этого соединения, группу X1 восстанавливают в гидроксиметильную; с) в полученном соединении формулы V
гидроксиметильную группу переводят в галоидметильную; d) полученное соединение формулы VI
где X2 галоген;
R3 галоген;
R4 низшая алкильная группа,
подвергают взаимодействию с соединением формулы VIIc
или солью этого соединения с кислотой H-X, где X, R7 R9 имеют значения, указанные для формулы I; f) полученное соединение формулы IX
где X4 группа формулы Ib
-P+(R7)(R8)R9X-;
М метилен;
R3 галоген;
R4 низшая алкильная группа;
R7 R9 и X- имеют значения, указанные для формулы I,
обрабатывают соединением формулы X
или солью этого соединения,
где X5 галоген или группа формулы X7-O-, в которой X7 низшая алкансульфонилгруппа, низшая алкоксикарбонильная группа или группа формулы Xа
где R1 0 и Y имеют значения, указанные для формулы I,
и при необходимости полученное соединение переводят в другое соединение формулы I, отделяют и/или полученное согласно изобретению свободное соединение переводят в соль, или полученную согласно изобретению соль переводят в соответствующее свободное соединение.
где R4 низшая алкильная группа;
R1 группа формулы Ib
-P+(R7)(R8)R9X-;
М метилен;
R2 группа формулы Id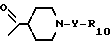
где R3 галоген;
R7 R9 фенильная группа;
X- анион галоидоводородной кислоты;
Y группа формулы Ie
-(C=O)-
R1 0 низшая алкоксильная группа,
в свободном виде или в виде соли, отличающийся тем, что b) соединение формулы III
где R3 галоген;
R4 низшая алкильная группа,
или соль этого соединения подвергают взаимодействию с параформальдегидом или триоксаном; с) в полученном соединении формулы V
оксиметильную группу переводят в галоидметильную группу; d) полученное соединение формулы VI
где X2 галоген;
R3 галоген;
R4 низшая алкильная группа,
подвергают взаимодействию с соединением формулы VIIc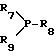
или солью этого соединения с кислотой HX, где X, R7 R9 имеют значения, указанные для формулы I; f) полученное соединение формулы IX
где X4 группа формулы Ib
-P+(R7)(R8)R9X-;
М метилен;
R3 галоген;
R4 низшая алкильная группа;
R7 R9 и X- имеют значения, указанные для формулы I,
подвергают взаимодействию с соединением формулы X
или солью этого соединения,
где X5 галоген или группа формулы X7-O-, в которой X7 низшая алкансульфонилгруппа, низшая алкоксикарбонильная группа, низшая алканоильная группа или группа формулы Xа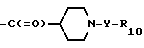
где R1 0 и Y имеют значения, указанные для формулы I,
и при необходимости полученное соединение переводят в другое соединение формулы I, отделяют и/или полученное согласно изобретению свободное соединение переводят в соль, или полученную согласно изобретению соль переводят в соответствующее свободное соединение.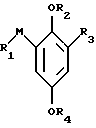
где R4 низшая алкильная группа;
R1 группа формулы Ib
-P+(R7)(R8)R9X-,
где М метилен;
R2 группа формулы Id
где R3 галоген;
R7 R9 фенильная группа;
X- анион галоидоводородной кислоты;
Y группа формулы Ie
-(C=O)-
R1 0 низшая алкоксильная группа,
в свободном виде или в виде соли, отличающийся тем, что е) соединение формулы VIII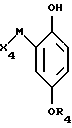
где X4 группа формулы Ib
-P+(R7)(R8)R9X-;
М метилен;
R4 низшая алкильная группа,
галогенируют в мета-положение по отношению к группе X4-M; f) полученное соединение формулы IX
где X4 группа формулы Ib
-P+(R7)(R8)R9X-;
М метилен;
R3 галоген;
R4 низшая алкильная группа;
R7 R9 и X- имеют значения, указанные для формулы I,
подвергают взаимодействию с соединением формулы X
или солью этого соединения,
где X5 галоген или группа формулы
X7-O-,
в которой X7 низшая алкансульфонилгруппа, низшая алкоксикарбонильная группа, низшая алканоильная группа или группа формулы Xа
где R1 0 и Y имеют значения, указанные для формулы I,
и при необходимости полученное соединение переводят в другое соединение формулы I, отделяют, и/или полученное согласно изобретению свободное соединение переводят в соль, или полученную согласно изобретению соль переводят в соответствующее свободное соединение.
где X5 галоген или группа формулы X7-O-, в которой X7 низшая алкансульфонилгруппа, низшая алкоксикарбонильная группа или группа формулы XVa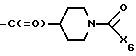
где X6 низшая алкоксигруппа, низшая алкенилоксигруппа или бензилоксигруппа, при условии, что X6 не является бензилоксигруппой, если X5 хлор,
и их соли.
X6 низшая алкоксигруппа,
и их соли.
где X5 галоген или группа формулы X7-O-, в которой X7 низшая алкансульфонилгруппа, низшая алкоксикарбонильная группа формулы XVa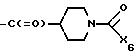
X6 низшая алкоксигруппа, низшая алкенилоксигруппа или бензилоксигруппа, при условии, что X6 не является бензилоксигруппой, если X5 хлор,
и их соли, отличающийся тем, что соединение формулы ХVIII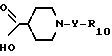
где Y и R1 0 имеют указанные значения,
или соль этого соединения подвергают взаимодействию с тионилгалогенидом, низшим алкансульфонилгалогенидом или сложным низшим алкиловым эфиром галогензамещенной муравьиной кислоты и при необходимости полученное соединение переводят в другое соединение формулы ХV, и/или полученное согласно изобретению свободное соединение переводят в соль, или полученную согласно изобретению соль переводят в соответствующее свободное соединение.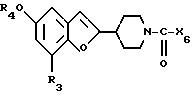
где X6 низш.алкокси, низш.алкенилокси или бензилокси,
или соединений формулы XII
где R3 галоген;
R4 низшая алкильная группа,
или их солей.
где R3 галоген;
R4 низшая алкильная группа,
фармацевтически приемлемых солей на основе производного гидрохинона, отличающийся тем, что g1) соединение формулы III
где R1 гидроксильная группа или низшая алкоксигруппа;
R4 низшая алкильная группа,
или соль этого соединения галогенируют путем обработки элементарным галогеном в низшем алканоле в мета-положение по отношению к группе R1-C(=O), причем карбоксигруппа R1-C(=O), если имеется, этерифицируется в низшую алкоксикарбонильную группу, в полученном соединении формулы IV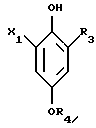
где X1 низшая алкоксикарбонильная группа;
R3 галоген;
R4 низшая алкильная группа,
или соли этого соединения группу X1 восстанавливают в гидроксиметил, полученное соединение формулы V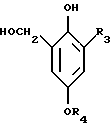
где R3 галоген;
R4 низшая алкильная группа,
обрабатывают в присутствии галоидоводородной кислоты формулы HX2 соединением формулы VIIс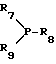
где R7 R9 -фенильная группа,
или солью соединения формулы VIIс с кислотой, и галоидоводородной кислотой формулы HX2; h) полученное соединение формулы XIV
подвергают взаимодействию с соединением формулы XV
или солью этого соединения,
где X5 галоген или группа формулы X7-O-, в которой X7 низшая алкансульфонилгруппа, или низшая алкоксикарбонильная группа, или группа формулы XVа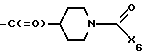
X6 низшая алкоксигруппа, низшая алкенилоксигруппа или бензилоксигруппа; i) полученное соединение формулы XVI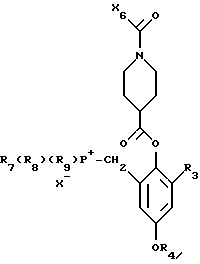
циклизуют в соответствующее соединение формулы XVII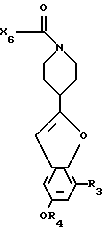
и j) из этого соединения отщепляют группу формулы -C(=O)-X6 и при необходимости полученное свободное соединение переводят в соль присоединения кислоты или полученную соль присоединения кислоты переводят в свободное соединение или другую соль присоединения кислоты.
где R3 галоген;
R4 низшая алкильная группа,
и их фармацевтически приемлемых солей на основе производного гидрохинона, отличающийся тем, что g2) соединение формулы III
где R3 галоген;
R4 низшая алкильная группа,
или соль этого соединения обрабатывают параформальдегидом или триоксаном и полученное соединение формулы V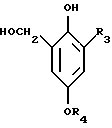
где R3 галоген;
R4 низшая алкильная группа,
подвергают взаимодействию в присутствии галоидоводородной кислоты формулы HX2 с соединением формулы VIIc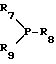
где R7 R9 фенильная группа,
или с солью присоединения кислоты к соединению формулы VIIc и галоидоводородной кислоты формулы HX2; h) полученное соединение формулы XIV
подвергают взаимодействию с соединением формулы XV
или с солью этого соединения,
где X5 галоген или группа формулы X7-O-, в которой X7 низшая алкансульфонилгруппа, низшая алкоксикарбонильная группа или группа формулы XVа
X6 низшая алкоксигруппа, низшая алкенилоксигруппа или в некоторых случаях необязательно замещенная низшей алкильной группой, низшей алкоксигруппой, галогеном или нитрогруппой фенилнизш.алкоксигруппа; i) полученное соединение формулы XVI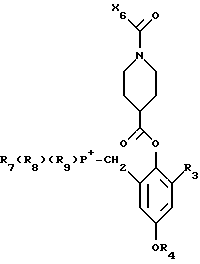
циклизуют в соответствующее соединение формулы XVII
j) из этого соединения отщепляют группу формулы -C(=O)-X6 и при необходимости полученное свободное соединение переводят в соль присоединения кислоты или полученную соль присоединения кислоты переводят в свободное соединение или в другую соль присоединения кислоты.
где R3 галоген;
R4 низшая алкильная группа,
и их фармацевтически приемлемых солей на основе производного гидрохинона, отличающийся тем, что g3) соединение формулы XIII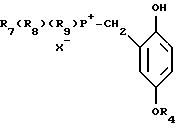
где R4 низшая алкильная группа;
R7 R9 фенильная группа,
галогенируют путем обработки элементарным галогеном в низшем алканоле в мета-положение по отношению к группе формулы R7(R8)(R9)P+CH2; h) полученное соединение формулы XIV
где R3 галоген,
подвергают взаимодействию с соединением формулы XV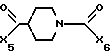
или солью этого соединения,
где X5 галоген или группа формулы X7-O-, в которой X7 низшая алкансульфонилгруппа, низшая алкоксикарбонильная группа или группа формулы XVа
X6 низшая алкоксигруппа, низшая алкенилоксигруппа или в некоторых случаях необязательно замещенная низшим алкилом, низшим алкоксилом, галогеном или нитрогруппой фенилнизш.алкоксигруппа; i) полученное соединение формулы XVI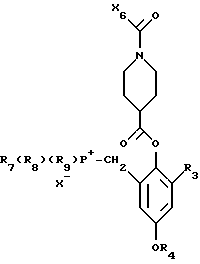
циклизуют в соответствующее соединение формулы XVII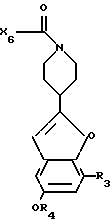
и j) из этого соединения отщепляют группу формулы -C(=O)-X6 и при необходимости полученное свободное соединение переводят в соль присоединения кислоты или полученную соль присоединения кислоты переводят в свободное соединение или в другую соль присоединения кислоты.
| US, патент, 3123648, кл.C 07C 43/225, 1964 | |||
| EP, заявка, 0302788, кл.C 07D 471/04, 1989 | |||
| DE, заявка, 2653147, кл.C 07D 405/04, 1974 | |||
| DE, патент, 2537837, кл.C 07D 405/04, 1976. |
Авторы
Даты
1997-11-10—Публикация
1992-09-03—Подача