Данное изобретение касается способа выделения высокоочищенного фактора VIII, в котором инактивированы вирусы, из плазмы крови или криопреципитата при помощи анионообменной хроматографии.
Европейская патентная заявка N 88108458.6 описывает способ получения высокоочищенного не содержащего вирусов антигемофилического фактора, заключающийся в том, что криопреципитат, содержащий фактор VIII, обрабатывают гидроксидом алюминия и биологически совместимыми органическими растворителями/детергентами, в предпочтительном варианте с последующей гельпроникающей хроматографией с применением ионообменного материала. Европейская патентная заявка N 88118478.2 описывает хроматографический материал на основе сополимеров олигоэтиленгликолей, глицидилметакрилатов, и пентаэритритолдиметакрилатов, которые особенно пригодны для получения высокоочищенного, не содержащего вирусов фактора VIII.
ЕП 0343275 AI касается способа получения высокоочищенного антигемофилического фактора (AHF или фактора VIII), который в процессе очистки криопреципитата становился не содержащим вирусом факторов в результате обработки биологически совместимыми органическими растворителями/детергентами. Способ заключается в том, что криопреципитат перед удалением из него вирусов оттаивали, экстрагировали водой, содержащей 1-3 E/мл гепарина при pH 6,5-7,5, смешивали затем с суспензией гидроксида алюминия и после охлаждения до 10-18oC и доведения величины pH до 6-7 центрифугировали и фильтровали и затем обрабатывали далее известным способом. Предпочтительно, в частности, подвергать пробу после удаления вирусов гельпроникающей хроматографии на ионообменных материалах. Известен способ очистки фактора VIII, получение его с высоким выходом и сохранением всех его признаков из исходного материала, содержащего фактор VIII и другие белки и факторы, описанный в Европейском патенте ЕП 0209041, включающий стадии: адсорбирования фактора VIII на гидрофобную, интерактивную матрицу, отделение нежелательных белков от фактора VIII и вымывание фактора VIII раствором, содержащим поверхностное активное вещество.
Элюирование фактора VIII осуществляют с помощью раствора, содержащего хлорид кальция и 440% этиленгликоль, а его промывку с помощью буферного раствора, содержащего хлорид натрия, глицин, хлорид кальция и гистидин.
Далее в ЕП 0209041 указывается, что использование определенных поверхностных активных агентов (см. пункт Ig) в элюирующем буфере абсолютно необходимо. Таким образом достигается эффективное восстановление AHF (антигемофилический фактор) активности из гидрофобной интерактивной матрицы. Однако данный способ не раскрывает эффективного удаления нежелательных белков.
Задачей настоящего изобретения является создание способа, способного улучшить выделение биологически активного фактора VIII из таких источников, как криопреципитат и плазма крови, и обеспечить более экономичный технологический процесс.
Поставленная задача достигается способом выделения высокоочищенного комплекса фактора VIII/фактора Виллебранда, в котором инактивированы вирусы, из плазмы крови или криопреципитата с использованием анионообменной хроматографии, при этом в качестве анионообменного материала используют материал для разделения на основе содержащих гидроксигруппы носителей, поверхности которых покрыты ковалентно связанными полимерами, содержащими повторяющиеся единицы, которые одинаковы или различны и представлены формулой I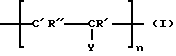
в которой
R' обозначает H или CH3,
Y обозначает 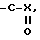 -CN, -CHO, -OH, -CH2, -NH2 или CH2NR2R3
-CN, -CHO, -OH, -CH2, -NH2 или CH2NR2R3
R' и R'' каждый обозначает H или CH3, тогда как, если Y OH, один из R' и R'' может также обозначать -OH
X обозначает -OH, -NR2R3 или -OR4,
R2 и R3 каждый означает алкильную, фенильную, фенилалкильную или алкилфенильную группу, имеющую до 10 атомов углерода в алкильной части, причем эти группы могут быть моно- или полизамещенными алкокси-, циано-, амино-, моно- или диалкиламино-, триалкиламмоний-, карбоксил-, сульфоновая кислота, ацетокси- или ацетаминогруппами, циклическую или бициклическую группу, имеющую 5 10 атомов углерода, в которой одна или несколько CH- или CH2-групп замещены N или NH, N или NH и S, N или NH и O, или сульфиносульфид, имеющий структуру
(CH2)n-SO2 - (CH2)n-S-(CH2)nOH,
где
n 2 6, и один из R2 и R3 может тоже обозначать H, причем R2 и R3 расположены друг к другу таким образом, чтобы обе части молекулы либо содержат кислотные или основные группы, либо одна из двух частей является нейтральной,
n обозначает 2 100, и
R4 обозначает алкильную, фенильную, фенилалкильную или алкилфенильную группу, имеющую до 10 атомов углерода в алкильной части, причем эти группы могут также быть моно- или полизамещены алкокси-, циано-, карбоксильной, сульфоновой кислотой или ацетоксигруппами.
Предпочтительно, когда в формуле I Y обозначает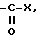
где
X OH или -OR4, причем R4 имеет значение, определенное выше.
Далее предпочтительны соединения, когда X обозначает - NR2R3, где R2 и R3 каждый обозначает алкил, алкоксиалкил, цианоалкил, аминоалкил, моно- или диалкиламиноалкил, триалкиламмонийалкил, карбоксиалкил, сульфоалкил, имеющие до 10 атомов углерода в алкильной части, фенил, который является незамещенным или моно- или полизамещенным алкилом, алкоксигруппой, алкоксиалкилом, цианогруппой, цианоалкилом, аминоалкилом, амино-, моно- или диалкиламиногруппой, моно- или диалкиламиноалкилом, триалкиламмонием, триалкиламмонийалкилом, карбоксигруппой, карбоксиалкилом, сульфоновой кислотой, сульфоалкилом, ацетокси- или ацетаминогруппой (группами), имеющими до 10 атомов углерода в алкильной части, циклическую или бициклическую группу, имеющую 5 10 атомов углерода, в которой одна или несколько CH- или CH2-групп замещены N или NH, N или NH и S, или N или NH и O,
или сульфонсульфид, имеющий структуру
-(CH2)n SO2 (CH2)n S - (CH2)nOH,
где
n 2 6, и один из R2 и R3 может также обозначать H, причем R2 и R3 приспособлены друг к другу таким образом, что обе части молекулы либо содержат кислотные или основные группы, либо одна из двух частей является нейтральной.
Наиболее предпочтительны соединения, когда Y обозначает - CH2NH2 или -CH2NR2R3, где
R2 и R3 каждый означает алкильную, фенильную, фенилалкильную или алкилфенильную группу, имеющую до 10 атомов углерода в алкильной части, причем эти группы могут быть моно- или полизамещенными алкокси-, циано-, амино-, моно- или диалкиламино-, триалкиламмоний-, карбоксил-, сульфоновая кислота, ацетокси- или ацетаминогруппами, циклическую или бициклическую группу, имеющую 5 10 атомов углерода, в которой одна или несколько CH- или CH2-групп замещены N или NH, N или NH и S, N или NH и O, или сульфиносульфид, имеющий структуру
(CH2)n SO2 (CH2)n S - (CH2)nOH,
где
n 2 6, и один из R2 и R3 может тоже обозначать H, причем R2 и R3 расположены друг к другу таким образом, чтобы обе части молекулы либо содержат кислотные или основные группы, либо одна из двух частей является нейтральной,
n обозначает 2 100.
Также предпочтительны повторяющиеся единицы, представленные формулой I, в которых Y обозначает -CN, -CHO или OH.
Было показано, что очистку фактора VIII в способе настоящего изобретения предпочтительно проводить путем промывания и элюирования буферами, имеющими последовательно увеличивающуюся ионную силу, которую корректируют при помощи солей четвертичного аммония, имеющих, по меньшей мере, одну углеводородную цепь из 1 6 атомов углерода и несущих гидрофильный заместитель, или при помощи таких солей в сочетании с поваренной солью.
При этом наиболее предпочтительно, когда соль четвертичного аммония представляет собой холинхлорид, а солевой градиент, получаемый с применением буферных систем, равен 0,1 1М в виде общих концентраций хлорида натрия и/или соли четвертичного аммония, определенного выше.
При помощи способа согласно изобретения достигается выделение фактора VIII с высоким выходом и высокой стабильностью продукта. Предпочтительно, чтобы в способе, проводимом в соответствии с данным изобретением, не был удален так называемый фактор фон Виллебранда, который должен оставаться во фракциях фактора VIII. Поэтому препараты фактора VIII можно применять также для больных, страдающих от недостаточности фактора фон Виллебранда. Кроме того, фактор VIII можно также применять в способах непрерывного вливания благодаря присутствию фактора фон Виллебранда, который облегчает природную стабилизацию фактора VIII.
Далее способ иллюстрируется при помощи следующих примеров.
Пример 1
Накопление фактора VIII из криопреципитата
Коммерчески доступный криопреципитат делят на кусочки размером 1 2 см и оттаивают при комнатной температуре в течение 3 4 часов. Эти кусочки суспендируют при перемешивании в приблизительно двойном объеме воды, содержащей 2 Е/мл Na-гепарина при температурах 20 25oC, pH суспензии доводят до 7,0 7,1 0,1М уксусной кислотой. Перемешивание продолжают при 20 - 25oC в течение 30 минут. На 1 кг криопреципитата добавляют 108 г 2%-ной суспензии гидроксида алюминия, и смесь перемешивают при комнатной температуре в течение 5 минут. Затем 0,1 М. уксусной кислотой доводят величину pH до 6,5 - 6,6. Пробу охлаждают до 16 14oC, центрифугируют в центрифуге Sharples AS-16 (Cepa 61) при скорости 1,0 L/минут. Супернатант фильтруют через фильтр Pall AB-1 U010ZP.
Пример 2
Приготовление хроматографической колонки
Для разделения экстрагированного криопреципитата применяют не менее 0,5 л ионообменной смолы на 1 кг криопреципитата. Высота колонки должна быть ≅ диаметра. После наполнения колонки смолой колонку сначала промывают 5 объемами раствора 0,1 М хлорида натрия. После этого ее промывают буфером A, имеющим следующий состав:
120 мМ хлорида натрия,
10 мМ цитрата натрия • 5 H2O,
120 мМ глицина,
1 мМ хлорида кальция • 2 H2O,
величину pH доводят 1 М HCl до 6,5-7,0.
Все буферы не должны содержать вирусов, так как последующие операции проводят с безвирусными экстрактами криопреципитата.
Пример 3
Пробу вносят в колонку и измеряют поглощение вытекающего из нее раствора при длине волны 280 нм. Фильтрат собирают и испытывают на активность фактора VIII, так как и продукт перед его внесением в колонку. Затем колонку промывают буфетом A до тех пор, пока поглощение вновь не достигнем его исходной величины. Затем колонку промывают буфером B, пока поглощение опять не вернется к базовой линии.
Буфер B имеет следующий состав:
180-200 мМ хлорида натрия,
10 мМ цитрата натрия • 5 H2O,
120 мМ глицина,
1 мМ хлорида кальция • 2 H2O,
pH 6,9-7,0.
Элюирование продукта проводили при помощи буфера C. Белковую фракцию, появляющуюся после добавления буфера C, собирали.
Буфер C имеет следующий состав:
400 мМ хлорида натрия,
1 мМ цитрата натрия • 5 H2O,
120 мМ глицина,
1 мМ хлорида кальция • 2 H2O,
pH 6,9-7,0.
После элюирования целевого продукта колонку промывали 5 объемами буфера D, который содержит 1 М раствора хлорида натрия.
Колонку регенерировали промыванием ее 0,1 N NaOH (3 объема колонки) с последующим промыванием 0,1N соляной кислоты (3 объема колонки) и промыванием колонки 5 объемами 25%-ного спирта в воде.
Пример 4
Собранные фракции разбавляли буфером E, состоящим из:
20 мМ цитрата натрия,
80 мМ глицина,
2,5 мМ хлорида кальция • 2 H2O,
pH 6,9-7,1, до тех пор, пока не была достигнута активность 26 или 35 E/мл. После этого доводили pH, если требовалось, до 6,9-7,1 и фильтровали через 0,45 мкм фильтр Sealklean. Впоследствии проводили стерильное фильтрование.
Пример 5
Если в качестве источника фактора VIII используют плазму человека, то применяют следующую процедуру:
Свежую или глубокозамороженную плазму человека доводят до температуры 20oC, иногда с использованием водяной бани. Плазму разбавляют 50% по объему воды и затем фильтруют. Фильтрат плазмы вносят в ионообменную колонку, содержащую EMD IMAE Fractogel (М) 650, уравновешенную предварительно буфером следующего состава:
50 мМ хлорида натрия,
10 мМ цитрата натрия,
120 мМ глицина,
1000 E/л гепарина,
pH 6,5-6,9.
После нанесения пробы, ионообменную смолу промывают несколько раз промывным буфером. Затем концентрацию поваренной соли увеличивают, промывая колонку сначала буфером, содержащим 100 мМ хлорида натрия, затем буфером, содержащим 160 мМ хлорида натрия, и после этого буфером, содержащим 200 мМ хлорида натрия. Фракции, содержащие фактор VIII, собирают и стабилизируют добавлением 1,0 мг/мл сывороточного альбумина человека. Полученный продукт обрабатывают далее так же, как в примерах 2-4, за исключением того, что коммерчески доступный криопреципитата здесь заменен полученными при помощи колонки фракциями.
Пример 6 Сравнительный эксперимент
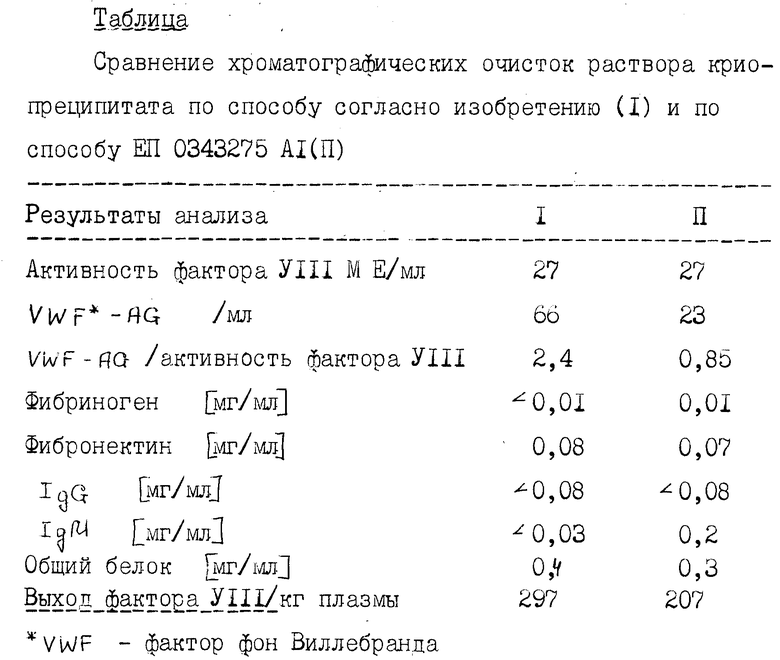
В каждом из двух опытом обрабатывали 0,3 кг криопреципитата, полученного из одной и той же плазмы. Одну процедуру проводили в соответствии с данным изобретением, а другую в соответствии со способом ЕП 0343275 AI. Фракции подвергали анализу и результаты, относящиеся к этим двум опытам, представлены в следующей таблице.
Работа по способу в соответствии с ЕП 03443275 AI приводит к получению только 23 фракций, каждая из которых содержит 270 М E фактора VIII, что соответствует выходу 20700 М E фактора VIII на 1 кг криопреципитата или 207 М E на 1 кг плазмы. Отсюда можно сделать вывод о преимуществе работы по способу согласно изобретению, который дает выход почти на 51% выше выхода, полученного при применении способа ЕП 0343275 AI.
Нежелательные белки, также как фибриноген и иммуноглобулин М (IgM), более эффективно удаляются в способе, соответствующем данному изобретению.
| название | год | авторы | номер документа |
|---|---|---|---|
| ОЧИСТКА И ПРИМЕНЕНИЕ ФАКТОРА, СПОСОБСТВУЮЩЕГО ЗАЖИВЛЕНИЮ РАН | 2007 |
|
RU2520817C2 |
| СПОСОБ ПОЛУЧЕНИЯ С ПОМОЩЬЮ ХРОМАТОГРАФИЧЕСКИХ МЕТОДОВ ВИРУСНО-ИНАКТИВИРОВАННОЙ ФРАКЦИИ, СОДЕРЖАЩЕЙ ФАКТОР VIII | 1994 |
|
RU2148411C1 |
| СПОСОБ ОЧИСТКИ ВИТАМИН К-ЗАВИСИМЫХ БЕЛКОВ, ТАКИХ КАК КОАГУЛЯЦИОННЫЙ ФАКТОР VII | 2011 |
|
RU2731720C2 |
| СПОСОБ ОЧИСТКИ ВИТАМИН К-ЗАВИСИМЫХ БЕЛКОВ, ТАКИХ КАК КОАГУЛЯЦИОННЫЙ ФАКТОР IX | 2011 |
|
RU2590726C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФИБРИНОГЕНА С ИСПОЛЬЗОВАНИЕМ СИЛЬНОЙ АНИОНООБМЕННОЙ СМОЛЫ И СОДЕРЖАЩИЙ ФИБРИНОГЕН ПРОДУКТ | 2011 |
|
RU2603103C2 |
| СПОСОБ ВЫДЕЛЕНИЯ И ОЧИСТКИ ЦЕЛЕВОГО БЕЛКА БЕЗ ПРИМЕСИ ПРИОНОВОГО БЕЛКА PrP | 2008 |
|
RU2491292C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА ФАКТОРА VIII | 2004 |
|
RU2253475C1 |
| Способ разделения белков крови | 1990 |
|
SU1837880A3 |
| КОНЪЮГИРОВАННЫЕ БЕЛКИ С ПРОЛОНГИРОВАННЫМ ДЕЙСТВИЕМ IN VIVO | 2009 |
|
RU2526804C2 |
| НОВЫЕ ЗАЩИТНЫЕ КОМПОЗИЦИИ ДЛЯ РЕКОМБИНАНТНОГО ФАКТОРА VIII | 2009 |
|
RU2510279C2 |
Назначение: изобретение относится к области высокоочищенного комплекса фактора VIII/фактора Виллебранда из плазмы крови или криопреципитата. Сущность изобретения: комплекс фактора VIII/фактора Виллебранда выделяют посредством анионообменной хроматографии. В качестве анионообменного материала используют материал на основе содержащих гидроксигрупп носителей, поверхности которых покрыты ковалентно связанными полимерами. 7 з.п.ф-лы, 1 табл.
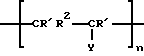
в которой R' H или CH3;
Y 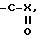 -CN, -CHO, -CH, -CH2 NH2 или CH2NR2R3;
-CN, -CHO, -CH, -CH2 NH2 или CH2NR2R3;
R' и R2 каждый H или CH3, тогда как, если Y OH, один из R' и R2 может также обозначать OH
X обозначает OH, -NR2R3 или -OR4;
R2 и R3 каждый означает алкильную, фенильную, фенилалкильную или алкилфенильную группу, имеющую до 10 атомов углерода в алкильной части, причем эти группы могут быть моно- или полизамещенными алкокси-, циано-, амино-, моно- или диалкиламино-, триалкиламмоний-, карбосил-, сульфоновая кислота, ацетокси- или ацетаминогруппами, циклическую или бициклическую группу, имеющую 5 10 атомов углерода, в которой одна или несколько CH- или CH2 групп замещены N или NH, N или NH и S,N или NH и O, или сульфиносульфид, имеющий структуру
-(CH2)n-SO2-(CH2)n-S- (CH2)nOH,
где n 2 6,
и один из R2 и R3 может также обозначать H, причем R2 и R3 расположены друг к другу таким образом, что обе части молекулы либо содержат кислотные или основные группы либо одна из двух частей является нейтральной;
n 2 100, и R4 обозначает алкильную, фенильную, фенилалкильную или алкилфенильную группу, имеющую до 10 атомов углерода в алкильной части, причем эти группы могут также быть моно- или полизамещены алкокси-, циано-, карбоксильной, сульфоновой кислотой или ацетоксигруппами.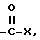
где X -OH или -OR4, где R4 определено в п.1.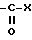
с X -NR2R3,
где R2 и R3 каждый обозначает алкил, алкоксиалкил, цианоалкил, аминоалкил, моно- или диалкиламиноалкил, триалкиламмонийалкил, карбоксиалкил, сульфоалкил, имеющие до 10 атомов углерода в алкильной части, фенил, который является незамещенным или моно- или полизамещенным алкилом, алкоксигруппой, алкоксиалкилом, цианогруппой, цианоалкилом, аминоалкилом, амино-, моно- или диалкиламиногруппой, моно- или диалкиламиноалкилом, триалкиламмонием, триалкиламмонийалкилом, карбоксигруппой, карбоксиалкилом, сульфогруппой, сульфоалкилом, ацетокси- или ацетаминогруппой (группами), имеющими до 10 атомов углерода в алкильной части, циклическую или бициклическую группу, имеющую 5 10 атомов углерода, в которой одна или несколько CH- или CH2-групп замещены N или NH, N или NH и S, или N или NH и O,
или сульфонсульфид, имеющий структуру
-(CH2)n-SO2-(CH2)n-S-(CH2)nOH,
где n 2 6, и один из R2 и R3 может также обозначать H,
причем R2 и R3 приспособлены друг к другу таким образом, что обе части молекулы либо содержат кислотные или основные группы, либо одна из двух частей является нейтральной.
| EP, заявка, 0209041, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1997-11-20—Публикация
1993-01-20—Подача