Изобретение касается новых металлоценов с бензоконденсированными производными инденила в качестве лигандов, которые могут применять предпочтительно в качестве компонентов катализатора при получении полиолефинов с высокой изотактичностью, плотным распределением молекулярной массы и высокой молекулярной массой.
Полиолефины о высокой молекулярной массой имеют значение, в частности, для изготовления пленок, пластин или крупных полых предметов, таких, как, например, труб или пресс-изделий.
Из литературы известно получение полиолефинов с применением растворимых соединений металлоцена в сочетании с алюминоксанами или другими сокатализаторами, которые могут на основании своей кислотности по Льюису превращать нейтральный металлоцен в катион и стабилизировать.
В качестве примера был предложен специальный метод предварительной активации металлоцена алюминоксаном, который ведет к значительному повышению активности катализаторной системы и четкому улучшению структуры гранул полимера (патент ФРГ N 3726067). Предварительная активация хотя и повышает молекулярную массу, однако значительное повышение не достигается.
Следующее, но еще не достаточное повышение молекулярной массы достигали путем применения, в частности, металлоцена с мостичной связью гетероатома при высокой активности металлоцена (выложенная заявка на европейский патент N 0336128).
Наряду о этим известны катализаторы на основе этиленбизинденилгафний-дихлорида и этилен-до(4,5,6,7-тетрагидро-1-инденил)гафнийдихлорида и метилалюминоксана, с которыми путем суспензионной полимеризации могут быть получены высокомолекулярные полипропилены (J.A. Ewen et al. J. Am. Chem. Soc. 109 (1987), 6544). Несмотря на соблюдение технически важных условий полимеризации, структура гранул получаемых таким образом полимеров неудовлетворительна и активность использованных катализаторов сравнительно мала. В связи с высокой стоимостью катализатора полимеризация с этими системами невозможна.
Заметное повышение молекулярной массы может быть достигнуто путем применения металлоценов, в которых ароматические П-лиганды, фиксированные мостиком, во 2-м положении (патент ФРГ N 4035886.0) или во 2-м и 4-м положении (патент ФРГ N 4128238.8) имеют заместители.
При промышленном производстве, выгодном экономически, необходимо осуществлять полимеризацию по возможности при высоких реакционных температурах, так как при повышенных температурах полимеризации выделяющуюся теплоту полимеризации можно отвести с незначительным количеством охлаждающей среды и поэтому заметно пониженной циркуляцией.
В этом отношении указанные металлоцены с заместителями во 2-м или 2-м и 4-м положениях по отношению к мостику при температуре полимеризации 70oC являются уже очень продуктивными, однако при этом требуемые молекулярные массы при технически соответствующей температуре полимеризации (например, 70oC) являются еще очень незначительными для технического использования, как, например, при изготовлении полимеров для труб и крупных полых предметов, а также специальных волокон.
Задача состояла в том, чтобы найти способ или катализаторную систему для производства полимеров с хорошим строением гранул и высокой молекулярной массой и большим выходом продукции. Путем использования водорода в качестве регулятора молекулярной массы весь интервал молекулярной массы может быть покрыт только одним металлоценом.
Неожиданно было обнаружено, что металлоцены со специальными производными инденила в качестве лигандов являются прекрасными катализаторами (компоненты катализатора) при производстве, в частности, изотактических полиолефинов с высокой молекулярной массой.
Исходя из этого предметом изобретения являются соединения нижеследующей формулы I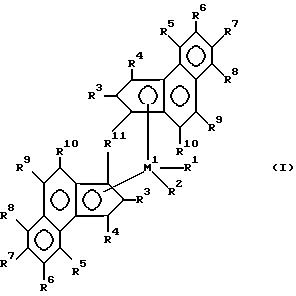
где M1 обозначает металл группы IVb, Vb или VIb периодической системы,
R1 и R2 являются одинаковыми или различными и означают атом водорода, C1-C10-алкилгруппу, C1-C10-алкоксигруппу, C6-C10-арилгруппу, C6-C10-арилоксигруппу, C7-C40-арилалкилгруппу, C7-C40-алкиларилгруппу, C8-C40-арилалкенилгруппу, группу ОН или атом галогена.
Радикалы R3 являются одинаковыми или различными и обозначают атом водорода, атом галогена, C1-C10-алкилгруппу, которая может быть галогенирована, C6-C10-арилгруппу, радикал -NR2, -SR, -OSiR3, -SiR3 или PR2-, где R является атомом галогена, C1-C10-алкилгруппой или C6-C10-арилгруппой, R4 R10 имеют значения, указанные для R3, или смежные радикалы R4 R10 с соединяющими их атомами образуют ароматическое или алифатическое кольцо.
R11 является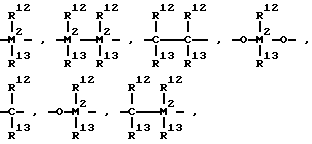 BR12,AlR12, -Ge-, -Sn-, -O-, -S-,SO,NR12,CO,PR12 илиP(O)R12,
BR12,AlR12, -Ge-, -Sn-, -O-, -S-,SO,NR12,CO,PR12 илиP(O)R12,
причем R12 и R13 являются равными или различными и обозначают атом водорода, атом галогена, C1-C10-алкилгруппу, C1-C10-фторалкилгруппу, C6-C10-арилгруппу, C6-C10-фторарилгруппу, C1-C10-алкоксигруппу, C2-C10-алкенилгруппу, C7-C40-арилалкилгруппу, C8-C40-арилалкенилгруппу, C7-C40-алкиларилгруппу или R12 и R13 в каждом отдельном случае образуют кольцо с соединяющими их атомами и M2 является кремнием, германием или оловом.
Алкил представляет собой разветвленный или неразветвленный алкил, галоген (галогенированный) обозначает фтор, хлор, бром или йод, предпочтительно фтор или хлор.
Заместители R4 R10 в обоих инденил-лигандах могут быть различными, несмотря на одинаковое обозначение (ср. определение R3).
В формуле I M1 является металлом группы IVb, Vb или VIb периодической системы, например титаном, цирконом, гафнием, ванадием, ниобием, танталом, хромом, молибденом, вольфрамом, предпочтительно цирконом, гафнием и титаном.
R1 и R2 являются одинаковыми или различными и обозначают атом водорода, C1-C10, предпочтительно C1-C3-алкилгруппу, C1-C10-, предпочтительно C1-C3-алкоксигруппу, C6-C10-, предпочтительно C6-C8-арилгруппу, C6-C10-, предпочтительно C6-C8-арилоксигруппу, C2-C10-, предпочтительно C2-C4-алкенилгруппу, C7-C40-, предпочтительно C7-C10-арилалкилгруппу, C7-C40-, предпочтительно C7-C12-алкиларилгруппу, C8-C40, предпочтительно C8-C12-арилалкенилгруппу или атом галогена, предпочтительно хлор.
Радикалы R3 R10 являются одинаковыми или различными и обозначают атом водорода, атом галогена, предпочтительно атом фтора, хлора или брома, C1-C10-, предпочтительно C1-C4-алкилгруппу, которая может быть галогенирована, C6-C10-, предпочтительно C6-C8-арилгруппу, остаток -NR2, -SR, -OSiR3, -SiR3 или -PR2, где R является атомом галогена, предпочтительно атомом хлора, или C1-C10-, предпочтительно атомом хлора, или C1-C10-, предпочтительно C1-C3-арилгруппой или C6-C10, предпочтительно C6-C8-арилгруппой.
R11 является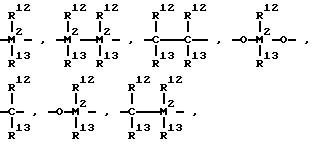 BR12,AlR12, -Ge-, -Sn-, -O-, -S-,SO,SO2,NR12,CO,PR12 илиP(0)R12,
BR12,AlR12, -Ge-, -Sn-, -O-, -S-,SO,SO2,NR12,CO,PR12 илиP(0)R12,
причем R12 и R13 являются одинаковыми или различными и обозначают атом водорода, атом галогена, C1-C10-, предпочтительно C1-C4-алкилгруппу, в частности метил-группу, C1-C10-фторалкилгруппу, предпочтительно CF3-группу, C6-C10-, предпочтительно, C6-C8-алкилгруппу, C6-C10-фторарилгруппу, предпочтительно, C1-C4-алкоксигруппу, в частности, метоксигруппу, C2-C10-, предпочтительно пентафторфенилгруппу, C1-C10, предпочтительно C1-C4-алкоксигруппу, в частности метоксигруппу, C2-C10-, предпочтительно C2-C4-алкенилгруппу, C7-C40-, предпочтительно C7-C10-арилалкилгруппу, C8-C40-предпочтительно C8-C12-арилалкенилгруппу, или C7-C40-, предпочтительно C7-C12-алкиларилгруппу или R12 и R13 образуют соответственно кольцо вместе с соединяющими их атомами.
M2 представляет собой кремний, германий или олово, предпочтительно, кремний и германий.
Для соединений формулы I предпочтительно, что M1 представляет собой цирконий или гафний, R1 и R2 являются одинаковыми и обозначают C1-C3-алкилгруппу или атом галогена. Радикалы R3 одинаковы и обозначают C1-C4-алкилгруппу. R4 - R10 являются одинаковыми или различными и обозначают водород или C1-C4-алкилгруппу и R11 является
причем M2 обозначает кремний и R12 и R13 являются одинаковыми иди различными и обозначают C1-C4-алкилгруппу или C6-C10-арилгруппу.
Кроме того, предпочтительными являются соединения I, в которых радикалы R4 и R10 обозначают водород и R5-R9 обозначают C1-C4-алкилгруппу или водород.
В частности, это относится к случаю, когда M1 представляет собой цирконий, R1 и R2 являются одинаковыми и обозначают хлор, радикалы R3 являются одинаковыми и обозначают C1-C4-алкилгруппу, R4 и R10 обозначают водород, R5 R9 одинаковы или различны и обозначают C1-C4-алкилгруппу группу или водород и R11 является
причем M2 кремний и R12 и R13 одинаковы или различны и обозначают C1-C4-алкилгруппу или C6-C10-арилгруппу.
Особенно предпочтительно соединения формулы I, где M1 является цирконием, R1 и R2 обозначают хлор, R3 является метилом, R4 R10 обозначают водород и R11 является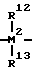
причем M2 кремний и R12 и R13 одинаковы или различны и обозначают метил или фенил; в частности, соединения I, указанные в примерах выполнения.
Предметом изобретения является также получение соединения формулы I, отличающийся тем, что соединение формулы IV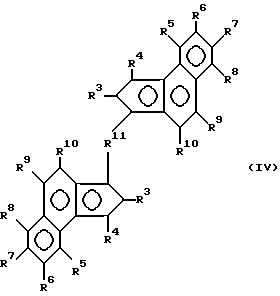
причем радикалы R3 R11 имеют значения, указанные в формуле I, и M3 обозначает щелочной металл, предпочтительно литий, превращают с соединением формулы V
M1X4, (V)
где M1 имеет значение, названное в формуле I, и X обозначает атом галогена, предпочтительно хлора; полученный продукт переводят в необходимое производное.
Получение металлоценов осуществляется по известному из литературы способу и изображено в следующей реакционной схеме (ср. далее примеры выполнения).

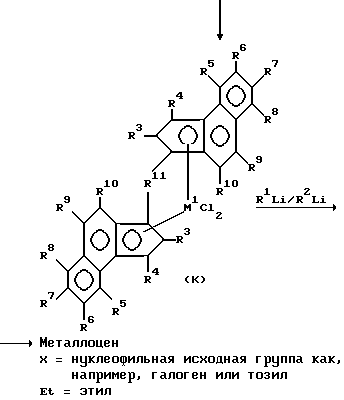
Производные нафталина формулы A имеются в продаже или могут быть получены известными из литературы методами ("Friedel Crafts and Related reactions", Wiley, New York, 1964, Vol. 11, p.659-766, Bull. Soc. Chim. Belges, 58 (1949) 87, J. Amer. Chem. Soc. 89 (1967) 2411).
Превращение в соединения формулы C осуществляется по известным из литературы методам путем реакции с замещенными радикалами малоновой кислоты формулы B в основных условиях, как например, в растворах этанола этанолата натрия (J. Org. Chem. 23 (1958) 1441, J. Amer. Chem. Soc. 70 (1948) 3569).
Соединения формулы C омыливаютоя гидроокисями щелочного металла, такими, как, например, гидроокись калия или гидроокись натрия по известным из литературы методам и путем термолиза полученной дикарбоновой кислоты по известным из литературы методам декарбоксилируются в соединения формулы D (J. Org. Chem. 23 (1958) 1441, J. Am. Chem. Soc. 70 (1948) 3569).
Замыкание кольца в замещенные бензоинданоны формулы E осуществляется по известным из литературы методам путем превращения хлорирующими реагентами, такими, как, например, SOCl2, в соответствующие хлорангидриды кислоты и последующей циклизации на катализаторе Фриделя-Крафтса в инертном растворителе, например AlCl3, или полифосфорной кислотой в хлористом метилене или CS2 (Organometallics 9 (1990) 3098, Bull. Soc. Chim. Fr. 3 (1967) 988, J. Org. Chem. 49 (1984) 4226).
Превращение в бензоинденовые производные формулы осуществляется по известным из литературы методам путем восстановления боргидридом натрия или алюмогидридом лития в инертном растворителе, таком, как, например, простой диэтиловый эфир или тетрагидрофуран, или путем алкилирования алкилирующими средствами формулы F или литийалкилами в соответствующие спирты и дегидратации спирта в кислых условиях, как, например, p-толуолсульфокислотой или щавелевой кислотой или путем превращения с обезвоживающими веществами, как, например, сульфат магнезия или молекулярное сито (Organometallics 9 (1990) 3098, Acta. Chem. Scand. B 30 (1976) 527, J. Amer. Chem. Soc. 65 (1943) 567).
Бензоинденовые производные формулы G могут быть синтезированы также по другому, не указанному здесь подробно пути синтеза, исходя из замещенного нафталина в 4 этапах синтеза (Bull. Soc. Chem. Fr. 3 (1967) 988).
Получение лигандных систем формулы J и превращение в хиральные металлоцены с мостичной связью формулы K, а также выделение требуемой рацемической формы в принципе известно (выложенная заявка Австралии, N 31478/89, J. Organomet. Chem. 342 (1988) 21, европейский патент N 0284707, европейский патент N 0320762). К тому же производное бензоиндена формулы G депротонируется сильным основанием, таким, как, например, бутиллитием, в инертном растворителе и превращается реагентом формулы H в лигандную систему формулы J. Затем его депротонируют двумя эквивалентами сильного основания, такого, как, например, бутиллитий, в инертном растворителе (соединение формулы IV) и превращают с соответствующим металлтетрагалогенидом, например тетрахлоридом циркония в соответствующем растворителе. Соответствующими растворителями являются алифатические и ароматические растворители, например гексан или толуол, эфирные растворители, например тетрагидрофуран или простой диэтиловый эфир или галогенированные углеводороды, например хлорид метилена. Разделение рацемической и мезоформы осуществляется путем экстракции или перекристаллизации соответствующими растворителями.
Превращение в металлоцены формулы I может осуществляться по известным из литературы методом, например путем превращения с алкилирующими средствами, например метиллитием (Organometallics 9 (1990) 1539, J. Amer. Chem. Soc. 95 (1973) 6263, европейский патент N 0277004).
Предложенные по изобретению металлоцены I являются высокоактивными компонентами катализатора для полимеризации олефинов.
Таким образом, изобретение включает также способ получения олефинового полимера путем полимеризации или сополимеризации олефина формулы Ra-CH=CH-Rb, где Ra и Rb являются одинаковыми или различными и обозначают атом водорода или радикал углеводорода с 1 14 атомами углерода, или Ra и Rb могут образовать кольцо со связующими их атомами, при температуре -60 200oC, при давлении 0,5 100 бар, в растворе, суспензии или в газовой фазе, в присутствии катализатора, который образуется из металлоцена в виде соединения переходного металла и сокатализатора, отличающийся тем, что металлоцен является соединением формулы I.
Хиральные металлоцены применяются предпочтительно в качестве рацемата. Но может быть использована также чистая R- или S- форма; эти чистые стереоизомерные формы могут обеспечить получение оптически активного полимера. Однако должна быть отделена мезоформа металлоценов, так как активный полимеризационный центр (атом металла) в этих соединениях из-за зеркальной симметрии на центральном металле не является больше хиральным и поэтому не может позволить получить высокоизотактический полимер. Если мезоформа не отделена, то наряду с изотактическими полимерами образуется также атактический полимер. Для определенного применения, например для мягких формованных изделий, это может быть вполне приемлемо.
Разделение стереоизомеров в принципе известно.
Согласно изобретению, в качестве сокатализатора используется предпочтительно алюминоксан формулы (II)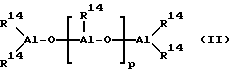
для линейного типа и/или формулы (III)
для циклического типа, причем в формулах (II) и (III) радикалы R14 могут быть одинаковыми или различными и обозначают C1-C6-алкилгруппу, C6-C18-арилгруппу, бензил или водород, и p обозначает целое число от 2 до 50, предпочтительно от 10 до 35.
Радикалы R14 предпочтительно являются одинаковыми и обозначают метил, изобутил, фенил или бензил, особенно предпочтительно, метил.
Если радикалы R14 различны, то это предпочтительно метил и водород или альтернативно метил и изобутил, причем водород или изобутил, предпочтительно содержатся в количестве 0,01 40% (количество радикалов R14).
Алюминоксан может быть подучен в различных видах известными способами. Один из методов, например, заключается в том, что соединение алюминийуглеводород и/или соединение гидридоалюминийуглеводорода с водой (газообразное, твердое, жидкое или связанное, например, в виде кристаллизационной воды) превращают в инертном растворителе (например, толуол). Для получения алюминоксана с различными алкильными группами R14 два различных триалкилалюминия (AlR3 + AlR'3) в соответствии с требуемым составом превращают с водой (сравни S. Pasynkiewicz, Polyhedron 9 (1990) 429 и выложенная заявка на европейский патент N 302424).
Точная структура алюминоксанов II и III неизвестна.
Независимо от способа получения общим для всех алюминоксановых растворов является меняющееся содержание непревращенного исходного соединения алюминия, которое находится в свободной форме или в виде продукта присоединения.
Является возможным перед введением в реакцию полимеризации предварительно активировать металлоцен алюминоксаном формулы (II) и/или (III). Благодаря этому активность полимеризации заметно повышается и улучшается структура кристалла.
Предварительное активирование соединения переходного металла проводится в растворе. При этом предпочтительно металлоцен в растворе алюминоксана растворяют в инертном углеводороде. В качестве углеводорода подходит алифатический или ароматический углеводород. Предпочтительно применяется толуол.
Концентрация алюминоксана в растворе находится в диапазоне от примерно 1 мас. до границы насыщения, предпочтительно от 5 до 30 мас. в каждом отдельном случае относительно общего раствора. Металлоцен может применяться в той же концентрации, предпочтительно все же в количестве от 10-1 до 1 моль на моль алюминоксана. Время предварительного активирования достигает от 5 мин до 60 ч, предпочтительно 5-60 мин. Работают при температуре -78oC - 100oC, предпочтительно 0 70oC.
Металлоцен можно также предварительно полимеризовать или нанести на носитель. Для предварительной полимеризации применяют предпочтительно олефин (или один из олефинов), использованный в полимеризации.
Подходящими носителями являются, например, силикагели, оксиды алюминия, твердый алюминоксан или другие неорганические материалы-носители. Подходящим материалом-носителем является также полиолефиновый порошок тонкого помола.
Согласно изобретению, вместо или наряду с алюминоксаном могут применяться соединения формул RxNH4-xBR'4, RxPH4-xBR'4, R3CBR'3 или BR'3 в качестве соответствующих сокатализаторов. В этих формулах x обозначает число от 1 до 4, предпочтительно 3, радикалы R являются одинаковыми или различными, предпочтительно одинаковыми и обозначают C1-C10-алкил, C6-C18-арил или 2 радикалы R образуют вместе со связующим их атомом кольцо, и радикалы R' являются одинаковыми или различными, предпочтительно одинаковыми и обозначают C6-C18-арил, который может быть заменен алкилом, галоалкилом или фтором.
В частности, R обозначает этил, пропил, бутил иди фенил и R' обозначает фенил, пентафторфенил, 3,5-бистрифтормелфенил, мезитил, хилил или толил (см. выложенную заявку на европейский патент N 277003, выложенную заявку на европейский патент N 277004 и выложенную заявку на европейский патент N 426638).
При использовании вышеуказанных сокатализаторов настоящий (активный) катализатор полимеризации состоит из продукта реакции металлоцена и одного из указанных соединений. Поэтому сначала этот продукт реакции получают предпочтительно вне полимеризационного реактора на отдельном этапе при использовании соответствующего растворителя.
Принципиально в качестве сокатализатора, согласно изобретению, подходит любое соединение, которое на основании своей кислотности по Льюису может перевести нейтральный металлоцен в катион и стабилизировать его ("неустойчивая координация"). Кроме того, сокатализатор или образованный из него анион не должны вступать в другие реакции с образованным катионом металлоцена (ср. выложенная заявка на европейский патент N 427697).
Для удаления имеющегося в олефине катализаторного яда предпочтительна очистка алюминийалкилом, например AlMe3 или AlEt. Очистка может осуществляться самостоятельно в полимеризационной системе, или олефин перед подачей в полимеризационную систему приводят в контакт с соединением алюминия и затем снова отделяют.
Полимеризация или сополимеризация проводится известным способом в растворе, в суспензии или в газовой фазе, непрерывно или периодически, на одной стадии иди многоступенчато при температуре -60 200oC, предпочтительно 30-80oC, особенно предпочтительно 50-80oC, полимеризируются или сополимеризируются олефины формулы Ra-CH=CH=Rb. В этой формуле Ra и Rb являются одинаковыми или различными и обозначают атом водорода или алкильный радикал с 1-14 атомами C. Однако Ra и Rb могут также образовать кольцо со связывающими их атомами C. Например, к таким олефинам относятся этилен, пропилен, 1-бутен, 1-гексен, 4-метил-1-пентен, 1-октен, норборнен или норбонадиен. Особенно часто полимеризуют пропилен и этилен.
В качестве регулятора молекулярной массы и/или для повышения активности подается в случае необходимости водород. Общее давление в полимеризационной системе достигает 0,5-100 бар. Предпочтительна полимеризация в особенно интересном в техническом плане диапазоне давления 5 64 бар.
При этом применяется металлоцен в концентрации, соответствующей концентрации переходного металла от 10-3 до 10-8, предпочтительно 10-4-10-7 моля переходного металла на 1 дм3 растворителя или на 1 дм3 объема реактора. Алюминоксан применяется в концентрации от 10-5 до 10-1 моля, предпочтительно 10-4-10-2 моля на 1 дм3 растворителя или на 1 дм3 объема реактора. Другие указанные сокатализаторы применяются примерно в эквимолярных количествах с металлоценом. Однако возможны также более высокие концентрации.
Если полимеризация проводится в суспензии или в растворе, то применяется инертный растворитель, употребимый при низком давлении. К примеру, применяют алифатический или циклоалифатический углеводород; в качестве такого может быть назван, например, пропан, бутан, пентан, гексан, гептан, изооктан, циклогексан, метилциклогексан.
Может быть использована также бензиновая или гидрированная дизельная нефтяная фракция. Можно употребить также толуол. Предпочтительно полимеризация осуществляется в жидких мономерах.
Если используются инертные растворители, то добавляются газообразные или жидкие мономеры.
Продолжительность полимеризации любая, так как используемая согласно изобретению катализаторная система показывает лишь незначительный, зависящий от времени спад полимеризационной активности.
Предложенный в изобретении способ отличается тем, что описанные металлоцены в технически особо интересном температурном диапазоне между 50 и 80oC дают возможность получать полимеры с высокой молярной массой, высокой стереоспецифичностью и хорошей кристаллической структурой.
В частности, предложенные в изобретении цирконоцены позволяют получать полимеры с высокой молекулярной массой или даже превосходят известные из уровня техники гафноцены. Однако они имеют недостаток, который заключается в незначительной полимеризационной активности и очень высокой стоимости катализатора, и полученные полимеры имеют плохую структуру порошка.
Синтез металлоценов I, использованных в примерах полимеризации.
Пример A. Синтез рац-диметилсиландиилбис(2-метил-4,5-бензоинденил)-циркондихлорида
1. Сложный диэтиловый эфир метил(2-нафтилметил)малоновой кислоты (1)
5,15 г (224 ммоль) натрия растворили в 150 мл абсолютного этанола при нагреве и при комнатной температуре смешали с 37,3 мл (217 ммоль) сложного диэтилового эфира метилмалоновой кислоты. При 0oC раствор из 50 г (217 ммоль) 2-бромметилнафталина (96%) медленно каплями добавляли в 270 мл этанола и нагревали еще 4-5 ч при кипении с обратным холодильником. Смесь выливали на ледяную воду и экстрагировали уксусным эфиром. Соединенные органические фазы высушивали сульфатом натрия и выпаривали. После сушки в вакууме масляного вакуум-насоса маслянистый остаток перемешивали с гексаном при 0oC, причем 55 г (81%) соединения I кристаллизовали.
2. 2-метил-3-нафтилпропионовая кислота (2)
33,2 г (105 ммоль) соединения I смешали в 70 мл этанола с раствором 23,7 г (422 ммоль) хлорида калия в 50 мл воды и нагревали 4 ч для обратного потока. После удаления растворителя твердый остаток соединили с уксусным эфиром, смешали с водой и соляной кислотой довели до pH 1. Водную фазу экстрагировали несколько раз уксусным эфиром. После сушки над сульфатом магния соединенные органические фазы полностью выпаривали. Остаток смешивали для кристаллизации с гексаном. Для декарбоксилирования оранжевое твердое вещество нагревали до 175oC до окончания выделения газа. Получили 21 г (93%) продукта 2 в виде оранжевого твердого вещества.
3. 2-метил-6,7-бензоиндан-1-он (3)
21 г (98 ммоль) соединения 2 смешивали при исключении влажности с 22 мл тионилхлорида и нагревали 30 мин при кипении с обратным холодильником. Затем отгоняли избыточный тионилхлорид. Остаток быстро освободили от летучих соединений в масляном вакуум-насосе и затем растворили в 25 мл метиленхлорида при Ar-защите. Раствор медленно по каплям вводили в суспензию 26 г (196 ммоль) хлорида алюминия в 60 мл метиленхлорида при комнатной температуре и нагревали еще 30 мин при кипении с обратным холодильником. Смесь выливали на лед и экстрагировали метиленхлоридом. Соединенные органические фазы сушили сульфатом натрия и выпаривали. Темный маслянистый остаток разделили на 600 г силикагеля 60 с помощью хроматографии. Смесью растворителя из гексан/уксусного эфира (9: 3) вымывалось 8,6 г (45%) соединения 3 (желтое твердое вещество).
4. 2-метил-4,5-бензоинден (4)
Раствор 7,8 г (39,7 ммоль) инданона3 в 400 мл смесь ТГФ/метанол (2:1) смешали порциями с 2,2 г (595 ммоль) натрийборгидрида и перемешивали 14 ч. Раствор наливали на HCl-кислый лед и экстрагировали. Соединенные органические фазы несколько раз промывали и высушивали сульфатом натрия. После удаления растворителя оставшееся масло оранжевого цвета растворяли в 240 мл толуола и нагревали с 570 мг (3,15 ммоль) p-толуолсульфокислота 15 80oC. Раствор несколько раз промывали водой при комнатной температуре, высушивали сульфатом натрия и выпаривали. Остаток разделили на 300 г силикагеля 60 посредством хроматографии. Смесью растворителя из гексан/простого диизопропилового эфира (20:1) смогли извлечь 4,7 г (65%) индена 4 (бесцветное масло).
1H-ЯМР-спектр (350 МГц, CDCl3): 8,02 (1, d), 7,84 (1, м), 7,59 (1, d), 7,52 (1, d), 7,38-7,48 (2, м), 7,06 (1, м), 3,42 (2, d), 2,25 (3, d).
5. Диметилбис(2-метил-4,5-бензоинденил)силан (5)
Раствор 4,6 г (25,5 толь) индена 4 в 50 мл ТГФ смешали с 10,2 мл (255 ммоль) 2,5М раствора бутиллития в гексане при комнатной температуре и нагревали 1 ч при кипении с обратным холодильником. Затем красный раствор добавляли по каплям к раствору 1,55 г (12 ммоль) диметилдихлорсилана в 10 мл тетрагидрофуран при комнатной температуре и нагревали 5-6 ч для кипения с обратным холодильником. Реакционный раствор поливали ледяной водой и несколько раз экстрагировали. Высушенные сульфатом натрия соединенные органические фазы выпаривали и высушивали в вакууме масляного вакуум-насоса. Остаток подвергали хроматографическому разделению в 300 г силикагеля 60. Смесью растворителя из гексана и 3% уксусного эфира сначала смогли извлечь 500 мг непревращенного эдукта 4. Затем таким же растворителем извлекали лигандную систему 5. После удаления растворителя можно было кристаллизовать лигандную систему путем перемешивания с гексаном (изомеры). Выход составил 1,7 г (34% или 44% относительно превращенного индена).
6. Рац-диметилсиландиилбис(2-метил-4,5-бензоинденил)циркондихлорид (6)
Раствор 1,7 г (4,1 ммоль) лигандной системы 5 в 20 мл тетрагидрофурана при комнатной температуре при Ar-защите смешали с 4,0 мл (10,2 ммоль) 2,5М раствора бутиллития и перемешивали 14 ч при комнатной температуре. Оставшийся после удаления растворителя остаток высушивали в масляном вакуум-насосе и промывали гексаном. Полученный таким образом светло-коричневый порошок высушивали несколько часов в вакууме масляного вакуум-насоса при температуре 40-50oC и при температуре -78oC ввели в суспензию 1,0 г (4,0 ммоль) тетрахлорида циркония в 25 мл хлористого метилена. После нагрева до комнатной температуры растворитель удаляли и остаток экстрагировали 20 мл толуола, чтобы удалить мезоформу цирконоцена 6. Затем остаток экстракта толуола экстрагировали 40 мл хлористого метилена. Раствор сконцентрировали до маленького объема и при температуре -35oC кристаллизовали. Из нескольких фракций смогли выделить всего 970 мг (42%) цирконоцена 6 в виде чистого рацемата.
1H-ЯМР-спектр рацемата (300 МГц, CDCl3): 7,86 (2, м), 27,78 (2, м), 7,60 (2, d), 7,48-7,56 (4, м), 7,36 (2, d), 7,27 (2, Sβ-IHd-CH3), 2,37 (6, S, Ind-CH3), 1,36 (6, S, Si-CH3). Спектр массы: 574 M+, правильный распад, правильная модель изотопов.
Пример B. Синтез рац-диметилсиландиил бис(2-метил-a-аценафтин-динил)циркондихлорида (10) (Nomenklatur analog Tebbe et al. J. Amer. Chem. Soc. 72 (1950) 3286)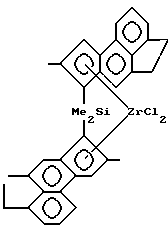
1. 2-метил-a-аценафтиндан-1-он (7)
Раствор 20 г (129 ммоль) a-аценафтена в 320 мл хлористого метилена смешали при комнатной температуре с 29,7 г (129 ммоль) 2-бромида бромизомасляной кислоты. Затем в течение 15 мин через воронку для позирования твердых веществ добавили 43,5 г (324 ммоль) AlCl3. После 30 мин перемешивания добавили ледяную воду и экстрагировали хлористым метиленом. Органическую фазу промыли водой и раствором NaHCO3 и высушили NaSO4. Остаток, оставшийся после удаления растворителяб профильтровали через короткую колонку с силикагелем. С гексан/уксусным эфиром (9:2) получили 25 г (87%) инданона 7.
1H-ЯМР (CDCl3, 100 МГц): 8,57 (d, 1), 7,60 (t, 1), 7,35 (d, 1), 7,25 (s, 1), 3,45 (q, 1), 3,40 (s, 4), 2,60-2,95 (m, 2), 1,35 (d, 3).
2. 2-метил-a-аценафтинден (8)
Раствор 20 г (90 ммоль) соединения 7 в 250 мл смеси ТГФ/метанола (2:1) по каплям добавляли с суспензии 3,8 г (100 ммоль) NaBH4 в 80 мл тетрагидрофурана. Смесь перемешивали при комнатной температуре 2 ч и смешали со 100 мл уксусного эфира и 100 мл слабоконцентрированного НСl. Нагревали 10 мин для кипения с обратным холодильником и экстрагировали уксусным эфиром. Органическую фазу промыли водой и высушили NaSO4. При концентрации и охлаждении до -35oС кристаллизовали в нескольких фракциях всего 16,3 г (88%) соединения 8.
3. Диметилбис(2-метил-a-аценафтинденил)силан (9)
10,8 г (52,4 ммоль) соединения 8 депротонировали аналогично примеру A/5 и преобразовали диметилдихлорсиланом. Органическую фазу выпарили и остаток подвергли хроматографическому разделению на силикагеле. С гексан/4%-уксусным эфиром смогли получить 6,2 г (51%) лигандной системы 9.
1H-ЯМР (CDCl3, 100 МГц): пара диастереомеров 7,1-7,8 (м, ароматические углеводороды-H), 4,0 (s, CH), 3,45 (s, CH2), 2,47 (d, CH3), 2,40 (d, CH3), -0,25 (s, SiCH3), -0,35 (s, SiCH3), -0,37 (s, SiCH3).
4. Рац-диметилсиландиилбис(2-метил-a-аценафтинденил)циркондихлорид (10)
4,9 (10,5 ммоль) лигандной системы 9 преобразовали аналогично примеру A/6. Сырой продукт, состоящий из рацемaтического соединения с мезоформой в соотношении 1: 1, несколько раз перекристаллизовали из хлороформа. Получили 1,3 г (20%) рацемата 10 в виде желто-оранжевого порошка.
1H-ЯМР (CDCl3, 100 МГц): 7,0-7,8 (м, ароматические углеводороды-H), 3,1-3,4 (м, CH2), 2,35 (S, CH3), 1,35 (S, SiCH3).
Пример C. Синтез рац-метилфенилсиландиилбис(2-метил-4,5-бензоинденил)циркондихлорида (12)
1. Метилфенилбис(2-метил-2,5-бензоинденил)силан (11)
Раствор 4,6 г (25,5 ммоль) 2-метил-4,5-бензоинден (4, пример A/4 в 40 мл ТГФ смешали при комнатной температуре при Ar-защите с 10,2 мл (25,5 ммоль) 2,5М раствора бутиллития в гексане и нагревали 1 ч при кипении с обратным холодильником. Затем красный раствор по каплям при комнатной температуре добавили к раствору 2,3 г (12 ммоль) метилфенилдихлорсилана в 10 мл тетрагидрофурана и 8 час нагревали при кипения с обратным холодильником. Переработка и очистка осуществлялись аналогично примеру A/5. Смесью растворителя из гексан/5%-уксусного эфира сначала могли получить непревращенный эдукт, а затем 1,4 г (25% относительно Si) лигандной системы 11 (изомеры).
2. Рац-метилфенилсиландиилбис(2-метил-4,5-бензоинденил)циркондихлорида (12)
Раствор 1,3 г (2,71 ммоль) лиганды 11 в 15 мл теграгидрофурана смешали при комнатной температуре при Ar-защите с 1,2 мл (3 ммоль) 2,5М раствора бутиллития в гексане и перемешивали в течение ночи при комнатной температуре. Растворитель удалили, остаток, крайне чувствительный к действию воздуха, промыли гексаном и несколько часов сушили в вакууме масляного вакуум-насоса. Порошок при температуре -78oC добавили в суспензию 680 г (2,9 ммоль) ZrCl4 в 15 мг CH2Cl2. После медленного нагревания до комнатной температуры перемешивали еще 1 ч при этой температуре и удалили растворитель. Остаток сначала промыли водой и затем экстрагировали с помощью CH2Cl2. При концентрировании и медленном охлаждении до -35oC кристаллизовали 380 мг (22%) цирконоцена 12 в виде чистого рацемата (желто-оранжевый кристаллический порошок). Образовавшиеся затем смешанные фракции (рацемат и 2 мезофазы) смогли очистить путем многоразовой перекристаллизации из хлороформа или толуола.
1H-ЯМР-спектр рацемата: (100 МГц, CDCl3): 6,8-7,9 (м, ароматические углеводороды-H), 7,4 (S, β -Ind-H), 2,4 (Ind-CH3), 1,3 (S, Si-CH3), масс-спектр: 538 M+, правильный распад, правильная модель изотопов.
Пример D. Синтез рац-метилфенилсиландиилбис(2-метил-a-аценафтинденил)циркондихлорида (14)
1. Метилфенилбис(2-метил-a-аценафтинденил)силан (13)
Раствор из 10,8 г (52,4 ммоль) 2-метил-a-аценафтиден (8, пример B/2) в тетрагидрофуране превращали аналогично примеру A/5 с 53 моль бутиллития и 4,9 г (26 ммоль) метилфенилдихлорсилана. Время реакции составило 12 ч. Обработка осуществлялась аналогичным способом. После хроматографического разделения с гексан/6% -уксусный эфир получали 6,0 г (44%) системы лигандов 13 (изомеры).
2. Рац-метилфенилсиландиилбис(2-метил-a-аценафтинденил)циркондихлорид (14)
5,0 г (9,4 ммоль) лигандной системы 13 преобразовали аналогично примеру A/6 19,7 ммоль бутиллитием и затем 2,2 г (9,4 ммоль) Zr-Cl4 обработали. Остаток для удаления мезоформ несколько раз перекристаллизовали из хлористого метилена. Получали 1,2 г (19%) металлоцена 14 в виде чистого рацемата в виде желто-оранжевого порошка.
1H-ЯМР (CDCl3, 100 МГц): 6,8-7,8 (м, ароматические углеводороды-H), 3,0-3,4 (м, CH2), 2,4 (S, CH3), 2,1 (S, CH3), 1,3 (S, SiCH3). Масс-спектр: 690 M+, правильный распад, правильная модель изотопов.
Пример E. Синтез рац-1,2-этaндиилбиc(2-мeтил-4,5-бeнзoиндeнил)циркондихлорида (15)
1. 1,2-бис(2-метил-4,5-бензоинденил)этан (14)
Раствор из 18,0 г (100 ммоль) 2-метил-4,5-бензоинден 4 (пример A/4/ в 400 мл ТГФ смешивали при комнатной температуре с 40 мл (100 ммоль) 2,5М раствора бутиллития в гексане и 30 мин нагревали для кипения с обратным холодильником. При -78oC вводили 9,35 г (50 ммоль) 1,2-диброметан. Смесь нагревали в течение ночи до комнатной температуры, выливали на солянокислую ледяную воду и экстрагировали простым диэтиловым эфиром. После промывки раствором NaHCO3 и высушивания с помощью MgSO4 растворитель удаляли и остаток подвергали хроматографическому разделению на силикагеле 60. С помощью гексан/6%-уксусного эфира элюировали непревращенный эдукт и побочный продукт (спиросоединение) 8,6 г (45%) лигандной системы 14.
2. Рац-1,2-этандиилбис(2-метил-4,5-бензоинденил)-циркондихлорид (15)
Раствор из 4,2 г (10,8 ммоль) лигандов 14 превращали аналогично примеру A/6 с бутиллитием и ZrCl4 Экстракция остатка хлористым метиленом/толуолом и кристаллизация при температуре -35oC дала 1,4 г (24%) металлоцена в виде чистого рацемата в виде желтого микрокристаллического порошка.
1H-ЯМР-спектр (100 МГц, CDCl3): 7,3-8,0 (м, ароматические углеводороды-H), 7,1 (Sβ-H), 3,4-4,1 (м, CH2CH2), 2,2 (S, CH3). Масс-спектр: 546 M+, правильная модель изотопов, правильный распад.
Пример F. Синтез рац-1,2-бутандиилбио(2-метил-4,5-бензоинденил)циркондихлорида (17)
1. 1,2-бис(2-метил-4,5-бензоинденил)бутан (16)
18,0 г (100 ммоль) 2-метил-4,5-бензоинден (4, пример A/4) превращали с аналогично примеру E/1 10,7 г (50 ммоль) 1,2-дибромбутаном (97%) и обработали. Хроматографическим разделением на силикагеле 60 гексан/2% уксусным эфиром получили непревращенный эдукт и спиросоединение 3,9 (19%) лигандной системы 16 в виде смеси изомеров. При последующем хроматографическом разделении на длинной колонке смогли с помощью смеси из гексана и затем гексан/1-З% уксусным эфиром разделить или обогатить отдельные изомеры.
2. Рац-1,2-бутандиилбис(2-метил-4,5-бензоинденил)циркондихлорид (17)
1,0 г (2,41 ммоль) лигандов 16 (2 изомера) преобразовали аналогично примеру А/6 бутиллитием и ZrCl4. Путем экстракции толуол/хлористым метиленом (5: 1) и медленной кристаллизацией путем концентрирования и охлаждения до -35oC получили всего 0,89 г (65%) кристаллических фракций металлоцена 17 различного состава различных изомеров рац- и мезоформ (путем дополнительного центра хиральности на мостике). При нормальной перекристаллизации могла получиться фракция рацемата 17 (пара диастереомеров). Масс-спектр: 574 М+, правильная модель изотопов, правильный распад.
Пример G. Синтез рац-диметилсиландиилбис(4,5-бензоинденил)циркондихлорида (23)
1. Сложный диэтиловый эфир 2-нафтилметилмалоновой кислоты (18)
34,7 г (217 ммоль) сложного диэтилового эфира малоновой кислоты превращали аналогично примеру A/1 и обработали. При обработке гексаном получили 87 г коричневого масла соединения 18.
2. 3-нафтилпропионовая кислота (19)
87 г соединения обработали аналогично примеру A/2 с помощью KOH и подвергли термолизу. Получили 36 г (83%) соединения 19 в виде бежевого порошка.
3. 6,7-бензоиндан-1-он (20)
33,6 (168 ммоль) соединения 19 преобразовали аналогично примеру A/3 с помощью SOCl3 и AlCl3. Время реакции циклизации составило 15 мин при температуре 40oC. После хроматографического разделения получили (частичное разложение на колонке) 9,4 г (30%) инданона 20 в виде желтоватого твердого вещества (частично маслянистого вещества).
1H-ЯМР-спектр (100 МГц, CDCl3): 9,15 (dd, 1, ароматические углеводороды-H), 7,35-81 (м, 5, ароматические углеводороды-H), 3,2 (м, 2, CH2), 2,80 (м, CH2).
4. 4,5-бензоинден (21)
9,4 г (51,6 ммоль) инданона 20 восстановили аналогично примеру A/4. Дегидратация осуществлялась в перегонном аппарате при добавлении 6 г MgSO4. При температуре 110oC и 0,6-0,9 мбар пропускали 2,6 (30%) индена 21 в виде бесцветного дистиллята, который затвердевал при комнатной температуре.
1H-ЯМР-спектр (100 МГц, CDCl3): 7,35-8,2 (м, 7, ароматические углеводороды-H и CH), 6,70 (dt, 1, CH), 3,55 (t, CH2).
5. Диметилбис(4,5-бензоинденил)силан (22)
3,25 г (19,6 ммоль) индена 21 превращали аналогично примеру A/5. Хроматографическим разделением на 600 г на силикагеле 60 получили с помощью гексана и гексан/уксусного эфира 20:1 наряду с эдуктом 1,8 г (47%) лигандной системы 22 (изомеры).
1H-ЯМР-спектр (100 МГц, CDCl3): 7,8-8,2 (м, ароматические углеводороды-H), 6,6-6,9 (м, CH), 3,5-4,1 (м, CH) -0,35-0,20 (несколько синглетов, SiCH3).
6. Рац-диметилсиландиилбис(4,5-бензоинденил)циркондихлорид (23)
1,6 г (4,12 ммоль) лигандов 22 превращали аналогично примеру A/6 бутиллитием и ZrCl4. После экстракции хлористым метиленом при температуре -35oC смогли выделить 520 мг (23%) металлоцена 23 в виде рацемата (желто-оранжевый порошок).
1-ЯМР-спектр (100 МГц, CDCl3): 7,2-8,0 (м, ароматические углеводороды-H), 7,2 (dβ, -CH), 6,4 (da, -CH), 1,2 (S, SiCH3).
Примеры полимеризации
Примеры 1 и 2. Сухой реактор объемом 16 дм3 промыли азотом и залили жидким пропиленом объемом 10 дм3. Затем добавили две трети указанного в таблице количества МАО в виде раствора толуола и состав перемешивали в течение 15 мин при температуре 30oC. Параллельно с этим приготовили толуольный раствор металлоцена диметилсилилбис(2-метил-4,5-бензоинденил)циркондихлорид в одной третьей указанного в таблице количества МАО и после 15 мин отстоя предварительно активировали. Раствор можно предварительно активировать также при перемешивании или встряхивании или в ультразвуковой ванне. Затем этот раствор подавали в реактор и начинали полимеризацию путем нагрева до заданной температуры. Процесс заканчивался путем охлаждения и релаксации через час. Полученный выход полимерного продукта и установленные аналитические данные указаны в табл. 1.
Примеры 3 и 4. Сухой реактор объемом 24 дм3 промыли пропиленом, удалили воздух и заполнили жидким пропиленом объемом 12 дм3. Затем добавили 25 см3 толуольного раствора метилалюминоксана (соответственно 37 ммоль А1, средняя степень олигомеризации p 18) и состав перемешивали при температуре 30oC в течение 15 мин.
Параллельно с этим указанные в табл.2 количества металлоцена рац-диметилсиландиилбис/2-метил-a-аценафтинденил/ZrCl2 растворили в 10 см3 толуольного раствора метилалюминоксана (15 ммоль A1), предварительно активировали соответственно примеру 1 и ввели в процесс полимеризации. Полимеризация проводилась аналогично полимеризации, описанной в примере 1. Условия полимеризации и результаты испытаний представлены в табл. 2.
Примеры 5 9. Повторили пример 3. Были использованы металлоцены, приведенные в табл. 3. Результаты испытаний также представлены в табл. 3.
Пример 10. Повторили пример 3, только использовали 2,6 мг металлоцена и дополнительно в реактор подали 2,5 ндм3 водорода. Активность металлоцена была 496 кг ПП/г металлоцена в час, коэффициент вязкости 187 см3/г, инд. пл. (230/5) 28,5 дг/мин, температура плавления 151oC.
Пример 11. Повторили пример 10, только количество водорода было 25 ндм3. Активность металлоцена была 598 мг полипропилена/г металлоцена в час, коэффициент вязкости 105 см3/г, температура плавления 149oC.
Пример 12. Повторили пример 3, только использовали 2,8 мг металлоцена рац-диметилсиландиилбис(2-метил-4,5-бензоинденил)дихлорида циркония и количество водорода было 15 ндм3. Активность металлоцена была 647 кг полипропилена/г в час, коэффициент вязкости 147 см3/г, температура плавления 148oC. Примеры 10-12 подтверждают хорошее соответствие водорода для регулирования молярной массы в предложенных в изобретении металлоценах.
Пример 13. Сухой реактор объемом 24 дм3 промыли пропиленом и заполнили 2,4 дм3 водорода и 12 дм3 жидкого пропилена. Затем добавили 35 см3 толуольного раствора метилалюминоксана (соответственно 52 ммоль A1, средняя степень олигомеризации p 19). Параллельно с этим растворили 3,9 мг рац-диметил-силандиилбис(2-метил-4,5-бензоинденил)дихлорид циркония в 13,5 см3 толуольного раствора метилалюминоксана (20 ммоль А1) и после 5-минутного отстоя предварительно активировали. Затем раствор подали в реактор и при непрерывной подаче 100 г этилена полимеризовали в течение 1 ч при температуре 60oC. Активность металлоцена составила 40 кг полипропилена/г металлоцена x час, содержание этилена статистического сополимера составило 5,7 мас. Коэффициент вязкости 407 см3/г, средняя молекулярная масса 508 500 г/моль, распределение молекулярной массы 2,4, температура плавления 135oC. Согласно 13C-ЯМР-спектроскопии этилен встраивался большей частью изолированно (статистически).
Пример 14. Сухой реактор объемом 150 дм3 промыли азотом и при температуре 20oC заполнили неароматизированным бензином объемом 80 дм3 с пределом кипения 100-120oC. Затем газовую камеру промыли пропиленом, освободив от азота, и заполнили 50 л жидкого пропилена, а также 64 см3 толуольного раствора метилалюминоксана (соответственно 100 ммоль A1, p 19). Содержимое реактора нагревали до 50oC и путем подачи водорода содержание водорода в газовой камере реактора установилось 0,2% и позже во время полимеризации путем последующей подачи в течение всего полимеризационного времени оставалось постоянным.
(Дополнительное испытание в неавтономном режиме путем газовой хроматографии)
14,9 мг рац-диметилсиландиилбис(2-метил-4,5-бензоинденил)дихлорид циркония растворили в 32 см3 толуольного раствора метилалюминоксана (50 ммоль) и подали в реактор. На первом этапе полимеризация осуществлялась при температуре 65oC в течение 6 ч. На втором этапе при температуре 50oC быстро подавали 3 кг этилена и через 4 ч при этой температуре полимеризация заканчивалась с помощью газа CO2. Получили 23,9 кг порошка блок-сополимера. Коэффициент вязкости 398 см3/г, средний вес массы моля 387 500 г/моль, дисперсность молярной массы 4,5; MEI (230/5 14,5 дг/мин. Блок-сополимер содержал 10,6 мас. этилена. Фракционирование дало 26,9 мас. этилен/пропилен-каучука. Температура стекла каучука была -48oC.
Пример 15. Повторили пример 10, при этом использовали 100 ндм3 водорода. Активность металлоцена была 605 кг полипропилена/г металлоцена в час, коэффициент вязкости 17 см3/г и температуры плавления 150oC.
Пример 15 показывает, что с относительно небольшими количествами водорода могут быть получены даже парафины с предложенными в изобретении металлоценами.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИОЛЕФИНОВ | 1992 |
|
RU2111211C1 |
| КАТАЛИЗАТОР ПОЛИМЕРИЗАЦИИ ОЛЕФИНОВ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ ОЛЕФИНОВОГО ПОЛИМЕРА | 1993 |
|
RU2111219C1 |
| МОСТИКОВЫЕ ХИРАЛЬНЫЕ МЕТАЛЛОЦЕНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 1992 |
|
RU2081876C1 |
| МЕТАЛЛОЦЕНЫ С АРИЛ-ЗАМЕЩЕННЫМИ ПРОИЗВОДНЫМИ ИНДЕНИЛА, СПОСОБ ПОЛУЧЕНИЯ ПОЛИМЕРОВ ОЛЕФИНА И КАТАЛИЗАТОР ПОЛИМЕРИЗАЦИИ ОЛЕФИНОВ | 1993 |
|
RU2118961C1 |
| СПОСОБ ПОЛУЧЕНИЯ СИНДИОТАКТИЧЕСКОГО ПОЛИОЛЕФИНА | 1992 |
|
RU2101296C1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТАЛЛОЦЕНОВ С МОСТИКОВЫМИ СВЯЗЯМИ | 1995 |
|
RU2161621C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИОЛЕФИНОВ | 1992 |
|
RU2078771C1 |
| МЕТАЛЛОЦЕНЫ, СОДЕРЖАЩАЯ ИХ КАТАЛИТИЧЕСКАЯ СИСТЕМА, СПОСОБ ПОЛИМЕРИЗАЦИИ ОЛЕФИНОВ, ПОЛИОЛЕФИН, ФОРМОВАННОЕ ИЗДЕЛИЕ | 1994 |
|
RU2142466C1 |
| БОРОРГАНИЧЕСКОЕ СОЕДИНЕНИЕ, СПОСОБ ЕГО ПОЛУЧЕНИЯ, КАТАЛИТИЧЕСКАЯ СИСТЕМА, СПОСОБ ПОЛУЧЕНИЯ ОЛЕФИНОВОГО ПОЛИМЕРА И ПОЛИОЛЕФИН | 1997 |
|
RU2147585C1 |
| СПОСОБ ПОЛУЧЕНИЯ СИНДИОТАКТИЧЕСКОГО (СО)ПОЛИМЕРА ПРОПИЛЕНА | 1992 |
|
RU2100375C1 |


Предложены металлоцены с бензоконденсированными производными инденила в виде лигандов, способ их получения и применения в качестве катализаторов. Очень эффективная система катализаторов для полимеризации олефинов состоит из сокатализатора, предпочтительно алюминоксана, и металлоцена формулы I.

где предпочтительно M1 обозначает Zr или Hf, R1 и R2 - галоген или алкил, R3 - алкил, R4-R10 - алкил или водород и R11 - (замещ.) алкиленовый или гетероатомный мостик. 4 с. и 8 з.п. ф-лы, 3 табл.

где М1 титан, цирконий или гафний;
R1 и R2, одинаковые или различные, галоген, алкил с 1 - 10 атомами углерода или арил с 6 10 атомами углерода;
R3, одинаковые или различные, водород или алкил с 1 10 атомами углерода;
R4 R1 0 имеют значения, указанные для R3, или смежные радикалы R4 R10 вместе с соединяющими их атомами образуют ароматическое или алифатическое кольцо;
R1 1 остаток формулы М2R1 2R1 3, CR1 2R1 3 или CR1 2R1 3 - CR1 2 R1 3, где М2 кремний, германий или олово, R1 2 и R1 3, одинаковые или различные
водород, алкильная группа с 1 10 атомами углерода или арил с 6 10 атомами углерода.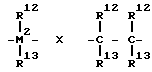
или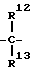
причем М2 кремний;
R12 и R1 3, одинаковые или различные, С1 - С4-алкильная группа или С6 С1 0-арилгруппа.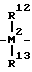
или
причем М2 кремний;
R1 2 и R1 3, одинаковые или различные, - С1 С4-алкильная группа или С6 - С1 0-арилгруппа.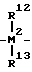
причем М2 кремний, R12 и R1 3, одинаковые или различные, метил или фенил.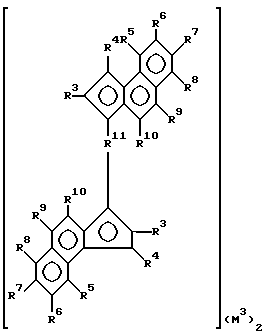
где R3 R1 1 имеют значения, указанные для формулы I;
М3 щелочной металл, предпочтительно литий,
вводят в взаимодействие с соединением формулы V
М1 Х4,
где М1 имеет значение, указанное в формуле I;
Х галоген, предпочтительно хлор,
и затем в случае необходимости в полученном продукте атомы галогенов переводят в соединения, в которых R1 и R2 алкил с 1 10 атомами углерода или арил, содержащий 6 10 атомов углерода.
Ra-CH=CH-Rb,
где Ra и Rb, одинаковые или различные, водород или алкил с 1 14 атомами углерода,
при -60 200oС и 0,5 100,0 бар в растворе, суспензии или газовой фазе в присутствии металлоценнового соединения титана, циркония или графия в качестве катализатора и циклического или линейного алюмоксана в качестве сокатализатора, отличающийся тем, что в качестве катализатора используют катализатор по п.8.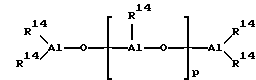
для линейного типа и/или общей формулы III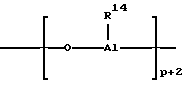
для циклического типа
где R1 4, одинаковые или различные, С1 - С6-алкильная группа, С6 С1 8-арилгруппа, бензил или водород; р 2 50, целое число.
| EP, патент, 3808268, кл.C 08F 10/00, 1989 | |||
| EP, патент, 3726067, кл.C 08F 4/60, 1989. |
Авторы
Даты
1997-12-10—Публикация
1992-11-30—Подача