Изобретение относится к области технических устройств, применяемых в биологии и медицине для определения показателей метаболизма и возбудимости клеточных элементов.
В литературе описано устройство для быстрой смены состава внеклеточной жидкости, представляющее собой укрепленный на пьезокерамическом элементе микрокапилляр. Раствор соответствующего вещества подается из него в форме микроструи, траектория которой контролируемо изменяется в зависимости от амплитуды электрического сигнала на пьезоэлементе.
Недостатком известного технического решения является то, что непосредственно в период подведения вещества химическому воздействию последовательно подвергаются все клеточные единицы, лежащие на пути перемещения микроструи жидкости из ее исходного положения в область локализации тестируемой клетки. Кроме того, в данном случае интервал времени от момента подачи сигнала на электромеханический преобразователь до момента начала аппликации составляет не менее 1,5 2,0 мсек. Это исключает возможность применения такого рода устройств при решении задач, связанных с определением показателей метаболизма и возбудимости нервных или мышечных клеток непосредственно в период их функциональной активности.
Целью настоящего изобретения является повышение избирательности (локальности) химического воздействия и увеличение скорости подведения вещества.
Достигаемый технический результат возможность полной смены состава внеклеточной жидкости в области локализации отдельной клеточной единицы в течение 0,3 мсек обусловлен тем, что укрепленный на электромеханическом преобразователе микрокапилляр устанавливают внутри подсоединенной к насосу отрицательного давления стеклянной микропипетки таким образом, что в исходном положении микрокапилляр полностью находится внутри нее, а при подаче управляющего сигнала на электромеханический преобразователь он выдвигается вперед по отношению к переднему ее краю, в результате чего во внеклеточной среде образуется замкнутая зона выхода вещества, размеры которой ограничены областью локализации отдельной клетки. Для увеличения скорости подведения вещества в качестве электродвигательного элемента используют координатный гальванометр (сельсин), запускаемый двухфазным электрическим сигналом, первая высокоамплитудная импульсная составляющая которого обеспечивает максимальное снижение времени задержки срабатывания устройства, а следующая за ней низкоамплитудная фаза определяет необходимую продолжительность периода подведения вещества.
На чертеже изображен общий вид предложенного устройства.
Устройство включает в себя коаксиально расположенные по отношению друг к другу стеклянный микрокапилляр 1 и стеклянную микропипетку 2, которая зафиксирована с помощью силиконового уплотнителя 3 внутри тройника 4. Подвижный микрокапилляр 1 помещен в отрезок инъекционной иглы 5, в верхней части которой находится резиновый колпачок 6. Для герметизации механических соединений здесь также используются силиконовые уплотнители соответствующего диаметра.
Представленное устройство вместе с координатным гальванометром 7 (сельсином чернилопишущего прибора Н338/6) закрепляют в держателе 8, который установлен на штанге позиционера, обеспечивающего точные микроперемещения устройства в области локализации тестируемой клетки.
Подача раствора биологически активного вещества осуществляется под давлением через полихлорвиниловый катетер 9, плотно надетый на микрокапилляр 1 и зафиксированный винтом 10 на осевой площадке электромеханического преобразователя 7. Соответственно, удаление жидкости из объема микропипетки 2 производится через боковой канал тройника 4, который подсоединен к насосу отрицательного давления. Исходное положение микрокапилляра 1 по отношению к микропипетке 2, а также амплитуда его перемещения регулируются двумя ограничительными винтами 11 и 12. Они же используются в качестве контактов, которые при помощи электрических проводников 13 включены в цепь определения скорости срабатывания устройства.
Устройство работает следующим образом. В исходном положении (поз. А на фиг.) микрокапилляр 1 полностью находится внутри подсоединенной к насосу отрицательного давления микропипетки 2, поэтому весь выходящий из него раствор биологически активного вещества удаляется через боковой канал тройника 4, не попадая в экстраклеточную среду. После подачи на электромеханический преобразователь двухфазного управляющего сигнала возникает угловое перемещение оси сельсина 7, вызывающее поступательное движение катетера 9 вместе с микрокапилляром 1, который, выдвигаясь вперед по отношению к переднему краю микропипетки 2, образует здесь замкнутую зону выхода вещества (поз. Б на фиг.). Оптимальная амплитуда первой составляющей управляющего электрического сигнала равняется 150 300 в, длительность 1 мсек. Продолжительность его второй, низкоамплитудной (10 в) фазы определяется в каждом конкретном случае в зависимости от необходимого периода аппликации вещества.
Оценка эффективности предложенного технического решения проводилась в рамках исследования идентифицированных клеток ППаI нервной системы беспозвоночных животных Helix lucorum.
Полуинтактный препарат моллюска помещают в ванночку для электрофизиологического тестирования. К области локализации исследуемой клетки сверху подводят инъекционную иглу, из которой со скоростью 0,3 мл/мин подается профильтрованный раствор Рингера для холоднокровных. Такая реализация схемы общего протока резко снижает вероятность блокирования входного канала насоса отрицательного давления в результате случайного попадания туда каких-либо микрочастиц из гемолимфы животного.
Затем к тестируемому нейрону с помощью микроманипулятора подводят устройство для локального подведения биологически активных веществ. Предварительно его подключают к шприцевому насосу (P + 0,6 атм), содержащему физиологический раствор 3H-лейцина (1 млкюри/мл ) с добавлением к нему витального красителя "трипановый синий" (0,1%) и к насосу отрицательного давления (P 0,2 атм). Устройство устанавливают таким образом, чтобы в момент максимального выхода микрокапилляра из микропипетки он оказывался бы на расстоянии около 30 мкм от плазматической мембраны нейрона. При помощи другого микроманипулятора к исследуемой клетке подводят регистрирующий микроэлектрод, сигнал с которого подают на вход усилителя биопотенциалов. Погружение микроэлектрода заканчивают после появления на выходе усилителя характерных высокоамплитудных импульсов, соответствующих разрядам клетки. Далее эти импульсы преобразуются триггерным устройством и подаются на вход генератора, формирующего двухфазный сигнал запуска сельсина, а также на вход фотостимулятора "Медикор" (длительность световой вспышки 0,2 мсек, время срабатывания 0,1 мсек).
При работе с нейронами ППаI, характеризующимися выраженной пачечно-групповой формой спонтанной активности, микровременную динамику подведения можно было определять непосредственно в ходе тестирования клетки в режиме ассоциированной с ее разрядной деятельностью аппликации биологически активного вещества. В этом случае освещение препарата короткими вспышками света, синхронизированными с определенной фазой генерации потенциала действия, создает визуальный эффект неподвижного (стробоскопического) изображения, соответствующего заданной (режимом "Delay" фотостимулятора) микровременной стадии работы рассматриваемого устройства. Как показывают полученные результаты, в течение первых 0,2 мсек от момента подачи управляющего сигнала микрокапилляр полностью выдвигается из микропипетки, а еще через 0,1 мсек в области локализации нейрона образуется замкнутая зона выхода вещества. Таким образом, предложенное устройство по сравнению с прототипом позволяет повысить скорость смены состава внеклеточной жидкости более чем в 5 раз.
Оценку избирательности указанного процесса проводили путем авторадиографического анализа пространственного распределения в нервной системе животного, меченного изотопами лейцина в условиях локального импульсного его подведения к нейрону ППаI. У каждой исследованной клетки регистрировали 6000 спайков, что соответствовало 1,5 2 часовому периоду ее инкубации. Продолжительность аппликации 3H-лейцина во время генерации каждого отдельного потенциала действия составляла 10 мсек. После завершения тестирования нервную ткань замораживали в изопентане, охлажденном жидким азотом до -70oC, а затем на 12 часов помещали в абсолютный этиловый спирт (Т -40oC). Срезы толщиной 10 мкм монтировали на предметных стеклах, которые после этого покрывали тонким слоем фотоэмульсии типа P. Время экспозиции всех радиоавтографов составляло 3 недели. При проявке использовали проявитель Д-19, а в качестве фиксажа 30% раствор гипосульфита. Количество поглощенного за 1 минуту изотопа оценивали путем подсчета количества зерен восстановленного серебра над контуром исследуемой клетки. При статистической обработке использовали критерий Стьюдента. Полученные результаты сопоставляли с контрольными определениями, в рамках которых аналогичное импульсное подведение 3H-лейцина осуществлялось в межспайковые интервалы времени. Были получены следующие результаты.
1. Данные по 1 основной серии (подведение импульсной метки в период генерации потенциала действия)
Количество исследованных клеток 15
Количество зерен восстановленного серебра 14,1±0,2
2. Данные по 1 контрольной серии (по группе нейронов, расположенных в непосредственной близости от тестируемой клетки)
Количество исследованных клеток 52
Количество зерен восстановленного серебра 1,2±0,1
3. Данные по 2 основной серии (подведение импульсной метки в межспайковые интервалы времени)
Количество исследованных клеток 15
Количество зерен восстановленного серебра 5,8±1,7
4. Данные по 2 контрольной серии (радиоактивный фон вне области локализации нервной системы)
Количество зерен восстановленного серебра 0,8±0,3
Таким образом, как показывают полученные результаты, предложенное устройство позволяет ограничить зону химического воздействия размером области локализации одной клеточной единицы интактной нервной системы, а также более чем в 5 раз по сравнению с прототипом увеличить скорость подведения биологически активного вещества к тестируемой клетке.
| название | год | авторы | номер документа |
|---|---|---|---|
| МИКРОЗОНД ДЛЯ ФУНКЦИОНАЛЬНОГО БИОХИМИЧЕСКОГО АНАЛИЗА | 1997 |
|
RU2127880C1 |
| УСТРОЙСТВО ДЛЯ МОДЕЛИРОВАНИЯ САМООРГАНИЗУЮЩИХСЯ СЕТЕЙ НЕФОРМАЛЬНЫХ НЕЙРОНОВ | 2011 |
|
RU2484527C1 |
| МНОГОКАНАЛЬНЫЙ ЭЛЕКТРОД С НЕЗАВИСИМЫМ ПЕРЕМЕЩЕНИЕМ МИКРОПРОВОДНИКОВ В ПУЧКЕ | 2009 |
|
RU2421253C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ БИОЛОГИЧЕСКОЙ АКТИВНОСТИ ВОДЫ | 2008 |
|
RU2377563C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ БИОЛОГИЧЕСКОЙ АКТИВНОСТИ ВОДЫ | 2008 |
|
RU2379681C1 |
| ПЕПТИДНЫЙ МОДУЛЯТОР ПУРИНЕРГИЧЕСКИХ РЕЦЕПТОРОВ | 2010 |
|
RU2422459C1 |
| Способ оценки нейротропной и/или нейротоксической активности веществ и их композиций | 2024 |
|
RU2830897C1 |
| Способ определения нейротропной активности веществ | 1979 |
|
SU996910A1 |
| НЕЙРОЭЛЕКТРОННЫЙ МНОГОКАНАЛЬНЫЙ ИНТЕРФЕЙС | 2007 |
|
RU2327202C1 |
| МУТАНТНЫЙ КАНАЛЬНЫЙ РОДОПСИН-2 | 2011 |
|
RU2595384C2 |
Устройство для локального подведения биологически активных веществ относится к медицине и может быть использовано для определения показателей метаболизма и возбудимости клеточных элементов. Укрепленный на электромеханическом преобразователе (7) микрокапилляр (1) устанавливают внутри подсоединенной к насосу отрицательного давления стеклянной микропипетки (2) таким образом, что в исходном положении микрокапилляр (1) полностью находится внутри нее, а при подаче управляющего сигнала он выдвигается вперед по отношению к переднему ее краю, в результате чего во внеклеточной среде образуется замкнутая зона выхода вещества. 1 з.п. ф-лы. 1 ил.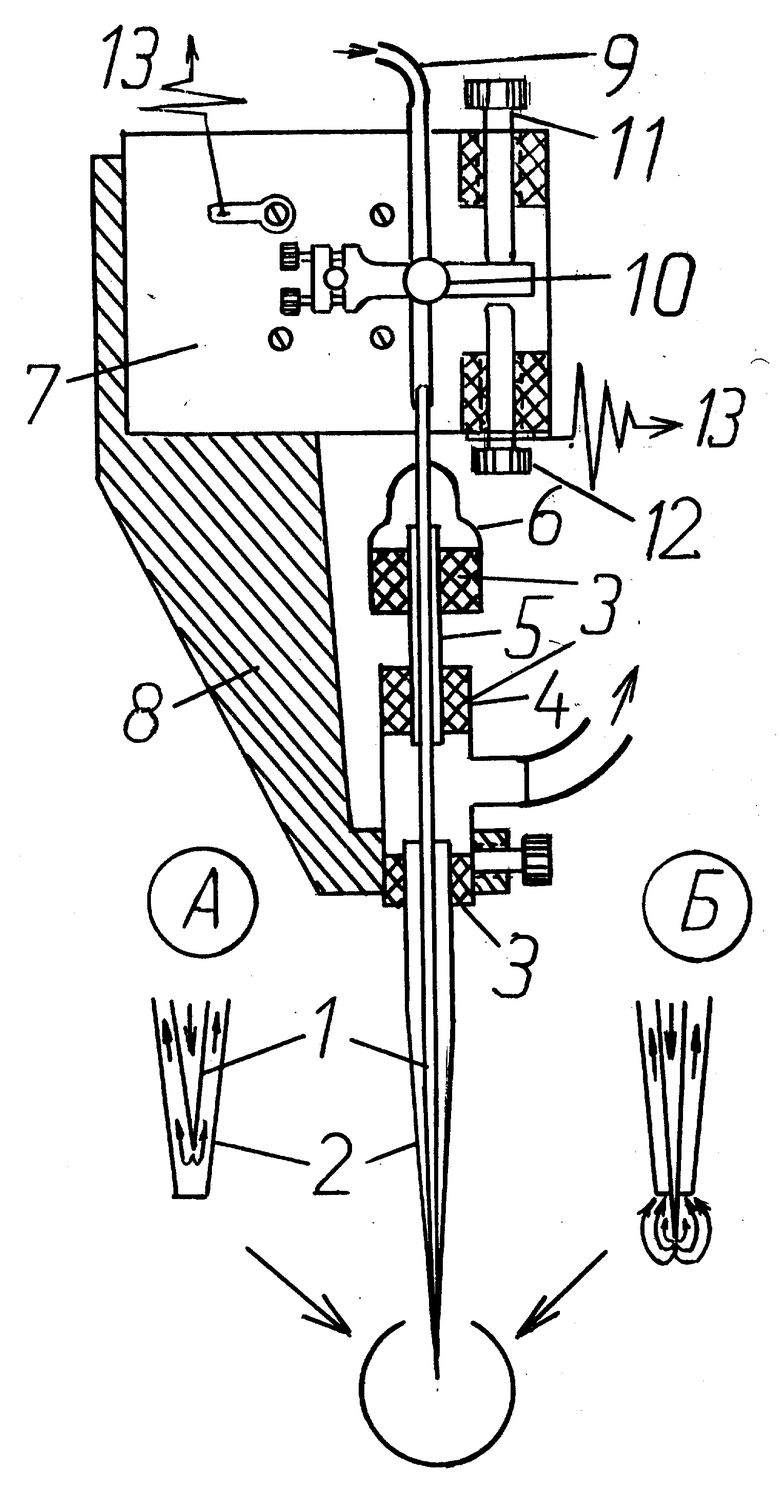
| CH | |||
| Franke, H | |||
| Hatt, J.Dudel | |||
| Liquid Filaments witch for ultrafact exchanges of solutions atexcised patehes of synaptic membrane of crayficn muscle | |||
| Кузнечная нефтяная печь с форсункой | 1917 |
|
SU1987A1 |
| ПЕЧНОЙ ЖЕЛЕЗНЫЙ РУКАВ (ТРУБА) | 1920 |
|
SU199A1 |
Авторы
Даты
1998-01-20—Публикация
1995-06-16—Подача