Изобретение относится к способу получения 4-метил-5-/2-хлоралкил/-тиазолов общей формулы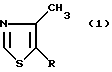
где R означает C1-5 -алкил с прямой цепью, замещенной атомом хлора в положении 2, с помощью частично известных промежуточных продуктов. Соединение общей формулы 1а ,
,
и его соли присоединения кислот (Клометиазол) является терапевтически широко применяемым активным ингредиентом антиконвульсивных и седативных средств. Соединение формулы 1а первоначально было описано в 1935 г. (J. Am. Chem. Soc. 57, 1876, 1935). Его гидрохлоридная и этандисульфонатная соли были описаны в GB-PS 792 158. Его фосфатная соль известна из US-PS 3 639 415.
Известные способы получения производных тиазола, незамещенных в положении 2, могут быть разделены на два основных типа. При работе по способам первого типа 2-незамещенный тиазол получают в одну стадию. В соответствии со способами второго типа получают производные тиазола, содержащие легко удаляемый заместитель в положении 2, и удаляют этот заместитель во второй стадии.
Согласно способам первого типа тиазольное кольцо образуется при взаимодействии галоидированного кетона или альдегида, которые галоидированы в α-положении, или альдегида с тиоформамидом (Elderfield, R.C.: Heterocyclic Compounds, 1957, т. 5, с. 516) (Реакционная схема А):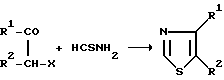 ,
,
R1 и R2 = алкил, арил или водород;
Х - галоид.
Этот тип способов дает хороший выход только в некоторых случаях (Buchman and Richardson: J. Am. Chem. Soc. 67, 395, 1945); Erne, Ramires ans Burger: Helv, Chem. Asta 34, 143, 1951). Другим недостатком этого способа являетСЯ трудность получения чистого тиоформамида. Для преодоления этого затруднения получение тиоформамида проводят в реакционной смеси из формамида и пятисернистого фосфора, но этот способ является успешным только в некоторых случаях (Ganapathe and Venkataraman: Proc. Indian Acad.Sci, 22, 362, 1955). Этот способ сильно загрязняет окружающую среду из-за использования пятисеристого фосфора.
Поскольку описанный выше прямой синтез трудно реализовать в промышленном масштабе, внимание было направлено на варианты непрямого синтеза. В одном из этих вариантов удаляют аминогруппу в положении 2 с помощью диазотирования и последующего восстановления диазониевой группы (Ganapathi and Venkataraman: Proc. Indian Acad. Sci. 22, 366, 1945). Производное 2-аминотиазола, необходимое для этого способа, может быть получено в отдельной стадии из α-галоидкетона с тиомочевиной (Tanida, Tamura and Sava: J. Pharm. Soc. Japan, 74, 652, 1954; С.А. 48, 10737, 1945) (Реакционная схема В).
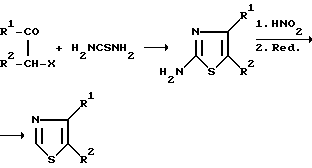
При таком пути целевые соединения могут быть получены с плохими выходами в интервале между 30 и 60%.
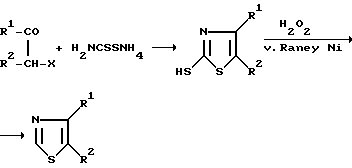
Другой возможностью является окислительное удаление тиогруппы в положении 2 тиазола (GB-PS 492 637; Buchman, Reims and Sargnet: J. Org. Chem 6, 764, 1941), или десульфирование производного 2-меркаптотиазола при кипячении с никелем Ренея в большом избытке (Cook et al.: J. Chem. Soc. 1954, 1947); Hurd and Rudner: J. Am. Chem. Soc. 73, 5157, 1951). Необходимый 2-меркаптотиазол также может быть получен в отдельную стадию из α-галогенкетона и дитиокарбамата аммония (например, GB-PS 492 637) (Реакционная схема С).
 .
.
Недостаток этого способа заключается в том, что для получения дитиокарбамата аммония необходим сероуглерод, требующий специального цеха при получении в промышленном масштабе из-за большой опасности возгорания. Кроме того, реагент и побочные продукты синтеза в значительной степени загрязняют окружающую среду. При десульфировании с никелем Ренея требуется большой избыток никеля, что значительно увеличивает стоимость синтеза.
Третьей возможностью является дегалоидирование производных 2-галогентиазола. Для этой цели используют главным образом цинк в среде уксусной кислоты (GB-PS 456 751; Gibbs and Robinson: J.Chem. Soc. 925, 1945; Andersad and Westphal: Ber. 70, 2035, 1937).
Каталитическое дегалоидирование описано только для случая 2-бромтиазол-4-карбоновой кислоты (Erlenmeyer and Morel: Helv. Chim. Acta 25, 1073, 1942). 2-Галоидтиазольные соединения, а именно исходный материал для способа, получают из производных 2-аминотиазола путем диазотирования и реакции Сэндмейера (Sava and Maeda: J. Pharm. Soc. Japan 76, 301, 1956; С.А. 50, 13875, 1956) или из производных 2-окситиазола с фосфорилхлоридом (GB-PS 456 751), или путем замыкания цикла α-тиоцианатокетонов с газообразным хлористым водородом (Elderfield: Heterocyclic Compounds, 1957, т. 5, с. 540, 1957). (Реакционные схемы Д и Е).
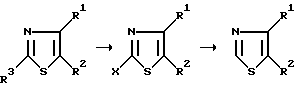
R3 - NH2, OH,
X = галоид.
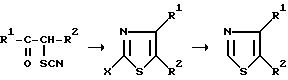
Ни один из приведенных выше способов не используется для получения ни соединений общей формулы 1 настоящего изобретения, ни для получения соединений формулы 1а. Соединение формулы 1а получали хлорированием соответствующего гидроксильного соединения тионилхлоридом (FR-PS 3 815 M; GB-PS 792 158 и NL-PA 6 51-0 389 - Реакционная схема F).
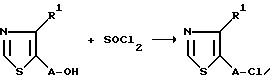
А - алкиленовая группа
Для Клометиазола формулы 1а был описан способ, в соответствии с которым окисляют подходящее 2-меркаптопроизводное перекисью водорода (CH-PS 200 248).
2-Хлор-4-метил-5-/2-хлорэтил/-тиазол формулы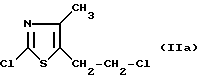
(Acta Pharm. Suec. 8, c. 49, 1982) и 2-окси-4-метил-5-/2-хлорэтил/-тиазол формулы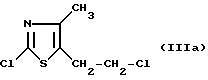
(Acta Pharm. Suec, 19, c. 37, 1982) являются известными соединениями. Однако ни одно из этих соединений не было предложено как подходящий промежуточный продукт для получения соединения формулы 1а.
Во всех общих формулах R имеет указанные выше значения.
Неожиданно мы обнаружили, что при взаимодействии известного 3,5-дихлор-2-алканона общей формулы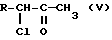
с неорганическим изотиоцианатом и превращении 3-тиоцианато-5-хлор-2-алканона общей формулы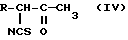
полученного таким образом, в 2-хлор-4-метил-5-/2-хлоралкил/-тиазол общей формулы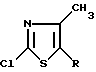
с газообразным хлористым водородом в органическом растворителе, с последующим гидрированием последнего в присутствии металлического катализатора в органическом растворителе, получают с хорошим выходом 4-метил-5-/2-хлоралкил/тиазолы общей формулы I высокой чистоты при выделении их из реакционной смеси известными способами, предпочтительно в виде их гидрохлоридов.
Соединения общей формулы I могут быть превращены в их соли присоединения кислот известными вообще способами. Они также могут быть получены при взаимодействии соединений общей формулы IV с водной минеральной кислотой и превращении полученных таким образом 2-окси-4-метил-5-/2-хлоралкил/тиазолов общей формулы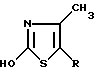
в соединениях общей формулы II с помощью галоидирующего агента с последующим гидрированием последних в соединениях общей формулы I, как описано выше.
Изобретение основано на следующих положениях: в соединениях общей формулы V реактивность заместителя - хлора в α- положении по отношению к карбонильной группе превосходит реактивность других хлорных заместителей на конце цепи до такой степени, что получают исключительно соединения общей формулы IV, не наблюдается образования ни дитиоцианатокетона, ни изотиоцианатокетона даже в следовых количествах.
Получение соединений общей формулы II, содержащих тиазольное кольцо, из соединений общей формулы IV не является очевидным из литературных данных.
Удаление заместителя - хлора в тиазольном кольце из дихлорных соединений общей формулы II при селективном гидрировании является неожиданным и неочевидным, поскольку неактивность хлорного заместителя в конце цепи не может быть ожидаемой для специалиста в этой области.
Превращение соединений общей формулы IV в производные 2-окситиазола общей формулы III предпочтительно в присутствии фосфорной кислоты, потом галоидирование соединений общей формулы III небольшим избытком галоидирующего агента в наиболее подходящем растворителе осуществляется со значительными технологическими и экологическими преимуществами.
Способ, описанный в примерах изобретения, является новым и представляет собой альтернативный синтетический путь, который не может быть выведен из известных способов получения Клометиазола общей формулы Ia.
Ниже приводится выгодный вариант способа изобретения для синтеза соединения общей формулы Ia.
Соединение формулы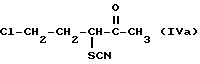
получают из известного соединения формулы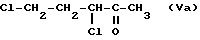
(Acta Chem. Hung, 3. 157, 1953) в воде, в органическом растворителе или в смеси воды и органического растворителя, с помощью неорганических тиоцианатов, предпочтительно тиоцианатов натрия, калия или аммония. Наиболее предпочтительно используют органический растворитель, например, ацетон, метилэтилкетон, этилацетат, бутилацетат, метанол, этанол, изопропилацетат или этилпропионат.
Реакция может быть проведена при температуре в интервале от 20 до 100oC, предпочтительно при температуре кипения растворителя, с эквивалентным количеством или незначительным (1-5 мол.%) избытком неорганического роданида.
Дихлорпроизводное общей формулы IIa получают при взаимодействии соединения формулы IVa, растворенного в органическом растворителе, с безводным газообразным хлористым водородом. В качестве растворителя наиболее предпочтительно используют несмешивающиеся с водой простые и сложные эфиры, которые нерастворимы в воде, например, этилацетат, бутилацетат или диизопропиловый эфир. Предпочтительно также могут быть использованы низшие алифатические спирты, например, метанол, этанол, н-пропанол, изопропанол или бутанол, низшие жирные кислоты, например, уксусная или пропионовая кислота, или галоидированные углеводороды, например, четыреххлористый углерод, хлороформ или 1,2 -дихлорэтан.
Реакцию проводят при температуре в интервале от 0 до 100oC, предпочтительно от 0 до 40oC.
Селективное гидрирование соединения формулы IIa проводят в присутствии металлического катализатора в органическом растворителе.
Металлическим катализатором предпочтительно является палладий на активированном угле или палладий, содержащий селен (примеры 1, 3 и 5 опубликованной заявки FCT N 89/2429), также могут быть использованы катализаторы, содержащие родий или рутений.
В качестве органического растворителя могут быть использованы низшие алифатические спирты, например, метанол, этанол, н-пропанол или изопропанол, низшие сложные эфиры алифатических карбоновых кислот, например, этилацетат, бутилацетат, метилацетат, изопропилацетат или этилпропионат, ароматические углеводороды, например, бензол или толуол, или простые эфиры с открытой цепью, например, целлозольв, метилцеллозольв, бутилцеллозольв, диметилцеллозольв или диглим.
Гидрирование можно проводить при атмосферном давлении или при слегка повышенном давлении (0,05-0,7 МПа).
Расщепляющий хлористый водород связывается с образованием тиазольного производного формулы Ia, затем оно может быть также извлечено в форме гидрохлорида формулы Ia.
Во время гидрирования в качестве связывающего кислоту агента может быть применен щелочной гидроксид, например, гидроксид натрия или калия или органическое основание, например, триэтиламин, затем получают само основное соединение формулы Ia.
При получении соединения формулы IIIa α-тиоцианатокетон формулы IVa обрабатывают водной фосфорной кислотой, в этом случае нет необходимости в органическом растворителе и не возникает проблемы коррозии в противоположность известным реагентам уксусная кислота - концентрированная серная кислота или уксусная кислота-концентрированная соляная кислота. Кроме того, во время обработки реакционной смеси не образуется опасных для окружающей среды побочных продуктов.
Реакцию проводят при температуре в интервале от 50 до 120oC, предпочтительно от 90 до 100oC.
При галоидировании соединений формулы IIIa в качестве галоидирующего агента используют галоидные соединения фосфора, например, фосфорилхлорид, пятихлористый фосфор или треххлористый фосфор.
В качестве органического растворителя могут быть использованы предпочтительно галоидированные алифатические углеводороды, например, 1,2-дихлорэтан, 1,1,2-трихлорэтан, трихлорэтилен или 1,1,2,2,-тетрахлорэтан, ароматические углеводороды, например, бензол, толуол или ксилол, особенно предпочтительно, галоидированные ароматические углеводороды, например, хлорбензол, 1,2-дихлорбензол или 1,2,4-трихлорбензол.
Реакцию проводят при температуре в интервале от 80 до 150oC, предпочтительно от 100 до 140oC.
Другие соединения общих формул I, II, III и IV предпочтительно могут быть получены по описанным выше способам.
Получение соединений общей формулы V описано в примерах, когда не имеется ссылок на литературные данные.
Пример 1. Прибавляют 77,8 г (0,5 моль) 3,5-дихлор-2-пентанона (полученного согласно Acta Chim. Hung. 3, 157, 1953) к раствору 49,9 г /0,513 моль/ роданида калия в 500 мл ацетона. Раствор кипятят при перемешивании в течение 4 ч. Реакционную смесь охлаждают до комнатной температуры, отфильтровывают осадок хлористого калия и промывают ацетоном. Фильтрат выпаривают, остаток растворяют в бензоле в бензольный раствор промывают 3 раза водой. После сушки над сульфатом натрия бензол отгоняют. Получают 62,2 г (93%) 3-тиоцианато-5-хлор-2-пентанона в виде красного масла. После разгонки при пониженном давлении получают светло желтое масло, его точка кипения равна 112oC при давлении 26,6 Па, n
Анализ для формулы C6H3ClNOS:
Вычислено, %: C 40,56; H 4,53; N 7,88; Cl 19,95; S 18,04;
Найдено, %: C 41,25; H 4,59; N 8,13; Cl 20,32; S 17,90.
Данные ЯМР подтверждают структуру.
Пример 2. Раствор 155,5 г (1 моль) 3,5-дихлор-2-пентанона с 83 г (1,024 моль) роданида натрия в 1 л метилэтилкетона кипятят 1 ч при перемешивании. Затем работают по методике примера 1. Получают 171 г (96,2%) 3-тиоцианато-5-хлор-2-пентанона, который после перегонки идентичен во всех отношениях продукту примера 1.
Пример 3. Суспензию 7,8 г (0,05 моль) 3,5-дихлор-2-пентанона с 3,9 г (0,051 моль) роданида аммония в 50 см3 метилэтилкетона кипятят 1 ч при перемешивании. Затем работают по методике примера 1. Получают 8,5 г (95,5%) 3-тиоцианато-5-хлор-2-пентанона, который после перегонки идентичен во всех отношениях продукту примера 1.
Пример 4. Раствор 7,8 г (0,05 моль) 3,5-дихлор-2-пентанона с 4,15 г (0,051 моль) роданида натрия в 50 см3 этанола кипятят 2 ч при перемешивании. Затем работают по методике примера 1. Получают 7,7 (87%) 3-тиоцианато-5-хлор-2-пентанона, который идентичен во всех отношениях продукту примера 1 после перегонки.
Пример 5. К раствору 4,86 г (0,05 моль) роданида калия в 10 см3 воды прибавляют 7,8 г (0,05 моль) 3,5-дихлор-2-пентанона и перемешивают реакционную смесь 3 ч при 80oС. После охлаждения отделяют выделившееся масло и водную фазу встряхивают дважды каждый раз в 20 см3 бензола. Отделенное масло объединяют с бензольным раствором, промывают водой и сушат над сульфатом натрия. После фильтрации и выпаривания получают 7,4 г (83,5%) 3-триоцианато-5-хлор-2-пентанона, который после перегонки идентичен во всех отношениях продукту примера 1.
Пример 6. Раствору 17,7 г (0,1 моль) 3-тиоционато-5-хлор-2-пентанона в 170 см3 безводного этилацетата насыщают газообразным хлористым водородом. Температуру реакционной смеси поддерживают ниже 10oC при охлаждении льдом. Полученный раствор оставляют на ночь при комнатной температуре. На следующий день раствор выливают на лед и устанавливают величину его рН меду 6 и 7 с помощью 20%-ного раствора гидроксида натрия. Разделяют фазы и водную фазу встряхивают со 150 см3 этилацетата. Объединенные этилацетатные растворы промывают до нейтрально реакции водой и 5%-ным раствором бикарбоната натрия, сушат над сульфатом натрия. После отгонки растворителя остаток разгоняют при пониженном давлении, получают 14,8 г (75,5%) 2-хлор-4-метил-5-/2-хлорэтил/-тиазола в виде светло-желтого масла. Точка кипения 104oC при давлении 40 Па, n
Анализ для формулы C6H7Cl2NS:
Вычислено, %: C 36,70; H 3,39; N 7,14; Cl 36,15; S 16,35;
Найдено, %: C 37,01; H 3,71; N 7,48; Cl 35,40; S 15,97.
ИК и ЯМР-спектры подтвержают структуру. По данным газовой хроматографии содержание продукта превышает 95%.
Пример 7. Растворяют 25 г (0,14 моль) 3-тиоцианато-5-хлор-2-пентанона в 170 см3 бутилацетата, насыщенного газообразным хлористым водородом. В реакционную смесь вводят газообразный хлористый водород до насыщения при охлаждении льдом, поддерживая температуру ниже 10oC. После насыщения реакционную смесь перемешивают еще 20 мин при охлаждении, затем температуру медленно повышают до 40oC. Реакционную смесь перемешивают при этой температуре 20 мин и после, охлаждения до комнатной температуры, выливают на лед. Устанавливают величину рН смеси между 7 и 8 при добавлении 40%-ного раствора гидроксида натрия. Затем смесь обрабатывают, как описано в примере 6.
Получают 20,8 г (76%) 2-хлор-4-метил-5-/2-хлорэтил/-тиазола, который идентичен во всех отношениях продукту примера 6.
Пример 8. Работают по методике примера 7 с тем исключением, что вместо бутилацетата используют абсолютный этанол. После окончания реакции смесь выпаривают в вакууме и прибавляют к остатку воду и 20%-ный раствор гидроксида натрия до величины рН 7. Затем работают по методике примера 7. Получают 17 г (62%) 2-хлор-4-метил-5-/2-хлорэтил/-тиазола, который идентичен во всех отношениях продукту примера 6.
Пример 9. Работают по методике примера 6 с той разницей, что вместо этилацетата используют диизопропиловый эфир. Получают 14 г (74%) 2-хлор-4-метил-5-/2-хлорметил/-тиазола, который идентичен во всех отношениях продукту примера 6.
Пример 10. Работают по методике примера 8 с той разницей, что вместо абсолютного этанола используют ледяную уксусную кислоту. Получают 20,2 г (73,5%) 2-хлор-4-метил-5-/2-хлорэтил/-тиазола, который идентичен во всех отношениях продукту примера 6.
Пример 11. Работают по методике примера 6 с той разницей, что вместо этилацетата используют четыреххлористый углерод. Получают 12 г (61%) 2-хлор-4-метил-5-/2-хлорэтил/-тиазола, который идентичен во всех отношениях продукту примера 6.
Пример 12. Прибавляют 355,5 г (2 моль) перегнанного 3-тиоцианато-5-хлор-пентанона к 360 см3 85%-ной фосфорной кислоты при перемешивании. Повышают температуру реакционной смеси до 95oC на водяной бане в течение примерно 1 ч, а затем перемешивают 1,5 ч при температуре между 95 и 100oC. Коричневый раствор охлаждают до 20oC и выливают в 660 см3 воды. После 1,5 ч перемешивания отфильтровывают выпавшие в осадок бежевые кристаллы, промывают до нейтральной реакции водой и сушат в вакууме при 60oC. Получают 337 г (95%) светло-бежевых кристаллов 2-окси-4-метил-5-/2-хлорэтил/-тиазола, т. пл. 151-152oC. После перекристаллизации из бензола точка плавления равна 157-158oC.
Анализ для C6H8ClNOS:
Вычислено, %: C 40,56; H 4,53; N 7,88; S 18,04; Cl 19,95;
Найдено, %: C 40,74; H 4,52; N 7,57; S 17,94; Cl 19,68.
Структура соединения подтверждена также данными ИК и ЯМР-спектров.
Пример 13. Работают по методике примера 12, используя неперегнанный 3-тиоцианато-5-хлор-2-пентанон (содержание 80% по данным газовой хроматографии). Получают 234 г (66%) 2-окси-4-метил-5-/2-хлорэтил/-тиазола, который плавится при 141-146oC.
Пример 14. Суспензию 177,6 г (1 моль) 2-окси-4-метил-5-/2-хлорэтил/-тиазола в 530 см3 безводного хлорбензола нагревают при перемешивании до 100oC. Вливают в раствор 306,6 г (2 моль) фосфорилхлорида в течение 30 мин, затем перемешивают при 125-130oC до тех пор, пока не прекратиться выделение хлористого водорода (около 2 ч). Реакционную смесь охлаждают до 20oC, затем ее выливают на 1,5 кг льда. Разделяют фазы, водную фазу дважды экстрагируют 200 см3 хлорбензола каждый раз. Объединенные фазы, содержащие хлорбензол, промывают не содержащей кислоты водой, а затем 5%-ным раствором бикарбоната натрия и выпаривают при пониженном давлении. Коричневый остаток фракционируют в вакууме. Получают 145 г (74%) 2-хлор-4-метил-5-/2-хлорэтил/-тиазола. Точка кипения равна 102oC при давлении 53,2 Па, n
Чистота: 99,4% (по данным газовой хроматографии).
Анализ для C6H7Cl2NS:
Вычислено, %: C 36,70; H 3,59; N 7,14; Cl 36,15; S 16,35;
Найдено, %: C 36,98; H 3,68; N 7,28; Cl 35,70; S 16,05.
Структура соединения также подтверждается данными ИК в ЯМР-спектров.
Пример 15. К раствору 63 г (0,32 моль) 2-хлор-4-метил-5-/2-хлорэтил/-тиазола в 630 см3 96%-ного этанола прибавляют 9 г влажного катализатора палладия на угле (содержание палладия 8%). Смесь гидрируют при атмосферном давлении. Окончание реакции определяется по прекращению поглощения водорода. После фильтрации катализатора раствор выпаривают, остаток растворяют в воде и раствор нейтрализуют бикарбонатом натрия (рН 7). Отделившееся масло встряхивают с хлороформом. Остаток после выпаривания хлороформного раствора разгоняют при пониженном давлении. Получают 47 г (91%) 4-метил-5-/2-хлорэтил/-тиазола. Его точка кипения равна 105oC при давлении 0,93 кПа, n
ИК- и ЯМР - спектры продукта идентичны для таковых аутентичного образца.
Пример 16. Работают по методике примера 15 с той разницей, то гидрирование проводят при давлении 0,3 МПа.
Получают 46,5 г (90%) 4-метил-5-/2-хлорэтил/-тиазола, который во всех отношениях идентичен продукту примера 15.
Пример 17. Работают по методике примера 15 с той разницей, что вместо этанола используют метанол.
Получают 42,9 г (83%) 4-метил-5-/2-хлорэтил/-тиазола, который идентичен во всех отношениях продукту примера 15.
Пример 18. Работа по методике примера 15 с той разницей, что после выпаривания отделяют твердый остаток.
Получают 61,5 г (97%) 4-метил-5-/2-хлорэтил/-тиазола гидрохлорида. После перекристаллизации из безводного этанола его точка плавления равна 136-137oC.
Анализ для C6H9Cl2NS:
Вычислено, %: C 36,37; H 4,58; N 7,07; Cl 35,79;
Найдено, %: C 36,18; H 4,52; N 7,10; Cl 35,89.
Пример 19. Работа по методике примера 15 с той разницей, что к раствору, полученному после фильтрации катализатора прибавляют ацетон и отфильтровывают выпавшее в осадок твердое вещество.
Получают 59,4 г (93,7%) 4-метил-5-/2-хлорэтил/-тиазола гидрохлорида. Его точка плавления равна 137-137,5o после перекристаллизации из безводного этанола.
Анализ для C6H9Cl2NS:
Вычислено, %: C 36,37; H 3,59; N 4,58; Cl 35,79;
Найдено, %: C 36,17; H 4,51; N 7,12; Cl 35,89.
Пример 20. Работают по методике примера 15 с той разницей, что прибавляют 9 г катализатора палладия на угле, содержащего селен. Этот катализатор был приготовлен согласно примеру 5 заявки РСТ, опубликованной под N WO-89/02429 (с. 12).
Получают 46,2 г (89,4%) 4-метил-5-/2-хлорэтил/-тиазола, который идентичен продукту примера 15 в отношении физических констант и содержания активного агента.
Пример 21. Прибавляют 83 г (1,024 моль) роданида натрия к раствору 155, 5 г (1 моль) 3,5-дихлор-2-пентанона в 1 л бутилацетата. Суспензию перемешивают 4 ч на горячей водяной бане. После охлаждения отфильтровывают образовавший хлористый натрий и фильтрат 3 раза промывают водой. После сушки над сульфатом натрия отгоняют бутилацетат.
Получают 168 (94%) 3-тиоцианато-5-хлор-2-пентанона в виде красного масла. После разгонки этот продукт идентичен продукту примера 1.
Пример 22. Прибавляют 83 г (1,024 моль) роданида натрия к раствору 155,5 г (1 моль) 3,5-дихлор-2-пентанона в 1 л бутилацетата. Суспензию перемешивают 4 ч на горячей водяной бане. После охлаждения отфильтровывают образовавшийся хлористый натрий, промывают фильтрат 3 раза водой и сушат над сульфатом натрия. После отфильтровывания осушающего агента светло-красно-коричневый фильтрат охлаждают до 10oC ледяной водой и насыщают газообразным хлористым водородом при перемешивании, поддерживая температуру 10oC. После насыщения реакционную смесь перемешивают еще 20 мин при охлаждении, затем медленно повышают температуру до 40oС. Реакционную смесь перемешивают 20 мин при этой температуре и выливают на лед после охлаждения до комнатной температуры. Разделяют фазы, водную фазу встряхивают со 150 см3 бутилацетата. Объединенные бутилацетатные растворы промывают до нейтральной реакции водой и 5%-ным раствором бикарбоната натрия, затем сушат над сульфатом натрия. После отгонки растворителя остаток разгоняют при пониженном давлении, получают 121 г (66%) 2-хлор-4-метил-5-/2-хлорэтил/-тиазола в виде светло-желтого масла, которое идентично во всех отношениях продукту примера 1.
Пример 23. Работают по методике примера 1, используя 8,45 г (0, 05 моль) 3,5-дихлор-2-гексанона, 5 г роданида калия и 50 см3 ацетона.
Получают 8,9 г (93%) 3-тиоцианато-5-хлор-2-гексанона. После разгонки при пониженном давлении он представляет собой светло-желтое масло, его точка кипения равна 107-108oC при давлении 53,3 Па, n
Согласно данным ИК-спектра продукт не содержит изотиоцианата.
Анализ для C7H10ClNS:
Вычислено, %: C 43,82; H 5,25; N 7,30; Cl 18,50; S 16,72;
Найдено, %: C 43,57; H 5,96; N 7,61; Cl 18,36; S 16,58.
Пример 24. Работают по методике примера 1, используя 18,3 г (0,1 моль) 3,5-дихлор-2-гептаанона, 10 г (0,102 моль) роданида калия и 100 см3 ацетона.
Получают 19,1 (93%) 3-тиоцианато-5-хлор-2-гептанона. После разгонки при пониженном давлении он представляет собой светло-желтое масло, его точка кипения равна 124oC при давлении 53,3 Па, n
Согласно данным ИК-спектра продукт не содержит изотиоцианата.
Анализ для C8H12ClNOS:
Вычислено, %: C 46,70; H 5,88; N 6,80; Cl 17,23; S 15,53;
Найдено, %: C 46,93; H 5,69; N 6,68; Cl 16,87; S 13,37.
Пример 25. Работают по методике примера 7, используя 9,6 г (0,05 моль) 3-тиоцианато-5-хлор-2-гексанона и 55 см3 бутилацетата.
Получают 7,7 г (80%) 2-хлор-4-метил-5-/2-хлорпропил/-тиазола в виде бесцветной жидкости. Ее точка кипения равна 96oC при 66,6 Па, n
Анализ для C7H9Cl2NS:
Вычислено, %: С 40,00; H 4,31; N 6,66; Cl 33,74; S 15,26;
Найдено, %: C 39,75; H 4,24; N 6,70; Cl 33,68; S 14,83.
Структура соединения подтверждена данными ИК- и ЯМР-спектров.
Пример 26. Работают по методике примера 7, используя 10,25 г (0,05 моль) 3-тиоцианато-5-хлор-2-гептанона и 55 см3 бутилацетата.
Получают 8,9 г (79,5%) 2-хлор-4-метил-5-/2-хлорбутил/-тиазола в виде бесцветной жидкости. Ее точка кипения равна 108oC при давлении 53,2 Па, n
Анализ для C8H11Cl2NS:
Вычислено, %: C 42,86; H 4,94; N 6,28; Cl 31,63; S 14,30;
Найдено, %: C 43,07; H 4,79; N 6,13; Cl 31,33; S 14,20.
Структура соединения подтверждена данными ИК- и ЯМР-спектров.
Пример 27. Работают по методике примера 15, используя 7 г (0,033 моль) 2-хлор-4-метил-5-/2-хлорпропил/-тиазола, 60 см3 96%-ного этанола и 1 г влажного палладия на угле в качестве катализатора (содержание палладия 8%).
Получают 5 г (86%) 4-метил-5-/2-хлорпропил/-тиазола в виде бесцветной жидкости. Ее точка кипения равна 78oC при давлении 40 Па, n
Анализ для C7H10ClNS:
Вычислено, %: С 47,30; H 5,73; N 7,97; Cl 20,17; S 18,24;
Найдено, %: C 47,53; H 5,25; N 7,63; Cl 20,46; S 18,18.
Структура соединения подтверждается данными ИК- и ЯМР-спектров.
Пример 28. Работают по методике примера 15, используя 5,3 г (0,024 моль) 2-хлор-4-метил-5-/2-хлорбутил/-тиазола, 50 см3 96%-ного этанола и 0,9 г влажного катализатора палладия на угле (содержание палладия 8%).
Получают 3,7 г (81%) 4-метил-5-/2-хлорбутил/-тиазола в виде бесцветной жидкости. Ее точка кипения равна 94oC при давлении 66,5 Па, n
Анализ для C8H12ClNS:
Вычислено, %: C 50,64; H 6,37; N 7,38; Cl 18,69; S 16,90;
Найдено, %: C 49,98; H 6,21; N 7,12; Cl 18,20; S 17,08.
Структура соединения подтверждается данными ИК- и ЯМР-спектров.
Пример 29. Работает по методике примера 12, используя 15,3 г (0,05 моль) 3-тиоцианато-5-хлор-2-гексанона и 16 см3 83%-ной фосфорной кислоты.
Получают 11,2 г (73%) 2-окси-4-метил-5-/2-хлорпропил/-тиазола, который плавится при 91-93oC.
Анализ для C7H10ClNOS:
Вычислено, %: C 43,85; H 5,25; N 7,30; Cl 18,48; S 16,72;
Найдено, %: C 43,52; H 5,12; N 7,05; Cl 18,50; S 16,82.
Структура соединения подтверждается данными ИК- и ЯМР-спектров.
Пример 30. Работают по методике примера 12, используя 13,3 г (0,064 моль) 3-тиоцианато-5-хлор-2-гептанона и 14 см3 85%-ной фосфорной кислоты.
Получают 9,5 г (71,5%) 2-окси-4-метил-5-/2-хлорбутил/-тиазола, который плавится при 84-85oC.
Анализ для C8H12ClNOS:
Вычислено, %: C 46,70; H 5,88; N 6,80; Cl 17,23; S 15,58;
Найдено, %: C 46,04; H 5,61; N 6,20; Cl 16,98; S 15,30.
Структура соединения подтверждается данными ИК- и ЯМР-спектров.
Пример 31. Работают по методике примера 14, используя 9,7 г (0,05 моль) 2-окси-4-метил-5-/2-хлорпропил/-тиазола, 15,3 г (0,1 моль) фосфорилхлорида и 26 см3 безводного хлорбензола.
Получают 8,4 г (83,3%) 2-хлор-4-метил-5-/2-хлорпропил/-тиазола в виде бесцветной жидкости. Ее точка кипения равна 102oC при давлении 80 Па, n
Анализ для C7H9Cl2NS:
Вычислено, %: C 40,00; H 4,31; N 6,66; Cl 33,74; S 15,26;
Найдено, %: C 39,85; H 4,35; N 6,76; Cl 33,65; S 14,95.
Структура соединения подтверждается данными ИК- и ЯМР-спектров.
Пример 32. Работают по методике примера 14, используя 7,4 г (0,036 моль) 2-окси-4-метил/-5-/2-хлорбутил/-тиазола, 11 г (0,072 моль) фосфорилхлорида и 19 см3 безводного хлорбензола.
Получают 6,7 г (83,3%) 2-хлор-4-метил-5-/2-хлорбутил/-тиазола в виде бесцветного масла. Его точка кипения равна 108oC при давлении 53,2 Па, α = 1,5352.
Анализ для C8H11Cl2NS:
Вычислено, %: С 42,86; H 4,94; N 6,28; Cl 31,63; S 14,30;
Найдено, %: C 42,98; H 4,81; N 6,21; Cl 31,44; S 14,20.
Структура соединения подтверждается данными ИК- и ЯМР-спектров.
Получение других исходных материалов.
Пример 1. 3,5-дихлоргексанон.
Смесь 17,7 г (0,1 моль) α-хлор-альфа-ацето-гамма-валеролактона (полученного согласно J. Am. Chem. Soc. 67, 398, 1945) и 35 см3 абс.соляной кислоты медленно нагревают до 90oC при перемешивании и перемешивают при этой температуре до тех пор, пока не прекратится образование газа. После охлаждения темный раствор выливают в 100 см3 воды, отделившееся масло экстрагируют хлороформом. Раствор, содержащий хлороформ, промывают 50 см3 5-%-ного раствора бикарбоната натрия. После выпаривания оставшееся масло разгоняют в вакууме. Получают 5 г (30%) 3,5-дихлор-2-гексанона в виде бесцветной жидкости. Точка кипения равна 38oC при давлении 26,6 Па.
Анализ для C6H10Cl2O:
Вычислено, %: C 42,62; H 5,96; Cl 41,94;
Найдено, %: C 42,77; H 5,76; Cl 41,50.
Структура соединения подтверждается данными ИК- и ЯМР-спектров.
Пример 2. 3,5-дихлор-2-гептанон.
а/ Альфа-хлор-альфа-ацетил-гамма-этил-γ-бутиролактон.
В раствор 58,2 г (0,37 моль) α-ацетил-гамма-этил-α-бутиролактона (полученного согласно J. Pharm. Sci. 52, 733, 1963) в 60 см3 бензола прибавляют по каплям при перемешивании и охлаждении 50 г (0,37 моль) сульфурилхлорида в течение 2 ч, поддерживая температуру реакционной смеси между 5 и 10oC. После окончания прибавления реакционой смеси дают нагреться до комнатной температуры и перемешивают при этой температуре до тех пор, пока не прекратится выделение газа. Затем ее выливают в 400 см3 воды, разделяют фазы и воду экстрагируют 200 см3 бензола. Раствор, содержащий бензол, промывают 100 см3 5%-ного раствора бикарбоната натрия. После выпаривания оставшееся масло разгоняют в вакууме. Целевое соединение получают в виде бесцветной жидкости в количестве 58,9 г (82,5%), ее точка кипения равна 91oC при давлении 80 Па, γ = 1,4623.
Анализ для C8H11ClO3:
Вычислено, %: C 50,40; H 5,81; Cl 18,60;
Найдено, %: C 50,63; H 5,55; Cl 18,84.
б/ 3,5-Дихлор-2-гептанон.
Получают целевое соединение по способу, описанному в примере 1, исходя из 49 г (0,26 моль) альфа-хлор-альфа-ацетил-гамма-этил-гамма-бутиролактона и 98 см3 абс.соляной кислоты. После разгонки получают 22 г (47%) целевого соединения. Его точка кипения равна 68-70oC при давлении 133,3 Па, γ = 1,4600.
Анализ для С7H12Cl2O:
Вычислено, %: C 45,91; H 6,60; Cl 38,73;
Найдено, %: C 45,66; H 6,55; Cl 38,90.
Изобретение относится к способу получения производных тиазола и их солей присоединения кислот формулы 1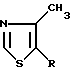 (I)
(I)
где R - C2-5 - алкил с прямой цепью, замещенный атомом хлора в положении 2, заключающемуся во взаимодействии 3,5-дихлор-2-алканона формулы V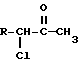 (V)
(V)
с неорганическим тиоцианатом, полученный 3-тиоцианато-5-хлор - 2-алканон формулы IV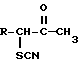 (IV)
(IV)
превращают в 2-хлор-4-метил-5-(2-хлоралкил)-тиазол формулы II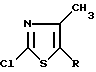 (II)
(II)
реакцией с газообразным хлористым водородом в органическом растворителе, гидрируют соединение (II) в присутствии металлического катализатора в органическом растворителе. 3 с. и 11 з. п. ф-лы.

где R С2 С5-алкил с прямой цепью, замещенный атомом хлора в положении 2,
или их солей присоединения кислот, отличающийся тем, что проводят взаимодействие 5-хлор-3-тиоцианато -2-алканона общей формулы IV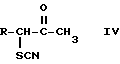
в органическом растворителе с газообразным хлористым водородом, чтобы получить 2-хлор-4-метил-5-(2 -хлоралкил)-тиазол общей формулы II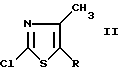
а затем гидрируют соединение общей формулы II в присутствии металлического катализатора в органическом растворителе, чтобы получить 4-метил-5-(2-хлоралкил)-тиазол общей формулы I, где R имеет указанные значения, и необязательно превращают соединение общей формулы I, где R имеет указанные значения, или его гидрохлоридную соль известным вообще способом в другую соль присоединения кислоты, или выделяют свободное соединение общей формулы I, где R имеет указанные значения, из его соли присоединения кислоты.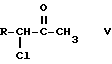
где R имеет указанные значения,
с неорганическим тиоцианатом и без выделения из реакционной смеси вводят во взаимодействие на следующей стадии по п. 1.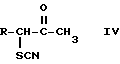
где R С2 С5-алкил с прямой цепью, замещенный атомом хлора в 2-положении.
с неорганическим тиоцианатом.
| US, патент, 3639415, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1998-01-27—Публикация
1992-10-30—Подача