Изобретение относится к новым фенилгидразиновым производным, обладающим инсектицидной, акарицидной и нематоцидной активностью.
Кроме того, изобретение относится к инсектицидным, акарицидным или нематоцидным композициям, содержащим указанные соединения, а также к способам борьбы с насекомыми, клещами и нематодами путем использования вышеупомянутых соединений или композиций.
Поражение культурных растений насекомыми, клещами и нематодами представляет серьезную проблему для сельского хозяйства. В защите от поражения нематодами, клещами и насекомыми нуждаются многие полевые культурные растения, например, такие, как соя, кукуруза, арахис, хлопок, люцерна, рис и табак.
Кроме того, в защите от поражения указанными вредителями нуждаются овощные растения, такие, как томаты, картофель, сахарная свекла, морковь, горох и т. п. , а также плодовые, орехоплодные, декоративные и семенные культуры, например, такие как яблони, персиковые деревья, миндаль, цитрусовые деревья и виноград.
Поэтому разработка новых эффективных пестицидов, включая инсектициды, акарициды и нематоциды, является в настоящее время особо актуальной.
При этом основные усилия ученых направлены, в частности, на разработку таких пестицидов, которые обладали бы как овицидной, так и ларвицидной активностью.
Известны алкилфенилгидразинкарбоксилаты, предназначенные для использования в качестве акарицидов (Chemical Abstracts 108(19): 163280d).
Были раскрыты замещенные фенилгидразины и фенилоксадиазолиноны, предназначенные для использования в качестве пестицидов (патент США 4725302).
Известны 7-замещенные 2,3-дигидробензофураны, предназначенные для использования в качестве пестицидов или промежуточных химических соединений (европатент 006747). Описаны арилгидразиды трифторуксусной кислоты, обладающие фунгицидной, бактерицидной, акарицидной и антисептической активностью ("Дервент", реферат 88-312695/44).
Были описаны также различные фенилгидразины, которые обладают активностью против насекомых и клещей (Chemical Abstracts 102(17): 152686 c).
Известны нитро-дифениловые эфиры гидразина, обладающие гербицидной активностью (заявка Франции 2440943).
Изобретение относится к соединению, имеющему структурную формулу I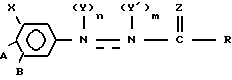
где простая или двойная связь;
простая или двойная связь;
Y'- водород;
n и m - независимо 1 или 0;
A и B - водород или группа формулы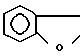
Y - H, C1-C4-алканоил, C1-C4-галогеналканоил, C1-C4-диалкоксифосфорил, C1-C4-алкиламинокарбонил, галогено-(C1-C4)-алкилсульфонил, C1-C4-алкоксикарбонил;
R- H, C1-C6-алкил, C1-C6-алкокси, C3-C6-циклоалкокси, галогено-(C1-C6)алкил, C1-C6-алкокси-(C1-C6)-алкил, фенил-(C1-C6)-алкокси, C2-C6-алкенил, C1-C6-алкилтио, C1-C6-алкоксикарбонил, C1-C6-алкиламино, фурил, тиенил, фенил-(C1-C6)алкил, галогено-(C1-C6)-алкокси, фенилокси-C3-C6-циклоалкил;
Z - O или S, при условии, что, если X - фенил, то R не является алкиламино-группой или C1-C6-алкоксикарбонилом; при условии, что n и m всегда равны 0, когда 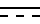 означает двойную связь; при условии, что, когда A и B - водород, X означает: a) фенил, низшую фенилалкокси-группу, фенокси-группу или бензил, причем фенильное кольцо каждого указанного заместителя может быть замещено галогеном, низшим алкилом, низшей алкоксигруппой, либо b) один заместитель из группы (a) - фенил, а второй выбран из C1-C4-алкокси, галогена, C1-C4-алкила и C1-C4-алкилтиогруппы, либо, когда A и B отличны от водорода, X - водород или низший алкокси.
означает двойную связь; при условии, что, когда A и B - водород, X означает: a) фенил, низшую фенилалкокси-группу, фенокси-группу или бензил, причем фенильное кольцо каждого указанного заместителя может быть замещено галогеном, низшим алкилом, низшей алкоксигруппой, либо b) один заместитель из группы (a) - фенил, а второй выбран из C1-C4-алкокси, галогена, C1-C4-алкила и C1-C4-алкилтиогруппы, либо, когда A и B отличны от водорода, X - водород или низший алкокси.
Изобретение относится также к инсектоакарицидонематоцидным композициям, содержащим в качестве активного ингредиента соединение общей формулы I и приемлемый носитель.
Изобретение также относится к способу борьбы с вредителями культурных растений, такими, как насекомые клещи или нематоды, который заключается в том, что места, нуждающиеся в защите от поражения указанными вредителями, обрабатывают эффективным количеством соединения формулы I.
Предлагаемые соединения имеют структурную формулу I, определенную выше. Предпочтительными являются соединения, у которых Y является водородом или COCF3.
Соединения формулы I могут быть получены посредством реакции замещенного фенилгидразина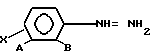
с ацилирующим агентом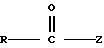
где Z является галогеном или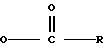
и эквивалентом акцептора HCl таким, как пиридин, в растворителе, таком, как толуол. Продукт этой реакции может быть затем ацилирован или подвергнут окислению с использованием окисляющего агента, такого, как Pd/воздух.
Композиции по изобретению включают в себя: а) соединение, имеющее структурную формулу I; b) соответствующий носитель. Этот носитель может быть твердым или жидким.
Примерами подходящих жидких носителей могут служить вода, спирты, кетоны, фенолы, толуол и ксилол. В целях облегчения транспортировки и применения конечных композиций в их состав могут быть включены различные добавки, которые обычно используются в таких случаях, например одно или несколько поверхностно-активных веществ (ПАВ) и/или инертные разбавители.
Альтернативно указанные пестицидные композиции могут содержать твердые носители и изготавливаться в виде дустов, гранул, смачиваемых порошков, паст, аэрозолей, эмульсий, эмульгируемых концентратов и водорастворимых твердых продуктов.
Например, пестицидные соединения по изобретению могут быть использованы в виде дустов, которые после смешивания с порошкообразными твердыми носителями (или абсорбирования на этих носителях), такими, как минеральные силикаты, например слюда, тальк, пирофиллит, и глины, а также с поверхностно - активным диспергирующим агентом, образуют смачиваемый порошок, который может быть затем непосредственно нанесен на целевые участки.
Альтернативно порошкообразный твердый носитель, содержащий смешанное с ним соединение, может быть диспергирован в воде с образованием суспензии, которая может быть использована непосредственно по назначению.
Гранулированные композиции, содержащие указанные выше соединения и предназначенные для внесения разбрасыванием междурядного внесения, введения в почву и протравливания семян, изготавливают предпочтительно с использованием носителя в гранулированной или пеллетированной форме, например, такого, как гранулированная глина, вермикулит, уголь или стержни кукурузных початков.
Альтернативно при использовании жидких носителей пестицидные соединения могут быть введены в жидкости или растворы для разбрызгивания, например в растворы, содержащие совместный с данным соединением растворитель, такой, как ацетон, бензол, толуол, или керосин, либо указанные соединения могут быть диспергированы в нерастворяющей среде, например в воде.
Для другого способа внесения пестицидных композиций, например, такого, как аэрозольная обработка, активное соединение может быть растворено в аэрозольном носителе, который при повышенном давлении является жидкостью, а при атмосферном давлении и нормальной температуре, например 20oC, является газом.
Аэрозольные композиции могут быть также получены сначала путем растворения соединения в менее летучем растворителе, а затем путем смешивания полученного раствора с более летучим жидким аэрозольным носителем.
Для пестицидной обработки растений (понятие "растение" также включает в себя части растения) соединения по изобретению предпочтительно вводят в водные эмульсии, содержащие поверхностно - активный диспергирующий агент, который может быть неионогенным, катионогенным или анионогенным.
Подходящими поверхностно-активными агентами являются известные соединения, например, такие, как соединения, описанные в патенте США 2547724 (столбцы 3 и 4).
Соединения по изобретению могут быть смешаны с указанными поверхностно - активными диспергирующими агентами в присутствии или в отсутствие органического растворителя, в результате чего могут быть получены концентраты, которые после добавления воды образуют водные суспензии предлагаемых соединений в нужной концентрации.
Кроме того, соединения по изобретению могут быть использованы в сочетании с носителями, которые сами по себе обладают пестицидной активностью, например инсектицидной, акарицидной, фунгицидной, или бактерицидной активностью.
Следует отметить, что количество пестицидов активного соединения в данной композиции будет зависеть от конкретного вредителя, от конкретной композиции и ее состава, от способа нанесения соединения/композиции и от конкретно обрабатываемого участка, а поэтому пестицидно эффективное количество активного соединения может широко варьироваться.
Однако, в основном, концентрация соединения, используемого в качестве активного ингредиента в пестицидно-эффективных композициях, может заключаться в пределах от около 0,1 до около 95 мас.%.
Разведения для разбрызгивания могут составлять лишь несколько частей на миллион, хотя, с другой стороны, при помощи методики для сверхмалых объемов могут быть с успехом использованы высококонцентрированные составы соединения по изобретению.
Если участками обработки являются сами растения, то концентрация на единицу площади может составлять от около 0,01 до около 50 фунтов на акр, причем для таких культурных растений, как кукуруза, табак, рис и т.п., предпочтительно использовать концентрации от около 0,1 до около 10 фунтов на акр.
Для борьбы с насекомыми растворы для разбрызгивания соединений могут быть нанесены непосредственно на самих вредителей или на растения, которыми они питаются или на которых они гнездятся. Указанные пестицидные активные композиции могут быть также введены в почву или в другую среду, в которой обитают вредители.
Вредные насекомые, нематоды и клещи поражают широкий ряд растений, включая декоративные и сельскохозяйственные культуры, и причиняют значительный ущерб этим растениям путем поедания их корней и/или листьев, высасывания жизненных соков растения, выделения токсинов, а также часто путем переноса на эти растения различных заболеваний.
Предлагаемые соединения могут быть предпочтительно использованы для минимизации или предупреждения указанных повреждений, причиняемых растениям вредителями.
Конкретные способы применения, а также выбор и концентрация указанных соединений в значительной степени зависят от географического региона, климата, топографии местности, толерантности растения и т.п.
В каждом конкретном случае любой специалист может легко выбрать подходящее соединение и определить концентрацию этого соединения и способ его введения путем обычного экспериментирования.
Особенно предпочтительным является использование предлагаемых соединений в качестве инсектицидов, нематоцидов и акарицидов путем опрыскивания листьев и/или обработки почвы.
Для более наглядной иллюстрации изобретения ниже приводятся конкретные примеры, которые, однако, не должны рассматриваться, как некое ограничение объема и сущности данного изобретения.
Пример 1. Получение (4-метокси- [1,1'-бифенил]-3-ил)гидразина гидрохлорида (промежуточное химическое соединение).
К 25 г 5-фенил-0-анизидина добавляли 250 мл воды и 450 мл концентрированной соляной кислоты и размешанный раствор охлаждали до 0oC.
Затем, поддерживая температуру 0oC, по капле добавляли 8,6 г нитрита натрия в 20 мл воды. После этого добавления смесь размешивали в течение 1 ч при 0oC. К реакционной смеси добавляли раствор 113 г хлорида олова в 200 мл концентрированной HCl, охлажденной до -20oC, после чего смесь снова размешивали в течение 1 ч.
Затем смесь подвергали вакуумной фильтрации, а полученный твердый остаток оставляли на ночь для осушки. Этот твердый остаток растворяли в горячей воде, подвергали гравитационной фильтрации, а полученный фильтрат охлаждали на льду.
Образовавшиеся твердые кристаллы подвергали вакуумной фильтрации и продукт оставляли для осушки в течение ночи. В результате этой процедуры получали 26 г гидрохлорида (4-метокси-[1,1'-бифенил]-3-ил)гидразина.
Пример 2. Получение 2-(4-метокси-1,2-бифенил-3-ил)гидразина пропановой кислоты (соединение 18).
К 5 г продукта примера 1 добавляли 100 мл воды и 40 мл 10%-ного раствора гидроксида натрия. Полученную смесь перемешивали в течение часа при комнатной температуре. Затем эту смесь экстрагировали эфиром, а эфирный экстракт осушали сульфатом натрия в течение получаса.
После этого эфирный экстракт фильтровали и выпаривали при пониженном давлении, в результате чего получали 4,6 г промежуточного соединения - (4-метокси-[1,1'-бифенил]-3-ил)гидразина.
К 4,6 г вышеописанного промежуточного соединения добавляли 150 мл толуола и 1,58 г пиридина, полученный раствор перемешивали и охлаждали до 0oC. Затем к раствору по капле добавляли 1,84 г пропионилхлорида.
После добавления пропионилхлорида раствор перемешивали в течение часа при 0oC, а затем дважды промывали 100 мл воды.
Водные фракции осушали и экстрагировали толуолом. Толуоловые фракции, полученные в результате экстрагирования, объединяли и выпаривали при пониженном давлении.
Полученное твердое вещество промывали гексаном и фильтровали, в результате чего получали 3,4 г 2-(4-метокси-[1,1'-бифенил]-3-ил)гидразида пропановой кислоты.
Пример 3. Получение 2-(4-метокси-[1,1'-бифенил]-3-ил)-2-(трифтороацетил)гидразида пропановой кислоты (соединение 73).
К 2,25 г продукта примера 2 добавляли 150 мл метиленхлорида. Полученный раствор перемешивали и охлаждали до 0oC. Затем к раствору по капле добавляли 1,75 г ангидрида трифторуксусной кислоты, колбу закрывали, а реакционную смесь перемешивали в течение ночи.
После этого растворитель выпаривали при пониженном давлении и получали твердое вещество, которое промывали гексаном и фильтровали.
В результате этой процедуры получали конечный продукт: 2,7 г 2-(4-метокси-[1,1'-бифенил-3-ил)-2-(трифтороацетил)гидразида пропановой кислоты, т. пл. 126oC.
Пример 4. Получение (4-бромо-[1,1'-бифенил]-3-ил)гидразина гидрохлорида (промежуточное химическое соединение).
При перемешивании к 4 г 4-бромо-[1,1'-бифенил]-3-амина добавляли 25 мл воды и 50 мл концентрированной соляной кислоты.
Полученный раствор охлаждали до 0oC. Затем при температуре, равной 0oC, к раствору по капле добавляли раствор 1,1 г нитрита натрия в 6 мл воды. После завершения добавления смесь перемешивали при 0oC в течение часа.
После этого к реакционной смеси добавляли раствор 20 г хлорида олова в 20 мл концентрированной соляной кислоты, охлажденной до -20oC, и смесь снова перемешивали в течение часа.
Образовавшийся осадок подвергали вакуумной фильтрации и полученное твердое вещество оставляли для осушки в течение ночи. Таким образом получали конечный продукт: (4-бромо-[1,1'-бифенил] гидразина гидрохлорид, который использовали в последующих реакциях без дополнительной очистки.
Пример 5. Получение карбоксилата изопропил 2-(4-бромо-[1,1'-бифенил]-3-ил)гидразина (соединение 139)
К продукту примера 4 добавляли 100 мл 10-%-ного водного раствора гидроксида натрия и полученную смесь перемешивали 30 мин при 10oC. Затем эту смесь экстрагировали эфиром, осушали сульфатом натрия в течение 2 ч и выпаривали, в результате чего получали (4-бромо-[1,1'-бифенил]-3-ил)гидразин (3 г).
К 3 г вышеуказанного гидразина добавляли 100 мл толуола и 1,5 г пиридина. Полученную смесь охлаждали с использованием ледяной бани. После этого к смеси по капле добавляли 12 мл 1 М раствора изопропилхлороформата в толуоле.
После добавления изопропилхлороформата раствор оставляли для перемешивания в течение ночи при комнатной температуре.
Затем этот раствор дважды промывали (каждый раз 100 мл воды), осушали сульфатом натрия в течение 2 ч и выпаривали при пониженном давлении.
Образовавшийся твердый осадок промывали гексаном и перекристаллизовывали из толуола, в результате чего получали 3 г изопропил 2-(4-бромо-[1,1'-бифенил]-3-ил)гидразинкарбоксилата, т.пл. 107-108oC.
Пример 6. Получение изопропил (4-бромо-[1,1'-бифенил]-3-ил)диазонкарбоксилата (соединение 161)
К 1,7 г продукта примера 4 добавляли 100 мл толуола и 0,4 г палладированного угля. Полученную смесь перемешивали в течение ночи при комнатной температуре, а затем отфильтровывали и толуол выпаривали при пониженном давлении.
В результате этой процедуры получали 1,5 г карбоксилата изопропил (4-бромо-[1,1'-бифенил]-3-ил)диазона в виде красного маслообразного вещества.
Пример 7. Получение 2-метокси-3-дибензофуранилгидразина (промежуточное химическое соединение).
При перемешивании к 10 г 3-амино-2-метоксидибензофурана добавляли 100 мл воды и 50 мл концентрированной соляной кислоты. Полученный раствор охлаждали до 0oC.
После этого к раствору по капле добавляли раствор 3,5 г нитрита натрия в 15 мл воды, поддерживая при этом температуру 0oC. После завершения добавления смесь перемешивали в течение 1 ч при 0oC.
К реакционной смеси добавляли раствор 40 г хлорида олова в 50 мл концентрированной соляной кислоты, охлажденной до -20oC. Затем эту смесь перемешивали в течение часа.
Образовавшийся осадок подвергали вакуумной фильтрации и полученное твердое вещество добавляли к раствору 70 г гидроксида натрия в 500 мл воды, охлажденной в ледяной бане.
После этого смесь экстрагировали эфиром, осушали сульфатом натрия в течение 2 ч и выпаривали с получением твердого продукта. Этот твердый продукт промывали гексаном и получали 7 г 2-метокси-3-дибензофуранилгидразина, т. пл. 113-115oC.
Пример 8. Получение карбоксилата изопропил 2-((2-метокси-3-дибензофуранил)гидразина (соединение 141).
К 2,3 г продукта примера 7 добавляли 100 мл толуола и 1 г пиридина. Полученную смесь охлаждали в ледяной бане. После этого к смеси по капле добавляли 10 мл 1 М раствора изопропилхлороформата в толуоле. После добавления раствор оставляли для перемешивания в течение ночи при комнатной температуре.
Затем этот раствор дважды промывали (каждый раз 100 мл воды), осушали сульфатом натрия (в течение 2 ч) и выпаривали при пониженном давлении.
Образовавшийся твердый осадок промывали гексаном и перекристаллизовывали из толуола, в результате чего получали 2 г карбоксилата изопропил 2-2-метокси-3-дибензофуранил)гидразина, т.пл. 178oC.
Пример 9. Получение изопропил (2-метокси-3-дибензофуранил)диазонкарбоксилата (соединение 157).
К 1,4 г продукта примера 7 добавляли 100 мл толуола и 0,3 г палладированного угля. Полученную смесь перемешивали в течение ночи при комнатной температуре, фильтровали, а толуол выпаривали при пониженном давлении.
В результате этой процедуры получали 1,2 г карбоксилата изопропил (2-метокси-3-дибензофуранил)диазона в виде красного маслообразного вещества.
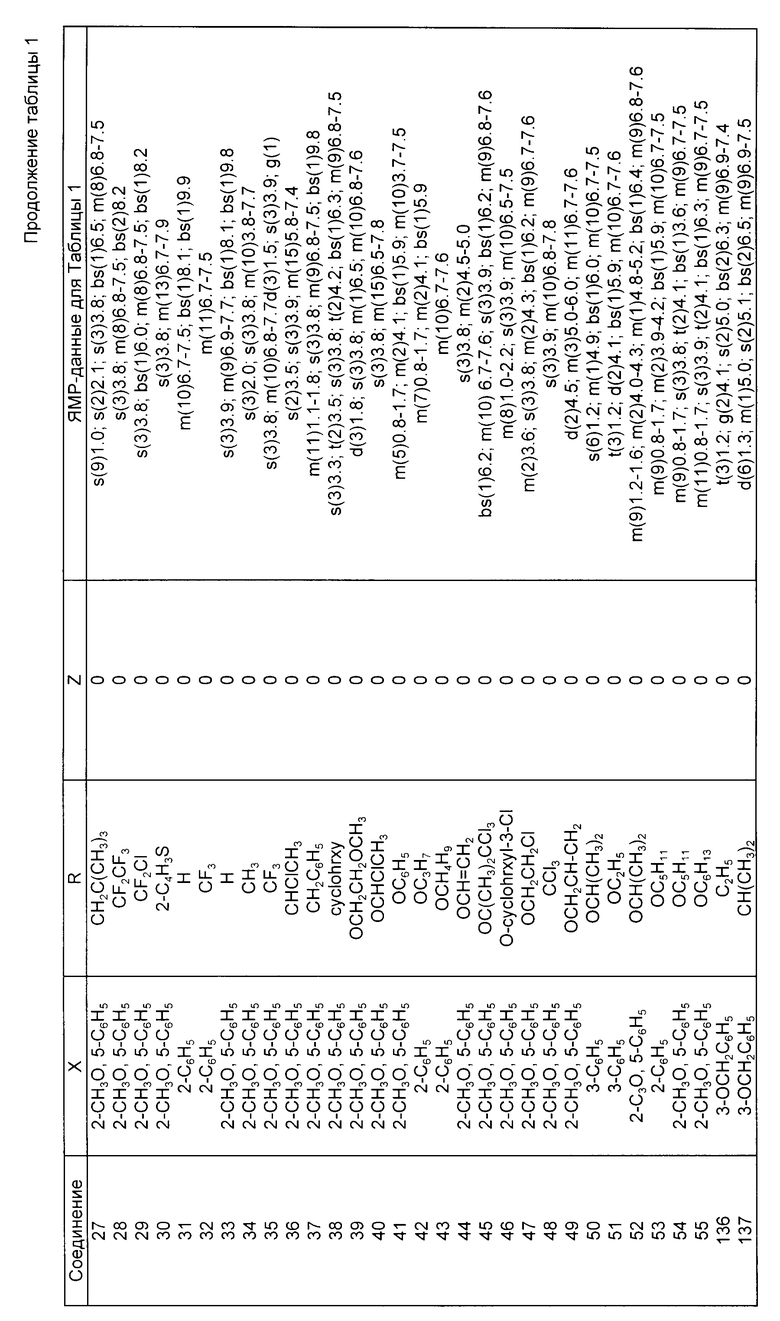
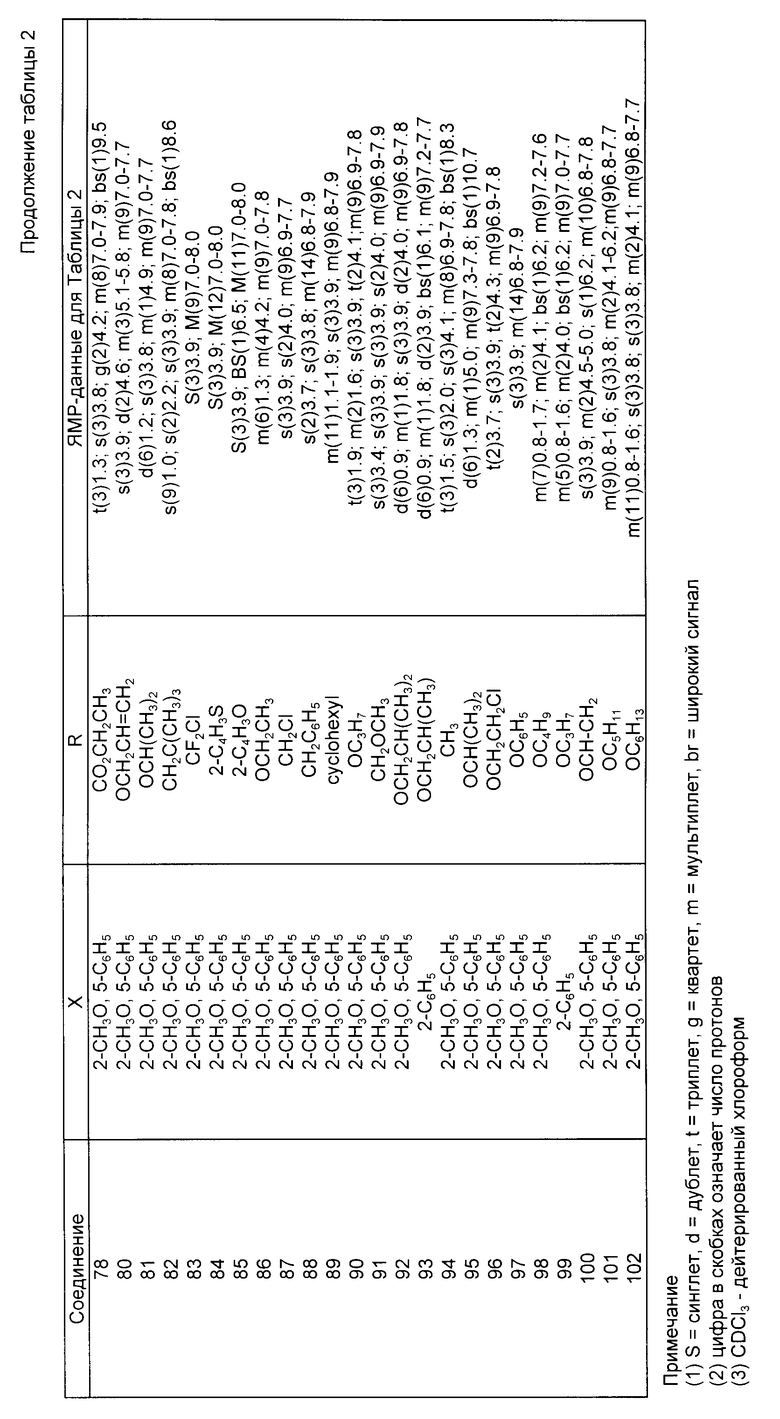
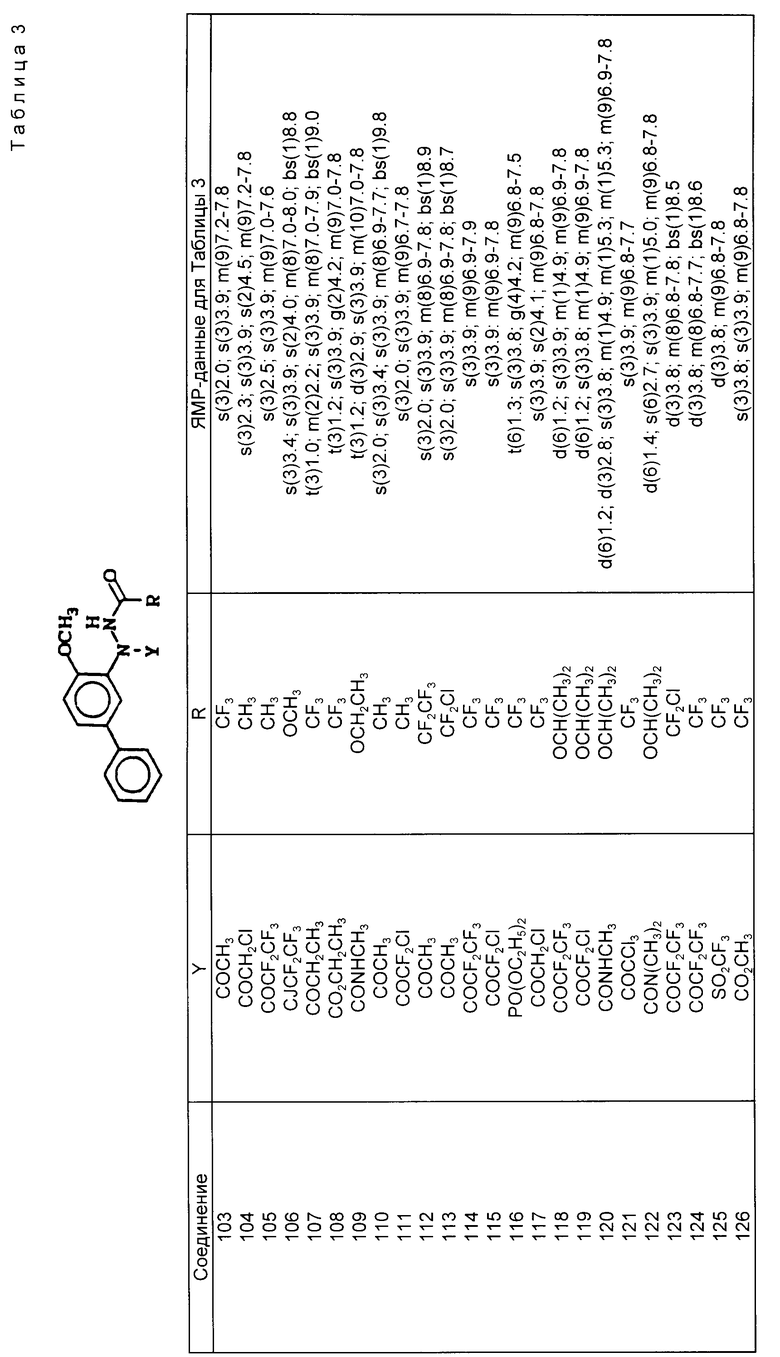
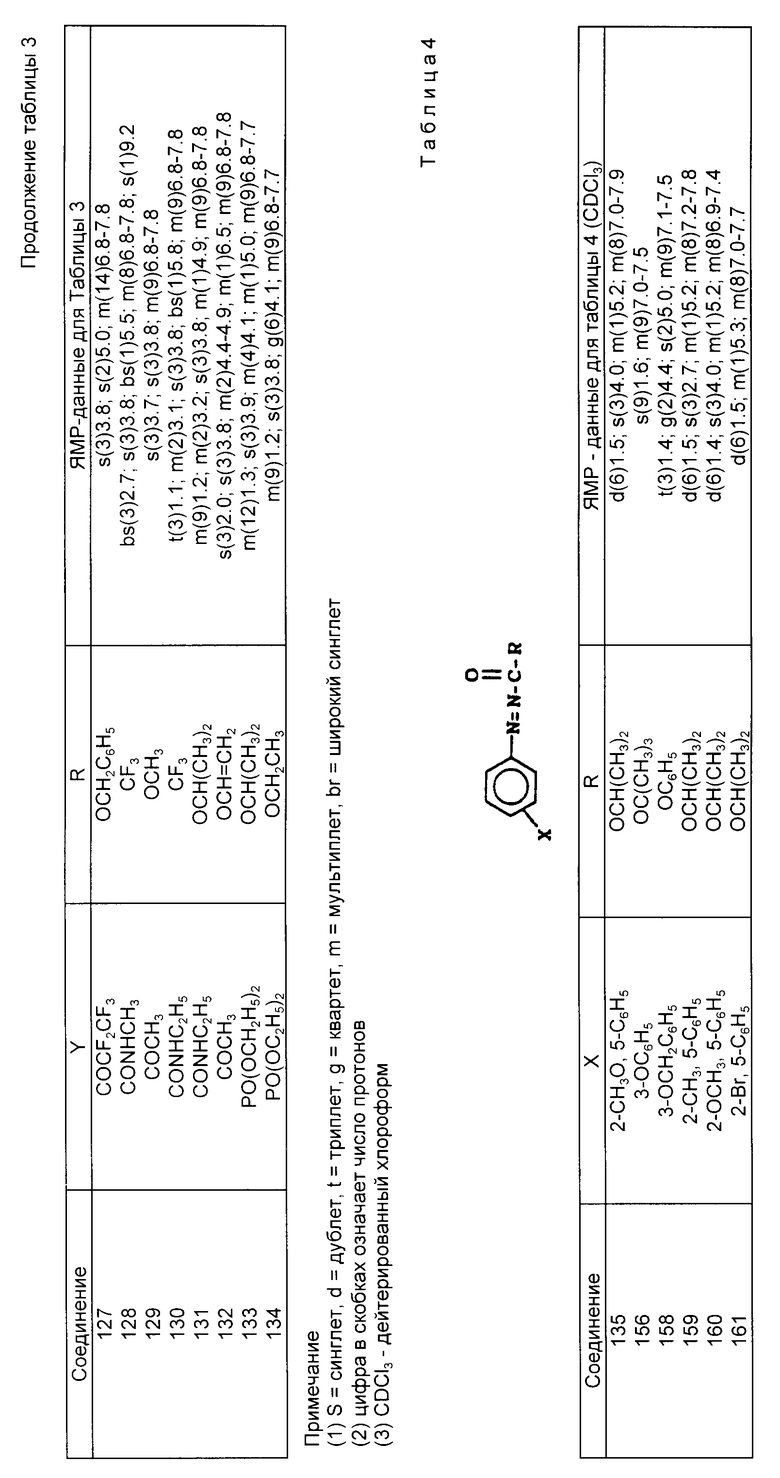
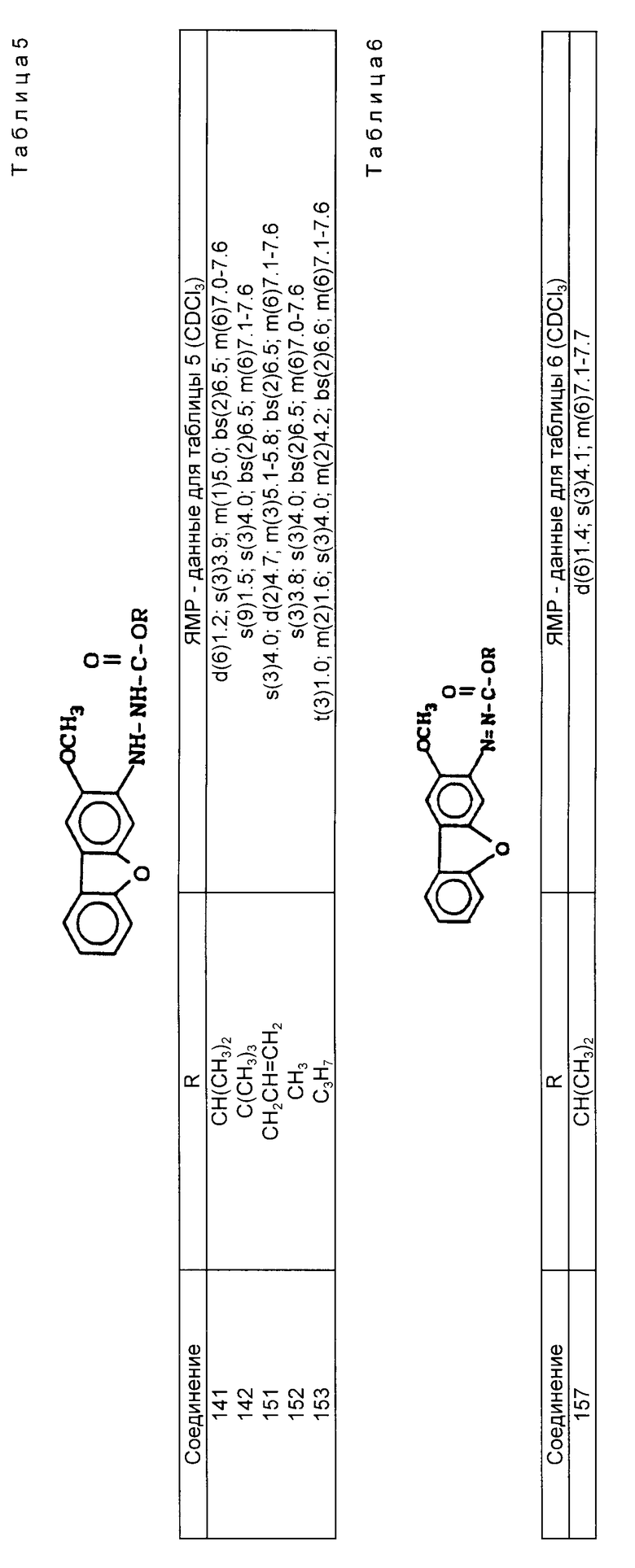
Соединения, систематизированные в табл. 1-6 (NN 1-161), были получены способами, в основном, аналогичными описанным в примерах, представленных выше.
Если исходные материалы не являются коммерчески доступными, то они могут быть синтезированы известными методами. Каждое из полученных таким образом соединений было проанализировано с помощью ЯМР-спектроскопии.
Пример 10. Получение композиций.
Представленные ниже примеры относятся к использованию предлагаемых соединений в качестве пестицидов.
Во всех нижеприведенных примерах маточные растворы соединений получали при концентрации 3000 г/млн. путем растворения 0,3 г испытываемого соединения в 10 мл ацетона с последующим добавлением 90 мл дистиллированной воды и нескольких капель этоксилированного сорбитанмонолаурата или аналогичного подходящего смачивающего агента.
Этот маточный раствор в соответствующих конкретных разведениях использовали в каждом примере. Все обсуждаемые ниже испытания, которые включали в себя обработку соединениями по изобретению, сопровождались контрольными тестами (без использования активного соединения), что позволяло проводить соответствующее сравнение и вычислить процент уничтожения вредителей.
Пример 11. Испытания против взрослых особей акаридов и против яиц/личинок клещей.
За один день до обработки к каждому из двух первичных листьев вигны китайской (одного из каждых двух растений в горшке) прикладывали расплавленный тенглфут (липкая бумага) в конфигурации цифры 8.
В каждой такой конфигурации более близко расположенный к стеблю кружок был предназначен для испытания на овицидную/ларвицидную активность, т.е. против яиц/личинок клещей, а кружок, более удаленный от стебля, был предназначен для испытания акарицидов против взрослых особей клещей.
За день до обработки группы взрослых клещей (Tetranychus urticae Koch) переносили на "овицидные" кружки и самок оставляли откладывать яйца до тех пор, пока до обработки не оставался один час, после чего их удаляли.
Растения опрыскивали 1000 ч./млн. раствором, полученным из маточного раствора (3000 ч./млн.), так, чтобы жидкость стекала с листьев.
Через день после обработки группы приблизительно из 25 взрослых особей клещей переносили в кружки для акарицидов против взрослых особей.
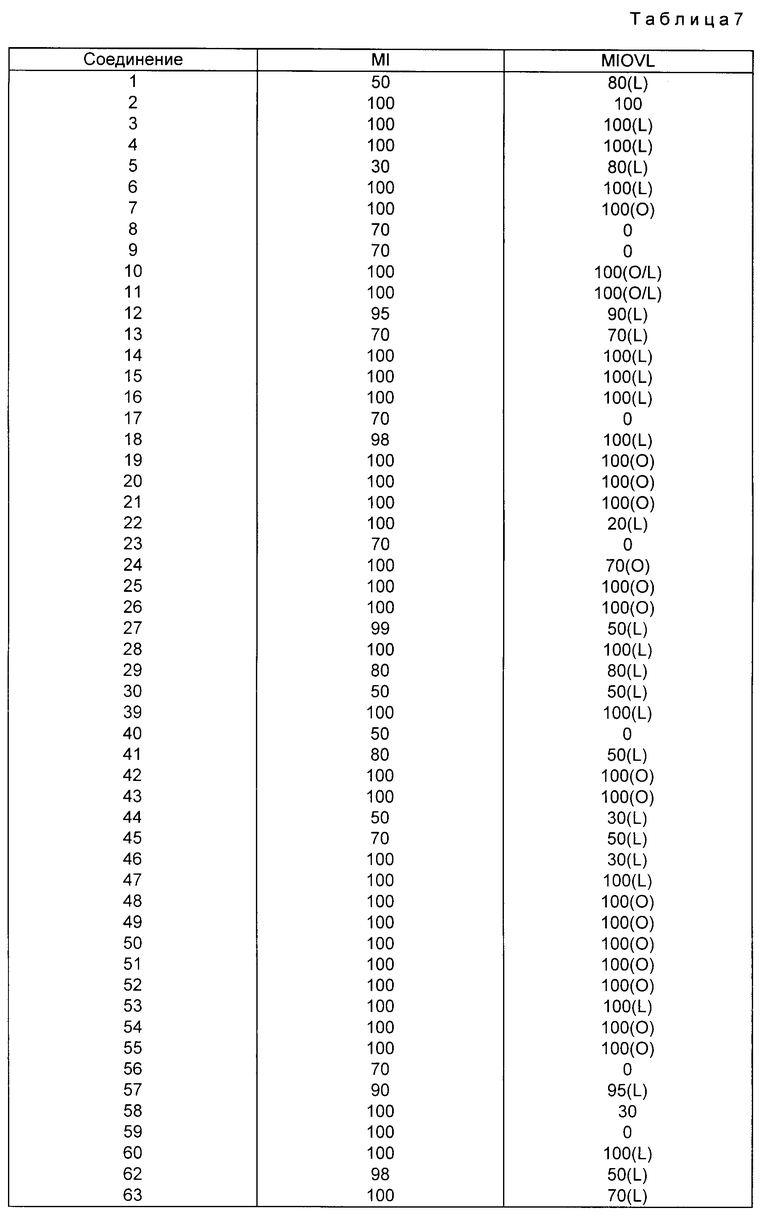
Пять дней спустя эти кружки осматривали для обнаружения живых клещей, оставшихся на листьях. Процент уничтожения клещей оценивали исходя из числа клещей, выживших на контрольных растениях.
Через 9 дней после обработки овицидные/ларвицидные кружки осматривали для обнаружения выведенных яиц и живых незрелых особей клещей. Процент уничтожения оценивали исходя из числа проклюнутых яиц и незрелых особей клещей, выживших на контрольных растениях.
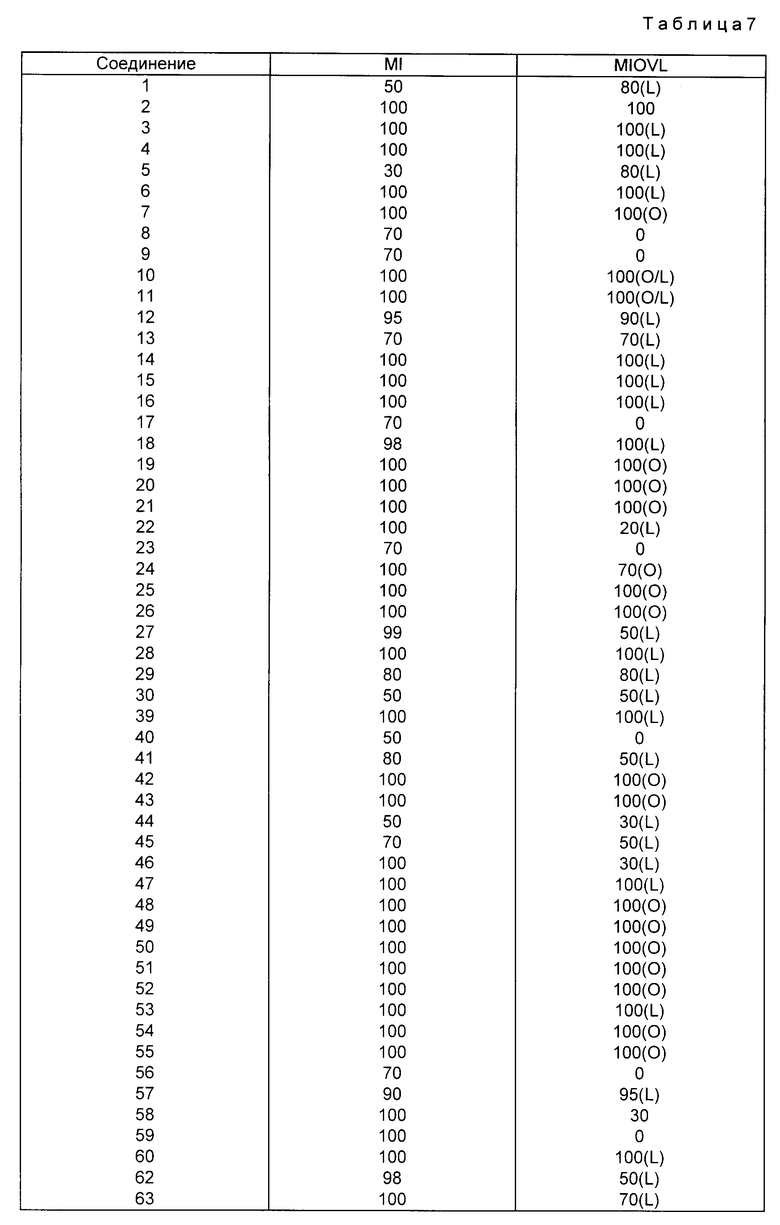
Если целью обработки являлись яйца, то результаты обозначали как овицидные (О), если обработка была направлена на незрелые особи, то результаты обозначали как ларвицидные (L).
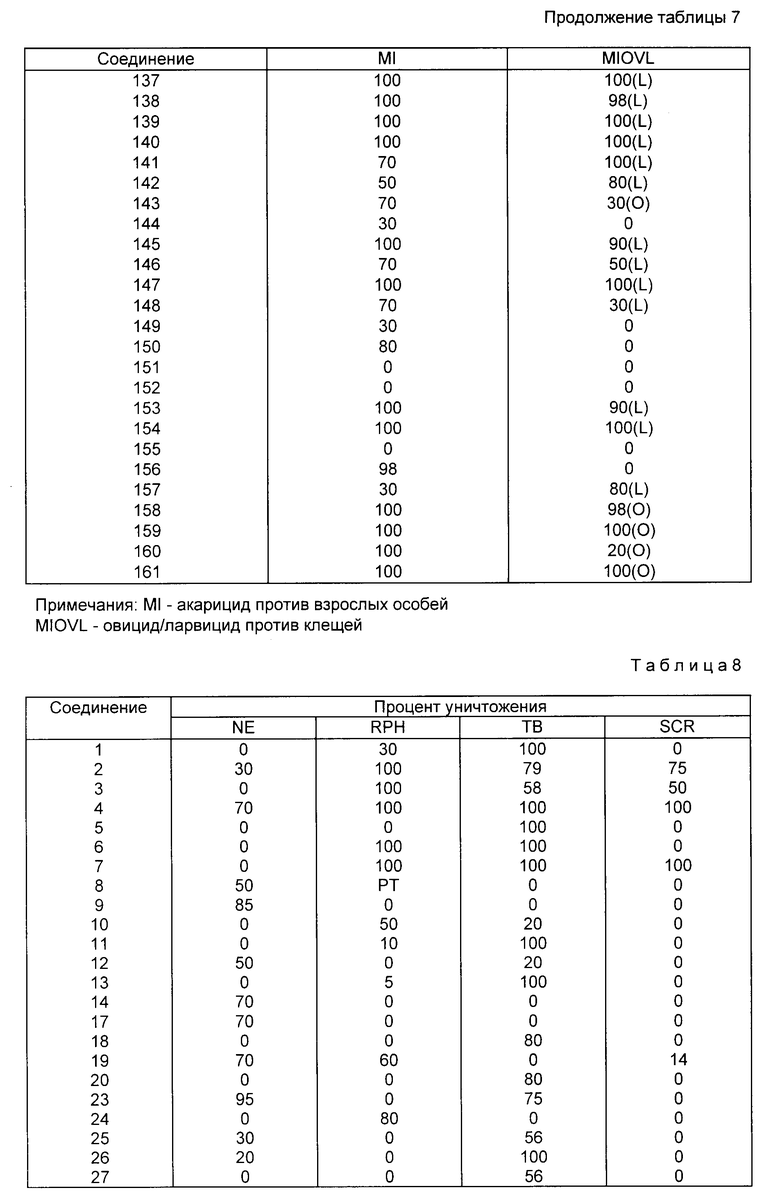
Результаты испытаний соединений на акарицидную активность против зрелых особей (M1) и против яиц/личинок (M10LV) представлены в табл.7.
Пример 12. Тест на красный плодовый клещ.
Яблоневые деревья (Orchard), зараженные красным плодовым клещем (Panonychus ulmi), опрыскивают водными растворами эмульгируемых концентратов отдельных соединений.
С использованием соединений N 103, 10, 11, 19, 20, 25, 26 и 82 при норме опрыскивания 150 ч/млн.а.к. было достигнуто более, чем 75% уничтожения вредителя.
Пример 13. Тест на нематоды.
Маточный раствор в 3000 ч./млн. разводили до 1000 ч./млн. Затем 500 г почвы в горшках, зараженной яйцами яванской галловой нематоды (Meloidogyne incognita), пропитывали 25 мл соединения (эксперимент проводили для каждого соединения) при концентрации в почве 50 ч./млн.
Через день после обработки в каждый горшок высаживали два саженца томатов. Через 19 дней после посадки корни растений исследовали на присутствие наростов и галлов и оценивали процент уничтожения, исходя из уровней заражения контрольных растений.
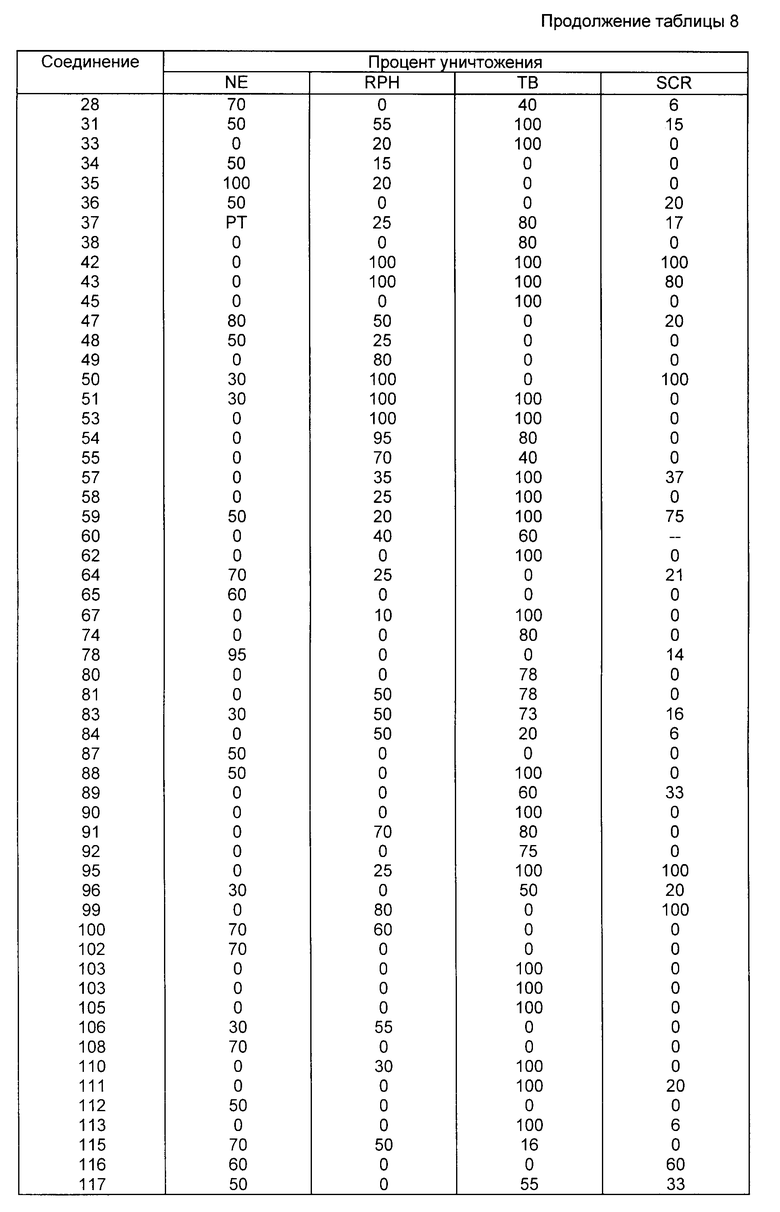
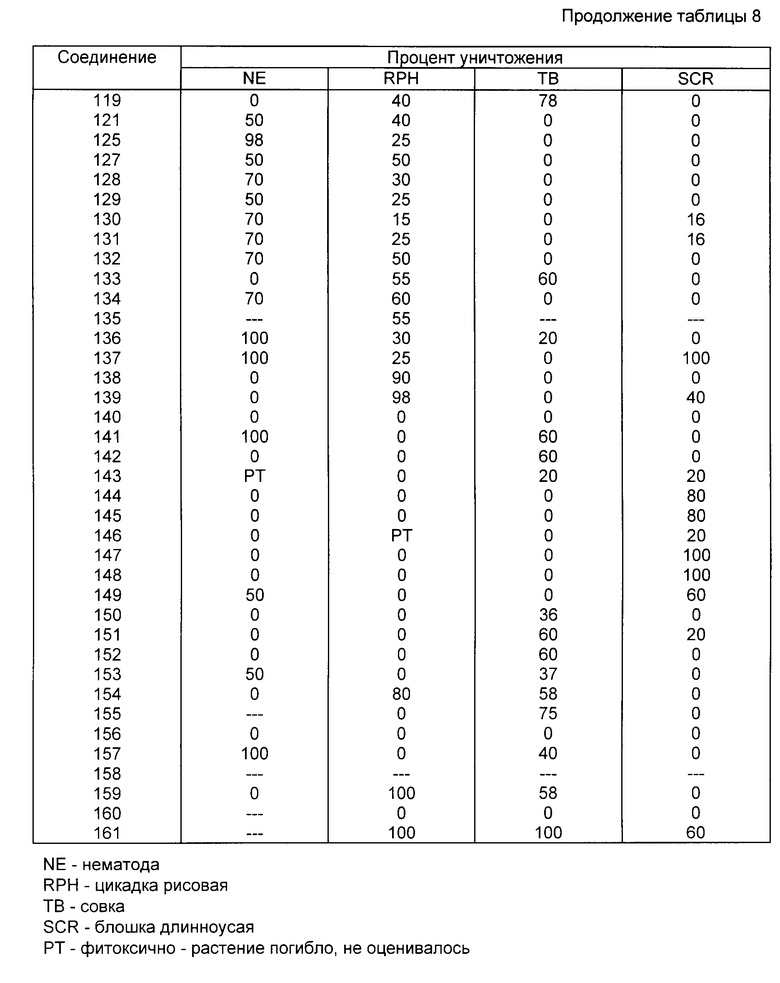
Результаты испытаний на уничтожение нематод (Ne) представлены в табл.8.
Пример 14. Тест с использованием листовой обработки против цикадки рисовой.
Маточный раствор в 3000 ч./млн. разводили до 1000 ч./млн. Один горшок, содержащий приблизительно 20 саженцев риса сорта Mars, обрабатывали каждой композицией путем опрыскивания с помощью пульверизатора.
Через день после обработки растения покрывали трубчатой клеткой и в каждую клетку переносили 20 взрослых особей цикадки рисовой (Sogarodes oryzicola).
Через пять дней после внесения цикадок для каждого горшка подсчитывали число выживших цикадок и вычисляли процент их уничтожения.
Пример 15. Тест на уничтожение совки.
В этом тесте использовали маточный раствор при концентрации 3000 ч./млн. 0,2 мл каждого соединения пипетировали на внутреннюю поверхность каждой из 5 камер с подкормкой, затем оставляли на некоторое время для того, чтобы этот раствор распространился по всей поверхности, и осушали в течение 2 ч.
После этого в каждую камеру вводили личинки Heliothis virescens на второй возрастной стадии. Через 14 дней для каждой обработки определяли число выживших личинок и вычисляли процент уничтожения, проведя корректировку по формуле Эбботта.
Результаты эксперимента на уничтожение совки (TB) представлены в табл.8.
Пример 16. Тест на уничтожение блошки длинноусой.
Маточный раствор (3000 ч./млн.) разводили до 100 млн. д. 2,5 мл каждого соединения пипетировали на фильтровальную бумагу (Whatman # 3), находящуюся на дне 100-миллиметровых чашек Петри. Два саженца кукурузы пропитывали раствором 100 ч./млн. в течение 1 ч, а затем переносили на чашки Петри.
Через 24 ч в каждую чашку вносили 5 личинок Diabrotica undecimpunctata на второй возрастной стадии. Пять дней спустя фиксировали число живых личинок и вычисляли процент уничтожения, проводя коррекцию по формуле Эбботта (см., J. Economic Entomology, 18, 265 - 267, 1925).
Результаты представлены в табл.8.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЕ ОКСАТИАЗИНА, СПОСОБ ЗАЩИТЫ ДРЕВЕСИНЫ ИЛИ КОМПОЗИЦИОННЫХ ДРЕВЕСНЫХ МАТЕРИАЛОВ, КОМПОЗИЦИЯ ДЛЯ ЗАЩИТЫ ДРЕВЕСИНЫ ИЛИ КОМПОЗИЦИОННОГО ДРЕВЕСНОГО МАТЕРИАЛА | 1994 |
|
RU2127266C1 |
| ПРОИЗВОДНЫЕ ФЕНОЛА И КОМПОЗИЦИЯ ДЛЯ ИНГИБИРОВАНИЯ РОСТА ИЛИ РЕПЛИКАЦИИ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА НА ИХ ОСНОВЕ | 1990 |
|
RU2108785C1 |
| СОЕДИНЕНИЯ, КОМПОЗИЦИЯ НА ИХ ОСНОВЕ В КАЧЕСТВЕ ПРОМОТОРА КАТАЛИЗАТОРА (ВАРИАНТЫ) И СПОСОБ ПОЛИМЕРИЗАЦИИ (ВАРИАНТЫ) | 1997 |
|
RU2199522C2 |
| ОРТОЗАМЕЩЕННЫЕ АРИЛАМИДЫ, СПОСОБ БОРЬБЫ С НАСЕКОМЫМИ, КОМПОЗИЦИЯ ДЛЯ БОРЬБЫ С НАСЕКОМЫМИ, ПРОМЕЖУТОЧНОЕ СОЕДИНЕНИЕ | 2002 |
|
RU2283839C2 |
| ПРОИЗВОДНЫЕ АМИДА N-СУЛЬФОНИЛКАРБОНОВОЙ КИСЛОТЫ, ВКЛЮЧАЮЩИЕ N-СОДЕРЖАЩЕЕ 6-ЧЛЕННОЕ АРОМАТИЧЕСКОЕ КОЛЬЦО, ФУНГИЦИДНАЯ И ГЕРБИЦИДНАЯ КОМПОЗИЦИИ И СПОСОБЫ БОРЬБЫ С СОРНЯКАМИ И ФИТОПАТОГЕННЫМИ ГРИБКАМИ | 1993 |
|
RU2117662C1 |
| ПОЛИЭФИР, СПОСОБ СООБЩЕНИЯ БЕЛИЗНЫ ПОЛИЭФИРУ, ТОНИРУЮЩИЙ СОСТАВ ПРЕМИКСА, ФОРМОВАННОЕ ИЗДЕЛИЕ | 1994 |
|
RU2142477C1 |
| ПРОИЗВОДНЫЕ ПИРИМИДИНА, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ И СПОСОБ БОРЬБЫ С СОРНЯКАМИ С ИСПОЛЬЗОВАНИЕМ КОМПОЗИЦИИ | 1990 |
|
RU2029471C1 |
| ПРОИЗВОДНОЕ БЕНЗИЛСУЛЬФИДА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПЕСТИЦИД | 1996 |
|
RU2170728C2 |
| ПРОИЗВОДНЫЕ СЕМИКАРБАЗОНОВ, СПОСОБ УНИЧТОЖЕНИЯ АРТРОПОДОВ, АРТРОПОДИЦИДНАЯ КОМПОЗИЦИЯ | 1989 |
|
RU2067092C1 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ПЕСТИЦИДОВ | 2013 |
|
RU2641916C2 |



Изобретение относится к соединениям, имеющим структурную формулу I, где X, Y, R и Z определены в описании заявки. Соединения по изобретению являются эффективными в борьбе против клещей, нематод, цикадки рисовой, совки и блошки длинноусой. Описаны также способы получения указанных соединений. Структурная формула I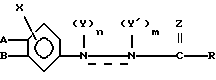
где  - простая или двойная связь. 3 с. и 11 з.п.ф-лы, 8 табл.
- простая или двойная связь. 3 с. и 11 з.п.ф-лы, 8 табл.
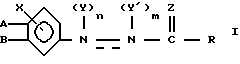
где 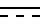 простая или двойная связь;
простая или двойная связь;
Y' - водород;
n и m - независимо 1 или 0;
А и В - водород или группа формулы
Y - водород, С1 - С4-алканоил, С1 - С4-галогеналканоил, С1 - С4-диалкоксифосфорил, С1 - С4-алкиламинокарбонил, галогено - С1 - С4-алкилсульфонил, или С1 - С4-алккоксикарбонил;
R - Н, С1 - С6-алкил, С1 - С6-алкокси, С3 - С6-циклоалкокси, галогено-С1 - С6-алкил, С1 - С6-алкокси С1 - С6-алкил, фенил-С1 - С6-алкокси, С2 - С6-алкенил, С1 - С6-алкилтио, С1 - С6-алкоксикарбонил, С1 - С6-алкиламино, фурил или тиенил, фенил-С1 - С6-алкил, галогено-С1 - С6-алкокси, фенилокси или С3 - С6-циклоалкил;
Z - О или S, при условии, что при Х - фенил R алкиламиногруппа или С1 - С6-алкоксикарбонил, при условии, что n и m всегда равны 0, когда  представляет собой двойную связь, и при условии, что, когда А и В - водород, Х - (а) фенил, низшая фенилалкоксигруппа, феноксигруппа или бензил, причем фенильное кольцо каждого указанного заместителя может быть замещено галогеном, низшим алкилом, низшей алкоксигруппой, либо (b) один заместитель из группы (а) - фенил и второй выбран из С1 - С4 - алкокси, галогена, С1 - С4 - алкила и С1 - С4-алкилтиогруппы, либо, когда А и В отличны от водорода, Х - водород или низший алкокси.
представляет собой двойную связь, и при условии, что, когда А и В - водород, Х - (а) фенил, низшая фенилалкоксигруппа, феноксигруппа или бензил, причем фенильное кольцо каждого указанного заместителя может быть замещено галогеном, низшим алкилом, низшей алкоксигруппой, либо (b) один заместитель из группы (а) - фенил и второй выбран из С1 - С4 - алкокси, галогена, С1 - С4 - алкила и С1 - С4-алкилтиогруппы, либо, когда А и В отличны от водорода, Х - водород или низший алкокси.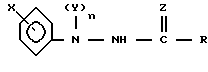
где Х - фенил;
Y - Н или COOCF3;
n = 1;
R - CF3, С1 - С4-алкил, С1 - С4-алкокси или С3 - С6-циклоалкил,
Z - кислород.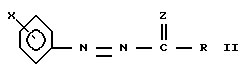 где Х определен в п.1 и представляет собой (а) фенил, низшую фенилалкоксигруппу, феноксигруппу или бензил, причем фенильное кольцо каждого заместителя может быть замещено галогеном, низшим алкилом, низшей алкоксигруппой, или (b) один заместитель - фенил, а второй выбран из С1 - С4-алкокси, галогена, С1 - С4-алкила и низшей алкилтиогруппы;
где Х определен в п.1 и представляет собой (а) фенил, низшую фенилалкоксигруппу, феноксигруппу или бензил, причем фенильное кольцо каждого заместителя может быть замещено галогеном, низшим алкилом, низшей алкоксигруппой, или (b) один заместитель - фенил, а второй выбран из С1 - С4-алкокси, галогена, С1 - С4-алкила и низшей алкилтиогруппы;
R - водород, С1 - С6-алкил, С1 -С6-алкокси, С1 - С4-галогеноалкил, или С3 - С6-циклоалкил;
Z - кислород.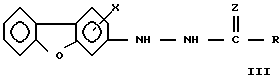
где Х - водород или низшая фенилалкоксигруппа;
R имеет указанные значения;
Z - кислород или сера.
где Х - водород или низшая алкоксигруппа;
R имеет значения, указанные в п.1;
Z - кислород или сера.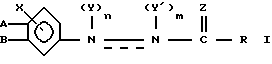
где  простая или двойная связь;
простая или двойная связь;
Y' - водород;
n и m - независимо 1 или 0;
А и В - водород или группа формулы
Y - водород, С1 - С4-алканоил, С1 - С2-галогеналканоил, ди-С1 - С4-алкоксифосфорил, С1 -С4-алкиламинокарбонил, галоген - С1 - С4-алкилсульфонил;
R - водород, С1 - С6-алкил, С1 - С6-алкокси, С3 - С6-циклоалкокси, галоген - С1 - С4-алкил, С1 - С4-алкокси С1 - С4-алкил, бензилокси, С2 - С4-алкенил, С1 - С4-алкилтио, С1 - С4-алкоксикарбонил, тиенил, бензил, галоген-С1 - С4-алкокси, С3 - С6-циклоалкил;
Z - кислород, при условии, что если Х является фенилом, то R не является С1 - С4-алкиламиногруппой или С1 - С4-алкоксикарбонилом, при условии, что n и m всегда равны 0, когда 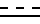 представляет собой двойную связь, R - С1 - С4-алкокси, Х - фенил и С1 - С4-алкил, А и В - водород, при условии, что когда А и В - водород, Х представляет собой (а) фенил, фенокси, бензил, фенил-С1 - С4-алкокси, либо (b) один заместитель - фенил и второй выбранный из группы: С1 - С4-алкокси, галоген, С1 - С4-алкилтио, С1 - С4-алкил, при условии, что когда А и В отличны от водорода, Х - С1 - С4-алкокси, R - С1 - С4-алкокси, n и m = 1.
представляет собой двойную связь, R - С1 - С4-алкокси, Х - фенил и С1 - С4-алкил, А и В - водород, при условии, что когда А и В - водород, Х представляет собой (а) фенил, фенокси, бензил, фенил-С1 - С4-алкокси, либо (b) один заместитель - фенил и второй выбранный из группы: С1 - С4-алкокси, галоген, С1 - С4-алкилтио, С1 - С4-алкил, при условии, что когда А и В отличны от водорода, Х - С1 - С4-алкокси, R - С1 - С4-алкокси, n и m = 1. - простая или двойная связь, Y - водород, n и m независимо представляет собой 1 или 0, А и В - водород, Y - водород, С1 - С4-алканоил, С1 - С4-галогеналканоил, ди-С1 - С4-алкоксифосфорил, С1 - С4-алкиламинокарбонил, галоген-С1 - С4-алкилсульфонил, С1 - С4-алкоксикарбонил, R - водород, С1 - С6-алкил, С1 - С6-алкокси, С3 - С6-циклоалкокси, галоген-С1 - С4-алкил, С1 - С4-алкокси-С1 - С4-алкил, бензилокси, С2 - С4-алкенил, С1 - С4-алкилтио, С1 - С4-алкоксикарбонил, С1 - С4-алкиламино, тиенил, фурил, галоген-С1 - С4-алкокси, фенокси, С3 - С6-циклоалкил, Z - кислород или сера, при условии, что, если Х - фенил, R не является С1 - С4-алкиламино, С1 - С4-алкоксикарбонилом, при условии, что n и m = 0, когда
- простая или двойная связь, Y - водород, n и m независимо представляет собой 1 или 0, А и В - водород, Y - водород, С1 - С4-алканоил, С1 - С4-галогеналканоил, ди-С1 - С4-алкоксифосфорил, С1 - С4-алкиламинокарбонил, галоген-С1 - С4-алкилсульфонил, С1 - С4-алкоксикарбонил, R - водород, С1 - С6-алкил, С1 - С6-алкокси, С3 - С6-циклоалкокси, галоген-С1 - С4-алкил, С1 - С4-алкокси-С1 - С4-алкил, бензилокси, С2 - С4-алкенил, С1 - С4-алкилтио, С1 - С4-алкоксикарбонил, С1 - С4-алкиламино, тиенил, фурил, галоген-С1 - С4-алкокси, фенокси, С3 - С6-циклоалкил, Z - кислород или сера, при условии, что, если Х - фенил, R не является С1 - С4-алкиламино, С1 - С4-алкоксикарбонилом, при условии, что n и m = 0, когда 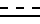 представляет собой двойную связь, Х фенил и С1 - С4-алкокси, R - С1 - С4-алкокси, Х представляет собой (а) фенил или фенил-C1 - С4-алкокси, фенокси, бензил, либо (b) фенил и второй компонент, выбранный из С1 - С4-алкокси, галогена, С1 - С4-алкила, С1 - С4-алкилтио.
представляет собой двойную связь, Х фенил и С1 - С4-алкокси, R - С1 - С4-алкокси, Х представляет собой (а) фенил или фенил-C1 - С4-алкокси, фенокси, бензил, либо (b) фенил и второй компонент, выбранный из С1 - С4-алкокси, галогена, С1 - С4-алкила, С1 - С4-алкилтио.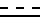 - простая или двойная связь, Y' - водород, n и m независимо представляет собой 1 и 0, А и В - водород или группа формулы
- простая или двойная связь, Y' - водород, n и m независимо представляет собой 1 и 0, А и В - водород или группа формулы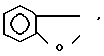
Y - водород, С1 -С4-алканоил, С1 - С4-галогеналканоил, ди-С1 - С4-алкоксифосфорил, С1 - С4-алкиламинокарбонил, галоген-С1 - С4-алкилсульфонил, С1 - С4-алкоксикарбонил, R - водород, С1 - С6-алкил, С1 - С6-алкокси, галоген-С1 - С4-алкил, бензилокси, С2 - С4-алкенил, С1 - С4-алкилтио, галоген-С1 - С4-алкокси, С1 - С4-алкоксикарбонил, бензил, Z - кислород, при условии, что если Х - фенил, R не является С1 - С4-алкоксикарбонилом, при условии, что n и m всегда равны 0, когда 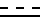 представляет собой двойную связь, А и В - группа
представляет собой двойную связь, А и В - группа
Х - С1 - С4-алкокси, R - С1 - С4-алкокси, при условии, когда А и В отличны от водорода, Х - С1 - С4-алкокси, R - С1 - С4-алкокси, при условии, когда А и В - водород, Х представляет собой (а) фенил, бензилокси, фенокси или (б) фенил и С1 - С4-алкокси.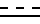 - простая или двойная связь, Y' - водород, n и m независимо равны 1 или 0, А и В водород, Y - водород, С1 - С4-алканоил, С1 - С4-галогеналканоил, ди-С1 - С4-алкоксифосфорил, С1 - С4-алкиламинокарбонил, галоген-С1 - С4-алкилсульфонил, С1 - С4-алкоксикарбонил, R - водород, С1 - С6-алкил, С1 - С6-алкокси, С3 - С6-циклоалкокси, галоген-С1 - С4-алкил, С1 - С4-алкокси-С1 - С4-алкил, бензилокси, С2 - С4-алкенил, С1 - С4-алкилтио, С1 - С4-алкоксикарбонил, С1 - С4-алкиламино, тиенил, фурил, галоген-С1 - С4-алкокси, фенокси, С3 - С6-циклоалкил, Z - кислород или сера, при условии, что если Х - фенил, R не является С1 - С4-алкиламино, С1 - С4-алкоксикарбонилом, при условии, что n и m = 0, когда
- простая или двойная связь, Y' - водород, n и m независимо равны 1 или 0, А и В водород, Y - водород, С1 - С4-алканоил, С1 - С4-галогеналканоил, ди-С1 - С4-алкоксифосфорил, С1 - С4-алкиламинокарбонил, галоген-С1 - С4-алкилсульфонил, С1 - С4-алкоксикарбонил, R - водород, С1 - С6-алкил, С1 - С6-алкокси, С3 - С6-циклоалкокси, галоген-С1 - С4-алкил, С1 - С4-алкокси-С1 - С4-алкил, бензилокси, С2 - С4-алкенил, С1 - С4-алкилтио, С1 - С4-алкоксикарбонил, С1 - С4-алкиламино, тиенил, фурил, галоген-С1 - С4-алкокси, фенокси, С3 - С6-циклоалкил, Z - кислород или сера, при условии, что если Х - фенил, R не является С1 - С4-алкиламино, С1 - С4-алкоксикарбонилом, при условии, что n и m = 0, когда 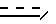 представляет собой двойную связь, Х - фенил и С1 - С4-алкокси, R - С1 - С4-алкокси, X представляет собой а) фенил или фенил (C1 - C4)-алкокси, фенокси, бензил, либо (б) фенил и второй компонент, выбранный из С1 - С4-алкокси, галогена, С1 - С4-алкила, С1 - С4-алкилтио.
представляет собой двойную связь, Х - фенил и С1 - С4-алкокси, R - С1 - С4-алкокси, X представляет собой а) фенил или фенил (C1 - C4)-алкокси, фенокси, бензил, либо (б) фенил и второй компонент, выбранный из С1 - С4-алкокси, галогена, С1 - С4-алкила, С1 - С4-алкилтио.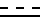 - простая или двойная связь, Y' - водород, n и m независимо равны 1 и 0, А и В - водород или группа формулы
- простая или двойная связь, Y' - водород, n и m независимо равны 1 и 0, А и В - водород или группа формулы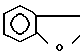
Y - водород, С1 - С4-алканоил, С1 - С4-галогеналканоил, ди-С1 - С4-алкоксифосфорил, С1 - С4-алкиламинокарбонил, галоген-С1 - С4-алкилсульфонил, С1 - С4-алкоксикарбонил, R - водород, С1 - С6-алкил, С1 - С6-алкокси, галоген-С1 - С4-алкил, бензилокси, С2 - С4-алкенил, С1 - С4-алкилтио, галоген-С1 - С4-алкокси, С1 - С4-алкоксикарбонил, бензил, Z - кислород, при условии, что, если Х - фенил, R не является С1 - С4-алкоксикарбонилом, при условии, что n и m всегда равны 0, когда 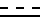 представляет собой двойную связь, А и В - группа формулы
представляет собой двойную связь, А и В - группа формулы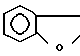
Х - С1 - С4-алкокси, R - С1 - С4-алкокси, при условии, когда А и В отличны от водорода, Х - С1 - С4-алкокси, R - С1 - С4-алкокси, при условии, когда А и В - водород, Х представляет собой (а) фенил, бензилокси, фенокси ии (b) фенил и С1 - С4-алкокси.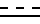 - простая или двойная связь, Y' - водород, n и m независимо равны 1 или 0, А и В - водород или группа формулы
- простая или двойная связь, Y' - водород, n и m независимо равны 1 или 0, А и В - водород или группа формулы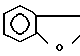
Y - водород, С1 - С4-алканоил, С1 - С4-галогеналканоил, ди-С1 - С4-алкоксифосфорил, С1 - С4-алкиламинокарбонил, галоген - С1 - С4-алкилсульфонил, R - водород, С1 - С6-алкил, С1 - С6-алкокси, С3 - С6-циклоалкокси, галоген - С1 - С4-алкил, С1 - С4-алкокси-С1 - С4-алкил, бензилокси, С2 - С4-алкенил, С1 - С4-алкилтио, С1 - С4-алкоксикарбонил, тиенил, бензил, галоген-С1 - С4-алкокси, С3 - С6-циклоалкил, Z - кислород, при условии, что если X является фенилом, то R не является С1 - С4-алкиламиногруппой или С1 - С4-алкоксикарбонилом, при условии, что n и m всегда равны 0, когда 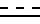 представляет собой двойную связь, R - С1 - С4-алкокси, Х - фенил и С1 - С4-алкил, А и В - водород; при условии, что когда А и В - водород, Х представляет собой (а) фенил, фенокси, бензил, фенил-С1 - С4-алкокси, либо (b) один заместитель - фенил и второй выбран из группы: С1 - С4-алкокси, галоген, С1 - С4-алкилтио, С1 - С4-алкил, при условии, что когда А и В отличны от водорода, Х - С1 - С4-алкокси, R - С1 - С4 - алкокси, n и m = 1.
представляет собой двойную связь, R - С1 - С4-алкокси, Х - фенил и С1 - С4-алкил, А и В - водород; при условии, что когда А и В - водород, Х представляет собой (а) фенил, фенокси, бензил, фенил-С1 - С4-алкокси, либо (b) один заместитель - фенил и второй выбран из группы: С1 - С4-алкокси, галоген, С1 - С4-алкилтио, С1 - С4-алкил, при условии, что когда А и В отличны от водорода, Х - С1 - С4-алкокси, R - С1 - С4 - алкокси, n и m = 1.
Приоритеты по признакам:
12.11.91 - соединение формулы I, где Х - фенил или фенилалкокси;
20.11.92 - Х отличен от фенила и фенилалкокси.
| FR патент, 2440943, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
Авторы
Даты
1998-04-27—Публикация
1992-11-17—Подача