Изобретение относится к производным амидов N-сульфонилкарбоновой кислоты, включающим 6-членное ароматическое N-содержащее кольцо, а также к композициям фунгицидным и гербицидным, содержащим такие соединения в качестве активного ингредиента, и способам борьбы с сорняками и фитопатогенными грибками.
Некоторые соединения, обладающие химическим строением, подобным химическому строению производных N-сульфонамидов, соответствующих настоящему изобретению, известны из заявки на патент Японии, N Hei 2-282371, где указано, что такие соединения действуют как модификаторы роста растений или как гербициды.
В сельскохозяйственном производстве болезни растений, вызванные патогенными грибками, принадлежащими к Comycetes, такими как ложная мучнистая роса, фитофтороз или подобные, встречаются на многих растениях и относятся к числу заболеваний, с которыми наиболее трудно бороться. По этой причине желательна разработка улучшенных средств борьбы.
Изобретатели синтезировали различные производные N-сульфонамидов, включающих N-содержащие 6-членные ароматические кольца, и выполнили широкие исследования их влияния на активность грибка. В результате найдено, что производные N-сульфонамидов, соответствующие настоящему изобретению, проявляют противогрибковую активность. Соединения, которые в соответствии с настоящим изобретением являются активными ингредиентами композиции, являются новыми и полезны в борьбе с различными сорняками на рисовых и вспаханных полях.
Настоящее изобретение предлагает биоцид, содержащий производное N-сульфонамида, включающее N-содержащее 6-членное ароматическое кольцо формулы /1/: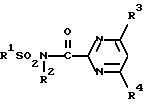
где
R1 - C1-C10-алкил, необязательно содержащий один или два заместителя, выбираемых из группы, включающей: галоген, C3-C5-циклоалкил, C1-C3-алкилтио, C1-C4-алкилсульфинил, C1-C4-алкоксикарбонил, C2-C4-алкилкарбонил; либо R1 - C2-C6-алкенил, необязательно содержащий один или два заместителя, выбранных из галогена, либо R1 - C2-C6-алкинил; либо R1 - цикло C5-C6-алкил, который может быть замещен оксогруппой; либо R1 - 1-пирролидинил, 2-метил-1-пиперидинил, 1-азиридинил, группа-NR5R6;
R2 - водород, (низший)алкокси(низший)алкил;
R3 и R4 - независимо друг от друга представляют собой галоген, C1-C4-алкил, низший алкокси, ди(низший)алкиламино;
R5 и R6 - независимо друг от друга представляют водород, C1-C5-алкил, низшую алкокси группу, низший алкенил, цикло(низший)алкил, низший алкинил, C1-C4-алкокси-C1-C4-алкил.
Более предпочтительным является производное амида N-сульфонилкарбоновой кислоты, включающее N-содержащее 6-членное ароматическое кольцо, в котором R1 - C1-C10-алкил, необязательно содержащий один или два заместителя, выбранных из группы, включающей: галоген, C3-C5-циклоалкил, C1-C3-алкилтио, C1-C3-алкилсульфинил, C1-C6-алкоксикарбонил, C2-C4-алкилкарбонил; или C2-C6-алкенил, необязательно содержащий один или два заместителя, выбранных из галогена; C2-C6-алкинил; или цикло-C5-C6-алкил, который может быть замещен оксогруппой; или 1-пирролидинил; 2-метил-1-пиперидинил; 1-азиридинил, или группа -NR5R6;
R2 - водород, метокси -C1-C3-алкил;
R3 и R4 - независимо друг от друга, представляют галоген, C1-C3-алкил, C1-C3-алкокси, ди(C1-C3)алкиламино;
R5 - водород, C1-C5-алкил, C1-C3-алкокси;
R6 - C1-C5-алкил, C2-C5-алкенил, цикло-C3-C5-алкил, C2-C5-алкинил.
Еще более предпочтительным является производное амида N-сульфонилкарбоновой кислоты, включающее N-содержащее 6-членное ароматическое кольцо, в котором R1 представляет собой C2-C6-алкенил, необязательно содержащий один или два заместителя, выбранных из галогена;
R2 - водород, метоксиметильная группа;
R3 и R4 - независимо друг от друга, представляют галоген, метил, метокси, диметиламино.
Еще одним аспектом изобретения является фунгицидная композиция, включающая активный ингредиент - производное амида пиримидинкарбоновой кислоты и целевые добавки, отличающаяся тем, что в качестве производного амида пиримидинкарбоновой кислоты она содержит соединение формулы: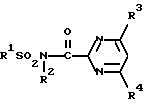
где
R1 представляет собой C1-C6-алкил, необязательно содержащий один или два заместителя, выбранных из группы, включающей галоген, C3-C5-циклоалкил; C1-C4-алкилтио и оксиранильную группу; или C2-C6-алкенил, необязательно содержащий 1 или 2 галогена, или группа -NR5R6, в которой R5 представляет собой водород, C1-C4-алкил, R6 представляет собой C1-C4-алкил, C2-C5-алкинил, C3-C5-циклоалкил; R2 представляет собой водород, C1-C4-алкокси-C1-C4-алкил; R3 представляет собой галоген, C1-C4-алкил, C1-C4-алкокси; R4 представляет собой C1-C4-алкокси, ди-(C1-C4)алкиламино, в эффективном количестве.
Следующим объектом изобретения является гербицидная композиция, включающая активный ингредиент - производное сульфированного амида пиримидинкарбоновой кислоты и целевые добавки, отличающаяся тем, что в качестве производного сульфированного амида пиримидинкарбоновой кислоты она содержит соединение формулы: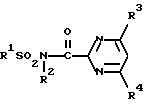
где
R1 представляет собой C1-C6-алкил, необязательно содержащий один или два заместителя, выбранных из группы, включающей: галоген, C3-C5-циклоалкил, C1-C4-алкилтио, C1-C4-алкилсульфинил, C1-C4-алкоксикарбонил, C2-C4-алкилкарбонил; C2-C6-алкенильную группу, необязательно содержащую один или два заместителя, выбранных из галогена; C2-C6-алкинил; C5-C6-циклоалкил, который может быть замещен оксогруппой; 1-пирролидинил; 2-метил-1-пиперидинил; 1-азиридинил или группу -NR5R6, в которой R5 представляет собой атом водорода, C1-C4-алкил, C1-C4-алкокси; R6 представляет собой C1-C4-алкил, C2-C5-алкенил, C1-C4-алкокси-C1-C4-алкил; R2 представляет собой атом водорода, C1-C4-алкокси-C1-C4-алкил; R3 представляет собой галоген, C1-C4-алкил,
C1-C4-алкокси; R4 представляет собой C1-C4-алкил, C1-C4-алкокси, ди(C1-C4)алкиламино в эффективном количестве.
Настоящим изобретением предложен также способ борьбы с фитопатогенными грибками путем обработки растений фунгицидной композицией, где в качестве фунгицидной композиции используют композицию, описанную выше, при дозе внесения 500 ч/млн активного ингредиента.
Также предложен способ борьбы с сорняками путем обработки почвы и/или растений гербицидной композицией, где в качестве композиции используют вышеописанную композицию при норме расхода активного ингредиента, 1,6 - 400 г/10 ар.
Производные N-сульфонамида, включающие N-содержащее 6-членное ароматическое кольцо, изображаемые формулой /1/, могут существовать в виде геометрических изомеров E-конфигурации и Z-конфигурации. Настоящее изобретение включает каждый геометрический изомер и их смеси в произвольном соотношении. В соединении формулы /1/ алкильная группа может означать, например, алкильную группу, содержащую от 1 до 10 атомов углерода; алкенильная группа может быть представлена алкенильной группой, содержащей 2 - 8 атомов углерода, алкинильная группа может быть алкинильной группой, содержащей от 2 до 8 атомов углерода; циклоалкильная группа может быть циклоалкильной группой, содержащей от 3 до 8 атомов углерода; алкоксигруппа может быть алкоксигруппой, содержащей от 1 до 6 атомов углерода; и атом галогена может быть хлором, бромом, фтором или иодом.
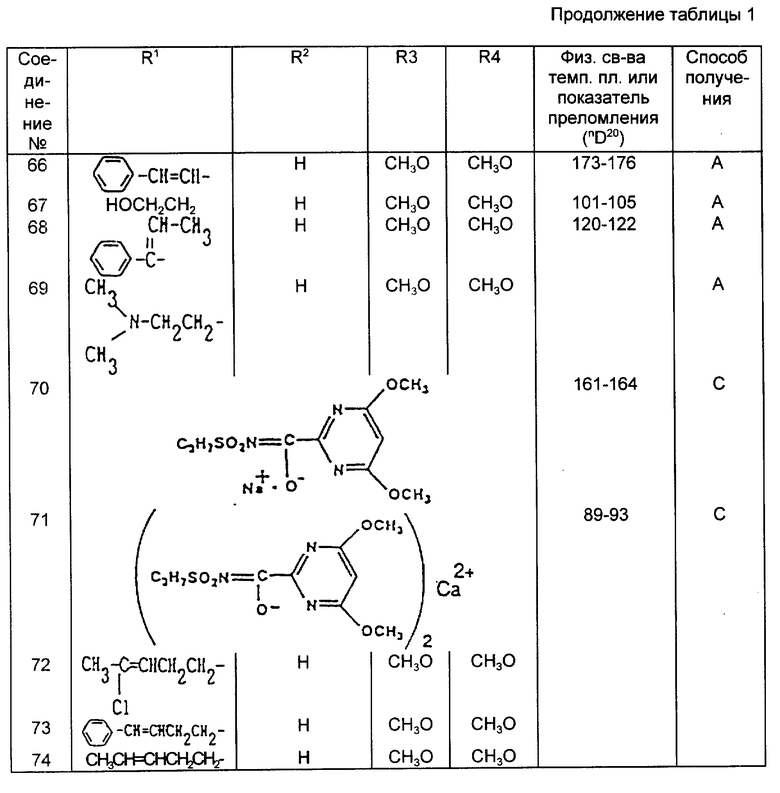
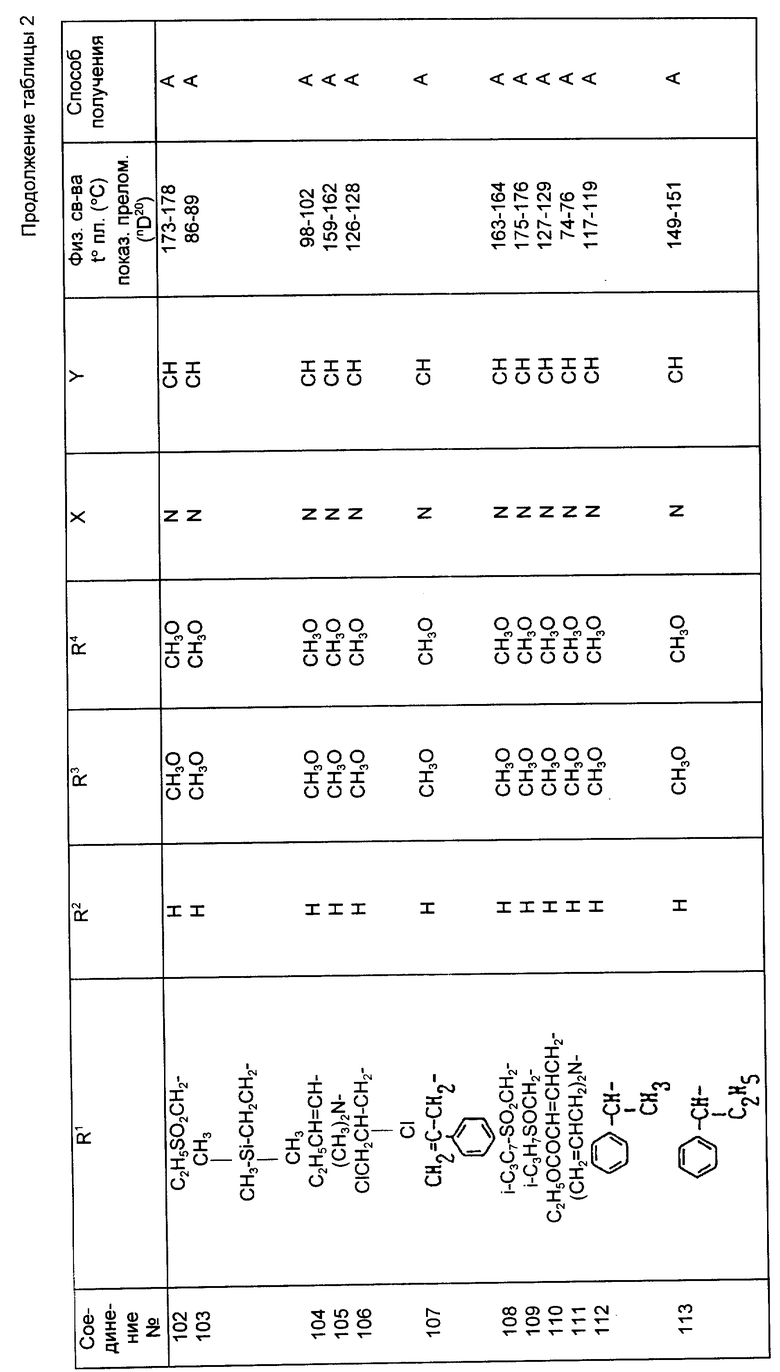
Далее, в табл. 1 и 2 дается список соединений, соответствующих настоящему изобретению. В последующем описании соединение будет упоминаться под номером, данном в табл. 1 и 2.
Соединения, соответствующие настоящему изобретению, могут быть получены препаративными способами A-E.
Препаративный способ A
/Схема 1/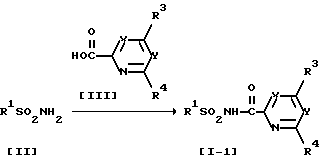
В этой схеме R1, R3, R4, X и Y имеют установленные выше значения.
Соединение, изображенное формулой [I-1] , может быть получено взаимодействием соединения, представленного формулой [II] с 1 ≈ 1,5 эквивалентами соединения, представленного формулой [III] , в растворителе в присутствии конденсирующего агента.
В качестве конденсирующего агента здесь можно упомянуть диэтилцианофосфат, N, N'-карбонилдиимидазол, тионилхлорид, N,N'-дициклогексилкарбодиимид, или т.п.
В качестве растворителя здесь можно упомянуть бензол, толуол, ксилол, дихлорметан, хлороформ, диэтиловый эфир, тетрагидрофуран, диоксан, ацетонитрил, N,N-диметилформамид, N,N-диметилацетамид, диметилсульфоксид, или подобные.
Реакция, при необходимости, может быть осуществлена в присутствии основания, такого как триэтиламин, гидрид натрия, пиридин и т.п.
Реакция может быть осуществлена при подходящей температуре, которая составляет от -20oC до +50oC, в течение времени от 30 мин до 20 ч.
Препаративный способ B
/Схема 2/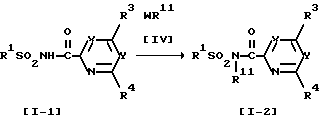
Здесь W представляет собой атом галогена, R1, R3, R4, X и Y имеют установленные выше значения, R11 представляет собой алкильную группу (необязательно замещенную алкоксигруппой или алкоксикарбонильной группой), бензильную группу или алкенильную группу.
Соединение, изображенное формулой [I-2] , может быть получено взаимодействием соединения, изображаемого формулой [I-1], с 1 ≈ 1,5 эквивалентами соединения, изображаемого формулой [IV], в растворителе в присутствии основания.
В качестве основания здесь могут быть упомянуты триэтиламин, гидрид натрия, пиридин или т.п.
В качестве растворителя здесь могут быть упомянуты бензол, толуол, ксилол, диэтиловый эфир, тетрагидрофуран, диоксан, ацетонитрил, N,N-диметилформамид, N,N-диметилацетамид, диметилсульфоксид или т.п.
Настоящая реакция может быть осуществлена при подходящей температуре от -20oC до +50oC за время от 30 мин до 20 ч.
Препаративный способ C
/Схема 3/
Здесь M+ представляет собой ион щелочного металла, щелочноземельного металла, аммония, аммонийорганический ион или ион переходного металла, и R1, R3, R4, X и Y имеют установленные выше значения.
Соединение изображенное формулой [I-3] , может быть получено взаимодействием соединения, изображаемого формулой [I-1], с 0,5 ≈ 1 эквивалентом основания в растворителе.
В качестве основания здесь могут быть упомянуты щелочные металлы, такие как натрий, калий или т.п., гидрид щелочного металла или гидрид щелочноземельного металла, такой как гидрид натрия, гидрид калия, гидрид кальция или т. п. , гидроксид щелочного металла или гидроксид щелочноземельного металла, такой как гидроксид натрия, гидроксид калия, гидроксид кальция или т.п., алкоксид щелочного металла, такой как метоксид натрия, трет-бутоксид калия или т.п., органический амин, такой как аммиак, изопропиламин или т.п.
В качестве растворителя здесь могут быть упомянуты бензол, толуол, ксилол, диэтиловый эфир, тетрагидрофуран, диоксан, ацетонитрил, метанол, этанол, N,N-диметилацетамид, диметилсульфоксид, вода, или т.п.
Настоящая реакция может быть осуществлена при подходящей температуре от -20oC до +50oC за время от 30 мин до 20 ч.
Препаративный способ D
/Схема 4/
Здесь R1, R3, R4, X и Y имеют значения, установленные выше.
Соединение, изображенное формулой [I-1] , может быть получено взаимодействием соединения, изображаемого формулой [VI], с 0,5 ≈ 1 эквивалентом соединения, изображаемого формулой [III] в растворителе.
В качестве растворителя здесь могут быть упомянуты бензол, толуол, ксилол, дихлорметан, хлороформ, диэтиловый эфир, тетрагидрофуран, диоксан, ацетонитрил, N,N-диметилформамид, N,N-диметилацетамид, диметилсульфоксид, или т. п.
Реакция может быть осуществлена в присутствии основания, такого как триэтиламин, гидрид натрия, пиридин, или т.п., если есть такая необходимость.
Настоящая реакция может быть осуществлена при подходящей температуре от -20oC до +50oC за время от 30 мин до 20 ч.
Препаративный способ E
/Схема 5/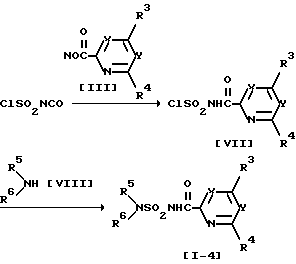
Здесь R3, R4, R5, R6, X и Y имеют установленные выше значения.
Соединение, изображенное формулой [I-4] , может быть получено взаимодействием соединения, изображаемого формулой [VII], с соединением, изображаемым формулой [VIII], в растворителе.
Реакция, при необходимости, может быть осуществлена в присутствии основания, такого как триэтиламин, гидрид натрия, пиридин, или т.п.
Соединение, изображенное формулой [VII] , может быть получено взаимодействием соединения, изображаемого формулой [III], с 1 ≈ 1,5 эквивалентами хлорсульфонилизоцианата в растворителе.
Для каждой из приведенных выше реакций в качестве растворителей могут быть упомянуты бензол, толуол, ксилол, диметилформамид, хлороформ, диэтиловый эфир, тетрагидрофуран, диоксан, ацетонитрил, диметилсульфоксид, или т. п. Настоящая реакция может быть осуществлена при подходящей температуре от -20oC до +50oC за время от 30 мин до 20 ч.
Способы получения соединений, соответствующих настоящему изобретению, будут подробно обсуждаться в следующих далее примерах.
Пример 1. Синтез N-изобутилсульфонил-4,4-диметоксипиримидин-2- карбоксиамида (соединение 8)
К раствору, содержащему 2,0 г (11 ммоль) 4,6-диметоксипиримидин-2-карбоновой кислоты, растворенной в 20 мл N,N-диметилформамида, добавляют 1,8 г (11 ммоль) N,N-карбонилдиимидазола, и смесь затем перемешивают в течение 1 ч при комнатной температуре, чтобы приготовить раствор, содержащий 4,6-диметоксипиримидин-2-карбонилимидазол в N,N-диметилформамиде. Далее, к раствору, содержащему 1,5 г (11 моль) изобутилсульфонамида, растворенного в 20 мл N, N-диметилформамида, добавляют 0,5 г (12 ммоль) 60%-ного гидрида натрия. После перемешивания смеси в течение 1 ч при комнатной температуре к ней при комнатной температуре по каплям добавляют раствор, содержащий 4,6-диметоксипиримидин-2-карбонилимидазол в N,N-диметилформамиде. После перемешивания реакционной смеси в течение 3 ч при комнатной температуре смесь выливают в холодную воду со льдом. Величину pH реакционной меси доводят разбавленной соляной кислотой до pH 2 ≈ 3. Органический слой экстрагируют дважды 200 мл этилацетата. Экстракт промывают водой, органический слой сушат над безводным сульфатом магния, затем концентрируют при пониженном давлении и поучают 3,1 г вязкой жидкости. Вязкую жидкость очищают колоночной хроматографией на силикагеле (смесь этилацетата с гексаном в соотношении 1:1), получая таким образом 2,7 г нужного продукта (выход 82,0%). Белые кристаллические гранулы, температура плавления 128 - 130oC.
Пример 2. Синтез N-(2-хлор-2-пропенилсульфонил)-4,6- диметоксипиримидин-2-карбоксиамида (соединение N 23)
Растворяют 2,4 г (13 ммоль) 4,6-диметоксипиримидин-2-карбоновой кислоты, 2,0 г (13 ммоль) 2-хлор-2-пропенилсульфонамида и 3,9 г (39 ммоль) триэтиламина в 50 мл дихлорметана, и смесь затем перемешивают в течение 30 мин при комнатной температуре. Затем к смеси добавляют 3,0 г (13 ммоль) 70% диэтилцианофосфата, и всю смесь перемешивают при комнатной температуре в течение ночи. Реакционную смесь промывают разбавленной соляной кислотой, чтобы удалить избыток триэтиламина, после чего продукт экстрагируют 50 мл насыщенного водного раствора бикарбоната натрия. Экстракт подкисляют разбавленной соляной кислотой до достижения pH 2 ≈ 3. Органический слой экстрагируют дважды 200 мл этилацетата. Экстракт промывают водой, органический слой сушат над безводным сульфатом магния и затем концентрируют при пониженном давлении, и получают 1,8 г вязкой жидкости. Вязкую жидкость очищают колоночной хроматографией на силикагеле (этилацетат : гексан = 1:1), получая таким образом 1,4 г нужного продукта (выход 33,7%). Порошок желтого цвета, температура плавления 125 -130oC.
Пример 3. Синтез 4,6-диметокси-N-метоксиметил-N- пропилсульфонилпиримидин-2-карбоксиамида (соединение N 48)
К раствору, содержащему 2,0 г (6,8 ммоль) 4,6-диметокси-N-пропилсульфонилпиримидин-2-карбоновой кислоты, растворенной в 100 мл N,N-диметилформамида, добавляют 0,32 г (8,0 ммоль) гидрида натрия небольшими порциями, и смесь затем перемешивают в течение 1 ч при комнатной температуре. После этого к смеси добавляют 0,54 г (6,8 ммоль) метоксиметилхлорида, и всю смесь перемешивают при комнатной температуре в течение 1 ч. Реакционную смесь выливают в воду. Органический слой экстрагируют толуолом и сушат над безводным сульфатом магния и затем концентрируют при пониженном давлении, получают сырой продукт, содержащий 4,6-диметокси-N-метоксиметил-N-пропилсульфонилпиримидин-2- карбоксиамид. Сырой продукт очищают колоночной хроматографией на силикагеле (этилацетат : гексан = 1:1), получая таким образом 0,5 г нужного продукта (выход 22,1%). Порошок белого цвета, температура плавления 59 - 62oC.
Пример 4. Синтез натриевой соли 4,6-диметокси-N-пропилсульфонилпиримидин-2-карбоксиамида (соединение N 70)
К раствору, содержащему 1,0 г (3,5 ммоль) 4,6-диметокси-N-пропилсульфонилпиримидин-2-карбоновой кислоты, растворенной в 20 мл метанола, добавляют 0,7 г (3,6 ммоль) метоксида натрия, и смесь затем перемешивают в течение 1 ч при комнатной температуре. Реакционную смесь концентрируют. К полученному остатку добавляют эфир. Кристаллы отфильтровывают, промывают эфиром и затем сушат, получая таким образом 0,9 г нужного продукта. Порошок белого цвета, температура плавления 161 -164oC.
Пример 5. Синтез 4,6-диметокси-N-бутилсульфонилпиримидин-2- карбоксиамида (соединение N 6)
Растворяют 3,0 г (16 ммоль) 4,6-диметоксипиримидин-2-карбоновой кислоты, 2,6 г (16 ммоль) бутилсульфонилизоцианата и 1,8 г (16 ммоль) триэтиламина в 200 мл хлороформа, и смесь затем перемешивают в течение 6 ч при комнатной температуре. После этого реакционную смесь промывают 10%-ной соляной кислотой и водой, органический слой сушат над безводным сульфатом магния и затем концентрируют при пониженном давлении, получают сырой продукт, содержащий 4,6-диметокси-N-бутилсульфонилпиримидин-2-карбоксиамид. Сырой продукт очищают колоночной хроматографией на силикагеле (этилацетат : гексан = 1:1), получая, таким образом, 1,5 г нужного продукта (выход 30,3%). Порошок белого цвета, температура плавления 82 - 83oC.
Пример 6. Синтез 4,6-диметокси-N-(изопропиламиносульфонил)пиримидин-2-карбоксиамида (соединение N 118)
К раствору, содержащему 3,0 г (16 ммоль) 4,6-диметоксипиримидин- 2-карбоновой кислоты, растворенной в 100 мл дихлорметана, добавляют небольшими порциями 2,8 г (20 ммоль) хлорсульфонилизоцианата, и смесь затем перемешивают в течение 1 ч при комнатной температуре. После этого к реакционной смеси при комнатной температуре добавляют по каплям 3,0 г (50 ммоль) изопропиламина, и смесь перемешивают при комнатной температуре в течение 3 ч. Реакционную смесь промывают 10%-ной соляной кислотой и водой. Органический слой сушат над безводным сульфатом магния и затем концентрируют при пониженном давлении, получают сырой продукт, содержащий 4,6-диметокси-N-(изопропиламиносульфонил)пиримидин-2-карбоксиамид. Сырой продукт очищают колоночной хроматографией на силикагеле (этилацетат : гексан = 1:3), получая, таким образом, 0,8 г нужного продукта (выход 16,0%). Порошок белого цвета, температура плавления 167 - 169oC.
Биоцид, соответствующий настоящему изобретению, представляет собой композицию, содержащую в качестве активного ингредиента производное N-сульфонамида (-N-сульфонилкарбоксиамида), включающего N-содержащее 6-членное ароматическое кольцо, изображаемое формулой [I]. В случае, когда соединения, соответствующие настоящему изобретению, используют в качестве биоцида, соединения, действующие как активный ингредиент, могут быть введены в подходящие составы, в зависимости от целей использования. Активный ингредиент обычно разбавляют инертной жидкостью или твердым носителем и при необходимости добавляют поверхностно-активное вещество, диспергатор, адъювант и т.п. Смесь затем формулируют в тонкий порошок, смачиваемый порошок, эмульгируемый концентрат, гранулы и т.п.
В качестве подходящего носителя, используемого в формулировке, здесь могут быть упомянуты, например, такие твердые носители, как тальк, бентонит, глина, диатомовая земля, белая сажа, вермикулит, каолин, гашеная известь, сульфат аммония, мочевина или т.п.; и такие жидкие носители, как изопропиловый спирт, ксилол, циклогексанон, метилнафталин, и т.п. Иллюстративные примеры поверхностно-активных веществ и диспергаторов включают соли динафтилметансульфоновой кислоты, алкиарилсульфоновой кислоты и лигносульфоновой кислоты, сульфатэфиры спирта, простые эфиры полиоксиэтиленгликоля, простые эфиры полиоксиэтиленалкиларила, моноалкилаты полиоксиэтиленсорбитана и т.п. Подходящими примерами вспомогательных веществ являются карбоксиметилцеллюлоза и т.п. Эти препараты могут применяться непосредственно или после разбавления до нужной концентрации.
Биоцид, соответствующий настоящему изобретению, может использоваться для опрыскивания стеблей и листвы, введения в воду для орошения или для внесения в почву. Количество активного ингредиента выбирают в зависимости от требований. Когда формулировку готовят в виде тонкого порошка или гранул, предпочтительно содержание активного ингредиента от 0,1 до 20 мас.%. Для эмульгируемого концентрата или смачиваемого порошка адекватным является количество активного ингредиента от 5 до 80 мас.%.
Дозы применения биоцида, соответствующего настоящему изобретению, могут изменяться в зависимости от типа используемого активного соединения, вида вредителя или заболевания, с которыми проводится борьба, природы проявления вредителя или заболевания, степени повреждений, окружающей среды, формы, в которой используется препарат, и т.п. Когда биоцид настоящего изобретения применяют непосредственно в виде тонкого порошка или гранул, рекомендуется выбирать дозу применения активного ингредиента в интервале от 0,1 г до 5 кг на 10 ар /0,1 га/, предпочтительно - в интервале от 1 г до 1 кг на 10 ар. Когда же биоцид настоящего изобретения находится в жидкой форме, такой как эмульгируемый концентрат, или в виде смачиваемого порошка, рекомендуется выбирать дозу применения активного ингредиента в интервале от 0,1 до 10000 ppm, предпочтительно - в интервале от 10 до 3000 ppm.
Биоциды, соответствующие настоящему изобретению, в составе описанных выше формулировок могут применяться для борьбы с заболеваниями растений, вызванными грибом, принадлежащим к Oomycetes. Такой гриб включает, но не ограничивается ими, Pseudoperonospora, такого как возбудителя ложной мучнистой росы на огурцах (Pseudoperonospora cubensis), Plasmopara, такого как возбудителя ложной мучнистой росы винограда (Plasmopara Vibicola), и Phytophtora, такого как возбудителя фитофтороза томата (Phytophtora intestans).
Биоцид, соответствующий настоящему изобретению, при необходимости может использоваться в сочетании с фунгицидами, инсектицидами, гербицидами, модификаторами роста растений, удобрениями или т.п.
Далее характерные формулировки иллюстрируются следующими далее примерами составов, в которых все проценты означают массовые проценты.
Пример состава 1
Тонкоизмельченный порошок
Смешивают до однородного состояния 2% соединения (93), 5% диатомовой земли и 93% глины и измельчают в тонкий порошок.
Пример состава 2
Смачиваемый порошок
Смешивают до однородного состояния 50% соединения (95), 45% диатомовой земли, 2% динафтилметансульфоната натрия и 3% лигносульфоната натрия и размалывают в смачиваемый порошок.
Пример состава 3
Эмульгируемый концентрат
Готовят однородный раствор из 30% соединения (80), 20% циклогексанона, 11% простого полиоксиэтиленалкиларильного эфира, 4% алкилбензолсульфоната кальция и 35% метилнафталина, получая таким образом эмульгируемый концентрат.
Пример состава 4
Гранулы
Смешивают до однородного состояния 5% соединения (98), 2% лаурилсульфоната натрия, 5% лигносульфоната натрия, 2% карбоксиметилцеллюлозы и 86% глины и размалывают. К размолотой смеси добавляют 20% воды. Полученную в результате смесь перемешивают и формуют в гранулы размером 14 - 32 меш с помощью экструзионного гранулятора, и затем сушат, получая нужные гранулы.
Биоцид, соответствующий настоящему изобретению, может быть использован в качестве гербицида для борьбы с вредными сорняками. В таком случае, что касается применения и прочего формулировки, предпочтительно, чтобы биоцид использовался в состояниях, наилучших для использования его в качестве гербицида. Однако, даже в состояниях, описанных для биоцида выше, биоцид, соответствующий настоящему изобретению, может осуществить задачи гербицида.
Эффект изобретения
Производные N-сульфонилкарбоксиамида, включающие N-содержащее 6-членное ароматическое кольцо, соответствующие настоящему изобретению, обнаруживают не только превосходную способность предотвращать заражение грибом, то также обнаруживает превосходную способность выводить патогенный гриб, принадлежащий к Oomycetes, после того, как он внедрился в растение-хозяина, вызывая заболевание растения, особенно при таких заболеваниях, как ложная мучнистая роса и фитофтороз, при низкой концентрации по сравнению с известными соединениями, описанными в заявке на патент Японии, первая публикация N Hei 2-282371. Кроме того, биоциды, соответствующие настоящему изобретению, имеют отличные показатели по таким свойствам, как остаточная активность и сопротивление действию осадков.
Кроме того, соединения, соответствующие настоящему изобретению, могут также бороться с сорняками, встречающимися на рисовых полях и на вспаханных полях. Соединения превосходно действуют против различных сорняков на вспаханных полях, включая широколистные сорняки, такие как duck-leaved, стройный амарант, марь белая обыкновенная, ипомея голубая, обыкновенный Cucklebur и т. п., так же, как и против многолетних и однолетних сорняков типа сыти, таких как purple nutsedge, yellow nutsedge, himekugu (cyperus brevifolius), осока, рисова сыть вееровидная, и т.п., и злаковых сорняков, таких как просо петушье, сорго алепское, лисохвост мышехвостниковидный и т.п., начиная от стадии прорастания и на стадии роста. Кроме того, соединения можно также применять для борьбы с однолетними сорняками на рисовых полях, с такими как ранняя горчица полевая, smallflower, ряска (утиный язык) и т.п., так же, как и против многолетних сорняков, таких как остролист японский (Japanese ribbon wapato), водяная сыть (water nutgrass), водяной каштан, японский камыш озерный, стрелолист узколистный, и т.п.
В качестве подходящих культур здесь можно упомянуть растения риса, обычные полевые культуры, фруктовые деревья и т.п.
Действие биоцидов, соответствующих настоящему изобретению, теперь будет иллюстрироваться следующими далее испытательными примерами.
Испытательный пример 1
Испытания эффективности предотвращения заражения огурцов ложной мучнистой росой (Pseudoperonospora cubensis).
Семена огурцов (сорт Sagaminanjiro) высевают в поливинилхлоридные (ПВХ) горшочки, с длиной каждой стороны 9 см, по 12 семян в каждый горшок. Семенам позволяют расти в теплице в течение 7 дней до стадии появления семядолей. Смачиваемый порошок, полученный в примере состава 2, разбавляют водой до концентрации 500 ppm активного ингредиента, и полученный водный препарат наносят в количестве 10 мл на горшок с рассадой в стадии семядолей. После высыхания на воздухе растения инокулируют спорами гриба, вызывающего на огурцах ложную мучнистую росу (Pseudoperonospora cubensis), и затем помещают во влажную камеру при 22oC на 24 ч, а затем помещают в теплицу. На седьмой день после инокуляции оценивают распространенность повреждений в соответствии с приведенными далее стандартами оценок, чтобы подтвердить предотвращающее действие соединений, соответствующих настоящему изобретению Результаты испытаний даются в табл. 3.
Для сравнения используют следующие соединения, раскрытые в заявке на патент Японии N Hei 2-282371:
Соединение для сравнения A: N-(2-хлорфенилсульфонил)-4,6- диметоксипиримидин-2-карбоксиамид;
Соединение для сравнения B: N-(2,6-дихлорфенилсульфонил)-4,6- диметоксипиримидин-2-карбоксиамид.
Стандарты оценок:
Группа A: повреждения не наблюдаются.
Группа B: площадь распространения менее 25%.
Группа C: площадь распространения 25% и более, но менее 50%.
Группа D: площадь распространения 50% и более (табл. 3).
Испытательный пример 2
Испытания эффективности обработки при заражении огурцов ложной мучнистой росой (Pseudoperonospora cubensis).
Семена огурцов (сорт Sagami hanjiro) высевают в поливинилхлоридные (ПВХ) горшки со стороной 9 см, по 12 семян в каждый горшок. Семенам позволяют прорастать в условиях теплицы в течение 7 дней до стадии семядолей. Сеянцы инокулируют путем опрыскивания суспензией зооспорангия гриба, вызывающего ложную мучнистую росу огурцов (Pseudoperonospora cubensis) и затем помещают во влажную камеру при 22oC на 24 ч. После высушивания на воздухе проводят обработку всходов огурцов водным препаратом, полученным при разбавлении водой смачиваемого порошка, изготовленного в примере состава 2, до концентрации 500 ppm, при дозе 10 мл на горшок. Всходы затем помещают в теплицу. На седьмой день после инокуляции оценивают степень поражения в соответствии со стандартами оценок, данными в испытательном примере 1, чтобы оценить действие обработки соединениями, соответствующими настоящему изобретению, зараженных растений. Результаты испытаний даются в табл. 4.
Испытательный пример 3
Испытания гербицидной эффективности при обработке почвы рисового поля
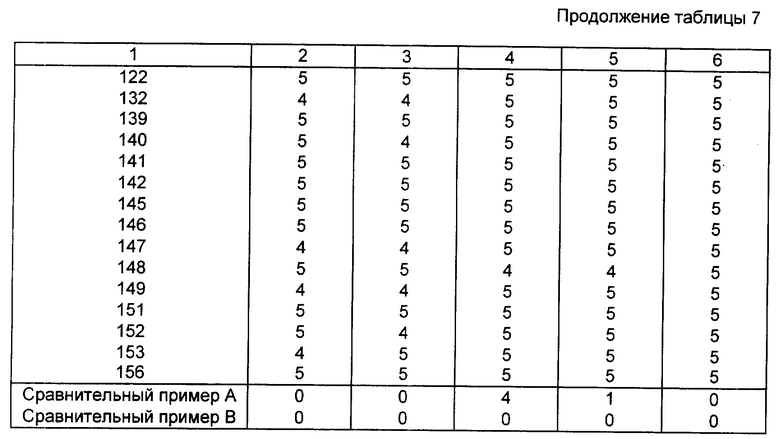
В пластмассовый вегетационный сосуд (100 см2), наполненный почвой с рисового поля, высевают раннюю горчицу полевую (сокращенно Eo), ряску (утиный язык) (сокращенно Mo) и японский озерный камыш (сокращенно Sc) и заливают водой слоем в 3 см. На следующий день смачиваемый порошок, полученный в соответствии с примером формулировки 2, разбавляют водой и обрабатывают почву с рисового поля с водой при дозе 100 г активного ингредиента на 10 ар, и вслед за этим оставляют для выращивания в теплице. Гербицидную оценку проводят на 21 день после обработки. Результаты оценивают в соответствии со стандартами, указанными в табл. 5, и представляют их в табл. 6 под соответствующими цифровыми индексами.
В качестве веществ для сравнения используют те же самые соединения, которые указаны в испытательном примере 1.
Испытательный пример 4
Испытание гербицидной эффективности при обработке почвы вспаханного поля
В пластмассовый вегетационный сосуд (120 см2), наполненный почвой со вспаханного поля, всевают петушье просо (сокращенно Ec), duck-leared (сокращенно Po), стройный арамант (сокращенно Am), обыкновенную марь белую (сокращенно Ch) и riceflatsedge (сокращенно Ci) и присыпают почвой. Смачиваемый порошок, полученный в соответствии с примером формулировки 2, разбавляют водой и равномерно распыляют по поверхности почвы со вспаханного поля, используя компактный разбрызгиватель, при дозе 100 л смачиваемого порошка на 100 ар, с таким расчетом, чтобы количество активного ингредиента составляло 400 г на 10 ар, и вслед за этим помещают для роста в теплицу. Гербицидную оценку проводят на 21 день после обработки. Результаты оценивают в соответствии со стандартами, приведенными в табл. 5, и представляют их в табл. 7 под соответствующими цифровыми индексами.
В качестве веществ для сравнения используют те же самые соединения, что в испытательном примере 1.
Испытательный пример 5
Испытания гербицидной эффективности при обработке стеблей и листвы
В пластмассовый вегетационный сосуд (120 см2), наполненный почвой со вспаханного поля, высевают петушье просо (сокращенно Ec), duck-leaved (сокращенно Po), стройный амарант (сокращенно Am), обыкновенную марь белую (сокращенно Ch) и rice flatsedge (сокращенно Ci) и затем помещают для выращивания в теплицу на 2 нед. Смачиваемый порошок, полученный в соответствии с примером формулировки 2, разбавляют водой и опрыскивают стебли и листву растений, обрабатывая все растение, начиная с верхней части, используя компактный разбрызгиватель, при дозе 100 л смачиваемого порошка на 10 ар, с таким расчетом, чтобы количество активного ингредиента составляло 400 г на 10 ар, и вслед за этим помещают в теплицу. Гербицидную оценку проводят на 14 день после обработки. Результаты оценивают в соответствии со стандартами, приведенными в табл. 5, и приводят их под соответствующими цифровыми индексами в табл. 8.
В качестве веществ для сравнения используют те же соединения, которые упоминаются в испытательном примере 1.
Испытательный пример 6
Испытания избирательности действия при обработке почвы со вспаханного поля
В пластмассовый вегетационный сосуд (600 см2), наполненный почвой со вспаханного поля, высевают семена культурной сои (сокращенно Gl), ипомеи голубой (сокращенно Ip) и обыкновенного cucklebur (сокращенно Xa) и присыпают почвой. На следующий день предварительно определенное эффективное количество (а. и. , г/10 ар) смачиваемого порошка, приготовленного в соответствии с примером формулировки 1, разбавляют водой, разбрызгивают равномерно по поверхности почвы со вспаханного поля, используя компактный разбрызгиватель, при дозе 100 л смачиваемого порошка на 10 ар, и затем помещают в теплицу. Гербицидную оценку проводят на 21 день после обработки. Результаты оценивают в соответствии со стандартами, приведенными в табл. 5, и представляют их в табл. 9 под соответствующими цифровыми индексами.
Испытательный пример 7
Испытания избирательности действия при обработке стеблей и листвы растений
В пластмассовый вегетационный сосуд (600 см2), наполненный почвой со вспаханного поля, высевают семена культурной сои (сокращенно Gl), ипомеи голубой (сокращенно Ip) и обыкновенного cucklebur (сокращенно Xa) и присыпают почвой, и вслед за этим помещают в теплицу для выращивания на 2 нед. Предварительно определенное эффективное количество (акт. ингр., г/10 ар) смачиваемого порошка, полученного в соответствии с примером формулировки 1, разбавляют водой и равномерно разбрызгивают по стеблям и листьям растений, по всему растению, начиная с верхней части, используя компактный разбрызгиватель, при дозе 100 л смачиваемого порошка на 10 ар, и помещают в теплицу. Гербицидную оценку проводят на 14 день после обработки. Результаты оценивают в соответствии со стандартами, установленными в табл. 5, и представляют в табл. 10 под соответствующими цифровыми индексами.
Испытательный пример 8
Испытание гербицидной эффективности при обработке почвы затопляемого рисового поля
В пластиковый горшок (100 см2), заполненный почвой с рисового поля, высевали семена раннего петушьего проса (используемая аббревиатура Eo), чемерицы зеленой (используемая аббревиатура Mo) и камыша японского (используемая аббревиатура Sc), после чего почву заливали водой на глубину до 3 см. На следующий день смачиваемый порошок, полученный в соответствии с примером состава 2, разбавляли водой и по каплям вводили в почву затопляемого рисового поля с водой при норме расхода 100 г активного ингредиента на 10 ар, после чего семена проращивали в теплице. Гербицидную оценку производили на 21-й день после обработки. Результаты определяли в соответствии со стандартами, как указано в табл. 11 и показано с помощью индексов в табл. 12.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОНДЕНСИРОВАННОЕ ГЕТЕРОЦИКЛИЧЕСКОЕ ПРОИЗВОДНОЕ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ГЕРБИЦИДНОЕ СРЕДСТВО | 1993 |
|
RU2105005C1 |
| ПРОИЗВОДНЫЕ АМИДА АЛКАНОВОЙ КИСЛОТЫ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ, СПОСОБ УНИЧТОЖЕНИЯ СОРНЯКОВ | 1991 |
|
RU2061687C1 |
| ПРОИЗВОДНЫЕ НИКОТИНОВОЙ КИСЛОТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ | 1994 |
|
RU2133746C1 |
| ПРОИЗВОДНЫЕ ПИРИМИДИНА, СПОСОБ БОРЬБЫ С СОРНЯКАМИ И ГЕРБИЦИДНЫЙ СОСТАВ | 1990 |
|
RU2041214C1 |
| ПРОИЗВОДНОЕ ПИКОЛИНОВОЙ КИСЛОТЫ И ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2112774C1 |
| ПРОИЗВОДНОЕ БЕНЗИЛСУЛЬФИДА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПЕСТИЦИД | 1996 |
|
RU2170728C2 |
| ПРОИЗВОДНЫЕ ФЕНИЛАЛКАНАМИДА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И СЕЛЬСКОХОЗЯЙСТВЕННЫЙ ИЛИ САДОВЫЙ ФУНГИЦИД | 1996 |
|
RU2156235C2 |
| ПИРИМИДИНОВЫЕ ПРОИЗВОДНЫЕ | 1992 |
|
RU2028294C1 |
| ПРОИЗВОДНЫЕ ПИКОЛИНОВОЙ КИСЛОТЫ ИЛИ ИХ КИСЛОТНО-АДДИТИВНЫЕ СОЛИ, СПОСОБ ИХ ПОЛУЧЕНИЯ, НЕРБИЦИДНАЯ КОМПОЗИЦИЯ И СПОСОБ БОРЬБЫ С СОРНЯКАМИ | 1991 |
|
RU2091380C1 |
| ПРОИЗВОДНЫЕ ПИРИМИДИНИЛОКСИАЛКАНАМИДОВ И ФУНГИЦИДЫ ДЛЯ СЕЛЬСКОГО ХОЗЯЙСТВА ИЛИ САДОВОДСТВА | 1997 |
|
RU2194040C2 |





Производные амида N-сульфонилкарбоновой кислоты, включающие N-содержащее 6-членное ароматическое кольцо, формулы
где R1 - C1-C10-алкил, возможно содержащий один или два заместителя, выбранных из галогена, C3-C5-циклоалкила, C1-C3-алкилтио, C1-C4-алкилсульфонила, C1-C4-алкоксикарбонила, C2-C4-алкилкарбонила, либо R1 - C2-C6-алкенил, C2-C6-алкинил, цикло-C5-C6-алкил, пирролидинил и др. R2 - водород, (низший) алкокси (низший) алкил, R3 и R4 - независимо представляют галоген, C1-C4-алкил и др. Соединения рекомендуются для создания фунгицидных и гербицидных композиций, которые используются для борьбы с сорняками и фитопатогенными грибками. 5 с. и 2 з.п. ф-лы, 12 табл.

где R1 - С1 - С10-алкил, необязательно содержащий один или два заместителя, выбираемых из группы, включающей галоген, С3 - С5-циклоалкил, С1 - С3-алкилтио, С1 - С4-алкилсульфинил, С1 - С4-алоксикарбонил, С2 - С4-алкилкарбонил, либо R1 - С2 - С6-алкенил, необязательно содержащий один или два заместителя, выбранных из галогена, либо R1 - С2 - С6-алкинил, либо R1 - цикло-С5 - С6-алкил, который может быть замещен оксогруппой, либо R1 - 1-пирролидинил, 2-метил-1-пиперидинл, 1-азиридинил, группа R5R6N-;
R2 - водород, (низший)алкокси(низший)алкил;
R3 и R4 независимо друг от друга - галоген, С1 - С4-алкил, низший алкокси, ди(низший)алкиламино;
R5 и R6 независимо друг от друга - водород, С1 - С5-алкил, низшая алкоксигруппа, низший алкенил, цикло(низший)алкил, низший алкинил, С1 - С4-алкокси-С1 - С4-алкил.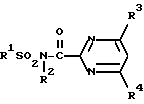
где R1 - С1 - С6-алкил, необязательно содержащий один или два заместителя, выбраныых из группы, включающей галоген, С3 - С5-циклоалкил, С1 - С4-алкилтио и оксиранильную группу; или С2 - С6-алкенил, необязательно содержащий 1 или 2 галогена, или группу -NR5R6, в которой R5 - водород, С1 - С4-алкил, R6 - С1 - С4-алкил, С2 - С5-алкинил, С3 - С5-циклоалкил, R2 - водород, С1 - С4-алкокси-С1 - С4-алкил, R3 - галоген, С1 - С4-алкил, С1 - С4-алкокси, R4 - С1 - С4-алкокси, ди(С1 - С4)-алкиламино, в эффективном количестве.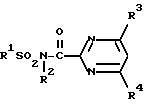
где R1 - С1 - С6-алкил, необязательно содержащий один или два заместителя, выбранных из группы, включающей галоген, С3 - С5-циклоалкил, С1 - С4-алкилтио, С1 - С4-алкилсульфинил, С1 - С4-алкоксикарбонил, С2 - С4-алкилкарбонил; С2 - С6-алкенильная группа, необязательно содержащая один или два заместителя, выбранных из галогена, С2 - С6-алкинил, С5 - С6-циклоалкил, который может быть замещен оксогруппой, 1-пирролидинил, 2-метил-1-пиперидинил, 1-азиридинил или группа -NR5R6, в которой R5 - водород, С1 - С4-алкил, С1 - С4-алкокси, R6 - С1 - С4-алкил, С2 - С5-алкенил, С1 - С4-алкокси-С1 - С4-алкил;
R2 - водород, С1 - С4-алкокси-С1 - С4-алкил;
R3 - галоген, С1 - С4-алкил, С1 - С4-алкокси;
R4 - С1 - С4-алкил, С1 - С4-алкокси, ди(С1 - С4)-алкиламино,
в эффективном количестве.
| JP, патент, 58-29785, С 07 С 143/82, 1983 | |||
| DE, патент, 3800267, C 07 D 403/06, 1989 | |||
| EP, патент, 444286, C 07 D 239/28, 1991. |
Авторы
Даты
1998-08-20—Публикация
1993-03-03—Подача