Изобретение относится к системам аккумулирования и генерирования энергии, в которых протекают обратимые химические реакции на противолежащих положительном (аноде) и отрицательном (катоде) электродах, и энергия накапливается в электролите (и извлекается из него) в зарядном и разрядном циклах. Реакции, представляющие интерес с точки зрения этого изобретения, являются по существу обратимыми, так что протекающий в такой системе ток заряжает ее путем накопления энергии в химических реагентах. Электрохимические реакции протекают на каждой стороне ионообменной мембраны, а через мембрану носители заряда переносятся селективно. Во время выделения энергии эти химические реакции идут в обратном направлении, осуществляя подачу тока (энергии) на нагрузку. В частности, данное изобретение относится к системам с регулированием величины pH электролита.
Для того, чтобы восстановить исходное состояние ячейки, в некоторых системах осуществляют восстановление или регенерацию реагентов вне ячейки, в отличие от систем, в которых проводят этот процесс путем пропускания тока через ячейку.
Такие системы для накопления и выделения энергии были известны в течение многих лет. Основные недостатки таких систем вытекали из практического применения того, что кажется простым прямым химическим процессом. Практические проблемы в таких системах также связаны с использованием вредных материалов, эффективностью, размером системы, закупориванием и засорением, образованием газа, осаждением на электроде и выпадением в осадок материалов, ограничениями по диффузии через мембрану, ценой материалов и стоимостью эксплуатации. Другим ограничением таких систем является снижение выхода энергии по мере разряда.
Основной химический процесс в этих системах характеризуется химическим уравнением, в котором реакция протекает в одном направлении при заряде системы и в противоположном направлении при генерировании системой энергии. Примером редокс-системы, т.е. системы, в которой восстановление и дополняющее его окисление протекают совместно, является система, описываемая следующим химическим уравнением:
Cr2+ + Fe3+ ⇄ Cr3+ = Fe2+ (1)
Недостатком этой системы является то, что хром дорог, кроме того, хром и железо, которые находятся на одной из сторон мембраны, проникают сквозь нее, загрязняя другую сторону. Это вызывает необходимость частой переработки электролита. Кроме того, для ускорения реакции необходимы катализаторы из благородных металлов. Известна система [1], в которой осуществляют постоянное противодействие тенденции возрастания pH.
Другим примером электрохимической ячейки для получения электроэнергии является элемент цинк-бром, в котором общую химическую реакцию можно записать следующим образом:
Zn + Br2 ⇄ Zn2+ + 2Br- (1a)
Основным недостатком этой системы является неоднородность осаждения цинка на электроде, что приводит к неустойчивости при циклировании комплекта ячеек.
Известна батарея цинк-бром [3], в которой цинк образует отрицательный электрод и участвует в электрохимических реакциях в ячейке. Одной из побочных реакций является выделение водорода с сопутствующей потерей ионов водорода в отрицательном электролите и повышением pH. Известная батарея снабжена средствами регулирования pH отрицательного электролита в направлении понижения путем выделения ионов водорода.
Наиболее близкой к предложенному изобретению по технической сущности и достигаемому эффекту является система [2] , в которой используют пару бром/сульфид. В [2] приведено описание электрически перезаряжаемой анионоактивной системы для накопления и выделения энергии с использованием реакции сульфид-полисульфид в католите и реакции иодид- полииодид, хлорид-хлор или бромид-бром в анолите с рециркулирующими электролитами.
Было обнаружено, что недостатком работы системы [2], в которой используют пару бром/сульфид, является то, что pH католита падает при периодическом циклировании системы, что приводит к тому, что ионы Н+ диффундируют и переносятся путем миграции в анолит, что приводит также к снижению pH анолита с сопутствующим образованием H2S.
Задачей настоящего изобретения является создание способа аккумулирования и/или генерирования энергии и устройства, в котором изменение величины pH и/или изменение концентрации гидроксил-ионов в каждой или в обеих камерах элемента компенсируется выделением гидроксил-ионов.
Задачей данного изобретения является также создание такого способа, в котором может быть осуществлена химическая перезарядка путем замены или восстановления одного или обоих электролитов вне элемента, что поддерживает элемент в работоспособном состоянии.
Задачей данного изобретения является также создание экономичного, т.е. электрически перезаряжаемого, устройства для получения энергии.
Кроме того, задачей данного изобретения является создание способа с достаточно высокой удельной энергией для практических применений.
Помимо этого, задачей данного изобретения является обеспечение достаточно полной отдачи энергии даже при низкой степени заряда системы, т.е. подача энергии системой остается относительно постоянной во времени, поддерживая практически одинаковый выход почти до полного разряда.
Поставленная задача решается в системе путем использования средств, позволяющих компенсировать изменения pH в электролите, включающих средства генерирования ОН- ионов путем разложения воды.
Таким образом, один из вариантов настоящего изобретения представляет собой электрохимическое устройство для аккумулирования и/или подачи энергии, содержащее
средства поддержания и циркулирования потоков электролита в полностью жидкостной системе, в которой активные составляющие полностью растворимы, в единичной ячейке или в комплекте повторяющихся структур ячеек, каждая из которых имеет камеру анолита, содержащую инертный положительный электрод и камеру католита, содержащую инертный отрицательный электрод, причем эти камеры отделены друг от друга ионообменной мембраной, электролит, циркулирующий в камере католита каждой ячейки в процессе генерирования энергии, содержит полностью растворимый сульфид, а электролит, циркулирующий в камере анолита в процессе генерирования энергии, содержит жидкий окисляющий агент,
средства восстановления и восполнения электролитов в камерах анолита и католита путем циркуляции электролита из каждой камеры к средствам хранения электролита, содержащим объем электролита, превышающий объем ячейки, и дополнительно средства компенсации изменений величины pH и/или изменений концентрации гидроксил-ионов в камере анолита, включающие средства генерирования OH- ионов путем разложения воды.
В другом варианте реализации данного изобретения предложен электрохимический способ аккумулирования и/или подачи энергии, включающий
поддержание и осуществление циркуляции потоков электролита в полностью жидкостной системе, активные компоненты которой полностью растворимы в отдельной ячейке или в наборе повторяющихся ячеек, в котором каждая ячейка имеет камеру анолита, содержащую инертный положительный электрод, и камеру католита, содержащую инертный отрицательный электрод, при этом камеры отделены друг от друга ионообменной мембраной, электролит, циркулирующий в камере католита каждой ячейки в процессе получения энергии содержит полностью растворимый сульфид, а электролит, циркулирующий в камере анолита в процессе получения энергии, содержит жидкий окисляющий агент,
восстановление или восполнение электролитов в камерах анолита и католита путем циркуляции электролита из каждой камеры к средствам его хранения, вмещающим объем электролита, превышающий объем ячейки, и дополнительно
компенсацию изменений pH и/или изменений концентрации гидроксил- ионов в камере анолита путем генерирования ОН- ионов и газообразного водорода путем разложения воды.
В предпочтительном варианте исполнения данного изобретения жидким окислителем, циркулирующим через камеру анолита в процессе получения энергии, является бром, а протекающая химическая реакция описывается следующим уравнением:
Br2 + S2- ⇄ 2Br- + S (2)
где ионы образуются солями этих реагентов. Для уравнения (2) этими солями предпочтительно являются соли калия, KBr и K2S, но и соли натрия будут работать почти также успешно, за исключением того, что Na2S значительно меньше растворим, чем К2S. Система содержит набор ячеек, каждая из которых имеет положительный и отрицательный электроды. Ионообменная мембрана в каждой ячейке между электродами разделяет ячейку на камеры анолита и католита. Электрохимическая реакция уравнения (2) в действительности протекает в виде раздельных, но зависимых реакций брома и серы. Реакция с участием брома протекает на положительной стороне мембраны, а реакция с участием серы - на отрицательной стороне мембраны.
При заряде ячейки (восстановление состояния ячейки), уравнение (2) протекает справа налево, а при разряде (подаче энергии на нагрузку) уравнение (2) протекает слева направо.
С точки зрения реакции с участием брома, в процессе заряда ионы Na+ переносятся через мембрану с положительной стороны на отрицательную сторону для того, чтобы соблюдался баланс зарядов и происходило превращение Na2S5 в Na2S. Сера, которая присутствует в виде полисульфид-иона с зарядом 2 (S2- Sx, где х может быть до 4), восстанавливается сначала до S2- Sx-1 и окончательно до S2-. Br- окисляется до Br2, который переходит в раствор в виде трибромид-ионов Br3-, которые способны снова окислять ионы S2- до серы во время разряда. Свободный бром слабо растворим в воде - лишь 3-4 г на 100 см3 воды. Однако он очень хорошо растворим в растворах бромидов, с которыми образует полибромид-ионы. Основным источником брома является морская вода.
Молекулярный бром (Br2) образуется в качестве необходимого компонента электрохимической реакции, а Br2 имеет тенденцию реагировать с водой с образованием кислот, например (в упрощенной форме):
Br2+H2O ⇄ HBr + HBrO (3)
Присутствие активированного угля на поверхности положительного электрода ускоряет (катализирует) этот процесс образования кислот, поэтому он обычно не используется на положительном электроде. Но для химизма процесса на отрицательной стороне такой проблемы не существует, и на отрицательном электроде активированный уголь применяется.
В том случае, если положительный электрод испытывает частичный недостаток в реагентах, и если потенциал при заряде достаточно высок, с электрода будет выделяться и удаляться некоторое количество кислорода, что также приводит к возникновению ионов Н+ (кислоты) в электролите.
Такого образования кислоты следует избегать, или по крайней мере сводить его к минимуму, потому что ионы H+ будут диффундировать и переноситься путем миграции на отрицательную сторону через катионообменную мембрану. Все это приводит к понижению pH на отрицательной стороне и, естественно, к образованию H2S Следовательно, работа системы ухудшается. Данное изобретение обеспечивает механизм регулирования величины pH (выделение H+) на положительной стороне.
Поток электролитов на обеих сторонах мембраны создается предпочтительно с помощью рециркуляции, а не единичного сплошного потока, как в большинстве применений. Электролиты, которые подвергают рециркуляции, хранятся в независимых контейнерах, которые могут содержать достаточно большое количество электролита для обеспечения конкретных требований предпочтительного исполнения. Процесс циркуляции позволяет также фильтровать электролиты или иным способом восстанавливать их свойства на основе обычных методов без отключения системы.
В системе, содержащей бром, при циркуляции электролита у положительной стороны бром адсорбируется из электролита поверхностью положительного электрода и/или его пористой основой. Это обеспечивает качественную пористую структуру, в которой бром может находиться в более высоких концентрациях (т. е. является более доступным при высоких плотностях тока). Подобная пористая структура позволяет достигать большей площади поверхности, что улучшает эффективность при разряде. Указанный пористый материал предпочтительно содержит частицы диоксида кремния или смесь диоксид кремния/активированный уголь, причем эти частицы обеспечивают большую площадь поверхности. Можно использовать один активированный уголь, но это увеличивает гидролиз Br2 водой с образованием HBr и чрезмерным понижением pH. Диоксид кремния снижает образование кислоты. Пористая поверхность диоксида кремния поставляет бром, потребляемый при разряде и, таким образом, обеспечивает работу на полную мощность вплоть до состояния, близкого к полному разряду. При таком разряде выходное напряжение ячейки остается почти постоянным, с небольшими поляризационными потерями.
Следует понимать, что электролит, циркулирующий в положительной камере в процессе получения энергии, может содержать не бром, а другой жидкий окисляющий агент. Если величина pH в положительной камере падает во время электрохимической реакции, pH электролита в положительной камере будет регулироваться в соответствии с данным изобретением. Если pH в положительной камере не падает, то корректировка pH в этой камере путем генерирования ионов OH не требуется.
Способ и устройство в соответствии с настоящим изобретением можно использовать для регулирования pH и/или концентрации гидроксил-ионов только в отрицательной камере ячейки. Средства компенсации изменений pH и/или изменения концентрации гидроксил- ионов в отрицательной камере включают генерирование ионов OH-, так как отрицательная сторона ячейки обычно должна работать при высоком pH и/или в присутствии свободных гидроксил-ионов для того, чтобы избежать образования ионов HS- из сульфида, содержащегося в католите.
Отрицательная сторона системы представляет собой электрод, который адсорбирует раствор S2- для последующего разряда и улучшает работу системы подобно тому, как это описано для анода. Обычно используется пористый активированный уголь. Активированный уголь на катоде повышает скорость реакции сульфида.
В срединных электродах (также называемых промежуточными или биполярными электродами) происходит сочетание вышеописанных явлений так, что при этом на одной поверхности основы формируется положительный электрод и на другой поверхности этой же основы отрицательный электрод.
Возможна некоторая утечка сульфида путем диффузии через мембрану от отрицательной стороны к положительной стороне. Результатом этого является появление в электролите свободной серы, которая фильтруется в процессе циркуляции электролита. Одним из путей преодоления деградации системы из-за таких утечек является периодическое включение фильтра в систему циркуляции электролита с отрицательной стороны электрода. Затем сера повторно растворяется в виде полисульфида и возвращается в электролит для повторного использования.
В системе, содержащей бром, может также происходить диффузия ионов брома на отрицательную сторону электрода, что приводит к потерям реагента на положительной стороне, возникновению дисбаланса в составе электролита и кулоновским потерям. Эту ситуацию можно исправить путем введения в электролит на отрицательной стороне электрода NaBr в некоторой (начальной) концентрации для того, чтобы обеспечить наличие ионов Br-, которые диффундируют обратно к положительной стороне и таким образом уравновешивают миграцию брома с положительной стороны.
Устройство содержит средства переноса ионов, преимущественно для системы, содержащей бром, с мембраной, преимущественно на основе фторуглеродного полимера (имеющего высокую химическую стойкость по отношению к брому), к которому привит с помощью гамма-излучения стирол, содержащий концевые группы сульфоновой или карбоксильной кислот для создания носителей зарядов. Эта мембрана является катионоселективной (через нее может происходить перенос положительных ионов, таких как Na+), что также эффективно препятствует миграции S2- через мембрану.
В этой системе возможно также периодически заменять электролит, целиком или частично, не прерывая работы ячейки. Это позволяет обрабатывать или восполнять электролит вне ячейки.
В других предпочтительных вариантах реализации натрий заменяют на калий, литий или аммоний, или смесь их, или же на другие подходящие заменители, в одном или обоих растворах (брома и сульфида).
Другие задачи, отличительные признаки и преимущества изобретения станут очевидными из последующего детального описания предпочтительных вариантов исполнения элемента со ссылками на сопровождающие его фигуры.
На фиг. 1 изображены схематически основные компоненты ячейки, используемой в предпочтительном варианте исполнения данного изобретения; на фиг.2 - схема набора ячеек, использующих систему фиг.1, стадии изготовления которого приведены на фиг.3; на фиг.4 - блок-схема системы с потоком жидкости с использованием ячейки фиг.1; на фиг.5 - блок-схема системы контроля pH как на положительной стороне, так и на отрицательной стороне ячейки фиг.1; на фиг.6 - другой тип ячейки с контролем pH; на фиг.7 - еще один тип ячейки с контролем pH; на фиг.8 - блок-схема ячейки с контролем pH на отрицательной стороне; на фиг.9 - типичный цикл для одной ячейки; и на фиг.10-11 иллюстрируют систему контроля pH в ячейке, описанную в примере 2.
На фиг. 1 изображена ячейка 10 с положительным электродом 12 и отрицательным электродом 14 и катионной мембраной 16, выполненной из фторуглеродного полимера с функциональными группами стиролсульфоновой кислоты, поставляющими носителей заряда. Мембрана 16 разделяет положительную и отрицательную стороны ячейки 10 и выбрана так, чтобы свести к минимуму миграцию брома с положительной стороны к отрицательной стороне и свести к минимуму миграцию S2- ионов с отрицательной к положительной стороне. Водный раствор NaBr 22 находится в камере 22С, расположенной между анодом 12 и мембраной 16, а в камере 24С, расположенной между катодом 14 и мембраной 16, находится водный раствор Na2Sx 24. Раствор K2Sx, который является более растворимым и более дорогим, чем Na2Sx используется в других вариантах исполнения.
Когда ячейка разряжена, в камере 22С ячейки находится раствор NaBr с молярностью до 6,0 М, а в камере 24С ячейки находится раствор Na2S5 с молярностью от 0,5 до 1,0 М. При использовании K2S5 возможна более высокая молярность.
Когда ячейка заряжена, происходит перенос ионов Na+ через катионную мембрану 16, как показано на фиг.1, с положительной стороны на отрицательную сторону ячейки. При окислении бромид- ионов на аноде образуется свободный бром, который растворяется в виде трибромид- или пентабромид-ионов. Сера восстанавливается на катоде, а пентасульфид Na2S5 по окончании процесса зарядки превращается в моносульфид. На положительной стороне протекает следующая реакция:
2Br- ⇒ Br2+2e- (4)
на отрицательной стороне протекает следующая реакция:
S=2e- ⇒ S2- (5)
Мембрана разделяет два электролита и препятствует смешению их в объеме, а также замедляет миграцию ионов S2- с отрицательной стороны и миграцию (диффузию) Br- и Br2 с положительной стороны на отрицательную сторону. Диффузия S2- приводит к кулоновским потерям, а также к появлению взвешенных осадков в анолите. Любое количество ионов S2-, присутствующих на положительной стороне, будет окисляться бромом, получающимся в ходе заряда. Сера нерастворима в воде или растворе NaBr и будет выпадать в виде суспензии или осадка тонкого порошка.
При продолжительном циклировании может происходить накопление серы на положительной стороне ячейки. Если сера улавливается встроенным в линию фильтром, она может быть возвращена к отрицательной стороне для повторного растворения при достаточно продолжительном времени работы.
При выделении энергии ячейка разряжается. В ходе этого процесса на обоих электродах идут обратимые реакции. На положительном электроде ион S2- окисляется до молекулярной серы. Электроны, образующиеся на отрицательном электроде, обеспечивают ток через нагрузку. Химическая реакция на аноде обеспечивает от 1,06 до 1,09 В, а химическая реакция на катоде обеспечивает от 0,48 до 0,52 В. Объединенные химические реакции создают напряжение разомкнутой цепи от 1,54 до 1,61 В на элемент.
Удельная энергия пары бром/сера будет лимитироваться допустимой максимальной концентрацией Br2 у положительной стороны, а не растворимостью используемых солей, таких как NaBr и Na2S, которая достаточно высока.
В процессе окислительно-восстановительных реакций реагирующие ионы S2- и Br- возвращаются в элементарное состояние. Катион, связанный с ними, не принимает участия в процессе получения энергии. Следовательно, катионы выбираются из соображений удобства. Предпочтительно выбирают катионы натрия или калия. Соединения натрия и калия доступны, они недороги и хорошо растворимы в воде. Возможно также использовать соли лития и аммония, но они дороже.
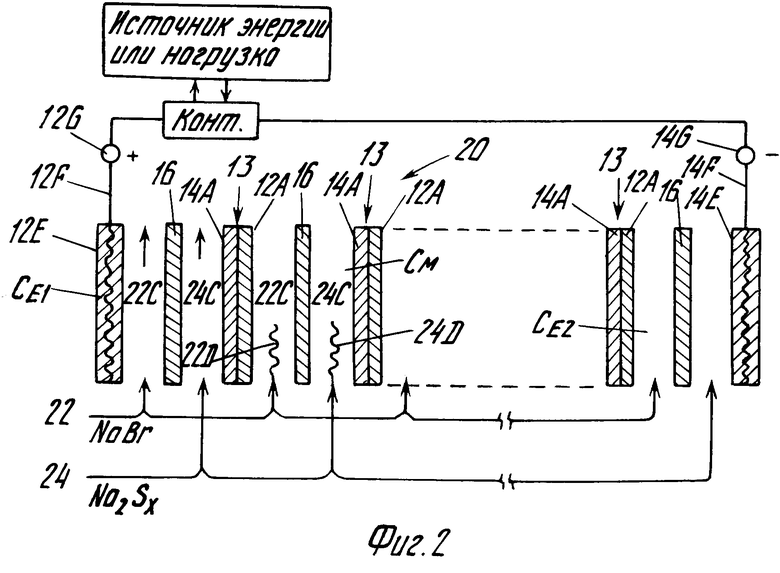
На фиг. 2 изображен набор 20 из нескольких ячеек, соединенных последовательно в электрическом и параллельно в жидкостном отношении. Ряд промежуточных электродов 13 (каждый из которых имеет положительную электродную сторону 12A и отрицательную электродную сторону 14A) и концевые электроды 12E (анод) и 14E (катод) отделены друг от друга мембранами 16 и экранами или сетчатыми разделителями (22D, 24D) во всех камерах ячейки 22C, 24C (части двух деталей 22D, 24C показаны в виде примера) с образованием концевых ячеек CE1и CE2 и ряда промежуточных ячеек CM (обычно 10-20; но следует отметить, что возможно использование значительно меньшего и значительно большего числа ячеек). Концевые электроды 12E (анод) и 14E (катод) имеют внутренние проводники 12F и 14F (обычно медные сетки), заключенные внутри них и переходящие во внешние выводы 12G, 14G, которые соединены с внешними нагрузками (например, с двигателем (двигателями) через контрольную цепь (CONT), а двигатель (двигатели) приводит в действие транспортное средство); или с источниками энергии (например, с сетью энергоснабжения при использовании элемента в качестве буферного устройства).
На фиг. 3 изображен вариант заключения в корпус набора ячеек, подобного изображенному на фиг.2. Набор ячеек 20 (такой, как показан на фиг.2) размещают между зажимными блоками СВ и погружают одной кромкой в неглубокий контейнер, в котором находится ванна с жидкой эпоксидной смолой (не показана). Эпоксидная смола затвердевает, образуя стенку батареи. Устройство снабжено трубопроводами для потоков, например 22М, с подводящими трубами 22Н для подачи раствора NaBr (подобное же устройство предназначено для подачи раствора сульфида натрия; не показано). Эти трубопроводы заделываются одновременно с кромками электродов и мембран.
Батарея поворачивается на 90o, и процесс повторяется трижды для образования четырех стенок. Трубопроводы и трубы для удаления электролита расположены в верхней части. Можно провести дополнительную герметизацию обратных сторон концевых электродов 12E, 14E.
Другим вариантом заключения в корпус батареи является использование растворимого или имеющего низкую температуру плавления твердого вещества для заполнения камер ячейки 22С, 24С, а также трубопроводов и труб всех ячеек батареи 20. Затем батарея погружается целиком в глубокую ванну с эпоксидной смолой. После того, как эпоксидная смола затвердеет, батарея подвергается действию воды или другого растворителя, подаваемого через ее систему циркуляции для того, чтобы растворить твердое вещество, или же нагревается для того, чтобы расплавить твердое вещество.
Другим эффективным способом заключения батареи в корпус является использование конструкции, состоящей из пластины и рамы (не показана), которая герметично присоединяется на короткий срок, что позволяет провести однократную заливку образующего корпус полимера (эпоксидной смолы). Этот полимер обеспечивает долгосрочную изоляцию по всем кромкам электродов и мембран.
В любом исполнении задачей герметизации является предотвращение попадания электролита из одной ячейки в другую, протечки между трубами и трубопроводами, утечки в окружающую среду, а также обеспечение короткой длины труб при малом их сечении.
На фиг. 4 изображена система со свободным потоком; система генерирования/аккумулирования энергии с использованием одной или более батарей или наборов элементов 20. В каждую ячейку 10 подают электролит посредством насосов 26 и 28 растворов NaBr и Na2S5 (22 и 24, соответственно). Электролиты 22 и 24 хранятся в контейнерах 32 и 34. Электролит в емкостях 32, 34 можно заменить на свежий путем замены емкостей на емкости, содержащие свежие электролиты и/или путем заполнения их из источника электролита по линиям 32R, 34R, при этом соответствующие линии (не показаны) предназначены для слива отработанного реагента.
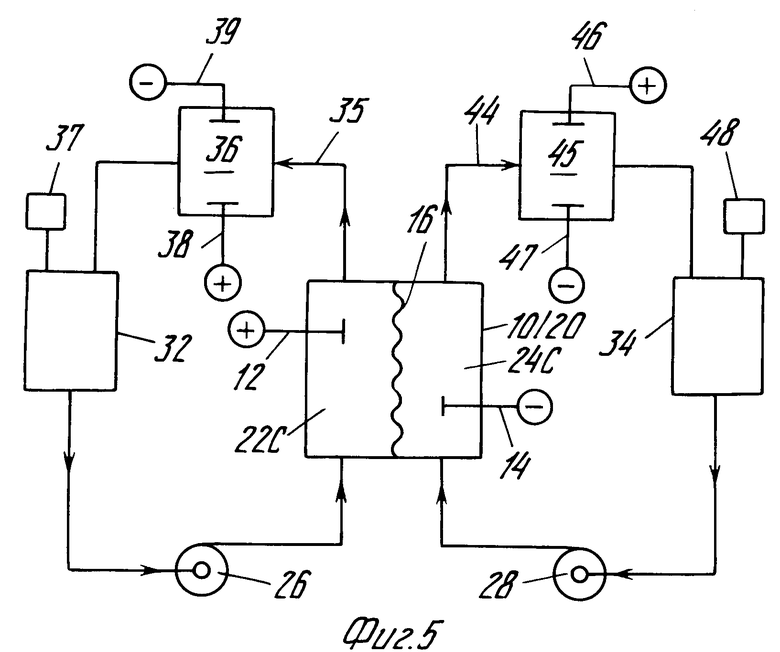
На фиг. 5А показана система в целом с контролем величины pH электролитов из обеих камер ячеек 22C и 24C, причем камера 22C имеет внутри положительный электрод 12, а камера 24C имеет внутри отрицательный электрод 14. Следует понимать, что в некоторых случаях контроль pH необходим только на одной стороне ячейки, что не выходит за рамки данного изобретения. Электролиты 22 и 24 закачивают из емкостей 32 и 34, соответственно, в соответствующие камеры 22C и 24C посредством насосов 26 и 28.
Электролит 22 поступает из камеры 22C ячейки и проходит по линии 35 в ячейку компенсации pH 36. Ячейка компенсации pH 36 содержит анод 38 и катод 39. Значение pH электролита 22, протекающего через ячейку компенсации pH 36, повышается за счет выделения газообразного водорода. Получаемый таким образом газообразный водород удаляется через клапан 37 емкости 32. Газообразный водород выделяется при разложении воды, а в растворе остаются ионы OH-, компенсирующие ионы H+, выделяющиеся на положительном электроде.
Другой тип ячейки компенсации pH для использования на положительной стороне электролита показан на фиг. 6B. В этом исполнении имеется ячейка 36' с анодом 38' и катодом 39'. Эта ячейка разделена на два отсека (41 и 42) посредством сепаратора из микропористой мембраны 40. H2, образующийся при разложении воды, может быть выведен непосредственно из ячейки 36' посредством клапана 43, что делает излишним клапан 37 на емкости 32. Полуреакция для процесса компенсации pH следующая:
H2O+e- ⇄ 1/2H2+OH- (6)
В ячейке компенсации pH бром выделяется на аноде, а H2 образуется на катоде; реакция в целом будет:
H2O+NaBr ⇄ NaOH+1/2Br2+1/2H2 (7)
Согласно фиг. 5, бром просто растворяется в анолите и становится доступным для разряда. H2 или удаляют через клапан 37 из емкости 32, или вводят через клапан самой pH-ячейки 36, если используется мембрана, как описано в пояснении к фиг.6.
Размещение pH-ячейки 36 в линии анолита, как показано на фиг.5 имеет то преимущество, что компенсация образования кислоты происходит на той же стороне, где эта проблема возникает, и это способствует выделению большего количества брома в виде побочного продукта, что увеличивает общую эффективность элемента.
Нанесение на анод диоксида кремния будет препятствовать чрезмерному подкислению положительной стороны и может привести к тому, что pH на положительной стороне будет расти, а не снижаться. Это происходит потому, что pH на положительной стороне будет повышаться по мере переноса ионов H+ через мембрану к отрицательной стороне. Любые H+ ионы, которые перемещаются к отрицательной стороне, образуют воду и, таким образом, выводятся из системы. На возрастание pH на положительной стороне можно влиять путем применения комбинированного покрытия на аноде из диоксида кремния с активированным углем. Диоксид кремния не воздействует непосредственно на pH, хотя pH и будет иметь тенденцию возрастать, как обсуждалось выше, в то время как наличие активированного угля будет вызывать падение pH. Таким образом, обеспечивается медленное снижение pH, которое легко компенсировать за счет полуреакции по уравнению (6) приведенному выше. Другим вариантом такой компенсации pH является пропускание по крайней мере части анолита через камеру, содержащую активированный уголь. При этом величина pH анолита снижается по мере того, как активированный уголь ускоряет реакцию по уравнению 5, приведенному выше. Таким образом, выделение ионов H+ (в виде HBr) можно контролировать путем уменьшения количества электролита, проходящего через камеру, содержащую активированный уголь, или путем лишь периодического пропускания анолита через эту камеру.
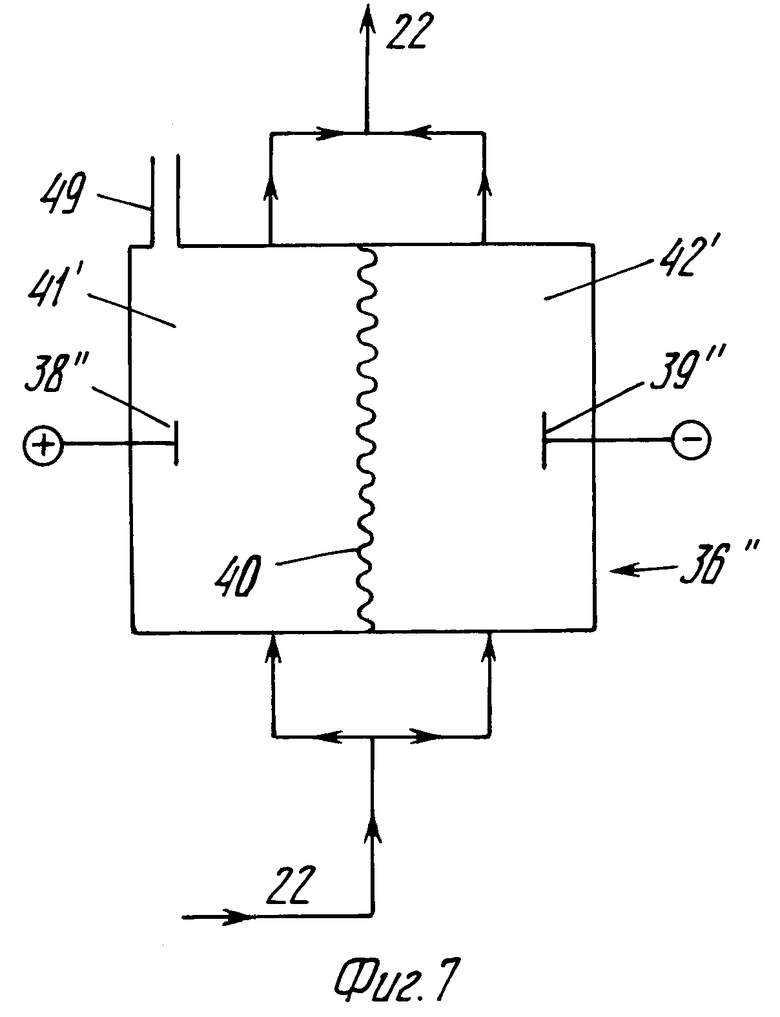
Другим способом регулирования роста величины pH на положительной стороне является использование иного типа ячейки контроля pH, которая показана на фиг.7.
Эта ячейка сконструирована так, чтобы имелся недостаток Br-иона, что приводит к образованию и выделению газообразного кислорода на аноде. Общая реакция будет соответствовать уравнению
2H2O+2Br2 ⇒ O2+4H=+4Br- (8a)
этом на аноде протекает реакция:
H2O=2H++(1/2)O2+2e- (8b)
а на катоде:
2e-+Br2 ⇒ 2Br- (8c)
Согласно фиг.7, ячейка 36'' имеет анод 38'' и катод 39''. Эта ячейка разделяется на два отсека 41' и 42' посредством сепаратора 40 (микропористой мембраны). Поток анолита разделяется надвое, причем одна часть проходит через положительную сторону 41 ячейки, а другая - через отрицательную сторону 42' ячейки. После того, как разделенные потоки выходят из ячейки, они вновь соединяются. Кислород, получаемый за счет разложения воды на аноде, может выпускаться непосредственно из ячейки 36'' через клапан 49.
Согласно фиг.5, ячейка компенсации pH помещается также со стороны отрицательного потока электролита ячейки.
Такая ячейка 45 имеет в своем составе анод 46 и катод 47. Электролит 24, выходящий из камеры 24С ячейки, проходит по линии 44 в ячейку компенсации pH 45. Путем пропускания электрического тока между положительным и отрицательным электродами ячейки 45, вода разлагается с образованием ионов H+ и OH-. Поток ионов ОН-, направленный в емкость 34, позволяет поддерживать электролит 24 при высоком значении pH, в то время как на катоде из воды выделяется H2 который выходит через клапан 48 емкости 34. На аноде сульфид-ионы окисляются до серы, что приводит к некоторому разряду системы.
Реакция в целом следующая:
2Na2S+2H2O ⇄ 2NaOH+H2+Na2S2 (9)
Свободная сера вызывает полимеризацию Na2S до дисульфида натрия, как показано выше.
В pH-ячейке можно использовать или не использовать микропористую мембрану, в зависимости от многосторонности функционирования системы и необходимости отделения газообразного водорода. Если желательно работать с мембраной, тогда ячейка будет иметь конструкцию, сходную с конструкцией, показанной на фиг. 6, с клапаном для отвода газообразного водорода с отрицательной электродной стороны ячейки, причем электролит 24 проходит к положительной электродной стороне ячейки. В таком варианте исполнения клапан 48 на емкости для электролита 34 не является необходимым.
Фигура 8 иллюстрирует систему компенсации pH для использования в отрицательном потоке электролита.
Ячейка 80 регулирования pH размещена на участке потока электролита 24 за камерой католита 4С ячейки. Отрицательная сторона ячейки 80 имеет катод, работающий в условиях недостатка разряжающихся частиц, 86. Между положительным электродом 82 и отрицательным электродом 86 течет постоянный ток, производя электролиз воды с образованием газообразного водорода на катоде 86; при этом образуются также ионы OH-, повышая pH раствора электролита и компенсируя, таким образом, миграцию ионов OH- от отрицательной стороны ячейки 10 к положительной стороне. Катод 86 ячейки 80 работает в условиях недостатка разряжающихся частиц для того, чтобы максимально увеличить получение ионов OH- и свести к минимуму образование сульфида натрия. Нехватка разряжающихся частиц на катоде 86 достигается нанесением на поверхность катода толстого пористого слоя 88, который снижает досягаемость отрицательной поверхности электрода для полисульфидов натрия, таким образом стимулируя электролиз воды. Предпочтительным пористым поверхностным слоем для катода 86 является нетканый полипропилен, такой как Webril, изготовляемый Kendall Co.
На аноде ячейки 80 для регулирования pH протекает следующая реакция:
S + Na2Sx ⇒ Na2Sx+1 (10a)
На катоде ячейки 80 для регулирования pH протекает следующая реакция:
H2O+e- ⇒ OH-+(1/2)H2 (10b)
Газообразный водород может быть выведен из емкости 34 посредством клапана 85.
При необходимости, в ячейке 80 для контроля pH можно использовать мембрану для того, чтобы разделить ячейку на камеру анолита и камеру католита. В таком исполнении продукт - газообразный водород - можно выводить непосредственно из камеры католита ячейки.
Изготовление электродов
Концевые электроды отличаются от промежуточных тем, что они должны иметь внедренный в их структуру металлический проводник, проходящий через всю площадь электрода. Это необходимо, так как сопротивление материала, из которого формируется основа электрода, слишком велико, чтобы обеспечить адекватную электрическую связь с внешней электрической цепью. Например, материал основы площадью 25х25 см (10' х 10') и толщиной 0,25 см (0,1') будет иметь сопротивление около 10 Ом, в то время как соответствующая ячейка имеет внутреннее сопротивление около 0,01 Ом. Лист меди толщиной 0,025 см приблизительно такой же площади, внедренный в электрод, снизит эффективное сопротивление примерно до 100 мкОм. Концевые электроды являются униполярными, в то время как промежуточные электроды являются биполярными. Лист проводящего материала представляет собой тонкую сетчатую структуру, внедренную по длине концевых электродов, что механически обеспечивает хороший контакт по пути прохождения тока.
Процесс изготовления биполярных промежуточных электродов осуществляется следующим образом. Основы формируют из графитовых хлопьев, смешанных со связующим из пластика или с любым другим подходящим связующим, обычно в массовом соотношении 1:1 этих компонентов. Эту смесь сушат путем нагревания и/или выдержки в эксикаторе, формируют из нее листы и прессуют горячим методом при температурах и давлениях, применимых для используемых материалов.
Затем эти основы покрывают на отрицательной поверхности частицами активированного угля, а на положительной поверхности -диоксидом кремния или смесью диоксид кремния/частицы активированного угля путем напыления таких частиц на поверхность помещенной в прессформу пластины с последующим горячим прессованием основы для полного уничтожения в ней пустот и вдавливания частиц в ее поверхность. В других предпочтительных вариантах используют вместо диоксида кремния любые цеолиты, отличные от таких силикатов, или подобные им материалы, как природные, так и синтетические. Пригодными типами активированного угля для использования при покрытии поверхности электродов, являются G212 (North American Carbon Co.); UU (Barnebey-Cheney Co.); GAC (Calgon Carbon Co.) или PCB (Calgon Carbon Co).
После каждой стадии прессования прессформу и ее содержимое охлаждали под давлением с использованием водяного теплообменника, для того, чтобы избежать изгиба или деформации, а также чтобы быть уверенным в получении компактной, непористой структуры.
Концевые электроды изготовляют путем получения основы смешением графитовых хлопьев и связующего из пластика таким же образом, как это было описано для процесса изготовления биполярных промежуточных электродов.
Эти основы затем образуют сандвич с проводящей сеткой, например медной, помещенной между ними. Эта сборка прессуется горячим методом с образованием основы концевого электрода и охлаждается под давлением, чтобы свести к минимуму деформацию.
Одна поверхность этой основы затем покрывается частицами активированного угля или диоксида кремния, или же смесью частиц активированный уголь/диоксид кремния в зависимости от того, положительный или отрицательный электрод изготовляется. Это достигается напылением требуемых частиц (активированного угля или диоксида кремния) на поверхность электрода с последующим горячим прессованием для вдавливания частиц в поверхность. После каждой стадии прессования прессформу и ее содержимое охлаждали, например, используя водяной теплообменник, для того, чтобы избежать изгиба или деформации.
Мембраны
Единственной мембраной, которую можно использовать в бромной системе, описанной в данном изобретении, является катионообменная мембрана на основе фторуглеродного полимера с привитым при помощи гамма-излучения стиролом с сульфоновой или карбоновой кислотой в качестве функциональных концевых групп. Фторуглеродом является предпочтительно фторированный сополимер этилен-пропилен. Мембрана изготовляется путем привития стирола на фторуглеродный полимер с использованием гамма-излучения с последующим сульфированием привитого полимера, например, с использованием хлорсульфоновой кислоты, или вводом функциональных карбокси-групп.
Такая мембрана имеет предпочтительно толщину от 0,005 до 0,0175 см (0,002 - 0,007 дюйма), более предпочтительно около 0,0125 см (0,0055 дюймов). Мембраны изготавливаются из пленки на основе этиленпропиленового сополимера желаемой толщины, к которому привит стирол с помощью гамма-излучения, например, источника кобальта-60. Прививка с помощью излучения винилзамещенных мономеров к пленкам полиолефинов известна из литературы [US 4230549, US 4339473].
При получении типичной мембраны для использования в данном изобретении фторуглеродную пленку сворачивают с промежуточным слоем из абсорбирующей бумаги в плотный рулон, который затем размещают в реакционном сосуде из нержавеющей стали. Затем в реакционный сосуд вводят раствор стирола в подходящем растворителе (например, в метиленхлориде), и рулон оставляют для пропитки, например, на 24 ч. Затем систему вакуумируют для удаления кислорода и рулон подвергают воздействию гамма-излучения, например от источника кобальта-60, до предварительно установленной общей дозы. Затем рулон промывают и подвергают сульфированию посредством реакции, например, с хлорсульфоновой кислотой. Сульфирование можно также провести с использованием дымящей серной кислоты.
Гамма-облучение фторуглеродного полимера приводит к образованию свободных радикалов, которые затем способны вступать в реакцию с мономером стирола. Электрическое сопротивление ионообменной мембраны непосредственно связано с процентным содержанием стирола, привитого на нее с последующим сульфированием, причем электрическое сопротивление снижается при возрастании процентного содержания привитого стирола. В целом эффективный интервал процентного содержания привитого стирола составляет от 10 до 35%, более предпочтительно от 10 до 20%. Процентное содержание выражается как прирост массы в результате присоединения стирола, деленный на начальную массу полимерной пленки, умноженную на 100. Электрическое сопротивление мембраны также связано с процентом сульфирования, который обычно составляет от 5 до 30%, более предпочтительно от 12 до 20%, причем электрическое сопротивление уменьшается при росте процента сульфирования.
Вышеописанная мембрана для использования в данном изобретении имеет связи углерод-фтор, которые сообщают ей стойкость по отношению к брому, бромиду или свободному радикалу брома, и таким образом обеспечивают долговременное использование в жестких условиях систем для аккумулирования и/или получения энергии, где электролит в камере анолита во время получения энергии содержит бром, а электролит в камере католита во время получения энергии содержит сульфид. Кроме того, такая мембрана имеет очень низкие скорости диффузии для бромид- и сульфид-ионов. В предпочтительном исполнении мембрана имеет толщину 0,0125 см (0,005 дюйма), что будет снижать диффузию (так что в ячейке не будет саморазряда). Сопротивление в 2N растворе NaOH около 0,10 - 0,20 Ом/см2, или около 0,015 - 0,03 Ом/дюйм2.
Другими характеристиками такой мембраны является селективная проницаемость, которая составляет около 85% в 1N растворе KC1, и сопротивление, составляющее от 0,20 до 1,0 Ом/см2 в 0,60 N растворе KCl.
Такая мембрана будет выдерживать при использовании предпочтительного процесса данного изобретения, основанного на реакциях с участием брома и серы, описанных выше, свыше 100 циклов при 2 молярной концентрации Br2 при полном заряде без ощутимой деградации. Кроме того, во время использования очень небольшое количество серы мигрирует на положительную сторону, и мембрана практически непроницаема для ионов серы.
Другим типом мембраны, который может быть использован в данном изобретении, является катионообменная мембрана из сополимера тетрафторэтилена и сульфонированного или карбоксилированного винилового эфира, как, например, мембраны, поступающие в продажу под названием Nafion (Du Pont) и Flemion (Asahi Glass). Эти мембраны имеют связи углерод-фтор, которые делают их стойкими по отношению к брому, бромиду или свободному радикалу брома и, таким образом, могут в течение продолжительного времени использоваться в системах для аккумулирования и/или получения энергии, подобных описанным здесь.
Более дешевым заменителем, который может использоваться в системе с железом, является гетерогенная структура, изготовляемая Sybron Chemical Co., называемая IONAC MC3470. Это катионообменная структура, содержащая в качестве функционального материала сульфированные смолы, связанные Кynar'ом. Этот материал нанесен на волокнистую плоскую подложку из стеклоткани или других полимерных волокон. Характеристики этой мембраны: толщина 0,040 см (0,016 дюйма), селективная проницаемость 96% и сопротивление около 5 Ом/см2 в 1N NaCl. Цена этой мембраны ниже, но электрическое сопротивление выше, чем у первой описанной мембраны.
Компенсация миграции
Одной из важных проблем повторного циклирования электролита на отрицательной стороне в системе, содержащей бром, является баланс миграции ионов брома с положительной стороны к отрицательной стороне. В соответствии с фиг. 1, происходит диффузия ионов брома в отрицательную сторону электрода, приводящая к потере реагента на положительной стороне, дисбалансу состава электролита и кулоновским потерям. Эту ситуацию можно скорректировать путем подвода NaBr соответствующей концентрации к отрицательной стороне электрода для создания ионов Br-, которые будут диффундировать обратно к положительной стороне и, таким образом, уравновешивать миграцию брома с положительной стороны. Согласно фиг.4, NaBr можно ввести в линию 30 для смешивания с электролитом 24, поступающим из емкости 34.
Соответствующая проблема миграции ионов серы с отрицательной стороны к положительной стороне мембраны решается следующим образом. Ионы серы осаждаются в виде серы, попадая в электролит на положительной стороне. Согласно фиг. 4, анолит, содержащий серу, перекачивается насосом 26 через вентиль 27, где он физически фильтруется в устройстве 25. Электролит отрицательной стороны посредством вентилей 29 подается в обход фильтра 25. Но периодически (а период определяется конкретной областью применения) вентили 27, 29 и 31 переключают таким образом, что электролит отрицательной стороны идет через фильтр 25, а электролит положительной стороны - в обход фильтра 25. Когда это происходит, свободная сера с фильтра переходит в раствор и, таким образом, снова возвращается в электролит отрицательной стороны. Когда вся сера растворится, вентили снова переключаются в первое из описанных состояний.
В обеих системах, поскольку перенос воды происходит через мембрану за счет осмоса или электроосмоса, необходимо делать поправку на это явление. Это осуществляют путем подачи воды к обедняемой стороне, например, обратным осмосом.
Улучшение энергетических характеристик.
Поверхности электродов на положительной и отрицательной сторонах покрыты пористыми материалами со значительной площадью поверхности. На катоде используется активированный уголь; на аноде для системы с бромом используется диоксид кремния или смесь активированный уголь/диоксид кремния, в то время как для системы с железом используются частицы активированного угля.
Частицы диоксида кремния адсорбируют бром из раствора на положительной стороне и обеспечивают лучший контакт с поверхностью электрода и электролитом. Активированный уголь адсорбирует раствор S2- на отрицательной стороне системы. Этот пористый материал обеспечивает большую площадь поверхности и таким образом повышает досягаемость серы при разряде. Это приводит к улучшению работы системы благодаря тому, что выходное напряжение и мощность поддерживаются постоянными вплоть до почти полного разряда системы. Поляризационные потери незначительны.
Использование комплексообразователей
В случае некоторых применений желательно контролировать бром. Хотя существует большое количество соединений, образующих комплексы или координационные соединения с бромом, большинство из них несовместимы с условиями проведения электролиза или будут быстро реагировать с окислителем - бромом.
Одним из наиболее подходящих веществ для образования комплексов с бромом в растворах солей высокой молярности является полиалкиленгликоль, например полиэтиленгликоль. Он представляет собой алифатическую эфирную цепь, и бром захватывается и/или присоединяется к этой структуре в высоком массовом соотношении. Предполагается, что захват и/или присоединение брома частично происходит механически за счет удерживания брома в промежутках между переплетающимися полимерными цепями в дополнение к действию слабых электрических сил. При таком использовании давление пара свободного брома существенно понижается, благодаря чему система становится более безопасной и удобной в обращении.
Полиэтиленгликоль может быть получен в широком интервале молекулярных масс, но даже при высокой молекулярной массе (4000) этот материал легко растворяется в воде. Предпочтительными соотношениями являются 25 - 100 г поолиэтиленгликоля на 300 - 500 г NaBr на литр электролита в разряженном состоянии.
Добавление комплексующего агента увеличивает вязкость электролита, делая перекачивание электролита несколько более трудным. Но, что более важно, добавление комплексообразователя увеличивает сопротивление электролита и, таким образом, внутреннее сопротивление ячейки. Таким образом, следует подбирать оптимальные условия, так, чтобы было добавлено достаточное количество комплексообразователя для полного связывания всего количества брома, возможного при полном заряде, с учетом возрастания внутреннего сопротивления ячейки.
Степень заряжения ячейки можно ограничить заданным значением, чтобы гарантировать, что не будет образовываться избыток брома. Кроме того, можно использовать агенты для связывания в комплекс брома в емкостях для хранения, но выделять не связанный в комплекс бром в самой ячейке, поддерживая таким образом низкое внутреннее сопротивление ячейки.
Комплексообразователь может также образовывать воскообразные (но способные растворяться в воде) осадки, которые полностью растворяются при разряде ячейки. Практика показывает, что разряд ячейки должен проводиться на некоторой регулярной основе, опять-таки зависящей от конкретного применения.
Получаемая энергия вряд ли уменьшается при использовании комплексообразователя, и переход энергии из одной формы в другую не затрудняется, так как бром легко отделяется от комплексообразователя. Кроме того, имеет место минимальное вредное воздействие комплексообразователя в модулях компенсации pH.
Другими пригодными комплексообразователями являются: галогениды тетраалкиламмония, 2-пирролиден, N-метилпирролидон и т.д. Кроме того, пригодные для данной системы комплексы с бромом дают другие гетероциклические соединения, например циклические структуры с атомами азота в кольце, такие как соединения пиридина.
Конкретные варианты реализации
Далее настоящее изобретение будет описано применительно к следующим примерам (не ограничиваясь ими).
Пример 1
Изготовление концевых электродов.
Две основы были получены путем смешения графитовых хлопьев (графитовые хлопья # 4012 Asbury Carbon Co.) со связующим - поливинилиденфторидом, PVDF (Pеnvalt's #461) в соотношении 1:1. Смесь нагревали для удаления влаги, формовали в листы и прессовали горячим методом при температуре 177oC (350oF) и давлении 1723 кПа (250 psi) в течение 10 мин, а затем охлаждали при том же давлении между охлаждаемыми водой пластинами.
Для того, чтобы нанести на основы поверхностный слой, их кромки были изолированы лентой, а затем их поместили на алюминиевую пластину - основание, покрытую тефлоновым листом, и на поверхность напылили смесь из 80% графита и 20% Кynar. Затем на поверхность основы напылили слой частиц активированного угля (G212; North American Carbon Co., или UU Barnebey-Cheney Co., или активированный уголь РСВ).
Поверх основы с напыленным слоем поместили лист высокотемпературной резины, затем лист тефлона и еще одну алюминиевую пластину. Затем эту структуру прессовали при 517 кПа (75 psi) при 177oC (356oF) в течение 10 мин с последующим охлаждением при том же давлении между охлаждаемыми водой пластинами.
Затем удаляли ленту с кромок напыленной стороны и на зачищенную кромку помещали рамку из резины. Затем электрод помещали вверх напыленной стороной на алюминиевую пластину, покрытую тефлоновым листом, и обращенную кверху поверхность покрывали тефлоновым листом и алюминиевой пластиной. Кромки этой сборки прессовали при 2413 кПа (350 psi.) в течение 210 мин, а затем охлаждали при том же давлении между охлаждаемыми водой пластинами. На этой стадии происходит герметизация листов основы по кромкам для того, чтобы медная сетка была полностью заключена внутри электрода во избежание коррозии при контакте с электролитом.
Изготовление ячейки
Герметичную единичную ячейку изготовляли путем размещения мембраны IONAC MC3470 между анодом и катодом. Четыре кромки ячейки были залиты эпоксидной смолой, чтобы скрепить ячейку, и выполнены отверстия, чтобы электролит можно было подавать в ячейку и удалять из нее.
Поддерживающие пластины из пластика были наложены на электроды с образованием внешних поверхностей ячейки; в этих пластинах выполнены отверстия. Пластиковые сетки были размещены с каждой стороны мембраны, чтобы создать достаточный зазор между электродами и обеспечить пространство для протока электролитов. Эти сетки предназначены для того, чтобы обеспечить турбулентность потока у поверхности электродов.
Конструкция ячейки предполагает отсутствие контакта электролита с медными сетками и приваренными к ним проволоками, создающими электрический контакт с ячейкой.
Общее расстояние между электродами составляло около 0,16 дюйма. Внутреннее сопротивление ячейки при активной поверхности ячейки 24 кв. дюйма составляло около 0,060 Ом.
Работа ячейки
Вышеописанную ячейку, имеющую электроды с покрытием из угля РСВ, использовали со следующими циркулирующими электролитами:
Положительная сторона - 200 см3 6М раствора NaBr
Отрицательная сторона - 200 см3 1,5М раствора Na2S5
Сопротивление ячейки - 0,06 Ом
Отрицательный раствор приготовляли путем растворения около 60 г порошкообразной серы в 200 см3 раствора 1,6 Na2S. Серу растворяли, медленно вводя ее при перемешивании в нагретый приблизительно до 90oC раствор сульфида натрия. Когда вся сера переходит в раствор, это указывает на образование раствора полисульфида натрия в избытке Na2S5.
Исходно растворы в ячейке находились в полностью разряженном состоянии, когда режим заряда был запущен первый раз в начале цикла #1.
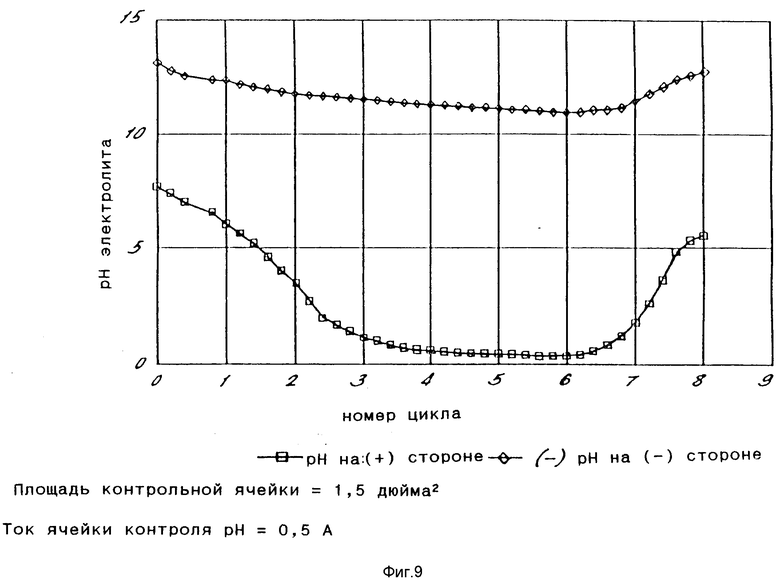
Было проведено восемь циклов для того, чтобы в общем охарактеризовать изменения pH при включенной и выключенной ячейке компенсации pH для контроля pH анолита. Ячейку заряжали постоянным током 4 А в течение 4 ч, а затем ее включили через электрическую нагрузку и разряжали постоянным током 4 А до достижения напряжения 0,50 В. Таким образом было проведено шесть циклов без компенсации pH, в то время как регистрировались данные по изменению pH в емкостях для хранения католита и анолита.
В начале седьмого цикла была приведена в действие ячейка контроля pH, погруженная в емкость для хранения анолита, и она работала при 0,5 А постоянного тока в течение последующих двух циклов, т.е. седьмого и восьмого.
Ячейка для контроля pH была сконструирована из электродов с ненапыленной поверхностью. Она имела активную площадь 7,74 см2 (1,2 кв. дюйма) и расстояние между электродами 0,94 см (3/8 дюйма). Ячейка работала примерно при 1,7 В.
Условия работы ячейки
pH положительной стороны
Начальное значение - 7,7
После 6 циклов - 0,3
После 2 циклов pH-коррекции - 5,5
pH отрицательной стороны
Начальное значение - 13,1
После 6 циклов - 11
После 2 циклов pH-коррекции - 12
На фиг.9 показано изменение pH по ходу цикла. Каждый полный цикл продолжается 8 ч. Следовательно, проведение эксперимента требует 64 ч.
Реакции, протекающие внутри ячейки компенсации (контроля) pH представлены ниже:
На аноде
2Br-=Br2+2e- (13a)
На катоде
2e-+1H2O+H2+2OH- (13b)
Бром выделяется на аноде ячейки регулирования pH и просто включается в процесс заряда. Гидроксил-ионы образуются в растворе на катоде ячейки регулирования pH, таким образом повышая pH и восстанавливая равновесие, необходимое для нормальной работы ячейки. Если pH в католите снижается слишком сильно, в электролите будет происходить нежелательное выделение H2S.
За весь период времени на восстановление значения pH было затрачено около 8 А•ч. Однако это составляет лишь около 3% общего заряда (128 А•ч), пропущенного через ячейку за время 32 ч заряда при 4 А.
Пример 2
Герметичная ячейка была изготовлена путем размещения покрытого РСВ углем катода и покрытого диатомовой землей анода совместно с катионообменной мембраной, сделанной из фторуглеродного полимера с привитым с помощью гамма-излучения стиролом, имеющим функциональные группы сульфоновой кислоты (RAI S24 4010-5). Расстояние между мембраной и каждым из электродов составляло 0,5 см.
Эта ячейка использовалась со следующими циркулирующими электролитами:
Положительная сторона - 300 см3 4 М NaBr
Отрицательная сторона - 300 см3 0,25 М Na2S5 и 1 М Na2S
Скорости потока электролита составляли приблизительно 0,5 л/мин через каждый из отсеков. Площадь активной поверхности ячейки составляла 155 см2.
Эта ячейка работала с ячейками регулирования pH типа, описанного в примере 1, погруженными и в емкости для анолита и католита. Ячейки регулирования pH работали приблизительно при 0,85 А постоянного тока на положительной стороне и от 1,5 до 2 А постоянного тока на отрицательной стороне в течение двух циклов, в продолжение которых ячейка заряжалась и разряжалась при постоянном токе 2 А.
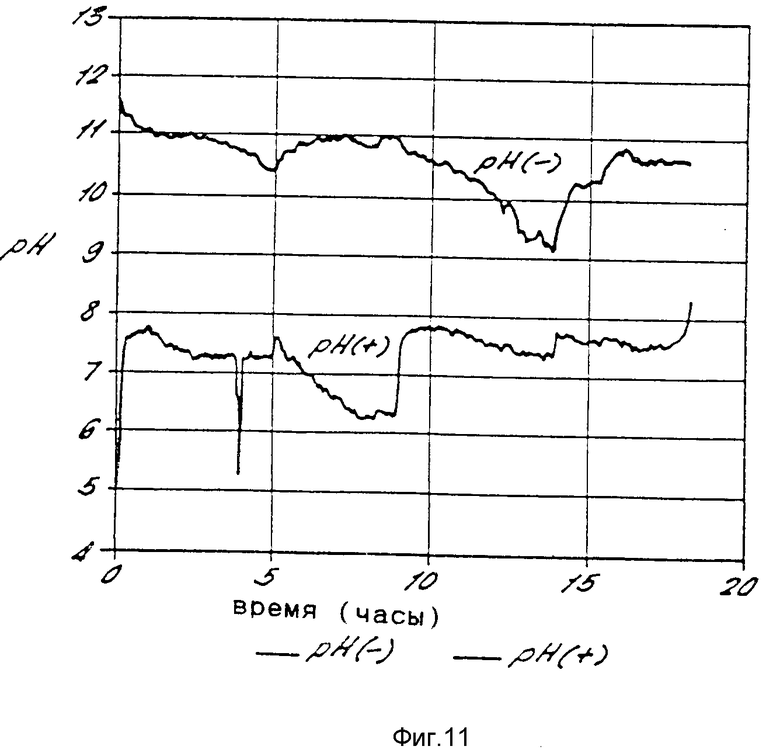
На фиг. 10 показано напряжение на ячейке во время циклирования ячейки. Фиг. 11 иллюстрирует pH положительного и отрицательного электролитов во время работы ячейки. По этому графику следует отметить, что при наличии ячейки контроля pH в анолите значение pH анолита поддерживается на достаточно высоком уровне. Кроме того, при наличии ячейки контроля pH в католите значение pH католита поддерживается на достаточно высоком уровне в течение большей части цикла.
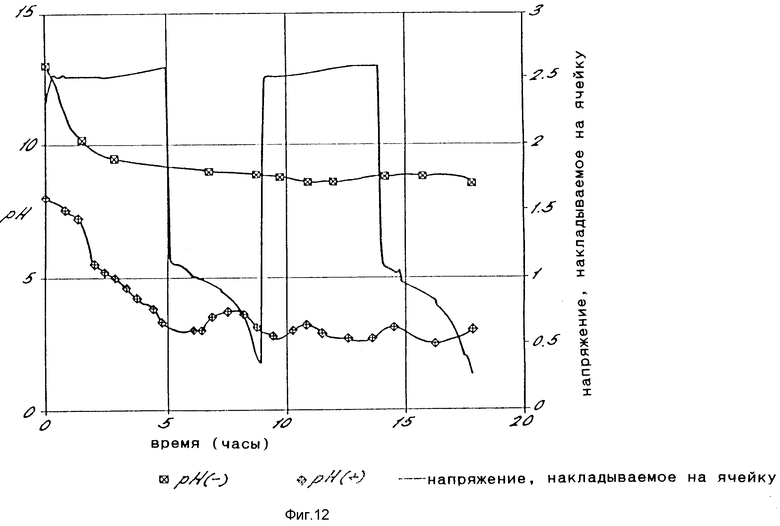
Затем ячейка работала в течение двух идентичных циклов без ячейки контроля pH как в анолите, так и в католите. Фиг.12 иллюстрирует как напряжение на ячейке, так и pH анолита и католита. Следует отметить, что pH как анолита, так и католита падает очень значительно, когда не принимается никаких мер по контролю pH.





Изобретение относится к электрохимическим системам аккумулирования и генерирования энергии. Электрический способ аккумулирования и/или генерирования энергии и устройство для его осуществления включают набор ячеек, в котором каждая ячейка содержит положительный электрод и отрицательный электрод: в каждой ячейке имеется мембрана, разделяющая ее на камеры католита и анолита для растворов катлоита и аналоита, которые рециркулируют через отдельные насосы и емкости для хранения обратно в камеры. Промежуточные электроды, расположенные между соседними ячейками в наборе, имеют как положительную сторону, так и отрицательную сторону. Может использоваться пара бром-сера. Устройство снабжено средствами компенсации изменений величины рН и/или изменений концентрации гидроксил-ионов у положительных и/или отрицательных сторон набора ячеек. Предусмотрены средства воздействия на имеющуюся ограниченную миграцию через мембрану или другие потери брома, серы и/или воды и ограничения эффекта подкисления за счет брома с сохранением высокой эффективности аккумулирования энергии и получением высокой мощности при стабильной работе в течение длительных периодов, а также с поддержанием выхода энергии и высокого уровня напряжения в течение практически всего разрядного цикла. 4 с., 8 з.п.ф-лы, 12 ил.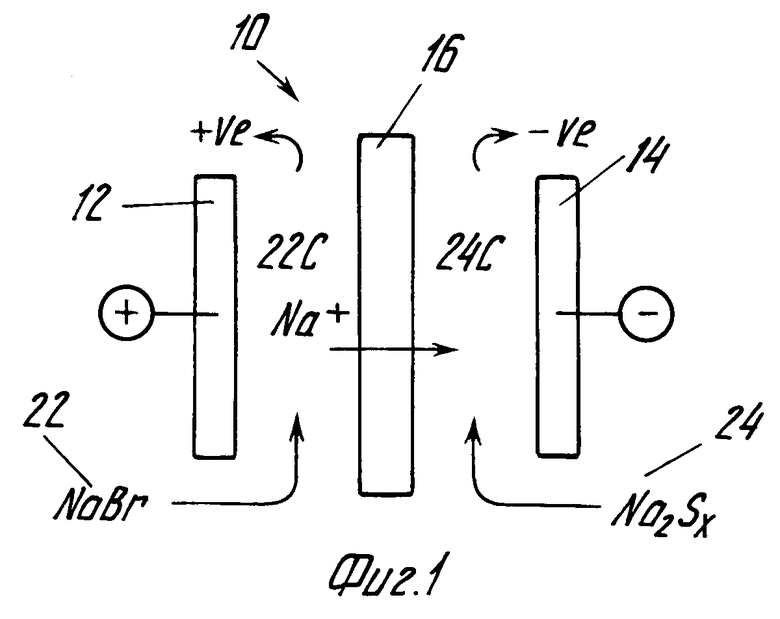
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| US, патент, 4069371, кл | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| US, патент, 4485154, кл | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| US, патент, 4343868, кл | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1998-04-27—Публикация
1993-10-13—Подача