Изобретение относится к области медицины, конкретно к средству, которое может найти применение для лечения бронхиальной астмы и других заболеваний, в патогенезе которых существенную роль играют процессы, происходящие на поверхности лейкоцитов (клеточная адгезия, взаимодействие с антигенами и др. ).
Проблема создания высокоэффективных фармакотерапевтических средств для лечения бронхиальной астмы как одного из самых распространенных и тяжелых заболеваний человека является весьма актуальной во всем мире. Выявлены неблагоприятные тенденции в отношении роста заболеваемости бронхиальной астмой. Несмотря на создание ряда бронходилятаторов и использование кортикостероидов пока не удается изменить тенденцию к распространению и ухудшению течения заболевания /1/.
Одно из возможных объяснений такой ситуации состоит в том, что патогенез бронхиальной астмы, как любой системной патологии человека, является сложным комплексом биохимических и патофизиологических процессов. К ним относится взаимодействие и взаиморегулирование систем иммунитета, метаболизма экзогенных и эндогенных соединений, генетически обусловленных особенностей сигнальных, рецепторных систем клетки и т.д.
Сейчас четко сформулирована концепция бронхиальной астмы как хронического иммунного (аллергического) воспаления дыхательных путей; выявлены многие ведущие звенья патогенеза бронхиальной астмы; определена роль зозинофилов и эозинофильных белков в повреждении слизистой бронхов, регулирующая роль Т-лимфоцитов и продуцируемых ими цитокинов; установлено значение лейкотриенов в бронхиальном воспалении /1/.
Успехи же в области фармакотерапии бронхиальной астмы сводятся главным образом к разработке рациональных лекарственных форм - ингаляционных (бета-2-адреномиметики, М-холинолитики, кортикостероиды, интал) и пероральных лекформ пролонгированного действия (бета-2-адреномиметики, теофиллин) /1/. По мнению клиницистов-пульмонологов, наиболее крупным достижением в этой области является создание ингаляционных кортикостероидов и высокоэффективных длительнодействующих бета-2-адреномиметиков-формотерола и сальметерола. Однако еще нет убедительных доказательств, что с помощью этих лекарств можно решить главный вопрос лечебной тактики при БА - необратимое подавление воспалительного процесса в дыхательных путях. Даже кортикостероиды только ингибируют, но не устраняют полностью иммунное воспаление в легких, и смертность от астмы остается по-прежнему высокой. Кроме того, перечисленные антиастматические лекарственные средства вызывают широкий спектр побочных эффектов: среди них - кардиотоксическое действие теофиллина и бета-2-адреномиметиков и хорошо известные отрицательные эффекты кортикостероидов (остеомаляция, нарушение электролитного баланса и др.).
Данное изобретение направлено на создание новых антиастматических средств из класса олигосахаридов (продукты хитина), действие которых обусловлено влиянием на клеточную адгезию.
Известны вещества, представляющие собой продукты деацетилирования хитина (молекулярная масса 300.000 - 1.000.000), обладающие противовоспалительным действием /2/.
Однако сведения о возможности их применения при бронхиальной астме отсутствуют.
Ближайшим аналогом заявляемого средства, обладающим антиастматическим и андиадгезионным действием является препарат интал (кромогликат натрия) /3/.
Задачей изобретения явилось создание нового высокоэффективного нетоксического лекарственного препарата из природного сырья для лечения бронхиальной астмы и других заболеваний, в патогенезе которых важную роль играет повышенная адгезия клеток.
Эта задача была решена разработкой средства, представляющего собой олигосахариды, являющиеся продуктами деацетилирования природного продукта хитина, а именно - олигомеры хитозана или их фармацевтически приемлемые соли. Предпочтительно, чтобы степень полимеризации олигомеров была равной 4-8.
Средство может дополнительно содержать фармацевтически приемлемые целевые добавки, такие как растворители, наполнители, диспергирующие агенты, эмульгаторы и т.п.
Олигомеры со степенью полимеризации 4-8 могут быть получены, например, по методу, описанному в /4/, путем проведения процесса деацетилирования хитина в концентрированном растворе серной кислоты (65%-ном) при 40-50oC, в течение 20-120 минут.
Однако могут быть использованы олигомеры хитозана, полученные любым известным способом.
Фармацевтически приемлемыми солями олигомеров хитозана могут быть ацетаты, гидрохлориды, нитраты или фосфаты.
Средство может быть выполнено в форме таблеток, гранул, капсул, порошка, ингаляционных форм, суспензии, растворы, мази или крема. Эти формы могут быть получены известными методами.
Другие активные ингредиенты, такие как антибактериальные вещества, могут быть добавлены к средству.
Количество олигомерного продукта в лекарственной форме может широко варьироваться, например, от 0,3 до 20% по массе.
Результаты исследований заявляемого средства
Пример 1.
1. Эксперименты in vitro.
1.1. Исследование влияния заявляемого средства на потенциальные клетки-мишени iv vitro.
С помощью олигосахаридов, меченных флуоресцентным веществом флюоресцеинизотиоцианатом (ФИТЦ), и соответствующей микроскопией установлено, что олигосахариды связываются с мононуклеарными клетками крови, причем это связывание наблюдается только по поверхности клеток. В саму клетку олигомеры не проникают.
Обзоры производили на 200-300 клетках с помощью флуоресцентного микроскопа. В качестве контроля использовали клетки, фиксированные на стеклах, которые инкубировали с олигомерами, а затем с олигомерами, меченными ФИТЦ: свечение при этом не было обнаружено.
Таким образом, авторами данного изобретения установлено, что олигомеры хитозана взаимодействуют с молекулами плазматической мембраны клеток, имеющими прямое отношение к воспалительным и иммунологическим процессам, в том числе к аллергическим ринитам.
1.2. Исследование действия олигомеров на моделях анафилактической бронхоконстрикции in vitro.
В эксперименте использовались морские свинки весом 350-500 г., сенсибилизированные инъекциями овальбумина в дозе 10 мкг и 100 мг Al(OH)3 на свинку по методу Andersson. Через 3-4 недели после начала сенсибилизации животных готовили препарат изолированной трахеи согласно Blattner с соавт. /1980/. Препарат трахеи помещали в термостатируемую камеру (37oC), содержащую раствор Кребса-Хенсляйта (119 mM NaCl, 4,8 mM KCl, 1,2 mM MgCl2, 1,2 mM CaCl2, 2,53 mM NaHCO3, 24,8 mM глюкозы, pH=7,4). Исходная нагрузка на препарат составляла 0,7-1 г. Исследование релаксирующей способности изучаемых веществ проводили в изотоническом режиме. Сокращение трахеи регистрировали с помощью Механотрона 6Мх2Б и самописца КСП-4. Релаксацию гладкомышечного препарата трахеи выражали в процентах от максимальной амплитуды сокращения, вызываемого добавлением в инкубационную среду медиатора. Определяли среднюю величину от измерений 4-5 отрезков. Строили кривую доза-эффект. ЕД50 определяли графически по методу Литчфилда и Вилкоксона.
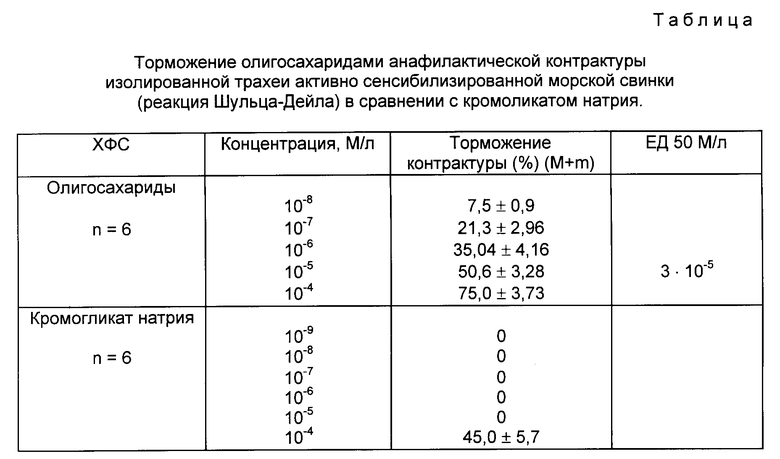
Установлено, что олигомеры вызывали эффект ингибирования анафилактической контрактуры изолированной трахеи сенсибилизированной морской свинки /табл. 1/. Препарат сравнения кромогликат натрия в этих условиях проявлял слабую активность.
Таким образом, показано антиастматическое действие олигосахаридов in vitro.
Пример 2.
2. Эксперименты in vivo.
2.1. Острая токсичность.
Токсичность олигосахаридов при оральном введении белым неинбредным мышам практически отсутствует - LD50 более 25 г/кг.
LD50 при парэнтеральном (внутрибрюшинном) введении мышам - 5,68±1,19 г/кг;
LD50 при внутрибрюшинном введении крысам - 4,73±1,33 г/кг.
2.2. Изучение бронхолитической активности олигомеров на экспериментальных моделях in vivo.
В эксперименте использовались морские свинки весом 350-500 г. Животных сенсибилизировали введением овальбумина в дозе 10 мкг и 100 мг Al(OH)3 на свинку по методу Andersson. Через 3-4 недели после начала сенсибилизации животных наркотизировали этаминалом натрия (40 мг/кг, внутрибрюшинно). У наркотизированной свинки выделяли трахею, вставляли в нее канюлю, которую подсоединяли с помощью системы полихлорвиниловых трубочек к датчику бронхоспазма и аппарату искусственного дыхания (Ugo Basile). В течение эксперимента поддерживался определенный режим дыхания: объем (V) дыхания составлял 6-8 мл, частота - в минуту. Разрешающую дозу овальбумина (150 - 200 мкг/кг) вводили внутривенно (V.jugularis) для получения максимального бронхоспазма, не вызывающего гибели животных от удушья. Исследуемое соединение вводили внутривенно (10 мг/кг за 15 мин до внесения разрешающей дозы овальбумина. С помощью самописца, подсоединенного к датчику, регистрировали изменения сопротивления дыхательных путей воздушному потоку, то есть величину бронхоконстрикторной реакции. Эффект исследуемого соединения оценивали по степени торможения бронхоспазма, выраженной в процентах по отношению к контролю.
Проведенные эксперименты позволили установить /рис. 1/, что олигосахаридный препарат при внутривенном введении за 15 минут до ОА вызывал выраженное антиастматическое действие. Действие кромогликата натрия на данной модели было более слабым, чем у олигомеров.
Примеры заявляемого средства.
Пример А. Олигомеры хитозана; степень полимеризации 4-8.
1% раствор (в изотоническом растворе хлористого натрия) для аэрозольного ингаляционного введения с помощью небуляйзера.
Пример Б. 1% раствор олигомера хитозана (в изотоническом растворе хлористого натрия) с добавлением антибиотиков.
Пример В. 1% раствор олигомеров хитозана (в изотоническом растворе хлористого натрия) для местного применения в виде капель для глаз и носа.
Пример Г. Сухой мелкодисперсный порошок олигомеров хитозана с размером частиц 5-10 микрон для ингаляционного введения с помощью дозирующего ингалятора типа циклохалер.
Пример Д. Таблетка с 0,25 г олигомеров хитозана для перорального применения, содержащая поливинилпирролидон низкомолекулярный медицинский (0,0157, г) /ФС 42-1194-79/, крахмал картофельный (9,0417 г) /ГОСТ 7699-78/, тальк (0,0094 г) /ВФС-42-2550-95/, магний стеариновокислый (0,0032 г) /ТУ-6-09-129-75/. Средняя масса таблетки 0,32 г.
Источники информации
1. Совместный доклад Национального института Сердце, Легкие и Кровь и Всемирной Организации Здравоохранения. Издание N 95-3659, январь, 1995.
2. Yasuhiro Horiuchi; Koji Kifune; Mobuyuki Tanimoto, Anti-inflammatory composition. EP. A 61 K 31/73, Publ. number: 0382 210 A1, 1990, 90/33.
3. Машковский М. Д. Лекарственные средства (Пособие для врачей). Медицина, Москва, 1993, т. 1, с. 362-363.
4. В. И. Максимов, В. М. Денисов и Н.В. Макаров. SU, Авторское свидетельство 1571047 A1, кл. C 08 B 37/08, 1990.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ N-АЦИЛЬНЫЕ ПРОИЗВОДНЫЕ АМИНОКИСЛОТ, И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ПРОТИВОАЛЛЕРГИЧЕСКИХ, АНТИАНАФИЛАКТИЧЕСКИХ И ПРОТИВОВОСПАЛИТЕЛЬНЫХ СРЕДСТВ | 2008 |
|
RU2406727C2 |
| ИЗОНИКОТИНОИЛГИДРАЗОН 2-ГИДРОКСИ-3-МЕТОКСИБЕНЗАЛЬДЕГИДА, ПРОЯВЛЯЮЩИЙ АНТИАСТМАТИЧЕСКУЮ, ПРОТИВОВОСПАЛИТЕЛЬНУЮ И АНТИАЛЛЕРГИЧЕСКУЮ АКТИВНОСТЬ | 1997 |
|
RU2139711C1 |
| АНТИАЛЛЕРГИЧЕСКОЕ И ПРОТИВОВОСПАЛИТЕЛЬНОЕ СРЕДСТВО | 1999 |
|
RU2170091C2 |
| N-АЦИЛЬНЫЕ ПРОИЗВОДНЫЕ АМИНОКИСЛОТ, ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕВЫЕ СОЛИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ПРИМЕНЕНИЕ В КАЧЕСТВЕ ГИПОЛИПИДЕМИЧЕСКИХ СРЕДСТВ | 2005 |
|
RU2335495C2 |
| АНТИАЛЛЕРГИЧЕСКОЕ И ПРОТИВОВОСПАЛИТЕЛЬНОЕ СРЕДСТВО | 1999 |
|
RU2160097C1 |
| СПОСОБЫ ПОЛУЧЕНИЯ N-АЦИЛЬНЫХ ПРОИЗВОДНЫХ АМИНОКИСЛОТ (ВАРИАНТЫ) | 2008 |
|
RU2378284C2 |
| ИНГАЛЯЦИОННЫЙ ПРЕПАРАТ, КУПИРУЮЩИЙ УДУШЬЕ ПРИ БРОНХИАЛЬНОЙ АСТМЕ И БРОНХОСПАЗМЕ | 2001 |
|
RU2191024C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ПРОТИВОВОСПАЛИТЕЛЬНОЙ, БРОНХОЛИТИЧЕСКОЙ, ПРОТИВОТУБЕРКУЛЕЗНОЙ АКТИВНОСТЯМИ | 2011 |
|
RU2448961C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ИНГАЛЯЦИИ | 2006 |
|
RU2338552C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ПРОИЗВОДНЫЕ ГЛУТАРИМИДОВ, И ИХ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ ЭОЗИНОФИЛЬНЫХ ЗАБОЛЕВАНИЙ | 2013 |
|
RU2552929C1 |
Использование: для лечения бронхиальной астмы и других заболеваний, в патогенезе которых существенную роль играют процессы, происходящие на поверхности лейкоцитов. Средство представляет собой олигомерные продукты деацетилирования хитина или фармацевтически приемлемые соли. Предпочтительная степень полимеризации олигомерных продуктов 4 - 8. Средство может дополнительно содержать фармацевтически приемлемые целевые добавки и биологически активные вещества иного действия. Задача изобретения - создание эффективного, нетоксичного средства из природного сырья. 3 з.п. ф-лы, 1 табл, 1 ил.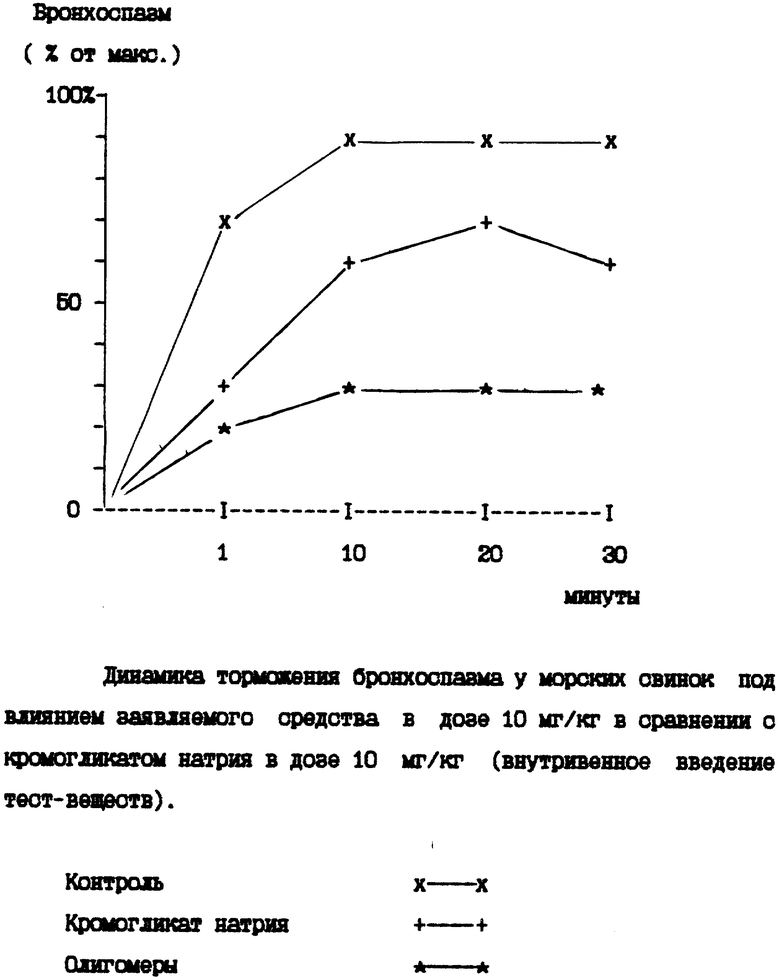
| Машковский М.Д | |||
| Лекарственные средства | |||
| - М.: Медицина, 1993, ч | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ получения и применения продуктов конденсации фенола или его гомологов с альдегидами | 1920 |
|
SU362A1 |
| US 5441932 A, 15.08.95 | |||
| US 5428025 A, 27.06.95 | |||
| US 5576305 A, 19.11.96 | |||
| Гидравлическая камера стабилометра | 1973 |
|
SU482649A1 |
| Способ размножения копий рисунков, текста и т.п. | 1921 |
|
SU89A1 |
| 0 |
|
SU154433A1 | |
Авторы
Даты
1998-08-20—Публикация
1997-07-16—Подача