Настоящее изобретение относится к новым фармацевтическим составам, включающим 9-цис ретиноевую кислоту, ее фармацевтически приемлемые соли и гидролизуемые сложные эфиры.
Кроме того, изобретение относится к 9-цис ретиноевой кислоте, ее фармацевтическим приемлемым солям и фармацевтически приемлемым гидролизуемым сложным эфирам, предназначенным к использованию в качестве лекарственных средств.
С другой стороны, изобретение относится к использованию 9-цис ретиноевой кислоты, ее фармацевтически приемлемых солей и ее фармацевтически приемлемых гидролизуемых сложных эфиров при производстве лекарственных средств для медицинских показаний, перечисленных ниже.
Известен фармацевтический состав, содержащий в качестве активного начала ретиноевую кислоту и фармацевтически приемлемый носитель (патент США, 4603146, кл. A 61 K 31/21, 1986).
В соответствии с настоящем изобретением обнаружено, что 9-цис ретиноевая кислота, ее фармацевтически приемлемые соли или ее фармацевтически приемлемые гидролизуемые сложные эфиры обладают в отношении эпителиальных повреждений противогиперпластическими, противометапластическими, противонеопластическими свойствами предупреждения и лечения опухолей, демонстрируя при этом ограниченную токсичность или иные отрицательные воздействия, вызываемые ретиноидами. Обнаружено, что патологические состояния, лечение которых связано с указанными свойствами, могут эффективно излечиваться путем введения 9-цис ретиноевой кислоты, ее фармацевтически приемлемых солей или ее фармацевтически приемлемых гидролизуемых сложных эфиров как системно, так и местно.
В соответствии с одним вариантом реализации настоящего изобретения 9-цис ретиноевая кислота, ее фармацевтически приемлемая соль или ее фармацевтически приемлемых гидролизуемые сложные эфиры при введении млекопитающим, имеющим предраковые поражения эпителия, способствуют замедлению развития повреждений. Это соединение регулирует рост клеток и дифференциацию этих предраковых поражений и способствует восстановлению клеток. Таким образом предупреждается развитие из этих повреждений эпителиальной карциномы.
В процессе лечения предзлокачественных или предраковых эпителиальных повреждений с целью замедления развития этих повреждений в карциномы применяют 9-цис ретиноевую кислоту, ее фармацевтически приемлемые соли или ее фармацевтически приемлемые гидролизуемые сложные эфиры. Причем пациентам, имеющими указанные повреждения, через рот, или местно в количестве, достаточном для замедления развития этих повреждений вводят данную кислоту. Количество вводимого препарата будет зависеть от количества и размеров повреждений и потребностей пациента.
9-цис ретиноевая кислота, ее фармацевтически приемлемые соли или ее фармацевтически приемлемые гидролизуемые сложные эфиры особенно эффективны при лечении предраковых и предзлокачественных поражений эпителия кожи, груди, толстой кишки, мочевого пузыря, пищевода, желудка, гортани, легких и полости рта. В соответствии с предпочтительным вариантом осуществления это соединение может быть использовано для лечения предзлокачественных или предраковых поражений, таких как различные лейкоплакии, в особенности губ и языка, а также предзлокачественных и предраковых поражений груди.
В соответствии с еще одним вариантом осуществления изобретения 9-цис ретиноевая кислота, ее фармацевтически приемлемые соли или ее фармацевтически приемлемые гидролизуемые сложные эфиры могут быть использованы для лечения карциномы или опухолей эпителиального происхождения с целью замедления развития этих опухолей. В соответствии с противокарциномными и противоопухолевыми свойствами этого соединения лечения опухолей этим соединением вызывает сокращение как числа, так и размеров этих опухолей. При использовании этого соединения как противоопухолевого агента это соединение особенно эффективно для замедления развития опухолей груди, кожи, толстой кишки, мочевого пузыря, пищевода, желудка, гортани, легких или губ. 9-цис ретиноевая кислота может вводиться пациентам описанным выше способом для случаев лечения пациентов, имеющих предзлокачественные или предраковые поражения.
Для лечения перечисленных выше заболеваний 9-цис ретиноевая кислота, ее фармацевтически приемлемые соли или ее фармацевтически приемлемые гидролизуемые сложные эфиры вводят или системно, или местно как состав, содержащий 9-цис ретиноевую кислоту и фармацевтически приемлемый носитель, совместимый с указанным соединением. При приготовлении такого состава может быть использован любой обычный фармацевтически приемлемый носитель. Когда лекарственное средство вводится через рот, оно обычно вводится через регулярные интервалы, чаще всего при приеме пищи или один раз в день. Установлено, что это соединение относительно нетоксично при местном применении и при приеме через рот.
Примерами состояний, включающих предзлокачественные и предраковые эпителиальные поражения или опухоли, лечение которых эффективно обеспечивается 9-цис ретиноевой кислотой, является актенический кератоз, мышьяковый кератоз, ксеродерма пигментная, болезнь Боуэна, лейкоплакия, метаплазия, дисплазия и папиллома слизистой оболочки, например, губ, языка, глотки и гортани, предраковые изменения бронхиальной слизистой оболочки, такие как метаплазия и дисплазия (в особенности у заядлых курильщиков и людей, работающих с асбестом и/или ураном), дисплазия и лейкоплазия шейки матки, дистрофия вульвы, предраковые изменения мочевого пузыря, например, метаплазия и дисплазия, папиллома мочевого пузыря, а также полипы кишечного тракта. Примеры опухолей или карционом условно злокачественного или злокачественного характера, эпителиального происхождения, лечение которых эффективно обеспечивается 9-цис ретиноевой кислотой, включают опухоли груди, опухоли кожи, например, базально-клеточная карцинома, опухоли толстой кишки, опухоли пищевода, опухоли желудка, опухоли гортани и опухоли легких.
Лечение предраковых поражения и злокачественных опухолей эпителиального характера могут осуществляться 9-цис ретиноевой кислотой, ее фармацевтически приемлемыми солями или фармацевтически приемлемыми гидролизуемыми сложными эфирами отдельно или в сочетании с другими мерами, такими как хирургическое вмешательство, лучевая терапия, гормональная терапия или лечение обычной химиотерапией (цитостатическими или цитотоксическими агентами) или модификаторами биологической чувствительности (интерфероны, интерлейкины или иные цитокины).
Более того, в соответствии с настоящим изобретением обнаружено, что 9-цис ретиноевая кислота, ее фармацевтически приемлемые соли или ее фармацевтически приемлемые гидролизуемые сложные эфиры, примененные местно к коже пациента, способствуют улучшению состояний, связанных со световым поражением. Поэтому местное применение соединений формулы I к коже пациентов, пострадавшей от солнечного облучения, позволяет прекратить сморщивание, эластоз и преждевременное старение, что ведет к улучшению внешнего вида кожи.
Благодаря местному применению соединений формулы I и фармацевтически приемлемых солей и гидролизуемых сложных эфиров достигается ускорение исправления повреждения кожи и обеспечивается более гладкий и юный внешний вид кожи.
В соответствии с настоящим изобретением обнаружено, что при введении через рот или местном применении 9-цис ретиноевой кислоты, ее фармацевтически приемлемых солей или ее фармацевтически приемлемых гидролизуемых сложных эфиров снижается салоотделение. Поэтому введение этого соединения, ведущего к уменьшению салоотделения и угреобразования, дает средство борьбы с такими заболеваниями как угри, сальные волосы и сальный скальп. Таким образом, введение настоящего соединения может быть использовано в качестве профилактики заболеваний, связанных с избыточным салоотделением, таких как угри и сальный скальп или волосы, или для их лечения.
Известно, что подавление образования и/или отделения сала является эффективным при лечении и/или предупреждении таких заболеваний, как угри. Увеличенное салоотделение может привести в таким дерматологическим заболеваниям, как себорея, включая перхоть, сальную кожу, сальные волосы, белые угри и черные угри.
В соответствии с настоящим изобретение местное применение и введение через рот соединения формулы I, его фармацевтически приемлемых солей и его фармацевтически приемлемых гидролизуемых сложных эфиров оказывается эффективными при лечении всех форм угрей, как воспалительного, так и невоспалительного характера.
Еще одним аспектом настоящего изобретения является то, что 9-цис ретиноевая кислота, ее фармацевтически приемлемые соли или ее фармацевтически приемлемые гидролизуемые сложные эфиры оказываются эффективными при лечении псориаза при их местном применении или введении через рот пациентам, страдающим псориазом. Их применение ведет к снижению воздействия заболевания псориазом на кожу.
К фармацевтически приемлемым солям относятся любые соли 9-цис ретиноевой кислоты, которые можно применять пациентам после фармацевтической обработки. Возможно применение любой обычной фармацевтически приемлемой соли. Среди обычных солей, применение которых возможно, находятся основные соли, включающие, например, соли щелочных металлов, таких как натрий или калий, соли щелочноземельных металлов, таких как кальций или магний, и соли аммония или алкиламмония.
В соответствии с настоящим изобретением 9-цис ретиноевая кислота может быть введена в форме ее фармацевтически приемлемых гидролизуемых сложных эфиров. Любой фармацевтически приемлемый гидролизуемый сложный эфир может быть использован в составах и методах, являющихся предметом настоящего изобретения. Среди сложных эфиров можно указать ароматические сложные эфиры, такие как бензил (OBzl) или бензил, замещенный низшим алкилом, галоином, нитрогруппой; или низший алкил, например, трет.-бутил; или циклопентил, циклогексил, циклогептил; или 9-флуоренилметил.
В соответствии с настоящим изобретением 9-цис ретиноевая кислота или ее фармацевтически приемлемые соли или ее фармацевтически приемлемые гидролизуемые сложные эфиры могут быть представлены в фармацевтически приемлемом для введения через рот или местного применения видов. Эти фармацевтические составы содержат указанную 9-цис ретиноевую кислоту или ее фармацевтически приемлемые соли и ее фармацевтически приемлемые гидролизуемые сложные эфиры в сочетании с совместимым фармацевтически приемлемым материалом носителя. Возможно применение любого обычного материала носителя. Материал носителя может быть органическим или неорганическим инертным материалом, пригодным для введения через рот. К подходящим носителям относятся вода, желатин, гуммиарабик, лактоза, крахмал, стеарат магния, растительные масла, полиалкиленгликоли, вазелин и тому подобные. Кроме того, фармацевтические составы могут содержать другие фармацевтически активные агенты. Возможно добавление, в соответствии со сложившей практикой приготовления лекарств, таких добавок как вкусовые вещества, консерванты, стабилизаторы, эмульгаторы, буферы и тому подобные.
Лекарственные средства могут быть приготовлены в любой обычной форме, включая: а) твердую форму для введения через рот, такую как таблетки, капсулы, пилюли, порошки, гранулы и тому подобные; и б) средства для местного применения, такие как растворы, суспензии, мази, кремы, гели, тонкие порошки, аэрозоли и тому подобные. Лекарственные средства могут быть стерилизованы и/или содержать адъюванты, такие как консерванты, стабилизаторы, смачивающие агенты, эмульгаторы, соли для варьирования осмотического давления и/или буферы.
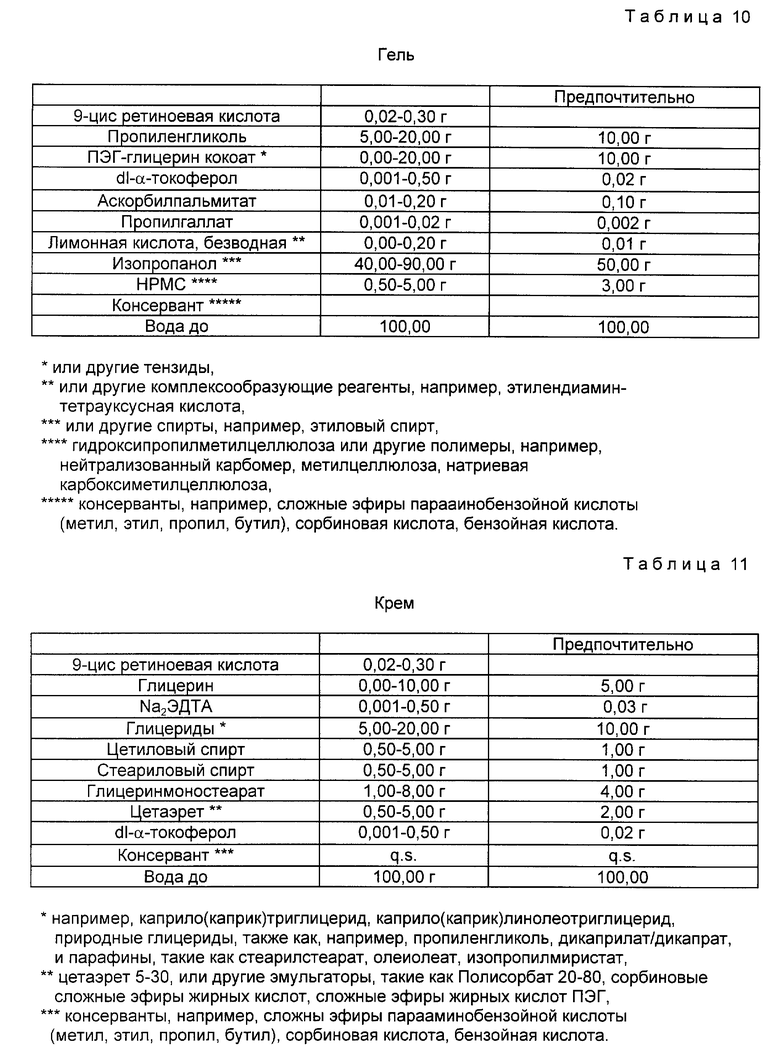
Для местного применения на коже указанное соединение предпочтительно готовить в виде мазей, тинктур, кремов, гелей, растворов, лосьонов, аэрозолей, суспензий, шампуней, мыла для волос, духов и т.п. На практике любой обычный состав, используемый для применения к скальпу или коже, может использоваться в соответствии с настоящим изобретением. Среди предпочтительных методов применения состава, содержащего агенты, являющиеся предметом настоящего изобретения, находятся формы гелей, лосьона и крема.
Фармацевтический состав для местного применения на коже может быть приготовлен путем смешивания указанного выше активного ингредиента с нетоксичным, терапевтически инертным, твердым или жидким носителем из числа обычно применяемых при приготовлении таких составов. Эти составы должны содержать по меньшей мере приблизительно 0,01% по весу активного ингредиента от суммарного веса состава. Поскольку активный ингредиент, 9-цис-ретиноевая кислота, относительно нетоксичен и нераздражающ, он может применяться в составах для местного применения в количествах, превышающих 0,15%. Предпочтительным является, чтобы эти составы содержали около 0,01 - 0,15% по весу активного ингредиента от суммарного веса состава. Предпочтительно также наносить эти составы на кожу один или два раза в день. Эти составы могут применяться в зависимости от потребностей пациента. При реализации изобретения активный ингредиент может наноситься в водном растворе или спиртовом растворе, таком как раствор в этиловом спирте.
При приготовлении составов для местного применения, описанных выше, возможно применение таких добавок как консерванты, сгустители, духи и тому подобных, обычных при приготовлении составов для местного применения. Кроме того, в составах для местного применения, включающих указанный выше активный ингредиент, могут быть использованы антиокислители или смеси обычных антиокислителей. Среди обычных антиокислителей, которые могут быть использованы в этих составах, может указать N- метил- -α- -токофероламин, токоферолы, бутилированный гидроксианизол, бутилированный гидрокситолуол, этоксихин и тому подобные. Фармацевтические составы на основе кремов, содержащие активный ингредиент, применяемые в соответствии с настоящем изобретением, составлены из водных эмульсий, содержащих спирт жирной кислоты, полутвердый нефтяной углеводород, 1,2-этиленгликоль и эмульгатор.
Составы мазей, содержащие активный ингредиент в соответствии с настоящим изобретением, включают полутвердый нефтяной углеводород с рассеянным в растворителе активным материалом. Составы кремов, содержащие активный ингредиент в соответствии с настоящем изобретением, предпочтительно представляют собой эмульсии, образованные из водной фазы увлажнителя, стабилизатора вязкости и воды, масляной фазы спирта жирной кислоты, полутвердого нефтяного углеводорода и эмульгатора, и фазы, содержащей активный ингредиент, распыленный в водном стабилизированном буферном растворе. Стабилизаторы могут быть добавлены в состав, предназначенный для местного применения. В связи с настоящим изобретением может быть использован любой обычный стабилизатор. Эти компоненты спирта жирных кислот получают путем восстановления насыщенной жирной кислоты с длинной цепью, состоящей из по меньшей мере 14 атомов углерода. Кроме того, обычно при приготовлении составов для местного применения для волос в соответствии с настоящим изобретением могут быть применены обычные духи и лосьоны. Кроме того, при желании, в составах для местного применения, являющихся предметом настоящего изобретения, могут использоваться обычные эмульгаторы.
Предпочтительная форма дозирования для введения через рот включает таблетки, капсулы из твердого или мягкого желатина, метилцеллюлозы или иного подходящего материала, легко растворяющегося в пищеварительном тракте. Дозирование для введения через рот, рассматриваемое в связи с настоящим изобретением, будет меняться в зависимости от потребностей конкретного пациента в соответствии с предписаниями лечащего врача. Обычно, однако, применяется ежедневная доза в пределах от приблизительно 0,01 мг до приблизительно 3 мг в расчете на 1 кг веса тела пациента и предпочтительно от приблизительно 0,025 мг до приблизительно 1,5 мг/кг. Эта доза может вводиться в соответствии с любым порядком дозировки, определенным врачом, в зависимости от потребностей пациента.
В сферу настоящего изобретения входит также включение терапевтически активного вещества в любом количестве в пределах дозы для введения в тонкую кишку через рот. Предпочтительно, однако, готовить составы, содержащие активное вещество, являющееся предметом настоящего изобретения, таким образом, чтобы каждая доза содержала от приблизительно 1 мг до приблизительно 50 мг активного вещества с подходящим терапевтически инертным заполнителем или разбавителем. Особенно предпочтительным является включение такой дозы в капсулы из мягкого желатина и таблетки.
Эффективность 9-цис ретиноевой кислоты при использовании в соответствии с настоящим изобретением демонстрируется на описанных ниже моделях.
А. Противоопухолевое воздействие 9-цис ретиноевой кислоты на линии клеток опухоли человека и на экспериментальную опухоль.
Сдерживающее действие на рост и размножение трансформированных линий клеток эпителия человека.
9-цис ретиноевую кислоту испытывали на линиях клеток опухоли человека SCC15 (клетки рака плоского эпителия языка) и A 431 (клетки рака плоского эпителия вульвы). Разрастание определяли по способности жизнеспособных клеток восстанавливать краситель МТТ [3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолбромид] за счет митохондриальной энзиматической активности (Mosmann Т. Rapid colorimetric assay for cellular growth and survival: application to proliferation and cytotoxic assays. J. Immunol. Methods 65: 55-63, 1983).
Результаты
Клетки рака плоского эпителия человека SCC 15 (язык):
Жизнеспособные клетки в % к контрольному образцу после 7 дн инкубации представлены в табл.1.
9-цис ретиноевая кислота при концентрации 3•10-7 M подавляет рост клеток на 46%, а в сочетании с IFNα- даже на 80%.
Клетки рака плоского эпителия человека A 431 (вульва):
Жизнеспособные клетки в % к контрольному образцу после 7 дн инкубации представлены в табл. 2.
9-цис ретиноевая кислота при концентрации 3•10-7 M подавляет рост клеток на 64%, а в сочетании с IFNα- даже на 77%.
9-цис ретиноевая кислота обладает выраженным подавляющим рост воздействием на две испытанные клеточные линии рака эпителия человека.
Далее исследовалось воздействие 9-цис ретиноевой кислоты на другие трансформированные линии клеток. Оценка разрастания была выполнена на линии клеток, содержащих вирус. SKv-II, трансформированную линию кератиноцита, содержащую вирус папилломы человека 16 (HPV 16) испытывали на подавление ее разрастания 9-цис ретиноевой кислотой в двух экспериментах с четырьмя воспроизведениями. В среду Игла помещали по 5•104 клеток в ячейке и выдерживали в термостате в течение 2 дн. До и после выдерживания в термостате с ретиноидом при концентрации 10-6M с помощью гемоцитометра проводили непосредственный подсчет количества клеток, одновременно подсчитывая клетки в контрольных образцах DMSO. Подавление роста выражено в % по сравнению с контрольными образцами.
Результат: 9-цис ретиноевая кислота при концентрации 10-6М подавляет разрастание трансформированных кератиноцитов человека SKv-II на 32,4% (р<0,001).
Б. Воздействие 9-цис ретиноевой кислоты на связанное с клетками опухолей развитие кровеносных сосудов.
В настоящее время точно установлено, что неограниченный рост опухолей зависит от развития кровеносных сосудов. Росту популяции клеток опухолей должно предшествовать увеличение числа новых капилляров, которые сходятся в опухоли. Поэтому сдерживание развития кровеносных сосудов сдерживает рост опухоли (Folkman J. How is blood vessel growth regulated in normal and neoplastic tissue? G. H. A. Clowed Memorial Award Lecture. Cancer Res. 46: 467-473, 1986; Sidky Y. A. and Borden E.C. Inhibition of angiogenesis by interferons: Effects on tumor - and lymphocyte-induced vascular responses. Cancer Res. 47: 5155-5161, 1987).
Опыты по оценке развития кровеносных сосудов были описаны ранее (Sidky Y. A. and Auerbach R. Lymphocyte induced angiogenesis: A quantitative and sensitive assay of the graft-vs-host reaction. J. exp. Med. 141: 1084-1100, 1975; Majewski S. et al. Inhibition of tumour-induced angiogenesis by systemically administered protamine sulphate. Int. J. Cancer 33: 831-833, 1984). Два опыта были проведены для испытания 9-цис ретиноевой кислоты. В первом опыте ретиноид добавили in vitro в клеточную линию перед инъекцией мышам. Во втором опыте мышам ввели внутрибрюшинно ретиноид in vivo до того, как под кожу ввели линию клеток опухоли.
Способ: Клетки двух онкогенных линий (SKv-e2 и HeLa) и линию неонкогенных клеток (SKv-e1) предварительно выдерживали в термостате in vitro в течение 48 ч с 9-цис ретиноевой кислотой при концентрации 10-7M с последующим подсчетом клеток и промывкой в среде ТС 199. Концентрацию клеток доводили до 2•105 жизнеспособных клеток на 0,1 мл среды и вводили под кожу подвергнутым рентгеновскому облучению, но не получавшим ретиноида мышам колонии Balc/c. Контрольным животным вводили опухолевые клетки, предварительно выдерживавшиеся в термостате с диметилсульфоксидом. Воздействие на развитие кровеносных сосудов определяли согласно методам, упомянутым выше.
Результаты
а) Влияние предварительного выдерживания in vitro с 9-цис ретиноевой кислотой на развитие кровеносных сосудов клеточных линий SKv-e2 (онкогенные), HeLa (онкогенные) и SKv-e1 (неонкогенные) у мышей колонии Balc/с (см. табл. 3).
В отличие от сдерживающего воздействия, которое 9-цис ретиноевая кислота оказывает на формирование новых кровеносных сосудов, которое вызвано двумя линиями онкогенных клеток, 9-цис ретиноевая кислота не подавляет развития кровеносных сосудов, вызванного неонкогенной подлинней.
б) Подавление вызванного клетками развития кровеносных сосудов путем предварительной обработки мышей колонии Balc/c 9-цис ретиноевой кислотой (см. табл. 4).
Обработка мышей 9-цис ретиноевой кислотой подавляла формирование новых кровеносных сосудов, когда им вводили клетки трех онкогенных линий. При использовании неонкогенных клеток такого эффекта не наблюдалось.
9-цис ретиноевая кислота подавляет in vitro и in vivo формирование новых кровеносных сосудов, вызываемое линиями онкогенных клеток. Поскольку для роста опухоли необходима прединкубация, 9-цис ретиноевая кислота оказывает не только прямое противоопухолевое воздействие через подавление разрастания и/или индуцирование дифференциации, но и препятствует развитию кровеносных сосудов, подавляя тем самым рост опухоли косвенным путем.
В. Воздействие 9-цис ретиноевой кислоты на химически индуцированную папиллому кожи мышей
Предупреждающее и терапевтическое воздействие ретиноидов на химически индуцированные опухоли кожи, дыхательных органов, пищеварительного и 5 мочевого трактов, а также молочных желез хорошо изучено (Bollag W. and Hartmann HR. Prevention and therapy of cancer with retinoids in animal and man. Cancer Surveys 2: 293-314, 1983). 9-цис ретиноевая кислота обладает выраженным терапевтическим воздействием на установившиеся папилломы кожи у мышей, ведя к уменьшению этих эпителиальных опухолей. Опыты на папилломе являются стандартными опытами для определения противоопухолевого воздействия ретиноидов.
Результаты приведены в табл. 5.
9-цис ретиноевая кислота обладает значительным терапевтическим противораковым воздействием на установившиеся папилломы кожи мышей химического происхождения, вызывая сокращения этих эпителиальных опухолей.
Г. Воздействие 9-цис ретиноевой кислоты на противопсориазное действие.
Противопсориазное действие можно определить по способности вызывать уменьшение химически индуцированной папилломы кожи мышей в опытной модели, описанной в параграфе В. Опыты на папилломе являются стандартными опытами для определения противопсориазного воздействия ретиноидов (Teelmann К., Bollag W. The relevance of the mouse papilloma test as a predictor of retinoid activity in human psoriasis. Dermatologica 180: 30-35, 1990).
Как можно видеть из данных, приведенных в параграфе В, 9-цис ретиноевая кислота обладает выраженным терапевтическим воздействием в этой модели из чего можно прогнозировать противопсориазное воздействие на человека.
Д. Воздействие 9-цис ретиноевой кислоты на угри и салоотделение.
Этиология угрей многофакторна, причем ключевую роль в их патологии играют избыточное салоотделение, гиперкератинизация и образование колоний микроорганизмов.
Для определения противоугревого воздействия были использованы следующие две модели:
1. Показатели опытов по противодействию развития сальных клеток человека хорошо согласовались с результатами клинических исследований соединений на пациентах, страдающих угрями (Doran T.I. and Shapiro S.S. Retinoid effects on sebocyte proliferation. In "Retinoids, Part B. Cell Differentiation and Clinical Applications". Methods in Enzymology, Volume 190. Ed. L.Packer, 15 Academic Press, pp.334-338, 1990).
2. Для определения противоугревого воздействия были использованы противокератозные опыты на носатых мышах (Mezick J.A., Bhatia М.С. and Capetola R.J. Topical and systemic effects of retinoids on horn-filled utriculus size in the rhinomouse. A model to quantify "antikeratinizing" effects of retinoids. J. Invest. Dermatol. 83, 110-113, 1984. Mezick J.A., Bhatia М.С., Shea L.M., Thorne E.G. and Capetola R.J. Anti-acne activity of retinoids in the Rhinomouse. In: Models of Dermatology, Maibach and Lowe (eds.), Karger (Basel), v.2, pp.59-63, 1985).
I. Разрастание сальных клеток
1. Метод
Сальные клетки изолировали от сальных желез взрослого человека, извлеченных из кожи лица, удаленной в процессе косметической операции, и приживляли в слое фибробластов ЗТЗ мыши (Doran T.I., Baff R., Jacobs P. and Pacia E. Characterization of human sebaceous cells in vitro. J. Invest. Dermatol. 96, 341-348, 1991). Клетки помещали в среду без испытываемого соединения, а через 24-48 ч добавляли испытываемое соединение в свежую среду. Культурам добавляли свежую среду, содержащую испытываемое соединение, каждые 48 ч. В день сбора результатов культуру промывали 0,03%-ным раствором EDTA в PBS, чтобы удалить только фибробласты ЗТЗ, с последующей инкубацией в 0,05% трипсина (0,03%) EDTA. Клетки переводили в суспензию, энергично перемешивали, чтобы получить суспензию отдельных клеток и пересчитали их на гемоцитометре. Результаты определяли как количество соединения, необходимое для сокращения разрастания жировых клеток на 50% (IC50) в мкМ по сравнению с контрольной культурой, которую обрабатывали только разбавителем.
II. Результаты
9-цис ретиноевая кислота оказалась активной in vitro при подавлении 10 разрастания жировых клеток человека с IC50 для 0,1 мкМ.
2. Уменьшение эллиптического мешочка у носатых мышей, противокератозный опыт
1. Метод
Самки носатых мышей (hrhrhrhr) в возрасте от 6 до 8 недель были получены в лаборатории Джексона. В группах использовалось по 6 животных. Соединение готовили, растворяя его в ацетоне. Испытываемые соединения наносили на спину мышей микропипеткой. В течение 5 дн три недели последовательно наносили ежедневно по 100 мкл испытываемого материала. Мышей умертвляли в атмосфере CO2. Из спины вырезали полоску кожи, которую сохраняли для гистологического исследования. Эпидерма, отделенная от дермы, была помещена в гистологические кассеты из проволочной сетки и дегидрировалась в 70%, 80%, 95%, 100% этаноле и ксилоле по 2 ч на каждой стадии. Образцы кожи извлекали из ксилоловой ванны и помещали на предметное стекло микроскопа. Для определения средней площади эллиптических мешочков был применен анализ изображения с использованием системы "Ультимедж". У каждой мыши было проанализировано приблизительно 150 эллиптических мешочков.
II. Результаты
Влияние 9-цис ретиноевой кислоты на уменьшение размеров эллиптических мешочков у носатых мышей после местного применения в течение 3 недель (см. табл. 6).
Все значения p были менее 0,001 при сопоставлении групп, обработанных соединением с группами, обработанными носителем. Для статистического определения использовали t-критерий Стьюдента.
9-цис ретиноевая кислота была активной в опытах по противоугревому и противокератозному воздействию.
Е. Клинические данные лечения пациентов с угрями обыкновенными 9-цис ретиноевой кислотой.
Восемь пациентов, 2 мужчин и б женщин, в возрасте от 15 до 48 лет, при среднем возрасте 27 лет, проходили лечение 9-цис ретиноевой кислотой в течение от 1 до 3 месяцев. Из 8 пациентов двое проходили лечение в течение 1 месяца, двое - 2 месяца и четверо - 3 месяца. Пять пациентов имели комедоны, семь - папулы, шесть - пустулы и один - узелки. Семь пациентов имели поражения только на лице, один пациент имел поражения на лице и на спине. 9-цис ретиноевую кислоту давали в следующем виде: 0,01% активного соединения в растворе этанолпропиленгликоля (50/50). Раствор наносили 1 раз в день по вечерам на участки, где присутствовали угревые поражения.
Количество поражений (комедонов, папул, пустул и узелков) подсчитывали раздельно перед началом лечения и через 1, 2 и 3 месяца лечения. Для каждого пациента определяли процентное уменьшение общего количества поражений по сравнению с исходным показателем и подсчитывали среднее значение.
Результаты были следующими: через 1 месяц общее количество поражений (8 пациентов) уменьшилось в среднем на 48%, через 2 месяца (6 пациентов) - на 72% и через 3 месяца (4 пациента) - на 77%. Особое внимание уделяли раздражению кожи. У двух пациентов в начале лечения наблюдались легкая эритема и небольшое шелушение, которые оказались исчезли через 1-2 недели, несмотря на продолжение лечения. Пациенты почти не обратили внимания на это побочное воздействие.
Лечение угрей 9-цис ретиноевой кислотой дало очень хорошие результаты, близкие с результатами, полученными с транс- или 13-цис ретиноевой кислотой. Концентрация лекарства, необходимая для успешного местного лечения равнялась 0,01% и была заметно ниже, чем для транс-ретиноевой кислоты или 13-цис ретиноевой кислоты, когда для получения тех же лечебных результатов необходима концентрация 0,05%. Кроме того, терапевтически эффективная концентрация 9-цис ретиноевой кислоты обладала значительно меньшим побочным эффектам по сравнению с транс- или 13-цис ретиноевой кислотой.
Ж. Активность 9-цис ретиноевой кислоты при световых поражениях.
1. Методы
Голых мышей подвергли ультрафиолетовому облучению, после чего применили местное лечение 9-цис ретиноевой кислотой, чтобы добиться исправления повреждений кожи.
Кожу из облученного и подвергнутого лечению участка подвергали гистологическому исследованию с целью определить степень восстановления. Восстановление определяли по внешнему виду нормализованной дермы, расположенной вниз от эпидермы до слоя сжатого эластина. Степень восстановления отражается на ширине этой зоны.
Методы описаны в Bryce G. F., Bogdan N.J., Brown С.С. Retinois acids promote the repair of the dermal damage and the effacement of wrinkles in the UVB-irradiated hairless mouse. J. Invest. Dermatol. 91, 175-180, 1988.
2. Результаты приведены в табл. 7.
3. Острая токсичность
Острую токсичность определяли на мышах-альбиносах Фюллинсдорфа. 9-цис ретиноевую кислоту переводили во взвесь в рапсовом масле и вводили внутрибрюшинно одной дозой. После введения разовой дозы определяли летальную дозу (ЛД) для 10%, 50% и 90% мышей через 24 ч, 10 дн и 20 дн. В каждой группе использовалось 10 мышей (см. табл. 8).
Следующие примеры иллюстрируют фармацевтические составы, содержащие 9-цис ретиноевую кислоту, как предложено в настоящем изобретении.
Соединение 9-цис ретиноевой кислоты может также быть обозначено названием (E,Z,E,E)-3,7-диметил-9-(2,6,6-триметил-1-циклогексен-1-ил)- 2,4,6,8-нонатетреновая кислота.
Примеры 1 - 7 представлены в табл. 9 - 15.
Процедура приготовления капсул из твердого желатина.
Активный ингредиент во влажном состоянии подвергают измельчению в растворе желатина, мальтодекстрина, dl-альфа-токоферола и аскорбата натрия. Полученную суспензию подвергают сушке распылением. Высушенный порошок перемешивают с микрокристаллической целлюлозой и стеаратом магния. 260 мг этой смеси помещают в капсулы из твердого желатина подходящего размера и цвета.
Процедура приготовления таблеток.
9-Цис ретиноевую кислоту смешивают с безводной лактозой и микрокристаллической целлюлозой.
Смесь гранулируют в воде с раствором/дисперсией поливинилпирролидона, dl-альфа-токоферола и аскорбата натрия. Гранулированный материал смешивают со стеаратом магния и после этого прессуют в сердцевины весом по 250 мг. На сердцевины наносят пленочное покрытие из раствора/суспензии указанного выше состава.
Процедура приготовления саше.
9-Цис ретиноевую кислоту смешивают с лактозой, микрокристаллической целлюлозой и натриевой карбоксиметилцеллюлозой. Смесь гранулируют в воде с раствором/дисперсией поливинилпирролидона, dl-альфа-токоферола и аскорбата натрия. Гранулы смешивают со стеаратом магния и вкусовыми добавками. Их засыпают в пакет-саше подходящих размеров.




Изобретение относится к медицине. Фармацевтический состав для лечения эпителиальных поражений или эпителиальных опухолей, лучевые поражения кожи, псориаза, лейкоплакии полости рта и для уменьшения салоотделения содержит 9-цис ретиноевую кислоту и фармавцевтически приемлемый носитель. Предложенный состав проявляет ограниченные токсичность и другие отрицательные эффекты, вызываемые ретиноидами. 6 з.п.ф-лы, 15 табл.
Приоритет по пунктам:
22.01.92, - по пп.1 - 3, 5 - 7;
23.01.92. - по п.4.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| US 4603146 A, 1986, A 61 K 31/20 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Шланговое соединение | 0 |
|
SU88A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Способ размножения копий рисунков, текста и т.п. | 1921 |
|
SU89A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| US 3966967, 1976, A 61 K 31/07. | |||
Авторы
Даты
1998-09-27—Публикация
1993-01-20—Подача