Настоящее изобретение относится к новым агонистам ретиноидов (ретиноидным агонистам) и способам их синтеза. Изобретение относится также к применению указанных новых ретиноидных агонистов и содержащим их фармацевтическим композициям.
Ретиноиды представляют собой структурные аналоги витамина А и включают как встречающиеся в естественных условиях, так и синтетические соединения. Такие ретиноиды, как полностью транс-ретиноевая кислота ("ATRA"), 9-цис-ретиноевая кислота, транс-3-4-дидегидроретиноевая кислота, 4-оксоретиноевая кислота, 13-цис-ретиноевая кислота и ретинол, являются плейотропными регуляторными соединениями, которые оказывают влияние на многочисленные воспалительные, иммунные и структурные клетки.
Например, ретиноиды модулируют пролиферацию эпителиальных клеток, морфогенез в легких и дифференцировку, воздействуя на ряд гормональных нуклеарных рецепторов, относящихся к суперсемейству стероидных/тиреоидных рецепторов. Ретиноидные рецепторы подразделяют на рецепторы ретиноевой кислоты (RAR) и ретиноидные Х-рецепторы (RXR), причем каждая группа состоит из трех различных подтипов (α, β и γ).
ATRA представляет собой встречающийся в естественных условиях лиганд рецепторов ретиноевой кислоты и обладает близкой аффинностью к связыванию с α-, β- и γ-подтипами. Для многих синтетических ретиноидных агонистов α-, β- и γ-подтипов RAR была установлена количественная взаимосвязь между структурой и активностью, что позволило выявить основные электронные и структурные характеристики, обусловливающие избирательную аффинность каждого из подтипов RAR (Douget и др. Quant. Struct. Act. Relat., 18, 107, 1999).
ATRA не связывается с RXR, для которого встречающимся в естественных условиях лигандом является 9-цис-ретиноевая кислота. Описаны также многочисленные синтетические ретиноидные агонисты α-, β- и γ-подтипов RXR и RAR (см., например, Billoni и др., US 5962508; Belloni и др., WO 01/30326, опубликована 3 мая 2001 г.; Klaus и др., US 5986131; и Bernardon и др., WO 92/06948, опубликована 30 апреля 1992 г.).
Ретиноиды, как правило, обладают противовоспалительной активностью в тканях, отличных от ткани легкого, могут изменять в них процесс дифференцировки эпителиальных клеток и могут ингибировать продуцирование матрикса стромальными клетками. Такие биологические действия ретиноидов позволили создать большое количество агентов для местного лечения дерматологических заболеваний, таких как псориаз, угри и гипертрофированные кожные рубцы. Ретиноиды применяли также для лечения вызванных световым излучением и связанных с возрастом повреждений кожи, заживления ран, вызванных, например, хирургическим вмешательством и ожогами (Mustoe и др. Science 237, 1987, с.1333; Sprugel и др., J.Pathol., 129, 1987, с.601; Boyd, Am.J.Med., 86, 1989, с.568), и в качестве противовоспалительных агентов для лечения артрита. Другие области медицинского применения ретиноидов включают лечение острой промиелозной лейкемии, аденокарциномы, плоскоклеточного рака и фиброза печени. Ретиноиды широко применяют также для лечения предраковых эпителиальных повреждений и злокачественных опухолей (карцином) эпителиального происхождения (Bollag и др., US 5248071; Sporn и др., Fed. Proc. 1976, с.1332; Hong и др., "Retinoids and Human Cancer" в The Retinoids: Biology, Chemistry and Medicine, под ред. М.В.Sporn, А.В.Roberts и D.S.Goodman, изд-во Raven Press, Нью-Йорк, c.597-630, 1994). Однако многие известные ретиноиды не обладают избирательным действием и поэтому оказывают вредные плейотропные действия, которые при применении ретиноидов в терапевтически эффективных количествах могут привести к смерти пациента. Таким образом, терапевтическое применение ретиноидов для лечения болезней, не связанных с раком, ограничено токсическими побочными действиями. Общий обзор ретиноидов приведен у Goodman и Gilman "The Pharmacological Basis of Therapeutics", главы 63-64, 9-е изд., изд-во McGraw-Hill, 1996.
Хроническое обструктивное заболевание легких (ХОЗЛ) относится к большой группе легочных заболеваний, которые приводят к нарушению нормального дыхания. Приблизительно 11% населения Соединенных Штатов страдает ХОЗЛ и имеются данные о том, что количество случаев заболевания ХОЗЛ возрастает. В настоящее время ХОЗЛ занимает четвертое место среди заболеваний, приводящих к смертельному исходу, в Соединенных Штатах.
ХОЗЛ обозначает заболевание, при котором происходит обструкция легких вследствие наличия по меньшей мере одного заболевания, входящего в группу, которая включает астму, эмфизему и хронический бронхит. Причина введения понятия ХОЗЛ заключалась в том, что указанные состояния часто встречаются одновременно и в конкретных случаях может оказаться затруднительным определить, какое заболевание является причиной обструкции легкого (Merck Manual, 1987). С клинической точки зрения ХОЗЛ характеризуется уменьшенной объемной скоростью выдоха из легких, которая остается постоянной в течение нескольких месяцев и в случае хронического бронхита может сохраняться в течение 2 или более последовательных лет. В наиболее серьезных случаях ХОЗЛ, как правило, проявляются симптомы, характерные для эмфиземы.
Эмфизема представляет собой заболевание, при котором происходит нарушение структур, осуществляющих газообмен в легком (например, альвеол), что вызывает неадекватную оксигенацию, которая может приводить к потере трудоспособности и смерти. С анатомической точки зрения эмфизему определяют по постоянному увеличению воздушного пространства, находящегося дистальнее терминальных бронхиол (например, дыхательных трубок), что характеризуется постепенным уменьшением эластичности легкого, уменьшением площади поверхности альвеол и газообмена и разрушением альвеол, что приводит к снижению дыхательной способности. Таким образом, характерными физиологическими аномалиями, связанными с эмфиземой, являются ухудшение газообмена и уменьшение объемной скорости выдоха.
Наиболее частой причиной возникновения эмфиземы является курение сигарет, хотя и другие токсины, встречающиеся в окружающей среде, могут оказывать влияние на разрушение альвеол. Вредные соединения, которые присутствуют в таких опасных агентах, могут активировать деструктивные процессы, включающие, например, высвобождение избыточного количества протеаз, которое не может быть нейтрализовано с помощью обычных защитных механизмов, таких как ингибиторы протеаз, присутствующие в легком. Нарушение баланса между протеазами и ингибиторами протеаз, присутствующими в легком, может приводить к разрушение эластинового матрикса, уменьшению эластической тяги легкого, повреждению ткани и непрерывному снижению функции легкого. Скорость развития такого повреждения легкого можно замедлять с помощью уменьшения количества токсинов в легком (т.е. путем прекращения курения). Однако поврежденные альвеолярные структуры не восстанавливаются и функция легкого не нормализуется. В зависимости от расположения пораженной области во вторичной дольке различают по меньшей мере четыре типа эмфиземы: панлобулярная эмфизема, центрилобулярная эмфизема, дистальная лобулярная эмфизема и парацикатрикальная эмфизема.
Основным симптомом эмфиземы является хроническая одышка. Другие важные симптомы эмфиземы включают (но не ограничиваясь ими) хронический кашель, изменение окраски кожи, вызванное недостатком кислорода, одышку при минимальной физической активности и стерторозное дыхание. Дополнительные симптомы, которые могут быть связаны с эмфиземой, включают (но не ограничиваясь ими) нарушения зрения, головокружение, временную остановку дыхания, страх, отечность, усталость, бессонницу и потерю памяти. Как правило, эмфизему диагностируют путем физического исследования, на основе которого выявляют ослабленные и аномальные шумы при дыхании, стерторозное дыхание и пролонгированный выдох. Для подтверждения диагноза эмфиземы можно проводить исследования функции легкого, выявление пониженных уровней кислорода в крови и рентгеноскопию грудной клетки.
В настоящее время отсутствуют эффективные методы реверсии клинических симптомов эмфиземы. В некоторых случаях путем введения в легкое с помощью ингялатора или распылителя лекарственных средств, таких как бронхолитические средства, β-агонисты, теофиллин, антихолинергетики, диуретики и кортикостероиды, можно улучшить нарушенное эмфиземой дыхание. В ситуациях, когда функция легкого нарушена настолько серьезно, что оно не может поглощать достаточное количество кислорода из воздуха, часто применяют обработку кислородом. Для лечения пациентов с тяжелой формой эмфиземы можно хирургическим путем удалять часть легкого. В этом случае удаляют поврежденные части легкого, что позволяет здоровым частям легкого расширяться более полно и работать более эффективно вследствие увеличения аэрации. Наконец, другим альтернативным методом хирургического лечения страдающих эмфиземой пациентов является трансплантация легкого, которая может улучшить качество жизни, но не приводит к существенному увеличению предполагаемой продолжительности жизни.
Альвеолы образуются в процессе развития организма путем деления мешочков, которые представляют собой газообменные элементы еще не сформировавшегося легкого. В настоящее время механизмы, управляющие образованием перегородок и их расположением в организме приматов, не изучены в достаточно полной мере. У млекопитающих, таких как крысы, решающую регуляторную роль играют ретиноиды, такие как ATRA, которая представляет собой многофункциональный модулятор клеточного развития, который может изменять как метаболизм внеклеточного матрикса, так и обычную дифференцировку эпителиальных клеток. Например, ATRA модулирует имеющие решающее значение факторы дифференцировки клеток легкого путем связывания со специфическими рецепторами ретиноевой кислоты, которые экспрессируются в соответствии с определенной временной и пространственной схемой. Координированная активация различных подтипов рецепторов ретиноевой кислоты связана с разветвлением легкого, образованием альвеол/образованием перегородок и активацией гена тропоэластина у новорожденных крыс.
В процессе образования альвеолярных перегородок в фибробластной мезенхиме, окружающей стенки альвеол, происходит увеличение гранул, в которых запасается ретиноевая кислота (Liu и др., Am.J.Physiol. 1993, с.265, L430; McGowan и др., Am.J.Physiol., 1995, с.269, L463) и экспрессия рецептора ретиноевой кислоты в легком достигает максимального значения (Ong и др., Proc. Natl. Acad. of Sci., 73, 1976, с.3976; Grummer и др., Pediatr. Pulm., 17, 1994, с.234). Параллельно с истощением этих гранул, в которых запасается ретиноевая кислота, происходит отложение нового эластинового матрикса и образование перегородок. Было установлено, что постнатальное введение ретиноевой кислоты крысам приводит к увеличению количества альвеол, что согласуется с концепцией о том, что ATRA и другие ретиноиды могут индуцировать образование альвеол (Massaro и др., Am.J.Physiol., 270, L305, 1996). Обработка новорожденных детенышей крыс таким глюкокортикостероидом, как дексаметазон, предотвращает образование перегородок и снижает экспрессию некоторых подтипов рецепторов ретиноевой кислоты. Было установлено, что увеличение количества ATRA предотвращает обусловленное дексаметазоном ингибирование образования альвеол. Кроме того, ATRA предотвращает обусловленное дексаметазоном уменьшение экспрессии рецептора ретиноевой кислоты и последующее образование альвеолярных перегородок в развивающемся легком крысы.
На моделях эмфиземы с использованием животных были получены данные о том, что ATRA индуцирует образование новых альвеол и восстанавливает эластическую тягу легкого до приблизительно нормальных значений (Massaro и др., Nature Med., 3, 1997, с.675; "Strategies to Augment Alveolization", National Heart, Lung and Blood Institute, RFA: HL-98-011, 1998; Massaro и др., US 5998486). Хотя в работах Massaro указывается, что ATRA способствует образованию новых альвеол, в этих публикациях не раскрыт механизм действия ATRA. Более важным является то, что применение ATRA вызывает в некоторых случаях токсические или побочные действия.
Таким образом, существует необходимость в разработке новых ретиноидных агонистов, пригодных для лечения дерматологических нарушений, эмфиземы и рака, применение которых не сопровождается связанными с токсичностью проблемами, характерными для ATRA или других ретиноидов.
В настоящем изобретении предложены новые ретиноидные агонисты, их применение в качестве терапевтических действующих веществ для лечения или предупреждения эмфиземы, рака и дерматологических нарушений, фармацевтические композиции, пригодные для лечения или предупреждения эмфиземы, рака и дерматологических нарушений.
Одним из объектов настоящего изобретения являются соединения, имеющие структурную формулу (I):
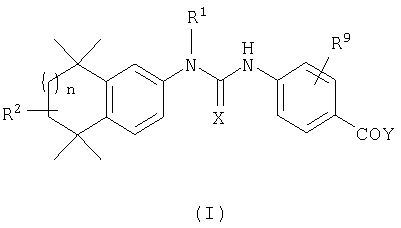
или их соли, сольваты или гидраты, где:
n обозначает целое число от 0 до 2;
Х обозначает S, О или NR3R4;
R3 и R4 независимо друг от друга обозначают водород, алкил, арил, арилалкил, циклоалкил или циклоалкилалкил или вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо;
Y обозначает -OR5, -SR5 или -NR6R7;
R5 обозначает водород, алкил, арил, арилалкил, циклоалкил или циклоалкилалкил;
R6 и R7 независимо друг от друга обозначают водород, алкил, арил, арилалкил, циклоалкил или циклоалкилалкил или вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо;
R1 обозначает С2-С8алкил;
R2 обозначает водород, алкил, гидрокси или оксо;
R9 обозначает водород, алкил, галоалкил, галоген, циано, нитро или алкокси.
Под объем настоящего изобретения подпадает также применение соединений формулы I в качестве фармацевтических действующих веществ, предлагаемых в изобретении, для лечения или предупреждения определенных хронических обструктивных заболеваний дыхательных путей, прежде всего хронического обструктивного заболевания легкого, включая хронический бронхит, эмфизему и астму у млекопитающих, прежде всего у человека, который курит или курил сигареты. Предпочтительным объектом изобретения является лечение или предупреждение панлобулярной эмфиземы, центрилобулярной эмфиземы или дистальной лобулярной эмфиземы у млекопитающих с использованием нетоксичных и терапевтически эффективных доз соединений, предлагаемых в изобретении
Под объем настоящего изобретения подпадает применение соединений, предлагаемых в изобретении, для лечения или предупреждения эмфиземы, рака или дерматологических нарушений. Кроме того, под объем настоящего изобретения подпадает применение фармацевтических композиций, содержащих соединения, предлагаемые в настоящем изобретении, для лечения или предупреждения эмфиземы, рака или дерматологических нарушений. Кроме того, под объем изобретения подпадает применение электрогидродинамических аэрозольных устройств, аэрозольных устройств и распылителей для введения композиций соединений, предлагаемых в изобретении, в легкое млекопитающего, страдающего от эмфиземы, рака или дерматологических нарушений или имеющего риск возникновения таких заболеваний.
Под объем изобретения подпадает также как системное применение, так и местное применение соединений, предлагаемых в изобретении, или сочетание указанных путей введения. Любое из указанных применений или оба можно осуществлять путем перорального введения, введения в слизистую оболочку или парентерального введения. Как указано выше, под объем изобретения подпадают средства введения соединений, предлагаемых в изобретении, непосредственно в легкое, такие как распылитель, ингалятор или другие известные устройства для введения. Под объем изобретения подпадает также способ лечения эмфиземы, рака или дерматологических нарушений, заключающийся в совместном применении соединений, предлагаемых в настоящем изобретении, и одного или нескольких других методов терапевтического лечения.
На фиг.1 проиллюстрировано действие соединения 27, являющегося избирательным агонистом RAR, на восстановление альвеол в опытах на модели эмфиземы с использованием крысиной эластазы.
На фиг.2 представлено сравнение воздействия соединения 27, являющегося избирательным агонистом RAR, и известных соединений 39 и 40, являющихся панагонистами, на уровни триглицеридов, выраженные в процентах по отношению к контролю (только носитель).
На фиг.3 представлено сравнение воздействия носителя и соединения 27, являющегося избирательным агонистом RAR, и известных соединений 39 и 40, являющихся панагонистами, на уровни триглицеридов, выраженные в мг/дл.
В контексте настоящего описания понятие «соединения, предлагаемые в изобретении» обозначает соединения общей формулы (I), включая (но не ограничиваясь ими) конкретные соединения, формулы которых приведены в настоящем описании. В настоящем описании соединения, предлагаемые в настоящем описании, обозначены с помощью их химической структуры и/или химического названия. Соединения, предлагаемые в изобретении, могут содержать один или несколько хиральных центров и/или двойных связей и поэтому они могут существовать в виде стереоизомеров, таких как изомеры с двойной связью (т.е. геометрические изомеры), энантиомеры или диастереомеры. Под объем изобретения подпадают соединения, имеющие приведенные в настоящем описании химические структуры и, следовательно, являющиеся соединениями, предлагаемыми в изобретении, включая все энантиомеры и стереомеры как в форме чистых стереоизомеров (например, чистых геометрических изомеров, чистых энантиомеров или чистых диастереомеров), так и в форме энантиомерных и стереоизомерных смесей. Энантиомерные и стереоизомерные смеси можно разделять с выделением входящих в их состав энантиомеров с помощью либо методов разделения, либо методов хирального синтеза, известных в данной области.
"Ацил" обозначает радикал -C(O)R, где R обозначает водород, алкил, циклоалкил, циклоалкилалкил, арил или арилалкил, где алкил, циклоалкил, циклоалкилалкил, арил и арилалкил имеют указанные в настоящем описании значения. Репрезентативные примеры включают (но не ограничиваясь ими) формил, ацетил, циклогексилкарбонил, циклогексилметилкарбонил, бензоил, бензилкарбонил и т.п.
"Ациламино" обозначает радикал -NR'C(O)R, где R' обозначает водород или алкил и R обозначает водород, алкил, циклоалкил, циклоалкилалкил, арил или арилалкил, где алкил, циклоалкил, циклоалкилалкил, арил и арилалкил имеют указанные в настоящем описании значения. Репрезентативные примеры включают (но не ограничиваясь ими) формиламино, ацетиламино, циклогексилкарбониламино, циклогексилметилкарбониламино, бензоиламино, бензилкарбониламино и т.п.
"Алкил" обозначает линейный насыщенный одновалентный углеводородный радикал, содержащий 1-8 атомов углерода, или разветвленный насыщенный одновалентный углеводородный радикал, содержащий 3-8 атомов углерода, например метил, этил, пропил, 2-пропил, н-бутил, изобутил, трет-бутил, пентил и т.п.
"Алкокси" обозначает радикал -OR, где R обозначает алкильную группу, как она определена в настоящем описании, например, метокси, этокси, пропокси, бутокси и т.п.
"Алкоксикарбонил" обозначает радикал алкокси-С(О)-, где алкокси имеет указанное в настоящем описании значение.
"Алкиламино" обозначает радикал -NHR, где R обозначает алкильную, циклоалкильную или циклоалкилалкильную группу, как они определены в настоящем описании. Репрезентативные примеры включают (но не ограничиваясь ими) метиламино, этиламино, 1-метилэтиламино, циклогексиламино и т.п.
"Алкилен" обозначает линейный насыщенный двухвалентный углеводородный радикал, содержащий 1-10 атомов углерода, или разветвленный насыщенный двухвалентный углеводородный радикал, содержащий 3-10 атомов углерода, например метилен, этилен, 2,2-диметилэтилен, пропилен, 2-метилпропилен, бутилен, пентилен и т.п.
"Алкилсульфонил" обозначает радикал -S(O)2R, где R обозначает алкильную, циклоалкильную или циклоалкилалкильную группу, как она определена в настоящем описании, например метилсульфонил, этилсульфонил, пропилсульфонил, бутилсульфонил и т.п.
"Алкилсульфинил" обозначает радикал -S(O)R, где R обозначает алкильную, циклоалкильную или циклоалкилалкильную группу, как она определена в настоящем описании, например метилсульфинил, этилсульфинил, пропилсульфинил, бутилсульфинил и т.п.
"Алкилтио" обозначает радикал -SR, где R обозначает алкильную, циклоалкильную или циклоалкилалкильную группу, как она определена в настоящем описании, например метилтио, этилтио, пропилтио, бутилтио и т.п.
"Арил" обозначает одновалентный моноциклический или бициклический ароматический углеводородный радикал, необязательно замещенный одним или несколькими заместителями, предпочтительно одним, двумя или тремя заместителями, предпочтительно выбранными из ряда, включающего ацил, алкил, ациламино, алкоксикарбонил, алкиламино, алкилсульфинил, алкилсульфонил, алкилтио, алкокси, амино, арилокси, азид, карбамоил, циано, диалкиламино, этилендиокси, галоген, галоалкил, гетероалкил, гетероциклил, гидрокси, гидроксиалкил, метилендиокси, нитро и тио. Более конкретно понятие арил включает (но не ограничиваясь ими) фенил, хлорфенил, фторфенил, метоксифенил, 1-нафтил, 2-нафтил и их производные.
"Арилалкил" обозначает алкильный радикал, как он определен в настоящем описании, в котором один из атомов водорода алкильной группы замещен арильной группой. Типичные примеры арилалкильных групп включают (но не ограничиваясь ими) бензил, 2-фенилэтан-1-ил, 2-фенилэтен-1-ил, нафтилметил, 2-нафтилэтан-1-ил, 2-нафтилэтен-1-ил, нафтобензил, 2-нафтофенилэтан-1-ил и т.п.
"Арилокси" обозначает группу -O-арил, где арил имеет указанное в настоящем описании значение.
"Арилалкилокси" обозначает группу арилалкил-O-, где арилалкил имеет указанное в настоящем описании значение.
"Карбамоил" обозначает радикал -C(O)N(R)2, где каждая группа R независимо обозначает водород или алкил, как он определен в настоящем описании.
"Карбокси" обозначает радикал -С(O)ОН.
"Циано" обозначает радикал -CN.
"Циклоалкил" обозначает насыщенный одновалентный циклический углеводородный радикал, состоящий из 3-7 кольцевых атомов углерода, например циклопропил, циклобутил, циклогексил, 4-метилциклогексил и т.п.
"Циклоалкилалкил" обозначает радикал -RaRb, где Ra обозначает алкиленовую группу и Rb обозначает циклоалкильную группу, как она определена в настоящем описании, например циклогексилметил и т.п.
"Диалкиламино" обозначает радикал -NRR', где R и R' независимо обозначают алкильную, циклоалкильную или циклоалкилалкильную группу, как она определена в настоящем описании. Репрезентативные примеры включают (но не ограничиваясь ими) диметиламино, метилэтиламино, ди(1-метилэтил)амино, (циклогексил)(метил)амино, (циклогексил)(этил)амино, (циклогексил)(пропил)амино, (циклогексилметил)(метил)амино, (циклогексилметил)(этил)амино и т.п.
"Галоген" обозначает фтор, хлор, бром или йод, предпочтительно фтор и хлор.
"Галоалкил" обозначает алкильную группу, замещенную одним или несколькими одинаковыми или различными атомами галогена, например -СН2Cl, -CF3, -СН2CF3, -СН2CCl3 и т.п.
"Гетероалкил" обозначает алкильный радикал, как он определен в настоящем описании, где один или несколько атомов водорода замещены заместителями, выбранными независимо друг от друга из ряда, включающего -ORa, -NRbRc и -S(O)nRd (где n обозначает целое число от 0 до 2), при этом подразумевается, что присоединение гетероалкильного радикала осуществляется через атом углерода, где Ra обозначает водород, ацил, алкил, циклоалкил или циклоалкилалкил; Rb и Rc каждый независимо друг от друга обозначает водород, ацил, алкил, циклоалкил или циклоалкилалкил; и, если n равно 0, то Rd обозначает водород, алкил, циклоалкил или циклоалкилалкил, а если n равно 1 или 2, то Rd обозначает алкил, циклоалкил, циклоалкилалкил, амино, ациламино, моноалкиламино или диалкиламино. Репрезентативные примеры включают (но не ограничиваясь ими) 2-гидроксиэтил, 3-гидроксипропил, 2-гидрокси-1-гидроксиметилэтил, 2,3-дигидроксипропил, 1-гидроксиметилэтил, 3-гидроксибутил, 2,3-дигидроксибутил, 2-гидрокси-1-метилпропил, 2-аминоэтил, 3-аминопропил, 2-метилсульфонилэтил, аминосульфонилметил, аминосульфонилэтил, аминосульфонилпропил, метиламиносульфонилметил, метиламиносульфонилэтил, метиламиносульфонилпропил и т.п.
"Гетероциклил" обозначает насыщенный или ненасыщенный неароматический циклический радикал, содержащий 3-8 кольцевых атомов, среди которых один или два атома представляют собой гетероатомы, выбранные из N, О или S(O)n (где n обозначает целое число от 0 до 2), а остальные кольцевые атомы представляют собой С. Гетероциклическое кольцо необязательно может быть замещено одним, двумя или тремя заместителями, выбранными независимо друг от друга из ряда, включающего алкил, галоалкил, гетероалкил, ацил, галоген, нитро, карбокси, циано, цианалкил, гидрокси, алкокси, амино, моноалкиламино или диалкиламино. Более конкретно понятие гетероциклил включает (но не ограничиваясь ими) тетрагидропиранил, пиперидино, N-метилпиперидин-3-ил, пиперазино, N-метилпирролидин-3-ил, 3-пирролидино, морфолино, тиоморфолино, тиоморфолино-1-оксид, тиоморфолино-1,1-диоксид, пирролинил, имидазолинил и их производные.
"Гетероциклилалкил" обозначает радикал -RаRb, где Ra обозначает алкиленовую группу, и Rb обозначает гетероциклильную группу, как она определена в настоящем описании, например тетрагидропиран-2-илметил, 2-или 3-пиперидинилметил и т.п.
"Гидроксиалкил" обозначает алкильный радикал, как он определен в настоящем описании, замещенный одной или несколькими гидроксигруппами, при условии, что один атом углерода несет не более одной гидроксигруппы. Репрезентативные примеры включают (но не ограничиваясь ими) 2-гидроксиэтил, 2-гидроксипропил, 3-гидроксипропил, 1-(гидроксиметил)-2-метилпропил, 2-гидроксибутил, 3-гидроксибутил, 4-гидроксибутил, 2,3-дигидроксипропил, 2-гидрокси-1-гидроксиметилэтил, 2,3-дигидроксибутил, 3,4-дигидроксибутил и 2-(гидроксиметил)-3-гидроксипропил, предпочтительно 2-гидроксиэтил, 2,3-дигидроксипропил и 1-(гидроксиметил)-2-гидроксиэтил. Таким образом, в контексте настоящего описания понятие "гидроксиалкил" используется для обозначения определенного поднабора гетероалкильных групп.
Понятие "уходящая группа" имеет значение, которое обычно употребляется в области органического химического синтеза, т.е. обозначает атом или группу, которая может быть замещена нуклеофилом, и оно включает галоген (такой как хлор, бром и йод), алкансульфонилокси, аренсульфонилокси, алкилкарбонилокси (например, ацетокси), арилкарбонилокси, мезилокси, тозилокси, трифторметансульфонилокси, арилокси (например, 2,4-динитрофенокси), метокси, N,O-диметилгидроксиламино и т.п.
"Оксо" обозначает радикал (=O).
"Карбокси" обозначает двухвалентный радикал (>С=0).
Понятие "фармацевтически приемлемый эксципиент" обозначает эксципиент, который можно применять для приготовления фармацевтической композиции и который в целом является безопасным, нетоксичным и не является нежелательным ни с биологической, ни с иной точки зрения, и оно включает эксципиенты, пригодные для применения в фармацевтике.
Понятие "фармацевтически приемлемый эксципиент", как оно используется в контексте настоящего описания и в формуле изобретения, относится как к одному, так и к нескольким таким эксципиентам.
"Фармацевтически приемлемая соль" соединения обозначает соль, которая является фармацевтически приемлемой и обладает требуемой фармакологической активностью исходного соединения. Такие соли включают: (1) кислотно-аддитивные соли, образованные с неорганическими кислотами, такими как соляная кислота, бромистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота и т.п., или образованные с органическими кислотами, такими как уксусная кислота, пропионовая кислота, капроновая кислота, циклопентанпропионовая кислота, гликолевая кислота, пировиноградная кислота, молочная кислота, малоновая кислота, янтарная кислота, яблочная кислота, малеиновая кислота, фумаровая кислота, винная кислота, лимонная кислота, бензойная кислота, 3-(4-гидроксибензоил)бензойная кислота, коричная кислота, миндальная кислота, метансульфоновая кислота, этансульфоновая кислота, 1,2-этандисульфоновая кислота, 2-гидроксиэтансульфоновая кислота, бензолсульфоновая кислота, 4-хлорбензолсульфоновая кислота, 2-нафталинсульфоновая кислота, 4-толуолсульфоновая кислота, камфорсульфоновая кислота, 4-метилбицикло [2.2.2]окт-2-ен-1-карбоновая кислота, глюкогептоновая кислота, 3-фенилпропионовая кислота, триметилуксусная кислота, трет-бутилуксусная кислота, лаурилсерная кислота, глюконовая кислота, глутаминовая кислота, гидроксинафтойная кислота, салициловая кислота, стеариновая кислота, муконовая кислота и т.п.; или (2) соли, которые образуются в том случае, когда присутствующий в исходном соединении кислый протон замещают ионом металла, например ионом щелочного металла, ионом щелочно-земельного металла или ионом алюминия; или объединяют с органическим основанием, таким как этаноламин, диэтаноламин, триэтаноламин, трометамин, N-метилглюкамин и т.п.
В настоящем описании понятия "про-лекарство" и "пролекарство" используются взаимозаменяемо и относятся к любому соединению, которое высвобождает in vivo исходное действующее вещество структурной формулы (I). Пролекарства соединения структурной формулы (I) получают путем модификации одной или нескольких функциональных групп, присутствующих в соединении структурной формулы (I), таким образом, чтобы модифицированная(ые) функциональная(ые) группа(ы) могли расщепляться in vivo с высвобождением исходного соединения. Пролекарства включают соединения структурной формулы (I), где гидрокси-, амино-, или сульфгидрильная группа в соединении структурной формулы (I) связана с любой группой, которая может отщепляться in vivo с восстановлением свободной гидроксильной, амино- или сульфгидрильной группы соответственно. Примеры пролекарств включают (но не ограничиваясь ими) сложные эфиры (например, ацетатные, формиатные и бензоатные производные), карбаматы (например, N,N-диметиламинокарбонил) гидроксильных функциональных групп соединений структурной формулы (I) и т.п.
Понятие "защитная группа" относится к группе атомов, которые после присоединения к реакционноспособной группе в молекуле маскируют, снижают или устраняют ее реакционную способность. Примеры защитных групп описаны у T.W.Green и P.G.Futs, "Protective Groups in Organic Chemistry", (изд-во Wiley, 2-е изд., 1991) и у Harrison и др. "Compendium of Synthetic Organic Methods", т. 1-8 (изд-во John Wiley and Sons, 1971-1996). Репрезентативные аминозащитные группы включают (но не ограничиваясь ими) такие группы, как формил, ацетил, трифторацетил, бензил, бензилоксикарбонил (CBZ), трет-бутоксикарбонил (Boc), триметилсилил (TMS), 2-триметилсилилэтансульфонил (SES), тритил и замещенный тритил, аллилоксикарбонил, 9-флуоренилметилоксикарбонил (FMOC), нитровератрилоксикарбонил (NVOC) и т.п. Репрезентативные гидроксизащитные группы включают (но не ограничиваясь ими) такие группы, в которых гидроксигруппа является либо ацилированной, либо алкилированной, такие как бензил, и простые тритиловые эфиры, а также простые алкиловые эфиры, простые тетрагидропираниловые эфиры, простые триалкилсилиловые эфиры и простые аллиловые эфиры.
В контексте настоящего описания понятие "млекопитающее" обозначает человека. В настоящем описании понятия "человек" и "пациент" используются взаимозаменяемо.
Понятия "лечить" или "лечение" эмфиземы, рака или дерматологического нарушения включают предупреждение болезни (т.е. прекращение развития по меньшей мере одного из клинических симптомов заболевания у млекопитающего, которое может иметь заболевание или быть предрасположенным к нему, однако еще не испытывает симптомов заболевания или они еще не проявляются), ингибирование заболевания (т.е. прекращение или уменьшение развития заболевания или по меньшей мере одного из клинических симптомов) или облегчение заболевания (т.е. достижение регресса заболевания или по меньшей мере одного из клинических симптомов). Понятие «предупреждать» или «предупреждение» включает введение лекарственного средства до проявления заболевания или нарушения.
"Терапевтически эффективное количество" обозначает количество соединения, которое после введения млекопитающему с целью лечения заболевания является достаточным для лечения такого заболевания. "Терапевтически эффективное количество" может варьироваться в зависимости от соединения, заболевания и его серьезности и от возраста, веса и т.д. млекопитающего, подлежащего лечению.
Ниже подробно описаны предпочтительные варианты осуществления изобретения.
Под объем настоящего изобретения подпадают новые соединения и применение указанных новых соединений в качестве фармацевтических действующих веществ для эффективного лечения эмфиземы, рака и дерматологических нарушений. Под объем изобретения подпадает лечение эмфиземы и родственных заболеваний, рака и дерматологических нарушений, которое сопровождается меньшими побочными действиями, характерными для встречающихся в естественных условиях и синтетических ретиноидов при их применении в терапевтически эффективных дозах, или при котором побочные действия отсутствуют. Побочные действия, связанные с применением ретиноидов в терапевтически эффективных дозах, включают (но не ограничиваясь ими) токсические действия, обусловленные избытком витамина А, такие как головная боль, лихорадка, сухость кожи и мембран, боль в костях, тошнота и рвота, психиатрические расстройства и нарушения желудочно-кишечного тракта.
Одним из объектов настоящего изобретения являются соединения структурной формулы (I):
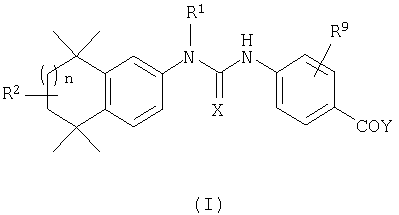
или их фармацевтически приемлемая соль, сольват или гидрат, где:
n обозначает целое число от 0 до 2;
X обозначает S, О или NR3R4;
R3 и R4 независимо друг от друга обозначают водород, алкил, арил, арилалкил, циклоалкил или циклоалкилалкил или вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо;
Y обозначает -OR5, -SR5 или -NR6R7;
R5 обозначает водород, алкил, арил, арилалкил, циклоалкил или циклоалкилалкил;
R6 и R7 независимо друг от друга обозначают водород, алкил, арил, арилалкил, циклоалкил или циклоалкилалкил или, вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо;
R1 обозначает С2-С8алкил;
R2 обозначает водород, алкил, гидрокси или оксо;
R9 обозначает водород, алкил, галоалкил, галоген, циано, нитро или алкокси.
В одном из вариантов осуществления изобретения n равно 1.
В другом варианте осуществления изобретения R1 предпочтительно обозначает С4-С8алкил, предпочтительно С4-С6алкил, наиболее предпочтительно пентил, прежде всего н-пентил.
В другом варианте осуществления изобретения, R2 обозначает водород или гидрокси, предпочтительно водород.
Еще в одном варианте осуществления изобретения, R9 обозначает водород или галоген, предпочтительно водород.
Еще в одном варианте осуществления изобретения, Х обозначает О или S, предпочтительно О.
В другом варианте осуществления изобретения Y обозначает OR5 и R5 обозначает предпочтительно водород или алкил, более предпочтительно водород.
Предпочтительными соединениями, предлагаемыми в изобретении, являются соединения, где n равно 1, R2 обозначает водород и Y обозначает OR5. Предпочтительно, Х обозначает О и Y обозначает ОН.
Предпочтительные соединения, предлагаемые в изобретении, включают соединения, представленные в таблице 1.
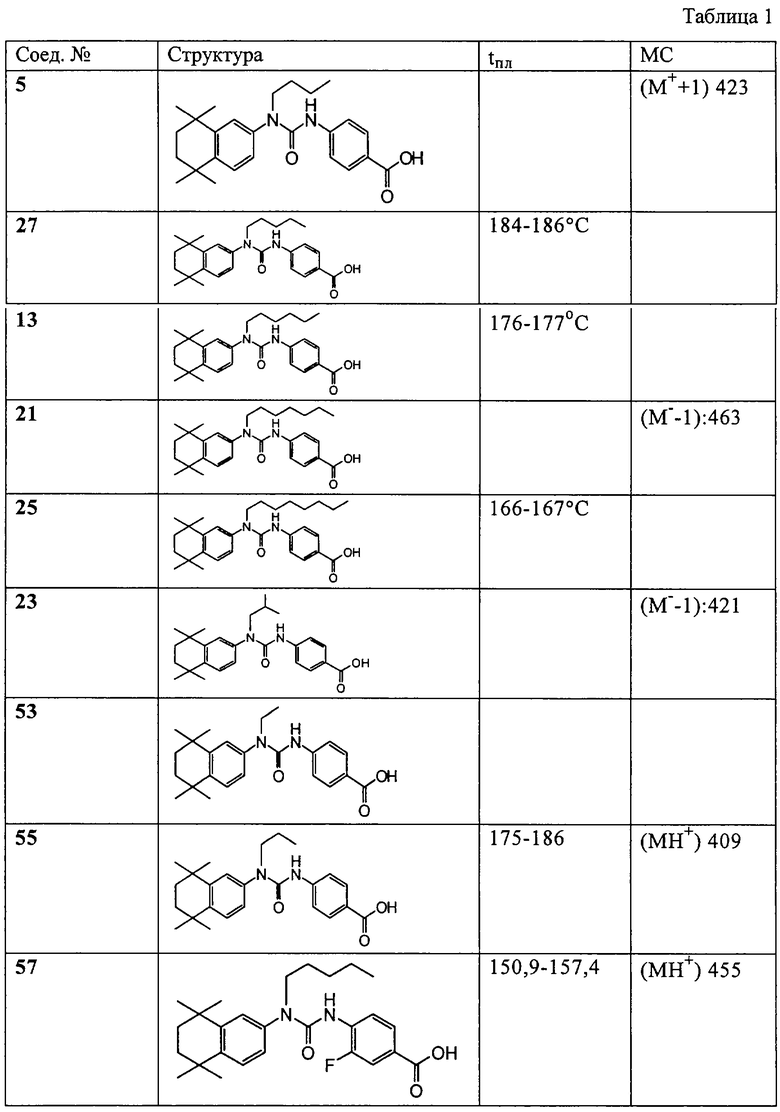
Соединения, предлагаемые в изобретении, можно получать с помощью методов синтеза, проиллюстрированных на схемах 1-3. Исходные продукты, которые можно применять для получения соединений, предлагаемых в изобретении, и их промежуточные продукты поступают в продажу, их можно получать хорошо известными методами синтеза или методами, представленными в настоящем описании. Специалистам в данной области должно быть очевидно, что для синтеза соединений, предлагаемых в изобретении, можно применять методы, отличные от тех, которые проиллюстрированы на схемах 1-3. Таким образом, методы, представленные на схемах в настоящем описании, являются иллюстративными и не ограничивают объем изобретения.
Схема 1
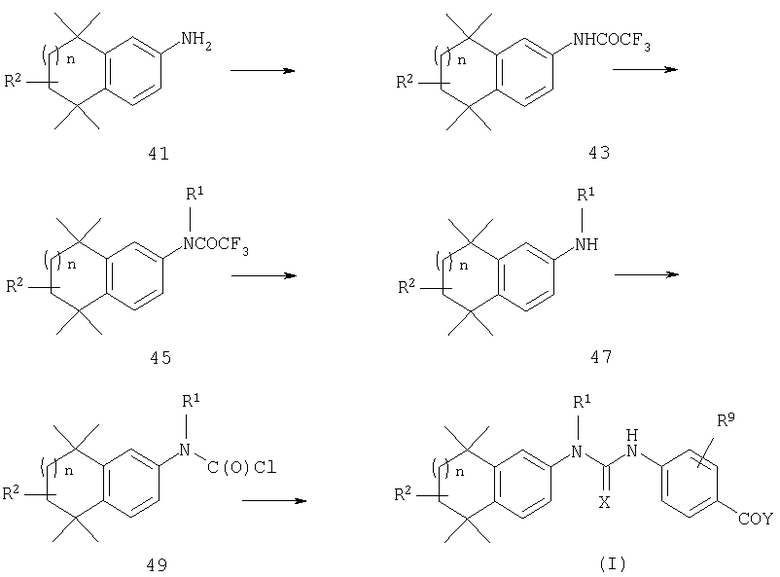
Как проиллюстрировано на схеме 1, ароматический амин 41 подвергают трифторацетилированию (например, с помощью трифторуксусного ангидрида, основания), получая трифторамид 43. Путем алкилирования (например, с помощью основания, алкилгалогенида) вторичного трифторамида 43 получают третичный трифторамид 45, у которого затем удаляют защитную группу (например, обработкой водным гидроксидом), получая моноалкиламин 47. Путем обработки соединения 47 фосгеном или соединением, эквивалентным фосгену, получают хлорформиат 49, который можно превращать в мочевину формулы (I) путем добавления соответствующего ароматического амина.
Схема 2
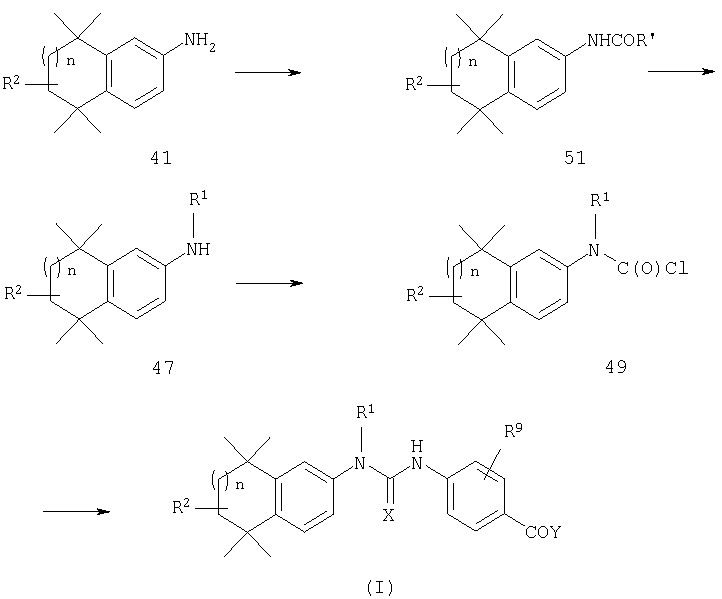
Как проиллюстрировано на схеме 2, ароматический амин 41 можно ацилировать многочисленными методами, известными специалисту в данной области, получая амид 51. Путем восстановления (например, с помощью алюмогидрида лития) получают первичный амин 47, который можно превращать в хлорформиат 49 и мочевину формулы (I), как описано выше.
Схема 3
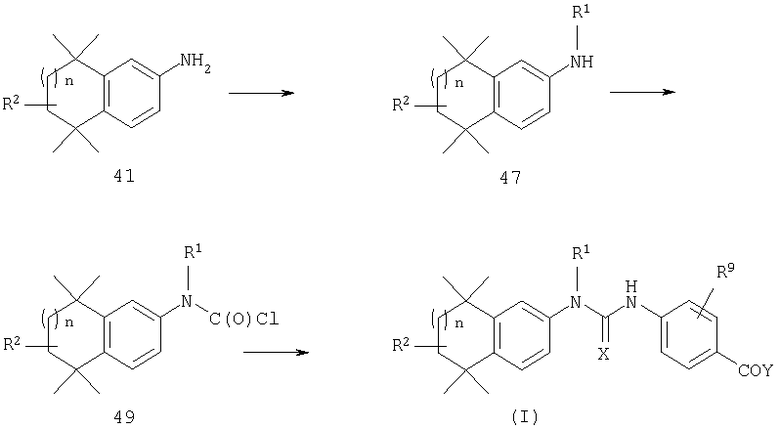
В альтернативном варианте, как проиллюстрировано на схеме 3, ароматический амин 41 можно подвергать металлированию (например, с помощью н-бутиллития) и непосредственному алкилированию, например, алкилгалидом, получая вторичный амин 47, который можно превращать в мочевину формулы (I), как описано выше. Специалисту в данной области известны другие методы получения вторичных аминов из первичных аминов, которые можно применять для получения соединений, предлагаемых в изобретении.
Соединения, предлагаемые в изобретении, которые представлены в настоящем описании, можно применять для стимулирования восстановления поврежденных альвеол и образования перегородок в альвеолах. Так способы, предлагаемые в изобретении, можно применять для лечения легочных заболеваний, таких как эмфизема. Способы лечения с использованием соединений, предлагаемых в изобретении, которые представлены в настоящем описании, можно применять также для лечения рака и дерматологических нарушений.
Избирательное действие соединения, предлагаемого в изобретении, в качестве агониста рецептора ретиноевой кислоты можно определять с помощью известных специалисту в данной области методов анализа связывания лиганда (Apfel и др. Proc. Natl. Acad. Sci. 89, 1992, с.7129; Teng и др. J.Med.Chem., 40, 1997, с.2445; Bryce и др., US 5807900, все документы включены в настоящее описание в качестве ссылки). Обработка агонистами RAR, прежде всего агонистами RAR-γ, может стимулировать восстановление альвеолярного матрикса и образование перегородок, что важно для лечения эмфиземы. Следует отметить, что при лечении эмфиземы могут оказаться эффективными агонисты RAR, которые не обладают избирательным действием в отношении γ-подтипа RAR.
Трансактивацию, которая представляет собой способность ретиноида активировать транскрипцию гена, когда транскрипция гена инициируется в результате связывания лиганда с конкретным типом исследуемого рецептора ретиноевой кислоты, можно оценивать с помощью известных в данной области методов (Apfel и др., Proc. Natl. Acad. Sci., 89, 1992, с.7129; Bernard и др. Biochem. And Biophys. Res. Comm., 186, 1992, с.977, публикации включены в настоящее описание в качестве ссылки).
Применимость соединений, предлагаемых в изобретении, для лечения дерматологических нарушений, вызываемых световым облучением или зависящих от возраста, и стимулирования заживления ран можно оценивать известными в данной области методами (Mustoe и др. Science 237, 1987, с.1333; Sprugel и др., J.Pathol, 129, 1987, с.601, публикации включены в настоящее описание в качестве ссылки). Методы, известные в данной области, можно использовать для оценки применимости соединений, предлагаемых в изобретении, для лечения дерматологических нарушений, таких как угри или псориаз (см. Boyd, Am.J.Med., 86, 1989, с.568 и процитированные ссылки; Doran и др. Methods in Enzymology, 190, 1990, 34, публикации включены в настоящее описание в качестве ссылки). Наконец, известными в данной области методами можно оценивать также эффективность соединений, предлагаемых в изобретении, в отношении лечения рака (Sporn и др. Fed. Proc., 1976, с.1332; Hong и др. "Retinoids and Human Cancer" в The Retinoids: Biology, Chemistry and Medicine, под ред. М.В.Sporn, А.В.Roberts и D.S.Goodman, изд-во Raven Press, Нью-Йорк, 1994, c.597-630, публикации включены в настоящее описание в качестве ссылки).
В случае применения соединений, предлагаемых в изобретении, для лечения или предупреждения эмфиземы или родственных заболеваний, рака или дерматологических нарушений их можно вводить или наносить индивидуально или в сочетании с другими агентами. Соединения, предлагаемые в изобретении, можно также вводить или наносить индивидуально или в сочетании с другими фармацевтически действующими веществами, включающими другие соединения, предлагаемые в изобретении. Соединение, предлагаемое в изобретении, можно вводить или наносить per se или в виде фармацевтических композиций. Конкретная фармацевтическая композиция должна зависеть от требуемого пути введения и она может быть выбрана специалистами в данной области. В данной области известны многочисленные композиции для местного или системного введения ретиноидных агонистов. Соединение, предлагаемое в изобретении, можно включать в состав любой такой композиции.
Фармацевтические композиции, содержащие соединение, предлагаемое в изобретении, можно приготавливать с помощью обычных процессов смешения, растворения, грануляции, изготовления драже, отмучивания, эмульгирования, капсулирования, улавливания или лиофилизации. Фармацевтические композиции можно приготавливать обычным методом с использованием одного или нескольких физиологически приемлемых носителей, разбавителей, эксципиентов или вспомогательных веществ, которые облегчают обработку соединения, предлагаемого в изобретении, при получении композиции, которую можно применять в фармацевтических целях. Соответствующая композиция зависит от выбранного пути введения.
Для местного применения соединение, предлагаемое в изобретении, можно включать в состав композиций в виде растворов, гелей, мазей, кремов, суспензий и т.д., как это хорошо известно в данной области.
Композиции, предназначенные для системного введения, включают композиции для введения путем инъекции, например подкожной, внутривенной, внутримышечной, внутриоболочечной или внутрибрюшинной инъекции, а также композиции, предназначенные для трансдермального введения, введения через слизистую оболочку, перорального или легочного введения. Композиции для системного введения можно приготавливать в сочетании с другим действующим веществом, которое улучшает клиренс слизи из дыхательных путей, осуществляемый с помощью реснитчатого эпителия слизистой оболочки, или уменьшает вязкость слизи. Такие действующие вещества включают (но не ограничиваясь ими) блокаторы натриевых каналов, антибиотики, N-ацетилцистеин, гомоцистеин и фосфолипиды.
Для введения путем инъекции соединение, предлагаемое в изобретении, можно включать в состав композиции в виде водных растворов, предпочтительно, на основе физиологически совместимых буферов, таких как раствор Хэнкса, раствор Рингера или физиологический соляной буфер. Раствор может содержать агенты для приготовления композиции, такие как суспендирующие, стабилизирующие и/или диспергирующие агенты.
В альтернативном варианте соединения, предлагаемые в изобретении, могут находиться в порошкообразной форме, предназначенной для восстановления перед применением с помощью пригодного носителя, например стерильной воды, не содержащей пирогенных веществ.
Для введения через слизистую оболочку в композиции применяют пенетранты, способствующие проникновению через барьер. Такие пенетранты известны в данной области.
Предназначенные для перорального введения композиции можно легко получать путем объединения соединения, предлагаемого в изобретении, с известными в данной области фармацевтически приемлемыми носителями. С использованием таких носителей соединения, предлагаемые в изобретении, можно включать в состав композиций в виде таблеток, пилюль, драже, капсул, жидкостей, гелей, сиропов, эмульсий, суспензий и т.п., предназначенных для приема внутрь пациентом, подлежащим лечению. Пригодные эксципиенты для пероральных твердых композиций, таких, например, как порошки, капсулы и таблетки, включают наполнители, такие как сахара, например, лактозу, сахарозу, маннит и сорбит; вещества на основе целлюлозы, такие как кукурузный крахмал, пшеничный крахмал, рисовый крахмал, картофельный крахмал, желатин, трагакантовую камедь, метилцеллюлозу, гидроксипропилметилцеллюлозу и натрийкарбоксиметилцеллюлозу и/или поливинилпирролидон (ПВП); агенты, способствующие грануляции и связующие агенты. При необходимости можно добавлять разрыхлители, такие как сшитый поливинилпирролидон, агар или альгиновая кислота или ее соль, такая как альгинат натрия. При необходимости на твердые лекарственные формы с помощью стандартных методов можно наносить сахарное покрытие или энтеросолюбильное покрытие. Методы приготовления композиций ретиноидных агонистов для перорального введения известны в данной области (см., например, композицию Accutane®, Physicians' Desk Reference, 54-e изд., 2000, с.2610).
Для пероральных жидких композиций, таких, например, как суспензии, эликсиры и растворы, пригодные носители, эксципиенты или разбавители, включают воду, физиологический раствор, алкиленгликоли (например, пропиленгликоль), полиалкиленгликоли (например, полиэтиленгликоль), масла, спирты, слабые кислотные буферы, имеющие значение рН от 4 до 6 (например, ацетат, цитрат, аскорбат с концентрацией от приблизительно 5,0 до приблизительно 50,0 мМ), и т.д. Кроме того, можно добавлять корригенты, консерванты, красители, желчные соли, ацилкарнитины и т.п.
Композиции для буккального применения могут находиться в форме таблеток, лепешек и т.д., которые приготавливают общепринятым методом.
Соединения, предлагаемые в изобретении, можно вводить непосредственно в легкое путем ингаляции для лечения рака, эмфиземы или дерматологических заболеваний (см. Tong и др., заявка РСТ, WO 97/39745; Clark и др., заявка РСТ, WO 99/47196, которые включены в настоящее описание в качестве ссылки). Введение соединений, предлагаемых в изобретении, путем ингаляции удобно осуществлять с помощью многочисленных различных устройств. Например, для введения соединений, предлагаемых в изобретении, непосредственно в легкое можно применять ингалятор с дозировочной шкалой ("ИДШ"), снабженный баллонами, которые содержат пригодный пропеллент с низкой температурой кипения, например дихлордифторметан, трихлорфторметан, дихлортетрафторэтан, диоксид углерода или другой пригодный газ. Устройства, представляющие собой ИДШ, поступают в продажу от многих поставщиков, таких как 3М Corporation, Aventis, Boehringer Ingleheim, Forest Laboratories, Glaxo-Wellcome, Schering Plough и Vectura.
В альтернативном варианте для введения соединения, предлагаемого в изобретении, можно применять ингалятор для сухого порошка (ИСП) (см., например, Raleigh и др. Proc. Amer. Assoc. Cancer Research Annual Meeting, 40, 1999, с.397, публикация включена в настоящее описание в качестве ссылки). Как правило, в устройствах типа ИСП используется механизм выброса газа для создания внутри контейнера облака сухого порошка, которое затем можно вводить путем ингаляции пациенту. Устройства типа ИСП также хорошо известны в данной области и поступают в продажу от многих поставщиков, например, от таких фирм, как Fisons, Glaxo-Wellcome, Inhale Therapeutic Systems, ML Laboratories, Qdose и Vectura. Широко распространенным вариантом является система ИСП, содержащая несколько доз (МДИСП), которая позволяет вводить более одной терапевтической дозы. Устройства типа МДИСП поступают в продажу от таких компаний, как AstraZeneca, GlaxoWellcome, IVAX, Schering Plough, SkyePharma и Vectura. Например, для использования в ингаляторе или инсуффляторе можно приготавливать желатиновые капсулы или картриджи, содержащие порошкообразную смесь соединения, предлагаемого в изобретении, с пригодной для таких систем порошкообразной основой, такой как лактоза или крахмал.
Другим типом устройства, которое можно применять для введения соединения, предлагаемого в изобретении, в легкое, является устройство для распыления жидкости, поступающее в продажу, например, от фирмы Aradigm Corporation. В системах для распыления жидкости используются распылительные головки с очень малыми отверстиями для того, чтобы жидкую композицию лекарственного средства превратить в аэрозоль, который затем можно вводить путем ингаляции непосредственно в легкое.
В одном из предпочтительных вариантов осуществления изобретения для введения соединения, предлагаемого в изобретении, в легкое используют распылительное устройство. Распылители создают аэрозоли из жидких композиций лекарственного средства с помощью, например, ультразвуковой энергии, что позволяет образовывать мелкие частицы, которые можно легко вводить путем ингаляции (см., например, Verschoyle и др. British J.Cancer, 80, прилож. 2, 1999, с.96, публикация включена в настоящее описание в качестве ссылки). Примерами распылителей могут служить устройства, поступающие в продажу от фирм Sheffield/Systemic Pulmonary Delivery Ltd. (см. Armer и др., US 5954047; van der Linden и др., US 5950619; van der Linden и др., US 5970974, которые включены в настоящее описание в качестве ссылки), Aventis and Batelle Pulmonary Therapeutics.
Еще в одном предпочтительном варианте осуществления изобретения для введения соединения, предлагаемого в изобретении, в легкое используют электрогидродинамическое (ЭГД) аэрозольное устройство. В аэрозольных устройствах ЭГД-типа для превращения жидких растворов или суспензий лекарственного средства в аэрозоль используют электрическую энергию (см., например, Noakes и др. US 4765539; Coffee, US 4962885; Coffee, заявка РСТ, WO 94/12285; Coffee, заявка РСТ, WO 94/14543; Coffee, заявка РСТ, WO 95/26234, Coffee, заявка РСТ, WO 95/26235, Coffee, заявка РСТ, WO 95/32807, содержание которых включено в настоящее описание в качестве ссылки). Электрохимические свойства композиции, содержащей соединение, предлагаемое в изобретении, могут представлять собой важные параметры, которые следует оптимизировать для введения указанного соединения в легкое с помощью аэрозольного устройства ЭГД-типа, и специалист в данной области может выполнить такую оптимизацию стандартным образом. Аэрозольные устройства ЭГД-типа позволяют вводить лекарственные средства в легкое более эффективно, чем существующие методы введения в легкое. Специалисту в данной области известны другие методы внутрилегочного введения соединения, предлагаемого в изобретении, и они подпадают под объем изобретения.
Жидкие композиции лекарственного средства, пригодные для применения с помощью распылителей и устройств для распыления жидкости и аэрозольных устройств ЭГД-типа, как правило, содержат соединение, предлагаемое в изобретении, в сочетании с фармацевтически приемлемым носителем. Предпочтительно, фармацевтически приемлемый носитель представляет собой жидкость, такую как спирт, вода, полиэтиленгликоль или исчерпывающе фторированный углеводород. Для изменения аэрозольных свойств раствора или суспензии соединений, предлагаемых в изобретении, необязательно можно добавлять другие соединения. Предпочтительно, такие соединения представляют собой жидкость, такую как спирт, гликоль, полигликоль или жирная кислота. Специалистам в данной области известны другие методы приготовления жидких растворов или суспензий лекарственного средства, пригодных для применения в аэрозольных устройствах (см., например, Biesalski, US 5112598; Biesalski, US 5556611, содержание которых включено в настоящее описание в качестве ссылки).
Соединение, предлагаемое в изобретении, можно включать в состав композиции для ректального или вагинального введения, таких как суппозитории или удерживающие клизмы, например, содержащие обычные основы для суппозиториев, такие как кокосовое масло или другие глицериды.
В дополнение к композициям, описанным выше, соединение, предлагаемое в изобретении, можно включать в состав композиции в виде депо. Такие обладающие пролонгированным действием композиции можно вводить путем имплантации (например, подкожно или внутримышечно) или путем внутримышечной инъекции. Так, например, соединение, предлагаемое в изобретении, или его слабо растворимое производное, например слабо растворимую соль, можно включать в состав композиции в сочетании с пригодными полимерными или гидрофобными веществами (например, в виде эмульсии в приемлемом масле) или ионообменными смолами.
В альтернативном варианте можно применять другие фармацевтические системы введения. Липосомы и эмульсии являются широко известными примерами носителей для введения действующих веществ, которые можно применять для введения соединения, предлагаемого в изобретении. Можно применять также определенные органические растворители, такие как диметилсульфоксид, хотя, как правило, это сопровождается повышением токсичности. Соединение, предлагаемое в изобретении, можно вводить также с помощью системы с контролируемым высвобождением. Согласно одному из вариантов осуществления изобретения можно использовать насос (Sefton, CRC Crit. Ref. Biomed. Eng., 14, 1987, с.201; Buchwald и др., Surgery, 88, 1980, с.507; Saudek и др., N.Engl. J.Med., 321, 1989, 574). Согласно другому варианту осуществления изобретения можно применять полимерные материалы (см. Medical Applications of Controlled Release, под ред. Langer и Wise, изд-во CRC Pres., Бока Ратон, шт.Флорида (1974); Controlled Drug Bioavailability, Drug Product Design and Performance, под ред. Smolen и Ball, изд-во Wiley, Нью-Йорк (1984); Ranger и Peppas, J.Macromol. Sci. Rev. Macromol. Chem., 23, 1983, с.61; см. также Levy и др., Science, 228, 1985, с.190; During и др., Ann. Neurol, 25, 1989, с.351; Howard и др., J.Neurosurg, 71, 1989, с.105). Согласно еще одному варианту осуществления изобретения систему с контролируемым высвобождением можно помещать вблизи ткани-мишени соединения, предлагаемого в изобретении, например легкого, в этом случае требуется только часть дозы, используемой при системном введении (см., например, Goodson, в Medical Applications of Controlled Release, выше, том 2, 1984, cc.115). Можно применять другие системы с контролируемым высвобождением (см., например, Langer, Science, 249, 1990, с.1527).
Если соединение, предлагаемое в изобретении, является кислотным, то его можно включать в состав любой из описанных выше композиций в форме свободной кислоты, фармацевтически приемлемой соли, пролекарства, сольвата или гидрата. Фармацевтически приемлемые соли обладают практически такой же активностью, что и свободная кислота, и их можно получать путем взаимодействия с основаниями. Фармацевтически приемлемые соли включают любые известные в данной области соли ретиноевой кислоты, пригодные для введения млекопитающим. Как правило, фармацевтические соли обладают большей растворимостью в водных и других протонных растворителях, чем соответствующее соединение в форме свободной кислоты. Таким образом, соединение, предлагаемое в изобретении, можно включать в состав любой из описанных выше композиций в форме сольвата, гидрата или пролекарства. Предпочтительные пролекарства включают гидролизуемые производные сложных эфиров, такие как ароматические сложные эфиры, сложные бензиловые эфиры и сложные (низш.)алкиловые эфиры, такие как сложные этиловые, циклопентиловые эфиры и т.д. Специалистам в области фармацевтики известны другие пролекарства.
Соединение, предлагаемое в изобретении, или композиции, в состав которых оно входит, как правило, следует применять в количестве, эффективном для достижения требуемой цели. Конечно, следует иметь ввиду, что количество должно зависеть от метода введения.
Для лечения или предупреждения эмфиземы, рака или дерматологических нарушений, соединения, предлагаемые в изобретении, или композиции, в состав которых они входят, вводят или наносят в терапевтически эффективном количестве. Подробные данные о терапевтически эффективных количествах соединений, предлагаемых в изобретении, для системного введения представлены в настоящем описании.
Фармакокинетический профиль соединений, предлагаемых в изобретении, является предсказуемым и может быть описан с помощью линейной фармакокинетической теории. Важным является то, что специалист в данной области может легко определить фармакокинетические параметры соединений, предлагаемых в изобретении, в организме человека. Специалист в данной области может определять диапазон стандартных фармакокинетических параметров после перорального введения однократной дозы соединения, предлагаемого в изобретении, с помощью известных в данной области методов (см., например, Khoo и др., J.Clin. Pharm, 22, 1982, с.395; Colburn и др. J.Clin. Pharm, 23, 1983, с.534; Colburn и др. Eur. J.Clin. Pharm., 23, 1983, с.689). Специалист в данной области может также измерять величины этих фармакокинетических параметров после введения нескольких доз согласно известным в данной области методам с целью определения того, происходит ли в конкретных условиях индукция или накопление соединения, предлагаемого в изобретении (Brazzel и др., Eur. J.Clin. Pharm., 24, 1983, с.695; Lucek и др., Clin. Pharmacokinetics, 10, 1985, с.38). С использованием фармакокинетических параметров, определенных с помощью указанных выше методов, в сочетании с данными о величинах доз, полученными на моделях с использованием животных, специалисты в данной области могут оценивать соответствующие уровни доз при системном введении соединений, предлагаемых в изобретении, необходимые для лечения эмфиземы, рака или дерматологических нарушений у млекопитающих (предпочтительно, у человека).
Величины доз и интервалы между их введением можно регулировать индивидуально для обеспечения уровней соединения, предлагаемого в изобретении, в плазме, которые являются достаточными для поддержания терапевтического действия. Обычные дозы для введения пациенту путем инъекции составляют от 0,1 мкг до приблизительно 10,0 мг, предпочтительно от приблизительно 1,0 мкг до приблизительно 1,0 мг, более предпочтительно от приблизительно 10,0 до приблизительно 300,0 мкг, наиболее предпочтительно от приблизительно 50,0 до приблизительно 200 мкг. Терапевтически эффективные уровни в сыворотке можно получать путем введения однократной суточной дозы или нескольких доз каждый день.
Количество соединения, предлагаемого в изобретении, должно, конечно, зависеть среди прочего от других факторов, в частности от пациента, подлежащего лечению, веса пациента, серьезности заболевания, пути введения и от решения лечащего врача. Например, дозу, находящуюся в фармацевтической композиции, можно вводить путем однократного введения, многократного введения или путем контролируемого высвобождения. Введение доз можно периодически повторять и вводить их индивидуально или в сочетании с другими лекарственными средствами и это следует продолжать в течение такого времени, которое необходимо для эффективного лечения эмфиземы.
Предпочтительно, терапевтически эффективная доза соединения, предлагаемого в изобретении, должна обеспечивать терапевтическое действие, не вызывая существенной токсичности. Токсичность соединений, предлагаемых в изобретении, можно определять с помощью стандартных фармацевтических методов и специалист в данной области может легко ее оценить. Соотношение доз, обладающих токсическим и терапевтическим действием представляет собой терапевтический индекс. Соединение, предлагаемое в изобретении, предпочтительно должно иметь существенно более высокий терапевтический индекс по сравнению с другими ретиноидными агонистами при лечении эмфиземы, рака или дерматологических нарушений. Доза соединения, предлагаемого в изобретении, предпочтительно должна обеспечивать такие концентрации в крови, которые представляют собой эффективную, обладающую низкой токсичностью или не обладающую токсичностью дозу.
Доза может варьироваться в этом диапазоне в зависимости от применяемой формы лекарственного средства и используемого пути введения. В каждом конкретном случае лечащий врач, учитывая состояние пациента, может выбрать наиболее подходящую композицию, путь введения и дозу (см., например, Fingl и др. в The Pharmacological Basis of Therapeutics, глава 1, 1975, с.1). Например, терапевтически эффективную дозу соединения, предлагаемого в изобретении, можно вводить как перорально, так и непосредственно в легкое.
Ниже изобретение более подробно проиллюстрировано на примерах, в которых подробно описано получение соединения и композиций, предлагаемых в изобретении. Специалистам в данной области должно быть очевидно, что могут быть сделаны многочисленные модификации, касающиеся как материалов, так и методов, без отклонения от объема изобретения.
Пример 1: Синтез 5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-иламина
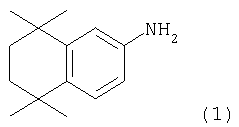
Раствор 5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталина (20,0 г, 106,2 ммоля) в 85 мл уксусного ангидрида при 0°С обрабатывали 12,2 мл уксусной кислоты, а затем 11,1 мл азотной кислоты (70%) и давали нагреться до комнатной температуры. Через 24 ч реакционную смесь сливали на 300 мл ледяной воды и трижды экстрагировали порциями по 150 мл простого эфира. Объединенные органические экстракты промывали четырьмя порциями по 100 мл 15%-ного водного раствора гидроксида натрия, двумя порциями по 200 мл воды и одной порцией 200 мл насыщенного раствора хлорида натрия. Органическую фазу сушили, фильтровали и концентрировали в вакууме, получая 23,93 г (97%) 6-нитро-5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталина (3) в виде твердого вещества светло-желтого цвета.
1,4 г 10%-ного Pd/C добавляли к раствору 6-нитро-5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталина (3) (23,93 г, 102,6 ммоля) в 1 л этанола. Образовавшуюся суспензию выдерживали при давлении Н2, равном 1 атмосфере, в течение 15 ч. Затем реакционную смесь фильтровали через целит (2Х) и концентрировали в вакууме. Остаток растворяли в 200 мл простого эфира и сушили над MgSO4. После фильтрации и концентрирования в вакууме получали твердое вещество светло-коричневого цвета, которое очищали экспресс-хроматографией (SiO2, 5-20%, этилацетат/гексан), получая 17,641 г (85%) 5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-иламина (1) в виде твердого вещества светло-желтого цвета, tпл: 68-69°C.
Пример 2: Синтез 4-[3-бутил-3-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)уреидо]бензойной кислоты (5)
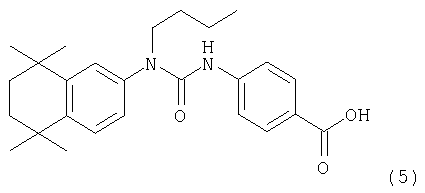
Раствор 5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-иламина (1) (0,3 г, 1,5 ммоля) в 30 мл тетрагидрофурана (ТГФ) охлаждали до -78°С и по каплям добавляли 2,5М раствор н-бутиллития (0,6 мл). Реакционной смеси давали нагреться до 0°С в течение 1 ч. Добавляли йодбутан (0,171 мл) при 0°С и реакционную смесь перемешивали при комнатной температуре в течение 15 ч. Затем реакционную смесь сливали на 50 мл насыщенного водного раствора хлорида натрия и экстрагировали тремя порциями по 50 мл этилацетата. Объединенные органические экстракты сушили над MgSO4, фильтровали и концентрировали в вакууме, получая масло коричневого цвета. Продукт очищали экспресс-хроматографией (SiO2, 5% этилацетат/гексан), получая 143 мг (37%) бутил(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин -2-ил)амина (7) в виде масла светло-желтого цвета.
Раствор бутил(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)амина (7) (143 мг, 0,55 ммоля) в 20 мл ТГФ обрабатывали 57 мг трифосгена (0,35 экв.), перемешивали при температуре дефлегмации в течение 3 ч и затем сливали на 50 мл ледяной воды. Смесь экстрагировали тремя порциями по 50 мл этилацетата. Объединенные органические экстракты сушили над MgSO4, фильтровали и концентрировали в вакууме, получая 368 мг бутил(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)карбамоилхлорида (9), который использовали без очистки.
Раствор бутил(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин -2-ил)карбамоилхлорида (9) (368 мг, 0,55 ммоля) в 30 мл пиридина обрабатывали 272 мг этил-пара-аминобензоата (3 экв.) и перемешивали при 40°С в течение 15 ч. Реакционную смесь концентрировали в вакууме, получая масло оранжевого цвета, которое очищали экспресс-хроматографией (SiO2, 2,5% метанол/дихлорметан), получая 131 мг (54%) этил 4-[3-бутил-3-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)уреидо]бензоат (11) в виде масла светло-желтого цвета.
Раствор этил 4-[3-бутил-3-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)уреидо]бензоата (11) (131 мг, 0,29 ммоля) в 15 мл метанола, 5 мл ТГФ и 5 мл воды обрабатывали 62 мг гидроксида лития (5 экв.) и перемешивали при комнатной температуре в течение 8 ч. Смесь концентрировали в вакууме и остаток подкисляли концентрированным раствором HCl. Затем смесь экстрагировали тремя порциями по 20 мл этилацетата. Объединенные органические экстракты сушили над MgSO4, фильтровали и концентрировали в вакууме, получая твердое вещество желтого цвета, которое очищали экспресс-хроматографией (SiO2, 20% этилацетат/гексан+несколько капель уксусной кислоты), получая 34 мг (28%) 4-[3-бутил-3-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)уреидо]бензойной кислоты (5) в виде твердого вещества светло-желтого цвета. МС (EI): (M++1) 423.
Пример 3: Синтез 4-[3-гексил-3-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)уреидо]бензойной кислоты (13)
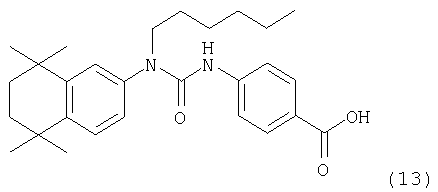
Раствор 5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-иламина (1) (0,5 г, 2,46 ммоля) в 20 мл дихлорметана обрабатывали последовательно 0,51 мл триэтиламина (1,5 экв.) и 0,35 мл гексаноилхлорида (1 экв.). Реакционную смесь перемешивали при комнатной температуре в течение 2 ч, разбавляли дополнительной порцией 20 мл дихлорметана и промывали двумя порциями по 50 мл воды и одной порцией 50 мл насыщенного водного раствора хлорида натрия. Органическую фазу сушили над MgSO4, фильтровали и концентрировали в вакууме, получая 740 мг (100%) (5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)амида капроновой кислоты (15) в виде масла светло-желтого цвета.
Раствор (5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)амида капроновой кислоты (740 мг, 2,46 ммоля) в 20 мл диэтилового эфира (эфира) обрабатывали 400 мг алюмогидрида лития (ЛАГ) и смесь нагревали до температуры дефлегмации в течение 90 мин. После охлаждения до 0°С, добавляли последовательно 0,4 мл воды, 0,4 мл 15%-ного водного раствора гидроксида натрия и 1,2 мл воды и реакционную смесь перемешивали при комнатной температуре в течение 30 мин. Добавляли MgSO4 и смесь фильтровали и концентрировали в вакууме, получая масло светло-желтого цвета. Продукт очищали экспресс-хроматографией (SiO2, 5% этилацетат/гексан), получая 635 мг (81%) гексил(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)амина (17) в виде бесцветного масла.
А раствор гексил(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)амина (17) (635 мг, 2,21 ммоля) в 10 мл толуола обрабатывали 1,0 мл 20%-ного раствора фосгена в толуоле, перемешивали при комнатной температуре в течение 9 ч и затем концентрировали в вакууме. Остаток разбавляли 15 мл пиридина и обрабатывали 730 мг этил-пара-аминобензоата (2 экв.). Реакционную смесь нагревали до 40°С в течение 15 ч и концентрировали в вакууме, получая масло оранжевого цвета. Продукт очищали экспресс-хроматографией (SiO2, 10% этилацетат/гексан, несмоченная насадка), получая 296 мг (28%) этил-4-[3-гексил-3-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)уреидо]бензоата (19) в виде масла желтого цвета.
Раствор этил-4-[3-гексил-l-3-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)уреидо]бензоата (19) (296 мг, 0,62 ммоля) в 8 мл этанола обрабатывали 694 мг гидроксида калия в 3 мл воды. Добавляли ТГФ (2 мл) и смесь нагревали до 45°С в течение 2 ч. Реакционную смесь разбавляли 10 мл воды и значение рН доводили до 2 с помощью концентрированной HCl и затем экстрагировали тремя порциями по 25 мл этилацетата. Объединенные органические экстракты сушили над MgSO4, фильтровали и концентрировали в вакууме, получая твердое вещество светло-желтого цвета. Продукт очищали путем растирания в пентане, в результате чего получали 231 мг (83%) 4-[3-гексил-3-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)уреидо]бензойной кислоты (13) в виде твердого вещества светло-желтого цвета, tпл: 17б,6-177,1°С.
Пример 4: Синтез 4-[3-гептил-3-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)уреидо]бензойной кислоты (21)
Следуя методу, описанному в примере 3, но заменяя гексаноилхлорид гептаноилхлоридом, получали 4-[3-гептил-3-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)уреидо]бензойную кислоту (21). МС (EI): (М+-1):463.
Пример 5: Синтез 4-[3-изобутил-3-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)уреидо]бензойной кислоты (23)
Следуя методу, описанному в примере 3, но заменяя гексаноилхлорид изобутирилхлоридом, получали 4-[3-изобутирил-3-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)уреидо]бензойную кислоту (23). МС (EI): (М+-1):421.
Пример 6: Синтез 4-[3-октил-3-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)уреидо]бензойной кислоты (25)
Следуя методу, описанному в примере 3, но заменяя гексаноилхлорид октаноилхлоридом, получали 4-[3-октаноил-3-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)уреидо]бензойную кислоту (25), tпл: 165,8-167,2°C.
Пример 7: Синтез 4-[3-пентил-3-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)уреидо]бензойной кислоты (27)
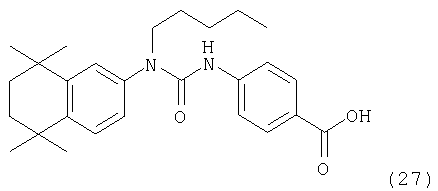
Раствор 5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-иламина (1) (10,0 г, 49,3 ммоля) в 150 мл пиридина охлаждали до 0°С и по каплям добавляли трифторуксусный ангидрид (34,2 мл). Реакционную смесь перемешивали при 0°С в течение 2 ч, разбавляли 300 мл этилацетата и промывали двумя порциями по 250 мл воды. Органическую фазу сушили над MgSO4, фильтровали и концентрировали в вакууме, получая масло желтого цвета. Продукт очищали экспресс-хроматографией (SiO2, 1:6 этилацетат/гексан), получая 15,05 г 2,2,2-трифтор-N-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)ацетамида (29) в виде бесцветного масла.
Раствор 2,2,2-трифтор-N-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)ацетамида (29) (15,05 г, 40,7 ммоля) в 105 мл диметилсульфоксида (ДМСО) обрабатывали гидроксидом калия (3,38 г) и затем охлаждали до 0°С. К реакционной смеси добавляли по каплям йодпентан (7,9 мл) в 15 мл ДМСО и температуре давали подняться до 23°С. Реакционную смесь перемешивали при комнатной температуре в течение 24 ч, разбавляли 200 мл воды и экстрагировали двумя порциями по 200 мл эфира. Объединенные органические экстракты промывали четырьмя порциями по 200 мл холодной воды, сушили над MgSO4, фильтровали и концентрировали в вакууме, получая масло коричневого цвета. Продукт очищали экспресс-хроматографией (SiO2, 1:15 этилацетат/гексан), получая 14,36 г 2,2,2-трифтор-N-пентил-N-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)ацетамида (31) в виде масла светло-желтого цвета.
Раствор 2,2,2-трифтор-N-пентил-N-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)ацетамида (31) (13,6 г, 37,5 ммоля) в 140 мл этанола обрабатывали раствором гидроксида калия (10,52 г) в 25 мл воды. Смесь перемешивали при комнатной температуре в течение 2 ч, разбавляли 100 мл воды и затем экстрагировали двумя порциями по 250 мл этилацетата. Объединенные органические экстракты промывали шестью порциями по 200 мл холодной воды или до тех пор, пока значение рН не становилось нейтральным. Органическую фазу сушили над MgSO4, фильтровали и концентрировали в вакууме, получая масло желтого цвета. Продукт очищали экспресс-хроматографией (SiO2, 10% этилацетат/гексан), получая 9,86 г пентил(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)амина (33) в виде масла золотистого цвета.
Раствор пентил(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)амина (33) (1,0 г, 3,6 ммоля) в 20 мл ТГФ обрабатывали 380 мг трифосгена (0,35 экв.). Реакционную смесь перемешивали при температуре дефлегмации в течение 3 ч, сливали на 30 мл ледяной воды и экстрагировали тремя порциями по 30 мл этилацетата. Объединенные органические экстракты сушили над MgSO4, фильтровали и концентрировали в вакууме, получая 1,26 г пентил(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)карбамоилхлорида (35) в виде твердого вещества белого цвета, которое использовали без очистки.
Раствор пентил(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)карбамоилхлорида (35) (900 мг, 2,6 ммоля) в 20 мл пиридина обрабатывали 481 мг этил-пара-аминобензоата (3 экв.) и перемешивали при 40 С в течение 15 ч. Реакционную смесь разбавляли 100 мл холодной воды и экстрагировали двумя порциями по 100 мл этилацетата. Объединенные органические экстракты сушили над MgSO4, фильтровали и концентрировали в вакууме, получая масло оранжевого цвета, которое очищали экспресс-хроматографией (SiO2, 5% этилацетат/гексан), получая 260 мг этил-4-[3-пентил-3-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)уреидо]бензоата (37) в виде масла светло-желтого цвета.
Раствор этил-4-[3-пентил-3-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)уреидо]бензоата (37) (360 мг, 0,77 ммоля) в 10 мл этанола обрабатывали 430 мг гидроксида калия в 2 мл воды. Добавляли ТГФ (2 мл) и смесь нагревали до 45°С в течение 2 ч. Реакционную смесь разбавляли 10 мл воды, значение рН доводили до 2 с помощью концентрированной HCl и затем экстрагировали тремя порциями по 25 мл этилацетата. Объединенные органические экстракты сушили над MgSO4, фильтровали и концентрировали в вакууме, получая твердое вещество светло-желтого цвета. Продукт очищали путем растирания в пентане, в результате чего получали 280 мг 4-[3-пентил-3-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)уреидо]бензойной кислоты (27) в виде твердого вещества белого цвета, tпл: 184-186°C.
Пример 8: Синтез 3-фтор-4-[3-пентил-3-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)уреидо]бензойной кислоты (57)
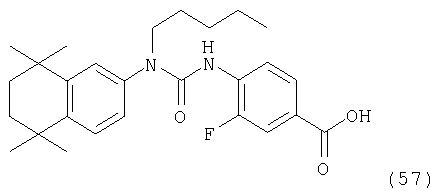
Раствор 3-фтор-4-нитротолуола (2 г, 12,82 ммоля) в 13 мл воды, содержащий 5,72 г Na2Cr2O7, обрабатывали, добавляя по каплям 14,2 мл концентрированной серной кислоты, перемешивали при комнатной температуре в течение 1 ч и затем разбавляли 20 мл воды. Смесь фильтровали и выделенное твердое вещество осторожно нагревали в 50 мл 2%-ного раствора гидроксида натрия. Образовавшийся раствор охлаждали и фильтровали и фильтрат подкисляли концентрированной HCl. Водную фазу экстрагировали двумя порциями по 100 мл этилацетата, объединенные экстракты промывали 100 мл водного насыщенного раствора хлорида натрия, сушили над MgSO4, фильтровали и концентрировали в вакууме, получая 1,6 г (68%) 3-фтор-4-нитробензойной кислоты в виде твердого вещества желтого цвета.
Раствор 3-фтор-4-нитробензойной кислоты (1,6 г, 8,65 ммоля) в 35 мл метанола при 0°С обрабатывали, добавляя по каплям 1,27 мл тионилхлорида, перемешивали при комнатной температуре в течение ночи и летучие компоненты удаляли в вакууме. Продукт очищали экспресс-хроматографией (SiO2, 5% метанол/дихлорметан), получая 1,7 г смеси (3:2), содержащей метил-3-фтор-4-нитробензоат и 3-метокси-4-нитробензойную кислоту (65). Смесь использовали непосредственно на следующей стадии.
К раствору полученной выше смеси, содержащей метил-3-фтор-4-нитробензоат и 3-метокси-4-нитробензойную кислоту (1,7 г) в 50 мл этилацетата, добавляли 150 мг 10%-ного палладия на древесном угле и выдерживали в течение 2 ч в атмосфере H2 (при давлении 45 фунтов/кв. дюйм). Реакционную смесь фильтровали через целит и концентрировали в вакууме. Продукт очищали экспресс-хроматографией (SiO2, 10% метанол/дихлорметан), получая 0,7 г метил-4-амино-3-фторбензоата в виде твердого вещества беловатого цвета.
Раствор пентил(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)амина (51) (390 мг, 1,45 ммоля) в 6 мл толуола обрабатывали 0,9 мл 20%-ного раствора фосгена в толуоле и перемешивали при комнатной температуре в течение 12 ч. Реакционную смесь концентрировали в вакууме, получая пентил(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)карбамоилхлорид в виде твердого вещества светло-желтого цвета. Твердое вещество растворяли в 5 мл пиридина, обрабатывали 0,5 г метил-4-амино-3-фторбензоата и перемешивали при 40°С в течение 3 дней. Летучие компоненты удаляли в вакууме и остаток подвергали экспресс-хроматографии (SiO2, 20% этилацетат/гексан), получая 17 мг метил-3-фтор-4-[3-пентил-3-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)уреидо] бензоата.
Раствор метил-3-фтор-4-[3-пентил-3-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)уреидо]бензоата (17 мг) в смеси 10 мл ТГФ/3 мл метанола/3 мл воды обрабатывали гидратом гидроксида лития (20 мг). Смесь перемешивали при комнатной температуре в течение 2 ч. Смесь разбавляли 5 мл воды и значение рН доводили до 2 с помощью концентрированной HCl. Смесь экстрагировали тремя порциями по 10 мл эфира. Объединенные органические экстракты сушили над MgSO4, фильтровали и концентрировали в вакууме, получая твердое вещество коричневого цвета. Продукт очищали путем растирания в гексане, получая 12 мг 3-фтор-4-[3-пентил-3-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)уреидо]бензойной кислоты (57) в виде твердого вещества желтого цвета, tпл: 151-157°С.
Пример 9: Оценка восстановления альвеол в легком крыс с помощью соединений, предлагаемых в изобретении
Эффективность соединений, предлагаемых в изобретении, в отношении восстановления альвеол можно оценивать на модели индуцируемой эластазой эмфиземы у крыс (Massaro и др. Nature, том 3, № 6, 1997, с.675; Massaro и др. US 5998486). Предпочтительно, животных разделяли на группы обработки приблизительно по восемь особей в каждой. Воспаление легкого и повреждение альвеол у самцов крыс линии Sprague Dawley индуцировали путем однократного введения приблизительно 2 ед./грамм веса тела эластазы поджелудочной железы (свиная эластаза, фирма Calbiochem).
Животных обрабатывали соединением, предлагаемым в изобретении, в сочетании с Miglyol, в удобных для перорального введения дозах (предпочтительно от приблизительно 10,0 до 0,0001 мг/кг), которые вводили перорально один раз в день, начиная с 21-го дня после повреждения. Контрольным группам вводили эластазу и через 21 день их обрабатывали носителем (Miglyol) в течение 14 дней. Животных умерщвляли через 24 ч после введения последней дозы путем обескровливания при глубокой анестезии. Во время обескровливания собирали кровь для анализа.
Легкие заполняли 10%-ным забуференным нейтральным раствором формалина путем его внутритрахеального введения с постоянной скоростью (1 мл/грамм веса тела/мин). Легкое вырезали и погружали в фиксатор за 24 ч до проведения анализа. Стандартными методами получали парафиновые срезы толщиной 5 мкм. Срезы окрашивали гематоксилином и эозином. У каждой крысы с помощью компьютерного морфометрического анализа проводили измерения альвеол в четырех областях легкого крысы. Среднее значение для каждой группы обработки определяли путем суммирования средней площади/крысу для всех групп обработки, включающих по восемь крыс, и восстановление альвеол после вызванного эластазой повреждения выражали в виде процента восстановления по отношению к группе, обработанной эластазой+носитель, который рассчитывали по следующей формуле:

В некоторых случаях вариабельность между особями в группе обработки была слишком велика для того, чтобы среднее значение для группы было статистически достоверным.
На фиг.1 представлены результаты, полученные для соединения 27. У крыс, которым вводили специфический в отношении RARγ агонист 27, восстановление альвеол было статистически достоверным (р≤0,05) при низких уровнях доз (0,01 или 0,001 мг/кг).
Пример 10: Воздействие агонистов RAR на уровни триглицеридов
В этом эксперименте использовали 60 самцов крыс линии Wistar Han (фирма Charles Rivers Laboratories). Исходный вес крыс составлял 200-250 г. На основе соединений, предлагаемых в изобретении, приготавливали композиции в Miglyol 812, Batch 000719, Product №6330 (фирма Condea) с добавлением 0,01% бутилированного гидроксианизола (БГА) и 0,01% бутилированного гидрокситолуола (БГТ). Проводили сравнение воздействий трех приведенных ниже агонистов RAR на уровни триглицеридов. Соединения 39 и 40 известны из существующего уровня техники (см. Hashimoto Yuichi; Kagechika Hiroyuki; Kawachi Emiko; Fukasawa Hiroshi; Saito Go; Shudo Koichi "Evaluation of differentiation-inducing activity of retinoids on human leukemia cell lines HL-60 and NB4", Biol. Pharm. Bull., 19(10), 1996, c.1322-1328; и Takagi Kanji; Suganuma Masami; Kagechika Hiroyuki; Shudo Koichi; Ninomiya Mitsuo; Muto Yasutoshi; Fujiki Hirota, "Inhibition of ornithine decarboxilase induction by retinobenzoic acids in relation to their binding affinities to cellular retinoid-binding proteins" J. Cancer Res. Clin. Oncol., 114(3), 1988, c.221-224), тогда как соединение 27 представляет собой соединение, которое получали согласно методу, приведенному в примере 7 настоящего описания.
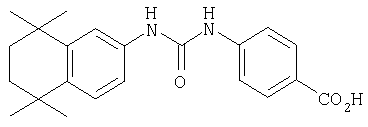
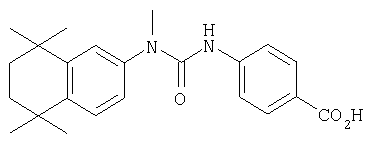
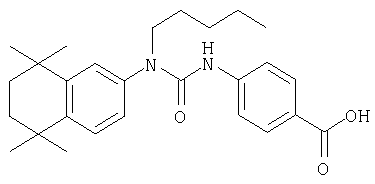
Животным вводили перорально соединения 27, 39 и 40 или носитель в течение 2 недель (один раз в день 1,0 мл композиции, содержащей суточную дозу, всего 10 доз). Дозы составляли 0,3, 1 и 3 мг/кг. Животных взвешивали два раза в неделю с целью мониторинга общей токсичности (% изменения веса и кожные изменения).
Животным не давали пищу в течение по меньшей мере 4 ч перед последним отбором образцов крови. После окончания эксперимента животных подвергали глубокой анестезии с использованием пентобарбитала i.p. (30-40 мг). С помощью сердечной пункции отбирали 5-6 мл крови для химического анализа крови (фирма Quality Clinical Lab, Маунтин Вью, шт. Калифорния) и анализа (конечного) с помощью прямой реакции Прауснитца-Кюстнера (ПК). Животных продвергали эвтаназии путем обескровливания в результате рассечения брюшной аорты или шеи. Плазму собирали и хранили при -20°С.
Количественную оценку уровня триглицеридов в плазме крыс можно проводить с помощью стандартных методов. В целом метод заключается в следующем: содержащиеся в плазме триглицериды можно превращать в дигидроксиацетон и перекись водорода путем последовательной обработки плазмы липазой и глицеролкиназой согласно инструкциям производителя набора триглицериды/GPO (фирма Boehringer Mannheim, № 1488872). Концентрацию перекиси водорода можно определять количественно колориметрическим методом с помощью химического анализатора Hitachi 911. У крыс нормальные уровни триглицеридов составляют от приблизительно 75 до приблизительно 175 мг/дл. Уровни триглицеридов являются удобной мерой токсичности.
Результаты приведены на фиг.2 и 3.
На фиг.2 представлены уровни триглицеридов, выраженные в процентах по отношению к контролю (обработка только носителем) (уровень в контроле принимали за 100%). Обработка соединениями 39 и 40, известными из существующего уровня техники, при всех изученных дозах приводила к повышению уровней триглицеридов по отношению к контролю (обработка только носителем) (>100%), причем при использовании соединения 40 уровни триглицеридов возрастали при увеличении дозы. В отличие от этого обработка соединением 27 несущественно повышала уровни триглицеридов и при использовании более высокой дозы эти уровни были меньше, чем в контроле (обработка только носителем) (<100%).
Пример 11: Аффинность к связыванию с ретиноидными рецепторами и их трансактивация
Аффинность к связыванию с RAR соединений, предлагаемых в изобретении, определяли с помощью метода анализа связывания лигандов, описанного у С.Apfel и др. Proc. Nat. Sci. Acad. (USA), 89, 1992, c.7129-7133. В этом анализе было установлено, что соединения обладали указанной активностью.
Изучение трансактивации каждого конкретного рецептора ретиноевой кислоты (α, β и γ) можно осуществлять с помощью известных в данной области методов (Apfel и др. Proc. Natl. Acad. Sci., 89, 1992, с.7129; Bernard и др., Biochem. and Biophys. Res. Comm., 186, 1992, с.977). Результаты оценки трансактивации при использовании выбранных соединений, предлагаемых в изобретении, сравнивали с данными, полученными при использовании известных из существующего уровня техники соединений 39 и 40. Результаты свидетельствуют о том, что соединения, предлагаемые в изобретении, прежде всего соединения 55 и 27, неожиданно обладают избирательным действием в отношении транскрипции, опосредуемой гамма-рецептором, в то время как соединения, известные из существующего уровня техники, являются пан-агонистами.
Пример 12: Пероральные композиции соединения, предлагаемого в изобретении
В таблице 2 представлены ингредиенты для дозируемой формы соединения, предлагаемого в изобретении, в виде таблетки:
Действующее вещество (т.е. соединение, предлагаемое в изобретении) смешивали с лактозой до образования однородной смеси. Остальные ингредиенты смешивали со смесью, содержащей лактозу, до получения однородного состояния и прессовали, получая отдельные таблетки с насечкой.
Пример 13: Пероральная композиция соединения, предлагаемого в изобретении
Капсулы, содержащие соединение, предлагаемое в изобретении, которые можно применять для лечения эмфиземы, можно приготавливать с использованием ингредиентов, представленных в таблице 3.
Указанные выше ингредиенты смешивали до однородного состояния и помещали в твердую желатиновую капсулу.
Пример 14: Композиция соединения, предлагаемого в изобретении, в виде суспензии
Ингредиенты, перечисленные в таблице 4, смешивали с получением суспензии, предназначенной для перорального введения.
Пример 15: Инъецируемая композиция соединения, предлагаемого в изобретении
Ингредиенты, перечисленные выше в таблице 5, смешивали с получением инъецируемой композиции.
Пример 16: Инъецируемая композиция соединения, предлагаемого в изобретении
Указанные выше ингредиенты смешивали, получая инъецируемую композицию.
Пример 17: Назальная композиция соединения, предлагаемого в изобретении
Указанные выше ингредиенты смешивали, получая суспензию для назального введения.
Пример 18: Композиция 13-цис-ретиноевой кислоты для ингаляции
Соединение, предлагаемое в изобретении, осторожно растворяли в 1,1,2-трихлор-1,2,2-трифторэтана без выпаривания какого-либо растворителя и образовавшийся раствор фильтровали и хранили в герметичном контейнере. Образовавшийся раствор и газообразный пропеллент в указанных в таблице 8 процентных соотношениях можно вносить с помощью методов, известных специалисту в данной области, в аэрозольные баллоны, представляющие собой готовые к применению формы. Для введения точной дозы соединения, предлагаемого в изобретении, можно использовать дозирующий клапан, предназначенный для выпуска 100-300 мкл спрея при одном нажатии.
Пример 19: Композиция соединения, предлагаемого в изобретении, для ингаляции
Cremophor RH 40 можно получать от корпорации BASF. Специалистам в данной области известны другие эмульгаторы или ускорители растворения, которые можно добавлять к водному растворителю вместо Cremophor RH 40. Соединение, предлагаемое в изобретении, эмульгатор, 1,2-пропиленгликоль и воду смешивали, получая раствор. Указанную выше жидкую композицию можно применять, например, в виде аэрозоля, в котором в качестве пропеллента используют соответствующий сжатый газ (например, азот или диоксид углерода).
Пример 20: Композиция соединения, предлагаемого в изобретении. предназначенная для применения с помощью ЭГД
Соединение, предлагаемое в изобретении, эмульгатор, полиэтиленгликоль и воду смешивали, получая раствор. Указанную выше композицию можно использовать в стандартных устройствах ЭГД-типа, известных в данной области.
Описанные выше варианты осуществления изобретения приведены только в качестве примеров, и специалистам в данной области должны быть очевидны многочисленные эквиваленты представленных в настоящем описании методов или они могут разработать их с помощью стандартных экспериментов. Подразумевается, что все такие эквиваленты подпадают под объем изобретения и охватываются приведенной формулой изобретения.
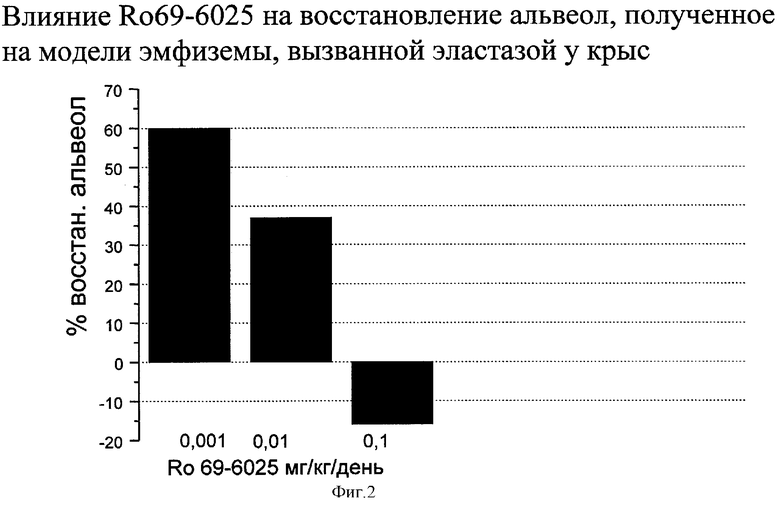
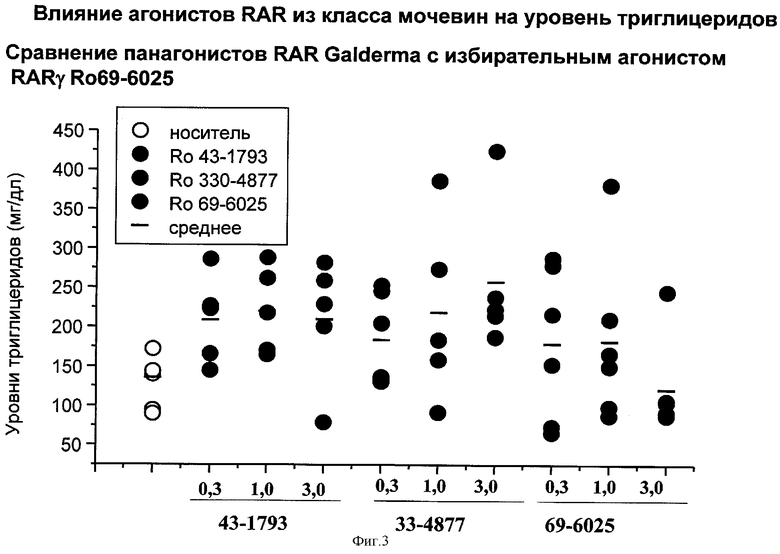
Изобретение относится к новым производным алкилмочевины формулы (I) или к их фармацевтически приемлемой соли, сольвату или гидрату, обладающим свойствами ретиноидных агонистов (RAR), фармацевтическим композициям и лекарственному средству. В соединении формулы (I)
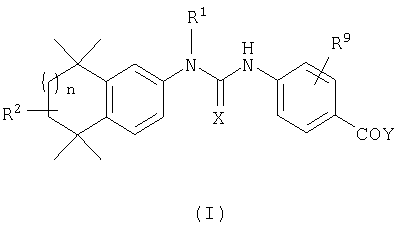
n обозначает целое число от 0 до 2; Х обозначает O; Y обозначает -OR5; R5 обозначает водород; R1 обозначает С2-С8алкил; R2 обозначает водород, алкил, гидрокси или оксо; R9 обозначает водород. 3 н. и 8 з.п. ф-лы, 3 ил., 10 табл.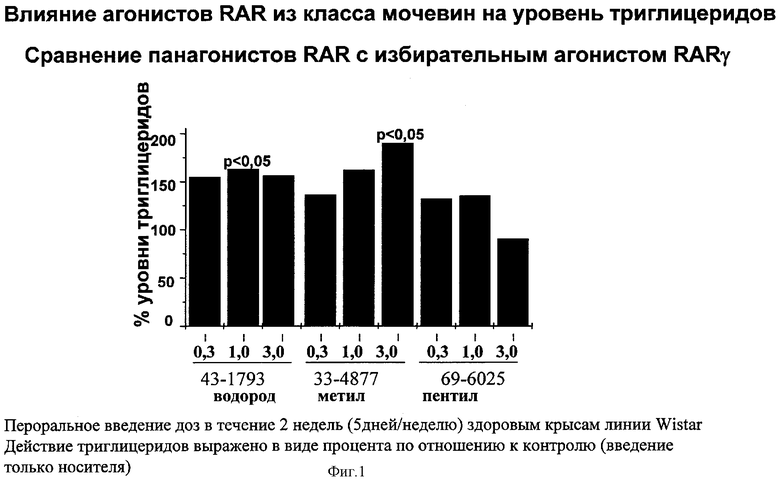
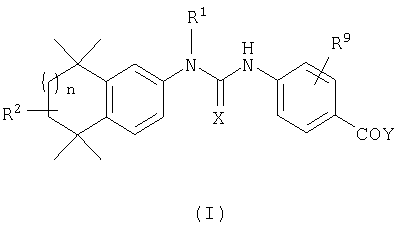
или его фармацевтически приемлемая соль, сольват или гидрат, где
n обозначает целое число от 0 до 2;
Х обозначает О;
Y обозначает -OR5;
R5 обозначает водород;
R1 обозначает С2-С8алкил;
R2 обозначает водород, алкил, гидрокси или оксо; и
R9 обозначает водород.
| СОЕДИНЕНИЯ, ОБЛАДАЮЩИЕ ИЗБИРАТЕЛЬНОСТЬЮ В ОТНОШЕНИИ РЕЦЕПТОРОВ РЕТИНОИДА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ (ВАРИАНТЫ), СПОСОБ МОДУЛИРОВАНИЯ ПРОЦЕССОВ (ВАРИАНТЫ), СПОСОБ ПОДАВЛЕНИЯ ПАТОЛОГИЧЕСКИХ СОСТОЯНИЙ | 1993 |
|
RU2144913C1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Автоматический огнетушитель | 0 |
|
SU92A1 |
| Chem | |||
| abstr | |||
| Плуг с фрезерным барабаном для рыхления пласта | 1922 |
|
SU125A1 |
| Chem | |||
| abstr | |||
| Шкив для канатной передачи | 1920 |
|
SU109A1 |
Авторы
Даты
2007-05-27—Публикация
2002-09-11—Подача