Изобретение относится к медицине, а именно к способу получения альбумина.
Препараты сывороточного альбумина, применяемые в настоящее время, занимают первое место по частоте и объему трансфузий среди препаратов крови, в связи с чем качественным показателям альбумина уделяется первоочередное внимание.
Основным показателем качества альбумина является сохранение нативности молекул альбумина в процессе получения и хранения препарата. Поэтому препарат с высоким содержанием мономерного альбумина имеет более высокую лечебную эффективность, осмотическую активность, длительный период циркуляции в организме и отличается отсутствием аллергических реакций (1).
В литературе известны способы получения мономерного альбумина. Однако они не нашли применения в крупномасштабном производстве либо из-за использования химических реагентов, не разрешенных Фармакопеей, таких как йодацетамид (2), либо из-за применения дорогостоящих реагентов - полиэтиленгликоля, ЭДТА, глютатиона, цистеина или малеиновой кислоты (3, 4, 5, 6), либо из-за больших капитальных и текущих затрат, которые требуются при использовании хроматографического оборудования и сорбентов (7).
Самый распространенный этанольный метод Кона достаточно трудоемкий, дорогостоящий, требует специального оборудования на всех этапах получения, отличается многостадийностью процесса, относительно малым выходом конечного продукта и не позволяет получать альбумин с высоким содержанием мономеров (8).
Наиболее близким к заявляемому способу является метод получения альбумина с использованием каприлата натрия (9). Способ предусматривает разделение смеси белков этиловым спиртом в концентрации (25% по объему) в присутствии каприлата натрия (0,3% по объему), отделение осадка денатурированных белков центрифугированием, осветляюшую фильтрацию центрифугата, осаждение очищенного альбумина, растворение осадки с последующим отделением спирта известными приемами и стабилизацией целевого продукта. На этом способе основан промышленный регламент производства альбумина (10).
Преимущества этого каприлатного метода в сравнении с другими каприлатными методами (4, 5, 11) в том, что процесс денатурации примесных белков ведется при температуре от 0 до 30oC, что существенно снижает энергозатраты. Кроме того, только данный способ получения альбумина отвечает требованиям ВОЗ, согласно которым время выдерживания альбумина при температуре 60oC не должно превышать 11 ч (12), в отличие от других модификаций каприлатного способа (4, 5, 11).
Однако, используя прототип, не удается получить мономерный альбумин из-за смены его фазового состояния в процессе получения: перевод в осадок при высоких концентрациях денатурирующего агента (40% этанол) и лиофильное высушивание способствуют образованию агрегатов. Пастеризацию конечного продукта проводят во флаконах, без дальнейшего удаления денатурированных белков и липопротеинов из лекарственной формы препарата. Это приводит к полимеризации альбумина и отрицательно сказывается на стабильности препарата при хранении. Кроме того, отсутствует контроль температуры непосредственно в растворе альбумина во время пастеризации и отсчет времени ведется по достижении температуры 60oC водой, окружающей флаконы с препаратом. Недостаточное время прогрева может представлять вирусологическую опасность в отношении вирусов гепатита и СПИДа, а передерживание препарата при этой температуре ведет к полимеризации альбумина.
Задачей, на решение которой направлено заявляемое изобретение, является разработка способа, условия проведения которого позволяют сохранить мономерность и апирогенность альбумина в процессе производства и хранения.
Достигаемый технический результат заключается в получении мономерного апирогенного альбумина, стабильного при хранении и значительном сокращении времени проведения технологического процесса. Кроме того, заявляемый способ позволяет повысить выход конечного продукта.
Сущность метода заключается в следующем. Альбумин получают из альбуминсодержащих растворов денатурацией примесных белков этанолом в присутствии каприлат-иона, удаляют денатурированные белки, осветляют центрифугат микрофильтрацией, разводят фильтрат до содержания этанола 1-10%, концентрируют альбумин ультрафильтрацией с последующей диафильтрацией. После этого выполняют стерилизующую фильтрацию, проводят пастеризацию "бач"-методом (в объеме), после чего проводят дополнительную стерилизующую фильтрацию для удаления денатурированных белков и липопротеинов фильтрацией. В заключение осуществляют розлив целевого продукта.
В отличие от прототипа, в заявляемом способе альбумин извлекают непосредственно из осветленного центрифугата ультрафильтрацией, исключая стадию перевода альбумина в осадок, одновременно во время последующей диафильтрации удаляется этанол, что исключает необходимость лиофилизации. Вместо пастеризации во флаконах используется пастеризация в "объеме" с последующим удалением денатурированных белков и липопротеинов дополнительной стерилизующей фильтрацией.
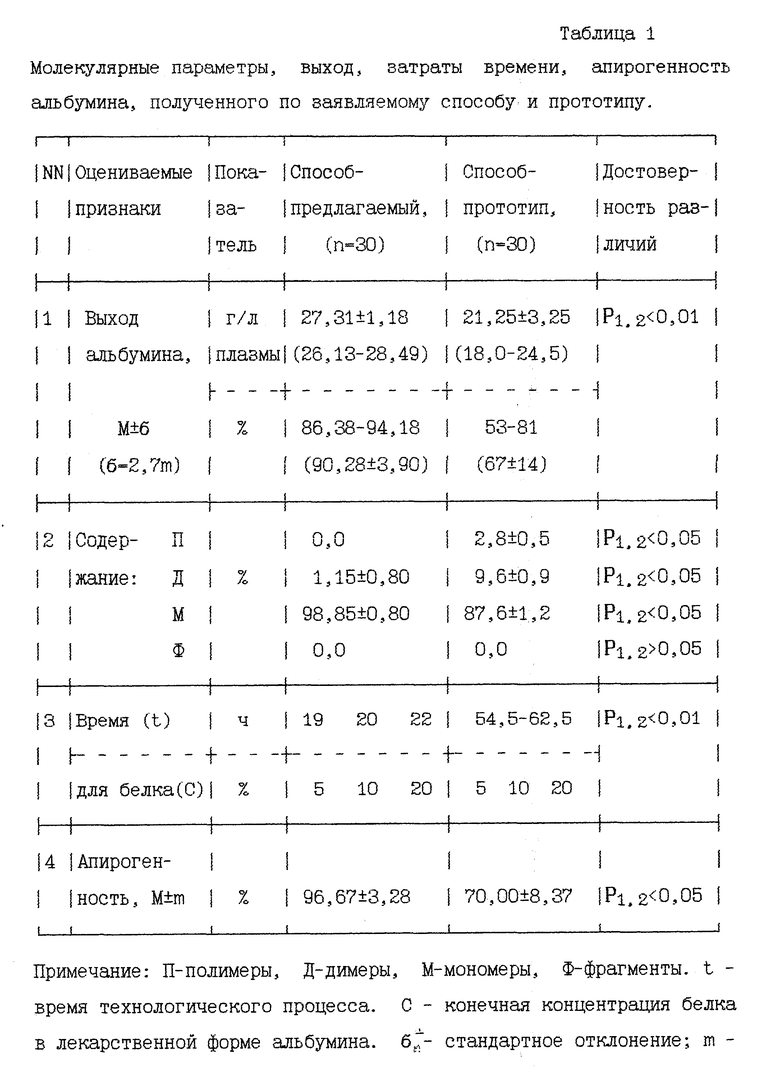
Совокупность признаков заявленного изобретения позволили получить следующие преимущества. Получение альбумина из центрифугата ультрафильтрацией, минуя стадию осаждения, позволяет избежать дегидратации молекулы альбумина и, как следствие, его агрегации и полимеризации. Диафильтрация против 5-7 объемов позволяет достичь такого содержания этанола, при котором не происходит полимеризации во время получения и хранения альбумина. Замена стадии осаждения на ультрафильтрацию позволяет также увеличить выход целевого продукта на 23% (табл. 1) в связи с тем, что альбумин является хорошо растворимым белком плазмы и его невозможно полностью перевести в осадок известными способами.
Пастеризация стерильного раствора альбумина в объеме позволяет точно осуществлять контроль и регулировать процесс подъема и охлаждения температуры альбумина в процессе пастеризации именно внутри самого раствора препарата. Процесс подъема, выдерживания, охлаждения температуры объективно регистрируется на диаграмме с отметкой времени. Так как процесс ведется при постоянном перемешивании, то достигается равномерность температуры в любой точке раствора, это гарантирует отсутствие высокого градиента температуры. Последующая осветляющая и стерилизующая фильтрация охлажденного продукта позволяет удалить из препарата невидимые невооруженным глазом денатурированные белки, липопротеины, которые остаются в препаратах, пастеризованных во флаконах. Эти нестабильные соединения могут выступать в качестве катализаторов процесса полимеризации во время хранения препарата.
Определение молекулярных параметров альбумина - содержания полимеров, димеров, мономеров, фрагментов осуществлялось согласно требованиям Европейской Фармакопеи методом гель-фильтрации на ультрагеле АсА34 (Фармация-ЛКБ, Швеция).
Пирогенность альбумина оценивалась согласно Государственной Фармакопее СССР, 11 издание, вып. 2 (13). Препараты 10% альбумина вводились кроликам в дозе 3 мл/кг массы тела внутривенно. Препарат считали апирогенным, если сумма повышения температур у трех кроликов меньше или равна 1,4oC(Σ ≤ +1,4)oC.
Представленные в табл. 1 данные указывают на высокое содержание мономеров (не менее 98%) и отсутствие полимеров, фрагментов в препаратах альбумина, полученных по заявляемому способу. Сравнение с прототипом (табл. 1) наглядно показывает значительное сокращение времени технологического процесса, увеличение выхода альбумина с одного литра плазмы и практически 100% получение апирогенного продукта.
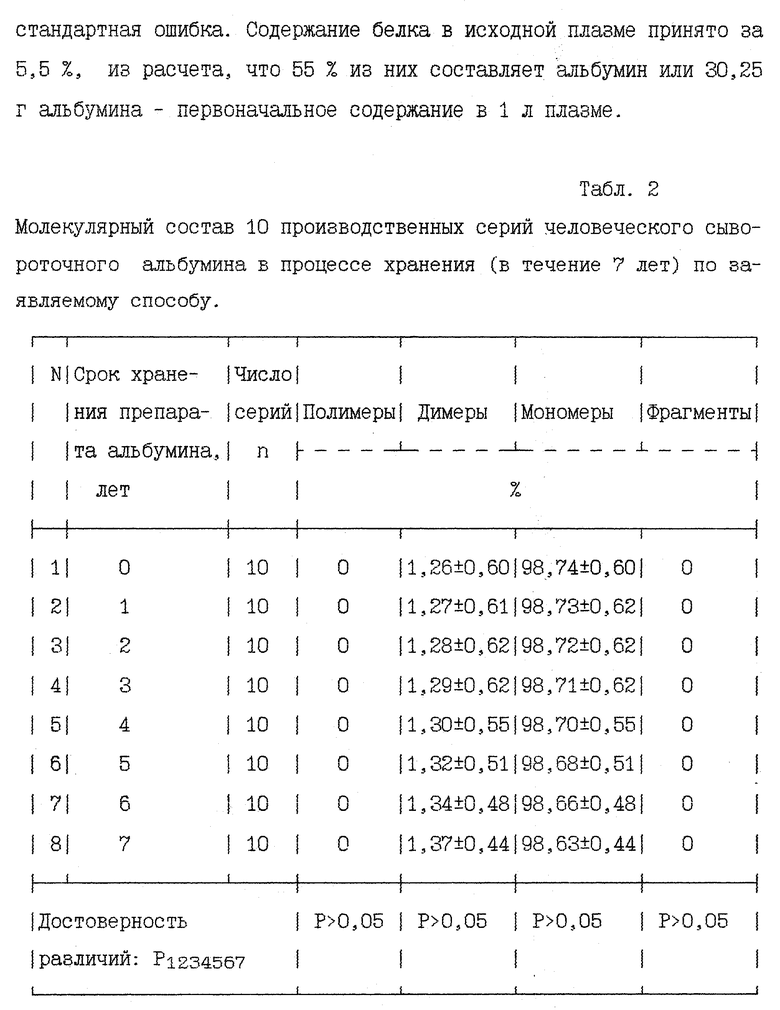
Важным для препарата альбумина является не только нативность свежеприготовленного альбумина, но и сохранение мономерности во время хранения. Представленные данные в табл. 2 указывают на отсутствие достоверных различий в молекулярных параметрах альбумина в течение всего срока наблюдения - 7 лет (при сроке годности препарата 5 лет), следовательно, полученный альбумин стабилен. Способ осуществляют следующим образом. Плазму, центрифугат фракции II + III по Кону или альбуминсодержащий раствор с содержанием белка 1-5,5% обрабатывают этанолом в концентрации 18-35% в присутствии каприлат-иона в концентрации 0,1-0,6% при 0-30oC, pH 2,0-5,0 и удаляют денатурированные белки центрифугированием. Полученный раствор осветляют фильтрацией, затем 0,1-1,0 М раствором NaOH повышают pH до 6,0-7,5 и разбавляют фильтрат дистиллированной водой или физиологически приемлемым буфером (например, 0,15 М раствором натрий хлорида) до концентрации этанола не выше 10%. Далее проводят ультрафильтрацию в тангенциальном потоке на мембранах или полых волокнах с пределом задержания 10000-30000 Да с последующей диафильтрацией для удаления этанола, солей и низкомолекулярных фрагментов с использованием 5-7 объемов 0-0,15 М раствора натрий хлорида или другого физиологически приемлемого буфера. Затем проводят окончательное концентрирование до содержания белка на 2-3% больше, чем концентрация белка в товарной продукции (от 5 до 25%). Проводят стерилизующую фильтрацию через мембраны 0,1-0,2 мк и перекачивают в стерилизованную емкость с мешалкой и рубашкой из нержавеющей стали или с эмалевым покрытием. Осуществляют пастеризацию раствора при 60oC в течение 10 ч (повышение температуры осуществляют в течение 1 ч). После пастеризации альбумин охлаждают до температуры 10-20oC в течение 1 ч, а затем проводят дополнительную стерилизующую фильтрацию и розлив по флаконам.
Пример N 1. Берут 200 л донорской плазмы. Путем фракционирования плазмы по Кону получают фракцию II+III, в количестве 380 л, содержащую 25% этанола, 2% белка, и pH 7,0. К полученному раствору добавляют каприловую кислоту до ее конечной концентрации 0,3%. Температуру раствора устанавливают 16oC подачей теплой воды в рубашку реактора, pH смеси снижают 1 М раствором соляной кислоты в количестве 10,3 л до pH смеси 3,3, перемешивают в течение 15 минут при 16oC. Затем pH смеси смещают до 4,4 1 М раствором NaOH, после чего центрифугируют для удаления образовавшегося осадка. Центрифугат осветляют фильтрацией через фильтрокартон Ф-1 (Тамбов). Получают фильтрат в объеме 424 л, содержащий 1,3% белка. В растворе подводят pH 1 М NaOH до pH 6,5 и добавляют 550 л дистиллированной воды до концентрации этанола в растворе 10%. Концентрируют раствор ультрафильтрацией до 9% белка на ультрафильтрационной установке с полыми волокнами ВПУ-15 с последующей диафильтрацией в постоянном объеме против 5 объемов 0,45% раствора натрий хлорида. Проводят окончательное концентрирование до содержания белка 10,5%. Проводят стерилизующую фильтрацию и заливают 52 л полуфабриката альбумина в стерильный сосуд, вместимостью 60 л из нержавеющей стали (с мешалкой и рубашкой). Осуществляют пастеризацию при 60oC в течение 10 ч (повышение температуры осуществляют в течение 1 ч). После пастеризации раствор в течение 1 часа охлаждают до температуры 20oC путем подачи холодной водопроводной воды в рубашку реактора. Проводят осветляющую, а затем стерилизующую фильтрацию. Целевой продукт разливают по флаконам. Выход альбумина - 90,25% Пирогенность препарата составляет: +0,2; +0,3; +0,3oC, в сумме +0,8oC. Молекулярные параметры (%): полимеры 0, димеры - 0,9, мономеры - 99,1, фрагменты - отсутствуют. Длительность технологического цикла - 20 ч.
Пример N 2. Исходное сырье - центрифугат II+III (из плацентарной сыворотки), в количестве 380 л, содержащий 25% этанола, 2,3% белка, pH раствора 7,0. К полученному раствору добавляют каприлат натрия до конечной концентрации 0,35%. Операции по получению фильтрата проводят по примеру 1. Далее в фильтрате (объем 424 л) подводят pH 7,2 и разбавляют 0,02 М раствором натрий хлорида температуры 16oC в соотношении 1:1,5. Первоначально концентрируют ультрафильтрацией до 7% белка на ультрафильтрационной установке фирмы Миллипор (Pellicon Cassette, мембраны PTGC, 10000 Да, 10 м2) с последующей диафильтрацией в постоянном объеме против 6 объемов апирогенной дистиллированной воды. Проводят окончательное концентрирование до 20,5% по белку. Стерильно фильтруют через мембрану 0,2 мк (фирмы Миллипор). Передавливают 26 л полуфабриката в стерильный эмалированный сосуд, вместимостью 60 л (с мешалкой и рубашкой). После пастеризации охлаждают до температуры 20oC в течение 45 минут. Стерильно фильтруют и разливают по флаконам Выход: 88,10%. Тест на пирогенность: повышение температуры на +0,1; +0,2; +0,2oC (Σ = +0,5oC). Молекулярные параметры (%): полимеры 0, димеры 0,4, мономеры 99,6, фрагменты 0. Время, необходимое для получения 20% альбумина - 22 ч.
Пример N 3. Исходное сырье плазма или сыворотка крупного рогатого скота. В 200 л сыворотки вводят каприловую кислоту до концентрации 0,5%, 96% этанол с температурой "10oC" до конечной концентрации 25 об.%. Операции по получению центрифугата осуществляют согласно примеру 1. Далее центрифугат осветляют микрофильтрацией в тангенциальном потоке на микрофильтрационной установке (0,2 мк) фирмы Sartorius (ФРГ). В фильтрате подводят pH 1 М раствором гидроокиси натрия до pH 6,8 и разбавляют 0,02 М раствором натрий хлорида температуры 16oC в соотношении 1:1,5. Проводят концентрирование альбумина ультрафильтрацией до 6% белка на ультрафильтрационной установке фирмы Sartorius с площадью 8 м2 с последующей диафильтрацией в постоянном объеме против 7 объемов физиологического раствора. Проводят окончательное концентрирование до 5,3% по белку. Стерильно фильтруют через мембрану 0,2 мк (фирмы Гельман, США). Передавливают 104 л полуфабриката в стерильный эмалированный сосуд, вместимостью 150 л (с мешалкой и рубашкой). Осуществляют пастеризацию при 60oC в течение 10 ч (повышение температуры осуществляют в течение 1 ч). После пастеризации охлаждают до температуры 15oC в течение 45 минут. Стерильно фильтруют и разливают по флаконам. Выход: 87,66%. Тест на пирогенность: повышение температуры на +0,1; +0,1; +0,2oC (Σ = +0,4oC). Молекулярные параметры, %: полимеры 0, димеры 0,5, мономеры 99,5, фрагменты 0. Время, необходимое для получения 5% альбумина - 20 ч.
Предложенная технология производства мономерного альбумина позволяет получать мономерный апирогенный вирусобезопасный альбумин, стабильный при хранении.
Источники информации
1) Auerswald W., Binder В., Dolechel W, Vergleich industriell Hergestellter Humanalbumine hinsichtlich des gehaltes an albuminaggregation. -Annales Immunologlae Hungaricae. / Ed. by Institute for serobacteriological production and research "Human", -1972, v. 16,37.
2) Me Meramy R.H. and Lee Y, Microheterogeneity in albumin: a contaminarit. Arch. Bioohem. Biophys. 1967, 122, 635-643.
3) Способ получения мономерного альбумина плазмы крови. Авт. св. СССР N 1250301. A 61 K 35/14, 1986.
4) SchneiderW. , H.Lefevre, H.Fiedler and L.J. McCarty. An alternative method of large scale plasma fractionation for the isolation of serum albumin. Blut, 1975, band 30, seite 121-134.
5) Способ получения альбумина. Патент СССР N 743564. A 61 K 37/02, 1980.
6) Способ выделения альбумина. Патент СССР 1127525. A 61 K 37/02, 1977.
7) Curling J.M., L.O.Lindquist, S.Eriksson. Chromatographic processing- of human plasma - a pilot plant study. Process Biochemistry, 1977, april, 22-28.
8) Kistler P. Develop. Biol. Standard., 1974, 27, 198-202.
9) Иванов М.И., А.А.Фром, А.А.Никитенко, В.М. Русанов, А.Е.Киселев, Л.И. Скобелев. Способ получения сывороточного альбумина. Авт. св. СССР N 467536. A 61 K 23/02, 1976.
10) Промышленный регламент производства альбумина из гемолизированной плазмы и сыворотки крови человеку. МЗ СССР, Москва, 1991.
11) Способ получения альбумина. Патент СССР N 591126. A 61 K 37/02, 1978.
12) СТД ВОЗ N 840. Комитет экспертов ВОЗ по стандартизации биологических препаратов. 43 доклад ВОЗ, Женева 1994, стр. 109. Приложение 2. Требования к сбору, обработке и контролю качества крови, компонентов крови и препаратов плазмы (Требования к биологическим препаратам N 27, пересмотр 1992 г).
13) Государственная фармакопея СССР. 11 издание, вып. 2, стр. 184.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ АЛЬБУМИНА | 1998 |
|
RU2140287C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПЛЕКСА ИММУНОГЛОБУЛИНОВ IgG, IgM И IgA ДЛЯ ВНУТРИВЕННОГО ВВЕДЕНИЯ | 2012 |
|
RU2492176C1 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРА АЛЬБУМИНА | 2001 |
|
RU2205020C2 |
| ОБЕДНЕННАЯ ПРЕКАЛЛИКРЕИНОМ АЛЬБУМИНОВАЯ ФРАКЦИЯ ПЛАЗМЫ КРОВИ | 2003 |
|
RU2321421C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВНУТРИВЕННОГО ИММУНОГЛОБУЛИНА | 1998 |
|
RU2140289C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИММУНОГЛОБУЛИНА ДЛЯ ВНУТРИВЕННОГО ВВЕДЕНИЯ И ЕГО ВАРИАНТЫ | 1999 |
|
RU2155069C1 |
| СПОСОБ ПОЛУЧЕНИЯ IGM-СОДЕРЖАЩЕГО КОНЦЕНТРАТА ИММУНОГЛОБУЛИНА | 1999 |
|
RU2158136C1 |
| Способ получения сывороточного альбумина | 1971 |
|
SU467536A1 |
| ПРЕПАРАТ ВНУТРИВЕННОГО ПРОТИВОАЛЛЕРГИЧЕСКОГО ИММУНОГЛОБУЛИНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2002 |
|
RU2238106C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЛЬБУМИНА ИЗ ПЛАЦЕНТЫ ЧЕЛОВЕКА | 1997 |
|
RU2139067C1 |
Изобретение относится к медицине, а именно к способу получения альбумина. Альбумин получают из альбуминосодержащих растворов денатурацией примесных белков этанолом в присутствии каприловой кислоты с последующим выделением альбумина из центрифугата. Осветленный центрифугат разводят дистиллированной водой или физиологически приемлемым буфером до концентрации этанола 1-10% концентрируют альбумин ультрафильтрацией с последующей диафильтрацией, пастеризацию проводят "в объеме" охлаждают альбумин и проводят дополнительную стерилизующую фильтрацию. Способ позволяет получить мономерный продукт. 2 табл.
Способ получения альбумина из альбуминсодержащих растворов, включающий введение в них каприлат-иона в присутствии этанола, удаление образовавшегося осадка центрифугированием, осветление центрифугита фильтрованием, концентрирование продукта и стерилизующую фильтрацию, отличающийся тем, что осветленный центрифугат разводят дистиллированной водой или физиологически приемлемым буфером до концентрации 1 - 10%, концентрируют альбумин ультрафильтрацией с последующей диафильтрацией, после стерилизующей фильтрации проводят пастеризацию "в объеме" при постоянном перемешивании, альбумин охлаждают и проводят дополнительную стерилизующую фильтрацию.
| Способ получения сывороточного альбумина | 1971 |
|
SU467536A1 |
| Способ получения альбумина и гемоглобина | 1984 |
|
SU1590031A3 |
| SU 215428 А1, 28.10.69. | |||
Авторы
Даты
1999-02-10—Публикация
1997-01-23—Подача