Изобретение относится к медицинской промышленности и может быть использовано для получения раствора альбумина, применяемого для внутривенного введения гемодинамического действия и парэнтерального питания.
Основным сырьем для получения раствора альбумина служат различные виды донорской плазмы, заготовленные согласно нижеперечисленным документам:
1. Инструкция по фракционированию крови на клеточные компоненты и плазму, утвержденная МЗ СССР 06-14/24 от 11.06.87 г.
2. Инструкция по медицинскому освидетельствованию доноров крови, плазмы, клеток крови, утвержденная МЗ РФ от 16.11.98 г.
3. Приказ МЗ СССР за 155 от 12.04. 90 г. "О совершенствовании деятельности учреждений службы крови".
Альбумин относится к полипептидам, по форме макромолекулы представляет собой глобулярный белок и является белковым компонентом гемоглобина.
Разделение белков плазмы крови доноров достигают путем изменения на разных этапах фракционирования величины рН, концентрации спирта, температуры и ионной силы. В процессе фракционирования химических превращений не происходит.
Известен способ получения раствора альбумина, разработанный НИИ гематологии и переливания крови МЗ УССР (типовой регламент производства раствора альбумина 5, 10, и 20%), утвержденный в 1987 г.
Способ заключается в фракционировании плазмы на фракционных столах с выделением сырого осадка альбумина и растворении его в апирогенной дистиллированной воде, центрифугировании и осветляющей фильтрации с последующим розливом для замораживания и сушки. После стадии лиофилизации сухой альбумин растворяют, подвергают стерилизационной фильтрации, производят розлив во флаконы и пастеризуют.
Недостатками известного способа являются трудоемкость процесса и невозможность получения более качественного продукта. Качественные показатели раствора альбумина, полученные по известному способу, соответствуют нормативным показателям.
Изобретением решаются задачи улучшения качества продукта и снижения трудоемкости технологического процесса.
Для достижения названного технического результата в предлагаемом способе, включающем стадии фракционирования плазмы на фракционных столах с выделением сырого осадка альбумина и растворением его в апирогенной дистиллированной воде с последующей осветляющей фильтрацией, розливом во флаконы и пастеризацией препарата, стадия сублимационной сушки заменена ультрафильтрацией на установке Sartakon-II (отмывание молекул спирта и других низкомолекулярных примесей 5-ти кратным объемом воды).
Это позволяет улучшить качество получаемого раствора альбумина и снизить трудоемкость процесса.
Предлагаемый способ поясняется чертежом, на котором изображена схема производства раствора альбумина (чертеж). На схеме показаны фракционные столы (1), центрифуги рефрижераторные (2), осветляющий фильтр (3), Sartakon (4), стерильный фильтр (5), закаточный станок (6), термостат (7).
Способ осуществляется следующим образом.
Фракционирование белков плазмы производится путем поэтапного отделения каждой фракции.
Стадии ТП 1.5, ТП 1.7, ТП 1.8, ТП 1.9 проводятся на одном оборудовании.
Плазма (на стадии 1.5), а затем центрифугаты на стадиях ТП 1.7 и ТП 1.8 загружаются в котел фракционного стола (1). Создаются условия, необходимые для выделения и созревания осадка определенной фракции белков. Затем вся смесь подается в центрифугу и после центрифугирования осадок утилизируется, а центрифугат снова подается в котел (1).
Полученный центрифугат на стадии ТП 1.9 утилизируется, а сырой осадок альбумина растворяется и подается на осветляющий фильтр (3). Процесс ультрафильтрации проводится на аппарате "Sartakon-II" (4).
Готовый раствор альбумина подается в установку для стерильной фильтрации (5) и розлива раствора во флаконы. Обкатка колпачков производится на закаточном станке (6). В термостатах (7) готовый продукт проходит пастеризацию и термостатирование. Пример.
I. Выделение фракции I.
В качестве сырья была взята плазма, предварительно проверенная на отсутствие антител к вирусу иммунодефицита человека (ВИЧ), вирусу гепатита С и поверхностного антигена вируса гепатита В.
В четыре котла, расположенных в двух фракционных столах с охлаждающими рубашками (по два в каждом), загрузили по 20 л плазмы - итого 80 л плазмы.
Плазма охлаждается до +1oС и к ней прибавляется охлажденный в малой ванне до -20oС 96% этиловый спирт, из расчета 90 мл спирта на 1 л плазмы. К концу осаждения температура смеси понижается до -3oС. По окончанию добавления спирта смесь перемешивается 2 ч и затем оставляется на два часа. В данных условиях в осадок выпадает фракция 1 белков плазмы, содержащая в основном фибриноген. Осадок отделяется на стаканчиковых рефрижераторных центрифугах Sorvall RC 3С Plus при t = -3oC и 3000 об/мин в течение 30 мин. Осадок не используется
II. Выделение фракции II+III.
Центрифугат I загружается в котел фракционного стола. Отбирается проба для определения исходного рН (6,8-7,4). После того, как температура центрифугата достигнет -5 -6oС, буфером 1 рН доводится до 5,8-5,9. Затем, из расчета 150 мл/л центрифугата I, добавляется 96%-ный этиловый спирт, охлажденный до -20oС, со скоростью 15 мл/мин. Осадок созревает 12 ч. Отделение осадка проводится на центрифугах Sorvall RC 3С Plus при температуре -6oС и 3200 об/мин в течение 30 мин. Осадок не используется.
III. Выделение фракции IV.
Центрифугат II помещается в котел фракционного котла и охлаждается до температуры -7oС. К нему со скоростью 15 мл/мин добавляется 96%-ный этиловый спирт, предварительно охлажденный до температуры -20oС, из расчета 450 мл/л центрифугата II. После добавления спирта смесь оставляется для созревания осадка на 12 ч. Осадок отделяется на центрифугах Sorvall RC 3С Plus при температуре -7oС и 3500 об/мин в течение 45 мин. Осадок не используется.
IV. Выделение фракции V (альбумин).
Прежде чем выделить фракцию V, центрифугат III подвергается осветляющей фильтрации с помощью напорного бака и фильтра с порами 0,8+0,65 μм в котел фракционного стола при температуре -7oС. После фильтрации проводится забор пробы для определения рН. Затем с помощью буфера 2 рН доводится до 4,7-4,9. Для полноты выделения осадка альбумина смесь остается во фракционном столе при температуре -7-9oС и непрерывном перемешивании на 16 ч. Осадок отделяется на центрифугах Sorvall RC 3С Plus при температуре -7oС и 3700 об/мин в течение 60 мин. Надосадочная жидкость не используется. Осадок взвешивается и хранится при температуре -20oС не более 30 дней. Таким образом, идет накопление осадка.
V. Обработка сырого осадка альбумина. Для дополнительной очистки от глобулинов осадок альбумина растворяется в апирогенной дистиллированной воде, предварительно охлажденной до +5oС, в соотношении 1:3. Растворение производится в котле, помещенном во фракционный стол, при постоянном перемешивании при температуре +5oС в течение 2 ч. При этом альбумин растворяется, а нестабильные примеси выпадают в осадок. Отделение осадка нестабильных примесей проводится с помощью осветляющей фильтрации на фильтрах с порами 0,8+0,65 μм.
VI. Ультрафильтрация раствора альбумина.
Освобождение раствора альбумина от спирта проводится на аппарате "Sartakon-II" в емкости из нержавеющей стали при температуре +4 +6oС. К одному объему раствора альбумина добавляется один объем апирогенной дистиллированной воды и начинается ультрафильтрация при входном давлении 2 бара, выходном 1,3-1,5 бара. По мере убывания раствора добавляется еще пять объемов апирогенной дистиллированной воды. По окончанию ультрафильтрации добавляют 30%-ный раствор каприлата натрия (консервант) из расчета 10 мл/л раствора альбумина и производят коррекцию рН раствора (рН должно быть 6,5-7,2).
VII. Получение готового продукта.
Готовый 10%-ный раствор альбумина передается на стерилизующую фильтрацию. Стерилизующая фильтрация и розлив альбумина во флаконы производится в стерильных условиях в ламинарном боксе с помощью фильтра с порами 0,45+0,2 μм и напорного бака. Флаконы укупориваются резиновыми пробками и обкатываются алюминиевыми колпачками. Вся серия препарата прогревается в термостатах при температуре 60±1oС в течение 10 ч для инактивации вируса инфекционного гепатита (пастеризация). После пастеризации препарат выдерживается при температуре +37oС в течение 2 недель (стабилизация белков), а затем подвергается всем видам контроля, маркировке и упаковке.
Был получен раствор альбумина со следующими показателями (аналитический паспорт прилагается).
Заявляемый способ позволяет получить раствор альбумина с более высокими качественными показателями (увеличивается содержание альбумина, снижаются цветность, содержание полимеров, натрий-иона и калий-иона). Значительно снижается трудоемкость процесса, т.е. уменьшаются производственные площади, сокращается расход электроэнергии, облегчаются условия труда, сокращается время получения альбумина. На получение раствора альбумина заявляемым способом выдана лицензия.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОЧИСТКИ ПРОТИВОСТОЛБНЯЧНОГО ПРЕПАРАТА ИММУНОГЛОБУЛИНА ЧЕЛОВЕКА | 1988 |
|
SU1628293A1 |
| СПОСОБ ПОЛУЧЕНИЯ IGM-СОДЕРЖАЩЕГО КОНЦЕНТРАТА ИММУНОГЛОБУЛИНА | 1999 |
|
RU2158136C1 |
| СПОСОБ ПОЛУЧЕНИЯ МОНОМЕРНОГО АЛЬБУМИНА | 1997 |
|
RU2125888C1 |
| Способ получения сывороточного альбумина | 1971 |
|
SU467536A1 |
| СПОСОБ ПОЛУЧЕНИЯ ИММУНОГЛОБУЛИНА ДЛЯ ВНУТРИВЕННОГО ВВЕДЕНИЯ | 1992 |
|
RU2068695C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИММУНОГЛОБУЛИНА ЧЕЛОВЕКА АНТИСТАФИЛОКОККОВОГО ДЛЯ ВНУТРИВЕННОГО ВВЕДЕНИЯ | 1996 |
|
RU2141341C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЕТЕРИНАРНОГО АЛЬБУМИНА | 2005 |
|
RU2286350C1 |
| Способ выделения альбумина | 1974 |
|
SU712089A1 |
| СПОСОБ ПОЛУЧЕНИЯ ИММУНОГЛОБУЛИНА ЧЕЛОВЕКА ПРОТИВ КЛЕЩЕВОГО ЭНЦЕФАЛИТА ДЛЯ ВНУТРИВЕННОГО ВВЕДЕНИЯ | 1996 |
|
RU2141342C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛЬБУМИНА | 1998 |
|
RU2140287C1 |
Изобретение относится к медицинской промышленности. Проводят фракционирование плазмы на фракционных столах с выделением сырого осадка альбумина. Растворение его в апирогенной дистиллированной воде с последующей осветляющей фильтрацией и ультрафильтрацией на установке Sartakon-2. Розлив во флаконы и пастеризацию препарата. Изобретение позволяет повысить качество продукта. 1 з.п.ф-лы, 1 ил.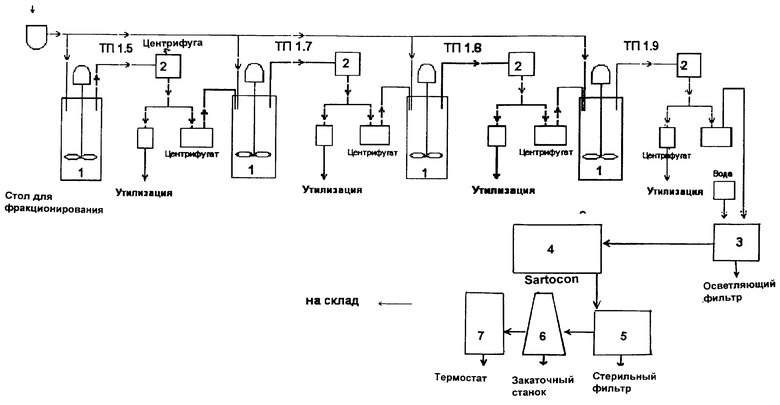
| Кипятильник для воды | 1921 |
|
SU5A1 |
| НИИ гематологии и переливания крови МЗ УССР | |||
| - Киев, 1987 | |||
| СПОСОБ ПОЛУЧЕНИЯ МОНОМЕРНОГО АЛЬБУМИНА | 1997 |
|
RU2125888C1 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИТОКСИЧЕСКОЙ СЫВОРОТКИ | 1992 |
|
RU2062617C1 |
| SU 1510149 А, 10.01.1998. | |||
Авторы
Даты
2003-05-27—Публикация
2001-07-13—Подача