Изобретение относится к сорбиновой кислоте или ее соли, содержащей низкие концентрации иона марганца (Mn++) в качестве стабилизатора.
Сорбиновая кислота (2,4 - гексадиеновая кислота) и ее соли, особенно сорбат калия, широко используются в качестве антимикробных средств для упакованных пищевых продуктов и фармацевтических и других важных для здоровья продуктов, предназначенных для использования людьми и животными. Сорбиновая кислота и ее соли являются особенно ценными как фунгистатические агенты для ингибирования или задержки роста плесеней и дрожжей. Хотя сорбиновая кислота и ее соли являются вполне стабильными в сухом состоянии, они являются чувствительными к окислению в водном растворе. Такое окисление приводит к таким продуктам, как кетоны и альдегиды, которые могут вызывать появление нежелательного вкуса и запаха, а полимеры альдегидов могут вызывать появление нежелательной окраски. Окисление сорбиновой кислоты или ее соли может привести в результате к потере достаточного количества иона сорбата, ухудшая желаемый антимикробный эффект.
Механизм окисления сорбиновой кислоты и средства для стабилизации против такого окисления были предметом значительных исследований. См., например, S. S. Arya et al, "Разложение продуктов сорбиновой кислоты в водных растворах", Food Chemistry, 29, (1988), с. 41-49; S.S. Arya "Стабильность сорбиновой кислоты в водных растворах", Journal of Agricultural and Food Chemistry, 28 (1980), 1246-1249, L. Pekkarinen et al. "Влияние солей тяжелых металлов на стабильность сорбиновой кислоты в окисляющих сернокислых растворах", Suomen Kemistilehti, 40, (1967), 54- 58, L. Pekkarinen "Механизм окисления сорбиновой кислоты молекулярным кислородом в воде", Suomen Kemistilehti, 42, N 3 (1969), 147-152, Y.N. Sofos "Сорбатные пищевые консерванты", CRC Press, Inc, Boca Raton, Florida (1989), Pekkarinen "Влияние ацетатов металлов на окисление сорбиновой кислоты молекулярным кислородом в уксусной кислоте и сравнение результатов с таковыми для элеостеариновых кислот", Acta Chemica Scandinavica, 26 (1972), 2367-2371, и Pekkarinen et al., "Влияние солей тяжелых металлов на стабильность сорбиновой кислоты в окисляющих разбавленных сернокислых растворах, Suomen Kemistilehti В, 40, N 2 (1967), 54-58.
Вышеупомянутые авторы обнаружили, что ионы тяжелых металлов, включая ион марганца (Mn++), были использованы для стабилизации сорбиновой кислоты и сорбатных солей от окисления. Являющиеся эффективными пропорции составляют 50 г/м (частей по массе на миллион) (S.S. Arya) и 10-2-10-3 моль/л (примерно 55-550 мг иона марганца на литр - Pekkarinen et al).
Настоящее изобретение основано на обнаружении того факта, что наличие очень малого количества иона марганца в водном растворе сорбиновой кислоты или ее соли является эффективным для стабилизации таких водных растворов от окисления. Изобретение обеспечивает стабилизированные водные растворы, содержащие сорбиновую кислоту или ее соль в антимикробном количестве, особенно в фунгистатическом количестве, и дополнительно содержащие от 0,1, а предпочтительно от 0,2 до примерно 5 г/м (частей по массе на миллион частей раствора) иона марганца, указанный ион марганца находится в количестве, достаточном для ингибирования или замедления окисления указанной сорбиновой кислоты или ее соли в такие окисленные продукты как ацетальдегид. Продуцирование ацетальдегида является нежелательным, потому что он полимеризуется (по реакции альдельной конденсации) с образованием хромогенов, и имеется известная корреляция между продуцированием ацетальдегида и снижением сорбата (Arya et al. (1988), подтверждается авторами здесь).
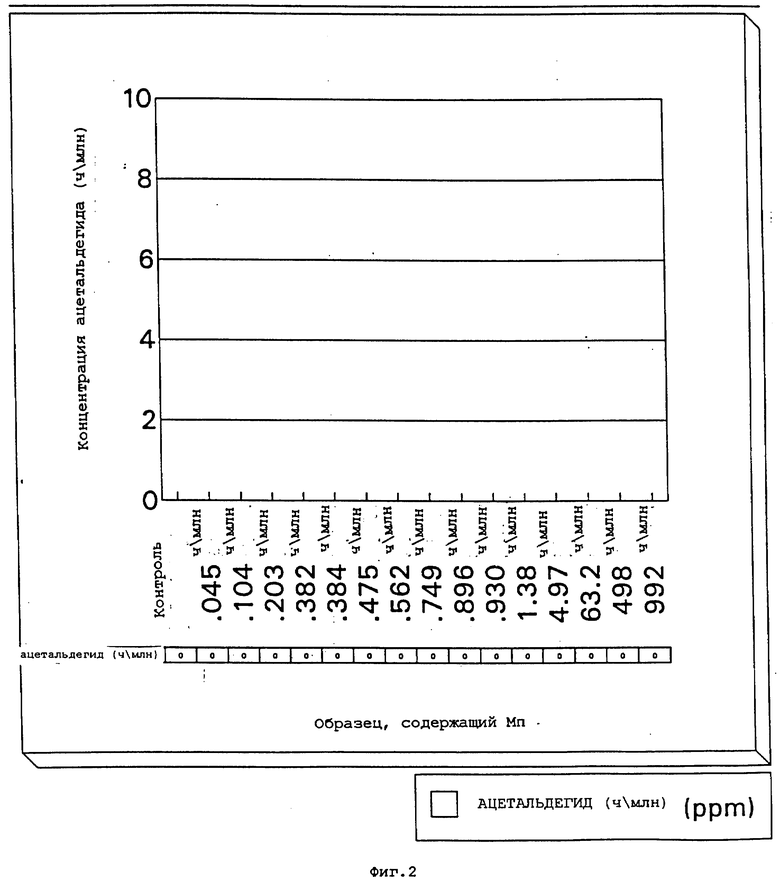
Фиг.1. представляет собой график концентрации ацетальдегида в свежеприготовленных водных растворах концентрата сукралозы, содержащих сорбат калия, в зависимости от концентрации иона магния;
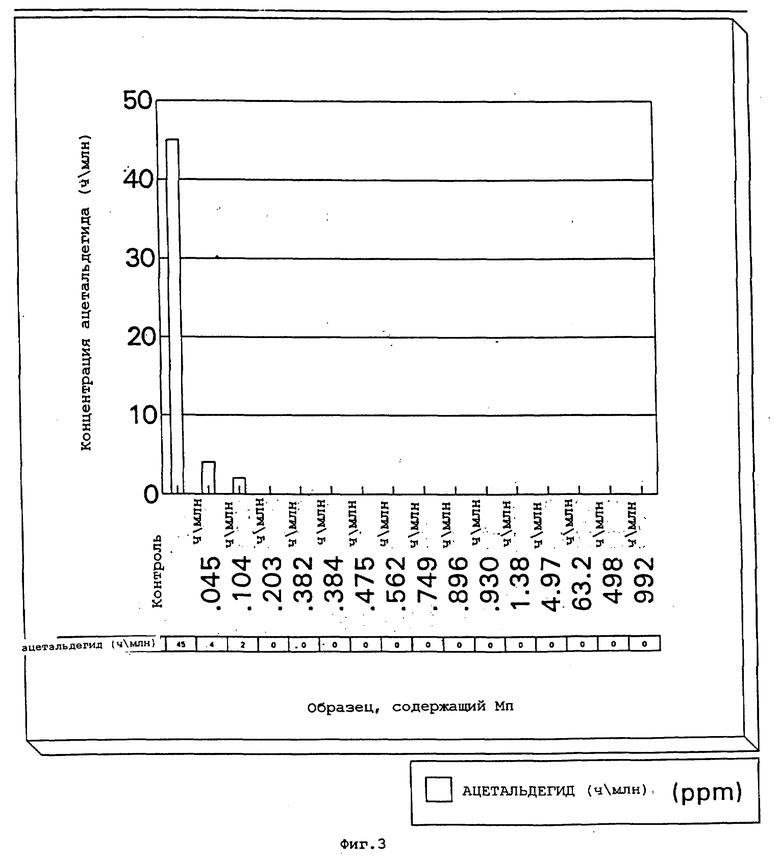
фиг.2 и 3 представляют собой графики концентраций ацетальдегида в тех же водных растворах в зависимости от концентрации иона после хранения при 50oC в течение 5 и 10 дней соответственно;
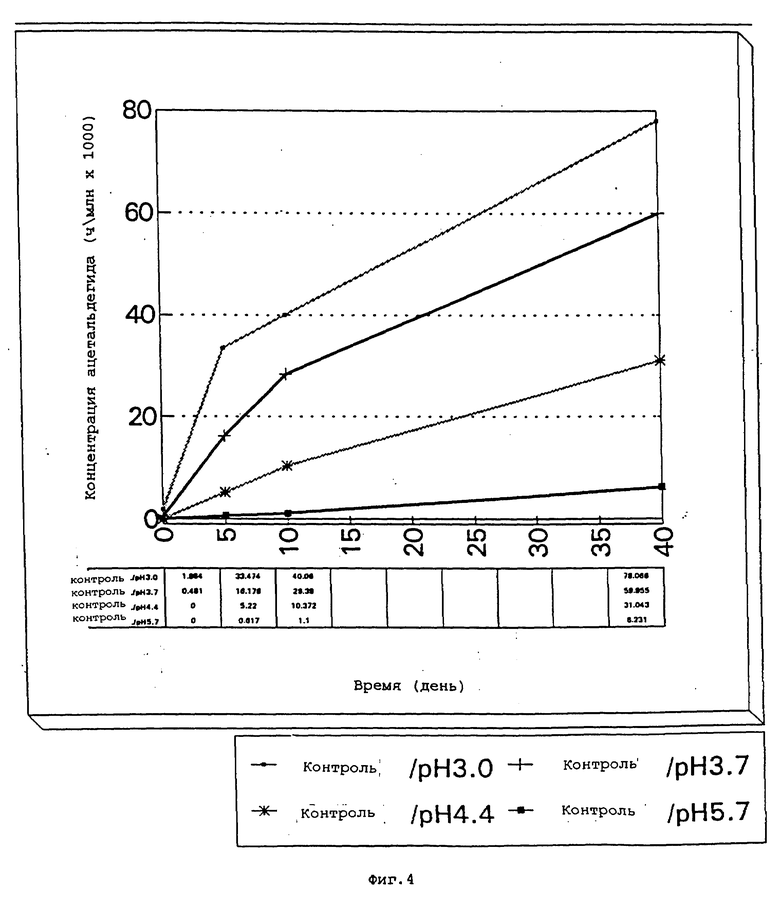
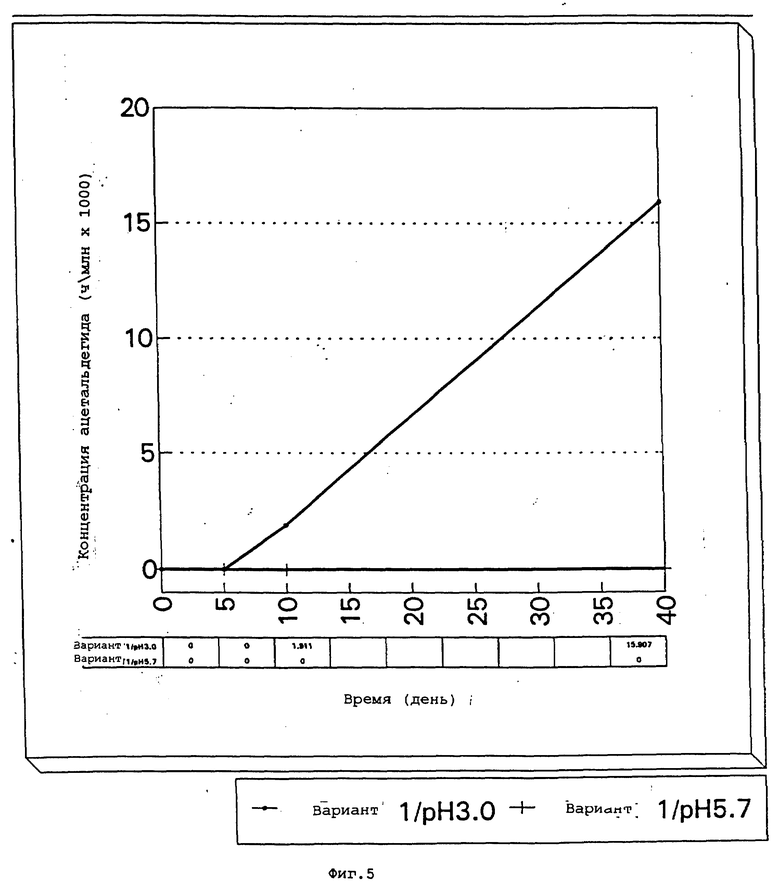
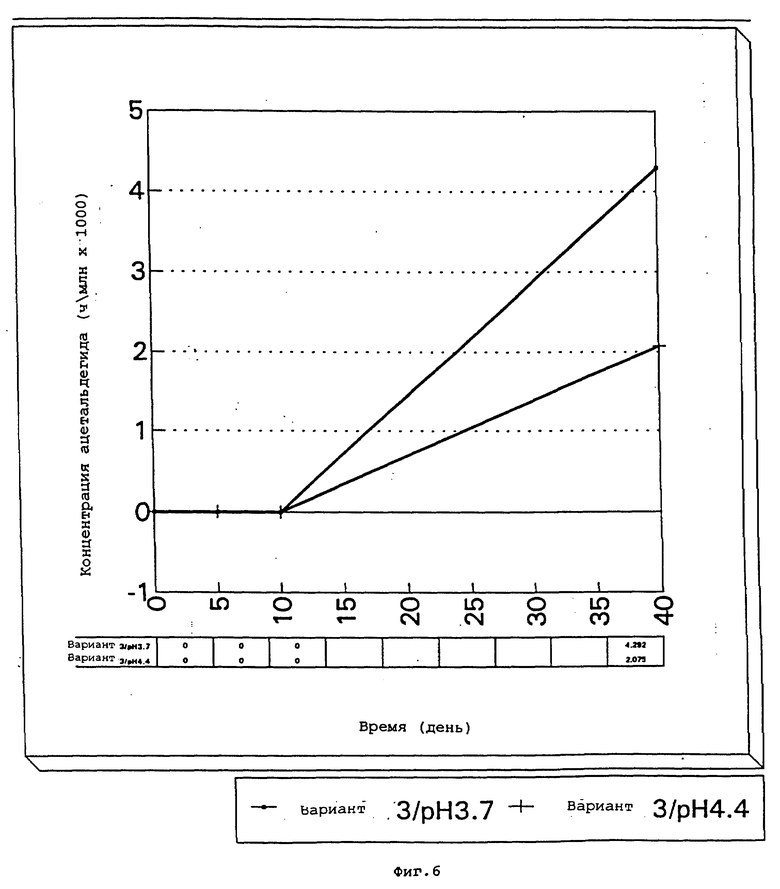
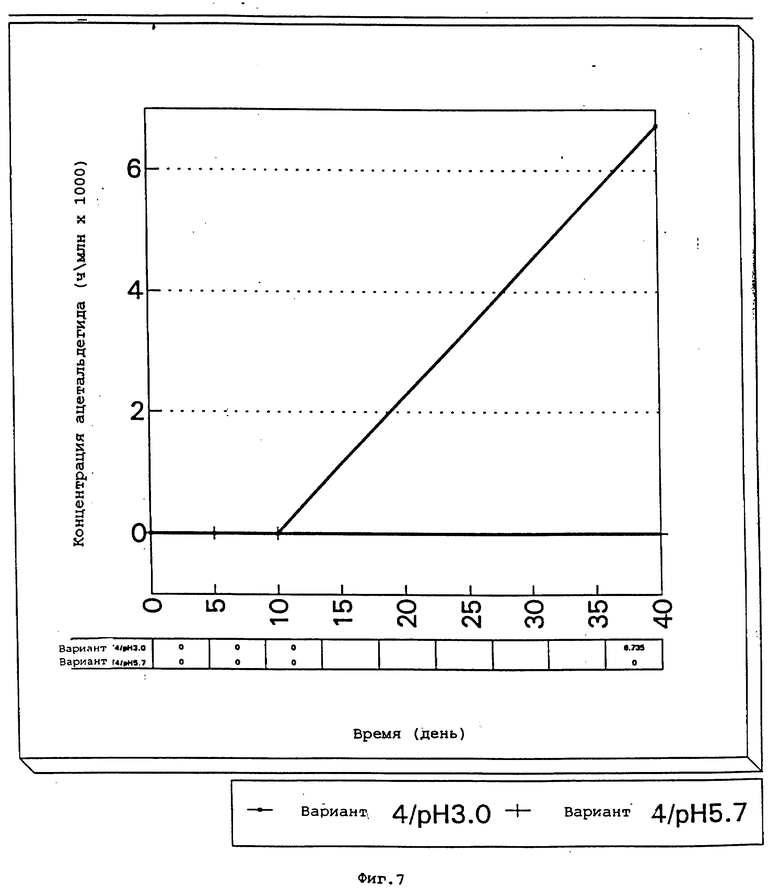
фиг. 4-7 представляют собой графики концентрации ацетальдегида подобных водных растворов (не содержащих сукралозы) в зависимости от концентрации иона марганца при различных pH после хранения при 50oC в течение 0, 5, 10 и 40 дней;
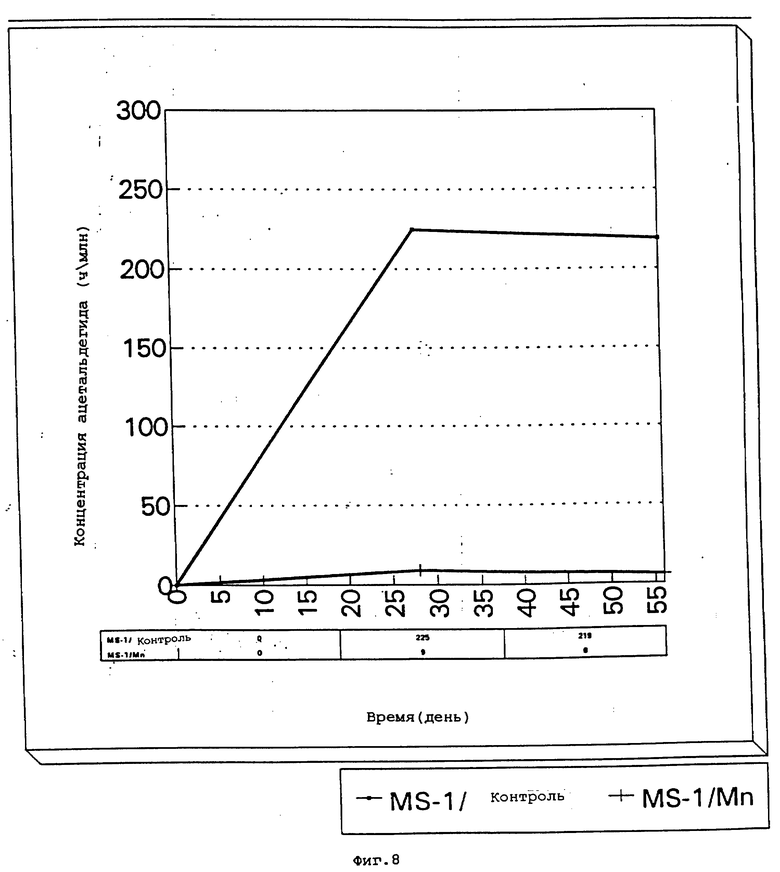
фиг. 8 представляет собой график концентрации ацетальдегида в полоскании для рта, содержащем фторид, в зависимости от концентрации иона марганца после хранения при 50oC в течение 0, 28 и 56 дней;
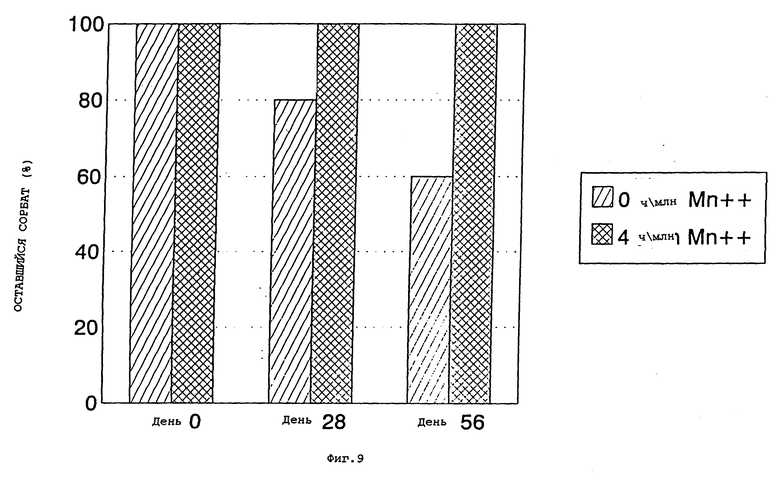
фиг. 9 представляет собой график процентного содержания исходного сорбата, оставшегося в полоскании для рта, содержащего фторид, в зависимости от концентрации иона марганца после хранения при 50oC в течение 0, 28 и 56 дней;
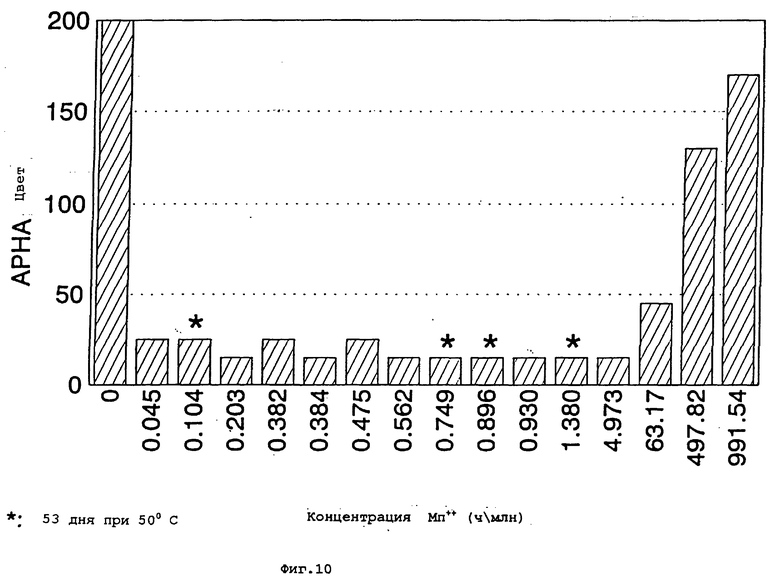
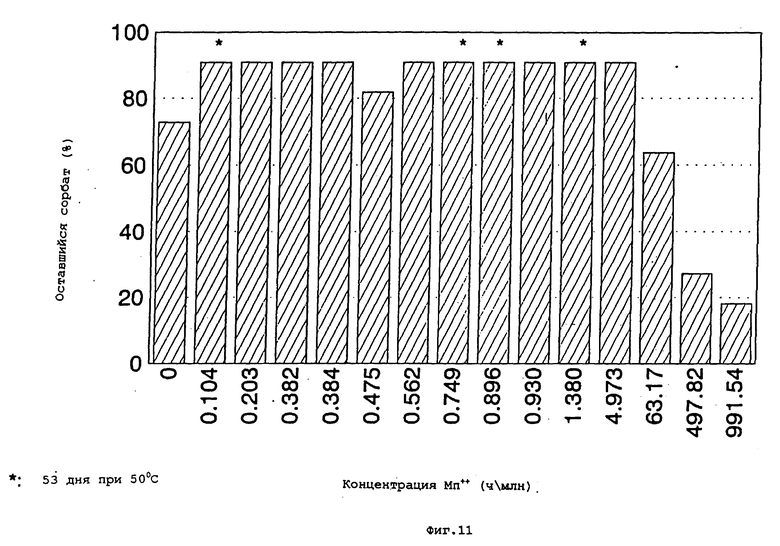
фиг.10 и 11 представляют собой соответственно графики развития окраски и оставшегося исходного сорбата в зависимости от концентрации иона марганца в водном растворе концентрата сукралозы, содержащего сорбат калия и различные концентрации иона марганца, после хранения в течение 53 или 59 дней при 50oC;
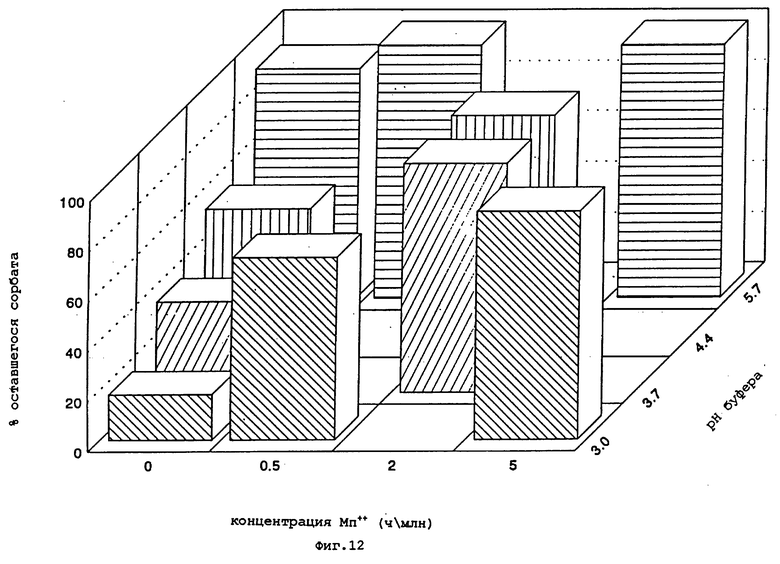
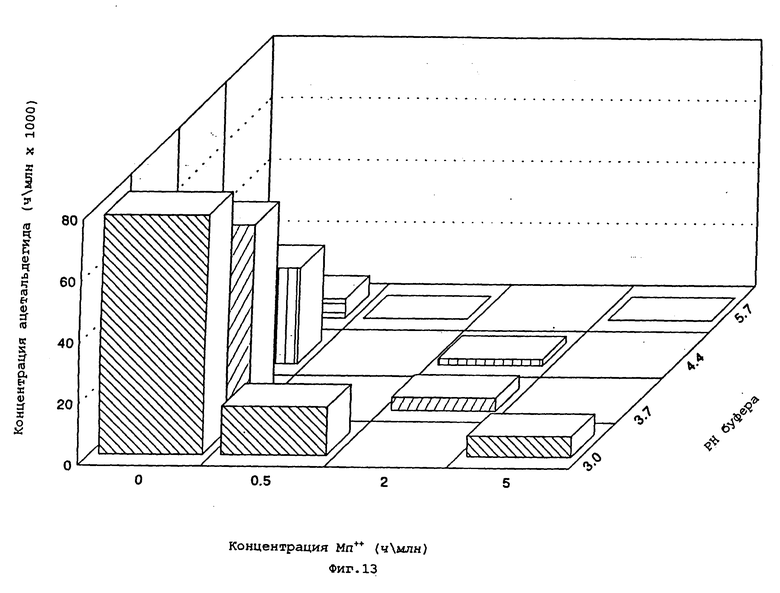
фиг. 12 и 13 представляют собой графики соответственно % оставшегося сорбата и концентрата ацетальдегида в забуферированном содержащем сорбат растворе с различными концентрациями иона Mn++ и при различных величинах pH после хранения при 50oC.
Водные растворы сорбиновой кислоты или ее соли (обычно сорбата калия или другой соли щелочного металла) настоящего изобретения содержат сорбиновую кислоту или ее соль в антимикробных пропорциях в количестве, достаточном, чтобы ингибировать или замедлять рост бактерий и предпочтительно плесеней и дрожжей, в растворе. Такие количества обычно находятся в интервале от примерно 0,005% (если нет других указаний, все приведенные здесь проценты являются массовыми, считая на общую массу раствора) до примерно 5%. Предпочтительно применять сорбат калия, потому что он обладает хорошей растворимостью в водных композициях и потому что он обычно считается безопасным для использования в пищевых и других продуктах, таких, как полоскание для рта, жидкости для промывки зубов, сиропы от кашля, тоники, приправы, сиропы, варенье и желе, газированные и неигристые напитки, мази и лосьоны на водной основе и т.п., которые предназначены для использования людьми и животными.
Ион марганца может быть добавлен к раствору любым обычным образом, например, при добавлении растворимой соли марганца, такой, как сульфат марганца MnSO4, к раствору. Количество добавленной соли марганца должно быть достаточным, чтобы обеспечить от 0,1, а предпочтительно от 0,2 до примерно 5 ч/м иона Mn++ в растворе. Альтернативным способом добавления иона Mn++ является пропускание стабилизируемого сорбатом раствора через слой активированного угля, содержащего ион марганца, чтобы ион переходил в раствор в желаемом количестве (и предпочтительно добавления сорбата после обработки активированным углем, поскольку активированный уголь может поглощать сорбат в значительных количествах).
Предпочтительная композиция изобретения представляет собой водные жидкие концентраты сукралозы, сильного подслащивателя, который имеет химическое название 4-хлор-4-деокси- α -галактопиранозил-1,6-дихлор-1,6-дидеокси -β- фруктофуранозид. Такие водные жидкие концентраты содержат от 3 до 35 мас.% (и предпочтительно 20-28 мас. %) сукралозы, консервирующая система включает сорбиновую кислоту или ее соль, буферную систему для поддержания pH от примерно 4 до 5,5, воду и от 0,1, а предпочтительно 0,2 до примерно 5 частей по массе на миллион частей раствора иона Mn++. Такие водные концентраты (без иона марганца) описаны Антенуччи с сотр. в EP-A-O 493 919, опубликованном 8 июля 1992 г.
Другие стабилизированные водные растворы изобретения включают полоскания для рта, жидкости для промывки зубов, сиропы от кашля, тоники, приправы, сиропы, варенья и желе, газированные и неигристые напитки, мази и лосьоны и т. п., содержащие сорбиновую кислоту или ее соль в качестве консерванта и от 0,1, а предпочтительно от 0,2 до примерно 5 частей по массе на миллион частей раствора иона марганца.
Пример 1. Для иллюстрации изобретения добавляют различные концентрации иона Mn++ (добавленного в виде моногидрата сульфата марганца) к водным растворам следующего состава, мас.%:
Ингредиент
Сукралоза - 25,000
Сорбат калия - 0,110
Бензоат натрия - 0,110
Безводная лимонная кислота - 0,272
Дигидрат нитрата натрия - 0,258
Очищенная вода - 74,250
Всего - 100,000
pH водного раствора - 4,4
Анализируют несколько растворов на содержание ацетальдегида с помощью газовой хроматографии в день 0 (т.е. свежеприготовленные) и после хранения при 50oC в течение 5 и 10 дней. Результаты приведены на фиг. 1-3. Как можно видеть из результатов, образцы, содержащие 0,2 ч/м или более иона Mn++, не показывают ацетальдегид после 10 дней.
Другие анализы показывают, что образцы, содержащие около 500 (по анализу 498) и около 1000 (по анализу 992) ч/м Mn++-иона, начинают терять сорбат после 5 дней (содержание сорбата было 0,09% после 5 дней и 0,08% после 10 дней). Эти образцы становятся окрашенными через 5 дней. Исходная APHA (American Public Health Association) окраска образца с 1000 г/м Mn++ была 10-20, через 5 дней окраска этого образца была 20-30, а через 10 дней она была 30-40. Исходная APHA окраска образца с 500 ч/м Mn++ была 5-10, через 5 дней она составляет 10-20, а через 10 дней она составила 20-30.
Образцы, содержащие примерно 5 и 63 ч/м Mn++, имели начальную окраску APHA 5-10, оба они остались без изменений через 5 дней, но имели APHA окраску 10-20 через 10 дней. Эти образцы не теряли содержания сорбата после 10 дней. Все эти образцы, включая контроль, остались без изменений как по окраске, так и по содержанию сорбата через 10 дней.
Анализы образцов, содержащих широкий интервал концентраций Mn++, на процент исходного оставшегося сорбата и развитие окраски после 59 дней при 50oC приведены на фиг.10 и 11 соответственно.
Пример 2. Были проведены следующие эксперименты для дальнейшей иллюстрации изобретения.
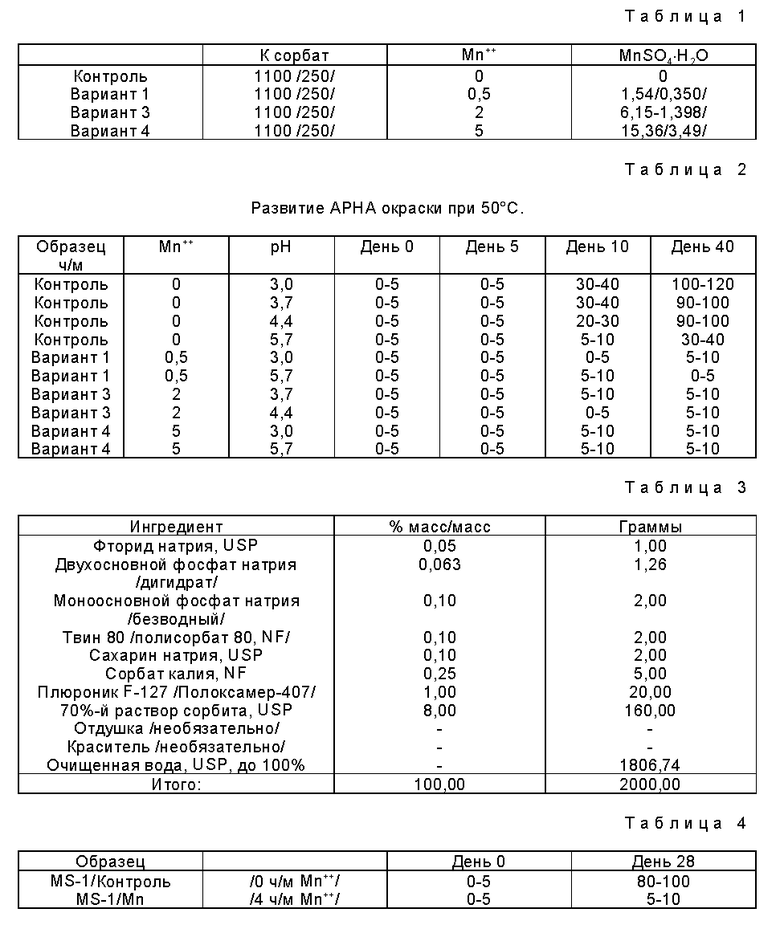
Образцы сорбата калия растворяют в равных весовых пропорциях деионизированной воды для получения 50% (мас./мас.) водных растворов. Прибавляют моногидрат сульфата марганца (MnSO4•H2O) в количествах (по массе), показанных в табл. 1 (действительно использованные количества в граммах показаны в скобках).
Вариант 2, который содержал 1 г/м Mn++, был получен, но не испытан.
Растворы были перенесены в лотки для сушки вымораживанием, заморожены и затем высушены замораживанием по следующей методике.
Должны быть выполнены предосторожности для осуществления сушки вымораживанием, поскольку сорбат калия может сублимироваться при температуре выше 60oC (Sofos, 1989). Выливают раствор сорбата калия и сульфата марганца в лотки для сушки вымораживанием и включают температурный датчик. Помещают лотки в устройство для сушки вымораживанием, температура которого установлена равной -45oC или ниже. Включают вакуум и устанавливают вакуум 100 мТорр или ниже. Включают обогрев сушки и устанавливают ее температуру, равной -8oC. Когда температура образца устанавливается -8oC, повышают температуру сушки до 10-12oC. Когда температура образца достигает 10-12oC, повышают температуру сушки до 25oC. Как только температура образцов достигнет 25oC, образцы являются сухими. Эта процедура занимает примерно 24-36 часов до завершения в зависимости от глубины раствора образца в лотке.
Образцы сорбата калия, высушенные сушкой вымораживанием, содержащие различные концентрации Mn++, растворяют в подкисленных буферных водных растворах следующего состава, мас./мас.%:
Ингредиенты
Бензоат натрия - 0,110
Сорбат калия /плюс Mn++ - 0,110
Безводная лимонная кислота - 0,272
Дигидрат цитрата натрия - 0,258
Гидроксид натрия, 50-й водный раствор - Сколько необходимо для нужного pH
Очищенная вода - До 100
Всего - 100
В табл. 2 приводятся величины pH для нескольких растворов и развития APHA окраски при 50oC в день 0 и через 5, 10 и 14 дней.
Образцы также испытывают на концентрацию ацетальдегида в дни 0, 5, 10 и 40; результаты представлены на фиг. 4-7.
Пример 2 иллюстрирует важный аспект настоящего изобретения, причем сорбат калия тщательно смешивают с ионом марганца, указанный ион марганца присутствует в количестве, достаточном для ингибирования окисления указанного сорбата калия в ацетальдегид, когда указанный сорбат калия растворен в водном растворе. Примерные полезные пропорции сорбат: Mn++ находится внутри интервала от примерно 11000:1 до примерно 200:1 по массе.
Данные, приведенные в примере 2, дополнительно иллюстрируют тот факт, что pH водного раствора является важным параметром, который следует учитывать при практическом осуществлении изобретения. Как можно видеть из приведенных данных, при более высоких величинах pH, таких как 5,7, скорость окисления с образованием окраски и ацетальдегида ниже, чем при pH около 3. Это проиллюстрировано на графиках, представленных на фиг. 12 и 13, которые соответственно показывают % оставшегося сорбата и концентрацию ацетальдегида в забуферированном растворе, содержащем сорбат и различные концентрации иона Mn++, при различных величинах pH после хранения при 50oC.
Пример 3. Готовят свободное от спирта фторированное полоскание для рта из следующих ингредиентов (см. табл.3).
Варианты хранили при 50oC в течение 28 дней, контролем являлся раствор приведенной выше рецептуры, пример изобретения, содержащий 4 ч/м Mn++-иона. Два образца испытывали на появление окраски со следующими результатами (см. табл. 4).
Оба хранившихся образца также испытывали на концентрацию ацетальдегида и анализировали на процент исходного сорбата, оставшегося в дни 0, 28 и 56. Результаты представлены на фиг.9.
Изобретение предназначено для использования в качестве антимикробных средств для упакованных пищевых и фармацевтических продуктов. Стабилизированный водный раствор содержит сорбиновую кислоту или ее соль в количестве, обеспечивающем антимикробный эффект, и стабилизирующий агент - раствор иона двухвалентного марганца от 0,1 до 5 ч по массе на миллион частей раствора, достаточном для ингибирования окисления указанной сорбиновой кислоты или ее соли в ацетальдегид. Стабилизированный раствор обладает хорошей растворимостью в композиции и является безопасным для использования в продуктах, обладает фунгицидной активностью. 2 с. и 19 з.п.ф-лы, 4 табл., 13 ил.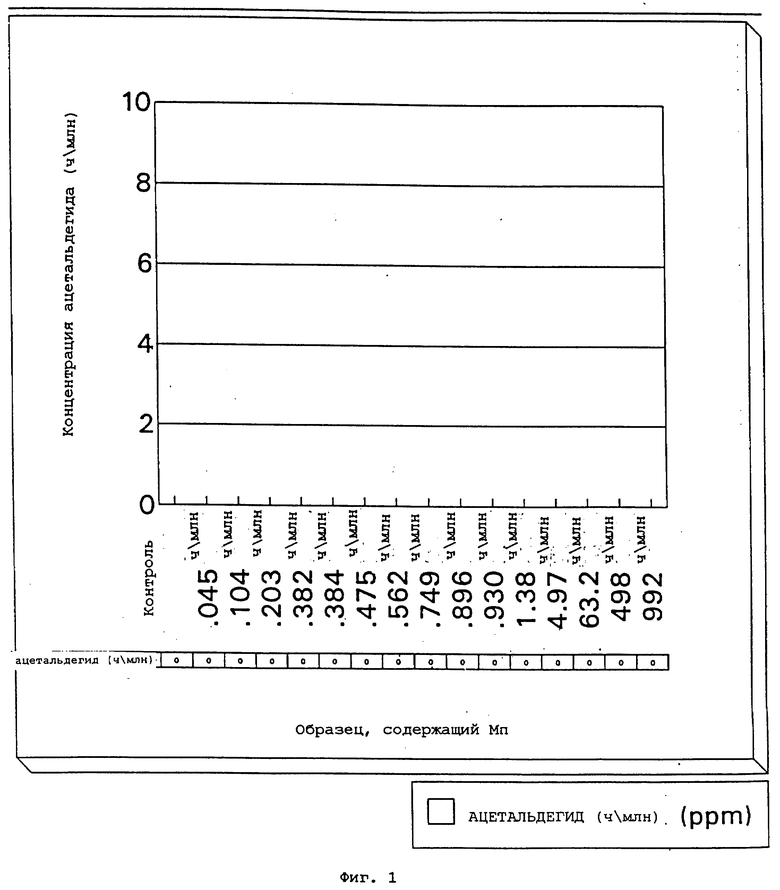
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| S.S.Arya | |||
| Стабильность сорбиновой кислоты в водных растворах | |||
| Journal of Agricultural and Food Chemistry | |||
| Видоизменение прибора с двумя приемами для рассматривания проекционные увеличенных и удаленных от зрителя стереограмм | 1919 |
|
SU28A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| J.N.Sofos | |||
| Сорбатные пищевые консерванты | |||
| CRG Press | |||
| Ine, Boca Raton, Florida, 1989. | |||
Авторы
Даты
1999-02-27—Публикация
1993-10-26—Подача