Настоящее изобретение относится к способу гидроцианирования нитридов с этиленовой ненасыщенностью до насыщенных динитрилов, особенно к гидроцианированию пентен-нитрилов до адипонитрила, одного из основных соединений для получения полиамида-66.
В патенте фракции N 1599761 описывается способ получения нитрилов путем добавления цианистоводородной кислоты к органическим соединениям, содержащим по крайней мере одну двойную этиленовую связь, в присутствии катализатора на основе никеля и триарилфосфита. Эту реакцию можно осуществлять в присутствии растворителя или без него.
Когда в этом способе уровня техники используют растворитель, то речь идет предпочтительно об углеводороде, таком как бензол или ксилолы, или о нитриле, таком как ацетонитрил.
Используемый катализатор представляет собой органический комплекс никеля, содержащий лиганды, такие как фосфины, арсины, стильбины, фосфиты, арсениты или антимониты.
В вышеуказанном патенте также рекомендуют наличие промотора, для активации катализатора, такого как соединения бора или соль металла, обычно кислота Льюиса.
В этом способе среда целиком органическая и один из ее основных недостатков заключается в трудности отделения, по окончании реакции, продуктов гидроцианирования от каталитического раствора, содержащего несколько составляющих (комплекс никеля, триарилфосфит, промотор), особенно с целью рециркуляции этого раствора в новую реакцию гидроцианирования. Такое отделение трудное и неполное и констатируют значительную потерю катализатора так же, как наличие вышеуказанного катализатора в продуктах гидроцианирования.
В патенте Франции А-2338253 предлагают осуществлять гидроцианирование соединений, содержащих по крайней мере одну этиленовую ненасыщенность, в присутствии водного раствора соединения переходного металла, особенно никеля, палладия или железа, и сульфированного фосфина.
Этот последний способ позволяет осуществлять хорошее гидроцианирование, особенно пентен-нитрилов, и легкое отделение каталитического раствора простой декантацией.
Полученные во время реакции гидроцианирования результаты относительно хорошие с различными веществами и особенно с производными олефинов, как пентен-нитрилы. Однако оказывается, что процентное содержание образовавшегося линейного динитрильного соединения по отношению к совокупности полученных изомеров обычно не превышает 65-70%. Кроме того, констатируют, что катализатор быстро дезактивируется.
В настоящем изобретении предлагается уменьшать эти недостатки, в особенности улучшать степень линейности получаемых продуктов и/или увеличивать продолжительность срока службы катализатора.
Настоящее изобретение представляет собой способ гидроцианирования алифатического нитрила с этиленовой ненасыщенностью путем взаимодействия с циановодородом в присутствии водного раствора катализатора, включающего соединение переходного металла и сульфированный фосфин, отличающийся тем, что вышеуказанный раствор содержит также сокатализатор, состоящий по крайней мере из одной кислоты Льюиса.
Преимущественно используемые в способе настоящего изобретения нитрилы с этиленовой ненасыщенностью представляют собой линейные пентен-нитрилы, как пент-3-ен-нитрил, пент-4-ен-нитрил и их смеси.
Эти пентен-нитрилы могут содержать обычно незначительные количества других соединений, как 2-метил-бут-2-ен-нитрил, 2-метил-пент-2-ен-нитрил, валеронитрил, адипонитрил, 2-метил-глутаронитрил, 2-этил-сукцинонитрил или бутадиен, полученные из предыдущей реакции гидроцианирования бутадиена и/или изомеризации 2-метил-бут-3-ен-нитрила до пентен-нитрилов.
В качестве соединения переходные металлов предпочтительно используют соединения никеля, палладия и железа. Используют соединения, растворимые в воде или способные переходить в раствор в условиях реакции. Остаток, связанный с металлом, не критический, если только он удовлетворяет этим условием.
Из вышеуказанных соединений наиболее предпочтительными соединениями являются соединения никеля; в качестве примеров, не ограничивающих объема охраны изобретения, можно назвать
соединения, в которых никель имеет нулевую степень окисления, как тетрацианоникелат калия K4(NiCN4), бис(акрилонитрил)-никель-(O), бис(циклоокта-1,5-диен)2-никель и производные, содержащие лиганды группы ya, как тетракис-(трифенилфосфин)-никель-(O) (в этом последнем случае соединение может быть растворено в несмешивающемся с водой растворителе, как толуол, затем водный раствор сульфированного фосфина экстрагирует часть никеля, причем в водном растворе, который отстаивается, появляется красное окрашивание);
соединения никеля, как карбоксилаты (особенно ацетат), карбонат, бикарбонат, борат, бромид, хлорид, цитрат, тиоцианат, цианид, формиат, гидроксид, гидрофосфит, фосфит, фосфат и производные, иодид, нитрат, сульфат, сульфит, арил- и алкильсульфонаты.
Нет необходимости в том, чтобы соединение никеля также было само растворимо в воде. Например, малорастворимый в воде цианид никеля очень хорошо растворяется в водном растворе фосфина.
Когда используемое соединение никеля соответствует стадии окисления никеля выше 0, добавляют в реакционную среду восстановитель никеля, реагирующий предпочтительно с никелем в условиях реакции. Этот восстановитель может быть органическим или неорганическим. В качестве примеров, не ограничивающих объема охраны изобретения, можно назвать BH4Na, порошок цинка, магний, BH4K и боргидриды, предпочтительно растворимые в воде.
Этот восстановитель добавляют в таком количестве, чтобы число эквивалентно окисления-восстановления составляло 1-10. Тем не менее не исключаются величины ниже 1 и выше 10.
Когда используемое соединение никеля соответствует стадии окисления никеля = 0, также можно добавлять восстановитель типа вышеуказанных, но это добавление необязательно.
Когда используют соединение железа, пригодны те же восстановители.
В случае палладия восстановителями, кроме того, могут быть элементы реакционной среды (фосфин, растворитель, олефин).
Используемые в настоящем изобретении сульфированные фосфины преимущественно представляет собой сульфированные фосфины общей формулы I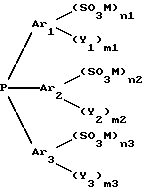
в которой Ar1, Ar2 и Ar3, одинаковые или разные, обозначают фенильные группы;
Y1, Y2 и Y3, одинаковые или разные, обозначают алкильный радикал с 1-4 атомами углерода; алкоксильный радикал с 1 - 4 атомами углерода; атом галогена;
M обозначает катионный, неорганический или органический остаток, выбираемый так, чтобы соединение формулы (I) было растворимо в воде, в группе, включающей H+; катионы, происходящие от щелочных или щелочноземельных металлов; N(R3R4R5R6)+ с R3, R4, R5 и R6, одинаковыми или разными, обозначающими алкильный радикал с 1 - 4 атомами углерода или атом водорода; другие катионы, происходящие от металлов, соли бензолсульфокислоты которых растворимы в воде;
"m1", "m2" и "m3" является целыми числами, одинаковыми или разными, 0 - 3;
"n1" "n2" и "n3"в являются целыми числами, одинаковыми или разными, 0 - 3, причем одно из них по крайней мере равно или выше 1.
В качестве примеров металлов, соли бензолсульфокислоты которых растворимы в воде, можно назвать свинец, цинк и олово.
Под выражением "растворимый в воде" в настоящем тексте понимают соединение, растворимое по крайней мере в количестве 0,01 г на литр воды.
Из фосфинов формулы (I) предпочтительные таковые, в которых
Ar1, Ar2 и Ar3 обозначает фенильные группы;
Y1, Y2 и Y3 обозначает группы, выбираемые среди алкильных радикалов с 1 - 2 атомами углерода; алкоксильных радикалов с 1 - 2 атомами углерода;
M обозначает катион, выбираемый в группе, включающей H+; катионы, происходящие от Na, K, Ca, Ba, NH+ 4; тетраметиламмоний-, тетраэтиламмоний-, тетрапропиламмоний-, тетрабутиламмоний-катионы;
"m1", "m2" и "m3" обозначает целые числа 0 - 3;
"n1", "n2" и "n3" обозначают целые числа 0 - 3, причем одно по крайней мере также выше 1.
Из этих фосфинов преимущественно предпочтительными являются соли натрия, калия, кальция, бария, аммония, тетраметиламмония и тетраэтиламмония моно-(сульфофенил)-дифенилфосфина, ди(сульфофенил)-фенил-фосфина и три(сульфофенил)-фосфина, в формулах которых группы SO3 находятся предпочтительно в мета-положении.
В качестве других примеров фосфинов формулы (I), которые могут быть использованы согласно способу изобретения, можно назвать щелочные или щелочноземельные соли, соли аммония, соли четвертичного аммония (3-сульфо-4-метил-фенил)-ди(4-метил-фенил)-фосфина; (3-сульфо-4-метокси-фенил) ди-(4-метокси-фенил)-фосфина; (3-сульфо-4-хлор-фенил)-ди-(4-хлор-фенил)-фосфина; ди-(3-сульфо-фенил)-фенил-фосфина; ди-(4-сульфо-фенил)-фенил-фосфина; ди-(3-сульфо-4-метил-фенил)-(4-метил-фенил)-фосфина; ди-(3-сульфо-4-метокси-фенил)-(4-метокси-фенил)-фосфина; ди-(3-сульфо-4-хлор-фенил)-(4-хлор-фенил)-фосфина; три-(3-сульфо-фенил)-фосфина; три-(4-сульфо-фенил)-фосфина; три-(3-сульфо''-4-метил-фенил)-фосфина; три-(3-сульфо-4-метокси-фенил)-фосфина; три-(3-сульфо-4-хлор-метил-фенил)-фосфина; (2-сульфо-4-метил-фенил)-(3-сульфо-4-метил-фенил)-(3,5 -дисульфо-4-метил-фенил)-фосфина; (3-сульфо-фенил)-(3-сульфо-4-хлор- фенил)-3,5-дисульфо-4-хлор-фенил)-фосфина.
Конечно можно использовать смесь этих фосфинов. В особенности можно использовать смесь моно-, ди- и триметасульфированных фосфинов.
Используемые в способе согласно настоящему изобретению сульфированные фосфины могут быть получены при применении известных способов. Так, согласно данным H.SCHINDLBAUER, Monatsch. Chem. 96, c. 2051 - 2057 (1965), натриевую соль (п-сульфофенил)-дифенил-фосфина можно получать путем введения во взаимодействие, в присутствии натрия или калия, п-хлорбензолсульфоната натрия с дифенилхлорфосфином. Согласно способу, описанному в J.Chem.Soc., с. 276 - 288 (1958) и в патенте Великобритании N 1066261, фенилфосфины формулы (I) можно получать, прибегая к реакции сульфирования ароматических ядер с помощью олеума, затем осуществляя нейтрализацию образовавшихся сульфогрупп с помощью соответствующего основного производного одного из металлов, который обозначает М в формуле (I). Полученный сырой сульфированный фосфин может содержать в смеси оксид соответствующего сульфированного фосфина, наличие которого, однако, не является помехой для осуществления способа гидроцианирования согласно настоящему изобретению.
Реакцию гидроцианирования обычно осуществляют при температуре 10 - 150oC, предпочтительно при 30 - 120oC.
Используемое количество никелевого соединения выбирают таким образом, чтобы на литр реакционного раствора содержалось 10-4 - 1, предпочтительно 0,005 - 0,5 моль никеля.
Количество фосфина формулы (I), используемое для приготовлен реакционного раствора, выбирают таким образом, чтобы число моль этого соединения, отнесенное к 1 моль элементного металла, составляло 0,5 - 2000, предпочтительно 2 - 300.
Кислота Льюиса, используемая в качестве сокатализатора, позволяет улучшать линейность получаемых динитрилов, т.е. процентное содержание линейного динитрила по отношению ко всей совокупности образовавшихся динитрилов, и/или увеличивать продолжительность срока службы катализатора.
Под кислотой Льюиса в настоящем тексте понимают, согласно обычному определению, соединения, являющиеся акцепторами электронных пар.
В частности, можно использовать кислоты Льюиса, цитированные в работе, изданной G.A. ALAH "Friedel - Crafts and related Reactions", т. 1, с. 191 - 197 (1963).
Кислоты Льюиса, которые могут быть использованы в качестве сокатализаторов в настоящем способе, выбирают среди соединений элементов групп Iб, IIб, IIIа, IIIб, IVa, IVб, Vа, Vб, VIб, VIIб, и VIII периодической системы элементов, соответственно тому, где вышеуказанные соединения по крайней мере частично растворимы и устойчивы в воде или преимущественно в водной фазе реакционной смеси. Чаще всего, но не ограничивающим объема охраны изобретения образом, эти соединения представляют собой соли, особенно галогениды, предпочтительно хлориды и бромиды, сульфаты, нитраты, сульфонаты, особенно трифторметансульфонаты, карбоксилаты, ацетилацетонаты, тетрафторбораты и фосфаты.
В качестве не ограничивающих объема охраны изобретения примеров таких кислот Льюиса можно назвать хлорид цинка, бромид цинка, иодид цинка, трифторметансульфонат цинка, ацетат цинка, нитрат цинка, тетрафторборат цинка, хлорид марганца, бромид марганца, хлорид никеля, бромид никеля, цианид никеля, ацетилацетонат никеля, хлорид кадмия, бромид кадмия, хлорид олова (II), бромид (II), сульфат олова (II), тартрат олова (II); хлориды, бромиды, сульфаты, нитраты, карбоксилаты или трифторметансульфонаты редкоземельных элементов, как лантан, церий, празеодим, неодим, самарий, европий, гадолиний, тербий, диспрозий, гольмий, эрбий, тулий, иттербий и лютеций; хлорид кобальта, хлорид железа-(II), хлорид иттрия.
Разумеется, можно использовать смеси нескольких кислот Льюиса.
В случае необходимости также представляет интерес стабилизация кислоты Льюиса в водном растворе путем добавления хлорида щелочного металла, как особенно хлорид лития или хлорид натрия. Молярное соотношение хлорида лития или хлорида натрия к кислоте Льюиса изменяется в очень широких пределах, например от 0 до 100, причем соотношение в отдельном случае может быть подобрано в зависимости от стабильности кислоты Льюиса в воде.
Из кислот Льюиса особенно предпочтительны хлорид цинка, бромид цинка, сульфат цинка, тетрафторборат цинка, хлорид олова (II), бромид олова (II), стабилизированный хлоридом лития хлорид олова (II), стабилизированный хлоридом натрия хлорид олова (II), смеси хлорида цинка с хлоридом олова (II), хлорид никеля, бромид никеля, ацетилацетонат никеля.
Используемый сокатализатор - кислота Льюиса - обычно составляет 0,01 - 50 моль на моль соединения переходного металла, преимущественно соединения никеля, и предпочтительно 1 - 10 моль на моль.
Используемый для гидроцианирования согласно изобретению каталитический раствор может быть получен перед его введением в зону реакции, например, путем добавления к водному раствору фосфина формулы (I) соответствующего количества выбранного соединения переходного металла, кислоты Льюиса и в случае необходимости восстановителя. Также можно получать каталитический раствор "in situ" простым смешиванием этих различных составляющих.
Хотя реакцию обычно проводят без гомогенизатора, может быть предпочтительным добавлением инертного органического растворителя, несмешивающегося с водой, который может быть растворителем для последующей экстракции.
В качестве примеров таких растворителей можно назвать ароматические, алифатические или циклоалифатические углеводороды, которые поддерживают в двухфазном состоянии реакционную среду.
Таким образом, с момента окончания реакции очень облегчается отделение, с одной стороны, водной фазы, содержащей сульфированный фосфин формулы (I), соединение переходного металла и кислоту Льюиса, и, с другой стороны, органической фазы, образованной вступающими в реакцию реагентами, продуктами реакции и в случае необходимости несмешивающимся с водой органическим растворителем.
Из органических растворителей, которые пригодны для использования в способе гидроцианирования, можно назвать бензол, толуол, ксилолы, гексан, циклогексан.
Способ изобретения можно осуществлять непрерывно или периодически.
Используемый циановодород может быть получен из цианидов металлов, особенно цианида натрия, или из циангидринов.
Циановодород вводят в реактор в газообразной или жидкой форме. Также можно его предварительно растворять в органическом растворителе.
В рамках периодического осуществления способа, на практике, в реактор, предварительно продутый с помощью инертного газа (такого, как азот, аргон), можно загружать либо водный раствор, содержащий всю совокупность или часть различных составляющих, таких как сульфированный фосфин, соединение переходного металла, возможные восстановитель и растворитель, кислота Льюиса, либо раздельно вышеуказанные составляющие. Обычно реактор затем доводят до выбранной температуры, после чего вводят пентен-нитрил. Затем вводят циановодород, предпочтительно непрерывным и регулируемым образом.
Когда реакция (которая может продолжать развиваться за счет добавления вышеуказанных составляющих) заканчивается, реакционную смесь после охлаждения извлекают и продукты реакции выделяют путем декантации, в случае необходимости с последующей экстракцией водного слоя с помощью соответствующего растворителя, такого как, например, несмешивающиеся с водой вышеуказанные растворители.
Водный каталитический раствор после этого можно рециркулировать в новую реакцию гидроцианирования.
В рамках непрерывного осуществления способа можно извлекать одну органическую фазу, тогда как водная каталитическая фаза остается в реакторе.
Следующие примеры иллюстрируют изобретение.
Пример 1.
1) Приготовление каталитического раствора Ni/TPPTS
В стеклянную колбу емкостью 1 л, снабженную магнитным стержнем и обратным холодильником, загружают 500 см3 раствора 300 ммоль натриевой соли трисульфированного трифенилфосфина (TPPTS) в воде; этот раствор дегазируют. Затем, при перемешивании и в токе аргона, вводят 20 г (73 ммоль) Ni (циклооктадиен)2, затем 350 см3 предварительно дегазированного орто-ксилола.
Нагревают при 45oC в течение 15 часов. После охлаждения двухфазную систему декантируют и сильно окрашенную в красный цвет водную фазу отделяют.
2) Гидроцианирование пент-3-ен-нитрила
В стеклянную колбу емкостью 150 см3, перемешивание в которой осуществляется с помощью турбины, загружают 34,8 см3 водного раствора катализатора Ni /TPPS, содержащего 5 ммоль никеля и 30 ммоль TPPTS. Нагревают при перемешивании до 60oC, затем, поддерживают эту температуру, последовательно инжектируют 3,2 см3 водного раствора, содержащего 20 ммоль хлорида цинка, 8 г (105 ммоль) пент-3-ен-нитрила (3PN).
Затем вводят циановодород по 1,8 г/час (67 ммоль/час) в течение 2-х часов.
По окончании опыта полученную реакционную смесь охлаждают, нейтрализуют с помощью концентрированного раствора гидроксида натрия возможный избыток введенного циановодорода и определяют количество составляющих путем газожидкостной хроматографии (ГЖХ).
Получают результаты:
степень превращения (TT) 3PN - 89%
выход (RT) адипонитрила (ADN) по отношению к превращенному 3PN - 66%
PT 2-метил-глутаронитрила (MGN) по отношению к превращенному 3PN - 26%
PT 2-этил-сукцинонитрила (ESN)по отношению к превращенному 3PN - 5%
PT валеронитрила (VN) по отношению к превращенному 3PN - 3%
линейность (*) - 68%
активность катализатора ** - 20
производительность в ADN (отнесенная к объему водной фазы) - 90 г/час, л
(*) образовавшийся ADN / образовавшиеся ADN + MGN + ESN
** число моль превращенного 3PN на моль введенного никеля
Примеры 2 - 5 и сравнительный опыт 1.
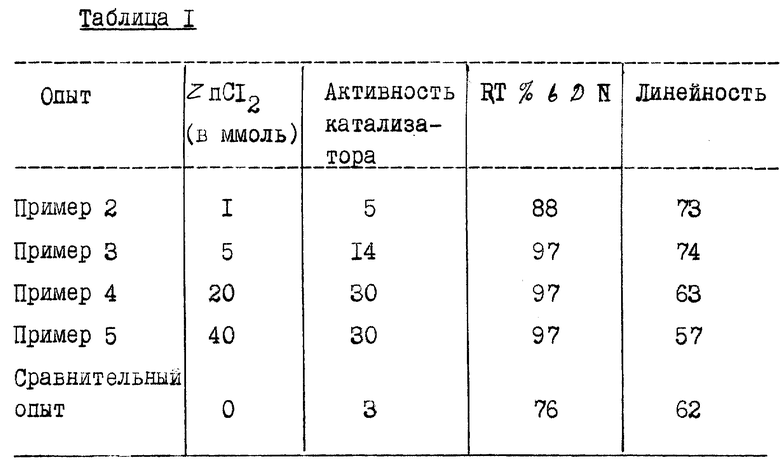
Повторяют пример 1 со следующими загрузками с условиями работы: Ni = 5 ммоль: TPPTS = 20 ммоль; ZnCl2 = см. таблицу 1; вода = до 38 мл; 3PN = 320 ммоль; скорость инжекции HCN = 68 ммоль/час; температура = 65oC.
В таблице 1 представлены полученные результаты (RT DN = выход ADN + MGN + ESN по отношению к превращенному 3PN).
Пример 6.
Повторяют пример 1 со следующими загрузками и условиями работы: Ni = 10 ммоль; TPPTS = 20 ммоль; ZnCl2 = 20 ммоль; воды = до 38 мл; 3PN = 320 ммоль; скорость инжекции НСП - 67 ммоль/час; температура = 65oC.
Получают следующие результаты:
RT в DN = 98%; активность катализатора = 15; линейность = 71%.
Примеры 7 и 8.
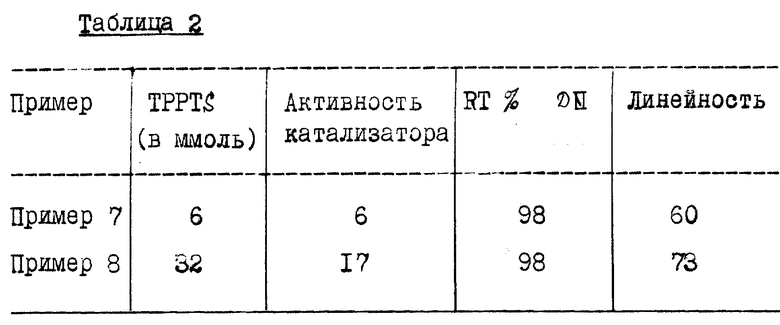
Повторяют пример 1 со следующими загрузками и условиями работы: Ni = 5 ммоль; TPPS = см. таблицу 2; ZnCl2 = 20 ммоль; вода = до 38 мл; 3PN = 320 ммоль; скорость инжекции HCN=67 ммоль/час; температура = 65oC.
Полученные результаты представлены в таблице 2.
Примеры 9 и 10.
Повторяют пример 1 со следующими загрузками и условиями работы: Ni = 5 ммоль; TPPS = 20 ммоль; ZnCl2 = 20 ммоль; вода = до 38 мл; 3PN = 320 ммоль; скорость инжекции HCN = см. таблицу 3; температура: см. таблицу 3.
В таблице 3 представлены полученные результаты (пример 4 также перенесен в таблицу 3).
Примеры 11 - 23.
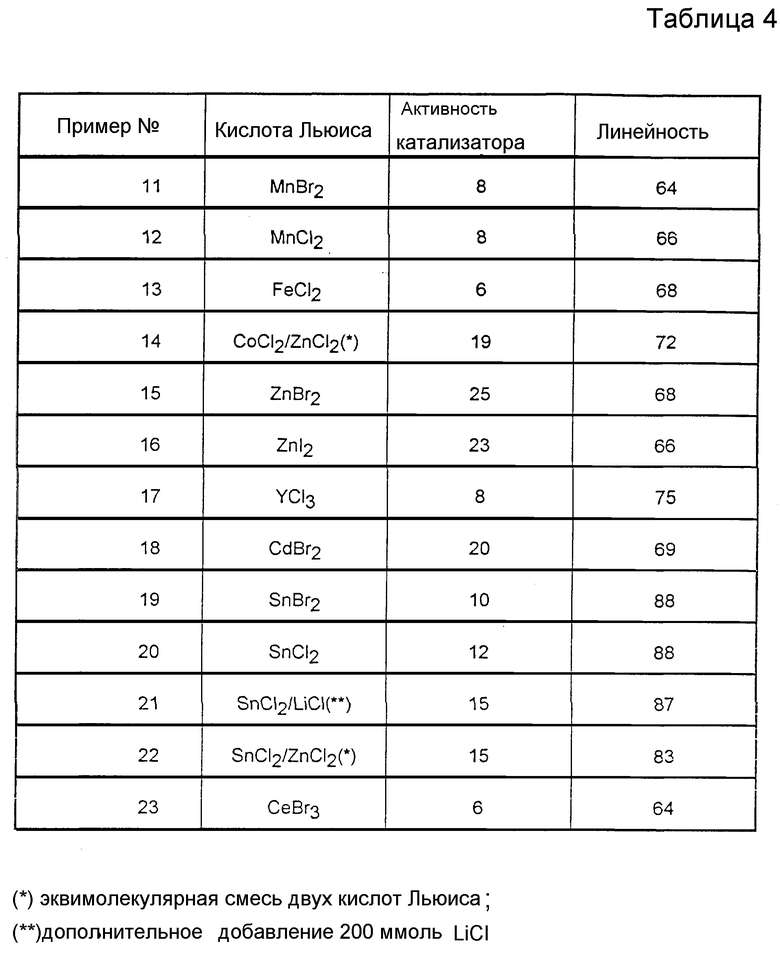
Повторяют пример 1 со следующими загрузками и условиями работы: Ni = 5 ммоль; TPPTS = 20 ммоль; кислота Льюиса (природы указанной в таблице 4) = 20 ммоль; вода = до 35 мл; 3PN = 200 ммоль; скорость инжекции HCN = 67 ммоль/час; температура = 65oC; продолжительность = 1 час.
Полученные результаты представлены в таблице 4.
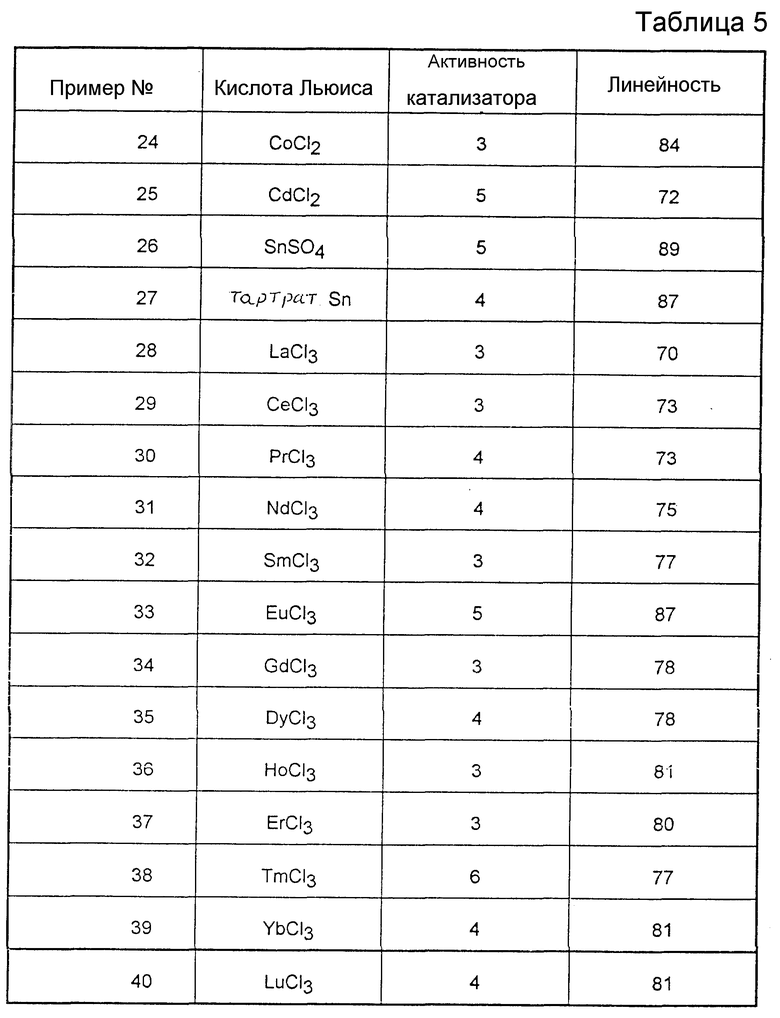
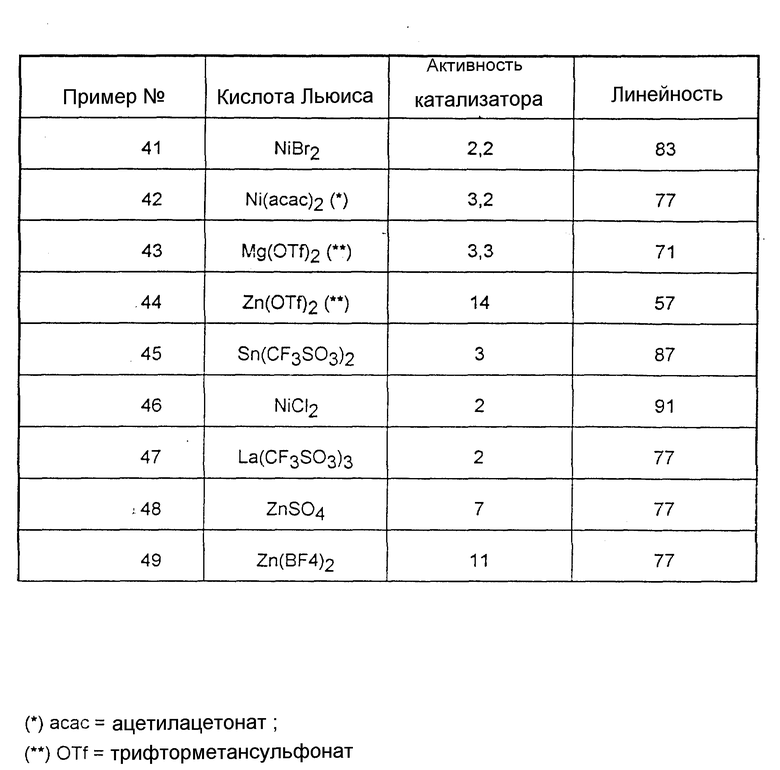
Примеры 24 - 49.
Повторяют пример 1 со следующими загрузками и условиями работы:
Ni = 5 ммоль; TPPTS = 20 ммоль; кислота Льюиса (природы, указанной в таблице 5) = 20 ммоль; вода = до 35 мл; 3PN = 200 ммоль; скорость инжекции HCN = 67 ммоль/час; температура = 65oC; продолжительность = 1 час.
Полученные результаты представлены в таблице 5.
Проведение процесса в присутствии восстановителя.
Этот прием является лишь вариантом способа изобретения. Катализатор в момент его использования содержит никель с нулевой степенью окисления и сульфированный трифенилфосфиновый лиганд.
Таким образом, имеется две следующие возможности:
либо приготовить катализатор из сульфированного трифенилфосфина и соединения никеля с нулевой степенью окисления (например, Ni - циклооктадиен);
либо приготовить катализатор из сульфированного трифенилфосфина и соединения никеля со степенью окисления 2, который восстанавливают ин ситу с помощью восстановителя.
Следовательно, каталитическая система является одной и той же, может меняться только способ ее приготовления.
Достигаемый в изобретении технический результат состоит в улучшении линейности получаемых продуктов и/или в увеличении срока службы катализатора, причем оба результата проиллюстрированы в описании.
Например, как видно из результатов таблицы 1, наблюдается увеличение линейности полученных продуктов по сравнению с продуктами, которые получены без кислоты Льюиса.
В примерах 4 и 5 достигаемая линейность равна или несколько ниже той, которая получена в сравнительном примере, однако продолжительность жизни катализатора выше в примерах осуществления изобретения. Так, показатель продолжительности жизни выражен в показателе "активность катализатора". Эта активность соответствует (как указано в примере 1) числу моль трансформированного пентеннитрила на моль введенного никеля. Чем выше продолжительность жизни катализатора, тем выше число, означающее его активность.
Следовательно, примеры описания показывают, что каталитическая система согласно изобретению имеет более продолжительный срок службы в отличие от катализатора уровня техники (без кислоты Льюиса).
Изобретение относится к улучшенному способу получения динитрилов. Описывается способ получения динитрилов путем гидроцианирования линейных пентеннитрилов, возможно содержащих незначительные количества других нитрилов, циановодородом в присутствии водного раствора катализатора, содержащего соединение никеля и сульфированного фосфина формулы I, где М - остаток катиона, выбираемого так, чтобы соединение формулы I было растворимо в воде; y1, y2, y3 - одинаковые или разные, выбираемые из группы; алкильный радикал с 1 - 4 атомами углерода, алкоксильный радикал с 1 - 4 атомами углерода, атом галогена; n1, n2, n3 - одинаковые или разные и равны 0 - 3, причем хотя бы один из них равен 1; m1, m2, m3 - одинаковые или разные числа, равные 0 - 3. Ar1, Ar2, Ar3 - фенил, заключающийся в том, что вышеуказанный раствор катализатора содержит по крайней мере одну киоту Льюиса. Технический эффект изобретения состоит в улучшении степени линейности целевого продукта и увеличении продолжительности срока службы катализатора. 16 з.п.ф-лы. 5 табл. 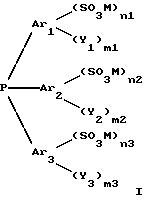

где M - остаток катиона, выбираемый так, чтобы соединение формулы I было растворимо в воде;
Y1, Y2, Y3 - одинаковые или разные, выбираемые из группы: алкильный радикал с 1 - 4 атомами углерода, алкоксильный радикал с 1 - 4 атомами углерода, атом галогена;
n1, n2, n3 - одинаковые или разные и равны 0 - 3, причем хотя бы одно из них равно 1;
m1, m2, m3 - одинаковые или разные числа, равные 0 - 3;
Ar1, Ar2, Ar3 - фенил,
отличающийся тем, что вышеуказанный раствор катализатора содержит по крайней мере одну кислоту Льюиса.
| US 4087452 А, 02.05.78 | |||
| Способ получения адипонитрила | 1977 |
|
SU677650A3 |
| US 4705881 А, 10.11.87 | |||
| US 3496217 А, 17.02.70. | |||
Авторы
Даты
1999-03-20—Публикация
1994-11-02—Подача