Изобретение относится к способу карбонилирования метанола или его реакционноспособного производного в присутствии галогенидного промотора и системы катализатора, включающей родиевый компонент и бидентантный фосфорно-серный лиганд. Настоящее изобретение также относится к новым родиевым комплексам.
Получение комплексов родия (I) и (II) с помощью смешанных серно-азотистых, фосфорных и мышьяковых лигандов описано H. A. Hodali и I.M. Kittaneh в Dirasat: Nat. Sci. (Univ. Jordan), 1983, 10, 47 - 55; CA., 1983, 101, 16218s.
Патент США N 4670570 раскрывает способ получения карбоновых кислот из спирта в присутствии системы катализаторов, включающей атом родиевого металла, фосфоросодержащий лиганд и галогенсодержащее соединение в качестве промотора. В соответствии с патентом США N 4670570, в фосфоросодержащем лиганде по крайней мере один атом кислорода (=O) присоединен к атому фосфора или атому углерода с образованием группы Z, и группа P = O или C = O в указанной группе Z расположена на удалении по крайней мере одного атома углерода и, предпочтительно, на удалении 2 - 4 атомов углерода от атома фосфора молекул, представленных с помощью формул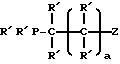
или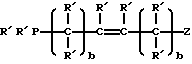
Говорится, что особенно предпочтительным лигандом является Ph2PCH2CH2P(= O)Ph2.
Международная заявка WO 92/04118 раскрывает новые предшественники катализаторов, имеющие фосфорно-азотный хелатный лиганд, присоединенный к металлу, причем данным металлом является, наиболее предпочтительно, Ph, Ni или Co. Хелатный лиганд включает в основном нереакционноспособную соединительную структуру основной цепи, которая соединяет два разных дативных центра, или донор, с анионным сайтом. В соответствии с международной заявкой WO 92/04118 предшественник катализатора имеет общую формулу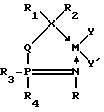
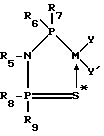
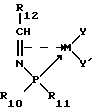
где M обозначает металл переходного ряда группы VIII B;
Y, Y' являются одинаковыми или разными и выбранными из CO, Cl-, фосфинов и олефиновых углеводородов;
R1-4, R6-12 являются одинаковыми или различными нереакционноспособными заместителями;
Q выбирают из (CH2)n, где n = 1 - 5, бензольного кольца, соединенного с P и X в о-положениях, олефина, соединяющего P и X посредством двойной связи, и (CH3)CH;
X обозначает P или As;
R обозначает замещенное ароматическое кольцо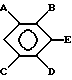
где A, B, C или D выбирают из F, H, NO2 и алкила и E обозначает эндоциклический азот или группу C-CN, либо ее изомер,
или R = SiMe3 или TiCl2Cp, где M обозначает метил или Cp обозначает циклопентадиен;
R5 обозначает арил или алкил; и
S* обозначает S, Se, O или N-R, причем R имеет вышеприведенные значения.
Среди характерных лигандов, приведенных в заявке WO 92/04118, находятся те, которые имеют общие формулы: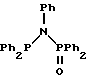
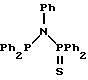
Предшественники катализаторов, описанные в заявке WO 92/04118, являются активными в качестве катализаторов в реакции карбонилирования метанола с образованием уксусной кислоты и ее производных, таких как метилацетат. Поскольку, в соответствии с заявкой WO 92/04118, способ осуществляют при температуре от 25oC до 200oC и давлении от 1 фунта на дюйм2 до 5000 фунтов на дюйм2 (0,07 кг/см2 - 351,6 кг/см2), предпочтительными условиями являются температура в диапазоне от 50oC до 120oC и давление в диапазоне от 40 до 400 фунтов на дюйм2 (2,812 - 28,12 кг/см2), и примеры даны только при температуре в диапазоне 80 - 90oC и давлении около 40 фунтов на дюйм2 (2,812 кг/см2).
Предшественники катализаторов, описанные в заявке WO 92/0411, не являются полностью удовлетворительными.
В соответствии с настоящим изобретением предлагается способ жидкофазного карбонилирования метанола или его реакционноспособного производного, который предусматривает взаимодействие окиси углерода с жидкой реакционной композицией, содержащей метанол или его реакционноспособное производное, галогенный промотор и систему родиевого катализатора, включающую родиевый компонент и бидентантный фосфорно-серный лиганд, причем лиганд содержит дативный центр фосфора, соединенный с дативным или анионным центром серы при помощи, в основном, нереакционноспособной структуры основной цепи, включающей два соединительных атома углерода или соединительный атом углерода и соединительный атом фосфора.
В одном предпочтительном варианте фосфорные и серные дативные центры или фосфорный дативный центр и анионный серный центр соединяются посредством двух соединительных атомов углерода в структуре основной цепи, причем данная структура основной цепи может включать неразветвленную гидрокарбильную группу -CH2-CH2-, разветвленную гидрокарбильную группу, такую как (CH3)CHCH2, или ненасыщенную гидрокарбильную группу, такую, как бензольное кольцо (необязательно замещенное некоординирующим заместителем, таким как -Si(CH3)3 или -CH3), соединенные в орто-положениях атомов фосфора и серы лиганда. Альтернативно, фосфорные и серные дативные центры или фосфорный дативный центр и анионный серный центр соединяются посредством соединительного атома углерода и соединительного атома фосфора в структуре основной цепи.
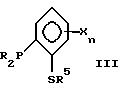
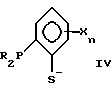
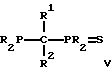
Предпочтительно, бидентатный фосфорно-серный лиганд имеет общую формулу I, II, III, IV или V: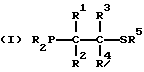
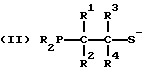
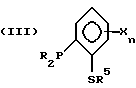
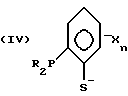
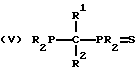
где значения R независимо выбирают из группы, состоящей из C1-C20-алкила, циклоалкила, арила, замещенного арила и необязательно замещенного аралкила;
значения R5 выбирают из группы, состоящей из C1-C20-алкила, циклоалкила, арила, замещенного арила, ацила и необязательно замещенного аралкила;
значения R1 - R4 независимо выбирают из группы, состоящей из водорода, C1-C20-алкила, необязательно замещенного аралкила;
X обозначает некоординирующий заместитель, такой как C1-C20-алкил, циклоалкил, арил, замещенный арил, C1-C20-алкокси, C1-C20-алкилтио, триалкилсилил или триарилсилил, предпочтительно Si(CH3)3 или метил;
n равно 0 - 4, предпочтительно 0 или 1.
Предпочтительно, значения R независимо выбирают из группы, состоящей из C1-C8-алкила, циклогексила, фенила и необязательно замещенного арила, а значения R5 выбирают из группы, состоящей из C1-C8-алкила, циклогексила, фенила, ацетила и бензила. Предпочтительно, значения R1-R4 независимо выбирают из водорода или C1-C8-алкила. Предпочтительно, когда n = 1, X обозначает -Si(CH3)3 в положении 6 или X обозначает -CH3 в положении 4.
Примерами предпочтительных лигандов являются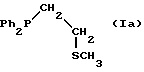
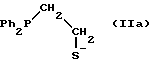
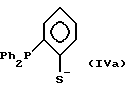
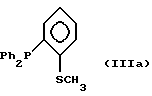
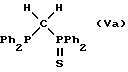
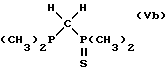
где Ph обозначает 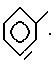
В способе настоящего изобретения реакционноспособные производные метанола включают диметиловый эфир, метилацетат и галоидметил, например, иодистый метил. Продуктами способа являются метилацетат и/или уксусная кислота. Предпочтительно, способ в соответствии с настоящим изобретением представляет собой способ карбонилирования метанола или его реакционноспособного производного с получением уксусной кислоты.
Способ настоящего изобретения пригодно осуществляют при температуре от 25oC до 250oC, предпочтительно от 50 до 250oC, более предпочтительно от 100 до 250oC, еще предпочтительнее от 135 до 250oC, и наиболее предпочтительно от 145 до 200oC.
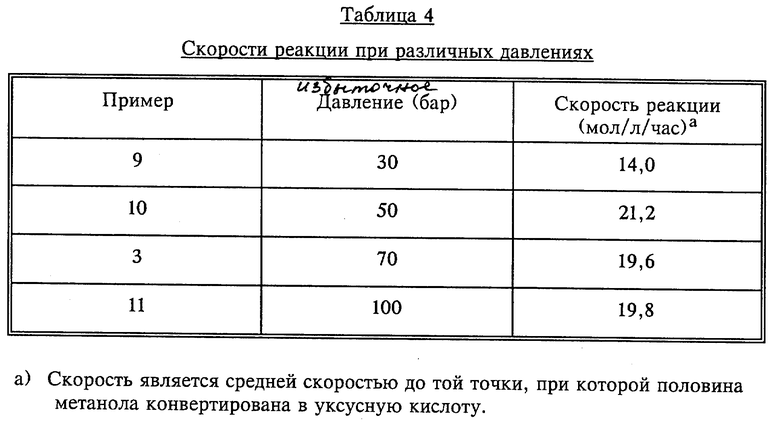
Способ настоящего изобретения пригодно осуществляют при избыточном давлении в диапазоне от 10 до 200 бар, предпочтительно от 20 до 200 бар, более предпочтительно от 30 до 200 бар, наиболее предпочтительно от 50 до 100 бар. Поскольку промотирующий эффект наиболее большой при наиболее высоких давлениях, экономические соображения могут диктовать давление, используемое промышленно.
Уксусная кислота может присутствовать в качестве растворителя в реакционной композиции в способе настоящего изобретения.
Вода может присутствовать в жидкой реакционной композиции способа настоящего изобретения, например, при концентрации в диапазоне от 0,1 до 20%, предпочтительно от 0,1 до 14 вес.% на основе полного веса жидкой реакционной композиции. Воду можно добавлять в жидкую реакционную композицию и/или можно образовывать in situ путем эстерификации метанола с помощью уксуснокислотного растворителя и/или уксуснокислотного реакционного продукта, присутствующего в жидкой реакционной композиции.
Родиевый компонент и бидентатный фосфорно-серный лиганд системы катализаторов можно добавлять в жидкую реакционную композицию настоящего изобретения в форме родиевого комплекса, в котором бидентатный фосфорносерный лиганд координирован с родием. Предпочтительно, родиевый компонент, имеющий замещаемые группы, предварительно смешан с бидентатным фосфорно-серным лигандом в пригодном инертном растворителе, например метаноле, перед прибавлением в жидкую реакционную композицию. По этой причине компонент RhIII может быть пригодным. При таких условиях родиевый компонент может быть добавлен в любой пригодной форме, например, в форме [Rh(CO)2Cl] 2, [Rh(CO)2I] 2, [Rh(Cod)Cl] 2, хлорида родия III, тригидрата хлористого родия III, бромида родия III, иодида родия III, ацетата родия III, дикарбонилацетилацетоната родия, RhCl(PPh3)3 и RhCl(CO)(PPh3)2.
Родиевый компонент системы катализаторов может присутствовать в жидкой реакционной композиции, например, при концентрации от 25 до 5000 частей на миллион родия, и молярном отношении родиевого компонента к бидентатному фосфорно-серному лиганду составляет диапазон от 1:0,5 до 1:4, предпочтительно при молярном отношении 1:1.
Предпочтительно галогенидный промотор представляет собой органическое соединение, содержащее йод, наиболее предпочтительно галогенидный промотор представляет собой иодистый алкил, предпочтительно иодистый метил. Концентрация йодистого алкила в жидкой реакционной композиции предпочтительно составляет от 1 до 30 вес.%, наиболее предпочтительно от 5 до 20 вес.%.
Также в соответствии с настоящим изобретением предлагается родиевый комплекс, имеющий формулу [Rh(CO)L]m или [Rh(CO)LY], где L обозначает бидентатный фосфорно-серный лиганд, имеющий общую формулу (II), (III), (IV) или (V), определенную выше, предпочтительно (IIa), (IIIa), (IVa), (Va) или (Vb); Y обозначает галоген, предпочтительно хлор, бром или иод; и m обозначает число меньше 10, обычно, по меньшей мере 2.
Изобретение теперь будет описано со ссылкой на следующие примеры, где Ph обозначает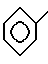
и Me - обозначает CH3-.
Все получения осуществляют в атмосфере азота, используя стандартные методики Schlenk. Растворители сушат перед использованием. Если не указано что-либо иное, то лиганды характеризуют с помощью 31P{1H} ЯМР-спектроскопии, а комплексы характеризуют с помощью 31P{1H} ЯМР, инфракрасной спектроскопии и микроскопического анализа, ЯМР-спектры регистрируют при температуре окружающей среды на спектрометре JEOL EX270 и сравнивают с 2H-синхронизирующим сигналом от растворителя с использованием Θp= 40480740 Гц (идеализированное значение для 85%-ного H3PO4): положительные сдвиги приведены ниже. Инфракрасные спектры регистрируют на спектрометре с преобразованием Фурье модели Perkin-Elmer 1600.
Получение лигандов
Лиганд моносульфид бис(дифенилфосфино)метана, то есть Ph2PCH2-P(S)Ph2 (Va), получают как описано D.E. Berry, J. Browning, K.R. Dizon и R.W. Hilts в Can. J. Chem. , 1988, 66, 1272. Лиганд 2-(дифенилфосфино)тиофенол 2-(Ph2P)C6H4(SH) получают по методу E. Block, G. Ofori-Okai и J. Zubieta, описанному в J. Am. Chem. Soc., 1989, 111, 2327. 31P{1H}-ЯМР (CDCl3): δp = -11,4 частей на миллион. Дифенил [2-(метилтио)фенил]фосфин: 31P(1H)-ЯМР (CDCl3): δp = -12,1 частей на миллион. Лиганды Ph2PCH2CH2P(= O)Ph2 и Ph2PCH2P(= O)Ph2 получают в соответствии с методом, описанным в заявке на Европейский патент 0072560. Трифенилфосфин и P(=S)Ph3 являются коммерческими веществами, которые получат из Aldrich.
Получение моносульфида бис(диметилфосфино)метана, Me2PCH2P(S)Me2, {Vb}
Раствор элементарной серы (0,848 г, 26,5 ммолей) в толуоле (70 см3) добавляют в течение 5 минут к раствору бис(диметилфосфино)метана (ex Strem; 3,6 г, 26,5 ммолей) в толуоле (60 см3) при температуре 0oC. Полученную смесь перемешивают в течение 30 минут при температуре 0oC и затем в течение 1 часа при комнатной температуре. Растворитель и непрореагировавший бис(диметилфосфино)метан удаляют при пониженном давлении с получением твердого вещества белого цвета (2,76 г), содержащего смесь Me2PCH2P(S)Me2 (60% выход на основе серы) и Me2(S)PCH2P(S)Me2 (40% выход).
Получение литий 2-(дифенилфосфино)этантиолата Ph2PCH2CH2(SLi)
Это получение заимствовано из методики, описанной J. R. Geigy в патенте Франции 1401930 и J. Chatt, J.R. Dilworth, J.A. Schmutz и J.A. Zubieta в J. Chem. Soc. Dalton Trans., 1979, 1595 - 1599. К раствору дифенилфосфина (ex Fluka; 0,134 см3, 0,144 г, 0,772 ммоля) в простом диэтиловом эфире (15 см3) добавляют бутиллитий (0,31 см3 2,5 М раствора в гексане) и раствор перемешивают в течение 30 минут при комнатной температуре. Затем добавляют этиленсульфид (0,46 см3, 0,109 г, 0,772 ммоля) и смесь перемешивают в течение 2 часов при комнатной температуре. Полученный эфирный раствор лития 2-(дифенилфосфино)этантиолата пригоден для получения комплексов аниона 2-(дифенилфосфино)этантиолата без дальнейшей обработки. 2-(Дифенилфосфино)этантиол:
31P(1H)-ЯМР (CDCl3): δp = -13,1 частей на миллион. [2-(Метилтио)этил] дифенилфосфин: 31P(1H)-ЯМР (CDCl3): δp = -13,4 частей на миллион.
Получение систем родиевых катализаторов
Получение [Rh(CO)LCl]; где L обозначает Ph2PCH2P(S)Ph2, {Va}
К раствору [Rh(CO)2Cl]2 (0,046 г, 0,118 ммоля) в метаноле (1,9 см3) добавляют суспензию Ph2PCH2P(S)Ph2 (0,099 г, 0,237 ммоля) в метаноле (1,9 мл). Растворитель удаляют из полученной смеси при пониженном давлении с получением твердого продукта оранжевого цвета (0,110 г, 80% выход).
Взаимодействие [Rh(CO2Cl]2 с Me2PCH2P(S)Me2, {Vb}
К раствору [Rh(CO)2Cl]2 (0,092 г, 0,237 ммоля) в метаноле (3,8 см3) при температуре 0oC добавляют раствор смеси Me2PCH2P(S)Me2 и Me2(S)PCH2P(S)Me2 (0,132 г с содержанием 0,474 ммоля Me2PCH2P(S)Me2, полученной, как описано выше, в метаноле (3,8 см3). Полученную смесь (преципитат желтого цвета в метаноле) используют непосредственно в качестве катализатора карбонилирования метанола.
Получение олигомера карбонилбис[P, μ -S)-2-(дифенилфосфино) бензол-тиолато]диродия (I) {[Rh(CO)L]m, где L обозначает 2-(Ph2P)C6H4(S-), IVa}
Смесь [Rh(CO)2Cl] 2 (0,15 г, 0,385 ммоля), 2-(дифенилфосфино)тиофенола (0,22 г. 0,747 ммоля), а также MeOLi (0,07 г, 1,6 ммоля) в метаноле (25 см3) кипятят с обратным холодильником в течение 30 минут. Полученный красновато-оранжевый преципитат продукта восстанавливают фильтрацией (0,287 г, выход 88%). Теперь предпочтительно перемешать реагенты в течение 30 минут при комнатной температуре вместо нагревания с обратным холодильником. C19H14OPRhS Mr = 424,26. Вычислено: C 53,79%, H 3,33%. Найдено: C 53,66%, H 3,43%. 31P(1H)-ЯМР (ацетон-d6): δp = +60,5 частей на миллион. (d, 1JPRh = 158 Гц). v(C ≡ O) = 1946 см-1 (Nujol mull).
Получение олигомера карбонилбис[(P, μ -S)-2-(дифенилфосфино)этантиолато] диродия (I) {[Rh(CO)L]m, где L обозначает Ph2PCH2CH2(S-), IIa}
К раствору литий 2-(дифенилфосфино)этантиолата (полученному, как описано выше) добавляют раствор [Rh(CO)2Cl]2 (0,15 г, 0,386 ммоля) в метаноле (10 см3) и полученную смесь перемешивают в течение 30 минут. Полученный оранжевый преципитат продукта восстанавливают фильтрацией (0,264 г, вход 91%). C15H14OPRhS Mr = 376,22. Вычислено: C 47,89%, H 3,75%. Найдено: C 48,01%, H 3,49%, 31P(1H)-ЯМР (ацетон-d6): δp = +63,7 частей на миллион. (d, 1JPRh = 158 Гц), v(C ≡ O) = 1947 см-1 (Nujol mull).
Получение хлорокарбонил [(P,S)-(дифенил)-{2-(метилтио)фенил}фосфин]родия (I) {[Rh(CO)LCl], где L обозначает 2-(Ph2P)C6H4(SMe), IIIa}
К раствору 2-(дифенилфосфино)тиофенола (0,227 г, 0,772 ммоля) в метаноле (25 см3) при температуре -20oC добавляют по каплям иодометан (0,048 см3, 0,109 г, 0,772 ммоля) в течение 15 минут. Раствор нагревают до комнатной температуры и добавляют раствор [Rh(CO)2Cl]2 (0,15 г, 0,386 ммоля) в метаноле (10 см3). Полученную смесь перемешивают в течение 2 часов и полученный бурый преципитат продукта восстанавливают фильтрацией (0,179 г, выход 49%). C20H17ClOPRhS Mr = 474,75. Вычислено: C 50,60%, H 3,61%. Найдено: C 50,88%, H 3,72%. 31P(1H)-ЯМР (CDCl3): δp = +70,3 частей на миллион. (d. 1JPRh = 158 Гц), v(C ≡ O) = 1998 см-1 (Nujol mull).
Получение хлорокарбонил [(P, S)-{2-(метилтил)этил}дифенилфосфин] родия (I) {[Rh(CO)LCl]; где L обозначает Ph2PCH2Ch2(SMe), Ia}
К раствору литий 2-(дифенилфосфино)этантиолата (полученному, как описано выше) добавляют по каплям иодометан (0,048 см3, 0,109 г, 0,772 ммоля) и смесь перемешивают в течение 2 часов. К этой смеси добавляют раствор [Rh(CO)2Cl] 2 ((0,15 г, 0,386 ммоля) в метаноле (15 см3) и полученную смесь перемешивают в течение 30 минут. Темно-бурый преципитат продукта восстанавливают фильтрацией (0,191 г, выход 58%). C16H17ClOPRhS Mr = 426,71. Вычислено: C 45,04%, H 4,02%. Найдено: C 44,26%, H 3,61%. 31P(1H)-ЯМР (CDCl3): δp = +72,7 частей на миллион. (d, 1JPRh = 162 Гц). v(C ≡ O) = 1984 см-1 (Nujol mull).
Общая методика карбонилирования метанола
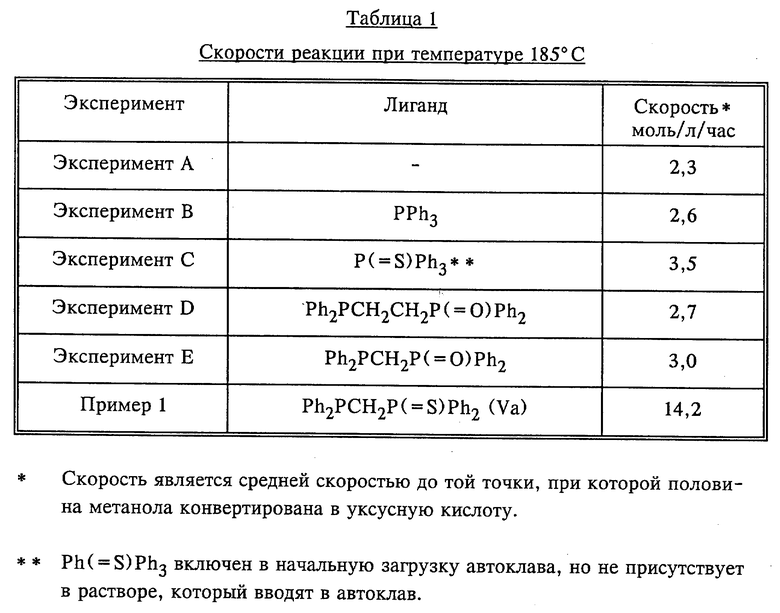
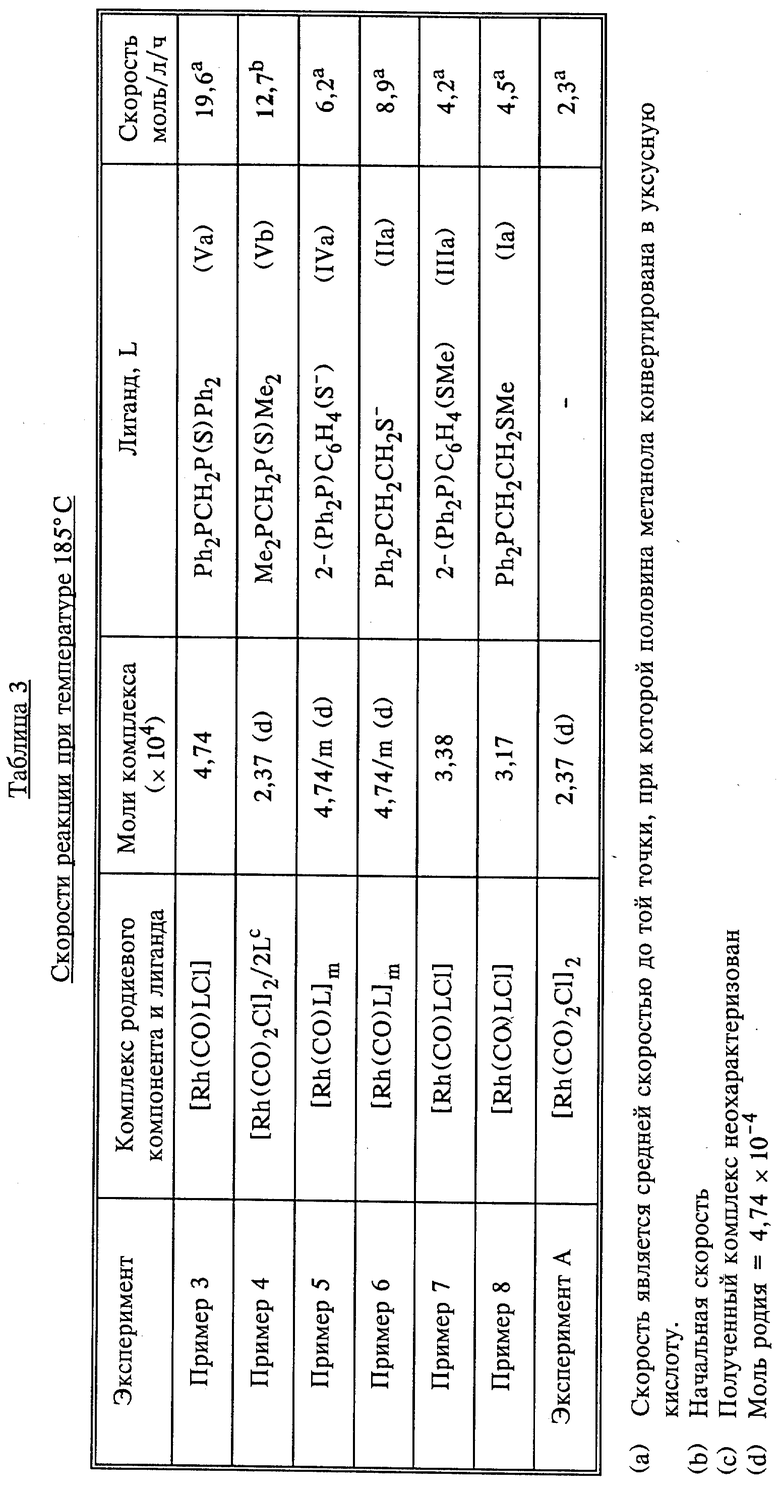
Метанол (22,69 г), уксусную кислоту (59,79 г) и метилиодид (6,84 г) загружают в автоклав Hastelloy B2 с объемом 150 см3, который снабжен смесителем Magnedrive (TM). Затем автоклав дважды промывают азотом и один раз окисью углерода. Реакционную смесь нагревают при начальном давлении 1 бар окиси углерода до желательной реакционной температуры с помощью электронагревающих катушек. Температуру реакционной смеси поддерживают в пределах 1oC от желательной реакционной температуры путем тщательного регулирования тепла, подаваемого на электронагревающие катушки. Используют быструю и постоянную скорость перемешивания (1000 об/мин). В первой серии экспериментов лиганд (1,89 • 10-3 молей) и [Rh(CO)2(Cl)]2 (0,092 г, 2,37 • 10-4 молей) частично или полностью растворяют в метаноле (5 г) (см. таблицы 1 и 2), и раствор или суспензию, в зависимости от конкретного случая, инъецируют в автоклав при одновременном повышении давления окиси углерода в автоклаве до избыточного давления, равного 70 бар. Во второй серии проводимых экспериментов родиевый комплекс (см. таблицу 3) инъецируют в автоклав в виде раствора или суспензии в метаноле (5 г) при одновременном повышении давления окиси углерода в автоклаве до избыточного давления, равного 70 бар. В обеих сериях проводимых экспериментов давление в автоклаве поддерживают за счет поглощения окиси углерода из балластного резервуара, и степень карбонилирования определяют путем измерения скорости потребления окиси углерода из балластного резервуара. К концу реакции, на что указывает поглощение окиси углерода, реакционную смесь охлаждают, автоклав вентилируют и пробу реакционной смеси анализируют газовой хроматографией, которая подтверждает образование уксусной кислоты в течение реакции. Результаты карбонилирования с использованием различных лигандов приведены в таблицах 1 - 3.
Результаты, приведенные в таблице 1, показывают, что при температуре 185oC скорость карбонилирования метанола в присутствии трифенилфосфина (лиганда третичного фосфина; Эксперимент B) только незначительно выше скорости в отсутствие фосфинового лиганда (Эксперимент A). Повышение скорости наблюдается в присутствии монодентатного лиганда на основе сульфида третичного фосфина, P(=S)PPh3, который используют в Эксперименте C. Данный лиганд также лучше по характеристикам в сравнении с лигандами на основе моноксида третичного бисфосфина, используемыми в Экспериментах D и E. Однако скорость реакции, полученная в соответствии с настоящим изобретением в присутствии Ph2PCH2P(= S)Ph2 (лиганда примера 1 на основе моносульфида третичного бисфосфина), в 6,2 раза выше той, которая получена в отсутствие фосфинового лиганда (Эксперимент A), и в 4,1 раза выше той, которая получена с использованием монодентатного лиганда на основе сульфида третичного фосфина, используемого в Эксперименте C. Более того, скорость карбонилирования, полученная в примере 1, в 4,7 раза выше той, которая получена в присутствии соответствующего моноксидного лиганда Ph2PCH2P(=O)Ph2 (Эксперимент E).
Результаты, приведенные в таблице 2, показывают, что при температуре 150oC скорость карбонилирования метанола в присутствии Ph2PCH2P(=S)Ph2 в 12,7 раз выше той, которая получена с использованием моноксидного лиганда Ph2PCH2P(=O)Ph2.
Результаты, приведенные в таблице 3, показывают, что при температуре 185oC, когда родиевый комплекс, имеющий бидентатный фосфорно-серный диганд, координированный с родием, загружают в автоклав (примеры 3 - 8), скорость карбонилирования метанола значительно выше скорости в Эксперименте A, когда в автоклав загружают [Rh(CO)2Cl] без бидентатного фосфорно-серного лиганда.
Эксперимент G
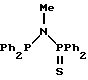
Эксперимент по карбонилированию осуществляют с использованием той же самой методики, которая описана для экспериментов в таблице 3, за исключением использования 0,474 ммоля [Rh(CO)LCl], где L обозначает Ph2PN(Ph)P(S)Ph2. Так, к раствору [Rh(CO)2Cl] 2 (0,092 г, 0,237 ммоля) в метаноле (3,8 см3) добавляют суспензию Ph2PN(Ph)P(S)Ph2 (0,233 г, 0,473 ммоля) в метаноле (3,8 см3). Лиганд Ph2PN(Ph)P(S)Ph2 получают в соответствии с методом M.S. Balakrishna et al., приведенным в Inorg. Chem., 1993, том 32, 5676 - 5681.
Полученную желтую суспензию 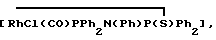 образованную в метаноле в течение 5 минут, используют непосредственно в качестве загрузки катализатора в эксперименте по карбонилированию. В данном эксперименте скорость крабонилирования (средняя скорость до той точки, при которой половина метанола конвертирована в уксусную кислоту) составляет 3,4 моль/л/час, что меньше скоростей для лигандов в соответствии с настоящим изобретением, приведенных в таблице 3. Использование Ph2PN(Ph)P(S)Ph2 в реакции карбонилирования описано в заявке PCT WO 92/04118. Это не является примером в соответствии с настоящим изобретением.
образованную в метаноле в течение 5 минут, используют непосредственно в качестве загрузки катализатора в эксперименте по карбонилированию. В данном эксперименте скорость крабонилирования (средняя скорость до той точки, при которой половина метанола конвертирована в уксусную кислоту) составляет 3,4 моль/л/час, что меньше скоростей для лигандов в соответствии с настоящим изобретением, приведенных в таблице 3. Использование Ph2PN(Ph)P(S)Ph2 в реакции карбонилирования описано в заявке PCT WO 92/04118. Это не является примером в соответствии с настоящим изобретением.
Примеры 9 - 11
Пример 3 повторяют при различных значениях давления и результаты данного эксперимента приведены в таблице 4.

Способ жидкофазного карбонирования метанола или его реакционноспособного производного включает взаимодействие окиси углерода с жидкой реакционной композицией, содержащей метанол или его реакционноспособное производное, галогенный промотор и родиевую каталитическую систему, содержащую родиевый компонент и бидентатный фосфорно-серный лиганд, причем лиганд содержит дативный центр фосфора, соединенный с дативным и анионным центром серы при помощи, в основном, нереакционноспособной структуры основной цепи, включающей два соединительных атома углерода или соединительный атом фосфора. Также предлагаются родиевые лигандные комплексы формулы [Rh(CO)L]m или [Rh(CO)LY], где Y обозначает галоген, m обозначает число меньше 10 и L выбирают из следующей группы бидентантных фосфорно-серных лигандов: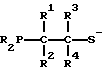
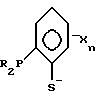
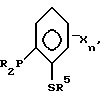
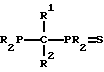
где значения R независимо выбирают из группы, состоящей из С1-С20-алкила, циклоалкила, арила, замещенного арила и необязательно замещенного аралкила; значения R5 выбирают из группы, состоящей из водорода, С1-С20-алкила, циклоалкила, арила, замещенного арила, ацила и необязательно замещенного аралкила; значения R1-R4 независимо выбирают из группы, состоящей из водорода, С1-С20-алкила и необязательно замещенного аралкила; Х обозначает С1-С20-алкил, циклоалкил, арил, замещенный арил, С1-С20-алкокси, С1-С20-алкилтио, триалкилсилил и n = 0-4. Новый тип катализаторов приводит к повышению скорости реакции и селективности процесса. 3 с. и 14 з.п. ф-лы, 4 табл.
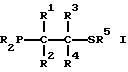
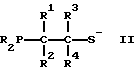
где значения R независимо выбирают из группы, состоящей из C1 - C20 алкила, циклоалкила, арила, замещенного арила и необязательно замещенного аралкила;
значения R5 выбирают из группы, состоящей из водорода, C1 - C20 алкила, циклоалкила, арила, замещенного арила, ацила и необязательно замещенного аралкила;
значения R1 - R4 независимо выбирают из группы, состоящей из водорода, C1 - C20 алкила и необязательно замещенного аралкила;
X обозначает C1 - C20 алкил, циклоалкил, необязательно замещенного арил, C1 - C20 алкоксил, C1 - C20 алкилтио, триалкилсилил или триарилсилил;
n = 0 - 4.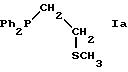
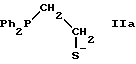
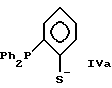
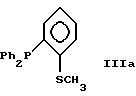
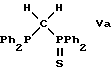
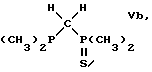
где Ph обозначает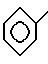
8. Способ по любому из предыдущих пунктов, отличающийся тем, что молярное соотношение родиевый компонент : бидентантный фосфорно-серный лиганд составляет от 1 : 0,5 до 1 : 4.
Приоритет по пунктам:
30.06.93 - по пп.1 - 11;
14.04.94 - по пп.12 - 16.
| Автоматический огнетушитель | 0 |
|
SU92A1 |
| US 4670570 A, 1986 | |||
| Способ получения уксусной кислоты и уксусного ангидрида | 1989 |
|
SU1766249A3 |
| DE 4034867 A, 1992 | |||
| НЕСУЩИЙ ВИНТ ВЕРТОЛЕТА | 1999 |
|
RU2146637C1 |
Авторы
Даты
1999-04-27—Публикация
1994-06-28—Подача