Настоящее изобретение относится к способам получения продуктов посредством удаления твердого замороженного растворителя из замороженной матричной смеси.
Сушка вымораживанием, т. е. лиофилизация, является хорошо известным способом сушки чувствительных к нагреванию материалов, чтобы защитить их от термического разрушения. В последнее время препараты, содержащие активные ингредиенты, такие как фармацевтические препараты, питательные вещества, диагностические средства, удобрения и инсектициды, получают сушкой вымораживанием водных растворов или суспензий, содержащие эти биоактивные ингредиенты. Обычные способы сушки вымораживанием или лиофилизацией включают замораживание материала при очень низкой температуре и последующую дегидратацию посредством сублимации в высоком вакууме.
Одной из проблем, которые возникают при применении обычного процесса сушки вымораживанием, является растрескивание высушенных вымораживанием препаратов. Как правило, растрескивание вызывается напряжениями, которые появляются при кристаллизации льда. Хотя растрескивание всегда является нежелательным, оно особенно нежелательно, когда используются капельные методы вымораживания. В таких случаях растрескивание замороженных капелек обычно дает в результате непригодные и неприглядные остатки растресканных капелек.
Другая проблема, с которой сталкиваются при применении известных способов сушки вымораживанием, представляет собой явление, называемое обратным оплавлением (meltback). Обратное оплавление происходит тогда, когда тепло, требуемое во время процесса сушки, оплавляет замороженный материал. Как таковое, обратное оплавление сводит на нет саму цель сушки вымораживанием для удаления воды посредством сублимации, в отличие от испарения. Чтобы избежать обратного оплавления при обычных способах сушки вымораживанием, одновременно можно сушить только ограниченное количество материала, или, с другой стороны, должны использоваться очень низкие температуры, в результате чего значительно растягивается время, требуемое для сублимации. Даже эти ограничения при обычных способах сушки вымораживанием не всегда оказываются достаточными для предотвращения оплавления.
Еще одной проблемой, свойственной общепринятым способам сушки вымораживанием, является отсутствие сопротивления потере целостности у высушенных вымораживанием веществ, т.е. они имеют очень низкую прочность. Как правило, при таких способах сушки вымораживанием получают продукты, которые крошатся при обращении с ними. При попытках решить эту проблему использовали различные способы сушки вымораживанием и упаковки. Например, патент США N 4305502 описывает способ формирования изделия определенной формы посредством процесса лиофилизации в углублении в листе пленочного материала. Однако при таких технических приемах упаковки не удается избежать проблем, связанных с общепринятыми способами сушки вымораживанием; таблетки по-прежнему рассыпаются, если переносятся в другую упаковку.
Что касается фармацевтических препаратов, то известные высушенные вымораживанием лекарственные формы не всегда обладают высокими скоростями растворения, когда вступают в соприкосновение с соответствующими растворителями, такими как вода, слюна или гастроинтестинальные жидкости. Быстрое растворение фармацевтических дозировочных форм может иметь решающее значение в случаях, когда желательно, чтобы фармацевтический препарат вошел в физиологическую систему как можно быстрее. Например, многие пациенты, особенно дети и старики, испытывают затруднения и дискомфорт при глотании твердых, плохо растворяющихся таблеток и капсул. С подобными трудностями сталкиваются и в ветеринарной практике, когда вводят орально фармацевтические препараты животным, которых лечат.
Разработаны различные способы сушки вымораживанием фармацевтических дозированных форм путем лиофилизации, чтобы обеспечить быстрое растворение дозированных форм. Патенты США NN 2166074, 3234091, 4371516 и 4302502, и патенты Соединенного Королевства NN 698767 и 1310824 все касаются высушенных вымораживанием дозированных форм, которые способны быстро растворяться. Кроме того, патент США N 4642093 предлагает процедуру приготовления высушенных вымораживанием (лиофилизованных) лекарственных форм в виде пены при использовании обычных технических приемов лиофилизации, что дает в результате быстро растворяющиеся фармацевтические дозированные формы.
В WO 91/09591 описан способ твердофазного растворения для удаления твердого растворителя (т.е. льда) из отвержденного (т.е. замороженного образца) с эталоном, таким образом удаляемым из твердой матрицы. Однако ни в описании, ни в примерах не описаны аминокислоты и их благоприятный вклад в конечный продукт. Еще одна проблема, присущая общепринятым способам лиофилизации, состоит в отсутствии однородной пористости лиофилизованного продукта. Однородная пористость в лиофилизованном продукте является критической величиной для последующего введения в дозировочную форму активного средства. Таким образом, существует потребность в способе получения дозировочной формы, который позволит избежать растрескивания и обратного оплавления, и придаст адекватную прочную пористость, и форма показывает высокую скорость растворения при приеме вовнутрь.
Задачей настоящего изобретения является создание усовершенствованной дозированной формы с более высокой прочностью, содержащей пористую сетку матричного материала, который быстро диспергируется в воде. Матричный материал составляют из по крайней мере 0,1 вес.% образующего матрицу средства, выбираемого из группы, состоящей из желатина, пектина, протеина соевого волокна и их смесей, и одной или нескольких аминокислот, содержащих от 2 до 12 атомов углерода. Предпочтительной аминокислотой является глицин, в то время как предпочтительным образующим матрицу веществом является желатин и/или пектин. В особенно предпочтительном варианте осуществления изобретения дозированная форма дополнительно включает маннит.
Дозированную форму образуют, подвергая раствор матричного материала лиофилизации или растворению в твердом состоянии. В предпочтительным вариантах осуществления настоящего изобретения раствор матричного материала, применяемого для формирования обладающей признаками изобретения дозированной формы, содержит от 0,1 вес.% до 15 вес.% матричного материала. Предпочтительно, раствор матричного материала включает от 0,1 вес.% до 3 вес.% образующего матрицу вещества, от 0,5 вес.% до 10 вес.% одной или нескольких аминокислот, и от 0,5 вес.% до 10 вес.% маннита.
Когда для образования твердой дозированной формы изобретения используют лиофилизацию, любое активное или биоактивное средство, содержащееся в дозированной форме, может присутствовать, что благоприятно в форме с покрытием. При таком варианте осуществления изобретения активное или биоактивное средство присутствует в форме частиц, и частицы средства покрыты соответствующим образующим покрытие средством /средствами/, чтобы защитить активное или биоактивное средство от действия растворителей, водной окружающей среды ротовой полости или другой полости со слизистой оболочкой, или условий окружающей среды, при которых растворялось бы или разрушалось упомянутое активное средство. Такие образующие покрытие материалы могут быть выбраны из природных или синтетических полимеров, которые по природе являются либо гидрофильными, либо гидрофобными, или других гидрофобных материалов, таких как жирные кислоты, глицериды, триглицериды и их смеси. Таким способом может быть приглушен вкус активного или биоактивного средства, причем в то же самое время создается возможность для быстрого растворения твердой дозированной формы при контакте с физиологическими растворителями. Примеры активных средств, на которые может быть нанесено покрытие, в соответствии с настоящим изобретением, включают ацетаминофен, ибупрофен, хлорфениламинмалеат, псевдоэфедрин и дектрометорфан.
Дозированные формы настоящего изобретения являются довольно крепкими по сравнению с дозированными формами известного уровня техники, особенно теми, которые получены лиофилизацией. Также дозировочные формы изобретения показывают значительно уменьшенную усадку или отсутствие ее в условиях высокой температуры или влажности - по сравнению с дозированными формами известного уровня техники, особенно теми, которые получены лиофилизацией. Дозированные формы изобретения быстро диспергируются в воде, например, менее чем за 10 секунд.
Дозированные формы, соответствующие настоящему изобретению, могут быть получены методом растворения в твердом состоянии при удалении твердого растворителя из отвержденных образцов. По этому способу одно или несколько взятых образующих матриц веществ /и, необязательно, образец, который переносится/ растворят или диспергируют в первом растворителе, отверждают, и затем вводят в контакт со вторым растворителем при температуре, равной или выше температуры точки отверждения второго растворителя, и при температуре, равной или ниже температуры точки отверждения первого растворителя. Первый растворитель в отвержденном состоянии, по существу, смешивается со вторым растворителем, в то время как образующее матрицу вещество /вещества/ /и образец, если присутствует/ по существу, не растворяются во втором растворителе. Первый растворитель посредством этого, по существу, удаляется из отвержденной матрицы, причем получается твердая матрица /необязательно содержащая образец/, по существу, не содержащая первого растворителя.
Или, одно или несколько образующих матрицу веществ /и, необязательно, образец, который переносится/ диспергируют или растворяют в первом растворителе, и затем отверждают единичный объем раствора или дисперсии. Отвержденный единичный объем вводят в контакт со вторым растворителем, как описано в предыдущем абзаце. По другому варианту, обработанная дозированная форма может контактировать с биоактивным агентом, чтобы получить дозированную форму, имеющую определенное количество диспергированного в ней биоактивного средства.
Другой целью настоящего изобретения является предложить систему твердых носителей для химических продуктов, с которой потребитель может добавлять их к среде для немедленного получения раствора или дисперсии нужной концентрации. И еще одной целью настоящего изобретения является предложить дозировочные формы, которые включают активные ингредиенты, такие как фармацевтические препараты, питательные вещества, удобрения и инсектициды.
Дозированные формы настоящего изобретения получают с минимальным растрескиванием или обратным оплавлением произведенного образца. Они быстро растворяются в соответствующих растворителях, имеют равномерную пористость и адекватную прочность при обращении с ними, т.е. устойчивость к нарушению целостности или разрушению в нормальных условиях производства и обращения с ними.
Дозировочные формы настоящего изобретения, и, в частности, формы, содержащие глицин в качестве одного из компонентов матрицы, обладают следующими преимуществами, быстро растворяются и рассыпаются, имеют приятный вкус и вызывают приятные ощущения во рту, имеют питательную ценность и низкую калорийность, и не обладают кариесогенностью. При фармацевтическом применении дозированные формы настоящего изобретения демонстрируют быстрое растворение при контакте с физиологическими растворителями, такими как вода, слюна или гастроинтестинальные жидкости. Следовательно, фармацевтические дозировочные формы настоящего изобретения обеспечивают быстрое распространение фармацевтического препарата в организме при приеме внутрь.
Дозированные формы настоящего изобретения для фармацевтического применения включают дозированные формы, обладающие мукоадгезивными свойствами или предназначенные для лекарственного средства при контролируемой норме; формы со стандартными дозами, предназначенные для подачи лекарственных средств в глаза, влагалище, ректальное отверстие и другие отверстия тела; твердые дозированные формы, предназначенные для замены жидких препаратов; сухие, содержащие лекарственные средства препараты для местного применения после рассасывания /восстановления/; получение содержащих лекарственные средства элементов или листов для местного применения; полученные более приятных на вкус дозированных форм лекарственных средств, которые обладают неприятными органолептическими свойствами; дозированные формы для перорального введения лекарственных средств людям, которые испытывают трудности при глотании таблеток или капсул.
Варианты осуществления настоящего изобретения могут быть использованы для различного применения. Применение в пищевой промышленности включает получение и доставку сухих продуктов, составленных из пищевых веществ; использование способа для селективной экстракции вещества в твердой форме в ходе процесса сушки; получение кондитерских изделий; приготовление дозирующих единиц для модификации свойств /например, вкуса, цвета и т.д./ или качества питьевой воды. Применение в ветеринарии включает приготовление стандартных доз для использования в ветеринарии; для приготовления аквариумных брикетов и кормов. В качестве применения в косметологии здесь можно упомянуть приготовление сухих систем для лечебного и косметического применения после рассасывания. Диагностическое применение включает фермент/кофакторы и системы биохимических носителей. Применение в санитарии представляет, например, приготовление стандартных единиц для очистки воды или получение ароматических элементов для личного применения, применения в доме и на производстве. Другие виды применения включают применение для составления носителей для красок и других художественных целей; применение для сельскохозяйственных продуктов и продуктов садоводства, требующих освобождения активного ингредиента в присутствии воды или дождя; применение для приготовления легко удаляемых формовочных или модельных материалов, или для получения легко удаляемых разделяющих и/или выравнивающих вспомогательных средств при конструировании или обработке.
Хотя следующее далее описание сосредоточивается на включении фармацевтических средств в качестве активных средств, следует понимать, что хорошие свойства способов изобретения и дозированных форм могут быть выгодно использованы в связи со многими различными типами активных агентов.
Прием растворения в твердом состоянии для получения матриц для доставки и дозированных форм начинается со смешения по крайней мере одного образующего матрицу вещества с первым растворителем. Эта смесь может быть водной по природе, и может содержать различные химические продукты, лекарственные средства и вспомогательные вещества в подходящем первом растворителе. Образующуюся в результате смесь охлаждения с регулируемой скоростью до полного отверждения, и затем погружают в подходящий второй растворитель при температуре ниже точки плавления первого растворителя. Отвержденный первый растворитель, по существу, растворяется во втором растворителе, и получают твердый продукт, по существу, свободный от первого растворителя, как матрицу и химические или лекарственные средства, присутствующие в исходной смеси. Оставшийся второй растворитель затем может быть удален испарением, чтобы выделить матрицы из ванны со вторым растворителем. С другой стороны, оставшийся второй растворитель может быть удален путем приведения в контакт образца с одним или несколькими дополнительными растворителями, имеющими большую летучесть, чем второй растворитель.
Различные ингредиенты, которые могут быть введены в начальную смесь, могут включать образующие матрицу агенты и вспомогательные компоненты. Образующие матрицу агенты, пригодные для применения в настоящем изобретении, включают материалы, которые происходят от животных или растительных протеинов, таких как желатины, декстрины, протеины семян сои, пшеницы и Psyllium смолы, такие как аравийская камедь, трепел /guar/, агар и ксантановая смола; полисахариды; альгинаты; карбоксиметилцеллюлозы; каррагинаны; декстрины; пектины; синтетические полимеры, также как поливинилпирролидон; и комплексы полипептидов с протеинанами или полисахаридами, такие как комплексы желатина с аравийской камедью.
Другие образующие матрицу материалы, пригодные для применения в настоящем изобретении, включают сахара, такие как маннит, декстроза, лактоза и галактоза; циклические сахара, такие как циклодекстрин; неорганические соли, такие как фосфат натрия, хлорид натрия и силикаты алюминия; и аминокислоты, содержащие от 2 до 12 атомов углерода, такие как глицин, L-аланин, L-аспаргиновая кислота, L-глутаминовая кислота, L-гидроксипропилин, L-изолейцин, L-лейцин и L-фенилаланин. Специалистам в этой области техники будет понятно, какие другие приемлемые образующие матрицу агенты могут быть использованы в настоящем изобретении.
Одно или несколько образующих матрицу средств могут быть включены в раствор или суспензию до отверждения. Образующий матрицу агент может присутствовать в дополнение к поверхностно-активной добавке или без нее. Кроме образования матрицы, образующей матрицу агент может способствовать сохранению дисперсии активного ингредиента в растворе или суспензии. Это особенно полезно в случае, когда активные ингредиенты недостаточно растворимы в воде, и должны быть, следовательно, скорее суспендированы, чем растворены.
В состав могут быть также введены вспомогательные компоненты, такие как консерванты, отдушки, антиокислители, поверхностно-активные вещества, загустители или красители. Другие вспомогательные компоненты включают активные или биоактивные средства, которые дозируют или доставляют. Такие активные средства могут включать фармацевтические препараты, питательные вещества, витамины, минеральные вещества, диагностические средства, удобрения и инсектициды. Примерами фармацевтических препаратов, которые могут быть включены в начальную смесь, являются малеат хлорфенирамина, псевдоэфедрин, детрометорфан, дигидрохлорид меклизина, галоперидол, альбутеролсульфат, дименгидринат и бензодиазепины, такие как диазепам, лоразепам и родственные им соединения. Однако, в сущности, любое фармацевтическое средство может быть использовано в связи с настоящим изобретением, и его любо добавляют к смеси, которую отверждают, либо фармацевтическое средство загружают впоследствии на предварительно сформированную матрицу с плацебо или дозированную форму.
Скорость, с которой растворяется образец, полученный по способу настоящего изобретения, в большой степени зависит от выбора образующего матрицу агента /агентов/ и их концентрации. В частности, дозированные формы размера, упомянутого в описанных далее примерах, будут достаточно быстро растворяться или диспергироваться, например, менее чем за 10 секунд или даже быстрее, например, менее чем за 5 секунд или даже меньше, например, около 3 секунд. Соединения /либо одно, либо в сочетании/, которые могут быть использованы в качестве образующего матрицу материала для получения плацебо или матриц, включают гидроэтилцеллюлозу, натрийкарбоксиметилцеллюлозу, микрокристаллическую целлюлозу, твердые кукурузные патоки, мальтрины /мальтодекстрины/, полидекстрины, пектины, каррагенаны, агар, хитозан, смолу лжеакации, ксантановую смолу, трагакант, гуаровую смолу, konjae муку, рисовую муку, клейковину пшеницы, натрийкрахмалгликолят, желатин /фармацевтического или пищевого качества/, протеин соевого волокна, картофельный протеин, папаин, пероксилазу ложечницу приморской, лицин, маннит, циклодекстрины /включая бета-циклодекстрин и гидроксипропил-бетациклодекстрин/, сахарозу, ксилит, галактозу, декстрозу, полигалактуроновую кислоту, алюмосиликат магния, трисиликат натрия или природные глины.
Предпочтительные образующие матрицу агенты включают желатины фармацевтического качества, пектины /нигидроизолированные, гидролизованные частично или гидролизованные/, глицин и маннит, либо в отдельности, либо в сочетании.
Еще одной стороной настоящего изобретения является предложение усовершенствованных твердых дозированных форм типа, содержащего пористую сетку из матричного материала, которая быстро расходится в воде, в частности, менее чем за десять секунд. Матричный материал в таких дозировочных формах состоит по крайней мере из 0,1 вес.% образующего матрицу агента, выбираемого из группы, состоящей из желатина, пектина, протеина волокна сои и их смесей, и из одной или нескольких аминокислот, содержащих от 2 до 12 атомов углерода. Последние аминокислоты включают, например, глицин, L-аланин, L-аспаргиновую кислоту, L-глутаминовую кислоту, L-гидроксипропилин, L-изолейцин, L-лейцин и L-фенилаланин.
Предпочтительное сочетание образующих матрицу агентов представляет собой сочетание желатина и одной или нескольких аминокислот, имеющих от 2 до 12 атомов углерода, особенно глицина. В таких сочетаниях аминокислота /аминокислоты/, относительно растворителя, применяемого для формирования матричного раствора, присутствуют в соотношении от 1 : 18 до 1 : 180, в частности, в соотношении от 1 : 30 до 1 : 100 по весу, относительно влажной основы. Такие матричные материалы могут содержать, кроме того, сахара, такие как маннит, декстроза, лактоза, галактоза, трегалоза, и циклические сахара, такие как циклодекстрины или замещенные циклодекстрины, в частности, маннит. Особенно предпочтительное сочетание образующих матрицу веществ включает желатин, глицин и маннит.
Раствор или суспензия, из которых получают дозировочные формы настоящего изобретения, могут также содержать вспомогательные компоненты, упомянутые выше, а также ксантановую смолу и полимеры акриловой кислоты и ее соли /называемые также карбомерами или карбоксивиниловыми полимерами, например, carbopolTM/, которые могут добавляться, например, для увеличения вязкости.
Соотношение материалов в этих сочетаниях может изменяться в некоторых пределах. В частности, отношение количества желатина, пектина или белка соевого волокна к количеству аминокислоты измеряется от 10 : до 1 : 5, в особенности - от 5 : 1 до 1 : 3, или, что более предпочтительно, - от 3 : 1 до 1 : 1. Предпочтительное соотношение представляет 1,5 : 1. Отношение количества маннита к желатину, пектину, протеину соевого волокна или к их смеси, находится в интервале от 5 : 1 до 1 : 5, в частности - от 2 : 1 до 1 : 2. Предпочтительное соотношение составляет 1,5 : 2.
Раствор или дисперсия веществ для получения матрицы содержит от 0,1 вес. % до 15 вес.% желатина, пектина, протеина соевого волокна или их смеси, в особенности - от 1% до 3%, предпочтительнее - от 1,2% до 2,5%. Они содержат, кроме того, от 0,1 вес.% до 10 вес.%, в частности - от 1 вес.% до 2,5 вес.%, аминокислоты, и от 0,1 вес.% до 10 вес.%, предпочтительно - от 1% до 3,0%, маннита, причем остальное составляет растворитель. Все проценты, упомянутые в этом абзаце, являются весовыми. Как правило, весовое отношение растворителя или дисперсионной среды к компонентам, не являющимся растворителем, составляет от 5 до 50, предпочтительно - от 10 до 30, например, 20.
В настоящем изобретении могут использоваться различные концентрации образующих матрицу агентов. Предпочтительные концентрации образующих матрицу агентов в подходящем растворителе составляет от 0,1 до 15% (вес/вес - в/в/). Более предпочтительными концентрациями являются концентрации от 0,5 до 4% (в/в). При фармацевтическом применении оптимальные результаты по способу настоящего изобретения получают, когда используют приблизительно 2% (вес/вес) водный раствор образующего матрицу агента.
Концентрации вспомогательных компонентов, включаемых в начальную смесь, ограничиваются, в первую очередь, растворимостью вспомогательного компонента /компонентов/ в растворителе, применяемом для растворения компонента. Требуемая концентрация определяется количеством агента, которое включают в дозировочную форму. Поэтому концентрации этих компонентов в начальных смесях могут изменяться в интервале от 0,0001 до 20%.
В настоящем изобретении могут использоваться различные растворители. В качестве первого растворителя должен быть выбран растворитель, который будет растворять и/или диспергировать образующие матрицу агенты и другие смешанные с ними агенты, входящие в образец. Кроме того, первый растворитель должен быть таким, чтобы его точка отверждения была выше точки отверждения второго растворителя. Предпочтительным первым растворителем является вода; другие подходящие в качестве первого растворителя растворители включат полиэтиленгликоли, карбоксиполиметилены, трет-бутиловый спирт, ацетонитрил, ацетамид и фенол. Первый растворитель может включать подходящее сочетание любых из этих растворителей, например, такое как растворяющая смесь воды и трет-бутилового спирта.
Второй растворитель должен действовать как хороший растворитель для отвержденного первого растворителя. Выгодно, когда растворяющий растворитель также имеет точку отверждения ниже точки отверждения первого растворителя. Требуемыми являются плацебо или дозированная форма, когда образец, по существу, сухой, и выгодно, чтобы второй растворитель имел относительно низкую точку кипения или относительно высокое давление паров, такое, что второй растворитель быстро испаряется из получаемого образца. Следовательно, предпочтительные вторые растворители будут иметь точки кипения или давление паров такие, что растворитель быстро испаряется при атмосферном давлении или при пониженном давлении. Предпочтительные вторые растворители для применения с водой в качестве первого растворителя включают вещества, которые смешиваются с водой. Такие вещества могут быть использованы в твердом, жидком или газообразном состоянии. Однако специалисты в этой области техники примут во внимание, что желательными могут быть твердые образцы формулировок, которые, в сущности, не являются сухими, но содержат значительные количества диспергированной в них жидкости. Следовательно, в качестве второго растворителя может быть использован растворитель, имеющий относительно высокую точку кипения, такой как, например, диметилформамид или этиленгликоль.
Является выгодным то, что компоненты дозировочной формы /образующие матрицу вещества и вспомогательные компоненты/ являются, по существу, нерастворимыми во втором растворителе, т.е., второй растворитель не будет растворять компоненты образца. Следовательно, в зависимости от этих компонентов, приемлемые вторые растворители включают метанол, этанол, ацетон, воду, изопропиловый спирт, метилизобутилкетон и жидкий диоксид углерода. Различные смеси этих растворителей могут составлять второй растворитель для настоящего изобретения. В настоящем изобретении могут быть использованы различные сочетания первого и второго растворителей. Предпочтительной системой первого и второго растворителей для фармацевтических целей является система вода : абсолютный этанол. С учетом компонентов образца, который получают, могут быть выбраны другие системы. Поэтому другие подходящие системы первого и второго растворителей, среди прочих, включают системы, содержащие трет-бутиловый спирт и воду, ацетамид и метанол, фенол и изобутилкетон и полиэтиленгликоль и спирт.
Смеси, которые отверждают, могут быть различными по форме. Они могут представлять собой растворы, суспензии, дисперсии, эмульсии или пены. Специалистам известны приемлемые способы получения каждой из них. Вспененный образец может быть получен путем диспергирования газа в жидкости. Предпочтительный способ получения такой пены описан в патенте США N 4642903.
Смесь может быть отверждена любым обычным способом охлаждения. Например, смесь может быть отверждена путем розлива в предварительно подготовленные формы и последующего охлаждения этих форм на полках холодильника или в морозильных камерах. С другой стороны, формы, содержащие смесь, могут быть пропущены, в трубе для замораживания, через поток холодного газа или пара, такого как жидкий азот. Предпочтительным способом отверждения смесей в формах являются обкладка форм сухим льдом до тех пор, пока смесь не отвердеет.
Альтернативным способом применения форм является отвержение капельным способом. Например, смесь может быть прокачена или подаваться под действием силы тяжести через отверстие, чтобы получить капли, шарики, или разбрызгиваться небольшими частицами. Эти капли затем могут быть отверждены при пропускании через холодный газ или жидкость, например, через жидкий азот или пары жидкого азота. Другая возможность состоит в том, что капли смеси могут быть отверждены в охлажденной жидкости, которая не смешивается со смесью. В таких случаях удельные плотности жидкости и смеси регулируются таким образом, чтобы капли могли либо проходить через охлажденную несмешивающуюся с ними жидкость, пока они отверждаются, или, напротив, отверждаемые капли могут плавать по поверхности охлажденной, несмешивающейся с ними жидкости. В последнем случае, при плавании по поверхности, облегчается сбор отвержденных капелек. Примером жидкости, которая может быть охлаждена, и которая не смешивается с большинством исходных водных смесей, является трихлорэтилен.
Полученную в результате отвержденную смесь вводят в контакт со вторым растворителем, за счет чего отвержденный первый растворитель растворяется во втором растворителе. Время контакта зависит от количества первого растворителя, который растворяют в твердой смеси. Это, в свою очередь, касается и объема отвержденной смеси. Требуемое время соотносится и с температурой второго растворителя.
Удобно, чтобы второй растворитель имел температуру, которая ниже точки отверждения первого растворителя. В случае использования системы вода : этанол температура второго растворителя может составлять от 0 до -100oС. Предпочтительной температурой для этой системы является температур от -4 до -20oС.
Для других систем предпочтительно, чтобы второй растворитель находился при температуре на 1-100oС ниже точки затвердевания первого растворителя. Более предпочтительной температурой для второго растворителя является температура на 4-20oС ниже точки затвердевания первого растворителя. При таких температурах количество второго растворителя, требуемое для растворения первого растворителя, должно составлять от 2 до 40 крат по отношению к общему весу несущей матрицы или дозировочных форм, которые получают.
Предпочтительный вес второго растворителя для применения при температуре на 10-20oС ниже температуры плавления первого растворителя, составляет 4-6-кратный общий вес дозировочной формы или матрицы, которые получают.
Предпочтительное количество этанола для применения при (-4oС) - (-20oС) в 20 раз превышает вес получаемых образцов. Например, чтобы получить 40 мл матрицы, следует использовать около 800 г этанола. При использовании таких предпочтительных температур и весовых количеств второго растворителя, время контакта матрицы со вторым растворителем составляет от 1 до 20 часов. Для системы вода : этанол предпочтительное время контакта составляет от 2 до 10 часов. При больших объемах необходимо большое время контакта. Такие предпочтительные времена контакта и температуры придают максимальную прочность и пористость обрабатываемой формулировке. Существуют различные способы осуществления контакта замороженного дозировочного элемента или матрицы со вторым растворителем. Такие способы включат погружение формулировки в ванну с растворителем и орошение формулировки растворителем. Предпочтительным способом контактирования отвержденной смеси со вторым растворителем является погружение.
Тесный контакт второго растворителя с дозировочной формой может быть обеспечен непрерывным или периодическим перемешиванием второго растворителя с образцом, или прокачиванием второго растворителя через сосуд, содержащий образец, с или без рециркуляции второго растворителя. С другой стороны, для облегчения растворения первого растворителя может быть использовано микроволновое воздействие.
Удаление полученного в результате обработанного образца или продукта из второго растворителя дает образец или дозированную форму, имеющие однородную пористость и высокое сопротивление разрушению. Продукт или препарат могут быть использованы сразу же, упакованы или сохранены.
С другой стороны, любое оставшееся количество второго растворителя может быть удалено при помещении продукта в вакуумную камеру при уменьшенном давлении, при выдержке летучего второго растворителя при атмосферном давлении при нормальной или повышенной температуре, или при пропускании струи воздуха или азота над образцом при нормальной или повышенной температуре с или без рециркуляции. При другом варианте, для содействия сушке могут быть использованы микроволны.
При другом варианте осуществления изобретения продукт может быть приведен в контакт с третьим растворителем, чтобы удалить оставшееся количество второго растворителя. Выгодно, когда третий растворитель представляет собой растворитель, имеющий большую летучесть, чем второй растворитель, так, что он будет легко испаряться из продукта. Этот третий растворитель преимущественно будет представлять собой растворитель, по существу, не смешивающийся с составляющими продуктами.
Препараты, содержащие такой агент, как химический продукт или лекарственное средство, которые не растворяются во втором, или растворяющем, растворителе, могут быть получены при непосредственном добавлении агента в дисперсию или в раствор, которые отверждают. Однако активные вещества, которые в значительной степени растворяются во втором растворителе, не следует добавлять в начальную смесь, так как некоторое количество такого химического продукта или лекарственного средства может быть потеряно при переходе во второй растворитель при растворении первого растворителя во втором растворителе. Поэтому, дозированные формы или матрицы, содержащие такие химические продукты или лекарственные средства, можно успешно получать, приготавливая сначала плацебо или чистую дозированную форму, и впоследствии вводя в контакт такую дозированную форму с определенным количеством активного средства в единице объема подходящего растворителя. Такие активные средства могут быть загружены или прибавлены к плацебо в виде раствора, суспензии, дисперсии или эмульсии вещества в растворителе-носителе, несмешивающемся с веществами плацебо. Таким образом, активное средство будет, по существу, распределяться в плацебо. Растворителю-носителю затем создают возможности для испарения при нормальном давлении и при нормальной или повышенной температуре, пропуская струю воздуха или азота над дозированной формой при нормальной или повышенной температуре, или помещая дозированную форму в вакуумную камеру при пониженном давлении и нормальной или повышенной температуре. При другом способе, для помощи при сушке могут быть использованы микроволны. С другой стороны, дозированная форма может быть помещена в вакуумную камеру для удаления оставшегося растворителя-носителя.
Активные средства, которые могут быть впоследствии нагружены на плацебо или чистую матрицу, включают вспомогательные компоненты, которые могут быть добавлены в начальную смесь, которую обрабатывают. Концентрация таких средств в растворе для последующей загрузки определяется количеством средства, требуемым в конечной обработанной дозировочной форме. Эти концентрации ограничиваются только растворимостью агента в растворителе для последующей загрузки, хотя в большинстве случаев предел растворимости может быть преодолен при использовании ряда последовательных загрузок и/или суспензий. Соответственно, концентрация активного средства может находиться в пределах от 0,0001% до 20% или более. Концентрация активного средства в конечной дозированной форме, полученной либо по этому способу, т.е., с последующей загрузкой, либо обычным предварительным смешением, связана с количеством активного средства, желательным для доставки в обработанной дозированной форме. Эта концентрация ограничивается растворимостью активного средства в растворе, хотя дозированные формы могут быть последовательно нагружены несколько раз, чтобы увеличить концентрацию до требуемого уровня. Кроме того, для последующей загрузки плацебо могут быть использованы суспензии агента /агентов/. Соответственно, концентрация активного средства в конечной матрице или дозированной форме может находится в интервале от менее 0,01 вес.% до более 300 вес.% от веса дозированной формы.
При применении настоящего изобретения могут быть получены дозированные формы самого разного объема, лежащего в интервале от 0,25 мл г до 30 мл или г и выше. Большие дозировочные формы могут быть успешно получены способом растворения в твердом состоянии, без длительной сушки, которая требуется при лиофилизации.
Когда применяют лиофилизацию, выгодно замораживать раствор вещества матрицы в формах, которые имеют покрытие или подкладку, чтобы легко удалять замороженное вещество. Предпочтительные формы делают из наполненного тальком полипропилена со слоем силикона или симетикона /simethicone/, сформированным горячей сушкой на поверхности /поверхностях/, контактирующих с раствором вещества матрицы.
Изобретение также иллюстрируется следующими далее примерами, которые не должны истолковываться, как ограничивающие объем и сущность изобретения конкретными процедурами, описанными в этих примерах.
Экспериментальная часть
Пример 1
Желатин /фармакопейный/ /15 г/, маннит /20 г/, аспартам /20 г/ и L-аланин /10 г/ растворяют в 935 г воды при постоянном перемешивании. Полученный в результат раствор аккуратно переносят в формы емкостью 1 г. Формы и их содержимое охлаждают сухим льдом в течение одного часа или быстро замораживают холодным газом в трубе для замораживания. Воду в состоянии льда удаляют подходящим способом /либо растворением в твердом состоянии, либо лиофилизацией/. Получают образец, т. е. сетку из несущего материала, которая быстро распадается когда принимается орально. Каждый из полученных образцов весит 65 мг. Этот процесс может быть повторен с заменой аланина на L-аспарагиновую кислоту, L-глутаминовую кислоту, L-гидроксипролин, L-лейцин, L-изолейцин и L-фенилаланин, либо на отдельное вещество, либо на их сочетание.
Пример 2
Состав А. Пектин /20 г/ растворяют в воде при нагревании и постоянном перемешивании. Полученный раствор помещают в автоклав при 121oС на 15 минут. Обработанному в автоклаве раствору затем дают возможность остыть до комнатной температуры. Обработанный в автоклаве раствор затем сушат подходящим способом. Высушенный, прошедший обработку в автоклаве пектин затем промывают этанолом. Промытый этанолом пектин фильтруют и сушат подходящим способом. Порошок промытого пектина используют в составе В.
Состав В. Высушенный, промытый этанолом пектин /12 г/, пектин /5 г/, маннит /20 г/, аспартам /5 г/ и L-аланин /20 г/ растворяют в 938 г очищенной воды при постоянном перемешивании. Полученный в результате раствор обрабатывают так, как описано в примере 1. Обработанный образец весит 62 мг и быстро растворяется в воде и во рту.
Пример 3
Маннит /20 г/, L-глутаминовую кислоту /25 г/ и аспартам /5 г/ растворяют в 942 г очищенной воды. В растворе диспергируют протеин соевого волокна /30 г/ и ксантановую смолу /0,5 г/. Полученную в результате дисперсию обрабатывают так, как описано в примере 1. Получают образец, т.е. сетку из несущего материала, которая быстро рассыпается - за одну-пять секунд - когда принимается через рот. Каждый из полученных образцов весит 58 мг.
Пример 4
Желатин /фармакопейный/ /15 г/, глицин /10 г/, маннит /20 г/, аспартам /13,3 г/, глутаминовую кислоту /2 г/, D&C желтый # 10 / 0,02 г/ и FD&C красный # 40 /0,02 г/ растворяют в очищенной воде /564,3 г/ при нагревании и постоянном перемешивании. Полученному в результате раствору дают возможность достичь комнатной температуры. К 624,6 г этого раствора при постоянном перемешивании добавляют 3 г высушенного распылением апельсина, 1 г натурального или искусственного подслащивателя и 11 г искусственной, с запахом малины, отдушки. Смесь перемешивают до тех пор, пока не получат однородную дисперсию.
Затем в душистой смеси суспендируют до однородного состояния тонкий порошок ацетаминофена, состоящий из активного ингредиента, инкапсулированного в гидрофобной оболочке на основе жирной кислоты /кислот/ или глицеридов. Полученную в результате суспензию переносят в формы емкостью 1,5 мл. Формы и их содержимое замораживанию в холодном газе в трубе для замораживания.
Воду в состоянии льда удаляют лиофилизацией. Получают образец, т.е. сетку из несущего материала, которая быстро распадается, когда принимается орально. Каждая из полученных единиц содержит 250 мг ацетаминофена.
Пример 5
Желатин /фармакопейный/ /15 г/, глицин /10 г/, маннит /20 г/, аспартам /13,3 г/, глутаминовую кислоту /2 г/, D&C желтый # 10 / 0,02 г/ и D&C зеленый # 5 /0,02 г/ растворяют в очищенной воде /597,9 г/ при нагревании и постоянном перемешивании. Полученному в результате раствору затем дают возможность достичь комнатной температуры. К 644,9 г этого раствора при постоянном перемешивании добавляют 7,5 г медово-лимонного lyptus и 1 г натуральной или искусственной отдушки. Смесь перемешивают до тех пор, пока не получат однородную дисперсию.
Тонкий порошок ибупрофена, состоящий из активного ингредиента, инкапсулированного в гидрофобной оболочке на основе жирной кислоты /кислот/ или глицеридов, затем суспендируют до однородного состояния в душистой смеси. Полученную в результате суспензию переносят в формы объемом 1,5 мл. Формы и их содержимое замораживают в холодном газе в трубе для замораживания.
Воду в состоянии льда удаляют лиофилизацией. Получают образец, т.е. сетку из несущего материала, которая быстро распадается, когда принимается орально. Каждая из полученных единиц содержит 200 мг ибупрофена.
Пример 6
Желатин /фармакопейный/ /15 г/, глицин /10 г/, маннит /20 г/, аспартам /13,3 г/, глутаминовую кислоту /2 г/, FD&C зеленый # 3 /0,01 г/, и FD&C красный # 40 /0,02 г/ растворяют в очищенной воде /761,7 г/ при нагревании и постоянном перемешивании. Полученному в результате раствору затем позволяют достичь комнатной температуры. К 822 г этого раствора при постоянном перемешивании добавляют 3 г искусственного виноградного и 1 г натурального или искусственного подслащивателя и отдушек. Смесь перемешивают до тех пор, пока не получат однородную дисперсию.
Затем в душистой смеси суспендируют до однородного состояния тонкий порошок гидрохлорида фенилпропаноламин и малеата хлорфенирамина, состоящего из активного ингредиента, инкапсулированного в гидрофобной оболочке на основе жирной кислоты /кислот/ или глицеридов. Полученную в результате суспензию переносят в формы объемом 0,5 мл. Формы и их содержимое замораживают в холодном газе в трубе для замораживания.
Воду в состоянии льда удаляют лиофилизацией. Получают образец, т.е. сетку из несущего материала, которая быстро распадается, когда принимается орально. Каждая из полученных единиц содержит 25 мг гидрохлдорида фенилпропаноламина и 4 мг малеата хлорфениламина.
Пример 7
Желатин /фармакопейный/ /15 г/, глицин /10 г/, маннит /20 г/, аспартам /13,3 г/, глутаминовую кислоту /2 г/ растворяют в очищенной воде /665,5 г/ при нагревании и постоянном перемешивании. Полученному в результате раствору затем позволяют достичь комнатной температуры. К 725,8 г этого раствора при постоянном перемешивании добавляют 5 г ментоловой отдушки. Смесь перемешивают до тех пор, пока не получат однородную дисперсию.
Затем в душистой смеси суспендируют до однородного состояния тонкий порошок гидрохлорида псевдоэфедрина, состоящего из активного ингредиента, инкапсулированного в оболочке на основе жирной кислоты /кислот/ или глицеридов. Полученную в результате суспензию переносят в формы объемом 1,5 мл. Формы и их содержимое затем замораживают в холодном газе в трубе для замораживания.
Воду в состоянии льда удаляют лиофилизацией. Получают образец, т.е. сетку из несущего материала, которая быстро распадается, когда принимается орально. Каждая из полученных единиц содержит 60 мг гидрохлорида псевдоэфедрина.
Испытания на прочность
1. Были проведены следующие испытания, чтобы оценить прочность единичной дозированной формы, полученной путем лиофилизацией в соответствии с настоящим изобретением, в сравнении с единичной дозированной формой, полученной с использованием метода твердофазного растворения.
2. Испытания проводили с использованием представленной ниже единичной дозированной лекарственной формы в весовых частях.
Ингредиент - Композиция
Желатин - 1,5
Маннит - 2
Глицин - 5
Аспартам - 0,5
Очищенная вода - 95
Композиция была переведена в единичную дозированную форму путем лиофилизации или в единичную дозированную форму путем твердофазного растворения.
3. После этого десять образцов каждой вышеописанной дозированной формы подвергали идентичному испытанию на пенетрацию, в котором металлический стержень известного веса опускали на верхнюю поверхность дозированной формы. Дозированные формы были расположены на 13-мм штамме. Все дозированные формы подвергали воздействию 145 граммов проникающего веса.
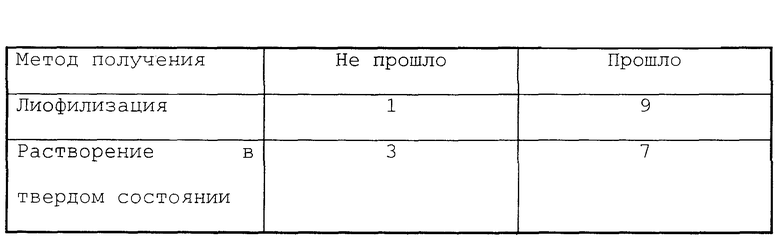
4. Во время испытаний на пенетрацию данная дозированная форма "не проходила", если она разбивалась на два или более куска при проникании. Данная дозированная форма "проходила", если после проникания она оставалась единым цельным куском. Для целей данного испытания центральная часть дозированной формы, которая могла быть выдавлена проникающим стержнем, не считается как отдельный отколотый кусок. Таким образом, "прошедшая" испытание проникающем дозированная форма могла тем не менее иметь выдавленный центр и/или единственную трещину от центру к периметру, так как это все еще является единым цельным куском.
5. Результаты испытаний на пенетрацию представлены в таблице. Для каждой конкретной дозированной формы приведено число "неудач", определенное выше.
6. На основании данных, проведенных испытаний сделан вывод, что единичные дозированные формы, содержащие глицин, полученные лиофилизацией, прочнее, чем полученные твердофазным растворением.
| название | год | авторы | номер документа |
|---|---|---|---|
| УЛУЧШЕННЫЕ ГОТОВЫЕ ЛЕКАРСТВЕННЫЕ ФОРМЫ, СОДЕРЖАЩИЕ ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ИМИДАЗОЛА | 2003 |
|
RU2349305C2 |
| БЫСТРОДИСПЕРГИРУЮЩАЯСЯ ЛЕКАРСТВЕННАЯ ФОРМА, НЕ СОДЕРЖАЩАЯ ЖЕЛАТИН | 2000 |
|
RU2242968C2 |
| ЛИОФИЛИЗИРОВАННЫЕ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ ДЛЯ ВАГИНАЛЬНОЙ ДОСТАВКИ | 2017 |
|
RU2753864C2 |
| БЫСТРО ДИСПЕРГИРУЕМЫЕ ЛЕКАРСТВЕННЫЕ ФОРМЫ, СОДЕРЖАЩИЕ РЫБИЙ ЖЕЛАТИН | 2000 |
|
RU2242969C2 |
| ЛИОФИЛИЗАТ НА ОСНОВЕ ПЕПТИДА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1994 |
|
RU2145234C1 |
| СПОСОБ СТАБИЛИЗАЦИИ ПОЛИПЕПТИДА, СПОСОБЫ ПОЛУЧЕНИЯ КОМПОЗИЦИЙ ПОЛИПЕПТИДА И КОМПОЗИЦИИ | 1994 |
|
RU2143889C1 |
| ДИСПЕРГИРУЕМЫЕ СТАБИЛИЗИРОВАННЫЕ ФОСФОЛИПИДОМ МИКРОЧАСТИЦЫ | 1999 |
|
RU2233654C2 |
| ТВЕРДЫЕ ИЛИ ПОЛУЖИДКИЕ ДОЗИРОВАННЫЕ ФОРМЫ С МОДИФИЦИРОВАННЫМ ВЫСВОБОЖДЕНИЕМ | 2008 |
|
RU2471480C2 |
| КОМПОЗИЦИИ И СПОСОБЫ УЛУЧШЕНИЯ ПЕРОРАЛЬНОГО ВСАСЫВАНИЯ ПРОТИВОМИКРОБНЫХ СРЕДСТВ | 2001 |
|
RU2282462C2 |
| БЫСТРОРАСТВОРИМАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2011 |
|
RU2566270C2 |
Изобретение относится к медицине. Твердая дозированная форма включает пористую сетчатую структуру матричного материала, быстродиспергируемого в воде. Форма выполнена из раствора, содержащего от 0,1 до 15 вес.% агента, образующего матрицу. Агент выбран из группы, состоящей из желатина, пектина, белка соевого волокна и их смесей и включает одну или несколько аминокислот, содержащих от 2 до 12 атомов углерода. Форма получена лиофилизацией указанного раствора матричного агента. Количественное соотношение желатина, пектина, белка соевого волокна или их смесей и аминокислоты находится в интервале от 10:1 до 1:5. Аминокислотой является глицин, L-аспарагиновая кислота, L-глутаминовая кислота, L-гидроксипролин, L-изолейцин, L-лейцин и L-фенилаланин. Форма может дополнительно включать активный ингредиент в форме частиц с покрытием. Покрывающим агентом является жирная кислота, глицерид, триглицерид или их смесь. Новая усовершенствованная дозированная форма диспергируется в воде менее чем за 10 с и имеет высокую прочность. 14 з.п.ф-лы, 1 табл.
| Огнетушитель | 0 |
|
SU91A1 |
| Криостат | 1971 |
|
SU450141A1 |
| US 4946684 A, 07.08.90 | |||
| US 5045565 A, 03.09.91. | |||
Авторы
Даты
1999-06-10—Публикация
1993-05-03—Подача