Данное изобретение относится к до сих пор неизвестному классу соединений, который проявляет противовоспалительные и иммуномодулирующие эффекты, также как и сильную активность при индуцировании дифференциации и ингибировании нежелательной пролиферации определенных клеток, включая раковые клетки и клетки кожи, к фармацевтическим композициям, содержащим эти соединения, к единичным дозировкам таких композиций и к их использованию при лечении и профилактике увеличения щитовидной железы, в частности вторичного увеличения щитовидной железы, связанного с почечной недостаточностью, ряда болезненных состояний, включающих сахарный диабет, повышенное давление, воспаление сальных желез, облысения, старения кожи, дисбаланса иммунной системы, воспалительных заболеваний, таких как ревматоидный артрит и астма, болезней, характеризующихся ненормальной клеточной дифференциацией и/или клеточной пролиферацией, таких как, например, псориаз и рак, для предотвращения стероидно индуцированной атрофии кожи, и для способствования остеогенезу и лечения остеопороза.
Соединения данного изобретения представлены общей формулой I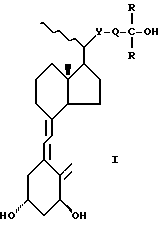
где Y является серой, S(O) или S(O)2; R обозначает C1-C3 алкил; или 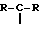 может образовывать C3-C8-членное карбоциклическое кольцо; Q является C1-C8 гидрокарбиленовым бирадикалом.
может образовывать C3-C8-членное карбоциклическое кольцо; Q является C1-C8 гидрокарбиленовым бирадикалом.
В контексте данного изобретения выражение гидрокарбиленовый бирадикал означает остаток после удаления двух атомов водорода из прямого, разветвленного или циклического, насыщенного или ненасыщенного углеводорода.
Значения R включают, но не ограничены ими, метил, трифторметил, этил, нормальный и изопропил.
Значения Q включают, но не ограничены ими, метилен, этилен, три-, тетра- и пентаметилен, -CH=CH-, -CH2-CH=CH-, -CH2CH2-CH=CH-, -CH2-C≡C-, -CH2CH2-C≡C-, фенилен (C6H4; орто, мета, пара), -CH2-(C6H4)-(орто, мета, пара) и -(C6H4)-CH2-(орто, мета, пара).
Соединения данного изобретения могут иметь более одной стереизомерной формы (например, 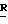 или
или 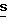 конфигурацию при C-20;
конфигурацию при C-20;  или
или  конфигурацию, когда присутствует двойная связь в группе Q). Объем изобретения охватывает все эти стереизомеры в чистой форме и их смеси. Кроме того, лекарства-предшественники I, в которых одна или более гидроксигруппы замещены группами, которые могут быть преобразованы в гидроксигруппы in vivo, находятся также в рамках данного изобретения.
конфигурацию, когда присутствует двойная связь в группе Q). Объем изобретения охватывает все эти стереизомеры в чистой форме и их смеси. Кроме того, лекарства-предшественники I, в которых одна или более гидроксигруппы замещены группами, которые могут быть преобразованы в гидроксигруппы in vivo, находятся также в рамках данного изобретения.
Показано, что 1α, 25-дигидрокси-витамин D3 (1,25 (OH)2D3) влияет на действия и/или производство интерлейкинов (Muller K et al., Immunol. Lett. 17, 361-366 (1988)), указывая на возможное использование этого соединения при лечении болезней, характеризуемых дисфункцией иммунной системы, например аутоиммунных болезней, СПИДа, индивидуальной реакции на прививки, и отторжения трансплантатов, или других состояний, характеризуемых ненормальным производством интерлейкина-1, например воспалительных болезней, таких как ревматоидный артрит и астма.
Показано также, что 1,25 (OH)2D3 способен стимулировать дифференциацию клеток и ингибировать избыточную клеточную пролиферацию (Abe E. et al., Proc. Natl. Acad. Sci., USA, 78, 4990-4994 (1981)), и было предположено, что это соединение могло бы быть полезным при лечении болезней, характеризуемых ненормальной клеточной пролиферацией и/или клеточной дифференциацией, таких как лейкемия, миелофиброз и псориаз.
Также предложено использование 1,25 (OH)2D3 или его лекарства-предшественника 1 α - OHD3 для лечения повышенного давления (Lind L. et al., Acta Med. Scand. 222, 423-427 (1987)) и сахарного диабета (Inomata S. et al., Bone Mineral 1, 187-192 (1986)). Другое показание для 1,25 (OH)2D3 предложено после недавнего наблюдения связи между врожденной устойчивостью к витамину D и облысением: лечение 1,25 (OH)2D3 может способствовать росту волос (Editorial, Lancet, March 4, p. 478 (1989)). Также, тот факт, что местное нанесение 1,25 (OH)2D3 уменьшает размер сальных желез в ушах самцов сирийских хомяков, дает возможность предположить, что это соединение могло бы быть полезным для лечения воспаления сальных желез (Malloy, V.L. et al., the Tricontinental Meeting for Investigative Dermatology, Washington, (1989).
Однако, терапевтические возможности при таких показаниях 1,25 (OH)2D3 являются жестко ограниченными хорошо известным сильным влиянием этого гормона на метаболизм кальция; повышенные концентрации в крови быстро вызывают гиперкальцемию. Таким образом, это соединение и некоторые из его сильнодействующих синтетических аналогов не являются полностью удовлетворительными для использования в качестве лекарств при лечении, например, псориаза, лейкемии или иммунных болезней, которые могут потребовать непрерывного приема лекарства в относительно высоких дозах.
В последнее время описано ряд аналогов витамина D, которые проявляют определенную степень селективности в отношении активности индуцирования клеточной дифференциации/ингибирования клеточной пролиферации по сравнению с влиянием на метаболизм кальция.
Последние исследования (Colston, K.W. et al., Biochem. Pharmacol. 44, 693-702 (1992)) поддерживают концепцию, что производные витамина D могут ингибировать пролиферацию клеток рака груди in vivo. Описаны возможные иммунологические свойства аналогов витамина D (Binderup. L. Biochem. Pharmacol. 43 1885-1892 (1992)).
Известен ряд тиа-аналогов витамина D. Описаны 23-тиа-аналоги (Kubodera, N. et al., Chem. Pharm. Bull. 39, 3221-3221 (1991) и заявка на Европейский патент номер 78704), и ряд 20R-23-тиа-аналогов опубликован в заявке на Международный патент N PCT/DK 91/00091, дата регистрации 22 марта 1991, публикация N WO 91/15475.
Далее, описан ряд 22-окса-аналогов витамина D (Murayma, E. et al., Chem. Pharm. Bull. 34, 4410-4413 (1986), Abe, J. et al., FEBS LETTERS 226, 58-62 (1987), заявка на Европейский патент N 184 112, Binderup, L. et al., Biochem. Pharmacol. 42, 1569-1575 (1991), заявка на Международный патент N PCT/DK 90/00036, дата регистрации 13 февраля 1990, публикация N 90/09991).
Тот факт, что существуют только малые структурные различия между соединениями, известными из литературы, упоминаемый выше, но большой разброс в их биологических активностях (сравни Binderup, L. et al., Biochem. Pharmacol. 42, 1569-1575 (1991)), предполагает, что настоящее состояние знаний не дает возможности предсказывать структуру аналогов витамина D, которые будут проявлять благоприятную степень селективности, отражающуюся в более высокой активности по отношению к дифференциации клеток in vitro, по сравнению со способностью к связыванию кишечными рецепторами витамина D in vitro. Более того, вопрос усложняется тем фактом, что способность к связыванию рецепторами in vitro не всегда аналогична той, которая обнаружена в исследованиях in vivo, вероятно отражая фармакокинетическое различие между соединениями.
Соединениями данного изобретения являются 22-тиа-аналоги витамина D, отличающиеся структурно от любых аналогов витамина D. Аналоги как с 20S, так и с 22R конфигурацией получают по способам данного изобретения. Эти соединения являются в высшей степени активными и проявляют отличную селективность. Так в частности, обнаружено, что соединения формулы I, имеют одно или более следующих преимуществ по сравнению с литературными данными, приведенными выше:
a) более сильное влияние на клеточную дифференциацию/пролиферацию;
b) более высокая селективность по отношению к сильному воздействию на клеточную дифференциацию/пролиферацию по сравнению с влиянием на метаболизм кальция;
c) более сильное воздействие на производство и действие интерлейкинов;
d) более высокая селективность в отношении влияния на производство и действие интерлейкина по сравнению с влиянием на метаболизм кальция;
e) более длительное время метаболического полураспада.
Соединения данного изобретения являются, следовательно, особенно пригодными для использования как для локального, так и для системного лечения и профилактики расстройств у человека и животных, которые характеризуются ненормальной клеточной пролиферацией и/или клеточной дифференциацией, таких как определенные дерматологические расстройства, включая псориаз и определенные формы рака, и/или дисбалансом иммунной системы, например при аутоиммунных болезнях, включая сахарный диабет, индивидуальную реакцию на прививку и отторжение трансплантантов. Соединения данного изобретения являются также пригодными для использования при лечении воспалительных заболеваний, таких как ревматоидный артрит и астма. Воспаление сальных желез, облысение и гипертония являются другими состояниями, которые могут лечиться соединениями данного изобретения. Наконец, поскольку после местного применения соединений данного изобретения наблюдается утолщение кожи, эти соединения могут быть пригодны для использования при лечении или предотвращении старения кожи, включая старение под действием света.
Из-за низкой тенденции соединений вызывать гиперкальцемию при непрерывном приеме, они, как ожидается, могут представлять ценность при долговременном лечении увеличения щитовидной железы (в частности, вторичного увеличения щитовидной железы, связанного с почечной недостаточностью), и для способствования остеогенезу и лечению остеопороза.
Данные соединения могут использоваться в комбинации с другими лекарственными препаратами. При предотвращении индивидуальной реакции на прививки лечение данными соединениями может с преимуществом быть объединено, например, с лечением циклоспорином A.
Соединения формулы I могут быть легко получены из производной I витамина D с помощью способов, представленных на схеме 1, или из CD-кольцевой производной 78 с помощью способов, представленных на схеме 2.
Используются следующие стандартные сокращения в тексте всего описания: Me= метил; Et= этил; THP=тетрагидро-4H-пиран-2-ил; TMS=триметилсилил; пет. эфир=петролейный эфир; THF=тетрагидрофуран; TBAF=тетра-(n-бутил)аммоний фторид тригидрат; Tf=трифторметан сульфонил; "HF"=5% гидрофторид в смеси ацетонитрил: вода (7:1, объем/объем); TBDMS=трет-бутилдиметилсилил; PPTS=пиридиний толуол-4-сульфонат; DPMS= дифенилметилсилил; Ts=4-метилбензолсульфонил; DMSO=диметилсульфоксид.
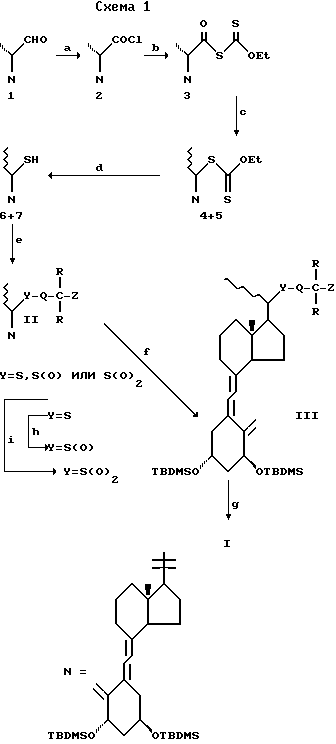
Q и R определены как выше и Z определено в примечаниях.
Хроматографическое разделение изомеров 20R и 20S может быть произведено после любой из стадий d, e, f или g, предпочтительно d, e или f. Хроматографическое разделение сульфоксидов с R и S конфигурацией производят после стадии h.
Примечания к схеме 1:
a) трет-Бутил гипохлорит/четыреххлористый углерод/20-100 мин
b) Калий O-этил дитиокарбонат/ацетон/-30oC/30 мин и 20oC/ 60 мин
c) Ртутная лампа/бензол/60oC/10-40 мин
d) Этаноламин/DMF/10-60 мин
e) IV (смотри ниже) /основание, такое как карбонат калия/ DMF/0,1-10 час или гидрид калия/18-Краун-6/THF/20-200 мин
f) Ртутная лампа/триплетный сенсибилизатор, например, антрацен/триэтил-амин/дихлорметан/10-15oC/10-60 мин
g) Снятие защиты со всех спиртовых групп, например, "HF" /этилацетат/20-200минилиTBAF/THF/60oC/20-200мин,илиPPTS/EtOH/50oC/20-200 мин
h) Натрий вольфрамат, дигидрат/1 экв. перекись водорода/гидрокарбонат натрия/хлороформ
i) Натрий вольфрамат, дигидрат/2 экв. перекись водорода/гидрокарбонат натрия/хлороформ.

T=уходящая группа, например, Br-, J-, TsO-, TfO-.
Z= OH или защищенная спиртовая группа, такая как TMS-O, TBDMS-O, DPMS-O или THP-O.
Синтез соединений 2-7 описан в примерах приготовления 1-4. Синтезы боковых блоков цепи IV проводят с помощью стандартных методик, описанных в литературе/ заявки на Международные патенты NN PCT/DK 90/00036 и PCT/DK 91/00091.
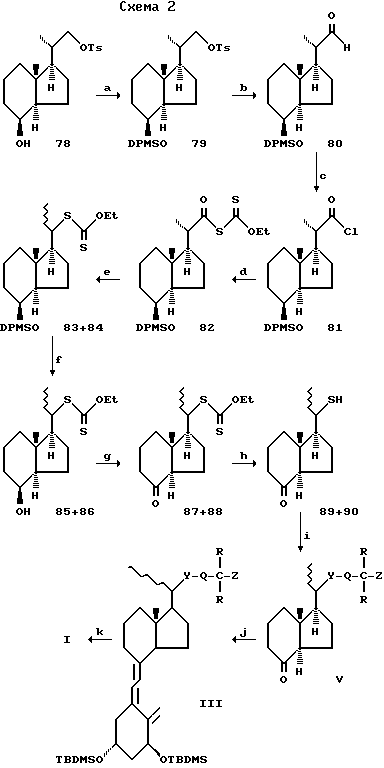
Q, R и Z определяются как выше.
Примечания к схеме 2^
a) DPMSCI /имидазол/DMF/ 20 час
b) 1 экв. натрий гидрокарбонат/DMSO/110oC/90 мин
с) трет-Бутил гипохлорит/четыреххлористый углерод/ 30-180 мин
d) Калий O-этилдитиокарбонат/ацетон/-30oC/60 мин и 20oC/ 60 мин
e) Ртутная лампа/бензол/60oC/10-40 мин
f) "HF"/этилацетат/60 мин
g) 1,1 экв. Оксалилхлорид/2,2 экв. DMSO/дихлорметан/-65oC/5 мин, а затем соединение 85 и 86/15 мин
h) Этаноламин/DMF/60 мин
i) IV (смотри примечания, схема 1) /основание, такое как карбонат калия/ DMF/0,1-10 час или гидрид калия/18-Краун-6/THF/20-200 мин
j) Соединение 99 (смотри ниже)H-бутиллитий/THF/-78oC/20 мин/затем V (смотри ниже)/THF/-78oC/120 мин
k) Снятие защиты со всех спиртовых групп, например, "HF" /этилацетат/20-200минилиTBAF/THF/60oC/20-200мин,илиPPTS/EtOH/50oC/20-200 мин/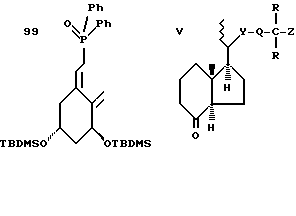
Синтез соединений 79-90 описывается в примерах получения 58-67.
Данные соединения предназначены для использования в фармацевтических композициях, которые являются пригодными для использования при лечении расстройств человека и животных, как описано выше.
Требуемое количество соединения формулы I (здесь и далее упоминаемое как активный ингредиент) для терапевтического действия будет, разумеется, изменяться в зависимости от применения конкретного соединения, а также в зависимости от способа введения и в зависимости от млекопитающего, подвергающегося лечению. Соединения данного изобретения могут вводится парэнтеральным, интраартикулярным, энтеральным или местным способами. Они хорошо абсорбируются, когда вводятся энтерально, и это является предпочтительным способом введения при лечении системных расстройств. При лечении дерматологических расстройств, подобных псориазу, или глазных болезней предпочтительными являются местные или энтеральные формы.
При лечении респираторных заболеваний, подобных астме, предпочтительным является аэрозоль.
Хотя является возможным вводить один только активный ингредиент в виде исходного вещества, является предпочтительным вводить его в виде фармацевтической композиции. Предпочтительно, чтобы активный ингредиент составлял от 0,1 миллионной части до 0,1% от веса препарата.
Под термином "единичная доза" подразумевается унитарная, то есть, единичная доза, которая может быть введена пациенту и которая является удобной в обращении и при упаковке, оставаясь в виде физически и химически стабильной единичной дозировки, содержащей либо активный материал как таковой или его смесь с твердыми или жидкими фармацевтическими разбавителями или носителями.
Композиции, как для ветеринарного использования, так и для медицинского, данного изобретения содержат активный ингредиент в смеси с фармацевтически приемлемым носителем и, возможно, с другим(и) терапевтическим(и) ингредиентом(ами). Носитель(и) должен(должны) быть "приемлемым(и)", в смысле, являться совместимыми с другими ингредиентами композиции и не вредить принимающему их.
Композиции включают, например, таковые в форме, пригодной для орального, ректального, парэнтерального (включая подкожное, внутримышечное и внутривенное) интраартикулярного и местного (наружного) введения.
Композиции могут быть удобно представлены в форме единичной дозы и могут быть приготовлены с помощью любого из способов, хорошо известных в фармации. Все способы включают стадии приведения активного ингредиента в соприкосновение с носителем, который включает один или более вспомогательных ингредиентов. Как правило, композиции приготавливают с помощью приведения активного ингредиента в однородный и тесный контакт с жидким носителем или с тонко измельченным твердым носителем, или с обоими, а затем, если необходимо, придают продукту желаемую форму.
Композиции данного изобретения, пригодные для орального приема, могут быть в форме дискретных единиц, таких как капсулы, саше, таблетки или лепешки, каждая содержащая предварительно определенное количество активного ингредиента; в форме порошка или гранул; в форме раствора или суспензии в водной жидкости или в неводной жидкости; или форме эмульсии, типа масло в воде, или эмульсии, типа вода в масле. Активный ингредиент может также вводиться в форме шарика, лекарственной кашки или пасты.
Таблетка может быть получена путем прессования или формования активного ингредиента, необязательно с одним или более вспомогательными ингредиентами. Прессованные таблетки могут получаться путем прессования в соответствующей машине активного ингредиента в свободно текущей форме, такой как порошок или гранулы, не обязательно смешанного с связующим агентом, смазывающим агентом, инертным разбавителем, поверхностно-активным веществом или диспергирующим веществом. Формованные таблетки могут быть получены путем формования в соответствующей машине смеси порошкообразного активного ингредиента и соответствующего носителя, увлажненных инертным жидким разбавителем.
Композиции для ректального введения могут быть в форме, суппозитария, включающего активный ингредиент и носитель, такой как масло какао, или в форме клизмы.
Композиции, пригодные для парэнтерального введения обычно включают стерильные масляный или водный препарат активного ингредиента, который предпочтительно является изотоничным с кровью пациента.
Композиции, пригодные для интраартикулярного введения, могут быть в форме стерильного водного препарата активного ингредиента, который может быть в микрокристаллической форме, например в форме водной микрокристаллической суспензии. Липосомные препараты или биораздражаемые полимерные системы также могут быть использованы при введении активного ингредиента как интраартикулярным, так и офтальмологическим путем.
Композиции, пригодные для местного применения, включая лечение глаз, включают жидкие или полужидкие препараты, такие как мази, примочки, гели, аппликанты, эмульсии, типа масло в воде или вода в масле, такие как кремы, мази или пасты; или растворы или суспензии, такие как капли.
Для лечения астмы может быть использована ингаляция порошка, самораспространяющихся или аэрозольных композиций, распространяющихся с помощью аэрозольного баллончика, распылителя или пульверизатора. Композиции при распространении предпочтительно имеют размер частиц в диапазоне от 10 до 100 микрон.
Такие композиции являются наиболее предпочтительными в форме тонкоизмельченного порошка для пульмонарного введения из устройства для ингаляции порошка или в виде самораспространяющихся распространяющих порошок препаратов. В случае самораспространяющихся композиций в виде раствора или аэрозоля, эффект может быть достигнут либо путем выбора клапана, имеющего желаемые характеристики распыления (то есть, являющегося способным производить аэрозоль, имеющий желаемый размер частиц), либо путем включения активного ингредиента в качестве суспендированного порошка с контролируемым размером частиц. Эти самораспространяющиеся композиции могут быть либо препаратами, распространяющими порошок, либо композициями, распространяющими активный ингредиент в виде капель раствора или суспензии.
Самораспространяющиеся распространяющие порошок композиции предпочтительно включают дисперсные частицы твердых активных ингредиентов и жидкий пропеллент, имеющий температуру кипения ниже 18oC при атмосферном давлении. Жидкий пропеллент может быть любым пропеллентом, о котором известно, что он является пригодным для введения лекарств, и может включать C1-C6 алкильные углеводороды или галогенированные C1-C6 алкильные углеводороды или их смеси; хлорированные или фторированные C1-C6 алкильные углеводороды являются особенно предпочтительными. Обычно пропеллент составляет от 45 до 99,9% вес/вес композиции, в то время как активный ингредиент составляет от 0,1 миллионной части до 0,1 вес/вес препарата.
В дополнение к рассмотренным выше ингредиентам композиции данного изобретения могут включать один или более дополнительных ингредиентов, таких как разбавители, буферы, отдушки, связующие, поверхностно-активные вещества, сгустители, смазывающие вещества, консерванты, например метилгидроксибензоат (включая антиоксиданты), эмульсифицирующие вещества и им подобные. Композиции далее могут включать другие терапевтически активные соединения, обычно применяемые при лечении рассмотренных выше патологических состояний.
Данное изобретение далее относится к способу лечения пациентов, страдающих одним из рассмотренных выше патологических состояний, упомянутый способ включает введение пациенту, нуждающемуся в лечении, эффективного количества одного или более соединений формулы I, оного или в комбинации с одним или более другими терапевтически активными соединениями, обычно применяемыми при лечении упомянутых патологических состояний. Лечение данными соединениями и/или другими терапевтическими соединениями может быть одновременным или с интервалами.
При лечении системных расстройств могут вводится дневные дозы соединения 1 от 0,1 до 100 μг, предпочтительно от 0,2 до 25 μг. При местном лечении дерматологических расстройств применяются мази, кремы или примочки, содержащие от 0,1 до 500 μг/г, а предпочтительно от 0,1 до 100 μг/г соединения формулы 1. Для местного (наружного) использования в офтальмологии применяются мази, капли или гели, содержащие от 0,1 до 500 μг/г, а предпочтительно от 0,1 до 100 μг/г соединения формулы I. Композиции для перорального приема приготавливают предпочтительно в виде таблеток, капсул или капель, содержащих от 0,05 до 50 μг, предпочтительно от 0,1 до 25 μг соединения формулы I на единичную дозу.
Далее изобретение будет проиллюстрировано последующими неограничивающими общими методиками, примерами приготовления и примерами. Общие методики, примеры приготовления и примеры.
Приводимые в качестве примеров соединения 1 перечислены в табл. 1, в то же время как соединения общей формулы II, III и V перечислены в табл. 2 (см. в конце описания).
Для спектров ядерного магнитного резонанса 1H (300 МГц) приведены значения химического сдвига δ, если не указано другого, для дейтерийхлороформных растворов, относительно внутреннего тетраметилсилана (δ = 0,00) или хлороформа (δ = 7,25). Значения для мультиплетов либо определены (дублет (d), триплет (t), квартет (q)), либо нет (m), дано в примерной средней точке, если не обозначен диапазон (s = синглет, b = уширенный).
Эфир является диэтиловым эфиром и его сушат над натрием. THF сушат над натрий/бензофеноном. Петролейный эфир относится к пентановой фракции. Реакции проводятся при комнатной температуре, если не отмечено другого. Методика выделения включает разбавление d определенным растворителем (либо органическим реакционным растворителем), экстракцию водой, а затем рассолом, сушку над безводным MgSO4 и концентрацию в вакууме для получения остатка. Хроматографию проводят на силикагеле.
Приготовление 1: 1(S), 3(R)-Бис-[трет-бутилдиметилсилилоксил-20(S)-хлоркарбонил-9,10-секпрегна-5(Z),7(E),10(19)-триен (соединение 2)
Соединение 1 (3,54 г) (Calverley, M. C. , Tetrahedron 43, 4609-4619 (1987)) растворяют в четыреххлористом углероде (35 мл) и добавляют трет-бутилгипохлорит (1,00 мл) при комнатной температуре. После перемешивания в течение 30 минут в атмосфере аргона реакционную смесь концентрируют в вакууме, получая указанное в заглавии соединение в виде масла.
ЯМР (CCl4): δ = 0,10 (m, 12H), 0,64 (s, 3H), 0,90 (s, 9H), 0,94 (s, 9H), 1,41 (d, 3H), 1,30 - 2,25 (m, 13H), 2,32 (bd, 1H), 2,53 (dd, 1H), 2,82 (m, 1H), 2,94 (m, 1H), 4,23 (m, 1H), 4,50 (m, 1H), 4,92 (m, 1H), 4,94 (m, 1H), 5,81 (d, 1H), 6,36 (d, 1H).
Приготовление 2: 1(S), 3(R)-Бис-трет-бутилдиметилсилилоксил- 20(S)-O-[[этилокси(тиокарбонил)-тио]карбонил]-9,10- секпрегна-5(Z),7(E),10(19)-триен (соединение 3)
Неочищенное соединение 2 (4,22 г) растворяют в ацетоне (35 мл) и добавляют калий O-этилдитиокарбонат (1,09 г) при перемешивании при -30oC в атмосфере аргона. Перемешивание продолжают в течение 30 минут. Реакционной смеси позволяют достичь комнатной температуры и через 60 минут реакционную смесь промывают насыщенным водным раствором гидрокарбоната натрия и извлекают (дихлорметан), получая указанное в заглавии соединение.
ЯМР: δ = 0,05 (m, 12H), 0,54 (s, 3H), 0,86 (s, 9H), 0,90 (s, 9H), 1,27 (d, 3H), 1,47 (t, 3H), 1,15 - 2,00 (m, 12H), 2,05 (bt, 1H), 2,28 (bd, 1H), 2,52 (m, 1H), 2,55 (dd, 1H), 2,87 (m, 1H), 4,21 (m, 1H), 4,52 (m, 1H), 4,67 (q, 2H), 4,94 (m, 1H), 4,98 (m, 1H), 5,82 (d, 1H), 6,43 (d, 1H).
Приготовление 3: 1(S),3(R)-Бис-[трет-бутилдиметилсилилоксил- 20(S)/20(R)-O-этилксантогенат-9,10-секпрегна- 5(Z), 7(E), 10(19)-триен (cоединения 4 и 5)
Неочищенное соединение 3 (4,45 г) растворяют в бензоле (150 мл) в колбе из стекла Pyrex в атмосфере аргона. Реакционную смесь нагревают до 60oC и облучают ультрафиолетовым светом ультрафиолетовой лампой высокого давления типа TQ760Z2 (Hanau) в течение 20 минут при перемешивании. Реакционную смесь концентрируют в вакууме и очищают с помощью хроматографии (дихлорметан/пет. эфир: 1/3), получая указанные в заглавии соединения.
ЯМР (4): δ = 0,06 (m, 12H), 0,64 (s, 3H), 0,86 (s, 9H), 0,89 (s, 9H), 1,42 (t, 3H), 1,48 (d, 3H), 1,20 - 1,82 (m, 9H), 1,85 - 2,15 (m, 4H), 2,29 (bd, 1H), 2,56 (dd, 1H), 2,88 (dd, 1H), 3,76 (m, 1H), 4,21 (m, 1H), 4,53 (m, 1H), 4,64 (m, 2H), 4,94 (m, 1H), 4,98 (m, 1H), 5,82 (d, 1H), 6,44 (d, 1H).
ЯМР (5): δ = 0,06 (m, 12H), 0,58 (s, 3H), 0,85 (s, 9H), 0,89 (s, 9H), 1,41 (d, 3H), 1,42 (t, 3H), 1,15 - 2,15 (m, 12H), 2,25 (bd, 1H), 2,29 (bd, 1H), 2,55 (dd, 1H), 2,87 (m, 1H), 3,65 (m, 1H), 4,21 (m, 1H), 4,52 (m, 1H), 4,63 (q, 2H), 4,94 (m, 1H), 4,98 (m, 1H), 5,81 (d, 1H), 6,44 (d, 1H).
Приготовление 4: 1(S),3(R)-Бис-[трет-бутилдиметилсилилоксил- 20(S)/20(R)-меркапто-9,10-секпрегна-5(Z), 7(E), 10(19)-триен (соединения 6 и 7)
К раствору соединения 4 и 5 (550 мг) в безводном N,N-диметилформамиде (6,0 мл) добавляют аминоэтанол (0,75 мл) в атмосфере аргона и при перемешивании. Перемешивание продолжают в течение 30 минут при комнатной температуре. Реакционную смесь обогащают (диэтиловый эфир). Остаток очищают с помощью хроматографии (диэтиловый эфир/пет. эфир: 1/20), получая смесь указанных в заглавии соединений.
ЯМР (6): δ = 0,06 (m, 12H), 0,55 (s, 3H), 0,85 (s, 9H), 0,90 (s, 9H), 1,41 (d, 3H), 1,15 - 2,47 (m, 15H), 2,55 (dd, 1H), 2,86 (bd, 1H), 2,94 (m, 1H), 4,21 (m, 1H), 4,52 (m, 1H), 4,93 (m, 1H), 4,98 (m, 1H), 5,82 (d, 1H), 6,44 (d, 1H).
ЯМР (7): δ = 0,06 (m, 12H), 0,59 (s, 3H), 0,86 (s, 9H), 0,90 (s, 9H), 1,51 (d, 3H), 1,15 - 2,47 (m, 15H), 2,55 (dd, 1H), 2,80 - 3,05 (m, 2H), 4,21 (m, 1H), 4,52 (m, 1H), 4,93 (m, 1H), 4,98 (m, 1H), 5,82 (d, 1H), 6,44 (d, 1H).
Общая методика 1: Алкилирование соединений 6 и/или 7 с получением соединений общей формулы II.
К раствору соединения 6 и/или 7 (1,0 ммоль) и 18 Краун-6 (0,5 ммоль) в безводном THF (10 мл), перемешиваемому в атмосфере аргона, добавляют гидрид калия (1,5 ммоль, 20% в масле), а затем требуемый алкилирующий агент IV (2,0 ммоль). Смесь перемешивают в течение 45 минут при комнатной температуре, а затем гасят несколькими каплями воды. Реакционную смесь обрабатывают (диэтиловый эфир), и остаток очищают с помощью хроматографии, получая разделенные соединения, указанные в заглавии.
Общая методика 2: Алкилирование соединений 6 и/или 7 с получением соединений общей формулы II
Раствор 6 и/или 7 (1,25 ммоль) перемешивают с твердым карбонатом калия (1,6 ммоль) в течение 15 минут в DMF (5 мл). Добавляют требуемый алкилирующий агент IV (1,5 ммоль) в DMF (3 мл), и смесь перемешивают в течение 3 часов. Обрабатывают (диэтиловый эфир), и хроматография дает разделенные соединения, указанные в заглавии.
Общая методика 3: Изомеризация соединений общей формулы II с получением соединений общей формулы III
Раствор соединения общей формулы II (0,1 ммоль), антрацена (0,2 ммоль) и триэтиламина (0,05 мл) в дихлорметане (4,0 мл) в атмосфере аргона в колбе из стекла Pyrex облучают ультрафиолетовым светом ультрафиолетовой лампой высокого давления, типа TQ760Z2 (Hanau) при приблизительно 10oC в течение 20 минут при перемешивании. Реакционную смесь концентрируют в вакууме и обрабатывают пет.эфиром (2 x 5 мл). После фильтрования фильтрат концентрируют в вакууме и очищают с помощью хроматографии (смесь дихлорметана и пет.эфира в качестве элюента), получая указанное в заглавии соединение.
Общая методика 4: Деблокировка соединений общей формулы III с получением соответствующих соединений 1 обработкой "HF"
К раствору соединения общей формулы III (0,05 ммоль) в этилацетате (0,25 мл) добавляют ацетонитрил (1,0 мл), а затем 5% раствор плавиковой кислоты в смеси ацетонитрил:вода, 7:1 (0,8 мл) в атмосфере аргона и при перемешивании. Перемешивание продолжают в течение 45 минут при комнатной температуре. Добавляют насыщенный водный раствор гидрокарбоната натрия (10 мл), и реакционную смесь обрабатывают (этилацетат). Остаток очищают с помощью хроматографии (этилацетат в качестве элюента), получая указанное в заглавии соединение.
Общая методика 5: Деблокировка соединений общей формулы III с получением соответствующих соединений 1 обработкой тетра-N-бутиламмонийфторидом
К раствору соединения общей формулы III (0,16 ммоль) в THF (5 мл) добавляют раствор TBAF (300 мг) в THF (5 мл) при перемешивании при 60oC в атмосфере аргона. Перемешивание продолжают в течение одного часа при 60oC, реакционную смесь промывают водным раствором гидрокарбоната натрия и обогащают (этилацетат). Остаток очищают с помощью хроматографии (этилацетат в качестве элюента), получая указанное в заглавии соединение.
Общая методика 6: Деблокировка соединений общей формулы III с получением соответствующих соединений 1 обработкой пиридинийтолуол-4-сульфонатом
PPTS (2 мг) добавляют к раствору соединения общей формулы III (0,16 ммоль) в 99% этаноле (2 мл), и смесь перемешивают при 50oC в атмосфере аргона в течение одного часа. Смесь промывают насыщенным водным раствором гидрокарбоната и обрабатывают (этилацетат). Исходный продукт очищают с помощью хроматографии (этилацетат в качестве элюента), получая указанное в заглавии соединение.
Общая методика 7: Окисление 22-тиасоединений общей формулы II с получением соответствующих изомерных сульфоксидов также общей формулы II
К смеси 22-тио соединения общей формулы II (0,15 ммоль), гидрокарбоната натрия (10 мг), 2% (вес/объем) раствора вольфрамата калия, дигидрата (10 μг) и метанола (0,5 мл) добавляют 30% перекись водорода (24 μг) и хлороформ (0,5 мл). После перемешивания при соответствующей температуре в течение нескольких часов добавляют воду и смесь обрабатывают (дихлорметан), получая остаток, который подвергается хроматографии для разделения чистых 22(R)- и 22(S)-сульфоксидов.
Общая методика 8: Окисление 22-тиониловых соединений общей формулы II с получением соответствующих сульфонильных соединений также общей формулы II
К смеси 22-тионилового соединения (22(R)- и/или 22(S) общей формулы II (0,15 ммоль), гидрокарбоната натрия (30 мг), 2% (вес/объем) раствора вольфрамата натрия, дигидрата (30 μг) и метанола (0,6 мл) добавляют 30% перекись водорода (36 μг). После перемешивания при соответствующей температуре в течение нескольких часов добавляют воду и смесь обрабатывают (дихлорметан), получая остаток, который подвергают хроматографии, получая указанное в заглавии соединение.
Общая методика 9: Алкилирование соединений 89 и/или 90 с получением соединений общей формулы V
Раствор соединения 89 и/или 90 (0,75 ммоль) перемешивают с твердым карбонатом калия (0,76 ммоль) в течение 15 минут в DMF (5 мл) в атмосфере аргона. Добавляют соответствующий алкилирующий агент IV (1,13 ммоль) в DMF (5 мл), и смесь перемешивают в течение 3 часов. Обогащают (диэтиловый эфир), и хроматография дает указанное в заглавии соединение.
Общая методика 10: Связывание соединений общей формулы V с [1Z,3S,5R]-[2-[3,5-Бис-[трет-бутилдиметилсилилоксил] -2- метиленциклогексилиден] этил] фенилфосфин оксидом, (соединение 99) с получением соединений общей формулы III
Раствор соединения 99 (0,60 ммоль) (Baggiolini, G.N. et al., J. Org. Chem. , 51, 3098 - 3108 (1986) в THF (7 мл) охлаждают до -78oC в атмосфере аргона и при перемешивании. Добавляют н-бутиллитий (0,60 ммоль, 1,6 М в гексане) в течение нескольких минут, и полученный в результате раствор глубокого красного цвета оставляют перемешиваться еще в течение 20 мнут. Затем добавляют соединения общей формулы V (0,50 ммоль, в 3 мл THF) в течение 5 минут к реакционной смеси. Смесь перемешивают в течение 2 часов, а затем дают возможность достичь комнатной температуры. Ее гасят каплей воды и обрабатывают (этилацетат/пет. эфир: 1/1). Остаток очищают с помощью хроматографии (смесь дихлорметана и пет.эфира в качестве элюента), получая соединения, указанные в заглавии.
Пример приготовления 5: соединения 8 и 9
Способ: общая методика 1.
Алкилирующий агент: 5-Бром-3-этил-3-триметилсилилоксипентан (0,5 г).
Пример приготовления 6: соединения 10 и 11
Способ: общая методика 1.
Алкилирующий агент: 6-Бром-3-этил-3-триметилсилилоксигексан (0,5 г).
ЯМР (10) : δ = 0,05 (m, 12H), 0,09 (s, 9H), 0,62 (s, 3H), 0,80 (t, 6H), 0,85 (s, 9H), 0,90 (s, 9H), 1,28 (d, 3H), 1,45 (q, 4H), 1,15-2,15 (m, 17H), 2,30 (bd, 1H), 2,47 (m, 2H), 2,55 (dd, 1H), 2,66 (m, 1H), 2,87 (m, 1H), 4,21 (m, 1H), 4,52 (m, 1H), 4,94 (m, 1H), 4,98 (m, 1H), 5,81 (d, 1H), 6,45 (d, 1H).
ЯМР (11) : δ = 0,05 (m, 12H), 0,09 (s, 9H), 0,57 (s, 3H), 0,81 (t, 6H), 0,85 (s, 9H), 0,89 (s, 9H), 1,38 (d, 3H), 1,46 (q, 4H), 1,15-2,17 (m, 17H), 2,29 (bd, 1H), 2,50 (m, 2H), 2,56 (dd, 1H), 2,65 (m, 1H), 2,87 (m, 1H), 4,21 (m, 1H), 4,52 (m, 1H), 4,94 (m, 1H), 4,98 (m, 1H), 5,82 (d, 1H), 6,44 (d, 1H).
Пример приготовления 7: соединения 12 и 13
Способ: общая методика 1.
Алкилирующий агент: 7-Бром-3-этил-3-триметилсилилоксигептан.
Пример приготовления 8: соединения 14 и 15
Способ: общая методика 2.
Алкилирующий агент: 3-(1-Этил-1-гидроксипропил)бензилбромид.
Пример приготовления 9: соединения 16 и 17
Способ: общая методика 1.
Алкилирующий агент: 6-Бром-3-этил-3-триметилсилилоскигекс-4-ен.
Пример приготовления 10: соединения 18 и 19
Способ: общая методика 1.
Алкилирующий агент: 6-Бром-3-этил-3-триметилсилилоксигекс-4-ен.
Пример приготовления 11: соединения 20 и 21
Способ: общая методика 1.
Алкилирующий агент: 5-Бром-2-метил-2-триметилсилилоксипентан.
Пример приготовления 12: соединения 22 и 23
Способ: общая методика 1.
Алкилирующий агент: 6-Бром-2-метил-2-тетрагидропиранилоксигексан.
Пример приготовления 13: соединения 24 и 25
Способ: общая методика 2.
Алкилирующий агент: 3-(1-Метил-1-гидроксиэтил)бензилбромид
Пример приготовления 14: соединения 26 и 27
Способ: общая методика 1.
Алкилирующий агент: 5-Бром-2-метил-2-триметилсилилоксипент-4-ене.
Пример приготовления 15: соединения 28 и 29
Способ: общая методика 1.
Алкилирующий агент: 5-Бром-2-метил-2-триметилсилилоксипент-4-ин.
Пример приготовления 16: соединения 30 и 31
Способ: общая методика 7.
Пример приготовления 17: соединения 32 и 33
Способ: общая методика 7.
Пример приготовления 18: соединение 34
Способ: общая методика 8.
Пример приготовления 19: соединение 35
Способ: общая методика 8.
Пример приготовления 20: соединение 36 и 37
Способ: общая методика 7.
Пример приготовления 21: соединение 38 и 39
Способ: общая методика 7.
Пример приготовления 22: соединение 40
Способ: общая методика 8.
Пример приготовления 23: соединение 41
Способ: общая методика 8.
Пример приготовления 24: соединение 42
Способ: общая методика 3.
Исходный материал: соединение 8.
Пример приготовления 25: соединение 43
Способ: общая методика 3.
Исходный материал: соединение 9.
Пример приготовления 26: соединение 44
Способ: общая методика 3.
Исходный материал: соединение 10.
ЯМР : δ = 0,05 (m, 12H), 0,08 (s, 9H), 0,60 (s, 3H), 0,81 (m, 6H), 0,86 (s, 18H), 1,27 (d, 3H), 1,45 (q, 4H), 1,15-2,15 (m, 17H), 2,21 (dd, 1H), 2,37-2,57 (m, 3H), 2,65 (m, 1H), 2,82 (m, 1H), 4,18 (m, 1H), 4,36 (m, 1H), 4,85 (m, 1H), 5,17 (m, 1H), 6,00 (d, 1H), 6,23 (d, 1H).
Пример приготовления 27: соединение 45
Способ: общая методика 3.
Исходный материал: соединение 11.
ЯМР: δ = 0,05 (m, 12H), 0,09 (s, 9H), 0,55 (s, 3H), 0,81 (t, 6H), 0,86 (s, 18H), 1,37 (d, 3H), 1,45 (q, 4H), 1,15-2,14 (m, 17H), 2,21 (dd, 1H), 2,44 (dd, 1H), 2,48 (m, 2H), 2,64 (m, 1H), 2,82 (m, 1H), 4,18 (m, 1H), 4,36 (m, 1H), 4,85 (m, 1H), 5,17 (m, 1H), 6,01 (d, 1H), 6,22 (d, 1H).
Пример приготовления 28: соединение 46
Способ: общая методика 3.
Исходный материал: соединение 12.
Пример приготовления 29: соединение 47
Способ: общая методика 3.
Исходный материал: соединение 13.
Пример приготовления 30: соединение 48
Способ: общая методика 3.
Исходный материал: соединение 14.
Пример приготовления 31: соединение 49
Способ: общая методика 3.
Исходный материал: соединение 15.
Пример приготовления 32: соединение 50
Способ: общая методика 3.
Исходный материал: соединение 16.
Пример приготовления 33: соединение 51
Способ: общая методика 3.
Исходный материал: соединение 17.
Пример приготовления 34: соединение 52
Способ: общая методика 3.
Исходный материал: соединение 18.
Пример приготовления 35: соединение 53
Способ: общая методика 3.
Исходный материал: соединение 19.
Пример приготовления 36: соединение 54
Способ: общая методика 3.
Исходный материал: соединение 20.
Пример приготовления 37: соединение 55
Способ: общая методика 3.
Исходный материал: соединение 21.
Пример приготовления 38: соединение 56
Способ: общая методика 3.
Исходный материал: соединение 22.
Пример приготовления 39: соединение 57
Способ: общая методика 3.
Исходный материал: соединение 23.
Пример приготовления 40: соединение 58
Способ: общая методика 3.
Исходный материал: соединение 24.
Пример приготовления 41: соединение 59
Способ: общая методика 3.
Исходный материал: соединение 25.
Пример приготовления 42: соединение 60
Способ: общая методика 3.
Исходный материал: соединение 26.
Пример приготовления 43: соединение 61
Способ: общая методика 3.
Исходный материал: соединение 27.
Пример приготовления 44: соединение 62
Способ: общая методика 3.
Исходный материал: соединение 28.
Пример приготовления 45: соединение 63
Способ: общая методика 3.
Исходный материал: соединение 29.
Пример приготовления 46: соединение 64
Способ: общая методика 3.
Способ: общая методика 3.
Исходный материал: соединение 30.
Пример приготовления 47: соединение 65
Способ: общая методика 3.
Исходный материал: соединение 31.
Пример приготовления 48: соединение 66
Способ: общая методика 3.
Исходный материал: соединение 32.
Пример приготовления 49: соединение 67
Способ: общая методика 3.
Исходный материал: соединение 33.
Пример приготовления 50: соединение 68
Способ: общая методика 3.
Исходный материал: соединение 34.
Пример приготовления 51: соединение 69
Способ: общая методика 3.
Исходный материал: соединение 35.
Пример приготовления 52: соединение 70
Способ: общая методика 3.
Исходный материал: соединение 36.
Пример приготовления 53: соединение 71
Способ: общая методика 3.
Исходный материал: соединение 37.
Пример приготовления 54: соединение 72
Способ: общая методика 3.
Исходный материал: соединение 38.
Пример приготовления 55: соединение 73
Способ: общая методика 3.
Исходный материал: соединение 39.
Пример приготовления 56: соединение 74
Способ: общая методика 3.
Исходный материал: соединение 40.
Пример приготовления 57: соединение 75
Способ: общая методика 3.
Исходный материал: соединение 41.
Пример приготовления 58: соединение 76 и 77
Способ: общая методика 10.
Исходный материал: соединение 91 и 92.
ЯМР (76) : δ = 0,05 (m, 12H), 0,10 (s, 9H), 0,60 (s, 3H), 0,87 (s, 18H), 1,22 (s, 6H), 1,28 (d, 3H), 1,10-2,05 (m, 15H), 2,20 (dd, 1H), 2,40-2,60 (m, 3H), 2,66 (m, 1H), 2,82 (m, 1H), 4,18 (m, 1H), 4,37 (m, 1H), 4,85 (m, 1H), 5,17 (m, 1H), 6,00 (d, 1H), 6,23 (d, 1H)
ЯМР (77) : δ = 0,05 (m, 12H), 0,10 (s, 9H), 0,56 (s, 3H), 0,87 (s, 18H), 1,22 (s, 6H), 1,37 (d, 3H), 1,10-2,10 (m, 15H), 2,20 (dd, 1H), 2,44 (dd, 1H), 2,55 (m, 2H), 2,65 (m, 1H), 2,82 (m, 1H), 4,17 (m, 1H), 4,36 (m, 1H), 4,85 (m, 1H), 5,17 (m, 1H), 6,01 (d, 1H), 6,22 (d, 1H).
Пример приготовления 60: 20(S)-(4-метилбензолсульфонилоксиметил)-8(S)-(метилдифенилсилилокси)-де-А,В-прегнан (соединение 79)
Соединение 78 (15,9 г) (Lythgoe, B.et al., y. Chem. Soc., Perkin Trans, 1, 2608-2612 (1977)) и имидазол (7,39 г) растворяют в ДМБ (250 мл). Добавляют дифенилметилхлорсилан (11,9 мл) и реакционную смесь перемешивают 20 часов в атмосфере аргона. Реакционную смесь распределяют между смесью вода/лед и диэтиловым эфиром. Органическую фазу промывают соляной кислотой (1H) и обогащают. Остаток очищают с помощью хроматографии (этилацетат/пет.эфир: 1/10), получая указанное в заглавии соединение.
ЯМР: δ = 0,62 (s, 3H), 0,97 (d, 3H), 0,99 (s, 3H), 1,05-2,00 (m, 13H), 2,45 (s, 3H), 3,80 (dd, 1H), 3,96 (dd, 1H), 4,13 (m, 1H), 7,37 (m, 8H), 7,58 (m, 4H), 7,79 (m, 2H).
Пример приготовления 61: 20(S)-формил-8(S)-метилдифенилсилилокси-де-А, В-прегнан (соединение 80)
Соединение 79 (5,80 г) и безводный гидрокарбонат натрия (908 мг) растворяют в DMSO (150 мл, предварительно нагревают до 150oC в течение 10 минут и дают возможность достичь комнатной температуры в атмосфере аргона), и раствор нагревают до 110oC в течение 90 минут. Смесь охлаждают до комнатной температуры и обрабатывают. Хроматография (диэтиловый эфир/пет. эфир: 1/20) остатка дает указанное в заглавии соединение.
ЯМР: δ = 0,62 (s, 3H), 1,06 (s, 3H), 1,09 (d, 3H), 1,05-2,00 (m, 12H), 2,37 (m, 1H), 4,16 (m, 1H), 7,37 (m, 6H), 7,57 (m, 4H), 9,57 (d,1H).
Пример приготовления 62: 20(S)-хлоркарбонил-8(S)-метилдифенилсилилокси)-де-А,В,-прегнан (соединение 81)
Соединение 80 (2,97 г) растворяют в четыреххлористом углероде (40 мл) и добавляют трет-бутилгипохлорит (1,30 мл) при комнатной температуре. После перемешивания в течение 90 минут в атмосфере аргона добавляют еще трет-бутилгипохлорит (0,50 мл). Через дополнительных 90 минут реакционную смесь концентрируют в вакууме, получая указанное в заглавии соединение. Оно используется непосредственно без дальнейшей очистки.
ЯМР: δ = 0,63 (s, 3H), 1,06 (s, 3H), 1,33 (d, 3H), 1,00-2,00 (m, 12H), 2,83 (m, 1H), 4,16 (m, 1H), 7,36 (m, 6H), 7,57 (m, 4H).
Пример приготовления 63: 20(S)-[[этокси(тиокарбонил)тио] -карбонил-8(S)-(метилдифенилсилилокси)-де-А,В,-прегнан (соединение 82)
Неочищенное соединение 81 растворяют в ацетоне (40 мл) и добавляют медленно (20 минут) натрий 0-этилдитиокарбонат (1,19 г) при перемешивании при -30oC в атмосфере аргона. Температуру поддерживают в течение 1 часа, а затем позволяют достичь комнатной температуры. Через 3 часа реакционную смесь в целом промывают насыщенным водным раствором гидрокарборната натрия и обогащают (дихлорметан). Хроматография (дихлорметан/пет. эфир: 1/3) дает заглавное соединение.
ЯМР: δ = 0,62 (s, 3H), 1,03 (s, 3H), 1,24 (d, 3H), 1,47 (t, 3H), 1,12-1,96 (m, 12H), 2,52 (m, 1H), 4,15 (m, 1H), 4,67 (q, 2H), 7,36 (m, 6H), 7,57 (m, 4H).
Пример приготовления 64: 20(S)/20(R)-[этокси(тиокарбонил)тио]-8(S)-(метилдифенилсилилокси)-де-А,В-прегнан (соединение 83/84)
Соединение 82 (3,23 г) растворяют в бензоле (70 мл) в колбе из стекла Pyrex в атмосфере аргона. Реакционную смесь нагревают до 60oC и облучают ультрафиолетовым светом от ультрафиолетовой лампы высокого давления, типа TQ760Z2 (Hanau) в течение 20 минут при перемешивании. Реакционную смесь концентрируют в вакууме, получая указанные в заглавии соединения без дальнейшей очистки.
ЯМР (83): δ = 0,63 (s, 3H), 1,14 (s, 3H), 1,42 (t, 3H), 1,47 (d, 3H), 1,00-2,03 (m, 12H), 3,79 (m, 1H), 4,15 (m, 1H), 4,65 (q, 2H), 7,36 (m, 6H), 7,58 (m, 4H).
ЯМР (84): δ = 0,63 (s, 3H), 1,08 (s, 3H), 1,39 (d, 3H), 1,42 (t, 3H), 1,00-2,00 (m, 11H), 2,24 (m, 1H), 3,68 (m, 1H), 4,15 (m, 1H), 4,65 (q, 2H), 7,36 (m, 6H), 7,58 (m, 4H).
Пример приготовления 65: 20(S)/20(R)-[этокси(тиокарбонил)тио]-де-А,В-прегнан-8(S)-ол (соединение 85/86)
К смеси соединений 83 и 84 (3,06 г) в этилацетате (20 мл) добавляют ацетонитрил (10 мл), а затем 5% раствор плавиковой кислоты в смеси ацетонитрил: вода 7:1 (30 мл) в атмосфере аргона и при перемешивании. Перемешивание продолжают в течение 1 часа при комнатной температуре. Добавляют насыщенный водный раствор гидрокарбоната натрия (100 мл) и реакционную смесь обогащают (этилацетат). Остаток очищают с помощью хроматографии (диэтиловый эфир/пет. эфир: 1:3), получая смесь указанных в заглавии соединений.
ЯМР (85): δ = 1,03 (s, 3H), 1,40 (t, 3H), 1,44 (d, 3H), 1,00-2,05 (m, 13H), 3,75 (m, 1H), 4,07 (m, 1H), 4,63 (m, 2H).
ЯМР (86): δ = 0,96 (s, 3H), 1,37 (d, 3H), 1,40 (t, 3H), 1,00-2,05 (m, 12H), 2,22 (m, 1H), 3,63 (m, 1H), 4,07 (m, 1H), 4,63 (m, 2H).
Пример приготовления 66: 20(S)/20(R)-[этокси(тиокарбонил)тио]-де-А,В-прегнан-8-он(соединение 87/88)
ДМСО (319 мг), растворенный в дихлорметане (2,0 мл), добавляют в течение 5 минут к перемешиваемому раствору оксалилхлорида (259 мг) в дихлорметане (4,0 мл) при -65oC в атмосфере аргона. Реакционную смесь перемешивают в течение 5 минут, при этом раствор соединения 85 и 86 в дихлорметане (2,0 мл) добавляют в течение 5 минут. Перемешивание продолжают в течение дополнительных 15 минут. Добавляют триэтиламин (1,25 мл). Реакционную смесь перемешивают в течение 15 минут и затем дают возможность нагреться до комнатной температуры. Добавляют соляную кислоту (1H, 15 мл), и реакционную смесь обрабатывают (дихлорметан), получая смесь указанных в заглавии соединений.
ЯМР (87): δ = 0,75 (s, 3H), 1,42 (t, 3H), 1,51 (d, 3H), 1,35-2,56 (m, 12H), 3,79 (m, 1H), 4,65 (q, 2H).
ЯМР (88): δ = 0,69 (s, 3H), 1,41 (d, 3H), 1,43 (t, 3H), 1,35-2,56 (m, 12H), 3,67 (m, 1H), 4,65 (q, 2H).
Пример приготовления 67: 20(S)/20(R)-меркато-де-A, B-прегнан-8-он (соединение 89/90)
К перемешиваемому раствору соединения 87 и 88 (512 мг) в безводном DMF (15 мл) добавляют аминоэтанол (1,50 мл) в атмосфере аргона. Реакционную смесь обрабатывают (диэтиловый эфир) после одного часа при комнатной температуре. Остаток очищают с помощью хроматографии (диэтиловый эфир/пет.эфир: 1: 2), получая смесь указанных в заглавии соединений.
ЯМР (89): δ = 0,66 (s, 3H), 1,44 (d, 3H), 1,30 - 2,62 (m, 13H), 2,93 (m, 1H).
ЯМР (90): δ = 0,70 (s, 3H), 1,37 (d, 3H), 1,30 - 2,62 (m, 13H), 2,86 (m, 1H).
Пример приготовления 68: соединение 91 и 92.
Способ: общая методика 9.
Алкилирующий агент: 4-Бром-2-метил-2-триметилсилилоксибутан (0,30 г)
ЯМР (91): δ = 0,09 (s, 9H), 0,70 (s, 3H), 1,21 (s, 6H), 1,28 (d, 3H), 1,00 - 2,75 (m, 17H).
ЯМР (92): δ = 0,09 (s, 9H), 0,66 (s, 3H), 1,21 (s, 6H), 1,39 (d, 3H), 1,00 - 2,75 (m, 17H).
Пример приготовления 69: соединение 93 и 94
Способ: общая методика 9.
Алкилирующий агент: 6-Бром-2-метил-2-триметилсилилоксигексан (0,26 г)
ЯМР (93): δ = 0,08 (s, 9H), 0,70 (s, 3H), 1,18 (s, 6H), 1,28 (d, 3H), 1,15 - 2,25 (m, 21H).
ЯМР (94): δ = 0,08 (s, 9H), 0,66 (s, 3H), 1,18 (s, 6H), 1,38 (d, 3H), 1,15 - 2,25 (m, 21H).
Пример приготовления 70: соединение 95 и 96
Способ: общая методика 9.
Алкилирующий агент: 3-(1-метил-1-триметилсилилоксиэтилэтил) бензилбромид (0,27 г).
ЯМР (95): δ = 0,09 (s, 9H), 0,44 (s, 3H), 1,31 (d, 3H), 1,55 (s, 6H), 1,20 - 2,65 (m, 13H), 3,71 (m, 2H), 7,15 (m, 1H), 7,23 (t, 1H), 7,30 (m, 1H), 7,39 (m, 1H).
ЯМР (96): δ = 0,08 (s, 9H), 0,54 (s, 3H), 1,40 (d, 3H), 1,55 (s, 6H), 1,20 - 2,65 (m, 13H), 3,73 (m, 2H), 7,15 (m, 1H), 7,23 (t, 1H), 7,30 (m, 1H), 7,39 (m, 1H).
Пример приготовления 71: соединение 56 и 57
Способ: общая методика 10.
Исходный материал: соединения 93 и 94.
ЯМР (56): δ = 0,05 (m, 12H), 0,09 (s, 9H), 0,60 (s, 3H), 0,86 (s, 18H), 1,19 (s, 6H), 1,27 (d, 3H), 1,10 - 2,12 (m, 19H), 2,20 (dd, 1H), 2,43 (m, 1H), 2,48 (m, 2H), 2,63 (m, 1H), 2,82 (m, 1H), 4,18 (m, 1H), 4,36 (m, 1H), 4,85 (m, 1H), 5,17 (m, 1H), 6,00 (d, 1H), 6,22 (d, 1H).
ЯМР (57): δ = 0,05 (m, 12H), 0,09 (s, 9H), 0,55 (s, 3H), 0,86 (s, 18H), 1,19 (s, 6H), 1,36 (d, 3H), 1,10 - 2,12 (m, 19H), 2,20 (dd, 1H), 2,43 (m, 1H), 2,48 (m, 2H), 2,63 (m, 1H), 2,82 (m, 1H), 4,18 (m, 1H), 4,36 (m, 1H), 4,85 (m, 1H), 5,17 (m, 1H), 6,00 (d, 1H), 6,22 (d, 1H).
Пример приготовления 72: соединение 58 и 59
Способ: общая методика 10.
Исходный материал: соединения 95 и 96.
ЯМР (58): δ = 0,05 (m, 12H), 0,08 (s, 9H), 0,39 (s, 3H), 0,86 (s, 9H), 0,87 (s, 9H), 1,29 (d, 3H), 1,56 (s, 6H), 1,15 - 2,10 (m, 13H), 2,20 (dd, 1H), 2,44 (m, 1H), 2,52 (m, 1H), 2,80 (m, 1H), 3,71 (s, 2H), 4,18 (m, 1H), 4,35 (m, 1H), 4,84 (m, 1H), 5,16 (m, 1H), 5,98 (d, 1H), 6,21 (d, 1H), 7,12 - 7,34 (m, 3H), 7,40 (m, 1H).
ЯМР (59): δ = 0,05 (m, 12H), 0,08 (s, 9H), 0,45 (s, 3H), 0,86 (s, 9H), 0,87 (s, 9H), 1,38 (d, 3H), 1,56 (s, 6H), 1,15 - 2,10 (m, 13H), 2,20 (dd, 1H), 2,44 (m, 1H), 2,52 (m, 1H), 2,80 (m, 1H), 3,73 (s, 2H), 4,18 (m, 1H), 4,35 (m, 1H), 4,84 (m, 1H), 5,16 (m, 1H), 5,98 (d, 1H), 6,21 (d, 1H), 7,12 - 7,34 (m, 3H), 7,40 (m, 1H).
Пример 1: 1(S),3(R)-Дигидрокси-20(R)-(3-этил-3-гидрокси-1-пентилтио)-9,10-секпрегна-5(Z),7(E),10(19)-триен(соединение 101)
Способ: общая методика 4.
Исходный материал: соединение 42.
Пример 2: 1(S), 3(R)-Дигидрокси-20(S)-(3-этил-3-гидрокси-1-пентилтио)- 9,10-секпрегна-5(Z),7(E),10(19)-триен(соединение 102)
Способ: общая методика 4.
Исходный материал: соединение 43.
Пример 3: 1(S),3(R)-Дигидрокси-20(R)-(4-этил-4-гидрокси-1- гексилтио)-9,10-секпрегна-5(Z),7(E),10(19)-триен(соединение 103)
Способ: общая методика 4.
Исходный материал: соединение 44.
ЯМР: δ = 0,62 (s, 3H), 0,86 (t, 6H), 1,28 (d, 3H), 1,46 (q, 4H), 1,15 - 2,10 (m, 20H), 2,32 (dd, 1H), 2,52 (m, 2H), 2,60 (dd, 1H), 2,66 (m, 1H), 2,83 (m, 1H), 4,23 (m, 1H), 4,43 (m, 1H), 5,00 (m, 1H), 5,33 (m, 1H), 6,01 (d, 1H), 6,38 (d, 1H).
Пример 4: 1(S),3(R)-Дигидрокси-20(S)-(4-этил-4-гидрокси-1- гексилтио)-9,10-секпрегна-5(Z),7(E),10(19)-триен(соединение 104)
Способ: общая методика 4.
Исходный материал: соединение 45.
ЯМР: δ = 0,58 (s, 3H), 0,86 (t, 6H), 1,38 (d, 3H), 1,47 (q, 4H), 1,20 - 2,15 (m, 20H), 2,31 (dd, 1H), 2,53 (m, 2H), 2,60 (dd, 1H), 2,65 (m, 1H), 2,83 (dd, 1H), 4,23 (m, 1H), 4,43 (m, 1H), 5,00 (m, 1H), 5,33 (m, 1H), 6,02 (d, 1H), 6,37 (d, 1H).
Пример 5: 1(S),3(R)-Дигидрокси-20(R)-(5-этил-5-гидрокси-1- гептилтио)-9,10-сек-прегна-5(Z),7(E),10(19)-триен(соединение 105)
Способ: общая методика 4.
Исходный материал: соединение 46.
Пример 6: 1(S),3(R)-Дигидрокси-20(S)-(5-этил-5-гидрокси-1- гептилтио)-9,10-сек-прегна-5(Z),7(E),10(19)-триен(соединение 106)
Способ: общая методика 4.
Исходный материал: соединение 47.
Пример 7: 1(S),3(R)-Дигидрокси-20(R)-[3-(1-этил-1-гидроксипропил)бензилтио]-9,10-сек-прегна-5(Z),7(E),10(19)-триен (соединение 107)
Способ: общая методика 4.
Исходный материал: соединение 48.
Пример 8: 1(S),3(R)-Дигидрокси-20(S)-[3-(1-этил-1-гидроксипропил)бензилтио]-9,10-сек-прегна-5(Z),7(E),10(19)-триен (соединение 108)
Способ: общая методика 4.
Исходный материал: соединение 49.
Пример 9: 1(S),3(R)-Дигидрокси-20(R)-[4-этил-4-гидроксигекс- 2-ен-1-илтио]-9,10-сек-прегна-5(Z),7(E),10(19)-триен(соединение 109)
Способ: общая методика 4.
Исходный материал: соединение 50.
Пример 10: 1(S),3(R)-Дигидрокси-20(S)-[4-этил-4-гидроксигекс- 2-ен-1-илтио]-9,10-сек-прегна-5(Z),7(E),10(19)-триен(соединение 110)
Способ: общая методика 4.
Исходный материал: соединение 51.
Пример 11: 1(S),3(R)-Дигидрокси-20(R)-[4-этил-4-гидроксигекс- 2-ен-1-илтио]-9,10-сек-прегна-5(Z),7(E),10(19)-триен(соединение 111)
Способ: общая методика 4.
Исходный материал: соединение 52.
Пример 12: 1(S),3(R)-Дигидрокси-20(S)-[4-этил-4-гидроксигекс- 2-ен-1-илтил]-9,10-сек-прегна-5(Z),7(E),10(19)-триен(соединение 112)
Способ: общая методика 4.
Исходный материал: соединение 53.
Пример 13: 1(S),3(R)-Дигидрокси-20(R)-[4-этил-4-гидроксипент- 1-илтио] -9,10-сек-прегна-5(Z),7(E),10(19)-триен(соединение 113)
Способ: общая методика 4.
Исходный материал: соединение 54.
Пример 14: 1(S),3(R)-Дигидрокси-20(S)-[4-метил-4-гидроксипент-1-илтио] -9,10-сек-прегна-5(Z),7(E),10(19)-триен(соединение 114)
Способ: общая методика 4.
Исходный материал: соединение 55.
Пример 15: 1(S),3(R)-Дигидрокси-20(R)-[5-метил-5-гидроксигекс-1-илтио] -9,10-сек-прегна-5(Z),7(E),10(19)-триен(соединение 115)
Способ: общая методика 6.
Исходный материал: соединение 56.
ЯМР: δ = 0,62 (s, 3H), 1,21 (s, 6H), 1,28 (d, 3H), 1,15 - 2,15 (m, 22H), 2,31 (dd, 1H), 2,43 - 2,70 (m, 4H), 2,83 (m, 1H), 4,23 (m, 1H), 4,43 (m, 1H), 5,00 (m, 1H), 5,33 (m, 1H), 6,00 (d, 1H), 6,38 (d, 1H).
Пример 16: 1(S), 3(R)-Дигидрокси-20(S)-[5-метил-5-гидроксигекс-1-илтио)-9,10-сек-прегна-5(Z),7(E),10(19)-триен(соединение 116)
Способ: общая методика 6.
Исходный материал: соединение 57.
ЯМР: δ = 0,58 (s, 3H), 1,22 (s, 6H), 1,38 (d, 3H), 1,15 - 2,15 (m, 22H), 2,31 (dd, 1H), 2,50 - 2,70 (m, 4H), 2,83 (m, 1H), 4,23 (m, 1H), 4,44 (m, 1H), 5,00 (m, 1H), 5,33 (m, 1H), 6,02 (d, 1H), 6,37 (d, 1H).
Пример 17: 1(S), 3(R)-Дигидрокси-20(R)-[3-(1-метил-1- гидроксиэтил)бензилтио]-9,10-сек-прегна-5(Z),7(E),10(19)-триен (соединение 117)
Способ: общая методика 4.
Исходный материал: соединение 58.
ЯМР: δ = 0,41 (s, 3H), 1,30 (d, 3H), 1,57 (s, 6H), 1,15 - 2,10 (m, 16H), 2,30 (dd, 1H), 2,40 - 2,65 (m, 2H), 2,81 (m, 1H), 3,73 (m, 2H), 4,22 (m, 1H), 4,42 (m, 1H), 4,97 (m, 1H), 5,31 (m, 1H), 5,97 (d, 1H), 6,35 (d, 1H), 7,15 - 7,38 (m, 3H), 7,48 (m, 1H).
Пример 18: 1(S), 3(R)-Дигидрокси-20(S)-[3-(1-метил-1- гидроксиэтил)бензилтио]-9,10-сек-прегна-5(Z), 7(E), 10(19)-триен (соединение 118)
Способ: общая методика 4.
Исходный материал: соединение 59.
ЯМР: δ = 0,49 (s, 3H), 1,40 (d, 3H), 1,58 (s, 6H), 1,15 - 2,10 (m, 16H), 2,30 (dd, 1H), 2,56 (m, 1H), 2,58 (dd, 1H), 2,81 (m, 1H), 3,75 (m, 2H), 4,22 (m, 1H), 4,42 (m, 1H), 4,98 (m, 1H), 5,32 (m, 1H), 5,99 (d, 1H), 6,35 (d, 1H), 7,15 - 7,38 (m, 3H), 7,46 (m, 1H).
Пример 19: 1(S), 3(R)-Дигидрокси-20(R)-[4-метил-4-гидроксипент- 2-ен-1-илтио]-9,10-cек-прегна-5(Z), 7(E), 10(19)-триен(соединение 119)
Способ: общая методика 4.
Исходный материал: соединение 60.
Пример 20: 1(S), 3(R)-Дигидрокси-20(S)-[4-метил-4-гидроксипент- 2-ен-1-илтио]-9,10-сек-прегна-5(Z), 7(E), 10(19)-триен(соединение 120)
Способ: общая методика 4.
Исходный материал: соединение 61.
Пример 21: 1(S), 3(R)-Дигидрокси-20(R)-[4-метил-4-гидроксипент- 2-ен-1-илтио]-9,10-сек-прегна-5(Z), 7(E), 10(19)-триен(соединение 121)
Способ: общая методика 4.
Исходный материал: соединение 62.
Пример 22: 1(S), 3(R)-Дигидрокси-20(S)-[4-метил-4-гидроксипент-2-ен-1-илтио]-9,10-сек-прегна-5(Z), 7(E), 10(19)-триен(соединение 122)
Способ: общая методика 4.
Исходный материал: соединение 63.
Пример 23: 1(S), 3(R)-Дигидрокси-20(R)-[5-этил-5-гидрокси -1-гептил-(R)-сульфинил)-9,10-сек-прегна-5(Z), 7(E), 10(19)-триен (соединение 123)
Способ: общая методика 4.
Исходный материал: соединение 64.
Пример 24: 1(S), 3(R)-Дигидрокси-20(R)-[5-этил-5-гидрокси-1-гептил-(S)-сульфинил)-9,10-сек-прегна-5(Z), 7(E), 10(19)-триен (соединение 124)
Способ: общая методика 4.
Исходный материал: соединение 65.
Пример 25: 1(S), 3(R)-Дигидрокси-20(S)-(5-этил-5-гидрокси-1- гептил-(R)-сульфинил)-9,10-сек-прегна-5(Z), 7(E), 10(19)-триен (соединение 125)
Способ: общая методика 4.
Исходный материал: соединение 66.
Пример 26: 1(S), 3(R)-Дигидрокси-20(S)-(5-этил-5-гидрокси-1- гептил-(S)-сульфинил)-9,10-сек-прегна-5(Z), 7(E), 10(19)-триен (соединение 126)
Способ: общая методика 4.
Исходный материал: соединение 67.
Пример 27: 1(S), 3(R)-Дигидрокси-20(R)-(5-этил-5-гидрокси-1- гептилсульфонил)-9,10-сек-прегна-5(Z), 7(E), 10(19)-триен (соединение 127)
Способ: общая методика 4.
Исходный материал: соединение 68.
Пример 28: 1(S), 3(R)-Дигидрокси-20(S)-(5-этил-5-гидрокси-1- гептилсульфонил)-9,10-сек-прегна-5(Z), 7(E), 10(19)-триен (соединение 128)
Способ: общая методика 5.
Исходный материал: соединение 69.
Пример 29: 1(S), 3(R)-Дигидрокси-20(R)-[3-(1-метил-1-гидроксиэтил)бензил-(R)-сульфонил]-9,10-сек-прегна-5(Z), 7(E), 10(19)-триен(соединение 129)
Способ: общая методика 4.
Исходный материал: соединение 70.
Пример 30: 1(S), 3(R)-Дигидрокси-20(R)-[3-(1-метил-1- гидроксиэтил)бензил-(S)-сульфинил]-9,10-сек-прегна-5(Z), 7(E), 10(19)-триен(соединение 130)
Способ: общая методика 4.
Исходный материал: соединение 71.
Пример 31: 1(S), 3(R)-Дигидрокси-20(S)-[3-(1-метил-1-гидроксиэтил)бензил-(R)-сульфинил]-9,10-сек-прегна-5(Z), 7(E), 10(19)-триен(соединение 131)
Способ: общая методика 4.
Исходный материал: соединение 72.
Пример 32: 1(S), 3(R)-Дигидрокси-20(S)-[3-(1-метил-1- гидроксиэтил)бензил-(S)-сульфинил]-9,10-сек-прегна-5(Z), 7(E), 10(19)-триен(соединение 132)
Способ: общая методика 4.
Исходный материал: соединение 73.
Пример 33: 1(S), 3(R)-Дигидрокси-20(R)-[3-(1-метил-1- гидроксиэтил)бензил-сульфонил] -9,10-сек-прегна-5(Z), 7(E), 10(19)-триен(соединение 133)
Способ: общая методика 5.
Исходный материал: соединение 74.
Пример 34: 1(S), 3(R)-Дигидрокси-20(S)-[3-(1-метил-1- гидроксиэтил)бензил-сульфонил] -9,10-сек-прегна-5(Z), 7(E), 10(19)-триен(соединение 134)
Способ: общая методика 5.
Исходный материал: соединение 75.
Пример 35: 1(S), 3(R)-Дигидрокси-20-(R)-(3-метил-3-гидрокси-1- бутилтио)-9,10-сек-прегна-5(Z), 7(E), 10(19)-триен(соединение 135).
Способ: общая методика 5.
Исходный материал: соединение 76.
ЯМР : δ = 0,62 (s, 3H), 1,24 (s, 6H), 1,30 (d, 3H), 1,10-2,10 (m, 18H), 2,31 (dd, 1H), 2,45 (m, 1H), 2,61 (m, 2H), 2,70 (m, 1H), 2,82 (m, 1H), 4,23 (m, 1H), 4,43 (m, 1H), 5,00 (m, 1H), 5,33 (m, 1H), 6,01 (d, 1H), 6,38 (d, 1H).
Пример 36: 1(S), 3(R)- Дигидрокси-20-(S)-(3-метил-3-гидрокси- 1-бутилтио)-9,10-сек-прегна-5(Z), 7(E),10(19)-триен(соединение 136).
Способ: общая методика 5.
Исходный материал: соединение 77.
ЯМР : δ = 0,58 (s, 3H), 1,25 (s, 6H), 1,39 (d, 3H), 1,20-2,10 (m, 18H), 2,31 (dd, 1H), 2,59 (m, 1H), 2,63 (m, 2H), 2,69 (m, 1H), 2,83 (m, 1H), 4,23 (m, 1H), 4,44 (m, 1H), 4,99 (m, 1H), 5,33 (m, 1H), 6,02 (d, 1H), 6,36 (d, 1H).
Пример 37: капсулы, содержащие соединение 103
Соединение 103 растворяют в арахисовом масле до конечной концентрации 1 μг/мл масла. Десять весовых частей желатина, 5 весовых частей глицерина, 0,08 весовых частей сорбата калия и 14 весовых частей дистиллированной воды смешивают вместе при нагреве и формуют в мягкие желатиновые капсулы. Последние затем наполняют каждую 10 μл масляного раствора соединения 103.
Пример 38: дерматологический крем, содержащий соединение 103
Соединение 103 (0,05 мг) растворяют в миндальном масле (1 г). К этому раствору добавляют минеральное масло (40 г) и самоэмульсифицирующийся пчелиный воск (20 г). Смесь нагревают до растапливания. После добавления горячей воды (40 мл) смесь тщательно перемешивают. Полученный в результате крем содержит приблизительно 0,5 μг соединения 103 на грамм крема.
Дополнительные экспериментальные данные
Биологическое тестирование. Влияние на раковые клетки in vitro.
Исследование клеточного роста осуществляли с использованием опухолевой клеточной линии человеческой гистиоцитемической лимформы U937 (Американская коллекция типовых культур - American Type Gulture Collection) (Rockville, MD). Клетки U937 доводили до 1 • 105 клеток/мл в RPMI 1640 (Gibco, США). В среду добавляли 2 мМ глутамина, 100 М.Е./мл пенициллина, 10 мкг/мл стрептомицина и 10% фетальной телячьей сыворотки (FCS/Gibco). Клетки (5 мл) инкубировали в увлажненной атмосфере в течение 96 часов при 37oC в присутствии 1,25 (OH)2 D3 или аналогов витамина D (от 10-12 до 10-7 М). К контрольным культурам добавляли 0,2% растворителя. В конце инкубирования клетки были сосчитаны и концентрация тестируемого соединения, приводящая к 50% ингибированию (IC50) роста клеток, рассчитывалась из кривой доза-ответ. Типичное значение IC50 для 1,25 (OH)2D3 составляло 5 • 10-8 М. Каждый эксперимент включал контрольный эксперимент в присутствиt и в отсутствии 1,25 (OH)2D3.
Влияние на гиперпролиферацию клеток кожи in vitro.
Самопроизвольно иммортализованная клеточная линия незлокачественного человеческого псориаза HaCaT была предоставлена доктором N.E.Fusenig, Немецкий Научно-исследовательский центр рака (German Cancer Research Center) (Гейдельберг, Германия) и банком опухолей (Tumorbank), DKFZ (Гейдельберг). Клетки растили в среде феноловый красный - свободная среда Дульбекко, модифицированная по способу Игла, с добавлением 2 мМ глутамина, 100 М.Е./мл пенициллина, 100 мкг/мл стрептомицина и 5% фетальной телячьей сыворотки (FCS/Gibco). Клетки высеивали при плотности 1 • 104 клеток на лунку на мультипланшеты. Тестируемые соединения (1,25 (OH)2D3 или аналоги витамина D (от 10-11 до 10-7 М) добавляли спустя 2 часа после посева. После инкубации в увлажненной атмосфере в течение 120 часов при 37oC, синтез ДНК определяли посредством внедрения тимидина: 1 мкСи/мл H3 - меченного тимидина - добавляли к клеткам и кластеры инкубировали в течение 4 часов. Затем клетки промывали трижды NaCl+25 мг/л немеченного тимидина, солюбилизировали в течение 5-10 минут в 1 мл 0,5 М раствора NaOH. Внедренный [H3] тимидин измеряли счетчиком бета-излучения. Рассчитывали концентрацию, приводящую к 50% максимального ответа (IC50). Типичные значения IC50 для 1,25 (OH)2D3 составляло 5 • 10-8 М. Каждый эксперимент включал контрольное определение в присутствии и в отсутствие 1,25 (OH)2D3, и каждый образец тестировался четырехкратно.
Значения, полученные для U937 и HaCaT, приведенные в таблице, относятся к величине для 1,25 (OH)2D3, то есть представляют собой соотношение между IC50 для 1,25 (OH)2D3 и IC50 для аналога витамина D (соединение по изобретению). Табличные значения (см. в табл.3 в конце описания) больше 1, таким образом, указывают, что при исследовании соединение было более активным и сильнодействующим, чем 1,25 (OH)2D3.
Пример 1
ЯМР δ = 0,62 (с, 3H), 0,86 (д, 3H), 0,87 (т, 6H), 1,10-3,00 (м, 28H), 4,23 (м, 1H), 4,43 (м, 1H), 4,99 (м, 1H), 5,33 (м, 1H), 6,01 (д, 1H), 6,37 (д, 1H).
Пример 2
ЯМР δ = 0,58 (с, 3H), 0,87 (т, 6H), 0,88 (д, 3H), 1,10-3,00 (м, 28H), 4,22 (м, 1H), 4,42 (м, 1H), 4,99 (м, 1H), 5,33 (м, 1H), 6,02 (д, 1H), 6,36 (д, 1H).



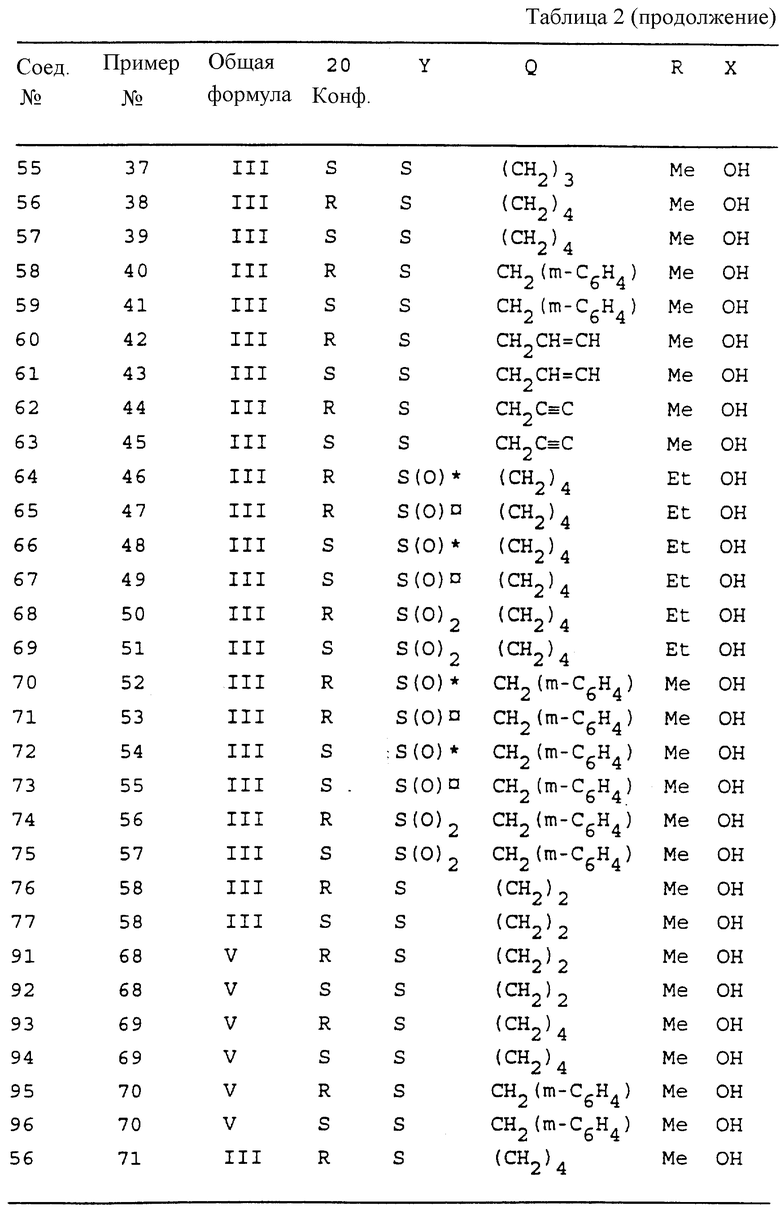
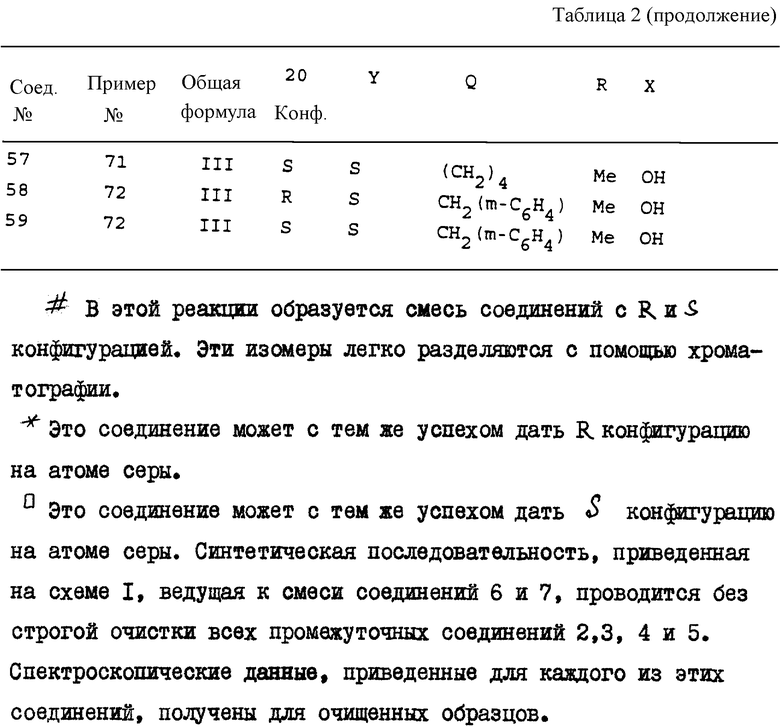

Аналоги витамина D общей формулы I, где Y - сера, R - С1-С3-алкил, или R-С-R может образовывать бензильный радикал, Q - С2-С4-алкилен, причем одна или более гидроксигрупп защищены в виде групп, которые могут быть преобразованы в гидроксигруппы in vivo, проявляют противовоспалительные и иммуномодулирующие эффекты, также как и сильную активность при индуцировании дифференциации и ингибировании нежелательной пролиферации определенных клеток. 4 с. и 5 з.п. ф-лы, 2 табл. 
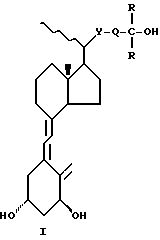
где Y является серой;
R является С1-С3-алкилом или 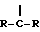 может образовывать бензильный радикал;
может образовывать бензильный радикал;
Q является С2-С4-алкиленом, причем одна или более гидроксигрупп защищены в виде групп, которые могут быть преобразованы в гидроксигруппы in vivo.
где N -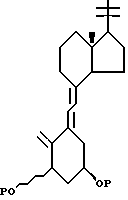
Р представляет защитную силильную группу,
b) соединение формулы 2 подвергают замещению калий-0-этилдитиокарбонатом с образованием соединения общей формулы 3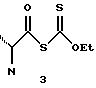
где N имеет значение, указанное выше;
с) соединение формулы 3 подвергают фотохимической реакции в инертной среде, например бензоле, в ходе которой первоначально полученный ацильный радикал декарбонилируют при соответствующей температуре с образованием алкильных радикалов, которые преимущественно соединяются с О-этилдитиокарбонатными радикалами с образованием двух С-20 изомеров общих формул 4 и 5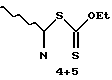
где N имеет значение, указанное выше,
d) полученное соединение формулы 4 и 5 или их смесь обрабатывают аминоэтанолом и превращают в тиолы общей формулы 6 или 7 или их смесь
где N имеет указанное значение,
е) далее полученное соединение формулы 6 или 7 или их смесь подвергают действию основания, например карбоната калия, в растворителе, например диметилформамиде, и с соответствующим алкилирующим агентом общей формулы IV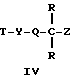
где R, Q имеют указанные значения;
Z представляет защитную группу;
Т представляет соответствующую уходящую группу, например бромид, с получением соединения общей формулы II в виде смеси двух С-20 изомеров или в виде энантиомерно чистых форм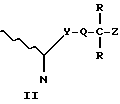
где N, Y, Q, Z и R имеют указанные значения;
f) после чего соединение формулы II подвергают в произвольной последовательности изомеризации под действием ультрафиолетового света в присутствии триплетного сенсибилизатора, например антрацена, и удалению защитных групп, например силильных групп, плавиковой кислотой или тетра-н-бутиламмонийфторидом с образованием желаемого соединения общей формулы I по п.1, в энантиомерно чистой форме или в виде стереоизомерной смеси.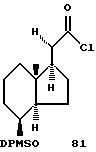
а) подвергают взаимодействию с трет-бутилгипохлоритом с получением соответствующего кислого хлорида; b) который далее вводят в реакцию замещения О-этилдитиокарбонатом калия с получением соединения общей формулы 82
где Р представляет защитную группу, например силильную группу;
с) соединение формулы 82 подвергают фотохимической реакции в инертной среде, например бензоле, в ходе которой первоначально полученный ацильный радикал декарбонилируют при соответствующей температуре с образованием алкильных радикалов, которые преимущественно соединяются с О-этилдитиокарбонатными радикалами с образованием двух С-20 изомеров общих формул 83 или 84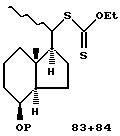
где Р имеет указанное значение;
d) полученное соединение формулы 83 или 84 их смесь подвергают удалению защитных групп, например силильной группы, плавиковой кислотой или тетра-н-бутиламмонийфторидом с образованием соответствующих гидроксисоединений, е) с последующим окислением, например реагентом на основе диметилсульфоксида с получением кетонов, f) которые далее обрабатывают аминоэтанолом и превращают в тиолы формулы 89 или 90 или их смесь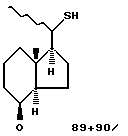
g) соединение формулы 89 или 90 или их смесь подвергают реакции с основанием, например карбонатом калия, в растворителе, например диметилформамиде, и соответствующим алкилирующим агентом формулы IV по п.5 для получения соединения формулы V в виде смеси изомеров или в энантиомерно чистой форме
где Y, Q, Z и R имеют указанные в п.5 значения;
h) и полученное соединение формулы V или смесь его изомеров связывают с анионом [1Z, 3S, 5R] -[2-[3,5-бис-[трет-бутилдиметилсилилокси]-2-метиленциклогексилиден] этил] дифенилфосфиноксида в реакции Хорнера-Виттига с образованием продукта формулы III в виде смеси стереоизомеров или в виде энантиомерно чистых форм
где Y, Q, Z и R имеют указанные значения;
TBDVS представляет тетрабутилдиметилсилил;
i) полученное соединение формулы III или его смесь подвергают удалению защитных групп, например, тетра-н-бутиламмонийфторидом или плавиковой кислотой с получением целевых продуктов общей формулы I по п.1.
| ФОРСУНКА | 1928 |
|
SU9992A1 |
| Chem | |||
| Pharm | |||
| Bull., 34, 4410 - 4413, 1986 | |||
| Chem | |||
| Pharm | |||
| Bull., 39, 3221 - 3224, 1991 | |||
| Тринус Ф.П | |||
| Фармако-терапевтический справочник | |||
| - Киев, Здоровья, 1989, с.288 | |||
| Способ лечения псориаза | 1986 |
|
SU1445729A1 |
| Пожарный двухцилиндровый насос | 0 |
|
SU90A1 |
| US 4749710, 1988. | |||
Авторы
Даты
1999-09-10—Публикация
1993-12-17—Подача