Изобретение относится к определенным 4(3H)-хиназолинонам, их агрохимически приемлемым солям и композициям и способам их применения в качестве фунгицидов общего действия или селективных фунгицидов, в частности, для борьбы с настоящей мучнистой росой злаков как для профилактики, так и в случае заражения.
В патентах США 3755582 и 3867384 описаны некоторые 4(3H)-хиназолиноновые фунгициды. В этих патентах, однако, не описаны соединения в соответствии с данным изобретением.
Сущность изобретения
Данное изобретение относится к замещенным 4(3H)-хиназолинонам формулы I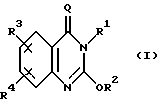
в которой Q является О;
R1 означает C3-C10 алкил или циклопропилметил;
R2 означает C3-C10 алкил;
R3 означает галоген; и
R4 означает водород или галоген;
при условии, что когда R1 является циклопропилметилом, R2 является CH2CH2CH3, R3 является 6-Br и R4 является H, обладающим фунгицидной активностью.
Предпочтительным является соединение 1, в котором R1 является C3-C8-алкилом и R2 является C3-C8 алкилом, а также cоединения группы, включающей 6-бром-3-пропил-2-пропилокси- 4(3H)-хиназолинон и 6-йод-3-пропил-2-пропилокси-4(3H)-хиназолинон.
Еще более предпочтительны соединения, которые выбирают из группы, включающей 6-бром-3-(циклопропилметил)-2-пропилокси- 4(3H)-хиназолинон и 6,8-дийод-3-пропил-2-пропилокси-4(ЗН)-хиназолинон.
Также предпочтительны соединения, выбранные из группы, включающей соединения 1, где
(1) R1 означает н-пропил, н-децил, изо- или н-бутил, изопропил, н-пентил, н-гексил или втор-бутил, R2 означает н-пропил и либо R4 является водородом, a R3 является 6-Br или 6-J, либо R4 является 8-J, a R3 является 6-J;
(2) соединения 1 где: R1 представляет н-пропил, R2 представляет изобутил, н-децил, трет-бутил, втор-бутил, изопропил, н-пентил, н-бутил или н-гексил и либо R4 является водородом, а R3 является 6-Br или 6-J, либо R4 является 8-J, a R3 является 6-J;
(3) соединения 1, где: R1 и R2 оба представляют н-пропил, и R3 является 6-J, a R4 является 8-Br или 8-J, R3 является 6-Cl, a R4 является 8-Cl; R3 является 6-Br, a R4 является 8-Cl или 7-Br, или R3 является 8-Br, a R4 является H;
(4) соединения 1, где: R1 представляет CH2CH2CH3, R2 представляет CH2CH2CH3, R4 представляет H и R3 представляет 6-Br, 7-Cl, 5-Cl, 7-F, 6-F, 6-Cl или 6-J;
(5) соединения 1, где: R1 представляет CH2CH2CH3, R3 представляет 6-Br; R4 представляет водород и R2 представляет (CH2)3CH3, изопропил, (CН2)4CH3, (CH2)5CH3 или CH2CH2C(CH3)3;
(6) соединения 1, где: R1 представляет CH2CH2CH3, R2 представляет CH2CH2CH3 и R3 и R4 представляют 6-Cl и 8-Cl, 6-Br и 8-Br или 6-J и 8-J;
(7) соединения 1, где: R1 представляет CH2CH2CH3, R3 представляет 6-Cl, R4 представляет водород и R2 представляет изопропил или (CH2)4CH3;
(8) соединения 1, где: R1 представляет (CH2)3CH3, R2 представляет CH2CH2CH3 или (CH2)3CH3, R3 - 6-Br, R4 - водород;
(9) соединения 1, где: R1 представляет CH2CH2CH3, R3 представляет 6-J, R4 представляет водород и R2 представляет (CH2)4CH3 или CH2CH2CH2CH3; (10) соединения 1, где: R2 представляет CH2CH2CH3, R3 представляет 6-Br, R4 представляет водород и R1 представляет CH2CH(CH3)2, (циклопропил) CH2 или CH(CH3)этил;
(11) соединение 1, где: R1 и R2 оба являются (CH2)4CH3, R3 представляет 6-Br и R4 представляет H; и
(12) соединения 1, где: R1 представляет (CH2)3CH3, R3 представляет 6-J, R4 представляет водород и R2 представляет (CH2)3CH3 или CH2CH2CH3.
Особенно предпочтительно фунгицидное соединение, которое представляет собой 6-йод-3-пропил-2-пропилокси-4(3H)-хиназолинон.
Следующим аспектом изобретения является фунгицидная композиция для борьбы с мучнистой росой пшеницы, включающая эффективное количество соединения по п.1 и по меньшей мере один из: (а) ПАВ, (b) органического растворителя и (с) по меньшей мере одного твердого или жидкого разбавителя.
Особенно предпочтительна фунгицидная композиция для борьбы с мучнистой росой пшеницы, включающая эффективное количество 6-йод-3- пропил-2-пропилокси-4(3H)-хиназолинона.
Следующим аспектом изобретения является способ борьбы с мучнистой росой пшеницы, включающий нанесение на растение или часть растения, которую необходимо защитить, производного 4(3H)-хиназолинона, отличающийся тем, что в качестве производного 4(3H)-хиназолинона используют соединение по п.1 в эффективном количестве.
Еще одним аспектом изобретения является способ борьбы с мучнистой росой, включающий использование 6-йод-3-пропил-2-пропилокси- 4(3H)-хиназолинона в эффективном количестве.
Далее изобретение иллюстрируется следующими неограничивающими примерами.
Пример 1.
Синтез 6-бром-3-пропил-2-пропилокси-4(3H)-хиназолинона
Все реакции проводят в атмосфере азота.
Стадия А.
К раствору 200 мл этанола, содержащего 37 г 2-амино-5- бромбензойной кислоты, добавляют по каплям 17,72 мл н-пропилизотиоцианата при перемешивании. Смесь нагревают с обратным холодильником в течение 8 час, оставляют охлаждаться до комнатной температуры и перемешивают примерно 60 час.
Смесь затем охлаждают до примерно 5oC и отфильтровывают, получая 15,42 г твердого вещества почти белого цвета.
Стадия Б.
К раствору, содержащему 15,4 г продукта со стадии А в 100 мл 10%-ного гидроксида натрия в пропаноле, добавляют 3,2 мл иод метана при перемешивании. Смесь перемешивают при комнатной температуре 10 мин, затем нагревают с обратным ' холодильником 1,5 час и затем оставляют охлаждаться до комнатной температуры и перемешивают в течение ночи. Реакционную смесь отфильтровывают, получая 11,47 г белого твердого вещества. Это твердое вещество очищают методом колоночной хроматографии на силикагеле, используя в качестве элюента гексан и затем 9:1 гексан:этилацетат. Отбор и выпаривание фракций, содержащих наименее полярный компонент (в соответствии с тонкослойной хроматографией, 6:1 гексан/этилацетат в качестве проявляющего растворителя), приводит к получению 6,55 г белого вещества с температурой плавления 97-99oC.
Стадия В.
К 150 мл пропанола, охлажденного до примерно -60oC, добавляют 0,83 г NaH (60% активного вещества в масле) при перемешивании. К этой смеси при -60oC добавляют 6,5 г очищенного продукта, полученного на стадии Б. Смесь оставляют нагреваться до комнатной температуры и перемешивают в течение примерно 48 час с получением прозрачного раствора. Раствор выливают в воду и дважды экстрагируют диэтиловым эфиром. Эфирные экстракты дважды промывают водой, сушат над сульфатом магния, фильтруют и затем выпаривают, получая 10,3 г масла. Метод тонкослойной хроматографии показывает наличие как исходного вещества, так и целевого продукта.
Стадия Г.
К пропанолу, охлажденному до -50oC, добавляют 0,60 г NaH (60% активного вещества в масле) при перемешивании. К этой смеси при -40oC добавляют продукт со стадии В и оставляют смесь нагреваться до комнатной температуры и перемешивают ~ 72 час. Затем смесь нагревают с обратным холодильником 30 мин, охлаждают до комнатной температуры, выливают в воду и дважды экстрагируют диэтиловым эфиром.
Соединенные эфирные экстракты трижды промывают водой, сушат над сульфатом магния, фильтруют и выпариванием фильтрата получают масло. Масло очищают методом хроматографии на силикагеле, элюируя гексаном и затем смесью 9:1 гексан/этилацетат. Отбор и выпаривание этих фракций, содержащих только наименее полярный компонент (тонкослойная хроматография на силикагеле, смесь 9:1 гексан/этилацетат в качестве проявляющего растворителя), приводит к получению 4,46 г соединения, указанного в названии, в виде твердого вещества белого цвета с температурой плавления 57-59oC: 1H ЯМР (400 МГц, CDCl3) 8,3 (s, 1H), 7,7 (m, 1H), 7,3 (m, 1H), 4,43 (t, 2H), 4,05 (t, 2H), 1,85 (m, 2H), 1,7 (m, 2H), 1,06 (t, 3H), 0,97 (t, 3H).
Пример 2.
Синтез 6-бром-3-н-бутил-2-н-пропиламино-4(3H)-хиназолинона
Стадия А.
К раствору 200 мл этанола, содержащего 15,15 г 2-амино-5- бромбензойной кислоты добавляют по каплям 9,3 мл н-бутил-изотиоцианата при перемешивании. К этому раствору добавляют 9,77 мл триэтиламина. Раствор нагревают с обратным холодильником 4 час, при этом осаждается твердое вещество. Реакционную смесь охлаждают до 0oC и фильтруют, получая 19,89 г почти белого твердого вещества с температурой плавления 246-248oC.
Стадия Б.
К раствору, содержащему 7 г продукта со стадии А, суспендированного в 50 мл хлороформа, добавляют 1,97 мл сульфурилхлорида при перемешивании. Раствор нагревают с обратным холодильником 5 час, затем охлаждают до комнатной температуры. Раствор выливают в воду и дважды экстрагируют метиленхлоридом. Органические экстракты сушат над сульфатом магния, фильтруют и затем выпаривают фильтрат с получением желтого твердого вещества. Его очищают хроматографией на силикагеле, элюируя смесью 6:1 гексан/этилацетат. Отбор и выпаривание фракций, содержащих только полярный компонент (тонкослойная хроматография на силикагеле, смесь 4:1 гексан/этилацетат в качестве проявляющего растворителя) приводит к получению 3,2 г белого твердого вещества с температурой плавления 56-58oC.
Стадия В.
К раствору, содержащему 1,02 г очищенного продукта со стадии Б, растворенного в тетрагидрофуране, добавляют 0,5 мл н-пропиламина. Реакционную смесь перемешивают в течение ~ 24 час при комнатной температуре. Затем смесь фильтруют и фильтрат выпаривают с получением масла. Масло растворяют в диэтиловом эфире и дважды промывают водой и один раз солевым рассолом. Эфирный раствор сушат над сульфатом магния, фильтруют и фильтрат выпаривают, получая 0,74 г конечного продукта в виде белого твердого вещества с температурой плавления 71-73oC: 1H ЯМР (400 МГц, CDCl3) 0,97-1,04 (m, 6H), 1,45 (m, 2H), 1,70 (m, 4H), 3,50 (m, 2H), 4,00 (t, 2H), 4,50 (8, 1H), 7,24 (d, 1H), 7,60 (d, 1H), 8,60 (s, 1H).
Пример 3.
Синтез 6-бром-3-н-пропил-2-н-пропилтио-4(3H)-хиназолинона
Стадия А.
К раствору 150 мл изопропанола, содержащего 29,7 г 2-амино-5-бромбензойной кислоты, по каплям добавляют 15,64 мл н-пропилизотиоцианата при перемешивании. Затем смесь нагревают 15 час с обратным холодильником. Смесь охлаждают до 0oC и фильтруют, получая 9,12 г твердого вещества почти белого цвета.
Стадия Б.
К раствору, содержащему 0,34 г продукта со стадии А, суспендированного в 20 мл хлороформа, 10%-ного гидроксида натрия в пропаноле, добавляют 0,22 мл йодпропана при перемешивании. Смесь перемешивают 1,5 час при комнатной температуре. Смесь выливают в воду и дважды экстрагируют метиленхлоридом. Экстракты в метиленхлориде дважды промывают водой, сушат над сульфатом магния, фильтруют и затем выпаривают фильтрат с получением белого твердого вещества. Его очищают хроматографией на силикагеле, элюируя смесью 8:1 гексан/этилацетат. Отбор и выпаривание фракций, содержащих только наименее полярный компонент (тонкослойная хроматография на силикагеле, смесь 6:1 гексан/этилацетат в качестве проявляющего растворителя) приводит к получению 0,27 г целевого продукта в виде белого твердого вещества с температурой плавления 65-67oC. 1H ЯМР (400 МГц, CDCl3) 0,99-1,10 (m, 6H), 1,80 (m, 4H), 3,25 (t, 2H), 4-10 (t, 2H), 7,41 (d, 1H), 7,78 (d, 1H), 8,30 (s, 1H).
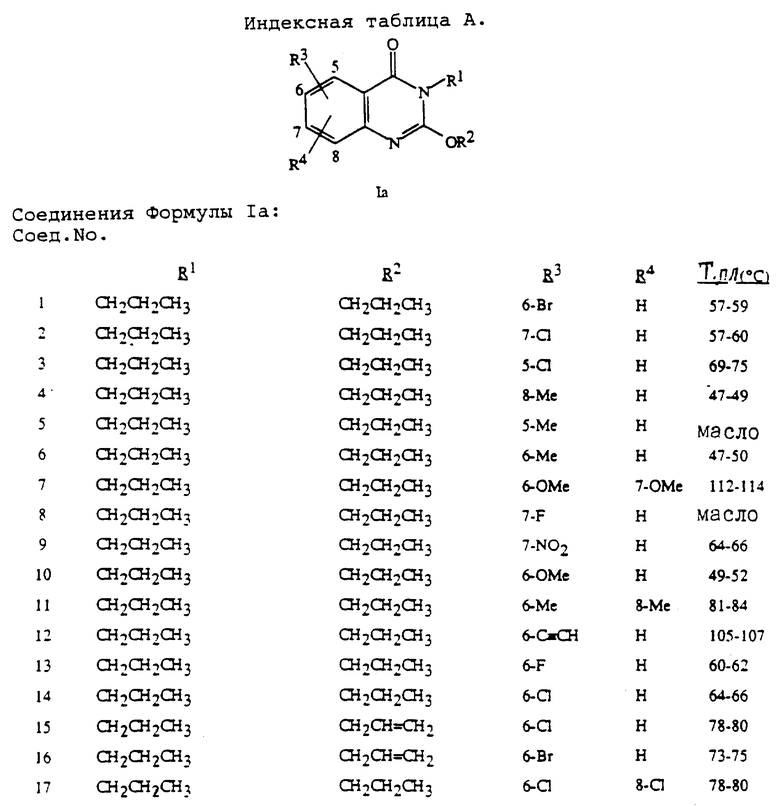
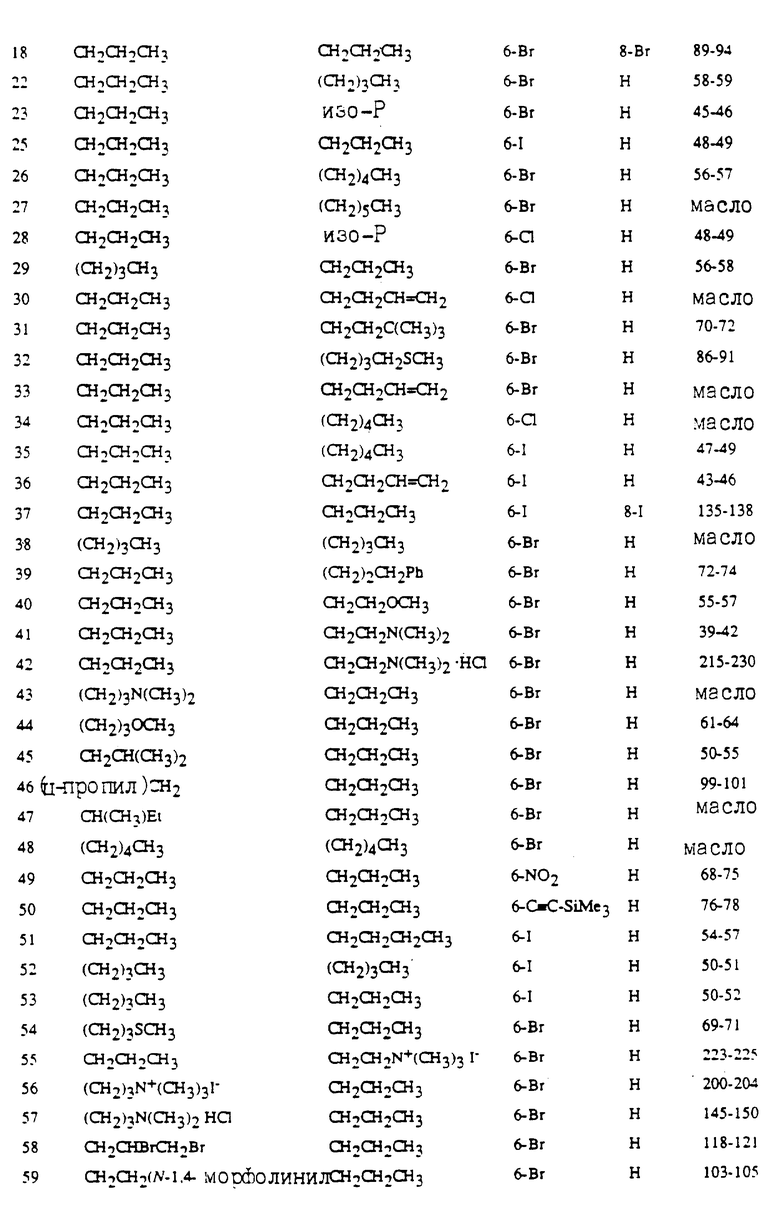
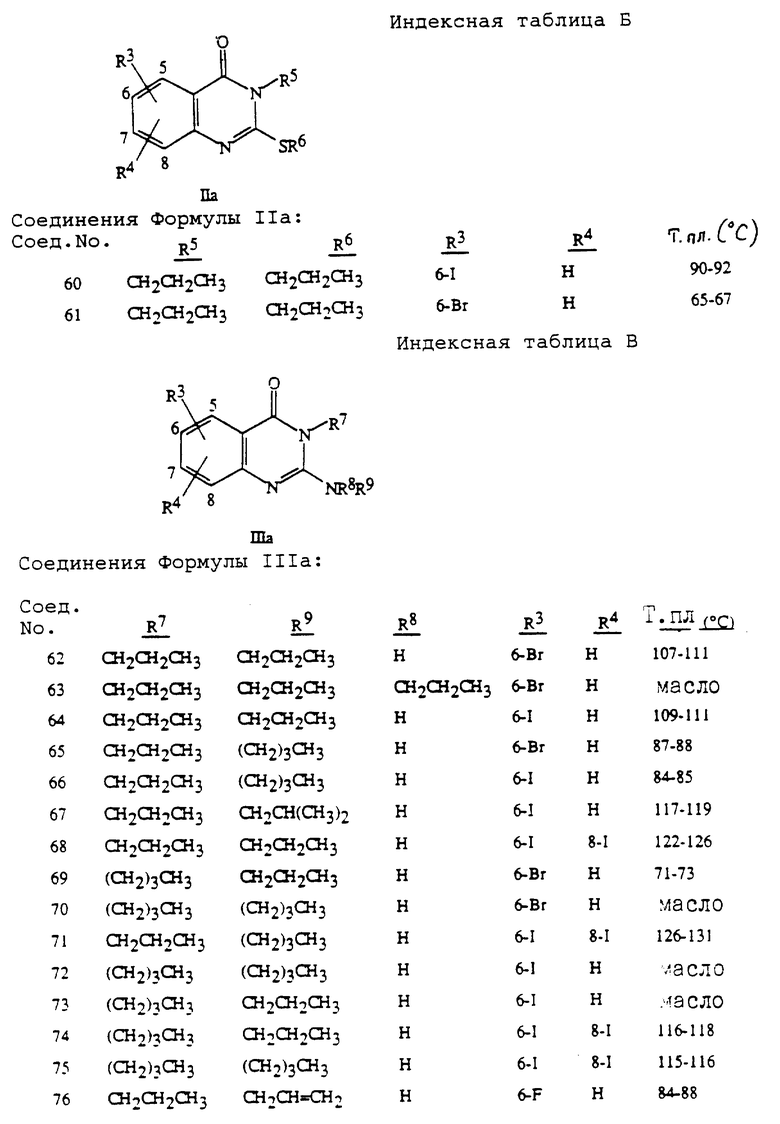
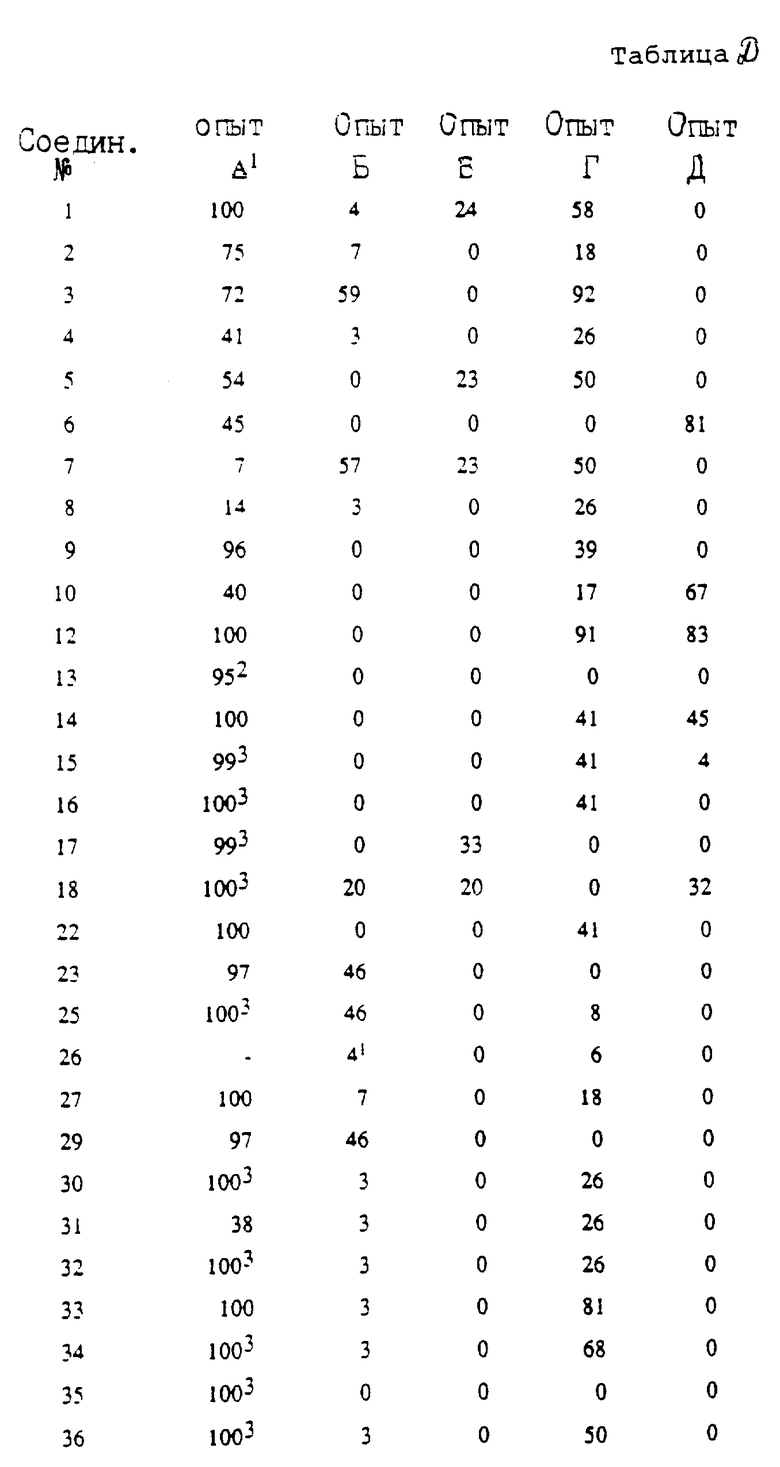
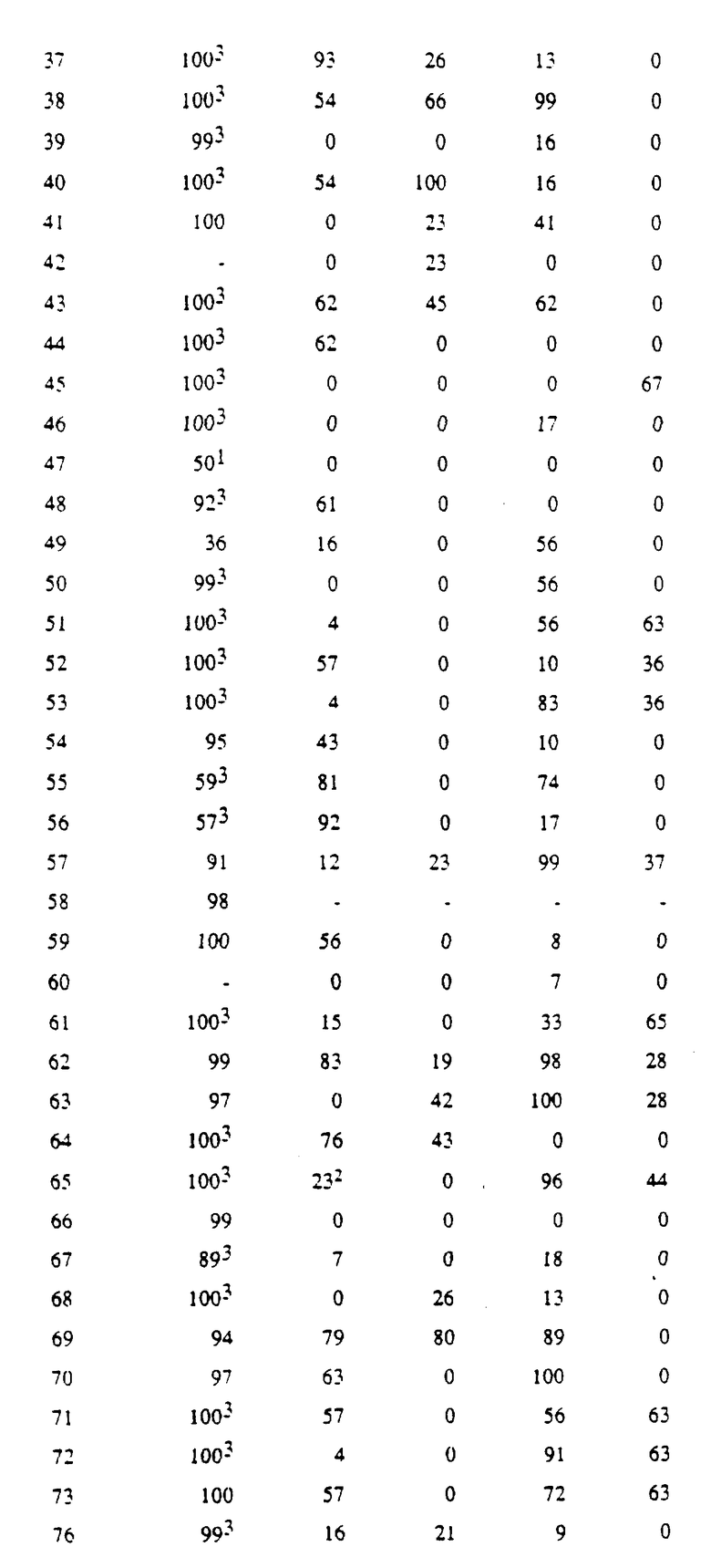
Используя методику примеров 1-3, можно получить соединения, представленные в таблицах (см. в конце текста).
В нижеследующих таблицах используют следующие сокращения. Все алкильные группы являются нормальными изомерами, если не оговорено иное. Структурные формулы см. в индексных таблицах А-В, где указана нумерация в циклических системах:
трет. = третичный
втор. = вторичный
n=нормальный
изо = изо
Me = метил
Et = этил
Ph = фенил
MeO = метокси
Pr = пропил
CN = циано
ц = цикло
MeS = метилтио
Bu = бутил
В нижеследующих таблицах a=1H ЯМР для масел помещены в индексной таблице Г.
Рецептуры/применение
Соединения по изобретению обычно используют в рецептурах в агрохимических композициях. Фунгицидные композиции по изобретению содержат эффективное количество, по меньшей мере, одного соединения формулы I, II или III, указанных выше, и, по меньшей мере, один из (а) поверхностно-активного агента, (б) органического растворителя и (в), по меньшей мере, одного твердого или жидкого разбавителя. Пригодные рецептуры могут быть получены обычными путями. Они включают дусты, гранулы, таблетки, растворы, суспензии, смачивающиеся порошки, эмульгируемые концентраты, сухие текучие смеси и так далее.
Разбрызгиваемые рецептуры могут быть разведены в подходящей среде и использованы в объемах от одного до нескольких сотен л на га. Концентрированные композиции используют как промежуточные для приготовления рецептур. Рецептуры обычно содержат эффективные количества активного ингредиента, разбавитель и ПАВ в следующих количествах, в сумме составляющих 100 вес.% (табл. 1).
Типичные твердые разбавители описаны в Watrins, et.al., Handbook of Insecticide Dust Diluents and Carriers, 2nd Ed., Dorland Books, Caldwele, New Jersey. Типичные жидкие разбавители и растворители описаны в Marsden, Solvents Guide, 2nd Ed., Interscience, New York, (1950).
Поверхностно-активные вещества и их применение описаны в McCutcheon's Detergents and Emulsifiers Annual, Allured Publ. Corp., Ridgewood New Jersey, а также в Sisely and wood, Enceclopedia of Surface Active Agents, Chemical Publ. Co., Inc., New York, (1964). Все рецептуры могут содержать небольшие количества добавок для уменьшения вспенивания, спекания, коррозии, роста микробов и тому подобное.
Методы приготовления таких композиций хорошо известны. Растворы получают простым смешением ингредиентов. Мелкодисперсные твердые композиции получают смешением и обычно размельчением компонентов в молотковой мельнице или смесителе для жидкостей. Вододиспергируемые гранулы могут быть получены агломерированием тонкодисперсных порошковых композиций, см., например, Cross et al. , Pesticide Formulations, Washington D.C., (1988), pp.251-259. Суспензии готовят мокрым перемалыванием; см., например, патент США 3060084. Гранулы и таблетки могут быть получены разбрызгиванием активного вещества на предварительно сформованные гранулированные носители или методом агломерирования. См. Browning, Agglomeration Chemical Engineering, December 4, 1967, pp. 147-148 Perry's Chemical Engineer's Hand book, 4th Ed., McGraw-Hill, New York, (1963), pp.8-57 и следующие и WO 91/13546. Гранулы могут быть получены как описано в патенте США 4172714.
Вододиспергируемые и водорастворимые гранулы можно приготовить как описано в DE 3246493.
Дальнейшую информацию, касающуюся методики приготовления рецептур, см., патент США 3235361, кол. 6, строка 6 - кол.7, строка 19 и примеры 10-42; патент США 3309192, кол.5, строка 43 - кол.7, строка 62 и примеры 8, 12, 15, 39, 41, 52, 53, 58, 132, 1380140, 162-164, 166, 167 и 169-182; патент США 2891855, кол. 5, строка 66 - кол.5, строка 17 и примеры 1-4; Klingman, Weed Control as a Science, John Wiley and Sons, Inc., Nеw York, (1961), pp.81-96; и Hance et al., Weed Control Hand book, 8th Ed., Blackwell Scientific Publicationa, Oxford (1989).
В следующих примерах указаны проценты по весу и все рецептуры приготовлены обычными методами. Соединение 1 обозначает соединение, описанное в индексной таблице А (см. в конце текста).
Пример А
Смачивающийся порошок
Соединение 1 - 65,0%
полиэтиленгликолевый эфир додецилфенола - 2,0%
лигносульфонат натрия - 4,0%
силикоалюминат натрия - 6,0%
монтмориллонит (прокаленный) - 23,0%
Пример Б
Гранулы
Соединение 37 - 10,0%
гранулы аттапульгита (низколетучее вещество, 0,71/0,30 мм; U.S.S. N 25-50 сита) - 90,0%
Пример В
Экструдированные таблетки
Соединение 25 - 25,0%
безводный сульфат натрия - 10,0%
технический лигнинсульфонат кальция - 5,0%
алкилнафталинсульфонат кальция - 1,0%
кальциевый/магниевый бентонит - 59,0%
Пример Г
Эмульгируемый концентрат
Соединение 37 - 20,0%
смесь маслорастворимых сульфонатов и полиоксиэтиленовых эфиров - 10,0%
изофорон - 70,0%
Соединения по изобретению пригодны в качестве агентов для борьбы с болезнями растений, особенно для борьбы с настоящей мучнистой росой злаков (например, Erysiphe graminis f.sp.tritici, агент, вызывающий настоящую мучнистую росу у пшеницы). Данное изобретение далее относится к способу борьбы с болезнями растений, вызванными патогенными грибками, включающему нанесение на растение или его часть, которые надо защитить, или на семена растений или ростки эффективного количества соединения формулы I, II или III или фунгицидной композиции, содержащей указанное соединение. Соединения и композиции по изобретению обеспечивают борьбу с болезнями, вызванными широким спектром патогенными грибками классов Basidiomycete, Ascomycete, Oomycete и Deuteromycete. Они эффективны для борьбы с широким спектром болезней растений, особенно, лиственных патогенов декоративных, овощных, полевых, злаковых и фруктовых культур. Эти патогены включают Plasmopara viticola, Phytophthora infestans, Peronospora tabacina, Pseudoperonospora cubensia, Pythium aphanidermatum, Alternaria brassicae, Septoria nodorum, Cercosporidium personatum, Cercospora arachidicola, Pseudocercosporella herpotrichoides, Cercospora beticola, Botrytia cinerea, Monilinia fructicola, Pyricularia oryzae, Podosphaera leucotricha, Venturia inaequalis, Erysiphe graminis, Uncinula necatur, Puccinia recondita, Puccinia graminis, Hemileia vastatrix, Puccinia striiformis, Puccinia arachidis, Rhizoctonia solani, Sphaerotheca fuliginea, Fusarium oxysporum, Verticillium dahliae, Pythium aphanidermatum, Phytophthora megasperma и другие роды и виды, относящиеся к таким патогенам.
Соединения по изобретению можно также смешать с одним или несколькими другими инсектицидами, фунгицидами, нематоцидами, бактерицидами, акарицидами, химикалиями, репеллентами, аттрактантами, феромонами, стимуляторами питания или другими биологически активными соединениями с образованием многокомпонентного пестицида, обладающего даже более широким спектром агрохимической защиты. Примеры других защитных агентов, с которыми можно смешивать соединения по изобретению, включают инсектициды, такие как ацефат, авермектин В, азинфосметил, бифентрин, бифенат, бупрофезин, карбофуран, хлордимеформ, хлорпирифос, цифлутрин, дельтаметрин, диазинон, дифлубензурон, диметоат, эсфенвалерат, фенпропатрин, фенвалерат, фипронил, флуцитринат, флуфенпрокс, флувалинат, фонофос, изофенфос, малатион, метальдегид мета-мидофос, метидатион, метомил, метопрен, метоксихлор, монокротофос, оксамил, паратион-метил, перметрин, форат, фосалон, фосмет, фосфамидон, пиримикарб, профенофос, ротенон, сульпрофос, тербуфос, тетрахлорвинфос, тиодикарб, тралометрин, трихлорфон и трифлумурон; фунгициды, такие как беномил, бластицидин S, бромуконазол, каптафол, каптан, карбендазим, хлоронеб, хлорталонил, оксихлорид меди, соли меди, цимоксанил, ципроконазол, циродинил, дихлоран, диклобутраз дикломезин, дифеноконазол, диниконазол, додин, эдифенфос, эпоксиконазол, фенаримол, фенбуконазол, фенпропидин, фенпропиморф, флукинконазол, флусилазол, флутоланил, флутриафол, фолпет, фуралаксил, гексаконазол, ипконазол, ипробенфос, ипродион, изопротиолан, касугамицин, манкозеб, манеб, мепронил, металаксил, метконазол, миклобутанил, неоазозин, оксадиксил, пенконазол, пенцикурон, фосетил-Al, пробеназол, прохлораз, пропиконазол, пирифенокс, пириметанил, пирокилон, сульфур, тебуконазол, тетраконазол, тиабендазол, тиофанат-метил, тиурам, триадимефон, триадименол, трициклазол, тритиконазол, униконзол, валидамицин и винклозолин; нематоциды, такие как альдоксикарб, фенамифос, фостиетан; бактерициды, такие как окситетрациклин, стрептомицин и трехосновный сульфат меди; акарициды, такие как амитраз, бинапакрил, хлорбензилат, цигексатин, дикофол, диенохлор, окись фенбутатина, гекситиазокс, окситиокинокс, пропаргит и тебуфенпирад; и биологические агенты, такие как Bacillus thuringiensis и baculovirus.
В определенных случаях особенно предпочтительны комбинации с другими фунгицидами, имеющими сходный спектр борьбы, но другой метод действия. Предпочтительные комбинации включают соединение формулы I, II или III и фунгицид, выбранный из группы: флусилазол, ципроконазол, тетраконазол, фепропиморф, фенпропидин, цимоканил, беномил, карбендазим, манкозеб и манеб.
Борьбу с болезнями растений обычно осуществляют нанесением эффективного количества соединения по изобретению или до, или после заражения, на часть растения, подлежащего защите, такую как корни, стебли, листва, фрукты, семена, клубни или луковицы, или на среду (почву или песок), на которой произрастают растения, подлежащие защите. Соединения можно наносить на семена для защиты семян и сеянцев.
Дозы нанесения этих соединений зависят от многих факторов в окружающей среде и их следует определять в условиях применения. Листва может быть защищена при обработке дозой от менее 1 г/га до 5000 г/га в расчете на активное вещество. Семена и саженцы обычно защищены, если семена обрабатывают дозой от 0,1 до 10 г на кг семян.
Следующие испытания показывают эффективность соединений по изобретению по отношению к определенным патогенам. Борьба с патогенами при помощи соединений по изобретению не ограничена, однако, этими видами. Описание соединений см. индексные таблицы А, Б и В. Испытуемые соединения вначале растворяют в ацетоне в количестве, равном 3% от конечного объема, и затем суспендируют с концентрацией 200 ppm в очищенной воде, содержащей 250 ppm ПАВ'а TremR 014 (эфиры многоатомного спирта). Полученные суспензии используют при следующих испытаниях.
Испытание А.
Испытуемую суспензию разбрызгивают на ростки пшеницы. На следующий день ростки инокулируют спорами Erysiphe graminis f.sp.tritici (обычный возбудитель настоящей мучнистой росы пшеницы) и инкубируют в камере роста при 20oC в течение 7 дней, после чего оценивают результаты.
Испытание Б.
Испытуемую суспензию разбрызгивают на ростки пшеницы. Ha следующий день ростки инокулируют суспензией спор Puccinia recondita (обычный возбудитель листовой ржавчины пшеницы) и инкубируют в насыщенной атмосфере при 20oC в течение 24 час и затем перемещают в камеру роста при 20oC в течение 6 час, после чего оценивают результаты.
Испытание В.
Испытуемую суспензию разбрызгивают на рассаду томатов. На следующий день рассаду инокулируют суспензией спор Phytophtora infеstans (обычный возбудитель фитофтороза картофеля и томатов) и инкубируют в насыщенной атмосфере при 20oC в течение 24 час и затем перемещают в камеру роста при 20oC в течение 5 дней, после чего оценивают результаты.
Испытание Г.
Испытуемую суспензию разбрызгивают на саженцы винограда. На следующий день саженцы инокулируют суспензией спор Plasmopara viticola (обычный возбудитель ложной мучнистой росы винограда) и инкубируют в насыщенной атмосфере при 20oC в течение 24 час, помещают в камеру роста на 6 дней при 20oC и затем инкубируют в насыщенной атмосфере при 20oC в течение 24 час, после чего оценивают результаты.
Испытание Д.
Испытуемую суспензию разбрызгивают на рассаду огурцов. На следующий день рассаду инокулируют суспензией спор Botrytis cinerea (возбудитель серой плесени у многих культур) и инкубируют в насыщенной атмосфере при 20oC в течение 48 час и перемещают в камеру роста при 20oC в течение 5 дней, после чего оценивают результаты.
Результаты испытаний А-Д приведены в таблице Д. Показатель 100 означает 100% эффективность борьбы, а 0 означает отсутствие действия (по отношению к контрольным образцам), "-" означает "не испытывалось".
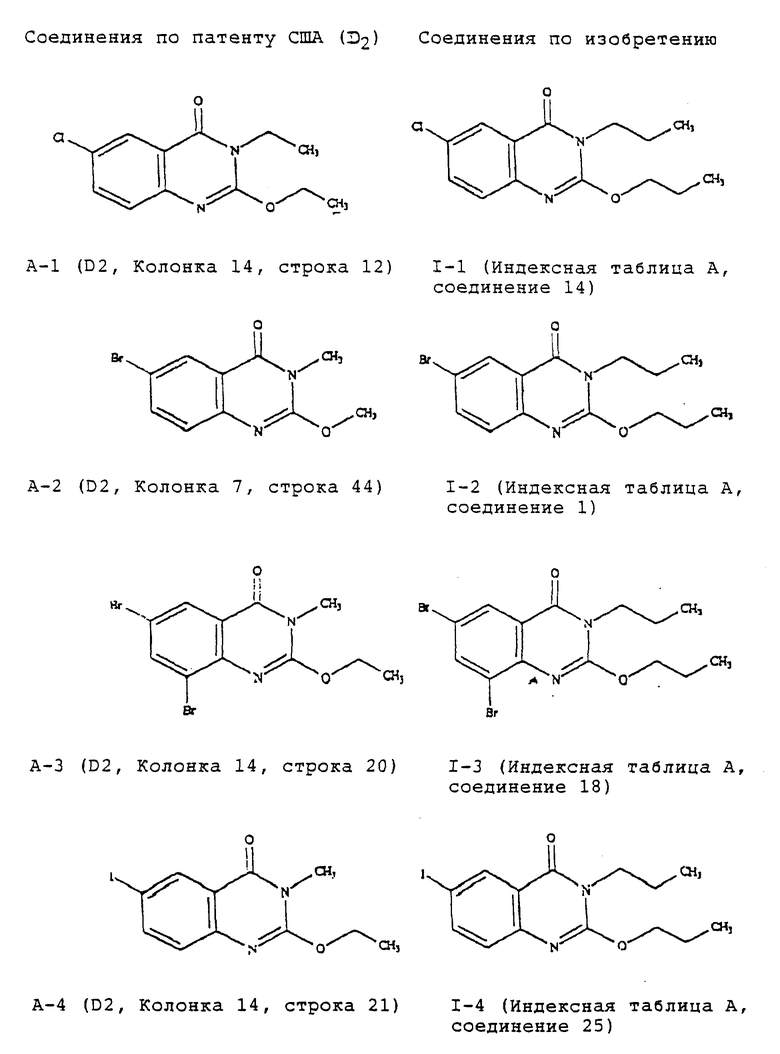
Данные эффективности сравнительного использования соединений А-1 - А-4, известных из предшествующего уровня техники, и соединений 1-1 - 1-4 настоящего изобретения для борьбы с мучнистой росой пшеницы. Методика испытаний та же, что приведена на стр. 50 заявки (испытание А; оценка 100 означает 100%-ное подавление заболевания, оценка 0 означает отсутствие подавления заболевания; ⊖ - отсутствие результатов испытания) (табл. 2).
Приведенные выше результаты показывают неожиданное превосходство соединений по изобретению в сравнении с ближайшим аналогом предшествующего уровня техники D2 (USP 3755582). Соединения по изобретению обеспечивают по существу полное подавление заболевания растений при использовании для борьбы с мучнистой росой пшеницы при норме расхода 2 ч/млн. Напротив, соединения-аналоги А-1 - А-4 обеспечивают значительно более слабый контроль при использовании их для борьбы с мучнистой росой пшеницы даже при более высоких нормах расхода (10 ч/млн). Эти данные ясно доказывают, что небольшие различия в структуре между соединениями аналогами и соединениями по изобретению действительно обеспечивают неожиданные преимущества соединений по изобретению в сравнении с соединениями предшествующего уровня техники. Замена коротких алкильных групп более длинными алкильными группами дает новые и неожиданно значительно более активные фунгицидные соединения.




Данное изобретение относится к определенным 4 (3Н)-хиназолинонам, их агрохимически приемлемым солям и композициям и способам их применения в качестве фунгицидов общего действия или селективных фунгицидов, в частности, для борьбы с настоящей мучнистой росой злаков как для профилактики, так и в случае заражения. Описываются вышеуказанные замещенные общей формулы I, где Q является O; R1 означает С3-C10 алкил или циклопропилметил; R2 означает С3-C10 алкил; R3 означает галоген; R4 означает водород или галоген, при условии, что когда R1 является циклопропилметилом, R2 является CH2CH2CH3, R3 является 6-Br и R4 является Н, обладающим фунгицидной активностью. 3 с. и 7 з.п.ф-лы, 7 табл.
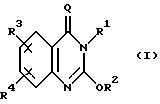
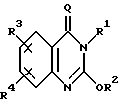
в которой Q является 0,
R1 означает C3-C10 алкил или циклопропилметил;
R2 означает C3-C10 алкил;
R3 означает галоген; и
R4 означает водород или галоген; при условии, что когда R1 является циклопропилметилом,
R2 является CH2CH2CH3;
R3 является 6-Br;
R4 является Н,
обладающие фунгицидной активностью.
(10) соединения 1, где R2 представляет CH2CH2CH3, R3 представляет 6-Br, R4 представляет водород и R1 представляет CH2CH(CH3)2, (циклопропил)CH2 или CH(CH3)этил; (11) соединения 1, где R1 и R2 оба являются (CH2)4CH3, R3 представляет 6-Br и R4 представляет H, и (12) соединения 1, где R1 представляет (CH2)3CH3, R3 представляет 6-I, R4 представляет водород и R2 представляет (CH2)3CH3 или CH2CH2CH3.
Приоритет по пунктам:
12.05.93 - по п.3 соединение 1;
28.10.93 - по п.2, соединение 2, пп.5; 6, 8, 9 и 10;
10.05.94 - по п.1; п.4 соединение I, пп.5 и 7;
| US 3775582, 1973 | |||
| US 3867384, 1975 | |||
| 3-Метил-2 @ -метилакрилоиламидо @ хиназолон-4 как термо- и светостабилизатор поливинилхлорида | 1986 |
|
SU1325048A1 |
| SU 229336, 1963 | |||
| Справочник по пестицидам, Москва, Химия, 1985, с.298. | |||
Авторы
Даты
1999-10-20—Публикация
1994-05-10—Подача