Настоящее изобретение относится к бициклическим ароматическим соединениям в качестве новых и биологически активных продуктов. Оно также относится к применению этих новых соединений в фармацевтических композициях, предназначенных для использования в медицине человека или ветеринарии, или в косметических композициях.
Соединения согласно изобретению обладают заметной активностью в области дифференциации и клеточной пролиферации и могут найти применение например, при топическом и системном лечении дерматологических заболеваний, связанных с нарушением кератинизации, дерматологических заболеваний (или других заболеваний) с воспалительной компонентой и/или иммуноаллергической компонентой, и дермических или эпидермических пролифераций, которые являются доброкачественными или злокачественными. Эти соединения, кроме того, могут найти применение для лечения заболеваний, вызывающих перерождение соединительной ткани, для борьбы против старения кожи, вызванного возрастом или световым облучением и для лечения расстройств при рубцевании. С другой стороны, они могут найти применение в офтальмологии особенно при лечении заболеваний роговицы. Вообще, они могут найти применение при лечении любого заболевания, которое ассоциировано с модификацией экспрессии рецепторов, принадлежащих к большой группе рецепторов стероидных и тиреоидных гормонов.
Соединения согласно изобретению также можно использовать в косметических композициях для гигиены тела и по уходу за волосами.
Соединения согласно изобретению могут быть представлены следующей общей формулой (I):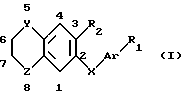
в которой:
R1 обозначает атом водорода, радикал - CH3, радикал -CH2 -О- R3;
радикал - CH2-O-CO-R4; радикал - O-R5, радикал -O-(CH2)m-(CO)n - R6; радикал - CO-R7, радикал -CO-O-R8, или еще радикал - S(O)p - R9, причем величины "m", "n" и "p", также, как различные радикалы R3 + R9 имеют нижеуказанное значение;
R9 обозначает атом водорода или атом галогена, низший алкильный радикал, радикал - NO2, радикал - O - COR4, радикал - OR9 или радикал: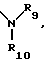
причем радикалы R4, R9 и R10 имеют нижеуказанное значение:
Ar обозначает радикал, выбираемый среди радикалов следующих формул (a) - (e):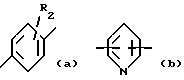
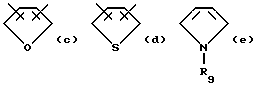
в которых R2 имеет вышеуказанное значение и R9 имеет нижеуказанное значение:
X обозначает -O-, -S(O)t - или радикал -NR9-, причем величина "t" и радикал R9 имеют нижеуказанное значение:
Y и Z обозначают -O- S(O)t - или радикал - CR11R12, причем величина "t" и радикалы R11 и R12 имеют нижеуказанное значение:
имея в виду, что в вышеуказанное:
- "m" обозначает целое число, равное 1, 2, или 3;
"n" обозначает целое число, равное 0 или 1;
"p" обозначает целое число, равное 0, 1, 2 или 3, и
"t" обозначает целое число, равное 0, 1 или 2;
- R3 обозначает атом водорода или низший алкильный радикал,
- R4 обозначает низший алкильный радикал,
- R5 обозначает атом водорода или низший алкильный радикал,
- R6 обозначает низший алкильный радикал или гетероцикл,
- R7 обозначает атом водорода, низший алкильный радикал или радикал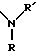
в котором R' и R'', одинаковые или разные, обозначают атом водорода, низший алкильный радикал, моно- или полигидроксиалкильный радикал, в случае необходимости замещенный арильный радикал или остаток аминокислоты или пептида или сахара; или взятые вместе, образуют гетероцикл;
- R8 обозначает атом водорода, линейный или разветвленный алкильный радикал с 1-20 C-атомами, алкенильный радикал, моно- или полигидроксиалкильный радикал, арильный или аралкильный радикал, в случае необходимости замещенный, или остаток сахара или остаток аминокислоты или пептида ;
- R9 обозначает атом водорода или низший алкильный радикал;
- R10 обозначает атом водорода или низший алкильный радикал;
- R11 обозначает атом водорода или низший алкильный радикал;
- R12 обозначает атом водорода или низший алкильный радикал;
- Y и Z одновременно не могут обозначать атом кислорода или радикал -S(O)t.
Изобретение также относится к солям соединений вышеприведенной формулы (I), в которой радикал R1 обозначает функцию карбоновой кислоты или сульфокислотную функцию или содержит аминную функцию, или радикал R2 обозначает аминную функцию, также, как и к хиральным аналогам вышеуказанных соединений. Когда соединения согласно изобретению находятся в форме солей, то речь идет предпочтительно о солях со щелочным или щелочноземельным металлом, или еще о солях цинка или органического амина.
Согласно настоящему изобретению, под "низшим алкильным радикалом" понимают радикал с 1-6 C-атомами, предпочтительно метальный, этильный, изопропильный, бутильный, трет.-бутильный и гексильный радикалы.
Под линейным или разветвленным алкильным радикалом с 1-20 C-атомами понимают особенно метильный, этильный, пропильный, 2-этилгексильный, октильный, додецильный, гексадецильный и октадецильный радикалы.
Под моногидроксиалкильным радикалом понимают радикал, содержащий предпочтительно 2 или 3 атома углерода, особенно 2-гидроксиэтильный, 2-гидроксипропильный или 3-гидроксипропильный радикал.
Под полигидроксиалкильным радикалом понимают радикал, содержащий предпочтительно 3-6 атомов углерода и 2-5 гидроксильных группы, такие, как 2,3 -дигидроксипропильный, 2,3,4-тригидроксибутильный, 2,3,4,5-тетрагидроксипентильный радикалы или остаток пентаэритритола.
Под арильным радикалом предпочтительно понимают фенильный радикал, в случае необходимости замещенный по крайней мере одним атомом галогена, гидроксилом или нитро-группой.
Под аралкильным радикалом предпочтительно понимают бензильный или фенетильный радикал, в случае необходимости замещенный по крайней мере одним атомом галогена, гидроксилом или нитро-группой.
Под алкенильным радикалом понимают радикал, содержащий предпочтительно 2-5 C-атомов и имеющий одну или несколько двойных связей (этиленовых ненасыщенностей), такой, как преимущественно аллильный радикал.
Под остатком сахара понимают остаток, происходящий в частности от глюкозы, галактозы или маннозы, или глюкуроновой кислоты.
Под аминокислотным остатком понимают особенно остаток, происходящий от лизина, глицина или аспарагиновой кислоты, а под остатком пептида понимают преимущественно дипептидный или трипептидный остаток, получающийся в результате комбинации аминокислот.
Наконец, под гетероциклом понимают предпочтительно пипередино-, морфолино-, пирролидино- или пиперазино- радикал, в случае необходимости замещенный в положении 4 алкильным радикалом с 1-6 C-атомами или моно- или полигидроксиалкильным радикалом, таким, как определенные выше.
Когда радикал R2 обозначает атом галогена, то он предпочтительно обозначает атом фтора, хлора или брома.
Из соединений вышеприведенной формулы (I), входящих в рамки настоящего изобретения, особенно можно назвать следующие:
4-(5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилокси) бензойная кислота,
4-(5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтио) бензойная кислота,
4-(5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилсульфинил) бензойная кислота,
4-(5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилсульфонил) бензойная кислота,
4-(5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтиламино) бензойная кислота,
5-(5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтио)-2- тиофенкарбоновая кислота,
4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилокси) бензойная кислота,
4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио) бензойная кислота,
4-(3-этил-5,5,8,8-тетраметил-5,6,7,8-тетрагидро-2-нафтилокси) бензойная кислота,
4-(3-изопропил-5,5,8,8-тетраметил-5,6,7,8-тетрагидро-2-нафтилокси) бензойная кислота,
4-(5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилокси)ацетофенон,
4-(5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилоксидбензальдегид,
4-(3-бром-5,5,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилокси) бензойная кислота,
3-метил-4-(5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтио) бензойная кислота,
3-метил-4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио) бензойная кислота,
3-метил-4-(3-этил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилокси) бензойная кислота,
6-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио) никотиновая кислота,
2-гидрокси-4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио) бензойная кислота,
2-хлор-4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио) бензойная кислота,
4-(3-этил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтио) бензойная кислота,
4-(3-изопропил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтио) бензойная кислота,
4-(3-н-пропил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтио) бензойная кислота,
4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио)бензолметанол,
4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио)бензальдегид,
N-этил-4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио)бензамид,
N-4-гидроксифенил-4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио)бензамид.
Согласно настоящему изобретению, особенно предпочтительными соединениями формулы (I) являются такие, в которых соблюдаются по крайней мере одно, и предпочтительно все, из нижеуказанных условий:
- R1 обозначает радикал - CO - R7,
- R2 обозначает низший алкильный радикал и радикал - OR9,
- Ar обозначает радикал формулы (а),
- и X обозначает -O-, -S- или -NR9-.
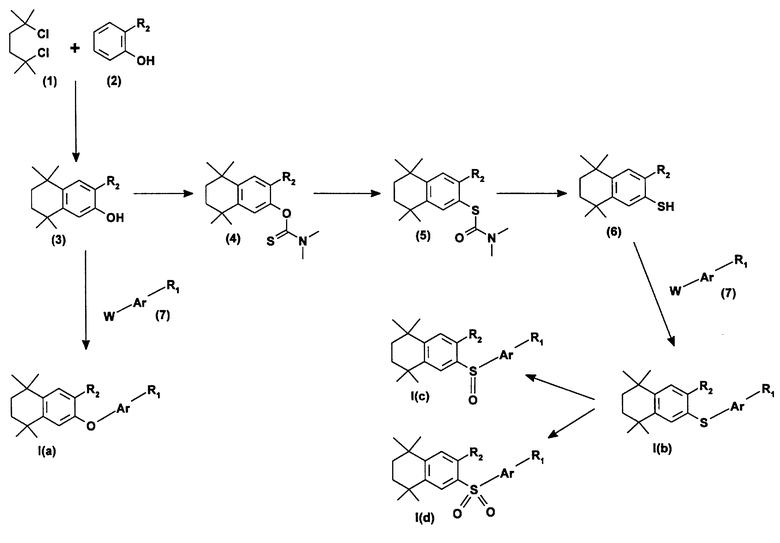
Предметом настоящего изобретения также являются способы получения соединений формулы (I), осуществляемые, в частности, согласно приведенным на чертеже реакционным схемам.
Так, соединения формулы (Ia) могут быть получены (см. чертеж) путем сочетания натриевой соли фенольного производного (3) с галогенированным производным (7), предпочтительно с бромированным или иодированным производный, в присутствии комплекса бромида меди с диметилсульфидом, в растворителе, таком, как пиридин. Что касается фенольных производных (3), то они могут быть получены путем реакции типа Фриделя-Крафтса из фенола (2) и дигалогенированного производного (I) в присутствии кислоты Льюиса, например, как хлоридиалюминия.
Соединения формулы (Ib) могут быть получены (см. чертеж) путем сочетания натриевой соли тиольного производного (6) с галогенированным производным (7), предпочтительно с бромированным или иодированным производным, в присутствии катализатора, такого, как некоторые комплексы переходных металлов, в спиртовом растворителе, таком, как этиловый или бутиловый спирт. В качестве пригодных катализаторов в особенности можно указать таковые на основе никеля или палладия, например, как комплексы Ni-(II) с различными фосфинами или тетракис (трифенилфосфин)палладия - (0). Тиольные производные (6) можно получить из фенольных производных (3) через диалкилтиокарбаматные производные (4) и (5) согласно общим условиям, описанным M.Newman и H.Karnes в F.Org. Chem 1966, 31, 3980-4.
Производные формулы (Ic) и формулы (Id) могут быть получены путем окисления производного формулы (Ib), например, используя мета-хлорнадбензойную кислоту.
Когда в общей формуле (I) X обозначает радикал - NR9, то тогда соединения могут быть получены согласно реакции типа Улльмана путем прямого нуклеофильного замещения галогенированного производного (7), предпочтительно иодированного производного, анилиновым производным (8), в присутствии основания, такого, как карбонат калия или N-метилморфолин, и меди: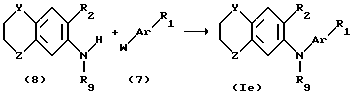
В вышеприведенных формулах и реакциях R1 и R2 имеют значения, вышеуказанные для общей формулы (I), или они означают их защищенные производные, чтобы они были совместимы с условиями реакции сочетания. В частности, когда они обозначают гидроксильный радикал, то его предпочтительно защищает в форма трет.-бутилдиметилсилилокси - или метоксиэтоксиметокси - группы. Удаление защитной группы осуществляют либо в присутствии тетрабутиламмонийфторида или триметилсиланиодида, либо в кислой среде (например, в соляной кислоте).
Соединения согласно изобретению активны по отношению к экспрессии некоторых маркеров дифференциации в человеческих кератиноцитах ин витро ( Anal. Biochemen 192, 232 - 236 (1991) и/или они обладают хорошей комедолитической активностью в тесте Souris-Rhino (Skin Pharmacology, 4, 65 - 73 (1991).
Соединения согласно изобретению особенно могут быть ценными в следующих областях:
1). для лечения дерматологических заболеваний, связанных с нарушением кератинизации, что приводит к дифференциации и пролиферации, особенно для лечения обыкновенных, черных полиморфных, красных угрей; узелковокистозных акне, конглобата, старческих акне, вторичных акне, например, вызванных солнечным излучением, медикаментозные или профессиональные акне;
2). для лечения других типов нарушений кератинизации, особенно для лечения ихтиозов, ихтиозоподобных состояний, болезни Darrier, подошвенных кератодермий, лейкоплазий и лейкоплазоподобных состояний, лишаев на коже или на слизистых оболочках (ротовых);
3). для лечения других дерматологических заболеваний, связанных с нарушением кератинизации с воспалительной и/или иммуноаллергической компонентой и особенно всех форм псориаза, кожного, слизистого ногтевого псориаза, и даже псориазного ревматизма, или кожной атопии, такой, как экзема, или респираторной атопии или гипертрофии десен; соединения также могут быть использованы при некоторых воспалительных заболеваниях, не представляющих собой нарушения кератинизации;
4). для лечения всех дермических или эпидермических пролифераций, доброкачественных или злокачественных, и которые могут быть вирусного происхождения, таких, как обычные бородавки, плоские юношеские бородавки и бородавчатоподобная эпидермодисплазия, оральные или флоридные папилломатозы, и пролифераций, которые могут быть вызваны ультрафиолетовым облучением, особенно в случае базо- и спиноцеллюлозных эпителиом;
5). для лечения других дерматологических нарушений, таких, как буллезные дерматозы и коллагенозы;
6). для лечения некоторых офтальмологических расстройств, например заболевании роговицы;
7). для восстановления или борьбы против старения кожи, которое является возрастным или фотоинициированным или, для уменьшений пигментаций и актинических кератозов, или для борьбы с любыми патологиями, ассоциированными с возрастным или актиническим старением;
8). для предупреждения или вылечивания стигматов эпидермической и/или дермической атрофии, вызываемой локальными или системными кортикостероидами, или любой другой формы кожной атрофии;
9). для предотвращения или лечения нарушений заживления или для профилактики или восстановления рубцов на коже при ее растяжении;
10) для борьбы с нарушениями жировой функции, таких, как гиперсеборинная акне или обычная себорея;
11) для лечения или профилактики раковых или предраковых состояний;
12) для лечения воспалительных заболеваний, таких как артрит;
13) для лечения любого заболевания вирусного происхождения, общего или кожного;
14) для профилактики или лечения от выпадения волос;
15) для лечения дерматологических или общих заболеваний с иммунологической компонентой;
16) для лечения заболеваний сердечно-сосудистой системы, таких, как артериосклероз.
В вышеуказанных областях терапии соединения согласно изобретению предпочтительно можно использовать в комбинации с другими соединениями, проявляющими активность ретиноидного типа с витаминами или их производными, с кортикостероидами, со средствами против свободных радикалов α-гидрокси- или α-кетокислотами или их производными, или с блокирующими ионные каналы средствами. Под витаминами D или их производными понимают, например производные витамина D2 или D3 например 1,25 - дигидроксивитамин D3. Под средствами против свободных радикалов понимают, например α-токоферол, супероксид Дисмутазу, Убихинол или некоторые агенты образования внутрикомплексных соединений с металлами. Под α-гидрокси или α-кетокислотами или их производными понимают, например молочную, яблочную, лимонную, гликолевую, миндальную, винную, глицериновую или аскорбиновую кислоты или их соли, амиды или сложные эфиры. Наконец, под блокирующими ионные каналы средствами понимают, например Миноксидил(2,4-диамино-6-пиперидино-пиримидин-3-оксид) и его производные.
Предметом настоящего изобретения также являются фармацевтические композиции, содержащие по крайней мере одно соединение формулы (I), указанной выше, один из его хиральных аналогов или одну из его солей.
Фармацевтическая композиция отличается тем, что она включает в фармацевтически приемлемом и совместимом со способом введения, предусмотренном для этой последней носителе по крайней мере одно соединение формулы (I), один из хиральных аналогов или одну из его солей в эффективном количестве.
Введение соединений согласно изобретению можно осуществлять энтеральным (кишечным), парентеральным, топическим или окулярным (главным) путем.
Для энтерального введения композиция может находиться в форме таблеток, желатиновых капсул с лекарством, драже, сиропов, свечей, растворов, порошков, гранулятов, эмульсий, микросфер или наносфер или пузырьков, липидных или полимерных, позволяющих осуществлять дозированное выделение активного начала. Для введения парентеральным путем композиции могут находиться в форме растворов или суспензий для перфузии или для инъекции.
Соединения согласно изобретению обычно вводят в суточной дозе около 0,01 - 100 мг/кг веса тела и это в 1-3 приема.
Для нанесения топическим путем фармацевтические композиции на основе соединений согласно изобретению могут находиться в форме мазей, кремов, молочка, помад, пудр, пропитанных тампонов, растворов, гелей, пульверизуемых препаратов, лосьонов или суспензий. Они также могут находиться в форме микросфер или наносфер или липидных или полимерных визикул или полимерных кусочков пластырей и гидрогелей, позволяющих контролированное высвобождение действующего начала. Эти композиции при топическом применении, кроме того, могут находиться либо в безводной форме, либо в водной форме.
Для введения через глаза они представляют собой глазные капли.
Композиции для топического введения или введения через глаза содержат по крайней мере одно соединение вышеуказанной формулы (I) или один из его оптических или геометрических изомеров или одну из его солей, в концентрации предпочтительно 0,001 - 5 вес.%, в расчете на общий вес композиции.
Соединения формулы (I) согласно изобретению также находят применение в косметической области, в особенности для гигиены тела и по уходу за волосами, и особенно для обработки кожи с тенденцией к акне для нового роста волос, против выпадения волос, для борьбы с жирным внешним видом кожи или волос, для защиты от вредного воздействия солнца или для обработки физиологически сухих кож, для предохранения и/или для борьбы с возрастным или фотоиндуцирующим старением.
В косметической области соединения согласно изобретению предпочтительно могут использоваться в сочетании с другими соединениями, обладающими активностью ретиноидного типа, с витаминами D или их производными, с кортикостероидами, со средствами против свободных радикалов, α-гидрокси- или α-кетокислотами или их производными, или с блокаторами ионных каналов, причем все эти различные продукты являются такими, которые указаны выше.
Настоящее изобретение, следовательно, относится к косметической композиции, которая отличается тем, что она включает, в косметически приемлемом и пригодном для топического применения носителе, по крайней мере одно соединение вышеуказанной формулы (I) или один из его хиральных аналогов или одну из его солей, причем эта косметическая композиция может находиться в форме крема, молочка, лосьона, геля, липидных или полимерных микросфер или наносфер или пузырьков, мыла или шампуня.
Концентрация соединения формул (I) в косметических композициях согласно изобретению предпочтительно составляет 0,001 - 3 вес.%, в расчете на всю совокупность композиции.
Лекарственные и косметические композиции согласно изобретению, кроме того, могут содержать инертные или фармакодинамически или косметически эффективные добавки или их смесь в частности: смачиватели, депигментирующие агенты, такие, как гидрохинон, азелаиновая кислота, кофеная кислота или койевая кислота, смягчающие агенты, гидратирующие агенты, как глицерин, ПЭГ-400, тиаморфолинон и его производные или мочевину, антисеборейные или противоакневые агенты, такие, как S-карбоксиметилцистеин, S-бензил-цистеамин, их соли или их производные, или бензоилпероксид, антибиотики, такие как эритромицин и его сложные эфиры, неомицин, клиндамицин и его сложные эфиры, тетрациклины, противогрибковые агенты, такие, как кетоконазол или полиметилен-4,5-изотиазолид-3-оны, агенты, благоприятствующие новому росту волос, например миноксидил(2,4-диамино-6-пиперидино-пиримидин-3-оксид) и его производные, диазоксид (7-хлор-3-метил-1,2,4-бензотиадиазин-1,1-диоксид) и фенитоин(5,4-дифенил-имидазолидин-2,4-дион); противовоспалительные нестероидные агенты; каротиноиды и, особенно, β-каротон; антипсориазные агенты, такие, как антралин и его производные, и, наконец, эйкоза-5,8,11,14-тетраиновая кислота и эйкоза-5,8,11-трииновая кислота, их сложные эфиры и амиды.
Композиции согласно изобретению также могут содержать улучшающие вкус агенты, консерванты, такие, как сложные эфиры пара-гидроксибензойной кислоты, стабилизаторы, регулирующие влажность агенты; регулирующие pH агенты, кодификаторы осмотического давления; эмульгаторы; УФ-А и УФ-В-фильтры, антиоксиданты, такие, как α-токоферол, бутилгидроксианизол или бутилгидрокситолуол.
Ниже приводится, в качестве иллюстрации и не ограничивая ими объема охраны изобретения, несколько примеров получения активных соединений формулы (I) согласно изобретению, также, как различные конкретные рецептуры на основе таких соединений.
Пример 1
4-(5,6,7,8-Тетрагидро-5,5,8,8-тетраметил-2- нафтилокси) бензойная кислота.
(а) Метил-4-(5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилокси)бензоат
В трехгорлую колбу, в атмосфере азота вводят 5,3 г (15 ммоль) 5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтола и 70 мл пиридина и маленькими порциями добавляют 430 мг (15 ммоль) гидрида натрия (80%-ного в масле). Перемешивают в течение 30 минут, добавляют последовательно 3,9 г (15 ммоль) метил-4-иодбензоата и 4,6 г (22,5 ммоль) комплекса бромида меди с диметилсульфидом и кипятят с обратным холодильником в течение 16 часов. Реакционную среду выпаривают досуха, обрабатывают остаток водой и диэтиловым эфиром, органическую фазу декантируют, сушат ее над сульфатом магния и выпаривают. Полученный остаток очищают путем хроматографии на колонке с диоксидом кремния, элюируя дихлорметаном с гексаном (50-50). После выпаривания растворителей получают 3,4 г (67%) целевого сложного метилового эфира.
(б) 4-(5,6,7,8-Тетрагидро-5,5,8,8-тетраметил-2-нафтилокси) бензойная кислота.
В колбу вводят 3,4 г (10 ммоль) полученного в п. (а) сложного эфира, 40 мл ТГФ и 40 мл 2 н. метанольного раствора гидроксида натрия и всю смесь перемешивают при комнатной температуре в течение 8 часов. Реакционную среду выпаривают досуха, остаток обрабатывают водой, подкисляют до pH 1, экстрагируют диэтиловым эфиром, органическую фазу декантируют, сушат над сульфатом магния и выпаривают. Полученный остаток очищают путем хроматографии на колонке с диоксидом кремния, элюируя смесью дихлорметана с диэтиловым эфиром (97-3). После выпаривания растворителей получают 2,3 г (71%) целевой кислоты с т. пл. 234-235oC.
Пример 2
4-(5,6,7,8-Тетрагидро-5,5,8,8-тетраметил-2-нафтилтио) бензойная кислота
(а) Этил-4-(5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтио)бензоат
В колбу вводят 30 мл этилового спирта, затем маленькими порциями добавляют 500 мг (23 ммоль) натрия и перемешивают всю смесь в течение 30 минут. После этого добавляют последовательно 2 г (9,1 ммоль) 5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтиола, 2,4 г (9,1 ммоль) метил-4-иодбензоата и 100 мг (0,09 ммоль) тетракис(трифенил-фосфин)палладия-(0), затем кипятят с обратным холодильником в течение 4-х часов. Реакционную среду выпаривают, остаток обрабатывают водой и этилацетатом, органическую фазу декантируют, промывают водой, сушат над сульфатом магния и выпаривают. Полученный остаток очищают путем хроматографии на колонке с диоксидом кремния, элюируя дихлорметаном. После выпаривания растворителя получают 2,1 г (63%) сложного этилового эфира.
(б) 4-(5,6,7,8-Тетрагидро-5,5,8,8-тетраметил-2-нафтилтио) бензойная кислота
Аналогичным вышеприведенному примеру 1(б) образом, из 1,9 г (5,2 ммоль) полученного в предыдущем п. (а) сложного этилового эфира получают 1,6 г (90%) целевой кислоты с т. пл. 187-188oC.
Пример 3
4-(5,6,7,8-Тетрагидро-5,5,8,8-тетраметил-2-нафтилсульфинил) бензойная кислота
(а) Этил-4-(5,6,7,8-Тетрагидро-5,5,8,8-тетраметил-2-нафтилсульфинил)бензоат
В колбу вводят 1,1 г (3,1 ммоль) этил-4-(5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтио)бензоата и 30 мл дихлорметана и затем добавляют 970 мг ( 3,1 ммоль) метахлорнадбензойной кислоты.
Всю смесь перемешивают при комнатной температуре в течение двух часов, реакционную среду выливают в воду, экстрагируют дихлорметаном, органическую фазу декантируют, сушат над сульфатом магния и выпаривают. Остаток очищают путем хроматографии на колонке с диоксидом кремния, элюируя дихлорметаном. После выпаривания растворителя получают 1 г (84%) целевого сложного эфира.
(б) 4-(5,6,7,8-Тетрагидро-5,5,8,8-тетраметил-2-нафтилсульфинил) бензойная кислота
Аналогичным вышеописанному примеру 1(б) образом, из 960 мг (2,5 ммоль) полученного в предыдущем п. (а) сложного этилового эфира, получают 890 мг (99%) целевой кислоты с т. пл. 214 - 216oC.
Пример 4
4-(5,6,7,8-Тетрагидро-5,5,8,8-тетраметил-2-нафтилсульфонил) бензойная кислота
(а) Этил-4-(5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилсульфонил)бензоат
В колбу вводят 1,05 г (2,8 ммоль) этил-4-(5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтио)бензоата и 30 мл дихлорметана и затем добавляют 2,45 г (7,12 ммоль) метахлорнадбензойной кислоты. Всю смесь перемешивают при комнатной температуре в течение двух часов, реакционную среду выливают в воду, экстрагируют дихлорметаном, органическую фазу декантируют, сушат над сульфатом магния и выпаривают. Остаток очищают путем хроматографии на колонке с диоксидом кремния, элюируя дихлорметаном. После выпаривания растворителя получают 1,09 г (95%) целевого сложного эфира.
(б) 4-(5,6,7,8-Тетрагидро-5,5,8,8-тетраметил-2-нафтилсульфонил) бензойная кислота
Аналогичным вышеприведенному примеру 1(б) образом, из 1,09 г (2,7 ммоль) полученного в предыдущем п. (а) сложного этилового эфира, получают 1 г (99%) целевой кислоты с т. пл. 216-220oC.
Пример 5
4-(5,6,7,8-Тетрагидро-5,5,8,8-тетраметил-2-нафтиламино) бензойная кислота
В колбу вводят последовательно 1,02 г (5 ммоль) 5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтиламина, 1,24 г (5 ммоль) 4-иодбензойной кислоты, 820 мкл (7,5 ммоль) N-метилморфолина, 360 мг (2,5 ммоль) Cu2O и 15 мл диоксана. Всю смесь кипятят с обратным холодильником в течение 24-х часов, реакционную среду выливают в 15 мл 5 н соляной кислоты, осадок отфильтровывают, промывают этот последний водой. Твердое вещество порошкуют в этиловом спирте, отфильтровывают, высушивают. Тогда получают 200 мг (12%) целевой кислоты с т. пл. 262-264oC.
Пример 6
5-(5,6,7,8-Тетрагидро-5,5,8,8-тетраметил-2-нафтилтио)-2-тиофенкарбоновая кислота
В колбу вводят 40 мл н-бутилового спирта, затем добавляют маленькими порциями 300 мг (13 моль) натрия, и всю смесь перемешивают в течение 30 минут. После этого добавляют последовательно 1,1 г (5 ммоль) 5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтиола, 1,1 г (5 ммоль) метил-5-бром-2-тиофенкарбоксилата и 230 мг (0,2 ммоль) тетракис(трифенилфосфин)палладия-(0), затем всю смесь кипятят с обратным холодильником в течение 4-х часов. Реакционную среду выпаривают, обрабатывают остаток водой и этилацетатом, органическую фазу декантируют, промывают водой, сушат над сульфатом магния, выпаривают. Полученная остаток очищают путем хроматографии на колонке с диоксидом кремния, элюируя смесью этилацетата с гексаном (60 - 40). После выпаривания растворителей получают 180 мг (10%) 5-(5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтио)-2-тиофенкарбоновой кислоты с т. пл. 141-142oC.
Пример 7
4-(3,5,5,8,8-Пентаметил-5,6,7,8-тетрагидро-2-нафтилокси) бензойная кислота
(а) 3,5,5,8,8-Пентаметил-5,6,7,8-тетрагидро-2-нафтол
В трехгорлую колбу вводят 50,8 г (0,27 моль) 2,5-дихлор-2,5-диметил-гексана, 30 г (0,27 моль) -2-метил-фенола и 500 мл дихлорметана. При 0oC добавляют маленькими порциями 14,8 г (0,11 моль) хлорида алюминия, и всю смесь перемешивают при комнатной температуре в течение 12 часов. Реакционную среду выливают в воду со льдом, экстрагируют дихлорметаном, органическую фазу декантируют, промывают содержащей бикарбонат водой, сушат над сульфатом магния и выпаривают. Полученный остаток порошкуют в гексане, отфильтровывают и тогда получают, после высушивания, 54,4 г (90%) целевого фенола с т.пл. 125-126oC.
(б) Метил-4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилокси)бензоат
Аналогичным вышеприведенному примеру 1(а) образом, путем взаимодействия 1,1 г (5 ммоль) 3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтола с 0,89 г (4,1 ммоль) метил-4-бромбензоата, получают 670 мг (46%) целевого сложного метилового эфира с т. пл. 133 - 135oC.
(в) 4-(3,5,5,8,8-Пентаметил-5,6,7,8-тетрагидро-2-нафтилокси) бензойная кислота
Аналогичным вышеприведенному примеру 1(б) образом, из 670 мг (1,9 ммоль) полученного в предыдущем п. (б) сложного метилового эфира, получают 620 мг (96%) целевой кислоты с т. пл. 208-210oC.
Пример 8
4-(3,5,5,8,8-Пентаметил-5,6,7,8-тетрагидро-2-нафтилтио) бензойная кислота
(а) 0-3,5,5,8,8-Пентаметил-5,6,7,8-тетрагидро-2-нафтилдиметилтиокарбамат
В колбу, в атмосфере азота, вводят 4,1 г (0,138 моль) гидрида натрия (30%-ный в масле) и 200 мл ДМФ. Охлаждают до 0oC и прикапывают раствор 25,2 г (0,115 моль) 3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтола в 100 мл ДМФ и всю смесь перемешивают до прекращения выделения газов. Затем добавляют раствор 18,55 г (0,15 моль) диметилтиокарбамоилхлорида в 200 мл ДМФ и снова всю смесь перемешивают в течение 8 часов при комнатной температуре. После этого реакционную среду выливают в воду, экстрагируют этилацетатом, органическую фазу декантируют, промывают водой, сушат над сульфатом магния, и, наконец, выпаривают. Полученный остаток очищают путем хроматографии на колонке с диоксидом кремния, элюируя смесью этилацетата с гексаном (30-70). После выпаривания растворителей получают 20 г (68%) целевого продукта с т.пл. 110 - 111oC.
(б) - 3,5,5,8,8-Пентаметил-5,6,7,8-тетрагидро-2-нафтилдиметилтиокарбамат
В колбу в атмосфере азота вводят 20,1 г (65,8 ммоль) полученного в предыдущем п. (а) продукта и в течение 6 часов нагревают при 240oC. Реакционную среду экстрагируют дихлорметаном, промывают водой, органическую фазу декантируют, сушат над сульфатом магния и выпаривают. Получают 18,1 г (90%) целевого продукта с т. пл. 138 - 139oC.
(в) 3,5,5,8,8-Пентаметил-5,6,7,8-тетрагидро-2-нафтилтиол
В колбу вводят 23 г (75 ммоль) полученного в предыдущем п. (б) продукта и 300 мл метилового спирта. Добавляют 30 г (75 ммоль) гидроксида натрия, и всю смесь кипятят с обратным холодильником в течение трех часов. Реакционную среду выпаривают, обрабатывают остаток водой, подкисляют концентрированной соляной кислотой и, наконец, отфильтровывают. Полученное твердое вещество промывают водой, сушат и тогда получают 18 г (99%) 3,5,5,8,8-пентаментил-5,6,7,8-тетрагидро-2-нафтилтиола с т.пл. 97 - 98oC.
(г) Этил-4-(3,5,5,8,8-пентаметил-5,5,7,8-тетрагидро-2-нафтилтио)бензоат
Аналогичным вышеописанному примеру 2(а) образом, путем взаимодействия 2 г (8,5 ммоль) 3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтиола с 2,24 г (8,5 ммоль) метил-4-иодбензоата, после перекристаллизации из этилового спирта, получат 2 г. (63%) сложного этилового эфира с т.пл. 109 - 110oC.
(д) 4-(3,5,5,8,8-Пентаметил-5,6,7,8-тетрагидро-2-нафтилтио) бензойная кислота
Аналогичным вышеописанному примеру 1(б) образом, из 2 г (5,2 ммоль) полученного в предыдущем п. (г) сложного этилового эфира, получают 1,58 г (85%) целевой кислоты с т. пл. 253 - 254oC.
Пример 9
4-(3-Этил-5,5,8,8-тетраметил-5,6,7,8-тетрагидро-2-нафтилокси) бензойная кислота
(а) 3-Этил-5,5,8,8-тетраметил-5,6,7,8-тетрагидро-2-нафтол
Аналогичным вышеописанному примеру 7(а) образом, путем взаимодействия 15 г (0,123 моль) 2-этилфенола с 22,5 г (0,123 моль) 2,5-дихлор-2,5-диметилгексана, после хроматографии на колонке с диоксидом кремния при элюировании дихлорметаном, получают 25,4 г (89%) целевого фенола с т.пл. 88-89oC.
(б) Метил-4-(3-этил-5,5,8,8-тетраметил-5,6,7,8-тетрагидро-2-нафтилокси)бензоат
Аналогичным вышеописанному примеру 1(а) образом, путем взаимодействия 2 г (8,6 ммоль) 3-этил-5,5,8,8-тетраметил-5,6,7,8-тетрагидро-2-нафтола с 1,52 г (7 ммоль) метил-4-бромбензоата, получают 1,5 г (56%) целевого сложного метилового эфира в виде масла желтого цвета.
(в) 4-(3-Этил-5,5,8,8-тетраметил-5,6,7,8-тетрагидро-2-нафтилокси) бензойная кислота
Аналогичным вышеописанному примеру 1(б) образом, из 1,5 г (4 ммоль) полученного в предыдущем п. (б) сложного метилового эфира, получают 1,24 г (86%) целевой кислоты с т. пл. 195 - 196oC.
Пример 10
4-(3-Изопропил-5,5,8,8-тетраметил-5,6,7,8-тетрагидро-2-нафтилокси) бензойная кислота
(а) 3-Изопропил-5,5,8,8-тетраметил-5,6,7,8-тетрагидро-2-нафтол
Аналогичным вышеописанному примеру 7(а) образом, путем взаимодействия 30 г (0,22 моль) 2-изопропилфенола с 40,3 г (0,22 моль) 2,5-дихлор-2,5-диметилгексана и после хроматографии на колонке с диоксидом кремния при элюировании смесью дихлорметана с гексаном (40-60), получают 48,9 г (90%) целевого фенола с т.пл. 79 - 80oC.
(б) Метил-4-(3-изопропил-5,5,8,8-тетраметил-5,6,7,8-тетрагидро-2-нафтилокси)бензоат
Аналогичным вышеописанному примеру 1(а) образом, путем взаимодействия 2 г (8,1 ммоль) 3-изопропид-5,5,8,8-тетраметил-5,6,7,8-тетрагидро-2-нафтола с 1,45 г (6,7 ммоль) метил-4-бромбензоата, получают 840 мг (33%) целевого сложного метилового эфира с т. пл. 115-116oC.
(в) 4-(3-Изопропил-5,5,8,8-тетраметил-5,6,7,8-тетрагидро-2-нафтилокси) бензойная кислота
Аналогичным вышеописанному примеру 1(б) образом, из 800 мг. (2,1 ммоль) полученного в предыдущем п. (б) сложного метилового эфира, получают 690 мг (90%) целевой кислоты с т.пл. 205-206oC.
Пример 11
4-(5,6,7,8-Тетрагидро-5,5,8,8-тетраметил-2-нафтилокси)ацетофенон
Аналогичным вышеописанному примеру 1(а) образом, путем взаимодействия 6,6 г (32 ммоль) 5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтола с 5,4 г (27 ммоль) 4-бромацетофенона, получают 6,3 г (72%) целевого кетона в форме слегка желтоватого масла.
Пример 12
4-(5,6,7,8-Тетрагидро-5,5,8,8-тетраметил-2-нафтилокси)бензальдегид
Аналогичным вышеописанному примеру 1(а) образом, путем взаимодействия 5,3 г (15 ммоль) 5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтола с 3,1 г (16,5 ммоль) 4-бромбензальдегида, после очистки путем хроматографии на колонке с диоксидом кремния при элюировании смесью дихлорметана с гексаном (50-50), получают 2,4 г целевого альдегида с т.пл. 75-76oC.
Пример 13
4-(3-Бром-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилокси) бензойная кислота
(а) Метил-4-(3-бром-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилокси)бензоат
Аналогичным примеру 1(а) образом, путем взаимодействия 1 г (3,5 ммоль) 3-бром-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтола с 770 мг (2,94 ммоль) метил-4-иодбензоата, получают 700 мг (58%) целевого сложного метилового эфира с т.пл. 135-136oC.
(б) 4-(3-Бром-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2- нафтилокси) бензойная кислота
Аналогичным примеру 1(б) образом, из 700 мг (1,6 ммоль предыдущего сложного метилового эфира, получают 650 мг (95%) 4-(3-бром-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилокси) бензойной кислоты с т. пл. 229 - 230oC.
Пример 14
3-Метил-4-(5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтио) бензойная кислота
(а) 3-Метил-4-иодбензойная кислота.
В трехгорлую колбу вводят 20 г (0,132 моль) 3-метил-4-амино-бензойной кислоты и 175 мл 20%-ной серной кислоты. При -10oC прикапывают раствор 11,9 г. ( 0,172 моль) нитрита натрия в 50 мл воды и перемешивают в течение двух часов. Этот раствор через охлажденную до -5oC капельную воронку прикапывают к раствору 35 г (0,211 моль) иодида калия, 35,2 г (0,185 моль) иодида меди и 175 мл 20%-ной серной кислоты. Перемешивают в течение 8 часов, реакционную среду отфильтровывают, полученное твердое вещество растворяют в этилацетате, полученный раствор промывают водой, затем раствором сульфита натрия, сушат над сульфатом магния и выпаривают. Получают 24,4 г (70%) 3-метил-4-иодбензойной кислоты с т. пл. 205-210oC.
(б) Метил-3-метил-4-иодбензоат
В колбу вводят 24,4 г. (0,093 моль) 3-метил-4-иодбензойной кислоты, 250 мл метанола и прикапывают 2,5 мл концентрированной серной кислоты. Кипятят с обратным холодильником в течение 12 часов, реакционную среду выпаривают, остаток обрабатывают этилацетатом и водой, органическую фазу декантируют, сушат над сульфатом магния и выпаривают. Остаток порошкуют в метаноле, отфильтровывают и получают 21,9 г (85%) целевого сложного метилового эфира с т.пл. 58-59oC.
(в) 3-Метил-4-(5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2- нафтилтио) бензойная кислота
Аналогичным примеру 2(а) образом, путем взаимодействия 2,4 г (11 ммоль) 5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтиола с 3 г (11 ммоль) метил-3-метил-4-иодбензоата, прямо получают 1,96 г. (51%) 3-метил-4-(5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтио) бензойной кислоты с т. пл. 195-196oC.
Пример 15
3-Метил-4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио) бензойная кислота
(а) Этил-3-метил-4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио)бензоат
Аналогичным примеру 2(а) образом, путем взаимодействия 2,55 г (11 ммоль) 3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтиола с 3 г (11 ммоль) метил-3-метил-4-иодбензоата, получают 1,86 г (43%) целевого продукта в виде сложного этилового эфира, представляющего собой оранжевого цвета масло.
(б) 3-Метил-4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио) бензойная кислота
Аналогичным примеру 1(б) образом, из 1,86 г (47 ммоль) вышеполученного сложного этилового эфира, получают 1,5 г (97%) 3-метил-4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио) бензойной кислоты с т.пл. 217-218oC.
Пример 16
3-Метил-4-(3-этил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилокси) бензойная кислота
(а) Метил-3-метил-4-(3-этил-5,6,7,8-тетрагидро-5,5,8,8- тетраметил-2-нафтилокси)бензоат
Аналогичным примеру 1(а) образом, путем взаимодействия 2,1 г (8,7 ммоль) 3-этил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтола с 2 г (7,2 ммоль) метил-3-метил-4-иодбензоата, получают 2,18 г (79%) целевого сложного метилового эфира в виде бледно-желтого масла.
(б) 3-Метил-4-(3-этил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2- нафтилокси) бензойная кислота
Аналогичным примеру 1(б) образом, из 2,18 г (5,7 ммоль вышеполученного сложного метилового эфира, получают 1,9 г (90%) 3-метил-4-(3-этил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилокси) бензойной кислоты с т.пл. 210-211oC.
Пример 17
6-(3,5,5,8,8-Пентаметил-5,6,7,8-тетрагидро-2-нафтилтио) никотиновая кислота
(а) Этил-6-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио)никотинат
Аналогичным примеру 2(а) образом, путем взаимодействия 800 мг (3,4 моль) 3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтиола с 900 мг (3,4 ммоль) метил-6-иодникотината, получают 620 мг (47%) целевого продукта в сложного этилового эфира.
(б) 6-(3,5,5,8,8-Пентаметил-5,6,7,8-тетрагидро-2-нафтилтио) никотиновая кислота
Аналогичным примеру 1(б) образом, из 620 мг (1,6 ммоль) вышеполученного сложного этилового эфира, получают 520 мг (90%) 6-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио) никотиновой кислоты с т.пл. 257 - 260oC.
Пример 18
2-Гидрокси-4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2- нафтилтио) бензойная кислота
(а) Этил-2-гидрокси-4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио)бензоат
Аналогичным примеру 2(а) образом, путем взаимодействия 2 г (8,53 ммоль) 3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтиола с 2,37 г (8,53 ммоль) метил-2-гидрокси-4-иодбензоата, получают 2,42 г (71%) целевого продукта в форме сложного этилового эфира с т.пл. 74-75oC.
(б) 2-Гидрокси-4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2- нафтилтио) бензойная кислота
Аналогичным примеру 1(б) образом, из 2,4 г (6,1 ммоль) вышеполученного сложного этилового эфира, получают 2,06 г (92%) 2-гидрокси-4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио) бензойной кислоты с т.пл. 197-200oC.
Пример 19
2-Хлор-4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио) бензойная кислота
(а) 2-Хлор-4-иодбензойная кислота
Аналогичным примеру 14(а) образом, из 10 г (58,3 ммоль) 2-хлор-4-аминобензойной кислоты, получают 14,26 г (80%) 2-хлор-4-иодбензойной кислоты.
(б) Метил-2-хлор-4-иодбензоат
Аналогичным примеру 14(б) образом, из 13,9 г (49,2 ммоль) 2-хлор-4-иодбензойной кислоты, получают 11,52 г (79%) целевого сложного метилового эфира в виде масла.
(в) Этил-2-хлор-4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2- нафтилтио)бензоат
Аналогичным примеру 2(а) образом, путем взаимодействия 2 г (8,5 ммоль) 3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтиола с 2,41 г. (8,5 ммоль) метил-2-хлор-4-иодбензоата, получают 1,25 г (35%) целевого продукта в форме сложного этилового эфира.
(г) 2-Хлор-4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио) бензойная кислота
Аналогичным примеру 1(б) образом, из 1,25 г (3 ммоль) вышеполученного сложного этилового эфира, получают 1 г (96%) 2-хлор-4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио) бензойной кислоты с т.пл. 202-205oC.
Пример 20
(3-Этил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтио) бензойная кислота
(а) O-3-Этил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилдиметилтиокарбамат
Аналогичным примеру 8(а) образом, путем взаимодействия 5 г (21 ммоль) 3-этил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтола с 3,5 г (2,8 ммоль) диметилтиокарбамоилхлорида, получают 4,9 г (72%) целевого продукта с т.пл. 82 - 83oC.
(б) S-3-Этил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилдиметилтиокарбамат
Аналогичным примеру 8(б) образом, из 4,5 г (14 ммоль) вышеполученного продукта, получают 4,5 г (99%) - 3-этил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилдиметилтиокарбамата в виде каштанового цвета масла.
(в) 3-Этил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтиол
Аналогичным примеру 8(в) образом, из 4,5 г (14 ммоль) вышеполученного продукта, получают 2,9 г (84%) целевого тиола в виде оранжевого цвета масла.
(г) Этил-4-(3-этил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2- нафтилтио)бензоат
Аналогичным примеру 2(а) образом, путем взаимодействия 2 г (8,5 ммоль) 3-этил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтиола с 2,1 г (8 ммоль) метил-4-иодбензоата, получают 1,9 г (64%) целевого продукта в форме сложного этилового эфира.
(д) 4-(3-Этил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтио) бензойная кислота
Аналогичным примеру 1(б) образом, из 1,9 г (5,1 ммоль) вышеполученного сложного этилового эфира, получают 1,7 г (89%-ю 4-(3-этил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтио) бензойной кислоты с т. пл. 232-235oC.
Пример 21
Этил-4-(3-изопропил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-3-нафтилтио)бензоат
(а) O-3-Изопропил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилдиметилтиокарбамат
Аналогичным примеру 8(а) образом, путем взаимодействия 5 г (20,3 ммоль) 3-изопропил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтола с 3,26 г (26,4 ммоль) диметилтиокарбамоилхлорида, получают 2,26 г (33%) целевого продукта с т.пл. 99 - 100oC.
(б) S-3-Изопропил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилдиметилтиокарбамат
Аналогичным примеру 8(б) образом, из 2,9 г (8,7 ммоль) вышеполученного продукта, получают 1,63 г (56%) S-3-этил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилдиметилтиокарбамата с т.пл. 103- 104oC.
(в) 3-Изопропил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтиол
Аналогичным примеру 8(в) образом, из 4,5 г (14 ммоль) вышеполученного продукта, получают 2,9 г (84%) целевого тиола в виде оранжевого цвета масла.
(г) Этил-4-(3-изопропил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтио)бензоат
Аналогичным примеру 2(а) образом, путем взаимодействия 1,35 г (5,1 ммоль) 3-изопропил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтиола с 1,1 г (5,1 ммоль) метил-4-бромбензоата, получают 1,3 г (66%) целевого продукта в виде сложного этилового эфира.
Пример 22
Этил-4-(3-н-пропил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтио)бензоат
(а) 3-н-Пропил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтол
Аналогичным примеру 7(а) образом, путем взаимодействия 13,6 г (0,1 моль) 2-н-пропилфенола с 18,3 г (0,1 моль) 2,5-дихлор-2,5-диметилгексана, после хроматографии на колонке с диоксидом кремния при элюировании дихлорметаном, получают 11,6 г (65%) целевого производного фенола с т.пл. 96-97oC.
(б) O-3-н-Пропил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилдиметилтиокарбамат
Аналогичным примеру 8(а) образом, путем взаимодействия 15 г (61 ммоль) 3-пропил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтола с 9,8 г (79 ммоль) диметилтиокарбамоилхлорида, получают 15,9 г (78%) O-3-н-пропил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилдиметилтиокарбамата.
(в) S-3-н-Пропил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2- нафтилдиметилтиокарбамат
Аналогичным примеру 8(б) образом, из 10 г (30 ммоль) вышеполученного продукта, получают 6,8 г (68%) S-3-н-пропил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилдиметилтиокарбамата с т.пл. 102-104oC.
(г) 3-н-Пропил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтиол
Аналогичным примеру 8(в) образом, из 6,8 г (20,4 ммоль) вышеполученного продукта, получают 5 г (93%) целевого тиола в форме бесцветного масла.
(д) Этил-4-(3-н-пропил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтио)бензоат
Аналогичным примеру 2(а) образом, путем взаимодействия 2 г (7,6 ммоль) 3-н-пропил-5,6,7,8-тетрагидро-5,5,8,8-тетраметил-2-нафтилтиола с 2 г (7,6 ммоль) метил-4-иодбензоата, получают 2 г (65%) целевого продукта в форме сложного этилового эфира.
Пример 23
4-(3,5,5,8,8-Пентаметил-5,6,7,8-тетрагидро-2-нафтилтио)бензолметанол
В трехгорлую колбу, в атмосфере азота, вводят 144 мг (3,8 ммоль) литийалюминийгидрата и 50 мл ТГФ. Затем прикапывают раствор 1,4 г (3,8 ммоль) этил-4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио)бензоата в 25 мл ТГФ и кипятят с обратным холодильником в течение 8 часов. Избыток гидрида разлагают с помощью раствора двойной соли виннокислого натрия-калия, реакционную среду экстрагируют этилацетатом. Органическую фазу декантируют, сушат на сульфатом магния, выпаривают. Полученный остаток очищают путем хроматографии на колонке с диоксидом кремния, элюируя смесью гептана с этилацетатом (90-10). Получают 660 мг (51%) целевого спирта с т.пл. 81-82oC.
Пример 24
4-(3,5,5,8,8-Пентаметил-5,6,7,8-тетрагидро-2-нафтилтио)бензальдегид
В трехгорлую колбу, в атмосфере азота, вводят 60 мкл (0,7 ммоль) оксалилхлорида и 5 мл дихлорметана. При -60oC добавляют 100 мкл (1,4 ммоль) ДМСО и перемешивают 10 минут, затем добавляют раствор 200 мг (0,6 ммоль) 4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио)бензолметанола в 5 мл дихлорметана и 400 мкл (3 ммоль) триэтиламина. При комнатной температуре в течение 1 часа перемешивают, затем реакционную среду выливают в воду, экстрагируют дихлорметаном, органическую фазу декантируют, сушат над сульфатом магния, выпаривают. Полученный остаток очищают путем хроматографии на колонке с диоксидом кремния, элюируя смесью гептана с этилацетатом (80-20). Получают 145 мг (73%) целевого альдегида с т.пл. 98-99oC.
Пример 25
N-Этил-4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио) бензамид
(а) 4-(3,5,5,8,8-Пентаметил-5,6,7,8-тетрагидро-2-нафтилтио)бензоилхлорид
В колбу вводят раствор 1,4 г (4 ммоль) 4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио) бензойной кислоты в 100 мл безводного дихлорметана, добавляют 900 мкл (4,4 ммоль) дициклогексиламина и перемешивают в течение часа. После этого добавляют 320 мкл (4,4 ммоль) тионилхлорида и перемешивают в течение часа. Выпаривают досуха, остаток обрабатывают безводным диэтиловым эфиром, отфильтровывают соль дициклогексиламина и фильтрат выпаривают. Получают 1,5 г (100%) сырого хлорангидрида кислоты, который используют таким, какой есть, в продолжении синтеза.
(б) N-Этил-4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио)бензамид
В колбу вводят 640 мкл (8 ммоль) 70%-ного раствора этиламина и 20 мл ТГФ. Прикапывают раствор 735 мг (2 ммоль) 4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио)бензоилхлорида и в 30 мл ТГФ и перемешивают при комнатной температуре в течение трех часов. Реакционную среду выливают в воду, экстрагируют этилацетатом, органическую фазу экстрагируют, сушат над сульфатом магния, выпаривают. Полученный остаток очищают путем хроматографии на колонке с диоксидом кремния, элюируя смесью гептана с этилацетатом (90-10). После выпаривания растворителей, получают 307 мг (41%) целевого этиламида с т.пл. 223-224oC.
Пример 26
N-4-Гидроксифенил-4-(3,5,8,8-пентаметил-5,6,7,8-тетрагидро-2- нафтилтио)бензамид
(а) N-4-Ацетоксифенил-4-(3,5,5,8,8)-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио)бензамид
Аналогичным примеру 25(б) образом, путем взаимодействия 735 мг (2 ммоль) 4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио)бензоилхлорида с 900 мг (6 ммоль) 4-аминобензилацетата, получают 250 мг (26%) целевого амида с т. пл. 186-187oC.
(б) N-4-Гидроксифенил-4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио)бензамид
Аналогичным примеру 2(а) образом, из 100 мг (0,2 ммоль) N-4-ацетоксифенил-4-(3,5,5,8,8-пентаметил-5,6,7,8-тетрагидро-2-нафтилтио)бензамида, получают 65 мг (71%) целевого продукта с т.пл. 236 - 237oC.
Пример 27
В этом примере иллюстрируют различные конкретные формулировки на основе соединений согласно изобретению.
А. Вводимая перорально формулировка
(а) Таблетка весом 0,2 г:
соединение, полученное в примере 7 - 0,001 г
крахмал - 0,114 г
дикальцийфосфат (вторичный фосфат кальция) - 0,020 г
диоксид кремния - 0,020 г
лактоза - 0,030 г
тальк - 0,010 г
стеарат магния - 0,005 г
(б) Суспензия для питья в ампулах по 10 мл.:
соединение примера 8 - 0,05 г
глицерин - 1,000 г
70%-ный сорбитол - 1,000 г
сахаринат натрия - 0,010 г
метил-пара-гидроксибензоат - 0,080 г
ароматизирующие средства - достаточное количество
очищенная вода - до общего количества 10 мл
Б. Применяемая топически формулировка
(а) Мазь
соединение примера 8 - 0,020 г
изопропилмиристат - 81,700 г
жидкое вазелиновое масло - 9,100 г
диоксид кремния ("Аэросил 200", выпускаемый в продажу фирмой ДЕГУССА) - 9,180 г
(б) Мазь
соединение примера 9 - 0,300 г
медицинский вазелен - до общего количества 100 г
(в) Неионный крем вода-в-масле
соединение примера 7 - 0,100 г
смесь образующих эмульсии ланолиновых спиртов, восков и масел (bucerine anhydre, выпускаемая в продажу фирмой BDF) - 39,900 г
метил-пара-гидроксибензоат - 0,075 г
пропил-пара-гидроксибензоат - 0,075 г
стерильная деминерализованная вода до - 100 г
(г) Лосьон
соединение примера 8 - 0,100 г
полиэтиленгликоль (ПЭГ-400) - 69,900 г
95%-ный этанол - 30,000 г
(д) Гидрофобная мазь
соединение примера 7 - 0,300 г
изопропилмиристат - 36,400 г
силиконовое масло ("Rhodarsil 47 V300", выпускаемое в продажу фирмой РОН-ПУЛЕНК) - 36,400 г
пчелиный воск - 13,600 г
силиконовое масло ("Abil 300 000 cst", выпускаемое в продажу фирмой ГОЛЬДШМИДТ) - до 100 г
(а) Неионный крем масло-в-воде
соединение примера 7 - 0,500 г
цетиловый спирт - 4,000 г
глицеринмоностеарат - 2,500 г
стеарат ПЭГ-50 - 2,500 г
масло сального дерева - 9,200 г
пропиленгликоль - 2,000 г
метил-пара-гидроксибензоат - 0,075 г
пропил-пара-гидроксибензоат - 0,075 г
стерильная деминерализованная вода до - 100 г
Описываются новые бициклические ароматические соединения общей формулы I, где R1 - группа СО-О-R8; R8 - водород, алкильный, линейный или разветвленный радикал с 1 - 20 атомами углерода или СОR; R - низший алкил; А - радикал, выбираемый из группы (а), (b), (d); Х - обозначает -O-, S(O)t или -NR9-; R2 - водород, галоген, низший алкил, группа OR9; t - целое число, равное 0, 1 или 2; R9 - водород, галоген, низший алкил, группа OR9; t - целое число, равное 0, 1 или 2; R9 - водород или низший алкил; R11 и R12 - водород или низший алкил или их соли. Соединения проявляют активность в отношении дифференциации и пролиферации клеток. Описываются также фармацевтические и косметические композиции на основе соединений формулы I. 3 с. и 11 з.п. ф-лы, 1 ил.
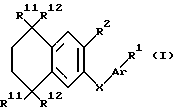
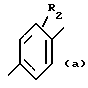
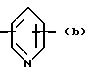
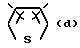
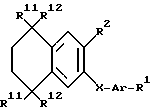
где R1 - группа CO-O-R8, где R8 - водород, алкильный, линейный или разветвленный, радикал с 1 - 20 атомами углерода или COR7, где R7 - низший алкил; Ar - радикал, выбираемый из следующей группы: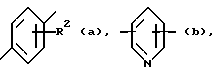
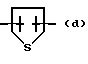
X - обозначает -O-, S(O)t или -NR9-;
R2 - водород, галоген, низший алкил, группа OR9;
t - целое число, равное 0,1 или 2;
R9 - водород или низший алкил;
R11 и R12 - водород или низший алкил;
или их соли.
| EP, 0155524, A1, 1985 | |||
| SU, 904522, A, 1982 | |||
| EP, 071535, A, 1982. |
Авторы
Даты
1999-11-20—Публикация
1995-04-25—Подача