Изобретение относится к медицине, а именно к стоматологии, к созданию средств, используемых для остановки небольших кровотечений в полости рта.
Известны и широко применяются в медицине многочисленные локальные гемостатические средства, приготовленные на основе компонентов крови /См. Адамян А.А. и др., Ж. "Хирургия им. Н.И.Пирогова", 1993, N 11, с. 81-85), природных полимеров (см. Адамян и др. Ж. "Хирургия им. Н.И.Пирогова", 1984, N 11, с. 47-51), синтетических как "Феракрил" (см. Ж. "Фармакология и токсикология", 1991, т. 54, N 5, с.36-40) и солей металлов (Чухаджян Г.А. и др., "Арм.хим. журнал", 1984, т. 27, N 10, с. 622-657) и др.
Наблюдения, накопленные в последние годы, показывают, что при разработке новых гемостатических средств следует учесть, что:
1) на любой раневой поверхности в полости рта присутствует обширная ассоциация различных микроорганизмов, которые (в особенности в условиях нарушений микроциркуляции, в десне, например, при пародонтите) являются причиной воспалительно-нагноительных послеоперационных осложнений;
2) некоторые гемостатические средства, в особенности, на основе природных биополимеров и компонентов крови, сами иногда являются питательной средой для размножения микроорганизмов;
3) имеется большая опасность инфицирования больных ВИЧ-инфекцией и вирусом гепатита-B при использовании лекарственных средств, имеющих в своем составе компоненты крови;
4) нередко составы на основе солей металлов вызывают ожоги и некроз мягких тканей слизистой полости рта;
5) особым требованием к гемостатическим средствам являются физико-химические свойства образовавшегося кровяного сгустка, плотный сгусток хорошо фиксируется на раневой поверхности, предотвращает повторное кровотечение, препятствует проникновению вторичной инфекции.
Известно гемостатическое средство, предназначенное для остановки локальных кровотечений, обладающее одновременно и антибактериальным действием.
В состав входит пищевой желатин и плазма крови крупного рогатого скота. В качестве антимикробного средства в состав включен канамицина сульфат (Авт. свид. СССР N 725289, A 61 K 35/14).
Известны синергические комбинации, обладающие выраженной противогеморрагической активностью, содержащие (%): 5-30 AlCl3, 10-35 дубильной кислоты, 5-25 FeCl3, 10-45 ZnCl2, и/или 1-10 K-Al - сульфата в качестве вяжущих средств и 0,01-2 ПАВ катионогенного (цетилпиридинийхлорид, бензалконийхлорид, бензэтонийхлорид, хлоргексидин, глюконат хлоргексидина), анионогенного (лаурилсульфатa) или амфотерного (твины, спаны и т.п.) типа в воде или в водно-органическом растворителе.
/РЖХ 190223П (1982) Противогеморрагические составы. Яп. пат. 56-139423, МКИ A 61 K 45/08, Ямамото Хиродзи).
Для остановки небольших кровотечений в полости рта патентуется применение препарата в содержании 10-40% вяжущих веществ (дубильная кислота, AlCl3, FeCl3, ZnCl2 и др.), 0,01-2% ПАВ (цетилпиридинийхлорид, бензалконийхлорид, бензэтонийхлорид, хлоргексидин, лаурилсульфат, твины, спаны и др.) и разбавители (смесь воды с глицерином, спиртом, пропиленгликолем и др.). Пример. Смесь 25 г AlCl3 и 0,5 г цетилпиридинийхлорида растворяют в воде и доводят объем до 100 мл.
/РЖХим 60190 П Зубоврачебные кровоостанавливающие составы, Ямамото Хиродзи, пат. США N4395398, МКИ A 61 K 33/30, A 61 K 33/26, НКИ 424-145/.
Задачей настоящего изобретения является расширение арсенала гемостатических средств местного действия, обладающего антимикробным действием.
Средство, предназначенное для применения в стоматологии для остановки небольших кровотечений в полости рта, состоит из солей металлов, их смеси друг с другом и/или с хлористым кальцием, четвертичного аммониевого соединения и водорастворимого биосовместимого синтетического полимера, растворенные в водной среде или в физиологическом растворе, при этом концентрация солей металлов колеблется в пределах 2,5 до 50% весовых, а их соотношение друг к другу от 9: 1 до 1:9, концентрация четвертичного аммониевого соединения от 0,005 до 5% весовых, а водорастворимого полимера не более 5% весовых в пересчете на общее количество смеси.
В качестве основы для гемостатического состава были выбраны соли металлов, как AlCl3, 6H2O, FeCl3, 6H2O, CaCl2 • H2O, AlK (SO4)2 • 12H2O, ZnCl2 безводный с Т пл.= 293oC, их комбинации, другие соли и комплексы. Содержание основного вещества в указанных солях должно быть не менее 96%. Содержание тяжелых металлов осаждаемых сероводородом, не более 0,002%.
В качестве четвертичного аммониевого соединения, обладающего антимикробным спектром, в первую очередь были испытаны препараты, выпускаемые промышленностью и разрешенные к применению в медицинской практике, как, например, "Катамин АБ" (Россия).
"Катамин АБ" - 50%-ный водный раствор алкилдименил бензиламмония хлорид с алкильными радикалами C10H21 - C18H37.
"Катамин АБ" обладает широким спектром антимикробного действия, подавляя при низких концентрациях рост грамположительных, грамотрицательных бактерий и грибов. (Рудзит Э.А., Антибиотики, 1981, т. 26, N 11, стр. 847-851).
По сравнению с антибиотиками, к которым быстро возникает лекарственная устойчивость, привыкание микроорганизмов к нему наступает значительно медленнее. Они отмечаются исключительной стабильностью, хорошо растворяются в воде
"Катамин АБ", продукт Московского завода
"Синтез" по ТУ (6-01-816-78, эмпирическая формула [R(CH3)2CHCH2C6H5] +Cl-, где R - смесь прямоцепочных алкильных остатков C10 - C18. Средний молекулярный вес 346-376. Выпускается в виде 50%-ного раствора в воде, pH - водного раствора 6,0-7,0.
В качестве антибактериальных веществ применены также другие представители четвертичных аммониевых соединений формулы R1R2R3R4N+X-, обладающие сильными антибактериальными свойствами /И.М.Уварова и др. Ж. Успехи химии, стр. 1217-1224/, где R1, R2, R3, R4 - алкильные, арильные, циклоалкильные, бензильные, гетероциклические, а X = Cl, Br, остатки различных органических и нерганических кислот.
Из синтетических полимеров применялись поливиниловый спирт (ПВС), поливинилпирролидон (ПВМ), карбоксиметилцеллюлоза (КМЦ) и др. водорастворимые синтетические полимеры и сополимеры, широко применяемые в фармацевтических составах, лекарственных средствах и инфузионных растворах.
Получение гемостатических средств осуществляется следующим образом.
Пример 1.
25 г гексагидрата треххлористого алюминия растворяют в 50 см3 дистиллированной воды, в полученный раствор добавляется 0,5 см3 "Катамина АБ" (50%-ный водный раствор), объем раствора водой доводят до 100 см3.
Пример 2.
50 г гексагидрата треххлористого алюминия растворяют в воде, добавляют 2 см3 "Катамина АБ" (50%-ный водный раствор) и водой объем смеси доводят до 100 см3.
Пример 3.
Аналогично примеру 1. Готовится гемостатическое средство на 50 г гексагидрата треххлористого алюминия и 5 см3 "Катамина АБ" (50%-ный раствор). Объем раствора доводится до 100 см3 водой.
Пример 4.
Аналогично примеру 1. Готовится раствор из 2,5 г гексагидрата треххлористого алюминия, 0,005 см3 "Катамина АБ" (50%-ный раствор). Объем раствора доводится до 100 см3 водой.
Пример 5.
50 г гексагидрата треххлористого железа растворяют в 50 см3 воды, добавляют 0,5 см3 "Катамина АБ" (50%-ный водный раствор) и объем раствора водой доводят до 100 см3.
Пример 6.
45 г гексагидрата треххлористого алюминия растворяют в воде, добавляется 5 г гидрата хлористого кальция, перемешивают до растворения, после чего добавляется 0,5 см3 "Катамина АБ" (50%-ный водный раствор) перемешивают и объем смеси водой доводят до 100 см3.
Пример 7.
25 г гексагидрата треххлористого железа растворяется в воде, добавляют 25 г гидрата хлористого кальция, перемешивают до растворения, после чего добавляют 0,5 см3 "Катамина АБ" (50%-ный водный раствор), перемешивают и объем смеси водой доводят до 100 см3.
Пример 8.
25 г додекагидрата алюмокалиевых квасцов растворяется в 50 см3 в воде, добавляется 0,05 см3 "Катамина АБ" (50%-ный водный раствор) и объем смеси водой доводится до 100 см3.
Пример 9.
2,5 г гексагидрата треххлористого алюминия растворяется в 50 см3 0,9%-ном изотоническом растворе хлористого натрия, добавляется 0,05 см3 "Катамина АБ" (50%-ный водный раствор) и объем доводится до 100 см3 0,9%-ным раствором хлористого натрия.
Пример 10.
10 г гексагидрата треххлористого алюминия, 10 г гексагидрата треххлористого железа и 5 г гидрата хлористого кальция растворяется в 50 см3 воды, добавляется 0,5 см3 "Катамина АБ" (50%-ный водный раствор) и объем смеси доводится до 100 см3 водой.
Пример 11.
25 г гексагидрата треххлористого алюминия растворяется в 50 см3 воды, добавляется 0,5 см3 "Катамина АБ" (50%-ный водный раствор), затем 0,5 г поливинилпирролидона и объем раствора доводится до 100 см3, перемешивается до полного растворения.
Пример 12.
25 г гексагидрата треххлористого алюминия растворяется в воде, добавляется 0,5 см3 "Катамина АБ" (50%-ный водный раствор), затем добавляется 1 г поливинилового спирта и объем раствора доводится до 100 см3 водой, перемешивается до полного растворения.
Пример 13.
Состав готовится аналогично примеру 1, но вместо "Катамина АБ" применяется 0,25 карбоксидодецил оксиметилтриметиламмоний хлористый.
Пример 14.
Состав готовится аналогично примеру 1, но вместо "Катамина АБ" применялся 0,25 г диоктилдиэтил аммонийбромистый.
Предложенные гемостатические средства были апробированы в экспериментальных и клинических условиях на добровольцах.
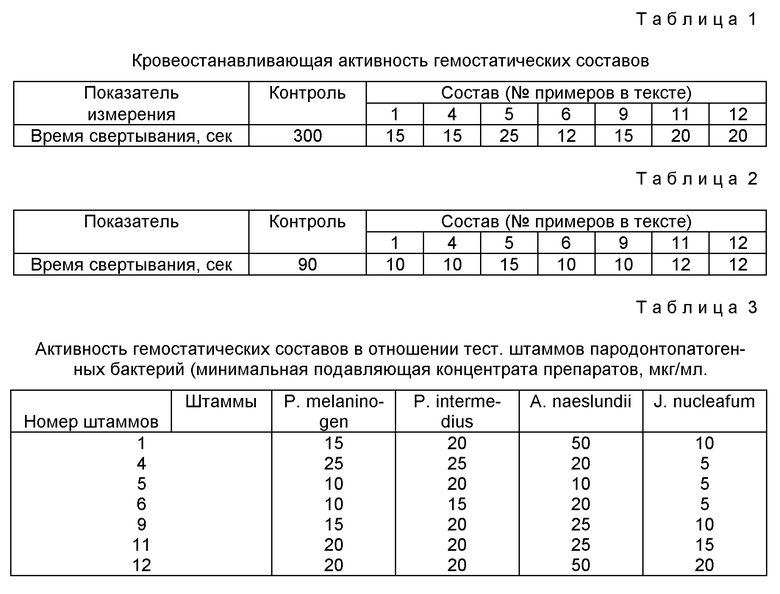
Эффективность предложенных гемостатических составов на свертываемость крови в условиях in vitro определяли по времени свертывания (Для определения времени свертывания в пробирку, содержащую 0,5 мл гемостатического состава, быстро добавляли 0,5 мл крови и засекали время. Кровь у кролика брали из сердца пункцией. Параллельно ставили контроль (только кровь).
Как следует из таблицы 1 все приведенные составы обладают высокой коагулирующей способностью по сравнению с нормой.
Исследовалась резистентность полученных сгустков к лизису (Методические рекомендации по определению свертывающей способности крови, Ленинград, 1971), что одним из важных требований, предъявляемых к гемостатическим средствам, является образование плотного кровяного сгустка, не подвергающегося лизису, этим уменьшается возможность повторного кровотечения. Исследование сгустков крови, получаемых при действии предложенных составов, показали увеличение резистентности к лизису по сравнению с контролем. Во всех исследованных составах разница в весе образующихся сгустков через 24 часа не отмечалось.
Исследование гемостатической активности полученных средств проводились на крысах самцах массой 150-200 г под нембуталовой анестезией (35 мг/кг массы). Обнажали печень и наносили на нее два надреза длиной 1 см и глубиной 1-2 мм. Затем одновременно марлевым тампоном тонким слоем наносили гемостатическое средство на первый надрез, а на второй - стерильный 0,9%-ный раствор NaCl (контроль) и засекали время до полного свертывания крови.
Определялась чувствительность важнейших пародонто-патогенных видов анаэробных бактерий к описанным средствам. Определяли минимальную подавляющую концентрацию (МПК). Исследование проводили с использованием кассетного микрометода разведения препаратов в плотной питательной среде.
/Р.В. Ушаков и соавт. "Кассетный микрометод определения чувствительности анаэробных микроорганизмов к антибактериальным препаратам", Ж. "Антибиотики и химиотерапия", 1991, т. 37, N 5, стр. 10-12).
Из растворов гемостатиков готовили разведения, содержащие соответственно 200, 100, 50, 20, 10, 5, 4, 2 и 1 мкг/мл активного вещества, которые использовались для заполнения кассеты с питательной средой. В качестве тест-культуры использовали клинические штаммы бактерий, выделенных от больных генерализованным пародонтитом:
1. Prevotella melaninogenica
2. Peptosteptococcus intermedius
3. Streptococcus sanguis.
4. Actinomyces naeslundii
5. Fusobacterium nucleatum
Указанные тест-культуры вносили в систему для определения чувствительности в количестве 10 клеток на 1 мл, в объеме 0,1 мл. Взвесь тест-культуры готовили в стерильном физиологическом растворе по оптическому стандарту мутности после выращивания в течение 48 часов при 37oC в анаэробных условиях (80% азота, 10% водорода, 10% углекислого газа).
Как видно из таблицы 3 гемостатические составы обладают высокой активностью в отношении тест-штаммов пародонтопатогенных видов: обличатно-анаэробных (P. melaninogenica, P. intermedius, A. naeslundii и F. nucleatum) и факультативно-анаэробных - S. sanguis.
Изучение антимикробной активности полученных составов проводились методом обеззараживания батистовых тест-объектов. Спектр бактерицидного действия изучен в отношении 7-ми патогенных грамположительных и грамотрицательных микроорганизмов,
S. aureus (906)
E. coli (1257)
S. typhimurium (55)
Sh. Sonnei (14)
Sh. flexneri (16)
Pr. mirabilis (15)
Ps. aeruginosa (124)
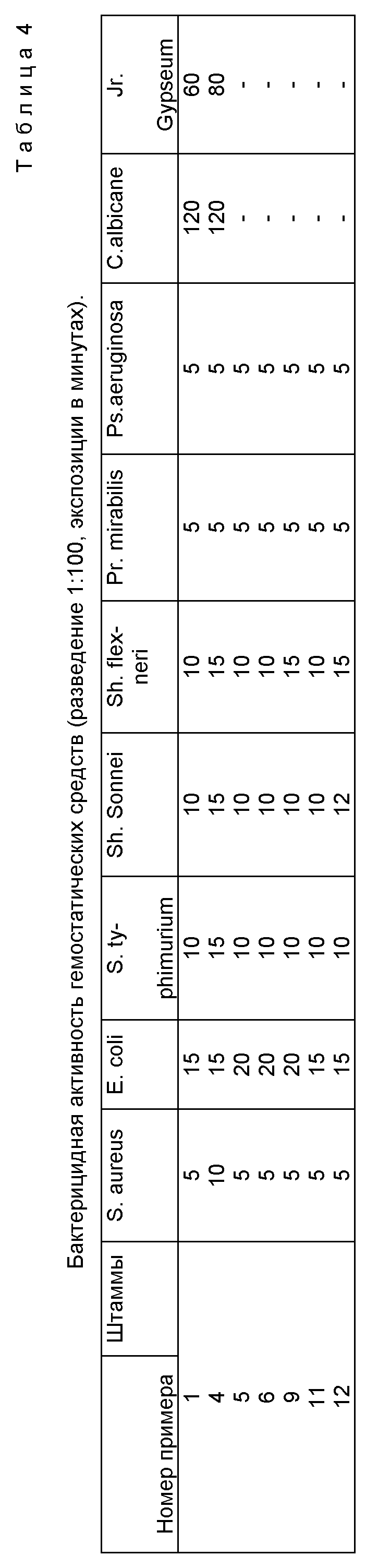
а фунгицидная активность - в отношении грибов C. albicans и Jr. gypseum при экспозициях от 5 до 120 минут. Указанные микроорганизмы были отобраны по признаку, устойчивости, превосходившей устойчивость эталонных штаммов. В качестве нейтрализатора использовали 0,1 и 4% - водные растворы додедилбензолсульфата натрия.
Результаты, приведенные в таблице 4 показывают, что полученные гемостатические составы с "Катином АБ" обладают бактерицидной, фунгицидной активностью.
Гемостатические составы могут быть использованы для остановки кровотечения:
- корневых каналов зубов после экстракции пульпы,
- из тканей пародонта при снятии зубных отложений парондотальных карманов,
-из лунки зуба,
- при лоскутной операции,
- из раневых поверхностей при проведении разного рода хирургических вмешательств в полости рта.
В корневые каналы зубов и в пародонтальные карманы препарат вносят с помощью турунды на 2-5 сек в лунки удаленных зубов вводят на ватных или марлевых тампонах размером 0,5 х 0,5 см на 10-15 сек. При необходимости дальнейшего послойного наращивания кровяного сгустка новый тампон, смоченный гемостатическим средством, вводят в лунку, не удаляя первоначально образовавшегося сгустка.
При откидывании лоскута, при хирургическом лечении пародонтита область слизисто-надкостичного лоскута покрывается гемостатическим средством в виде аппликации.
Апробация предложенных составов гемостатических средств показала, что они:
- обладают высокой гемостатической активностью быстро свертывают кровь;
- обладают широким спектром антимикробного действия;
- имеют высокую стабильность по отношению к ферментам, кислотам и солям и др. компонентам роговой жидкости;
- привыкание к нему штаммов микроорганизмов отсутствует или наступает медленно;
- не вызывают ожоги и некрозы мягких тканей полости рта;
- бесцветны, не затрудняют визуальные наблюдения;
- безопасны, в отличие от гемостатических средств на основе компонентов крови и других биологических и природных полимеров;
- образуют плотный кровяной сгусток, который не теряет свою механическую твердость в течение 24 часов.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИМИКРОБНОЕ СРЕДСТВО | 2000 |
|
RU2180222C2 |
| ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИЕ САМОКЛЕЯЩИЕСЯ ПЛЕНКИ МЕСТНОГО ДЕЙСТВИЯ ДЛЯ ДОСТАВКИ ДОЗИРОВАННЫХ КОЛИЧЕСТВ ФТОР-ИОНОВ | 2000 |
|
RU2179454C2 |
| ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКОЕ СРЕДСТВО МЕСТНОГО ДЕЙСТВИЯ В ВИДЕ САМОКЛЕЯЩЕЙСЯ ПЛЕНКИ ДЛЯ РЕМИНЕРАЛИЗАЦИИ ТВЕРДЫХ ТКАНЕЙ ЗУБОВ | 2003 |
|
RU2238078C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ПОЛОСТИ РТА | 1994 |
|
RU2075965C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНАСТЕЗИРУЮЩИМ И АНТИБАКТЕРИАЛЬНЫМ ДЕЙСТВИЕМ | 1998 |
|
RU2153326C2 |
| АНТИМИКРОБНОЕ СРЕДСТВО | 2002 |
|
RU2216335C1 |
| СРЕДСТВО И СПОСОБ ОТБЕЛИВАНИЯ ЗУБОВ | 2005 |
|
RU2283081C1 |
| ПРОЛОНГИРОВАННЫЕ ЛЕКАРСТВЕННЫЕ ФОРМЫ МЕСТНОГО ДЕЙСТВИЯ, ОКАЗЫВАЮЩИЕ АКТИВИРУЮЩЕЕ ВЛИЯНИЕ НА ИММУННУЮ СИСТЕМУ | 2001 |
|
RU2185807C1 |
| ПРОЛОНГИРОВАННЫЕ ЛЕКАРСТВЕННЫЕ ФОРМЫ МЕСТНОГО ДЕЙСТВИЯ, ОБЛАДАЮЩИЕ АНТИБАКТЕРИАЛЬНОЙ И ИММУНОАКТИВИРУЮЩЕЙ СПОСОБНОСТЬЮ | 2001 |
|
RU2185806C1 |
| АДГЕЗИВНАЯ ПЛЕНКА ДЛЯ ФИКСАЦИИ СЪЕМНЫХ ПРОТЕЗОВ | 2001 |
|
RU2225705C2 |
Изобретение относится к области медицины, а именно стоматологии, и касается средств, используемых для остановки кровотечений в полости рта. Гемостатическое средство содержит смесь солей металлов с СаСl2, четвертичное аммониевое соединение и водорастворимый биосовместимый синтетический полимер, растворенные в водной среде или среде 0,9%-ного раствора NаСl. Средство обладает высокой коагулирующей способностью, а также антимикробной активностью, имеет высокую стабильность по отношению к ферментам, кислотам и солям. 4 з.п.ф-лы, 4 табл.
Соли металлов - 2,5 - 50,0
Четвертичное аммониевое соединение - 0,025 - 5,0
Вода или физиологический раствор - Остальное
при этом соотношение солей металлов в смеси составляет 9:1 - 1:9.
| Патент США N 4395398, A 61 K 33/26, 1978 | |||
| Способ остановки кровотечения | 1983 |
|
SU1263248A1 |
| SU 6198622 A, 25.11.79. | |||
Авторы
Даты
1999-12-10—Публикация
1997-10-31—Подача