Изобретение относится к аналитической химии органических соединений и может быть использовано для контроля технологических и очищенных сточных вод предприятий лакокрасочной и текстильной промышленности.
Аналогом может служить редоксиметрическое титрование гидроксибензойных кислот в водных растворах с фотометрической индикацией точки эквивалентности [1]. Для определения нитробензойных кислот данный метод ранее не применялся.
В качестве прототипа выбран способ определения м-нитробензойной кислоты методом хроматографии на бумаге [2]. Недостатки прототипа - сравнительно высокие пределы обнаружения (1,2 мг/дм3) и длительность анализа (60-90 мин).
Задачи изобретения - снижение пределов обнаружения и сокращение продолжительности анализа.
Поставленные задачи достигаются тем, что в качестве пробоподготовки применяют экстракционное концентрирование трет.бутиловым спиртом в присутствии 15-20 мас. % сульфата лития по отношению к пробе; последующее определение осуществляют непосредственно в экстракте методом фотометрического титрования по редоксиметрическому механизму (титрант - водный раствор йода).
Технический результат состоит в том, что данный способ позволяет определить м-нитробензойную кислоту в водных растворах на уровне 2,42 мкг/дм3, продолжительность анализа 30-40 мин. Предел обнаружения снижается за счет предварительного концентрирования и фотометрического титрования кислоты по редоксиметрическому механизму. Продолжительность анализа сокращается за счет исключения стадии реэкстракции, поскольку определение кислоты осуществляется непосредственно в экстракте.
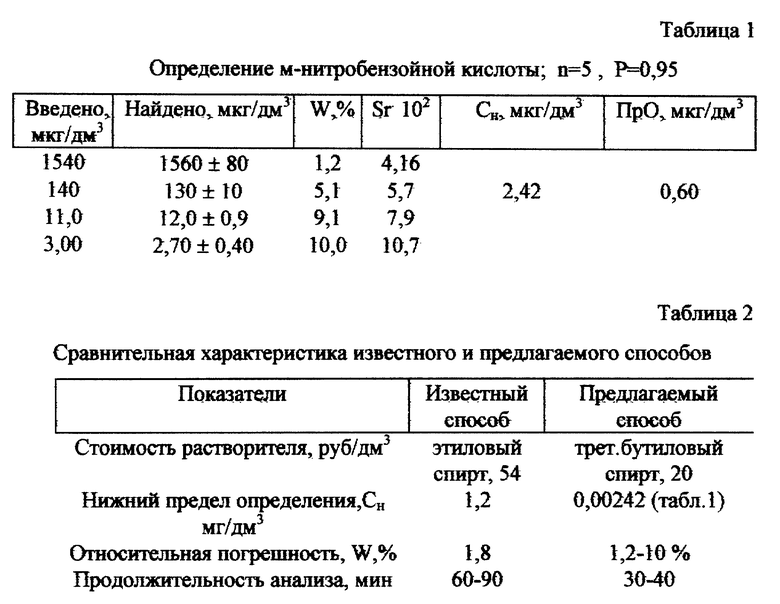
Способ осуществляется следующим образом. К 100 см3 водной пробы, содержащей м-нитробензойную кислоту, добавляли сульфат лития из расчета 15-20 мас.% по отношению к водной пробе, 20 см3 трет.бутилового спирта и экстрагировали 15 мин. После полного расслаивания системы (1-2 мин) органическую фазу отделяли, количественно переносили в ячейку для фотометрического титрования и титровали водным раствором йода (фиг. 1). Содержание м-нитробензойной кислоты (m, мг) находили по формуле
m - 0,01 • C • V • M/R,
где C - концентрация титранта, моль/дм3; V - объем титранта, пошедший на титрование кислоты, см3; R - степень извлечения кислоты при экстракции трет. бутиловым спиртом, %; M - эквивалентная масса кислоты, г/моль.
Применение способа иллюстрируется следующими примерами.
Пример 1.
К 100 см3 водной пробы, содержащей 1,54 мг/дм3 м-нитробензойной кислоты, добавляли сульфат лития из расчета 15 мас.% по отношению к водной пробе, 20 см3 трет.бутилового спирта и экстрагировали в течение 15 мин. После полного расслаивания системы (1-2 мин) органическую фазу отделяли и количественно переносили в ячейку для фотометрического титрования и титровали водным раствором йода. Результаты определения приведены в табл.1.
Пример 2.
К 100 см3 водной пробы, содержащей 0,14 мг/дм3 м-нитробензойной кислоты, добавляли сульфат лития из расчета 15 мас.% по отношению к водной пробе, 20 см3 трет.бутилового спирта. Далее анализ проводили аналогично примеру 1.
Пример 3.
К 100 см3 водной пробы, содержащей 0,011 мг/дм м-нитробензойной кислоты, добавляли сульфат лития из расчета 15 мас.% по отношению к водной пробе, 20 см3 трет.бутилового спирта. Далее анализ проводили аналогично примеру 1.
Пример 4.
К 100 см3 водной пробы, содержащей 0,001 мг/дм3 м-нитробензойной кислоты, добавляли сульфат лития из расчета 15 мас.% по отношению к водной пробе, 20 см3 трет.бутилового спирта. далее анализ проводили аналогично примеру 1.
Пример 5.
К 100 см3 водной пробы, содержащей 0,15 мг/дм3 м-нитробензойной кислоты, добавляли сульфат лития из расчета 16 мас.% по отношению к водной пробе, 20 см3 трет.бутилового спирта. Далее анализ проводили аналогично примеру 1.
Пример 6.
К 100 см3 водной пробы, содержащей 0,15 мг/дм3 м-нитробензойной кислоты, добавляли сульфат лития из расчета 17 мас.% по отношению к водной пробе, 20 см3 трет.бутилового спирта. Далее анализ проводили аналогично примеру 1.
Пример 7.
К 100 см3 водной пробы, содержащей 0,15 мг/дм3 м-нитробензойной кислоты, добавляли сульфат лития из расчета 18 мас.% по отношению к водной пробе, 20 см3 трет.бутилового спирта. Далее анализ проводили аналогично примеру 1.
Пример 8.
К 100 см3 водной пробы, содержащей 0,15 мг/дм3 м-нитробензойной кислоты, добавляли сульфат лития из расчета 19 мас. % по отношению к водной пробе, 20 см3 трет.бутилового спирта. Далее анализ проводили аналогично примеру 1.
Пример 9.
К 100 см3 водной пробы, содержащей 0,15 мг/дм3 м-нитробензойной кислоты, добавляли сульфат лития из расчета 20 мас.% по отношению к водной пробе, 20 см3 трет.бутилового спирта. Далее анализ проводили аналогично примеру 2.
Пример 10.
К 100 см3 водной пробы, содержащей 0,15 мг/дм3 м-нитробензойной кислоты, добавляли сульфат лития из расчета 14 мас.% по отношению к водной пробе, 20 см3 трет.бутилового спирта. Органический растворитель не выделяется в самостоятельную фазу. Дальнейшее определение невозможно.
Пример 11.
К 100 см3 водной пробы, содержащей 0,15 мг/дм3 м-нитробензойной кислоты, добавляли сульфат лития из расчета 21 мас.% по отношению к водной пробе, 20 см3 трет.бутилового спирта. Высаливатель выделяется в самостоятельную твердую фазу. Дальнейшее определение невозможно.
По полученным результатам определения м-нитробензойной кислоты в водных растворах и рекомендациям [3] рассчитаны относительная погрешность (W, %), относительное стандартное отклонение (Sr), предел обнаружения (ПрО, мкг/дм3) и нижний уровень определяемых концентраций (Cн, мкг/дм3), табл.1.
Сравнительная характеристика известного и предлагаемого способов (табл. 2) объективно оценивает преимущества и недостатки описанного способа.
Определению м-нитробензойной кислоты мешают пирогаллол, резорцин, галловая и β-резорциловая кислоты; не мешают 10-кратные избытки фенола, бензойной, о- и п-нитробензойных кислот.
Предлагаемый способ применим для анализа технологических и очищенных сточных вод предприятий лакокрасочной и текстильной промышленности.
Литература
1. Эшворт М.Р.Ф. Титриметрические методы анализа органических соединений. Методы косвенного титрования. -М.: Химия, ч.1. -1972. -243 с.
2. А.с. 129645, СССР МКИ4 G 01 N 30/90. Способ определения м-нитробензойной кислоты /Бардин В.В., Крауклиш И.В., Леонтьева Л.Б., Мохов А.А. // Изобретения. -1987.-N 8, -с.194.
3. Золотов Ю.А., Дорохова Е.Н., Фадеева В.И. Основы аналитической химии. -М.: Высшая школа, 1996.-Т.1.-383 с.
Изобретение относится к аналитической химии органических соединений и может быть использовано для контроля технологических и очищенных сточных вод предприятий лакокрасочной и текстильной промышленности. В способе в качестве пробоподготовки применяют экстракционное концентрирование трет.бутиловым спиртом в присутствии 15-20 мас.% сульфата лития по отношению к пробе. Последующее определение осуществляют непосредственно в экстракте методом фотометрического титрования по редоксиметрическому механизму (титрант - водный раствор йода). Технический результат состоит в том, что данный способ позволяет определить м-нитробензойную кислоту в водных растворах на уровне 2,42 мкг/дм3, продолжительность анализа 30 - 40 мин. Предел обнаружения снижается за счет предварительного концентрирования и фотометрического титрования при определении кислоты по редоксиметрическому механизму. Продолжительность анализа сокращается за счет исключения стадии реэкстракции, поскольку определение кислоты осуществляется непосредственно в экстракте. 1 ил., 2 табл.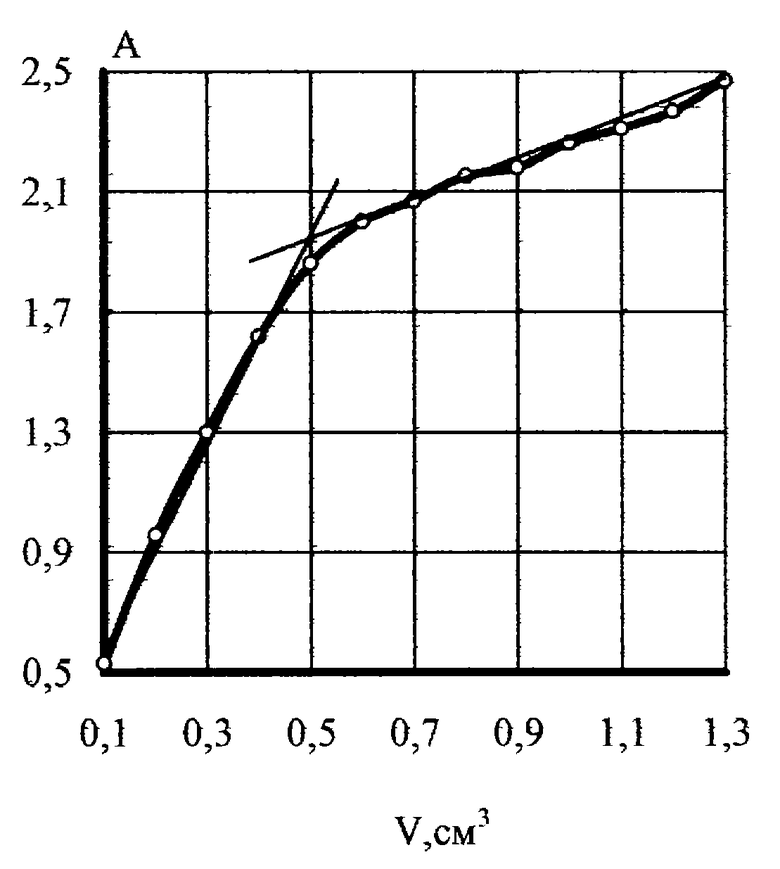
Способ определения м-нитробензойной кислоты в водных растворах, включающий пробоподготовку и последующее определение, отличающийся тем, что в качестве пробоподготовки применяют экстракционное концентрирование трет.бутиловым спиртом в присутствии 15 - 20 мас.% сульфата лития по отношению к пробе, определение м-нитробензойной кислоты осуществляют непосредственно в экстракте методом фотометрического титрования водным раствором йода по редоксиметрическому механизму.
| Способ определения 3,5-динитробензойной кислоты | 1981 |
|
SU1006984A1 |
| Способ определения 2,3,6-трихлорбензойной кислоты | 1985 |
|
SU1242778A1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ БЕНЗОЙНОЙ ИЛИ 2-ОКСИБЕНЗОЙНОЙ КИСЛОТ В ПРОБЕ, СОДЕРЖАЩЕЙ ОДНУ ИЗ НИХ | 1994 |
|
RU2084871C1 |
| US 4276049 A, 30.06.81 | |||
| Коренман И.М | |||
| Фотометрический анализ | |||
| Методы определения органических соединений | |||
| - М.: Химия, 1975, с.64, 281. | |||
Авторы
Даты
1999-12-10—Публикация
1998-05-26—Подача