Изобретение относится к медицине, а именно к способам детоксикации крови, и может быть использовано при лечении заболеваний, сопровождающихся септической интоксикацией и полиорганной недостаточностью.
Известен способ криоафереза путем гепарин-холодовой обработки плазмы больного с последующим отделением плазмы от криоглобулинового осадка и возвращением ее больному (1, 2).
Известен способ криоплазмосорбции, сочетающий вышеуказанный способ с перфузией плазмы через сорбент (3).
Однако вышеизвестные способы не обеспечивают:
а) не гарантируют стерильности плазмы при сепсисе;
б) полного очищения плазмы от токсических метаболитов при тяжелой печеночной недостаточности;
в) выпадения криоосадка у больных со сниженной преципитацией криоглобулинов (4).
Цель изобретения: повышение степени детоксикации плазмы при криоаферезе и обеспечение ее стерильности. Цель достигается тем, что плазму охлаждают не при +4oC, а при -10oC и после отделения ее от криоосадка подвергают плазмосорбции с кратностью 5-7 раз, плазмодиализу и ультрафиолетовому облучению.
Способ осуществляют следующим образом. В плазму больного, полученную во время плазмафереза, добавляют согласно известной методике гепарин и оставляют при -10oC на 16-20 часов. Затем плазму размораживают при комнатной температуре, центрифугируют при -5oC и отделяют от криоосадка. После обработки плазмы при -10oC у больных со сниженной преципитацией криоглобулинов выпадает осадок объемом 1/3 - 1/4 пакета. Затем плазму подвергают перфузии через сорбент при скорости 120-150 мл/мин со следующей кратностью: при уровне билирубина до 40 мкм/л - 5-кратно, 40-70 мкм/л - 7-кратно, 70-90 мкм/л - 7-кратно на двух флаконах (т.е. 14-кратно). При уровне мочевины выше 20 ммоль/л дополнительно проводят плазмодиализ при скорости перфузии 250-400 мл/мин в течение 1,5-2 часов. После плазмосорбции (плазмодиализа) во флакон с плазмой через иглу вводят световод от аппарата для внутривенного ультрафиолетового облучения крови и облучают при волне 2545 нм в течение 20 мин. Больному плазму возвращают на следующем сеансе. Предлагаемый способ применен в клинических условиях.
Примеры выполнения способа.
Больной Б., 34 г., клинический диагноз: Вторичный хронический септический эндокардит. Сочетанный митральный порок. Абсцесс правого желудочка. НК 2А. Операция протезирования митрального клапана и аннулопластики 3-створчатого клапана. В послеоперационном периоде сепсис, передний медиастинит.
В лабораторных анализах: Л 19000 П-6 С80 Л-10 М-4 СОЭ 24/48 мм, билирубин 28 мкм/л, мочевина 10 ммоль/л, общий белок 60 г/л, "средние молекулы" 0,6/0,45 ед. Бак. посев крови: грамположительная палочка, посев из раны: синегнойная палочка. Ввиду неэффективности длительной антибактериальной терапии проведено 3 сеанса криоафереза с дополнительной обработкой плазмы по вышеуказанной методике. Состояние улучшилось после второго сеанса, стойкая нормализация температуры после третьего. Улучшилось заживление раны. Нормализовался лейкоцитоз и формула крови, содержание "средних молекул" снизилось до 0,18/0,13 ед., содержание циркулирующих иммунных комплексов со 130 ед. до 30 ед.
Выписан с выздоровлением.
Больной Г., 38 лет, операция митральной комиссуротомии, пластики фиброзного кольца митрального клапана. В послеоперационном периоде септический шок, полиорганная недостаточность: острая сердечная, печеночная, почечная. Состояние крайней тяжести, фебрильная температура с ознобами, периферические признаки глубокого расстройства микроциркуляции. Цианоз губ, акроцианоз. ЧД - 26 мин, в нижних отделах легких жесткое дыхание. АД - 115/75 мм на фоне постоянной инфузии допмина в дозе 7 мкг/кг/мин, ЧСС - 92 в мин, мерцательная аритмия. В лабораторных анализах: Лейкоцитоз 16000 сдвиг влево, СОЭ 34 мм. Бак. посев крови: грамположительная палочка, билирубин 76,6 мкм/л, мочевина 24 ммоль/л, "средние молекулы" 2,0/1/4 ед. АКТ: признаки ДВС - синдрома с высоким фибриногеном (8,0 г/л) и низкой антитромбиновой активностью (65%).
Учитывая прогрессирующий эндотоксикоз и неэффективность консервативной терапии, проведены два сеанса плазмафереза: первый с замещением донорской плазмой, второй с замещением аутоплазмой, обработанной по предлагаемой методике, включая этап плазмодиализа, ввиду тяжелых пирогенных реакций на донорскую плазму. После обработки содержание в аутоплазме билирубина, мочевины, "средних молекул" в пределах нормы. Бак.посев аутоплазмы стерилен, из криоосадка высевалась грамположительная палочка. После двух сеансов нормализация температуры, гемодинамических показателей, улучшение общего состояния. Увеличился диурез. Разрешение печеночной и почечной недостаточности с нормализацией лабораторных анализов к 8 суткам.
У обоих больных при обработке плазмы при +4oC криопреципитации не было, при -10oC выпал криоосадок весом 50-75 г.
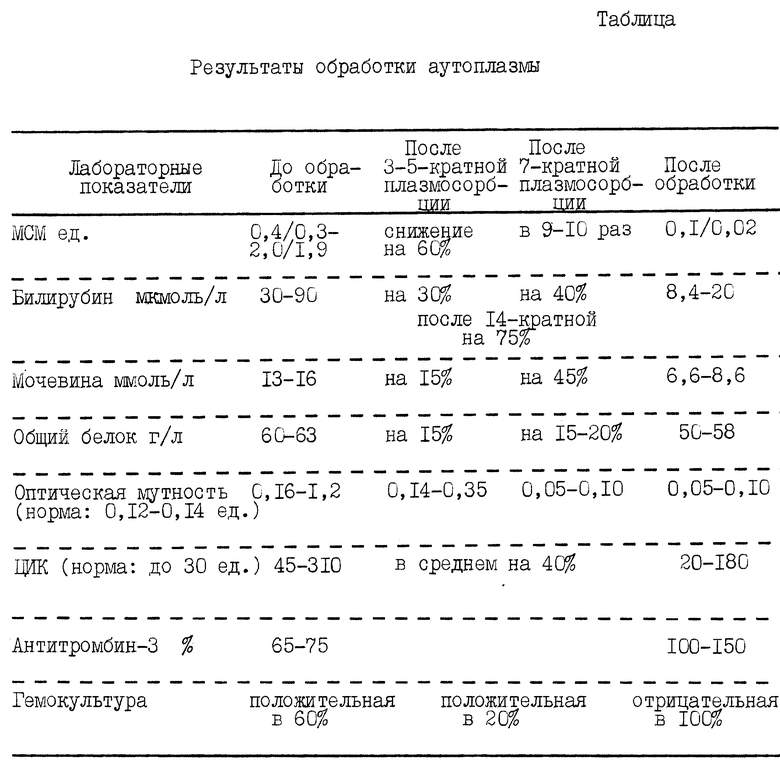
Таким образом, после обработки по предлагаемому способу (см. таблицу) аутоплазма становится прозрачной, нетоксичной по содержанию метаболитов, стерильной. Снижается содержание циркулирующих иммунных комплексов, восстанавливается антитромбиновая активность.
Предлагаемый способ позволяет использовать метод криоафереза у больных со сниженной преципитацией криоглобулинов, высоким содержанием токсических метаболитов (билирубина до 90 мкм/л, мочевины свыше 20 ммоль/л, "средних молекул" до 2,0 ед.), кроме того, ультрафиолетовое облучение дополнительно обеспечивает стерильность плазмы.
Способ значительно повышает степень детоксикации плазмы крови при криоаферезе.
Литература
1. Bruce C., Mc Lead R., Sasseti V. "Blood", 1980, v.55, p.866.
2. С. А. Васильев, В. Г.Савченко, В.М.Городецкий и др. "Изменение концентрации фибронектина в процессе проведения лечебного плазмафереза". "Тер. архив", 1984, N 6, с.35-38.
3. Ав. свидетельство СССР N 157950.
4. С. А. Васильев, Е.Е.Ефремов. "Снижение эффективности холодовой гепариновой преципитации плазменного фибронектина при сепсисе". - "Тер.архив", 1986, N 10, с.117-123.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДЕТОКСИКАЦИИ ОРГАНИЗМА ПРИ РАЗВИТИИ ХИРУРГИЧЕСКОГО ЭНДОТОКСИКОЗА | 1996 |
|
RU2144393C1 |
| СПОСОБ ЭКСТРАКОРПОРАЛЬНОЙ ГЕМОКОРРЕКЦИИ ПРИ ПОСЛЕОПЕРАЦИОННОЙ ПОЛИОРГАННОЙ НЕДОСТАТОЧНОСТИ НА ФОНЕ ИНФЕКЦИОННОГО ЭНДОКАРДИТА ВЫСОКОЙ СТЕПЕНИ АКТИВНОСТИ | 2001 |
|
RU2209091C2 |
| СПОСОБ НЕПРЕРЫВНОГО ПЛАЗМАФЕРЕЗА У ДЕТЕЙ РАННЕГО ВОЗРАСТА | 2001 |
|
RU2208455C2 |
| СПОСОБ ПРОВЕДЕНИЯ ПЛАЗМОСОРБЦИИ | 1999 |
|
RU2162344C1 |
| СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ПЕЧЕНИ | 2002 |
|
RU2217173C2 |
| СПОСОБ ПРЕДУПРЕЖДЕНИЯ ГНОЙНО-СЕПТИЧЕСКИХ ОСЛОЖНЕНИЙ У КАРДИОХИРУРГИЧЕСКИХ БОЛЬНЫХ | 1998 |
|
RU2181606C2 |
| СПОСОБ ПРОФИЛАКТИКИ ПОСЛЕОПЕРАЦИОННЫХ СЕПТИЧЕСКИХ ОСЛОЖНЕНИЙ ПРИ КОРРЕКЦИИ ПРИОБРЕТЕННЫХ ПОРОКОВ СЕРДЦА НА ФОНЕ ПРОГРЕССИРУЮЩЕЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ | 1997 |
|
RU2144363C1 |
| СПОСОБ ПРОФИЛАКТИКИ РЕЦИДИВОВ СЕПТИЧЕСКОГО ЭНДОКАРДИТА ПРИ РЕПРОТЕЗИРОВАНИИ КЛАПАНОВ СЕРДЦА | 1997 |
|
RU2163493C2 |
| Способ лечения атеросклероза | 1991 |
|
SU1805972A3 |
| СПОСОБ ПЛАСТИКИ МИТРАЛЬНО-АОРТАЛЬНОГО КОНТАКТА ПРИ АОРТАЛЬНО-МИТРАЛЬНОМ ПРОТЕЗИРОВАНИИ | 1999 |
|
RU2196526C2 |
Изобретение относится к медицине, а именно к способам детоксикации крови, и может быть использовано при лечении заболеваний, сопровождающихся септической интоксикацией и полиорганной недостаточностью. Способ включает холодовую обработку аутоплазмы при -10oC, 5-7-кратную плазмосорбцию, плазмодиализ и ультрафиолетовое облучение. Технический результат: способ позволяет использовать метод криоафереза у больных со сниженной преципитацией криоглобулинов, повышает степень детоксикации плазмы крови, обеспечивает стерильность плазмы. 1 з.п.ф-лы, 1 табл.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| СПОСОБ ОЧИСТКИ ПЛАЗМЫ КРОВИ | 1992 |
|
RU2014847C1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ детоксикации крови | 1988 |
|
SU1579507A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| US 4613322, 23.09.86 | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| СПОСОБ ВЫБОРА ПЕРВИЧНОЙ СХЕМЫ АНТИБАКТЕРИАЛЬНОЙ ТЕРАПИИ ПРИ ЛЕЧЕНИИ БОЛЬНЫХ С ПЕРФОРАЦИЕЙ ЯЗВЫ ЖЕЛУДКА И ДВЕНАДЦАТИПЕРСТНОЙ КИШКИ | 2013 |
|
RU2552329C2 |
Авторы
Даты
2000-01-20—Публикация
1996-07-01—Подача