Изобретение относится к биотехнологии, а конкретно - к области анализа флуоресцентно-меченых фрагментов ДНК с использованием метода капиллярного электрофореза и может быть широко использовано для различных видов генотипирования, применяемых в криминалистике, при создании геномных баз данных для идентификации личности, при установлении родства и решении вопросов спорного отцовства; для ДНК-анализов в сельском хозяйстве при селекции и паспортизации ценных пород животных, сортов растений и др.; для диагностики онкологических и инфекционных заболеваний и мониторинга протекания заболеваний; для диагностики наследственных заболеваний, а также предрасположенности к ним; для расшифровки генома человека, животных и растений; для поиска и изучения новых генов, ответственных за важные физиологические процессы (рак, старение и др.).
Известен прибор для капиллярного электрофореза, содержащий систему параллельно-ориентированных капилляров со светопроводящими участками, к которым через световоды подводится лазерное излучение, две системы линз, одна из которых фокусирует лазерное излучение на каждый из капилляров, вторая система линз собирает флуоресцентный сигнал с каждого из капилляров в соответствующий световод. Блок модуляции, содержащий специальный диск, с выполненными в нем отверстиями и модулирующий по частоте сигнал с различными электрическими составляющими от каждого капилляра. Фотодетектор, регистрирующий флуоресцентные сигналы с каждого капилляра после их прохождения через светофильтр, отрезающий лазерное излучение. Посредством частотной модуляции флуоресцентного сигнала капилляры дискриминируются по частоте электрического сигнала с фотодетектора (ЕР 0793 098 A1, МПК 6 G 01 N 27/447, G 01 N 21/59, G 01 N 21/64, опубл. 1997 г.).
Несмотря на достаточно высокую чувствительность системы детекции, отсутствие движущихся узлов и элементов, известный прибор характеризуется недостаточной надежностью системы детекции, относительно сложной системой фокусировки на капилляр, отсутствием возможности использования более десяти капилляров. Отсутствует информация и о практическом использовании и коммерциализации изобретения.
Известна система множественной флуоресцентной детекции с использованием капиллярного электрофореза для определения исследуемых веществ в образцах, содержащая по крайней мере два капилляра, расположенных в одной плоскости, часть цилиндрической поверхности которых прозрачна для света, каждый из которых содержит исследуемый образец, заполнен разделяющим полимером и имеет входящий и выходящий концы, помещенные в катодную и анодную ванночки, к которым приложено высокое напряжение, узел облучения каждого образца в каждом капилляре когерентным светом, включающий источник лазерного излучения, которое фокусируется одним из объективов и подводится к торцу каждого капилляра посредством световодов, узел детекции, включающий второй объектив, собирающий флуоресцентный сигнал, который через адаптер регистрируется ПЗС-матрицей (патент США N 5498324, МПК 6 G 01 N 27/26, опубл. 1996 г.). В данном устройстве практически удалось устранить недостатки, присущие устройству, описанному выше, однако конструкция его оптической части предполагает серьезные проблемы с фокусировкой на капилляр. Возможно, это обстоятельство является одной из причин отсутствия информации о коммерциализации изобретения.
Известно другое устройство, предназначенное для разделения и анализа высокомолекулярных биополимеров методом электрофореза, содержащее систему капилляров, концы которых помещены в катодную и анодную ванночки, и к которым приложено высокое напряжение, при этом капилляры в зоне детекции размещены в специальной кювете и выполнены с разрывом, лазер, излучением которого, сфокусированного линзой, облучаются одновременно все капилляры, при этом флуоресцентный сигнал собирается оптической системой, включающей линзу и светофильтр, отрезающий лазерное излучение и через световод подается на регистрирующее устройство, а через аналого-цифровой преобразователь поступает в компьютер для последующей обработки (патент США N 5584982, МПК 6 G 01 N 27/26, G 01 N 27/447, опубл. 1996 г.).
Одна из особенностей данной конструкции - разрыв капилляров в зоне детекции в специальной кювете - позволила исключить достаточно сложную систему сканирования и использовать лазер относительно небольшой мощности для одновременного облучения всех капилляров. Эти особенности конструктивного выполнения устройства способствовали его практической реализации в коммерческих целях.
Наиболее близкой к настоящему изобретению по технической сущности и достигаемому результату при использовании является система для возбуждения и детекции излучения от множества капиллярных каналов, содержащая капилляры, расположенные на поперечно сканирующем столике. Концы капилляров, помещенные в катодную и анодную ванночки, подключены к источнику высокого напряжения. Лазерный источник облучает капилляры в зоне детекции, а оптический сигнал преобразуется оптической системой, включающей объектив, фокусирующий лазерное излучение и собирающий флуоресцентный сигнал, дихроичное зеркало, отражающее лазерное излучение и направляющее его в объектив, а также пропускающее флуоресцентный сигнал, два светофильтра, один из которых отрезает отраженное от капилляра лазерное излучение, а второй - интерференционный светофильтр. Пройдя эту оптическую систему, сигнал регистрируется фотоэлектронным умножителем (ФЭУ). В одном из вариантов реализации устройства, флуоресцентный сигнал может разделяться на четыре эквивалентных пучка, каждый из которых пропускают через соответствующий интерференционный светофильтр и регистрируют ФЭУ. Сигнал с ФЭУ после усиления поступает в компьютер для соответствующей обработки (патент США N 5274240, МПК 6 G 01 N 21/64, опубл. 1993 г.).
Главной особенностью данной конструкции является совмещение узла, фокусирующего лазерное излучение, и узла, собирающего флуоресцентный сигнал, в одном микрообъективе. Это существенно облегчает фокусировку на капилляр и значительно упрощает конструкцию. Однако такое техническое решение имеет серьезный недостаток, связанный с тем, что этот микрообъектив собирает не только полезный сигнал, но и все отраженное лазерное излучение, которое существенно уменьшает соотношение сигнал/шум. Кроме того, большое количество дополнительных фильтров, необходимых для отрезания отраженного лазерного излучения, значительно ослабляет полезный сигнал и уменьшает общую чувствительность установки. Однако, несмотря на эти недостатки, данная конструкция получила коммерческую реализацию.
В основу данного изобретения положена задача создания универсального устройства, позволяющего проводить все виды генетических анализов, обеспечивая комплексное решение задач анализа генетического материала при проведении генно-инженерных работ, молекулярно-биологических, генетических или микробиологических исследований.
Технический результат при использовании данного изобретения заключается в повышении чувствительности анализатора за счет ориентации лазерного излучения под углом α к оси микрообъектива, а также за счет использования предложенной оптической схемы для обработки флуоресцентного сигнала, включающей дифракционную решетку (вместо системы интерференционных светофильтров в прототипе). Это позволило на порядок сократить потери полезного сигнала, значительно увеличить соотношение сигнал/шум и обеспечить детекцию меньшего количества ДНК в капилляре, что существенно снижает требования к пробоподготовке.
Поставленная задача, с достижением указанного выше технического результата решается тем, что в известном многоканальном капиллярном генетическом анализаторе с использованием электрофореза, содержащем заполненные разделяющим полимером и расположенные на сканирующем столике капилляры, концы которых помещены в катодную и анодную ванночки и подключены к источнику высокого напряжения, устройство когерентного излучения, включающее лазер и узел фокусировки лазерного излучения, оптическую систему, включающую микрообъектив и блок спектрального анализа флуоресцентного сигнала, блок регистрации флуоресцентного сигнала, соединенный с компьютером, устройство когерентного излучения ориентирует лазерное излучение на капилляр под углом 10o - 80o к оси микрообъектива, оптическая система содержит установленные последовательно по ходу оптического луча микрообъектив, узел визуального контроля фокусировки на капилляр и блок спектрального анализа флуоресцентного сигнала, включающий дифракционную решетку, разлагающую флуоресцентный сигнал в спектр, и фокусирующие линзы, установленные по ходу соответствующих спектральных полос, блок регистрации флуоресцентного сигнала содержит фотоприемники, расположенные в фокусах соответствующих линз блока спектрального анализа, при этом выход каждого фотоприемника через АЦП соединен со входом компьютера, а дополнительный фотоприемник для регистрации отраженного лазерного излучения размещен в спектральной полосе, соответствующей лазерному излучению и его выход соединен с одним из входов АЦП;
- а также тем, что в нем устройство когерентного излучения содержит по крайней мере второй лазер, а узел фокусировки лазерного излучения включает расположенные последовательно по ходу лазерного излучения одного из лазеров смеситель, зеркало, фокусирующую линзу и второе зеркало, установленное в оптическом канале второго лазера, ориентирующее излучение на смеситель, который может быть выполнен в виде дихроичного зеркала;
- а также тем, что узел контроля фокусировки на капилляр содержит установленные последовательно по ходу отраженного флуоресцентного сигнала отражатель, линзу, экран и окуляр, причем отражатель установлен подвижно с возможностью его вывода из оптического канала с флуоресцентным сигналом по окончании процесса фокусировки, отражатель при этом может быть выполнен в виде призмы полного внутреннего отражения, а экран - в виде матового стекла;
- а также тем, что блок регистрации флуоресцентного сигнала может содержать интерференционные светофильтры, расположенные перед соответствующими фотоприемниками, в качестве которых могут быть использованы фотоэлектронный умножитель, или фотодиод, или ПЗС-линейка, или ПЗС-матрица.
Изобретение иллюстрируется графическим материалом, на котором представлено:
на фиг. 1 - принципиальная схема предлагаемого анализатора;
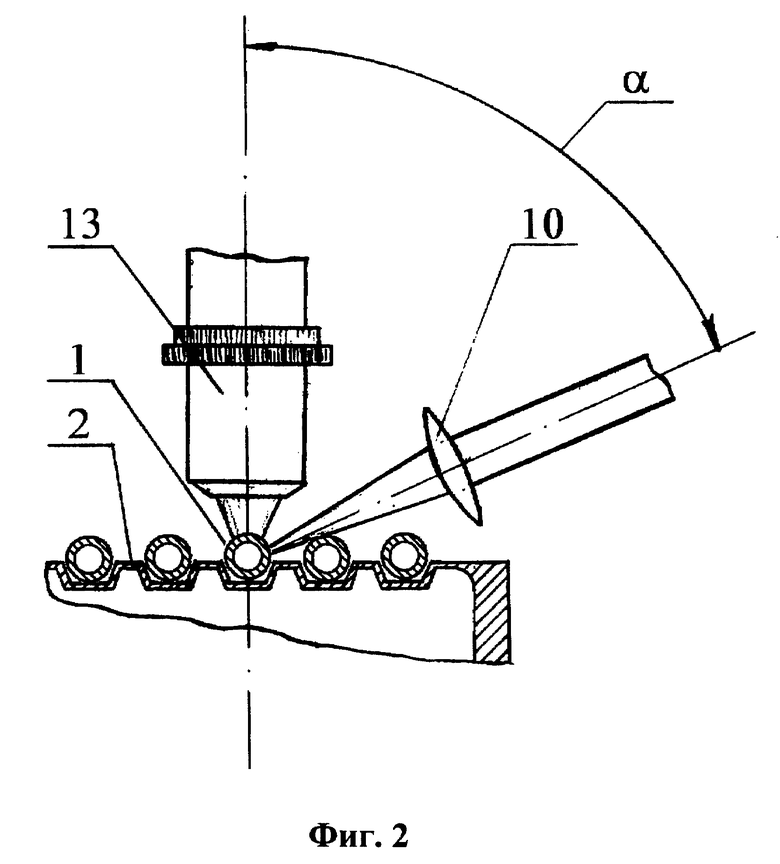
на фиг. 2 - увеличенный узел фокусировки лазерного излучения и сбора флуоресцентного сигнала;
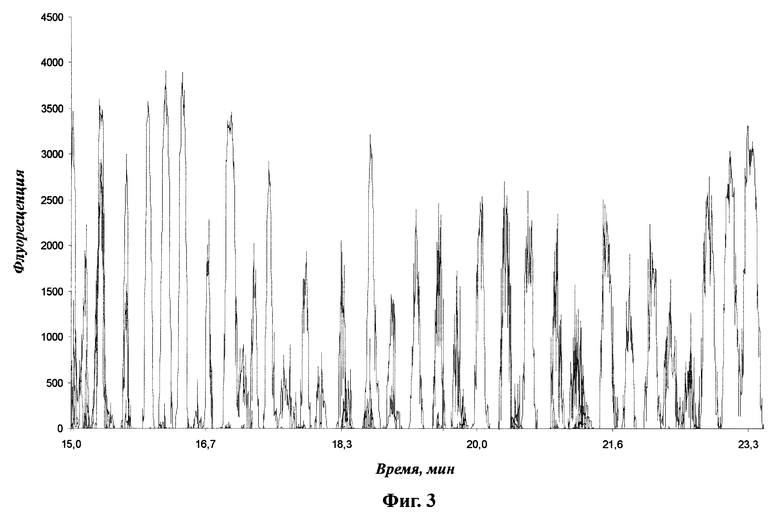
на фиг. 3 - результаты электрофоретического разделения флуоресцентно-меченых сиквенсных фрагментов ДНК, полученных методом Сэнгера;
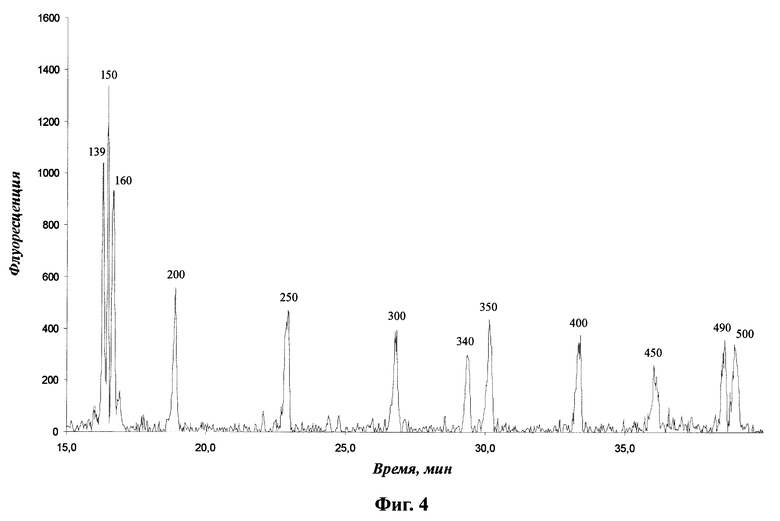
на фиг. 4 - результаты электрофоретического разделения флуоресцентно-меченых ДНК-маркеров TAMRA-500 фирмы Perkin-Elmer Corp., США.
Настоящее изобретение представляет собой систему на основе капиллярного электрофореза, в которой лазер последовательно возбуждает исследуемые образцы, находящиеся внутри капилляров, а система детекции последовательно регистрирует флуоресцентные сигналы с каждого капилляра. Данная система применима к большому количеству капилляров, в частности, к стандартному формату (96 или 384 капилляра), используемому в молекулярно-биологической практике.
Обычно при капиллярном электрофорезе капилляры заполняют разделяющим полимером с электропроводящим буферным раствором, а концы капилляров погружают в ванночки с электропроводящим буферным раствором. К концам капилляров приложено высокое напряжение (обычно порядка 1 - 15 кВ). Образец, содержащий один или более флуоресцентно-меченых компонентов, наносят в капилляр, прикладывая к концам капилляра, один из которых погружен в исследуемый образец, высокое напряжение. Образец может наноситься в капилляр под давлением. Один и тот же образец может быть нанесен в несколько капилляров, также как различные образцы могут быть нанесены в разные капилляры. Обычно концы капилляров, в которые наносятся образцы, особым образом упорядочены и зафиксированы в специальном устройстве, и концы этих капилляров при нанесении образцов погружают в пробирки с образцами. После того, как образцы уже нанесены в капилляры, эти концы капилляров вынимают из пробирок с образцами и погружают в ванночку с буферным раствором. После приложения высокого напряжения образцы мигрируют к другим концам капилляров. В процессе миграции вдоль капилляров происходит электрофоретическое разделение образцов. После разделения компоненты образцов регистрируются детектором. Детекция может происходит в момент, когда вещества еще находятся в капиллярах, или на выходе из капилляров.
Длина капилляров выбирается такой, чтобы достичь необходимой эффективности разделения компонентов образца. Обычно, чем длиннее капилляр, тем большее время потребуется для миграции образца через него, но при этом компоненты образца будут разделены друг от друга на большие расстояния. Однако, удлинение "электрофоретического пути" приводит к уширению мигрирующих зон разделяемых компонентов, что затрудняет анализ данных электрофоретического разделения. Обычно, в капиллярном электрофорезе используют капилляры от 10 см до 5 м в длину (чаще всего, от 20 до 200 см). Внутренний диаметр капилляра может быть от 5 до 300 мкм (чаще всего используют капилляры с внутренним диаметром от 20 до 100 мкм).
Капилляры изготавливаются из прочного и долговечного материала, чтобы они не разрушались при многократном их использовании в капиллярном электрофорезе. Обычно они изготавливаются из неорганических материалов, таких как кварц, стекло или из органических материалов, таких как политетрафторэтилен, полифторэтилен, полиамид, поливинилхлорид, поливинилфторид, полистирол, полиэтилен.
Когда возбуждение флуоресценции и/или детекция осуществляется через стенку капилляра, важно, чтобы капилляр был сделан из прозрачного для света материала. Прозрачный материал, из которого изготовлены капилляры не должен флуоресцировать при облучении капилляров светом, использующимся для возбуждения исследуемых образцов. Возможна и другая ситуация, когда капилляр не прозрачен для света или может флуоресцировать, но в нем есть часть, которая прозрачная и не флуоресцирует сама по себе. Например, внешнюю стенку кварцевых капилляров обычно покрывают полиимидным покрытием, чтобы капилляры не были ломкими. Такое покрытие может излучать флуоресценцию в широком диапазоне длин волн до 600 нм. И, если использовать схему возбуждения через стенку капилляра, в котором не удалено такое покрытие, то флуоресценция покрытия может накладываться на слабый сигнал от образца. Поэтому обычно полиимидное покрытие удаляют с части капилляра, в которой будет проводиться детекция, каким-нибудь простым способом, например, обработкой серной кислотой или прожиганием пламенем. В капиллярах с внутренним диаметром 0,1 мм или менее обычно формируют прозрачную зону шириной от 0,01 - 1,0 мм.
В электрофорезе буферный раствор для разделения представляет собой электролит, состоящий из катионов и анионов. Обычно этот электролит содержит ионные компоненты в концентрации 0,005 - 10 моль/литр (чаще всего 0,01 - 0,5 моль/литр). В электрофорезных системах электролит представляет собой смесь воды, органических растворителей и солей. В качестве таких компонентов могут быть неорганические соли, такие как фосфаты, бикарбонаты и бораты; органические кислоты, такие как уксусная, пропионовая, лимонная, хлоруксусная и им подобные кислоты и их соответствующие соли; алкиламины, такие как метиламины; спирты, такие как этанол, метанол; многоатомные спирты, такие как алкандиолы; азотсодержащие растворители, такие как ацетонитрил, пиридин и им подобные; кетоны, такие как ацетон и метилэтилкетон; алкиламиды, такие как формамид, N-метил- и N-этилформамид и им подобные.
Электрофоретические разделения могут проводиться при наложении высокого напряжения довольно широкого диапазона 500 - 30000 В (чаще всего 1000 - 20000 В).
В качестве разделяющего полимера, которым заполнены капилляры, могут использоваться как растворы линейных полимеров, например линейные или разветвленные производные полиакриламида, растворы различных производных целлюлоз, растворы полиэтиленоксидов и полиэтиленгликолей с различной молекулярной массой и др.
Многоканальный капиллярный генетический анализатор предназначен для разделения, детекции и анализа группы флуоресцентно-меченых макромолекул, представляющих генетический материал живых организмов. Это такие вещества, как ДНК (дезоксирибонуклеиновая кислота), РНК (рибонуклеиновая кислота), их фрагменты и их комбинации, хромосомы, гены и их комбинации. Данный генетический анализатор применим для ДНК-диагностики, а именно для секвенирования ДНК, анализа фрагментов ДНК и ДНК-фингерпринтинга.
Многоканальный капиллярный генетический анализатор включает следующие функционально независимые узлы: капилляры, закрепленные на сканирующем столике, устройство когерентного излучения, оптическую систему, блок спектрального анализа и блок регистрации флуоресцентного сигнала, компьютер.
На фиг. 1 схематически показано устройство анализатора.
Капилляры 1, наполненные разделяющим полимером, размещены в специальном узле крепления 2 на поперечно сканирующем столике 3. Капилляры имеют внутренний диаметр 100 мкм и внешний 200 мкм. К концам капилляров, помещенных в катодную 4 и анодную 5 ванночки, заполненные буферным раствором, приложено высокое напряжение (до 10 кВ). В зоне детекции капилляры под углом одновременно облучаются двумя лазерами: 532 нм 6 и 488 нм 7. Лазеры 6, 7, зеркала 8, 9, линза 10 и дихроичное зеркало 11 образуют устройство когерентного излучения 12, в котором зеркало 8 служит для направления излучения второго лазера на смеситель, выполненный в виде дихроичного зеркала 11, зеркало 9 служит для направления смешанного лазерного излучения на капилляры, а линза 10 фокусирует это излучение внутри капилляра. Флуоресцентный сигнал собирается микрообъективом 13 и разлагается в спектр дифракционной решеткой 14 в блоке спектрального анализа 15. Четыре спектральные линии после прохождения через соответствующие интерференционные светофильтры 16 фокусируются линзами 17 на соответствующие фотоэлектронные умножители (ФЭУ) 18 блока регистрации флуоресцентного сигнала 19. Сигналы с каждого ФЭУ через аналого-цифровой преобразователь 20 поступают в компьютер 21 для окончательной обработки. Присвоение спектральной характеристики конкретному капилляру происходит по сигналу с дополнительного фотоприемника, в качестве которого может использоваться фотодиод 22, т. к. сигнал на фотодиоде 22 возникает только в случае наличия отраженного от капилляра лазерного излучения, что, в свою очередь, происходит лишь в момент попадания капилляра в фокус объектива 13. Фотодиод 22 расположен в спектральной полосе, соответствующей лазеру 532 нм. Для проверки фокусировки объектива 13 на капилляр предусмотрен узел визуального контроля фокусировки 23, состоящий из последовательно установленных подвижной призмы 24, линзы 25, матового стекла 26 и окуляра (на фиг. 1 не показан). В момент проверки фокусировки призма 24 находится в положении, показанном на фиг. 1; после проверки призма 24 выводится из оптического канала в положение, показанное на фиг. 1 пунктиром.
Фотодиод 22 расположен в спектральной полосе, соответствующей длине волны лазерного излучения, и предназначен для улавливания отраженного от внешней поверхности капилляра 1 лазерного луча. В тот момент, когда капилляр попадает в зону детекции, т.е. в фокус микрообъектива 13, лазерный луч отражается от поверхности капилляра 1, и на фотодиоде 22 возникает соответствующий электрический сигнал. Этот сигнал служит командой для накопления данных с этого капилляра и записи в соответствующий файл. Такое использование фотодиода 22 позволяет: сократить объем конечного файла данных и не записывать незначащую информацию, не привязываться к абсолютной координате капилляра, т. к. положение капилляра в фокусе микрообъектива 13 определяется сигналом с фотодиода 22 и запись в файл происходит только в момент облучения капилляра. Это обстоятельство, в свою очередь, позволяет существенно снизить требования к сканирующему столику, т.к. точность позиционирования не имеет принципиального значения, и это удешевляет конструкцию. Кроме того, такое решение позволяет также упростить алгоритм накопления данных с капилляров, т.к. запись в соответствующий файл происходит строго по сигналу с фотодиода 22.
Одним из существенных отличий, характеризующих предлагаемое изобретение, является облучение капилляров лазером под углом α к оси микрообъектива 13, который может находиться в пределах 10o - 80o (фиг. 2).
Нижний предел угла α обусловлен конструкцией и фокусным расстоянием микрообъектива. Однако слишком маленький угол значительно увеличивает количество рассеянного и отраженного лазерного излучения, попадающего в микрообъектив, и тем самым существенно уменьшает соотношение сигнал/шум.
Верхний предел ограничен диаметром капилляров и расстоянием между ними. Экспериментально, с учетом перечисленных условий, определен диапазон угла α, составляющий 10o - 80o. Для решения большинства задач оптимальный диапазон угла α составляет 30o - 50o от оси микрообъектива.
Одним из отличий настоящего изобретения является использование в конструкции устройства когерентного излучения 12 двух лазеров 6, 7. В соответствии с изобретением в анализаторе в качестве флуоресцентных меток молекул ДНК используются коммерчески доступные стандартные красители: FAM λпоглощения= 496 нм,  516 нм), JOE λпоглощения= 520 нм,
516 нм), JOE λпоглощения= 520 нм,  550 нм), TAMRA ( λпоглощения= 550 нм,
550 нм), TAMRA ( λпоглощения= 550 нм,  580 нм), ROX λпоглощения= 575 нм,
580 нм), ROX λпоглощения= 575 нм,  605 нм). Использование четырех флуоресцентных красок обусловлено одним из применений данного изобретения - определением нуклеотидной последовательности ДНК, при котором необходимо определить последовательность четырех видов мономеров, составляющих молекулу ДНК. Для этой цели используется четырехкрасочный подход, при котором каждому типу мономеров соответствует определенный флуоресцентный краситель. По последовательности флуоресцентных сигналов в процессе электрофоретического разделения фрагментов ДНК можно определить нуклеотидную последовательность ДНК. Поскольку спектры поглощения всех красок довольно широкие, целесообразно возбуждать флуоресценцию нескольких красок одним лазером. В данной установке для возбуждения красок JOE, TAMRA, ROX используется твердотельный YAG - Nd3+ лазер 532 нм. Для возбуждения краски FAM используется аргоновый лазер с одной линией излучения 488 нм. Для возбуждения всех красок возможно использовать только один аргоновый лазер с двумя линиями излучения 488 нм и 514,5 нм. Однако, в этом случае недостаточно возбуждается краска ROX, и требуются большие мощности аргонового лазера, а это вызывает фотовыцветание других красок. Поэтому для получения более равномерных спектров эмиссии всех красителей, а также для получения более сильных флуоресцентных сигналов предпочтительнее использовать два лазера меньших мощностей - до 10 мВт.
605 нм). Использование четырех флуоресцентных красок обусловлено одним из применений данного изобретения - определением нуклеотидной последовательности ДНК, при котором необходимо определить последовательность четырех видов мономеров, составляющих молекулу ДНК. Для этой цели используется четырехкрасочный подход, при котором каждому типу мономеров соответствует определенный флуоресцентный краситель. По последовательности флуоресцентных сигналов в процессе электрофоретического разделения фрагментов ДНК можно определить нуклеотидную последовательность ДНК. Поскольку спектры поглощения всех красок довольно широкие, целесообразно возбуждать флуоресценцию нескольких красок одним лазером. В данной установке для возбуждения красок JOE, TAMRA, ROX используется твердотельный YAG - Nd3+ лазер 532 нм. Для возбуждения краски FAM используется аргоновый лазер с одной линией излучения 488 нм. Для возбуждения всех красок возможно использовать только один аргоновый лазер с двумя линиями излучения 488 нм и 514,5 нм. Однако, в этом случае недостаточно возбуждается краска ROX, и требуются большие мощности аргонового лазера, а это вызывает фотовыцветание других красок. Поэтому для получения более равномерных спектров эмиссии всех красителей, а также для получения более сильных флуоресцентных сигналов предпочтительнее использовать два лазера меньших мощностей - до 10 мВт.
Многоканальный капиллярный генетический анализатор работает следующим образом.
В режиме определения нуклеотидной последовательности ДНК используются капилляры с эффективной длиной (т.е. длиной до зоны детекции) 50 см, внутренним диаметром 100 мкм и внешним диаметром 200 мкм. Капилляры промывают 1 мл H2O, затем в течение 20 мин 3 мл 1 н. раствора HCl. После промывки 5 мл H2O внутренняя поверхность капилляров в течение 20 мин обрабатывается 3-(Триметоксисилил)пропил метакрилатом (2%-ный раствор в C2H5OH), и затем высушивается воздухом в течение 30 - 40 мин. Разделяющий полимер, содержащий 6%-ный раствор акриламида, 1-х ТВЕ-буфер (89 мМ Трис, 89 мМ H3BO3, 2 мМ ЭДТА) и 8 М раствор мочевины, фильтруют через 0,22 мкм фильтр и дегазируют под вакуумом в течение 15 мин. После дегазирования к этому раствору добавляют 0,03% (об.) ТЕМЕД и 0,03% персульфата аммония, и сразу после этого капилляры заполняют получившейся реакционной смесью, чтобы процесс полимеризации происходил внутри капилляра.
Подготовку проб ДНК проводят с использованием набора реагентов ABI PRISMR ABI PRISM® Dye Primer Cycle Sequencing Kit фирмы Perkin-Elmer Corp., США по протоколам, рекомендуемым фирмой-производителем.
Пробы наносят электрокинетическим способом, посредством приложения напряжения +5 кВ в течение 20 с.
Электрофорез проводят в течение 1,5 ч при 150 В/см и температуре +55oC.
Данные электрофоретического разделения приведены на фиг. 3.
В режиме разделения фрагментов ДНК с помощью капиллярного электрофореза используются капилляры с эффективной длиной (т.е. длиной до зоны детекции) 30 см, внутренним диаметром 100 мкм и внешним диаметром 200 мкм. Капилляры промывают 1 мл H2O, затем в течение 20 мин 3 мл 1 н. раствора HCl. После промывки 5 мл H2O внутреннюю поверхность капилляров в течение 20 мин обрабатывают 3- (Триметоксисилил)пропил метакрилатом (2%-ный раствор в C2H5OH), и затем высушивают воздухом в течение 30-40 мин. Разделяющий полимер, содержащий 2%-ный раствор гидроксипропилметилцеллюлозы (HPMC), 1-х ТВЕ-буфер (89 мМ Трис, 89 мМ H3BO3, 2 мМ ЭДТА) и 8 М раствор мочевины, отфильтровывают через 0,22 мкм фильтр и дегазируют под вакуумом в течение 15 мин. После дегазирования капилляры заполняют получившимся раствором полимера.
В качестве контрольного образца использовали набор ДНК-маркеров TAMRA-500 фирмы Perkin-Elmer Corp., США.
Пробы наносят электрокинетическим способом, посредством приложения напряжения +3 кВ в течение 15 с.
Электрофорез проводят в течение 40 мин при 600 В/см и температуре +55oC.
Данные электрофоретического разделения ДНК-маркеров TAMRA-500 фирмы Perkin-Elmer Corp. (США) приведены на фиг. 4. Над каждым пиком показаны длины соответствующих фрагментов ДНК в нуклеотидных парах.
Таким образом, многоканальный капиллярный генетический анализатор, в соответствии с настоящим изобретением, позволяет проводить все необходимые виды анализов генетического материала:
- определять нуклеотидную последовательность ДНК;
- разделять флуоресцентно-меченые фрагменты ДНК;
- проводить количественные анализы генетического материала,
т. е. комплексно решать задачи при проведении генно-инженерных работ, молекулярно-биологических, генетических и микробиологических исследований.
Изобретение относится к биотехнологии. Анализатор содержит капилляры, размещенные на сканирующем столике, устройство когерентного излучения, узел фокусировки лазерного излучения и дополнительный фотоприемник. Узел фокусировки ориентирует излучение на капилляры под углом 10 - 80o к оси микрообъектива. Технический результат - повышение чувствительности. 9 з.п.ф-лы, 4 ил.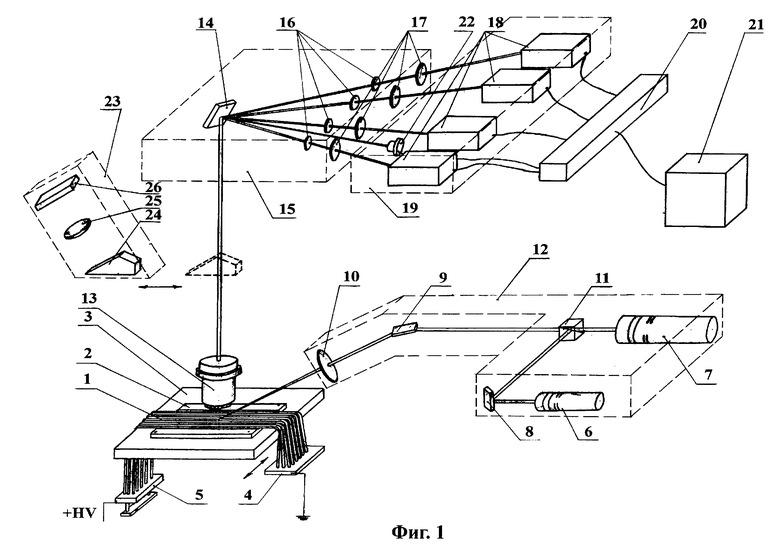
| US 5274240 A, 28.12.93 | |||
| Устройство для анализа биологических растворов и суспензий | 1990 |
|
SU1777056A1 |
| Многоканальный оптический спектрометр | 1990 |
|
SU1775621A1 |
| US 5498324 A, 12.03.96 | |||
| US 5584982 A, 17.12.96 | |||
| EP 0793098 A1, 03.09.97. | |||
Авторы
Даты
2000-01-27—Публикация
1999-07-13—Подача