Настоящее изобретение относится к области аналитического приборостроения, а конкретно - к области генетического анализа с использованием метода капиллярного электрофореза.
Многоканальный капиллярный генетический анализатор предназначен для установления первичной структуры молекул ДНК, выделенных из биологических образцов (в частности, из крови и ткани пациентов), с целью обеспечения потребностей медицины и медико-биологических научных исследований, а также для санитарного, экологического, медико-биологического и криминалистического контроля.
Основной методикой для установления первичной структуры молекул ДНК является секвенирование, в результате применения которой определяются нуклеотидные последовательности.
При секвенировании в составе роботизированного комплекса используются специализированные устройства: устройство подготовки пробы и генетический анализатор.
В устройстве подготовки пробы с помощью набора реагентов получают образец нуклеиновых кислот. Затем с помощью реакции амплификации получают смесь фрагментов ДНК разной длины с шагом 1 нуклеотид. На конец каждого фрагмента при подготовке пробы помещаются два флуоресцентных красителя (донор и акцептор), обеспечивающих перенос энергии при возбуждении от одного лазера.
В генетическом анализаторе разделение фрагментов ДНК выполняется под действием электрического поля в капилляре, заполненном гелем. На выходе четырех цветовых каналов флуоресцентного детектора регистрируются сигналы в виде четырех последовательностей пиков, соответствующих сочетаниям нуклеотидов и флуоресцентных красителей на конце каждого анализируемого фрагмента ДНК. В результате обработки сигналов пикам в каждом цветовом канале присваиваются соответствующие буквенные обозначения А, С, G и Т. Расположения буквенных обозначений нуклеотидов в анализируемой последовательности должно соответствовать увеличению длины фрагментов.
В результате разделения фрагментов ДНК наблюдается последовательность пиков, время выхода которых зависит от длины фрагментов с шагом 1 нуклеотид. Различие молекулярных масс, размеров и пространственной конфигурации соседних нуклеотидов и их флуоресцентных меток (красителей) вызывает изменение электрофоретической подвижности соседних фрагментов, при этом на реальных графиках флуоресценции наблюдается неравномерное распределение соседних пиков. Частичное или полное наложение соседних пиков является основной причиной ошибок при определении реальной нуклеотидной последовательности. Поэтому необходимо обеспечить либо постоянную электрофоретическую подвижность фрагментов при подготовке пробы, либо выравнивание интервалов между соседними пиками при обработке сигналов четырех цветовых каналов флуоресцентного детектора.
Согласно известному изобретению «UV excitable fluorescent energy transfer dyes» (Флуоресцентные красители с передачей энергии, патент США № US 8604186 В2, 2013 г.) при подготовке пробы краситель-донор может быть соединен с красителем-акцептором с использованием различных вставок таким образом, что краситель-акцептор поглощает по существу всю энергию красителя-донора. Однако постоянство электрофоретической подвижности фрагментов ДНК этим патентом не обеспечивается.
Известен патент «Probes labelled with energy transfer coupled dyes» (Пробы, помеченные связанными красителями с передачей энергии, патент США № US 5688648, 1997 г.). Разделение молекул нуклеиновых кислот выполняется с помощью разных наборов флуоресцентных красителей. Разные наборы могут быть модифицированы путем изменения расстояния между донором и акцептором, чтобы обеспечить максимальный перенос энергии. Однако, поскольку 4 разных нуклеотида в соединении с разными красителями сильно отличаются между собой по пространственной конфигурации, то одновременное обеспечение близких характеристик их электрофоретической подвижности весьма затруднительно.
Согласно известному изобретению «Atropisomers of asymmetric xanthene fluorescent dyes and methods of DNA sequencing and fragment analysis» (Атропоизомеры асимметричных ксантеновых флуоресцентных красителей и методы секвенирования ДНК и фрагментных анализов, патент ЕПВ № WO 2002036832 А2, МПК C12Q 1/68, C07D 405/12, C07K 14/00, С07Н 21/00, C07D 311/82, С07Н 19/20, С07Н 19/10, C12N 15/09, 2002 г.), способ анализа фрагментов ДНК включает в себя процессы разделения меченых фрагментов и обнаружения разделенных меченых фрагментов. Электрофорез является процессом разделения с использованием зависимости от размера фрагментов, а меченые красителями с передачей энергии фрагменты ДНК обнаруживаются по их флуоресценции. Подготовка пробы и обработка результатов анализа этим патентом не обеспечиваются.
Ближайшим из известных изобретений по технической сущности и назначению является патент «Многоканальный капиллярный генетический анализатор» (патент РФ №2145078, МПК G01N 21/64, G01N 27/447, 2000 г.). Этот анализатор предназначен для разделения, детекции и анализа группы флуоресцентно-меченых макромолекул, представляющих генетический материал живых организмов.
Многоканальный капиллярный генетический анализатор включает следующие функциональные узлы: капилляры, устройство когерентного излучения, оптическую систему, блок спектрального анализа, блок регистрации флуоресцентного сигнала и компьютер.
Капилляры, наполненные разделяющим полимером, размещены на поперечно сканирующем столике. К концам капилляров, помещенных в катодную и анодную ванночки, заполненные буферным раствором, приложено высокое напряжение. В зоне детекции капилляры под углом одновременно облучаются двумя лазерами, входящими в состав устройства когерентного излучения с помощью оптической системы, фокусирующий лазерное излучение и собирающий флуоресцентный сигнал. Флуоресцентный сигнал разлагается в спектр дифракционной решеткой в блоке спектрального анализа. Четыре спектральные линии после прохождения через соответствующие интерференционные светофильтры фокусируются линзами на соответствующие фотоэлектронные умножители (ФЭУ) блока регистрации флуоресцентного сигнала. Сигналы от каждого ФЭУ после аналого-цифрового преобразования поступают в компьютер.
Этот многоканальный капиллярный генетический анализатор позволяет проводить анализы генетического материала, в том числе определять нуклеотидную последовательность ДНК.
Недостатком этого генетического анализатора можно считать значительные ошибки при определении нуклеотидной последовательности, возникающие при отсутствии технических решений для выравнивания и определения погрешностей нуклеотидных последовательностей, а также отсутствие базы данных, которая может упростить выполнение множества однотипных анализов. В этом генетическом анализаторе не учитываются особенности выполнения операций подготовки проб при работе на роботизированном комплексе.
Целью предлагаемого изобретения является уменьшение ошибок при определении нуклеотидной последовательности путем выравнивания этой последовательности в автоматическом и ручном режиме, вычисления погрешностей определения параметров каждого нуклеотида в последовательности, формирования, пополнения и многократного использования базы данных, которая содержит параметры выравнивания нуклеотидной последовательности, признаки подготовки пробы и параметры генетического анализа и используется для успешного выполнение множества однотипных анализов. Целью предлагаемого изобретения также является обеспечение непрерывности выполнения операций подготовки и анализа пробы при работе на роботизированном комплексе.
Указанная цель достигается за счет того, что многоканальный капиллярный генетический анализатор, содержащий заполненные разделяющим полимером капилляры, к концам которых приложено высокое напряжение, устройство когерентного излучения, оптическую систему, блок спектрального анализа, блок регистрации флуоресцентного сигнала и компьютер, снабжен базой данных, блоком оптимизации, блоком выравнивания и блоком определения погрешностей, при этом вход базы данных связан с выходом блока регистрации флуоресцентного сигнала, база данных соединена двухсторонней связью с блоком оптимизации, блоком выравнивания и блоком определения погрешностей, а выходы базы данных соединены с входами компьютера.
С выхода блока регистрации флуоресцентного сигнала на вход базы данных передаются сигналы четырех последовательностей пиков, соответствующие сочетаниям нуклеотидов и флуоресцентных красителей на конце каждого анализируемого фрагмента ДНК, переданные сигналы сохраняются в базе данных.
С выхода базы данных на вход блока оптимизации передаются сигналы четырех последовательностей пиков, а с выхода блока оптимизации на вход базы передаются параметры выравнивания.
С выхода базы данных на вход блока выравнивания передаются сигналы четырех последовательностей пиков и параметры выравнивания, а с выхода блока выравнивания на вход базы передаются сигналы выровненной последовательности пиков, при этом каждый пик может быть аппроксимирован известной математической функцией, например, функцией Гаусса.
С выхода базы данных на вход блока определения погрешностей передаются сигналы выровненной последовательности пиков, а с выхода блока выравнивания на вход базы передаются буквенные обозначения и значения погрешностей определения параметров каждого пика в последовательности.
Выходы базы данных соединены с входами компьютера, при этом на экране компьютера одновременно индицируются полученные после выравнивания или аппроксимированные сигналы в виде четырех совмещенных по времени графических последовательностей пиков, буквенные обозначения и значения погрешностей определения параметров каждого пика.
База данных, блок оптимизации, блок выравнивания и блок определения погрешностей или некоторые из них могут быть выполнены в виде интегральных схем. Роботизированный комплекс для молекулярно-генетических исследований содержит устройство подготовки пробы, при этом выход устройства подготовки пробы соединен с входом генетического анализатора, а выход блока программного обеспечения роботизированного комплекса - с входом базы данных для передачи признаков наборов флуоресцентных красителей и параметров генетического анализа.
Роботизированный комплекс имеет механическое устройство и устройство управления, обеспечивающие непрерывность выполнения операций подготовки и анализа пробы.
Настоящее изобретение поясняется чертежами, на которых представлено:
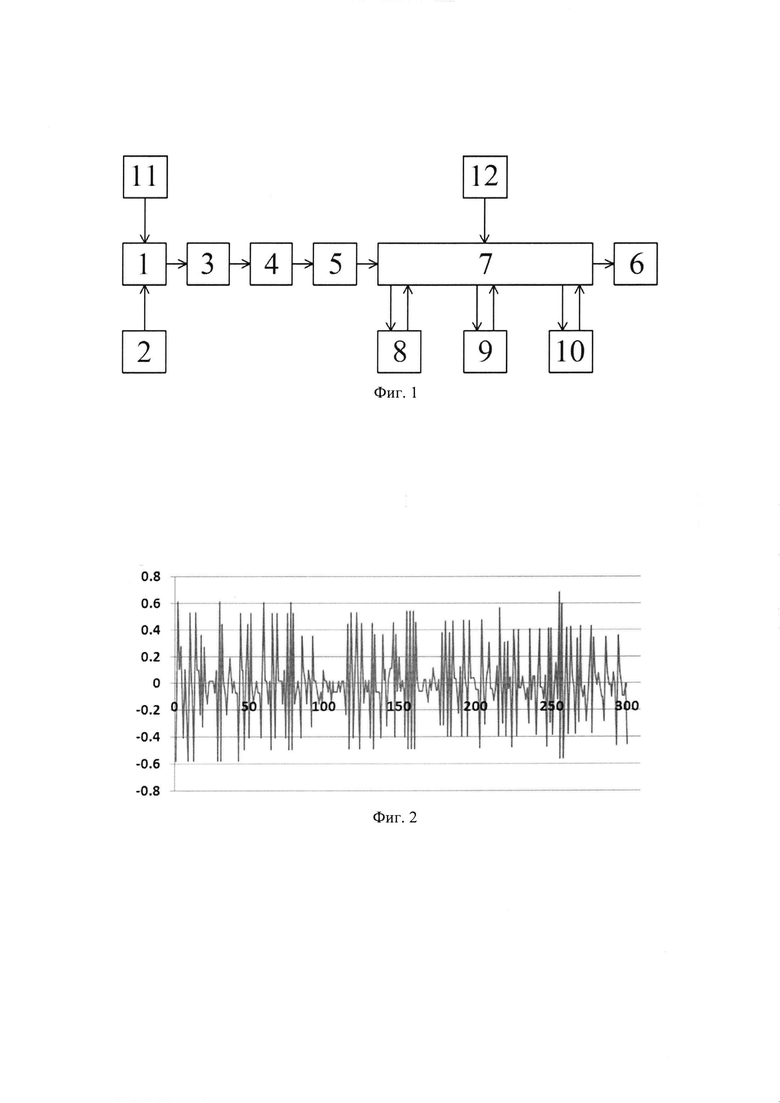
на фиг. 1 - блок-схема, отражающая функциональный состав и соединения блоков предлагаемого многоканального капиллярного генетического анализатора;
на фиг. 2 - график относительной погрешности определения временных интервалов анализируемой последовательности пиков (вертикальная ось) в зависимости от номера пика (горизонтальная ось). Для наглядности точки графика соединены прямыми линиями;
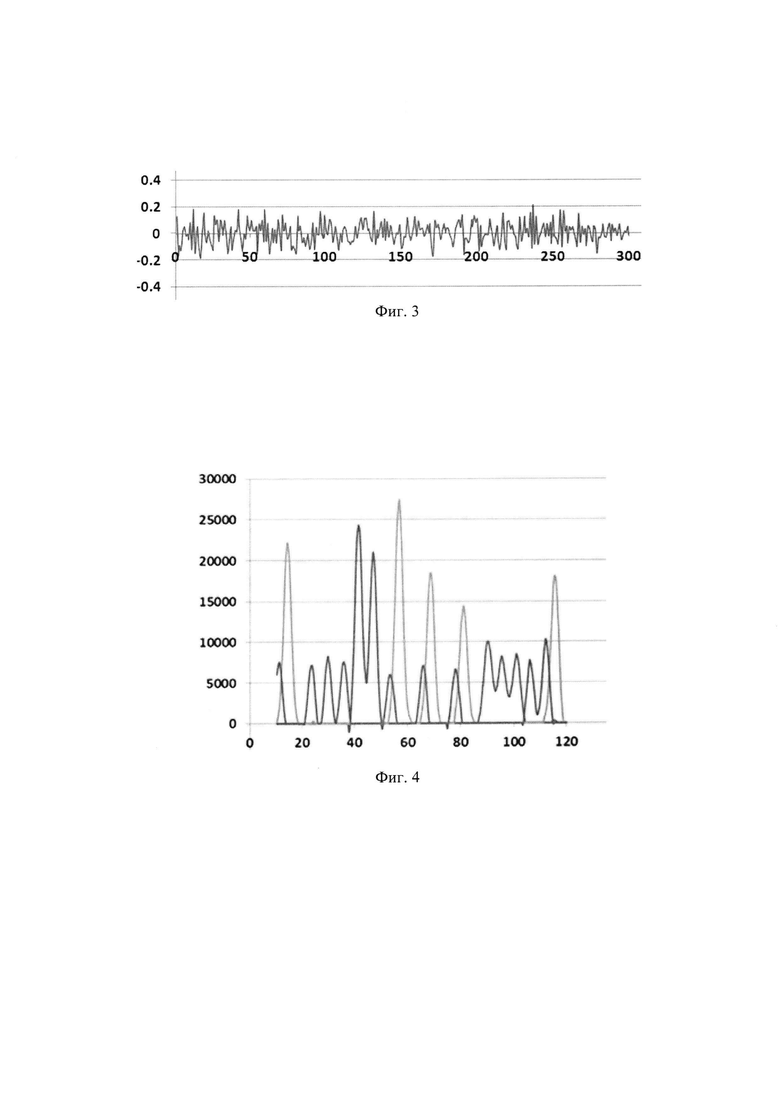
на фиг. 3 - график относительной погрешности определения временных интервалов выровненной последовательности пиков (вертикальная ось) в зависимости от номера пика (горизонтальная ось);
на фиг. 4 - фрагмент анализируемой последовательности пиков. Вертикальная ось - интенсивность флуоресценции в относительных единицах (о. е.), горизонтальная ось - время в секундах;
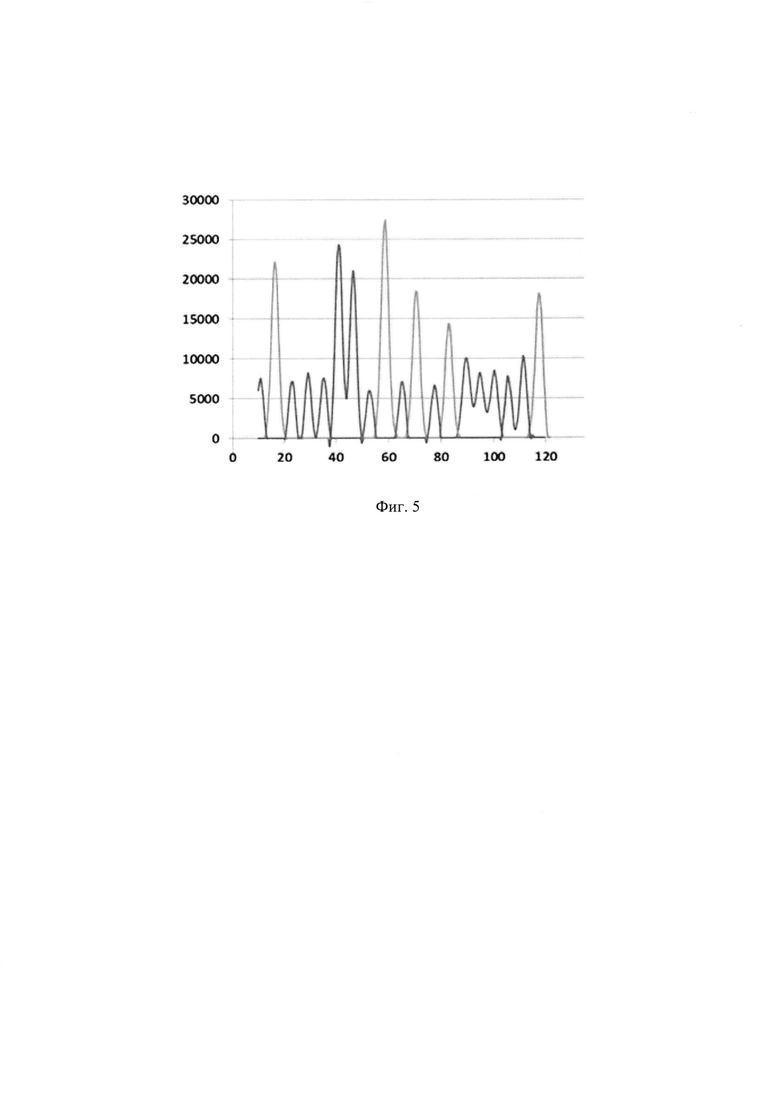
на фиг. 5 - фрагмент выровненной последовательности пиков. Вертикальная ось - интенсивность флуоресценции в относительных единицах (о. е.), горизонтальная ось - время в секундах.
В предлагаемом многоканальном капиллярном генетическом анализаторе использованы технические решения, приведенные на блок-схеме, изображенной на фиг. 1. Многоканальный капиллярный генетический анализатор, содержащий заполненные разделяющим полимером капилляры 1, к концам которых приложено высокое напряжение, устройство когерентного излучения 2, оптическую систему 3, блок спектрального анализа 4, блок регистрации флуоресцентного сигнала 5 и компьютер 6, снабжен базой данных 7, блоком оптимизации 8, блоком выравнивания 9 и блоком определения погрешностей 10, при этом вход базы данных связан с выходом блока регистрации флуоресцентного сигнала, база данных соединена двухсторонней связью с блоком оптимизации, блоком выравнивания и блоком определения погрешностей, а выходы базы данных соединены с входами компьютера, кроме того выход устройства подготовки пробы 11 соединен с входом генетического анализатора 1, а выход блока программного обеспечения роботизированного комплекса 12 - с входом базы данных 7.
С выхода блока регистрации флуоресцентного сигнала на вход базы данных передаются сигналы четырех последовательностей пиков, соответствующие сочетаниям нуклеотидов и флуоресцентных красителей на конце каждого анализируемого фрагмента ДНК, переданные сигналы сохраняются в базе данных.
С выхода базы данных на вход блока оптимизации передаются сигналы четырех последовательностей пиков, а с выхода блока оптимизации на вход базы передаются параметры выравнивания.
С выхода базы данных на вход блока выравнивания передаются сигналы четырех последовательностей пиков и параметры выравнивания, а с выхода блока выравнивания на вход базы передаются сигналы выровненной последовательности пиков, при этом каждый пик может быть аппроксимирован известной математической функцией, например, функцией Гаусса.
С выхода базы данных на вход блока определения погрешностей передаются сигналы выровненной последовательности пиков, а с выхода блока выравнивания на вход базы передаются буквенные обозначения и значения погрешностей определения параметров каждого пика в последовательности.
Выходы базы данных соединены с входами компьютера, при этом на экране компьютера одновременно индицируются полученные после выравнивания или аппроксимированные сигналы в виде четырех совмещенных по времени графических последовательностей пиков, буквенные обозначения и значения погрешностей определения параметров каждого пика.
База данных, блок оптимизации, блок выравнивания и блок определения погрешностей или некоторые из них могут быть выполнены в виде интегральных схем.
Генетический анализатор сопряжен с устройством подготовки пробы, при этом выход устройства подготовки пробы соединен с входом генетического анализатора, а выход блока программного обеспечения роботизированного комплекса - с входом базы данных для передачи признаков наборов флуоресцентных красителей и параметров генетического анализа. Эти признаки и параметры используются многократно при выполнении однотипных анализов.
Генетический анализатор сопряжен с механическим устройством и устройством управления, обеспечивающим непрерывность выполнения операций подготовки и анализа пробы.
Работает предлагаемый многоканальный капиллярный генетический анализатор следующим образом.
При электрофорезе капилляры 1 заполняют разделяющим полимером, а концы капилляров погружают в ванночки с электропроводящим буферным раствором. Исследуемый образец, содержащий флуоресцентно-меченые компоненты, вносят в капилляр, прикладывая к концам капилляра, один из которых погружен в исследуемый образец, высокое напряжение. Концы капилляров вынимают из пробирок с образцами и погружают в ванночку с буферным раствором. Под действием высокого напряжения компоненты образцов мигрируют к другим концам капилляров. В процессе миграции вдоль капилляров происходит электрофоретическое разделение компонентов образцов. В результате разделения компоненты образцов последовательно детектируются с помощью устройства когерентного излучения 2, оптической системы 3, блока спектрального анализа 4 и блока регистрации флуоресцентного сигнала 5.
Устройство когерентного излучения 2, в состав которого входит лазер, обеспечивает одновременное возбуждение флуоресценции четырех красителей исследуемого образца в капилляре. Излучение флуоресценции с помощью оптической системы 3, блока спектрального анализа 4 и блока регистрации флуоресцентного сигнала 5 преобразуется в четырех спектральных каналах в цифровые сигналы.
Цифровые сигналы, полученные от каждого исследуемого образца в четырех каналах с буквенными обозначениями А, С, G, Т, сохраняются в базе данных 7 и передаются в блок оптимизации 8. Цифровые сигналы могут быть представлены на экране компьютера 6 в виде четырех графиков, при этом горизонтальные оси могут соответствовать номерам отсчетов или единицам времени, а вертикальные оси - интенсивности сигналов флуоресценции в относительных единицах.
В блоке оптимизации 8 выполняется предварительная обработка цифровых сигналов исследуемого образца: коррекция нулевой линии, фильтрация шума, устранение перекрестных помех в спектральных каналах, обострение пиков и определение времен выхода пиков. В результате получаются 4 набора дискретных величин с условными обозначениями tnA, tnC, tnG, tnT.
Величины tnA, tnC, tnG, tnT. соответствуют временам выхода пиков с порядковыми номерами n и буквенными обозначениями А, С, G, Т, совпадающими с обозначениями цветовых каналов.
Величины tnA, tnC, tnG, tnT. объединяются в общую временную последовательность с новыми номерами пиков N. Общая временная последовательность разбивается на несколько участков, при этом начало и конец каждого участка должны совпадать с вершинами пиков в одном из цветовых каналов, например в канале А.
В блоке оптимизации 8 формируется аналитическая базовая функция tNB, аппроксимирующая зависимость времен выхода пиков от номера пика N. Для этого выбирается участок с минимальными помехами и разрешением, достаточным для уверенного определения соседних пиков.
На этом участке задается базовая аппроксимирующая зависимость tNB полиномом третьей (или более высокой степени) от переменной величины N с произвольными коэффициентами D по формуле 1:
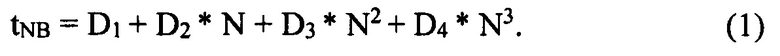
Вычисляются базовые временные интервалы между соседними пиками базовой последовательности по формуле 2:

Вычисляются временные интервалы между соседними пиками анализируемой последовательности по формуле 3:

Вычисляется относительная погрешность определения временных интервалов между соседними пиками анализируемой последовательности путем сравнения с базовыми временными интервалами по формуле 4:

В этой формуле величина pN выражена в базовых относительных единицах (б.о.е.).
На фиг. 2 приведен в графическом виде пример вычисления относительной погрешности определения временных интервалов между пиками исходной анализируемой последовательности на участке 300 нуклеотидов. Видно, что многие относительные погрешности pN имеют величину порядка ±0,5 б.о.е., при этом вычисленное значение СКО приблизительно равно 0,28 б.о.е.
Коэффициенты полинома аппроксимирующей зависимости D1, D2, D3, D4 определяются в блоке оптимизации 8 методом последовательного приближения при условии достижения минимальной суммы квадратов погрешностей pN и сохраняются в базе данных 7.
Вводятся параметры выравнивания с обозначениями d. В первом канале можно принять параметр выравнивания dA=0, в остальных трех каналах параметры выравнивания имеют обозначения dC, dG, dT. Параметр выравнивания dA=0 обеспечивает неизменность положения пиков в этом канале.
Вычисляются времена выхода пиков tV после выравнивания по формулам 5:
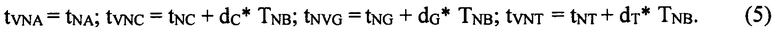
Задаются в первом приближении нулевые величины dC, dG, dT.
Вычисляются временные интервалы между соседними пиками последовательности после выравнивания с использованием этих коэффициентов по формуле 6:

Вычисляется относительная погрешность определения временных интервалов между пиками последовательности путем сравнения с базовыми временными интервалами по формуле 7:

Определяются параметры выравнивания dC, dG, dT с помощью метода последовательного приближения при условии достижения минимальной суммы квадратов погрешностей pVN. Параметры выравнивания dC, dG, dT на других участках вычисляются аналогично. Можно ввести коэффициент K, который учитывает зависимость базовых временных интервалов TNB от номера участка. При условии, что для первоначально выбранного участка K=0, параметры выравнивания для любого другого участка с номером U могут быть вычислены по формулам 8:
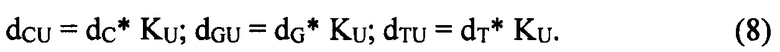
Параметры выравнивания всех участков сохраняются в базе данных 7. Повторение определения и сохранения параметров выравнивания для других анализируемых проб, которые подготовлены с использованием других наборов флуоресцентных меток и других условий электрофореза, позволяет создать, обновлять и многократно использовать собственную базу данных, содержащую параметры выравнивания, при анализе исследуемых образцов.
На фиг. 3 приведен в графическом виде пример вычисления относительной погрешности определения временных интервалов между пиками выровненной последовательности на участке 300 нуклеотидов. Видно, что многие максимальные погрешности имеют величину порядка ±0,15 б.о.е., при этом вычисленное значение СКО равно 0,08 б.о.е. По результатам сравнения можно сделать следующий вывод: после выравнивания значительно уменьшаются максимальные относительные погрешности определения временных интервалов и значение СКО (примерно, в 3-3,5 раза).
На фиг. 4 приведен пример совмещения четырех сигналов фрагмента исходной анализируемой последовательности, содержащего 19 пиков. Видно, что некоторые соседние пики (1 и 2, 8 и 9, 10 и 11, 12 и 13, 18 и 19) от фрагментов ДНК, окрашенных разными красителями, в значительной степени взаимно перекрываются.
В блоке выравнивания 9 выполняется изменение положения сигналов флуоресценции согласно параметрам выравнивания dC, dG, dT, полученным из базы данных 7.
Сигналы после выравнивания сохраняются в базе данных 7 и поступают на вход компьютера 6, где индицируются на экране в виде четырех совмещенных цветных графиков.
На фиг. 5 приведен пример сигналов фрагмента последовательности после выравнивания в виде 19 пиков, при этом пики располагаются равномерно.
В блоке выравнивания 9 определяются времена выхода пиков после выравнивания tV, каждому пику присваивается новый номер N и буквенное обозначение А, С, G, Т согласно цветовым каналам. Эти результаты сохраняются в базе данных 7 и индицируются на экране компьютера 6.
В блоке определения погрешностей 10 вычисляются величины относительной погрешности определения временных интервалов между пиками с номерами N и (N-1) по формуле 9:

Величины относительной погрешности pVN сохраняется в базе данных 7.
Значения относительной погрешности пиков из базы данных 7 передаются в компьютер, где индицируются на экране одновременно с графическими и буквенными изображениями соответствующих пиков. Значение pVN, близкое к значениям плюс 0,5 или минус 0,5, может быть использовано для принятия решения в автоматическом или ручном режиме: вставить неопределенный пик или исключить из последовательности случайный пик. Дополнительным критерием может служить значительное отличие амплитуды такого пика от амплитуды соседних пиков в этом же спектральном канале.
В блоке определения погрешностей 10 вычисляется ширина каждого пика последовательности после выравнивания. Для этого определяется аппроксимирующая зависимость полиномом третьей (или более высокой степени) базовой ширины пика от номера N, и определяются величины относительного отклонения ширины каждого реального пика от базовой ширины. Эти величины сохраняются в базе данных 7, индицируются на экране компьютера и могут быть использованы для принятия решения в автоматическом или ручном режиме разделить некоторые пики на два пика или исключить из последовательности случайный узкий пик.
В блоке определения погрешностей 10 вычисляется временное положение точек графика каждого пика последовательности после выравнивания слева tLN и справа tRN от вершины пика на уровне 0,6 или 0,5 от высоты пика. Вычисляется асимметрия пика с номером N при времени вершины пика tN по формуле 10:

Вычисляется отличие асимметрии D каждого пика от средней величины AS на участке по формуле 11:

Значительная величина DN может служить признаком наложения двух пиков.
В блоке определения погрешностей 10 выполняется поиск совпадения некоторых пиков выровненной последовательности в разных цветовых каналах. По результатам совпадения можно сделать вывод о том, что образец содержит смесь нуклеиновых кислот.
Предложен генетический анализатор, в котором функциональные блоки выполнены в виде интегральных схем. Таким образом, обеспечивается возможность уменьшить их габариты и обеспечить короткие функциональные соединения.
Предложен генетический анализатор, входящий в состав роботизированного комплекса, который содержит устройство подготовки пробы, при этом выход устройства подготовки пробы соединен с входом генетического анализатора, а выход блока программного обеспечения роботизированного комплекса - с входом базы данных для передачи наборов признаков флуоресцентных красителей и параметров генетического анализа. Каждый из используемых наборов признаков и параметров может быть сохранен с названием «Методика анализа» и условным порядковым номером. Набор содержит информацию о красителях, электрофоретической подвижности компонентов пробы, свойствах геля и других особенностях выполняемых анализов. Эти признаки и параметры используются в генетическом анализаторе для ускорения анализа серии анализируемых образцов, имеющих однотипные признаки и параметры. Этот генетический анализатор сопряжен с механическим устройством и устройством управления роботизированного комплекса, обеспечивающими непрерывность выполнения операций подготовки и анализа пробы и удобство при эксплуатации за счет выполнения операций подготовки пробы и генетического анализа без участия оператора; таким образом, исключаются субъективные ошибки.
Многоканальный капиллярный генетический анализатор согласно предлагаемому изобретению обеспечивает уменьшение ошибок при определении нуклеотидной последовательности путем выравнивания этой последовательности в автоматическом и ручном режиме, вычисления погрешностей определения параметров каждого нуклеотида в последовательности, формирования, пополнения и многократного использования базы данных, которая содержит параметры выравнивания нуклеотидной последовательности, признаки подготовки пробы и параметры генетического анализа и используется для успешного выполнение множества однотипных анализов. Предлагаемый многоканальный капиллярный генетический анализатор также обеспечивает непрерывность выполнения операций подготовки и анализа пробы при работе в составе роботизированного комплекса для молекулярно-генетических исследований.
Источники информации
1. Патент США № US 8604186 В2. UV excitable fluorescent energy transfer dyes. МПК C09B 11/24, C07H 19/20, C07H 21/04, C07D 263/62, C07H 19/04, C12N 15/09, C07H 19/10, G01N 33/58, G01N 33/53, C07D 213/00, C07H 21/00, C12Q 1/68, G01N 33/566, 10.12.2013 г.
2. Патент США № US 5688648 A. Probes labelled with energy transfer coupled dyes. МПК G01N 33/542, G01N 33/533, C12Q 1/68, G01N 33/566, G01N 33/53, G01N 33/58, 18.11.1997 г.
3. Патент ЕПВ № WO 2002036832 A2. Atropisomers of asymmetric xanthene fluorescent dyes and methods of DNA sequencing and fragment analysis. МПК C12Q 1/68, C07D 405/12, C07K 14/00, C07H 21/00, C07D 311/82, C07H 19/20, C07H 19/10, C12N 15/09, 10.05.2002 г.
4. Патент РФ №2145078. Многоканальный капиллярный генетический анализатор. МПК G01N 21/64, G01N 27/447, 27.01.2000 г.
Изобретение относится к многоканальному капиллярному генетическому анализатору, содержащему заполненные разделяющим полимером капилляры, к концам которых приложено высокое напряжение, устройство когерентного излучения, оптическую систему, блок спектрального анализа, блок регистрации флуоресцентного сигнала и компьютер, отличающемуся тем, что он снабжен базой данных, блоком оптимизации, блоком выравнивания и блоком определения погрешностей, при этом вход базы данных связан с выходом блока регистрации флуоресцентного сигнала, база данных соединена двухсторонней связью с блоком оптимизации, блоком выравнивания и блоком определения погрешностей, а выходы базы данных соединены с входами компьютера. Техническим результатом предлагаемого изобретения является уменьшение ошибок при определении нуклеотидной последовательности путем выравнивания этой последовательности в автоматическом и ручном режиме. Техническим результатом также является обеспечение непрерывности выполнения операций подготовки и анализа пробы. 8 з.п. ф-лы, 5 ил.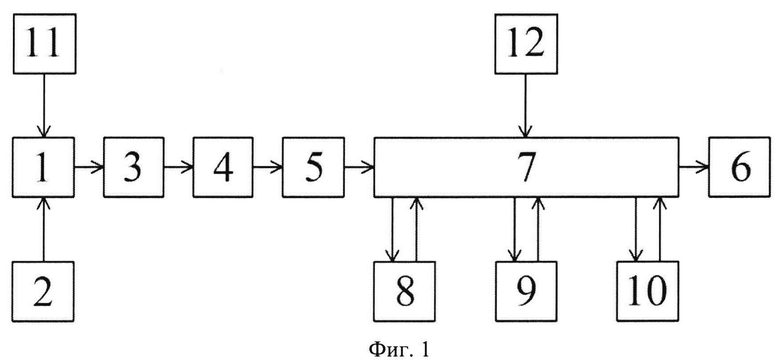
1. Многоканальный капиллярный генетический анализатор, содержащий заполненные разделяющим полимером капилляры, к концам которых приложено высокое напряжение, устройство когерентного излучения, оптическую систему, блок спектрального анализа, блок регистрации флуоресцентного сигнала и компьютер, отличающийся тем, что он снабжен базой данных, блоком оптимизации, блоком выравнивания и блоком определения погрешностей, при этом вход базы данных связан с выходом блока регистрации флуоресцентного сигнала, база данных соединена двухсторонней связью с блоком оптимизации, блоком выравнивания и блоком определения погрешностей, а выходы базы данных соединены с входами компьютера.
2. Многоканальный капиллярный генетический анализатор по п. 1, отличающийся тем, что с выхода блока регистрации флуоресцентного сигнала на вход базы данных передаются сигналы четырех последовательностей пиков, соответствующие сочетаниям нуклеотидов и флуоресцентных красителей на конце каждого анализируемого фрагмента ДНК, переданные сигналы сохраняются в базе данных.
3. Многоканальный капиллярный генетический анализатор по п. 2, отличающийся тем, что с выхода базы данных на вход блока оптимизации передаются сигналы четырех последовательностей пиков, а с выхода блока оптимизации на вход базы данных передаются параметры выравнивания.
4. Многоканальный капиллярный генетический анализатор по п. 3, отличающийся тем, что с выхода базы данных на вход блока выравнивания передаются сигналы четырех последовательностей пиков и параметры выравнивания, а с выхода блока выравнивания на вход базы данных передаются сигналы выровненной последовательности пиков, при этом каждый пик может быть аппроксимирован известной математической функцией, например функцией Гаусса.
5. Многоканальный капиллярный генетический анализатор по п. 4, отличающийся тем, что с выхода базы данных на вход блока определения погрешностей передаются сигналы выровненной последовательности пиков, а с выхода блока определения погрешностей на вход базы данных передаются буквенные обозначения и значения погрешностей определения параметров каждого пика в последовательности.
6. Многоканальный капиллярный генетический анализатор по п. 5, отличающийся тем, что выходы базы данных соединены с входами компьютера, при этом на экране компьютера одновременно индицируются полученные после выравнивания или аппроксимированные сигналы в виде четырех совмещенных по времени графических последовательностей пиков, буквенные обозначения и значения погрешностей определения параметров каждого пика.
7. Многоканальный капиллярный генетический анализатор по п. 6, отличающийся тем, что база данных, блок оптимизации, блок выравнивания и блок определения погрешностей или некоторые из них могут быть выполнены в виде интегральных схем.
8. Многоканальный капиллярный генетический анализатор по п. 7, отличающийся тем, что он сопряжен с роботизированным комплексом для молекулярно-генетических исследований, который содержит устройство подготовки пробы, при этом выход устройства подготовки пробы соединен с входом генетического анализатора, а выход программного обеспечения роботизированного комплекса - с входом базы данных для передачи наборов признаков флуоресцентных красителей и параметров генетического анализа.
9. Многоканальный капиллярный генетический анализатор по п. 8, отличающийся тем, что он сопряжен с механическим устройством и устройством управления, обеспечивающим непрерывность выполнения операций подготовки и анализа пробы.
| СПОСОБ СПЕЦИФИЧЕСКОЙ ИДЕНТИФИКАЦИИ ПОСЛЕДОВАТЕЛЬНОСТЕЙ ДНК | 2017 |
|
RU2665631C2 |
| Трехфазная электропечь для получения сероуглерода | 1960 |
|
SU132203A1 |
| Способ анализа последовательности нуклеотидов | 2017 |
|
RU2663693C1 |
| МНОГОКАНАЛЬНЫЙ КАПИЛЛЯРНЫЙ ГЕНЕТИЧЕСКИЙ АНАЛИЗАТОР | 1999 |
|
RU2145078C1 |
| Трехфазная электропечь для получения сероуглерода | 1960 |
|
SU132203A1 |
| WO 2012096955 A1, 19.07.2012 | |||
| CN 102533994 A, 04.07.2012. | |||
Авторы
Даты
2019-12-02—Публикация
2018-12-03—Подача