Изобретение относится к композициям, предназначенным для лечения состояний и заболеваний, например рака; к использованию указанных композиций для лечения состояний и заболеваний; к способам лечения состояний и заболеваний и к направленной поставке лекарственного средства к целевой ткани в целях лечения заболеваний.
Предпосылки создания изобретения
В статье Сандры Блейксли, озаглавленной "Solid cores of tumors keeping out best drugs" и опубликованной 8 июля 1989 г., под ред. Globe и Mail, Торонто, Онтарио, указывается, что все возрастающее количество исследователей считает, что, в основном, неправильное понимание структуры твердых опухолей приводит ученых к составлению лекарственных средств от рака, которые однако обречены на неудачу при лечении многих пациентов.
Как упоминается в указанной статье, по мнению д-ра Хебермана, директора Питтсбургского ракового центра, в последние десятилетия исследователи рака просто разрабатывают лекарственные средства, вводят их в кровоток, в результате чего осуществляют обработку опухоли, однако при этом эти исследователи не берут в расчет, каким образом лекарственное средство распределяется в опухоли, после того как оно достигнет этой опухоли.
В указанной статье также сообщается, что по мнению д-ра Judah Folkman, ведущего исследователя в области факторов роста крови в Гарвардском медицинском училище, в течение многих лет врачи считали, что опухоль наращивает свою систему кровоснабжения. Согласно указанной статье это утверждение неверно. Опухоли сдавливают свою систему кровоснабжения. Эта компрессия делает их более твердыми для введения лекарственных средств.
Далее, в статье указывается, что большинство людей считают, что опухоль представляет собой не что иное, как коллекцию раковых клеток. По мнению д-ра Jain, другого исследователя, на самом деле опухоль состоит только на 50% из клеток. Другая половина представляет собой кровеносные сосуды и интерстициальное пространство. По мнению этого ученого, интерстициальное пространство в опухоли похоже на пространство между мрамором, уложенным в ящик.
Кроме этого, в указанной статье сообщается, что независимо от того, каким образом смешиваются и вводятся биологические средства, они должны пересекать стенки кровеносных сосудов, а затем пересекать интерстиции для достижения своих целей - раковых клеток. В этой статье указывается также, что все опухоли отличаются друг от друга, и каждая опухоль включает в себя различные области. Кроме того, опухоли ежедневно меняются, поскольку они растут и их части перестраиваются. Большая часть кровеносных сосудов внутри опухоли расположена в высшей степени беспорядочно, имеет скрученный, извитый вид и сращивается с близлежащими сосудами.
По мнению д-ра Jain, поскольку опухоль растет, то ее внешние области обрастают новыми кровеносными сосудами из окружающей нормальной ткани. При этом также образуются несколько аномальных кровеносных сосудов, происходящих из самой опухоли. Поскольку опухоль растет в ограниченном пространстве, многие из этих скрученных кровеносных сосудов, находящихся вблизи ее центра, разрушаются. В свою очередь, опухолевые клетки, находящиеся вблизи этих сосудов, очевидно, погибают, хотя если их трансплантировать другим животным, они могут активно расти и образовывать раковую опухоль. В этих некротических областях образуется высокое давление. Кровеносные сосуды и жидкая плазма в интерстициальном пространстве сдавливаются. Это давление мешает кровеносным молекулам, включая кислород, проникнуть в центральные области опухоли.
Давление в нормальных тканях также не является неоднородным и по мнению д-ра Jain такие большие молекулы, как антитела, могут достигать своей цели посредством конвекции, вызываемой разницей в давлении. Но в центре опухоли, где давление является однородно высоким, этой конвекции не происходит.
Кроме того, по мнению д-ра Jain молекулы мигрируют посредством диффузии, механизм которой напоминает каплю чернил, распространяющуюся в воде.
Д-р Jain проводил измерения диффузии антитела в опухоли и обнаружил, что для достижения однородной концентрации в опухоли путем диффузии для таких больших молекул требуются дни, недели или месяцы. К тому времени может оказаться, что получить успешное лечение уже слишком поздно.
И, наконец, жидкость, которая образуется в интерстиции, медленно вытекает из опухоли, вымывая молекулы, пытающиеся достичь центра опухоли.
В своей заявке на патент Канады сер. N 568512 авторы настоящей заявки описывают новую композицию, предназначенную для лечения рака при использовании в сочетании с другими способами лечения, по крайней мере, с таким, как термотерапия (гипертермия), и по желанию с такими, способами, как химиотерапия (или облучение), которая включает в себя, например, в фармацевтически приемлемом носителе:
(a) глюкозо-ингибирующее (нетоксичное) количество средства, которое блокирует белок, транспортирующий глюкозу (активная молекула-носитель) в мембрану, предотвращая транспорт глюкозы в клетку; и
(b) эффективное нетоксичное количество лекарственного средства, которое (i) повышает проникновение и перенос средства (а) через ткань, окружающую различные клеточные элементы, в основном, известные, как рубцовая ткань или фиброзная ткань, окружающая раковую опухоль, и (ii) изменяет свойства проницаемости ткани, окружающей опухоль, что способствует проникновению средства а в центр опухоли.
Авторы также описывают комбинацию и композицию, предназначенные для лечения рака; причем указанная комбинация включает в себя:
(a) глюкозо-ингибирующее нетоксичное количество средства, которое блокирует белок, транспортирующий глюкозу (активная молекула-носитель) в мембрану, предотвращая транспорт глюкозы в клетку и
(b) эффективное (нетоксичное) количество лекарственного средства, которое (i) повышает проникновение и перенос средства а через ткань, окружающую различные клеточные элементы, в основном, известные как реакция рубцовой ткани или фиброзной ткани вокруг раковой опухоли, и (ii) изменяет свойства проницаемости ткани, окружающей опухоль, что способствует проникновению средства в центр опухоли.
После введения композиции или комбинации, содержащей средства (a) и (b), пациенту с метаболически активными опухолевыми клетками, опухоль и раковые клетки, ее составляющие, подавляются по крайней мере термотерапией (гипертермией). В связи с этим следует указать, что если средство (а) проникает в опухолевые клетки и опухолевые клетки подавляются, то имеется неадекватное количество глюкозы, приемлемое для продолжения метаболической функции в раковых клетках. Таким образом, опухолевая клетка разрушается при ее снабжении энергией и погибает. Авторы настоящей заявки также раскрывают способ лечения рака, который заключается во введении (например, в фармацевтически приемлемом носителе):
(a) глюкозо-ингибирующее (нетоксичное) количество средства, которое блокирует белок, транспортирующий глюкозу (активная молекула-носитель в мембране), предотвращая транспорт глюкозы в клетку; и
(b) эффективное (нетоксичное) количество лекарственного средства, которое (i) усиливает проникновение и перенос средства (a) через ткань, окружающую различные клеточные элементы, в основном, известные как рубцовая ткань или фиброзная реакционная среда вокруг раковой опухоли, и (ii) изменяет свойства проницаемости ткани, окружающей опухоль, что способствует проникновению средства (a) в центр опухоли при обработке раковых клеток средствами термотерапия (гипертермии). В некоторых случаях могут быть также использованы другие способы лечения (например, химиотерапия и/или облучение).
В таком глюкозо-ингибирующем количестве, которое блокирует белок, транспортирующий глюкозу в клетки (в раковых клетках наблюдается большее количество глюкозы, чем в нормальных клетках) может быть использован:
Флоретин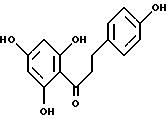
Флоридзин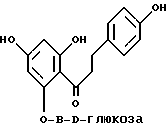
или их аналоги, включая глюкуронид флоридзина; 4-дезокси- флоретин-2-D-глюкозид и т.п.
Эффективное количество указанного средства способствует:
(i) усилению проникновения и переноса средства (a) через ткань, окружающую различные клеточные элементы, известные, в основном, как рубцовая ткань или фиброзная реакционная среда вокруг раковой опухоли; и
(ii) изменению проницающих свойств ткани, окружающей опухоль, облегчая доступ средства а к центру опухоли, которое может содержать диметилсульфоксид (ДМСО), метилсульфонилметан (МСМ) (называемый также метилсульфонметаном) или другие носители типа молекул-переносчиков, обладающих способностью к
(i) усилению проникновения и транспорта средства (a) через ткань, окружающую различные клеточные элементы, в основном, известные как рубцовая ткань или фиброзная реакционная среда вокруг раковой опухоли, и
(ii) изменению проницающих свойств ткани, окружающей опухоль, способствующему облегчению доступа средства а к центру опухоли.
В статье "Toxic drug tamed but still potent", опубликованной в Ontario Medicine, т. 8; N 16, 21 авг. 1989 г. описывается использование системы доставки липосомального лекарственного вещества к целевому участку в виде капсулы, содержащей высокотоксичный, но при этом высокоэффективный противогрибковый агент, и тем самым иллюстрируется, каким образом токсичное лекарственное средство может быть внесено в нетоксичные лекарственные средства, не создавая при этом угрозы при клиническом применении.
В этой статье указывается следующее:
"Сначала казалось, что липосомы представляют широкие возможности в качестве системы доставки лекарственного средства к целевому участку почти для всех фармацевтических агентов. Однако, исследования, проводимые в этой области за последние два десятилетия, показали, что указанные искусственные сферы размером в клетку могут спонтанно образовываться лишь с небольшим подклассом имеющихся в настоящее время лекарственных средств, что крайне ограничивает их использование".
Хоффер изучал действие аскорбиновой кислоты (витамин C) на состояние здоровья пациента. В своей статье он описывает эффект применения витамина C при лечении рака. Он также обсуждает открытие Камерона и Поллинга относительно использования аскорбиновой кислоты в 10-граммовых дозах для лечения раковых больных, введение которой повышает выживаемость пациентов, больных раком в последней стадии развития болезни. Хоффер также указывает на безопасность использования аскорбиновой кислоты даже в очень высоких дозах. На стр. 11 его исследования указывается, что аскорбиновая кислота является водорастворимой, способной к набуханию, но не имеет LD50. Хоффер отмечает, что:
"Если витамин не может быть полностью абсорбирован из желудочно-кишечной системы, то он будет удерживать воду в кишечнике, вызывая понос, который будет водяным, но не опасным, если только он не приведет к дегидратации; что заставит пациентов быстро снизить дозу. В указанных дозах он использовался миллионами людей. Известны пациенты, которые принимали 30 г в день в течение 30 лет. Это более безопасно, чем такая же таблетка соли. Это средство не дает камней в почках, не вызывает пернициозную анемию, не вызывает бесплодие у женщин и не вызывает рака."
Целью настоящего изобретения являются композиции, пригодные для использования их при лечении заболеваний и состояний, использование указанных композиций в лечении заболеваний и состояний, способы лечения заболеваний и состояний, и способы доставки лекарственных и терапевтических средств к целевым участкам при лечении заболеваний, например рака, и состояний.
Другие цели настоящего изобретения будут понятны специалистам из дальнейшего описания изобретения, в котором заявители обращаются к литературе, не отражающей данные их изобретения.
Гиалуроновая кислота представляет собой встречающийся в природе гликозаминоглюкан. Он имеет молекулярную массу величиной от 50 000 Да и выше и образует высоковязкие растворы. Что касается фактической молекулярной массы гиалуроновой кислоты с биологической точки зрения, то здесь имеет место значительная неопределенность: при определении молекулярной массы гиалуроновой кислоты обычно получают различные значения в зависимости от используемого метода, источника, способа выделения и т.п. Указанная кислота содержится в тканях животных, например в цереброспинальной жидкости, синовиальной жидкости, в петушином гребне, коже, а также в некоторых стрептококках. Были получены различные виды гиалуроновой кислоты. В патенте США 4141973 описывается получение гиалуроновой кислоты якобы высокой степени чистоты и не вызывающей никаких побочных действий в качестве противовоспалительного средства; при этом указанная гиалуроновая кислота имела молекулярную массу, превышающую 750 000 Да, а предпочтительно 1200000 Да, и предназначалась для лечения различных артикулярных состояний.
Патент США 4801619 относится к гиалуроновой кислоте, имеющей молекулярную массу около 3•106 Да или выше и вводимой внутрь сустава, которая обладает способностью к снижению содержания протеогликана в синовиальной жидкости до нормального уровня. Согласно этому патенту указанный факт благоприятствует метаболизму протеогликана в суставе. В этом патенте указывается, что гиалуроновая кислота может быть использована как при лечении воспалительных заболеваний, так и дегенеративных изменений, вызванных применением симптоматических препаратов, таких как кортикостероидные препараты. Таким образом, очевидно, что гиалуроновая кислота с достаточно высокой молекулярной массой как бы нейтрализует побочные эффекты, которые могут быть вызваны кортикостероидами или другими симптоматическими препаратами, вызывающими аналогичные эффекты. При применении кортикостероидов количество гиалуроновой кислоты в синовиальной полости, согласно указанному патенту, возрастает и поэтому, как утверждают авторы патента, их препараты гиалуроновой кислоты оказывают благоприятное действие при таких клинических симптомах, как боли в суставах, опухлость и увечья.
В патенте указывается, что авторы достигают своей цели путем внутриартикулярного введения эффективного количества гиалуроновой кислоты со средней молекулярной массой 3•106 Да, а предпочтительно с молекулярной массой, превышающей 4•106 Да, при этом молекулярная масса не должна превышать 7•106 Да. Доза вводимой гиалуроновой кислоты устанавливается предпочтительно в пределах от 5 мг до 80 мг. Количество водного раствора кислоты (или ее соли), используемого при каждом введении, в основном, составляет менее 60 мл, например, менее 20 мл. Обычно кислоту вводят в виде водного раствора 2 мас.%, разведенного буфером до физиологического pH, например, в виде водорастворимой натриевой соли. Точное количество зависит от конкретного обрабатываемого сустава.
В Merck index Specifies указывается, что гиалуроновая кислота имеет молекулярную массу в пределах 50000 - 8•106 в зависимости от источника, способов получения и методов определения. В публикации Merck указывается также, что гиалуроновая кислота используется в хирургии офтальмологической.
В патенте США 4 808 576 сообщается, что гиалуроновая кислота является хорошо известным средством, применяемым для предотвращения осложнений при травмах суставов, если оно наносится непосредственно на поврежденную ткань, при этом, если оно вводится в место, удаленное от поврежденной ткани, то оно будет донесено до этой поврежденной ткани путем естественных процессов в организме животного. Таким образом, указанная гиалуроновая кислота, согласно указанному патенту, может быть введена в любой терапевтически приемлемой форме и любым стандартным способом введения, например, внутривенно, внутримышечно, подкожно и наружно.
Это, как указывается в патенте, делает применение гиалуроновой кислоты гораздо более удобным и привлекательным. Например, согласно патенту лечение артритов у лошадей или человека уже больше не требует трудоемких внутрисуставных инъекций.
В патенте США 4 725 585 описывается способ повышения или регулирования иммунной защиты организма, который заключается во введении млекопитающему терапевтически эффективного количества гиалуроновой кислоты.
В столбце 1 строках 43-46 указанного патента сообщается, что изобретение основано на неожиданном открытии, что введение гиалуроновой кислоты млекопитающим способствует значительному повышению иммунитета.
В рассматриваемом патенте в качестве гиалуроновой кислоты используется Хилон Т. М., поставляемый Pharmacia AB, Уппсала, Швеция. Pharmacia AB также имеет право на прибыль от внедрения патента США 4141973. В столбце 1 (строка 19) указывается, что если инфекционное заболевание пациента плохо поддается лечению, то вместо гиалуроновой кислоты для повышения иммунитета пациенту вводили гиалуроновую кислоту и антибиотик. Хотя в патенте указывается, что антибиотик вводили в сочетании с гиалуроновой кислотой, однако, фактически, вследствие того, что гиалуроновую кислоту вводили подкожно и вследствие того, что пациентом был сердечный больной, то специалистам понятно, что любой антибиотик вводят отдельно, хотя он может быть введен одновременно - внутривенно (вероятно) или внутримышечно (менее вероятно). Таким образом, (наиболее вероятно) гиалуроновую кислоту вводили, согласно указаниям в патенте, в целях предотвращения возможного возникновения других инфекций в целях повышения иммунной защиты, а не в каких-либо других целях.
В патенте США 4 636 524 раскрываются заструктурированные гели гиалуроновой кислоты, взятой в чистом виде или в смеси с другими гидрофильными полимерами, и содержащие различные вещества или ковалентно связанные низкомолекулярные вещества, и способы их получения. Эти продукты, как указывается в патенте, могут быть использованы в самых различных областях, включая косметические препараты и в системах доставки лекарственного средства к целевому участку.
Кроме того, в патенте указывается, что гиалуроновая кислота является известной как биологически толерантный полимер, т.е. при введении человеку она не вызывает иммунного ответа, и заструктурированные гели гиалуроновой кислоты могут быть использованы в различных медицинских целях. Заструктурированные гели, модифицированные другими полимерами или низкомолекулярными веществами, согласно патенту, могут быть использованы в качестве системы доставки лекарственного средства. Например, авторы патента обнаружили, что гепарин, введенный в заструктурированный гель гиалуроновой кислоты, сохраняет его антитромбогенетическую активность.
Авторы патента также утверждают, что они также обнаружили, что заструктурированные гели гиалуроновой кислоты могут замедлять высвобождение низкомолекулярных веществ, диспергированных в них, но ковалентно связанных с макромолекулярной матрицей геля.
В патенте США 4 736 024 описываются новые лекарственные средства, используемые для наружного применения и содержащие:
(i) активное фармакологическое средство (или смесь фармакологических средств), приемлемое для наружного применения, и
(ii) наполнитель, приемлемый для наружного применения, и содержащий гиалуроновую кислоту или молекулярную фракцию гиалуроновой кислоты или ее соль со щелочным металлом, щелочноземельным металлом, магнием, алюминием, аммонием или фармакологическое вещество, необязательно используемое вместе с дополнительными наполнителями, приемлемыми для наружного применения.
Заявители настоящей заявки ознакомились с недавно опубликованным японским патентом 61000017, датированным 86/01/06, где указывается (в англ. реферате), что указанный патент относится к использованию гиалуроновой кислоты или структурированной гиалуроновой кислоты или ее солей в качестве активного ингредиента в целях ингибирования метастаз карциномы.
Согласно упомянутому реферату патента, более 1,0% гиалуроновой кислоты растворяли в щелочном водном растворителе, а предпочтительно добавляли более 50% H2O раствора органического растворителя, напр. спирта, ацетона, диоксана, по отношению к полному раствору. Предпочтительный pH составляет 12-14. Затем добавляли многофункциональное эпокси-соединение и подвергали реакции при 10-60oC, а предпочтительно при 20-40oC, в течение 24 час. Степень образования поперечных связей структурированной гиалуроновой кислоты или ее соли регулировалось путем изменения молярного отношения гиалуроновой кислоты или ее соли и многофункционального эпокси-соединения. Предпочтительной гиалуроновой кислотой является кислота с вязкостью 0,2-30 и мол.массой 4000-2 000 000. Согласно патенту гиалуроновая кислота используется в нескольких лекарственных формах. Клиническая доза гиалуроновой кислоты или заструктурированной гиалуроновой кислоты обычно составляла 25 мг - 5 г в день (р.о.) и 10 мг - 2,5 г/л дозы (инъекц.). В реферате патента указывается, что гиалуроновая кислота не оказывает побочного действия в отличие от других противораковых средств и обладает аналгезирующим и тканевосстанавливающим действием.
В Европатенте 0295092 описывается использование фрагментов гиалуроновой кислоты вместе с наполнителем в качестве системы доставки указанных фрагментов путем нанесения на кожу в целях достижения дермального слоя кожи, обработки кровеносных сосудов и стимулирования роста волос или восстановления роста полос. Предпочтительными фрагментами гиалуроновой кислоты являются полисахариды, содержащие от 7 до 25 моносахаридных единиц. Согласно патенту, очевидно, что чем больше фрагменты гиалуроновой кислоты, тем труднее доставка этих фрагментов в дермальный слой кожи, если только эти фрагменты не являются частью композиции, составленной с целью повышения активности этих фрагментов.
Таким образом, может быть использована комбинация для усиления активности фрагментов гиалуроновой кислоты, а в частности для усиления их проникновения через кожу при наружном нанесении. Некоторую роль в повышении активности могут также играть, как указывается в патенте, наполнители для фрагментов гиалуроновой кислоты.
Некоторые усилители активности, согласно патенту, обладают способностью стимулировать или усиливать рост волос. Среди прочих усилителей, в качестве такого усилителя активности может быть использован миноксидил. Таким образом, фрагменты гиалуроновой кислоты и миноксидил используются для стимуляции роста волос.
В заявке на Европатент 0179442 указывается, что там, где имеется значительное количество свободных радикалов, гиалуроновая кислота распадается или разлагается еще до того, как она даст положительный эффект.
В сообщении о патенте Канады 1240929 описывается комбинация соединения сульфата хондроитина и гиалуроната для защиты поврежденных травмой клеточных слоев и ткани животных и человека.
В заявке на Европатент 0208623 описывается использование гиалуроновой кислоты в целях увеличения активности некоторых протеаз. В заявке также сообщается об использовании гиалуроновой кислоты для лечения заболеваний соединительной ткани, включая злокачественные опухоли и сердечно-сосудистые нарушения.
В заявке на Европатент 270317 описывается комбинация противовирусного средства с недостаточным ингибирующим действием и соединения (например, гиалуроновой кислоты), обладающего активностью, ингибирующей слияние клеток, и/или активностью, ингибирующей адсорбцию вируса, для лечения вирусных заболеваний.
В патенте США 4840941 описывается использование эффективного количества гиалуроновой кислоты в качестве активного средства для лечения ретровирусных заболеваний в сочетании с фармацевтически приемлемым носителем, разбавителем или наполнителем.
В патенте США 4851521 и в заявке на Европатент 0265116 описываются фракции гиалуроновой кислоты, структурированные сложные эфиры гиалуроновой кислоты и их получение. В патенте США 4 851521 описывается введение сложных эфиров гиалуроновой кислоты в фармацевтические препараты в качестве активных ингредиентов и в качестве носителей для офтальмологических лекарственных средств для наружного применения (см. столбец 11, строки 35-42 и столбец 12, строка 62 - столбец 13 строка 3) и суппозитории для системного действия вследствие чрезкожной абсорбции.
В указанном патенте в столбце 13 (строки 5-31) сообщается следующее:
"Действие сложных эфиров гиалуроновой кислоты как носителей позволяет использовать их в качестве сопутствующих лекарственных средств в препаратах упомянутого выше типа, где активное вещество действует не только при местном применении или путем насальной или ректальной абсорбции, например, при введении путем впрыскивания или ингаляции, но и также путем перорального введения или парентерального введения, например, внутримышечно, подкожно или внутривенно, поскольку такое введение благоприятствует абсорбции лекарственного средства в месте введения. Следовательно, новое лекарственное средство может широко применяться в различных областях медицины, таких как терапия внутренних болезней: например, при лечении сердечно-сосудистых заболеваний, инфекционных заболеваний дыхательных путей, пищеварительной системы, почек, болезней эндокринной системы, онкология, психиатрия и т.п.; и поэтому эти лекарственные средства могут быть классифицированы с точки зрения их специфического действия как анастезирующие средства, аналгезирующие средства, противовоспалительные средства, средства для заживления ран, антимикробные средства, адренергические агонисты или антагонисты, цитостатики, противоревматические средства, гипотенсивные средства, мочегонные средства, половые гормоны, иммуностимуляторы и иммунодепрессанты; например, одно из лекарственных средств, имеющее активность, уже описанную для терапевтически активных спиртов, используемых в качестве этерифицирующего компонента согласно настоящему изобретению, или для терапевтически активных оснований, используемых для салификации свободных гидроксильных групп..."
Фуросемид ингибирует реабсорбцию натрия в восходящем сегменте петли нефрона в ее проксимальном и дистальном отделах. Действие лекарственного средства не зависит от ингибирующего воздействия на карбоангидразу или альдостерон. Фуросемид является известным средством, стимулирующим диурез, которое используется в тех случаях, когда наблюдается резистентность к другим диуретикам. Это средство воздействует лишь на функцию почек и не имеет другого фармакологического действия. В организме человека он абсорбируется из желудочно-пищеварительного тракта. Обычно, диурез наблюдается через 30 минут после внутривенного введения средства и его действие продолжается около 2 часов.
При различных обстоятельствах у пациента может вырабатываться относительная резистентность к действию лазикса. Это может происходить по разным причинам, но чаще всего это явление бывает следствием скопления большого количества жидкости в результате периферической водянки, развивающейся из-за недостаточного питания или/и прогрессирующей карциномы. В последнем случае, наблюдается заметное снижение уровня альбумина, и по всей вероятности, возрастает проницаемость и трансудация жидкости из сосудов. Поэтому такие пациенты обладают относительной резистентностью к диуретикам любого типа, включая и лазикс, введенный внутривенно в больших дозах.
Были проведены широкие исследования в целях определения недостаточности иммунной функции организма, обусловленной развитием опухолевых клеток. Джерн (Jerne), а затем Бернет (Bernett) предположили, что иммунная система играет главную роль в иммунологическом "наблюдении" по уничтожению атипичных клеток. Эта концепция, хотя и кажется несколько упрощенной, все же остается основной приемлемой идеей для объяснения сложного механизма иммунного распознавания и иммунной функции, имеющих место у высших млекопитающих.
Кроме того, предполагается, что опухоли развиваются в результате местной или генерализованной иммунной супрессии. Однако, по мнению Моллера, если имеет место общая иммуносуппрессия, то обычно развиваются лишь некоторые типы опухолей, в основном, опухоли лимфо-ретикулярной системы. Это наблюдение подтверждается исследованием симптоматики и иммунной системы, хотя в отдельных случаях, и часто можно объяснить почему, раковые клетки развиваются как бы независимо от состояния иммунной системы.
Эксперименты, проведенные в 1974 г., показали, что при опухолевых заболеваниях имеет место нарушение фагоцитной функции.
В начальных экспериментах были обнаружены супрессорные клетки, являющиеся частью иммунной системы; они представляют собой тип Т-клеток системы фагоцитов. Их присутствие наблюдается при неоплазии, хронических бактериальных инфекциях, при выздоровлении от массивных ранений и хронических грибковых инфекций.
Эксперименты, проведенные на животных, подтвердили, что при неопластических заболеваниях функция фагоцитов изменена. Очевидно, в живых организмах при указанных заболеваниях функция макрофагов блокируется. В основном, если эти клетки удалить из in vivo-среды, промыть в солевом растворе и культивировать, их функция нормализуется. Такая блокировка, очевидно, является следствием избыточного продуцирования простагландина раковой тканью или самими фагоцитами.
В основных исследованиях, проведенных за последние 70-е и 80-е годы, имеются значительные разногласия относительно роли иммунотерапии при лечении рака. Активация или "агрессивность" макрофагов, очевидно, также имеет значение. Однако, при исследовании Ромасом и Фоком перитональных макрофагов, полученных от пациентов с раковым заболеванием, было обнаружено, что эти макрофаги, который были уже активированными, "сосуществовали" с раковыми клетками и не вызывали их деструкцию.
В начале этого года независимыми исследователями было показано, что недостаточная функция макрофагов или предполагаемое блокирование этой функции является следствием избыточного продуцирования простагландина, которое может быть устранено с помощью кортикостероидов, A A, и нестероидных противовоспалительных средств, например, индометацина и напроксена (NaprosynTM). Кроме того, на опухолях животных было снова продемонстрировано, что эти вещества могут изменять реакцию на злокачественные клетки и что, используя различные комбинации этих веществ вместе с иммуностимулирующими агентами, можно добиться надежного успеха в подавлении экспериментальных опухолей. Например, Лала Lala и коллеги, комбинируя индометацин-терапию с использованием интерлейкина-2, показали, что можно достичь хороших результатов при лечении экспериментальных опухолей.
Однако, использование любого из указанных средств создает реальную угрозу для осуществления in vivo-эксперимента на человеке. Все нестероидные противовоспалительные средства (НСПВС) являются весьма токсичными при попадании в желудочно-кишечные, неврологические и другие области организма. Таким образом, существующий в настоящее время способ основан на том, что указанные средства, попадая в человеческий организм, пораженный болезнью, в достаточных количествах, проникают в патологическую ткань и способствуют изменению локального продуцирования простагландина. При внутривенном введении индометацина и других лекарственных средств было обнаружено, как и в экспериментах, проведенных авторами настоящей заявки, что введение этих средств по отдельности дает недопустимое побочное действие в человеческом организме. Поэтому в организм человека может быть введено лишь недостаточное количество указанных средств, что дает более чем случайную реакцию в неоплазмах.
Однако, имеется большое количество показаний, на основании которых можно утверждать, что причина развития опухоли и механизм иммунного "наблюдения" за первичной клеткой относится к продуцированию простагландина. Этот постулат требует лишь изменения количества простагландина, синтезируемого клетками, когда они становятся "злокачественными", для установления механизма блокирования первичной клетки при любой иммунной реакции, т.е. макрофага. Поэтому представляется особенно важным разработать некоторую комбинацию НСПВС в целях клинического применения для повышения иммунного ответа на опухолевое заболевание и другие состояния, связанные с избыточным синтезом простагландина, который представляет собой причину патогенеза некоторых состояний, например, артритов и других так называемых воспалительных заболеваний соединительной ткани и/или автоагрессивных состояний.
См. также следующие работы:
1. Modulation of Immunity in Cancer patient by prostaglandin antagonists, Immunity to cancer II, Alan R, Liss, Inc., и
2. Goodwin, I.S. (1981 г.) Prostaglandin E and cancer Growth potentiаl for Immunotherapy with Prostaglandin syntesis Inhibitors, Augmentative agents in cancer therapy, Raven Press Нью-Йорк.
В патенте США 4711780 описывается фармацевтическая композиция, содержащая витамин C, цинковую соль, серосодержащую аминокислоту и предназначенная для обработки поверхностного эпителия в целях его регенерации. При обработке половых путей может быть добавлена гиалуроновая кислота, как указывается в патенте.
Публикация японского патента 63/045223 относится к лечению заболеваний, вызываемых ретровирусами. Как указывается в патенте, гиалуроновая кислота используется для профилактики или лечении от лейкемии или СПИДа путем подавления репликации вируса.
В статье др. Samuel Asculai, озаглавленной "Inactivation of Herpes Simplex Viruses by Nonionic Surfactants", опубликованной в Antimicrobial Agent and Chemoterapy, в апреле 1978, стр. 686-690 описываются неионогенные поверхностно-активные вещества, например ноноксинол, обнаруженный в DelfenTM, содержащие эфирные или амидные связи между гидрофильными и гидрофобными частями молекулы и быстро инактивирующие инфективность вирусов простого герпеса. Эта активность неионогенных поверхностно-активных веществ (ПАВ) основана на их способности растворять липид-содержащие мембраны. Этот факт подтверждается путем наблюдений ПАВ-деструкций цитоплазматических мембран млекопитающих и оболочек вируса простого герпеса. Патентованные вагинальные контрацептивные препараты, содержащие неионогенные ПАВ, также инактивируют инфективность вируса простого герпеса. Эти наблюдения дают возможность предположить, что неионогенные ПАВ, содержащиеся в соответствующих препаратах, могли бы эффективно способствовать предупреждению переноса вируса простого герпеса.
Краткое описание изобретения
Авторами настоящей заявки было обнаружено, что комбинации и композиции (например, препараты для инъекций) могут быть получены в целях введения млекопитающим для лечения заболеваний или состояний в терапевтически эффективных нетоксичных количествах; при этом указанные комбинации или композиции могут включать в себя лекарственные и/или терапевтические средства, используемые для лечения заболеваний или состояний, например, свободно-радикальный акцептор, напр., аскорбиновая кислота (витамин C)), витамин C (для лечения мононуклеоза), противораковое средство, химиотерапевтическое средство, противовирусные средства (например, неионогенное ПАВ, такое как ноноксинол-9 [нонилфеноксиполиэтокси-этанол] имеющееся в контрацептивной пасте DelfenTM), анионогенные ПАВ (напр., хлорид пиридиния) и катионогенные ПАВ (напр. , хлорид бензалкония)), нестероидные противовоспалительные средства (НСПВС) (например, индометацин, напроксен и (+/-)трометаминовая соль кеторолака (поставляемого под маркой ToradolTM)) и стероидные противовоспалительные средства, противогрибковое средство, дезинтоксифицирующие средства (например, при клизмах, вводимых ректально), аналгетики, бронхолитические средства, антибактериальные средства, антибиотики, средства для лечения сосудистой ишемии (например, при диабетах и болезни Бергера), моноклональное антитело, миноксидил для местного употребления для роста волос, диуретики (например, фуросемид, поставляемый под торговой маркой ЛазиксTM, иммунодепрессанты (например, циклоспорины), лимфокины (такие, как интерлейкин-2 и т.п. ), альфа- и бета-интерферон и т.п., которые вводятся вместе с некоторым количеством (или в некоторое количество) гиалуроновой кислоты и/или ее солей (например, натриевой соли) и/или гомологов, аналогов, производных, комплексов, сложных эфиров, фрагментов, и/или субъединиц указанной гиалуроновой кислоты (предпочтительно, гиалуроновой кислоты и ее солей), достаточным для облегчения проникновения лекарственного средства через ткань (включая рубцовую ткань) в месте обработки через клеточные мембраны в отдельные целевые клетки. При введении указанных комбинаций или композиций пациентам, страдающим от различных заболеваний и нарушений, наблюдается неожиданное улучшение состояния пациентов.
Композиции настоящего изобретения могут быть введены внутривенно, внутриартериально, внутрибрюшинно, внутриплеврально, чрескожно, путем наружного нанесения, ректально, перорально или путем прямой инъекции, например, в опухоль, абсцесс или аналогичное место локализации болезни или путем наложения на тампон, закрепленный на коже пациента. Гиалуроновая кислота и/или ее соли и лекарственное средство могут быть введены для лечения отдельно, но в достаточном для лечения количестве и в соответствующей временной последовательности, предпочтительно, совместно, а более предпочтительно одновременно, желательно в одно и то же место (например, одно - внутривенно, а другое - с обратной стороны).
Согласно одному варианту осуществления настоящее изобретение относится к комбинации, подходящей для лечения заболеваний или состояний и содержащей терапевтически эффективные нетоксичные количества:
(a) лекарственного и/или терапевтического средства для лечения заболеваний или состояний такого, как свободно радикальный акцептор (например, аскорбиновая кислота (витамин C)), витамин C (для лечения мононуклеоза), противораковое средство, химиотерапевтическое средство, противовирусное средство (например, неионогенное ПАВ, такое как ноноксинол-9 [нонилфеноксиполиэтоксиэтанол], имеющееся в контрацептивной пасте DelfenTM), анионогенные ПАВ (напр., хлорид пипридиния) и катионогенные ПАВ (например, хлорид бензалкония), нестероидные противовоспалительные средства (НСПВС), например индометацин, напроксен и (+/-)трометановая соль кеторолака (поставляемого под торговой маркой ToradolTM)) и стероидные противовоспалительные средства, противогрибковое средство, дезинтоксифицирующее средство (например, при клизмах, вводимых ректально), аналгезирующее средство, бронхолитическое средство, антибактериальное средство, антибиотики, средства для лечения сосудистой ишемии (например, диабетов и болезни Бергера), моноклональное антитело, миноксидил для наружного употребления для роста волос, мочегонные средства (например, фуросемид, поставляемый под торговой маркой ЛазиксTM), иммунодепрессанты (например, циклоспорины), лимфокины (такие, как интерлейкин-2) и т.п., альфа- и бета интерферон и т.п., и
(b) достаточное количество гиалуроновой кислоты и/или ее солей (например, натриевой соли) и/или гомологов, аналогов, производных, комплексов, сложных эфиров, фрагментов, и/или субъединиц гиалуроновой кислоты, предпочтительно гиалуроновой кислоты и ее солей; при этом указанное количество должно быть достаточным для облегчения проникновения лекарственного средства через ткань (включая рубцовую ткань) в месте обработки и через клеточные мембраны в целевые клетки.
Указанная комбинация может быть введена отдельно или в виде смеси или раствора. Если комбинация вводится отдельно, то предпочтительно одновременное введение в одно и то же место.
В соответствии с другим вариантом осуществления настоящее изобретение относится к композиции, предназначенной для использования в лечении состояний или заболеваний и содержащей терапевтически нетоксичное количество лекарственного и/или терапевтического средства для лечения заболеваний или состояний таких, как свободно-радикальный акцептор (напр., аскорбиновая кислота, (витамин C) для лечения мононуклеоза)), противораковое средство, химиотерапевтическое средство, противовирусные средства (например, неионогенное ПАВ, такое как ноноксинон-9 [нонилфеноксиполиэтокси-этанол] имеющееся в контрацептивной пасте DelfenTM)), анионогенные ПАВ (напр., хлорид пиридиния) и катионогенные ПАВ, напр., (хлорид бензалкония), нестероидные противовоспалительные средства (НСПВС), например, индометацин, напроксен и (+/-)трометаминовая соль кеторолака (поставляемого под маркой ToradolTM)) и стероидные противовоспалительные средства, противогрибковое средство, дезинтоксифицирующие средства (например, при клизмах, вводимых ректально), аналгетики, бронхолитические средства, антибактериальные средства, антибиотики, средства для лечения сосудистой ишемии (например, при диабетах и болезни Бергера), моноклональное антитело, миноксидил для местного употребления для роста волос, диуретики например, фуросемид (поставляемый под торговой маркой ЛазиксTM), иммунодепрессанты (например, циклоспорины), лимфокины (такие, как интерлейкин-2 и т.п.), альфа- и бета-интерферон и т.п., которые вводятся вместе с некоторым количеством (или в некоторое количество) гиалуроновой кислоты, и/или ее солей (например, натриевой соли), и/или гомологов, аналогов, производных, комплексов, сложных эфиров, фрагментов, и/или субъединиц указанной гиалуроновой кислоты), предпочтительно, гиалуроновой кислоты и ее солей, достаточным для облегчения проникновения лекарственного средства через ткань (включая рубцовую ткань) в месте обработки через клеточные мембраны в отдельные целевые клетки.
В соответствии со следующим вариантом осуществления настоящее изобретение относится к способу лечения состояний или заболеваний у млекопитающих, заключающемуся во введении указанным млекопитающим комбинации терапевтически эффективного нетоксичного количества:
(a) лекарственного и/или терапевтического средства для лечения заболеваний или состояний такого, как свободно-радикальный акцептор (например, аскорбиновая кислота витамин C), витамин C (для лечения мононуклеоза), противораковое средство, химиотерапевтическое средство, противовирусное средство (например, неионогенное ПАВ, такое, как ноноксинол-9 [нонилфеноксиполиэтокси-этанол] , имеющееся в контрацептивной пасте DelfenTM)), анионогенные ПАВ (напр. , хлорид пиридиния) и катионогенные ПАВ (например, хлорид бензалкония), нестероидные противовоспалительные средства (НСПВС), например индометацин, напроксен и (+/-)трометановая соль кеторолака (поставляемого под торговой маркой ToradolTM)) и стероидные противовоспалительные средства, противогрибковое средство, дезинтоксифицирующее средство (например, при клизмах, вводимых ректально), аналгезирующее средство, бронхолитическое средство, антибактериальное средство, антибиотики, средства для лечения сосудистой ишемии (например, диабетов и болезни Бергера), моноклональное антитело, миноксидил для наружного употребления для роста волос, мочегонные средства, например фуросемид, (поставляемый под торговой маркой ЛазиксTM)), иммунодепрессанты (например, циклоспорины), лимфокины (такие, как интерлейкин-2 и т.п.), альфа- и бета интерферон и т.п., и
(b) достаточное количество гиалуроновой кислоты, и/или ее солей (например, натриевой соли), и/или гомологов, аналогов, производных, комплексов, сложных эфиров, фрагментов, и/или субъединиц гиалуроновой кислоты, предпочтительно гиалуроновой кислоты и ее солей, при этом указанное количество должно быть достаточным для облегчения проникновения лекарственного средства через ткань (включая рубцовую ткань) в месте обработки и через клеточные мембраны в целевые клетки.
Предпочтительно, если (a) и (b) вводят одновременно и в одно и то же место, например, одно средство вводят внутривенно, а другое - с обратной стороны.
В соответствии с очередным вариантом осуществления настоящее изобретение относится к способу лечения состояний или заболеваний у млекопитающих, заключающемуся во введении указанным млекопитающим терапевтически эффективного нетоксичного количества композиции, содержащей терапевтически эффективное количество лекарственного и/или терапевтического средства для лечения заболевания или состояния, такого как акцептор свободных радикалов (напр., аскорбиновая кислота - витамин C), витамин C (для лечения мононуклеоза), противораковое средство, химиотерапевтическое средство, противовирусные средства (например, неионогенное ПАВ, такое как ноноксинол-9 [нонилфеноксиполиэтокси-этанол), имеющееся в контрацептивной пасте DelfenTM)), анионогенные ПАВ (напр. , хлорид пиридиния) и катионогенные ПАВ (напр. , хлорид бензалкония), нестероидные противовоспалительные средства (НСПВС), например индометацин, напроксен и (+/-)трометаминовая соль кеторолака (поставляемого под маркой ToradolTM)) и стероидные противовоспалительные средства, противогрибковое средство, дезинтоксифицирующие средства (например, при клизмах, вводимых ректально), аналгетики, бронхолитические средства, антибактериальные средства, антибиотики, средства для лечения сосудистой ишемии (например, при диабетах и болезни Бергера), моноклональное антитело, миноксидил для местного употребления для роста волос, диуретики, например, фуросемид (поставляемый под торговой маркой ЛазиксTM)), иммунодепрессанты (например, циклоспорины), лимфокины (такие, как интерлейкин-2 и т. п.), альфа- и бета-интерферон и т.п., которые вводятся вместе с некоторым количеством (или в некоторое количество гиалуроновой кислоты) и/или ее солей, например натриевой соли и/или гомологов, аналогов, производных, комплексов, сложных эфиров, фрагментов, и/или субъединиц указанной гиалуроновой кислоты, предпочтительно, гиалуроновой кислоты и ее солей, достаточное для облегчения проникновения лекарственного средства через ткань (включая рубцовую ткань) в месте обработки через клеточные мембраны в отдельные целевые клетки.
В соответствии со следующим вариантом осуществления настоящее изобретение относится к доставке терапевтически эффективного количества лекарственного и/или терапевтического средства для лечения заболевания или состояния у млекопитающего к целевому участку; причем указанная доставка заключается во введении терапевтически эффективного нетоксичного лекарственного и/или терапевтического средства, например, такого как свободно-радикальный акцептор (например. , аскорбиновая кислота), витамин C (для лечения мононуклеоза), противораковое средство, химиотерапевтическое средство, противовирусные средства (например, неиногенное ПАВ, такое как ноноксинол-9 [нонилфеноксиполиэтокси-этанол] , имеющееся в контрацептивной пасте DelfenTM)), анионогенные ПАВ (напр, хлорид пиридиния) и катионогенные ПАВ (напр. , хлорид бензалкония), нестероидные противовоспалительные средства (НСПВС), например индометацин, напроксен и (+/-)трометаминовая соль кеторолака (поставляемого под маркой ToradolTM)), и стероидные противовоспалительные средства, противогрибковое средство, дезинтоксифицирующие средства (например, при клизмах, вводимых ректально), аналгетики, бронхолитические средства, антибактериальные средства, антибиотики, средства для лечения сосудистой ишемии (например, при диабетах и болезни Бергера), моноклональное антитело, миноксидил для местного употребления для роста волос, диуретики, например фуросемид, (поставляемый под торговой маркой ЛазиксTM)), иммунодепрессанты (например, циклоспорины), лимфокины (такие, как интерлейкин-2 и т. п.), альфа- и бета-интерферон и т.п., которые вводятся вместе с некоторым количеством или в некоторое количество гиалуроновой кислоты и/или ее солей (например, натриевой соли и/или гомологов, аналогов, производных, комплексов, сложных эфиров, фрагментов, и/или субъединиц указанной гиалуроновой кислоты и ее солей, достаточное для облегчения проникновения лекарственного средства через ткань (включая рубцовую ткань) в месте обработки через клеточные мембраны в отдельные целевые клетки.
Таким образом, согласно другому варианту осуществления настоящее изобретение относится к использованию комбинации или композиции, предназначенных для лечения заболевания или состояния и включающих в себя терапевтически эффективное нетоксичное
количество лекарственного и/или терапевтического средства для лечения состояния или заболевания, такого как свободнорадикальный акцептор (например, аскорбиновая кислота, витамин C) витамин C (для лечения мононуклеоза), противораковое средство, химиотерапевтическое средство, противовирусные средства (например неионогенное ПАВ, такое, как ноноксинол-9 [нонилфеноксиполиэтокси- этанол] имеющееся в контрацептивной пасте DelfenTM)), анионогенные ПАВ (напр. , хлорид пиридиния) и катионогенные ПАВ (напр. , хлорид бензалкония), нестероидные противовоспалительные средства (НСПВС), например индометацин, напроксен и (+/-) трометаминовая соль кеторолака (поставляемого под маркой ToradolTM)) и стероидные противовоспалительные средства, противогрибковое средство, дезинтоксифицирующие средства (например, при клизмах, вводимых ректально), аналгетики, бронхолитические средства, антибактериальные средства, антибиотики, средства для лечения сосудистой ишемии (например, при диабетах и болезни Бергера), моноклональное антитело, миноксидил для местного употребления для роста волос, диуретики, например фуросемид, (поставляемый под торговой маркой ЛазиксTM)), иммунодепрессанты (например, циклоспорины), лимфокины (такие, как интерлейкин-2 и т. п)., альфа- и бета-интерферон и т.п., которые вводятся вместе с некоторым количеством (или в некоторое количество гиалуроновой кислоты), и/или ее солей (например, натриевой соли), и/или гомологов, аналогов, производных, комплексов, сложных эфиров, фрагментов, и/или субъединиц указанной гиалуроновой кислоты предпочтительно, гиалуроновой кислоты и ее солей, достаточное для облегчения проникновения лекарственного средства через ткань (выключая рубцовую ткань) в месте обработки через клеточные мембраны в отдельные целевые клетки.
Авторы настоящей заявки утверждают, что гиалуроновая кислота, и/или ее соли, и/или гомологи, аналоги, производные, комплексы, сложные эфиры, фрагменты и/или субъединицы гиалуроновой кислоты облегчают перенос лекарственного средства к месту обработки и проникание этого средства через ткань (включая рубцовую ткань) и через все клеточные мембраны, обеспечивая попадание в отдельные целевые клетки.
Для иллюстрации облегчения доставки или переноса химического средства в целевой участок в организме млекопитающего проводили эксперимент, в котором непосредственно в опухоль вводили этиловый спирт, после чего делали ультразвуковой анализ, который показал, что введенный спирт не был диспергирован по всей опухоли. Затем в опухоль вводили этиловый спирт вместе с гиалуроновой кислотой и/или ее солями, и после соответствующего ультразвукового анализа убедились, что этиловый спирт был диспергирован по всей опухоли.
Хотя заявители предполагают, что гиалуроновая кислота облегчает перенос и доставку лекарственного средства, однако настоящее изобретение может быть использовано независимо от рассматриваемого способа действия гиалуроновой кислоты, и/или ее солей, и/или ее гомологов, аналогов, производных, комплексов, сложных эфиров, фрагментов и субъединиц.
Комбинация гиалуроновой кислоты и ее солей и других форм с различными химическими веществами и лекарственными средствами, например, витамином C, противоракового средства и т.п. способствует изменению их распределения и клиническому эффекту в человеческом организме и обеспечивает направленную доставку препарата к неперфузировнной ткани и/или патологической ткани. Например, использование аскорбиновой кислоты (витамин C) в качестве свободнорадикального акцептора (50 г в день - 1000-кратная дневная доза, используемая в терапевтических целях как витамин), введенного внутривенно вместе с 300 - 500 мг гиалуроновой кислоты (гиалуронат натрия) вызывало немедленное стихание боли в кости и мускульной боли и снижало воспалительную реакцию у больных раком. Гиалуроновая кислота повышает противоопухолевую активность и действие аскорбиновой кислоты. Очевидно, что вследствие этой повышенной активности свободные радикалы удаляются благодаря действию акцептора свободных радикалов. В любом случае, пациент чувствует себя лучше. Аналогичное явление имеет место при использовании фуросемида и гиалуроновой кислоты, где активность фуросемида возрастает незначительно, если эту комбинацию вводить в "нормальный" организм, но эта активность сразу сильно возрастала, когда указанную комбинацию вводили пациенту с неполностью перфузированной почкой или с недостаточной функцией почки, обусловленной недостаточным внутрисосудистым объемом.
Аналогичная ситуация возникала и при эксперименте с (НСПВС). Поскольку требовалось большое количество нерастворимого индометацина, то химический продукт солюбилизировали с использованием н-метилглюкамина при разведении 5 мг/мл н-метилглюкамина (НМГ). Затем это вещество пропускали через 22-мкм миллипористый фильтр для получения стерильности. Этот материал является нетоксичным при 16-кратной терапевтической дозе, и из этих соображений его сочли подходящим для использования на человеке. Так, например, ИндоцидTM, солюбилизированный в НМГ, вводили человеку либо в опухоль (интраперитонально, интраплеврально, либо интраваскулярно) в различных дозах вплоть до 10 мг/кг, где каждую дозу индаметацина комбинировали с 200 - 1000 мг гиалуроновой кислоты, например "LifeCoreTM", гиалуронат натрия, разбавленной в первоначальном растворе индометацина и НМГ, например с "LifeCoreTM". В результате получали соответствующую смесь, которая может быть надежно введена любым стандартным способом. Аналогичные клинические исследования были проведены с гиалуроновой кислотой, полученной другими способами, т.е. путем экстракции. Экстрагированный материал предпочтительно использовать для введения в опухоль, внутрибрюшинно или внутриплеврально.
Таким образом, в соответствии с настоящим изобретением, когда (НСПВС), например индометацин, растворенный в н-метилглюкамине, или другой (НСПВС) вводили вместе с гиалуроновой кислотой в количестве, превышающем 200 мг на 1-2 мг/кг веса тела (НСПВС) (в одном случае вводили индометацин и НМГ), то при этом не наблюдалось никаких побочных явлений или интоксикаций, таких как желудочно-кишечные расстройства, неврологические отклонения, депрессия и т. п., даже при повышенных количествах индометацина (если это необходимо). Когда количество гиалуроновой кислоты снижалось ниже указанного количества, то побочные явления возникали вновь. Кроме того, повышенная реакция, наблюдаемая при комбинировании (НСПВС) (например ИндоцидTM) с гиалуроновой кислотой, ясно иллюстрирует, что указанная комбинация обеспечивает направленную доставку лекарственного средства к патологической ткани, даже если это лекарственное средство вводится стандартной внутривенной инъекцией. Так, например, больному, наблюдаемому по поводу ракового заболевания, помимо других химических веществ (например, витамина C, флоретина и противораковых лекарственных средств), вводили 50 - 200 мг (НСПВС-гилуроновой кислоты) гиалуронат натрия, например индометацин, и гиалуроновую кислоту, в результате чего сразу исчезали боли. Затем за короткий промежуток времени наблюдалось рассасывание злокачественных опухолей с улучшением функций легких и печени, если опухоль присутствовала в этих органах. Так, например, при гибели опухолевых клеток дербис и опухолевые токсины значительно лучше удаляются организмом посредством действия макрофагов, активность которых возрастает при добавлении НСПВС (нестероидного антивоспалительного средства), вводимого вместе с гиалуроновой кислотой (или ее солью, или другой ее формой). Таким образом, заявители считают, что добавление (НСПВС) нестероидных противовоспалительных средств с гиалуроновой кислотой (например, гиалуронатом натрия) способствует разблокированию макрофагов путем предупреждения продуцирования простагландина, блокирующего функцию макрофага. Отсюда можно заключить, что гиалуроновая кислота (и ее соль, и ее другие формы) не только повышает активность (НСПВС), но и также снижает побочное действие и токсичность, ассоциируемые с использованием ингибиторов синтеза простагландина.
Примерами подходящих химиотерапевтических средств являются новантрон Митоксантрон, метотрексат, 5-FU (5-фторурацил), карбоплатина, метил CCNU, вводимый перорально, и Митомицин C.
В одном случае метотрексат вводили вместе с гиалуроновой кислотой на поверхность опухолевой ткани, например, в области грудной клетки, в течение 5-7 дней последовательно. Гематологические показатели пациента были снижены, по крайней мере, по сравнению с результатами, полученными с такими же дозами метотрексата, вводимыми внутривенно или перорально.
Кроме того, во многих случаях при разрушении опухоли после описанного ранее лечения печень часто не может справляться с выводом опухолевых токсинов, дебриса и клеточных остатков, что приводит пациента к смерти. В данном случае можно использовать не только гиалуроновую кислоту с соответствующим (НСПВС), но и вводить гиалуроновую кислоту (гиалуронат натрия) с дезинтоксифицирующим средством в толстую кишку при помощи клизмы.
Гиалуроновая кислота и ее соли могут быть использованы в различных дозах от 10 до 1000 мг на 70 кг веса тела, при этом оптимальная доза соответствует 50 - 350 мг на 70 кг веса тела человека. Поскольку гиалуроновая кислота не является токсичной, то она может быть введена и в избыточной дозе (например, 3000 мг на 70 кг веса тела), и при этой дозе она не дает побочных эффектов.
Таким образом, в настоящем изобретении комбинируют гиалуроновую кислоту и/или ее соли с цитотоксичным химиотерапевтическим средством (например, либо гиалуроновую кислоту вводят непосредственно за указанным лекарственным средством), если они не могут быть предварительно смешаны, либо их смешивают перед введением. Авторы настоящей заявки использовали, например, адриамицин, который вводили перед гиалуроновой кислотой, метотрексат, причем эти два агента смешивали вместе, митомицин C, блеомицин, 5-фторурацил, новантрон, карбо- и цис-платину, и во всех последних случаях лекарственное средство смешивали непосредственно с гиалуроновой кислотой в дозе 10 мг на мл гиалуроновой кислоты, повышая общую дозу до 100 мл с использованием стандартной дозы данного лекарственного средства.
Как указывалось ранее, заявители использовали в качестве лекарственных средств флоридзин, флоретин и 5-дезоксиглюкоронид флоридзина вместе с диметилсульфоксидом для конкурентного блокирования транспорта глюкозы в неопластические клетки. Указанные лекарственные средства могут быть также объединены с гиалуроновой кислотой в аналогичных дозах по отношению к уже упомянутым лозам для химиотерапевтических средств, где флоретин является солюбилизированным, например, агентом N-метилглюкамином.
Так, например, схема лечения различных опухолевых заболеваний может включать в себя введение аскорбиновой кислоты и онкостатина IV, комбинацию флоретина, солюбилизированного в N-метилглюкамине, со смесью гиалуроновой кислоты или ее соли с использованием дозы 2 - 4 г флоретина, солюбилизированного как описано выше, с 30 мг - 1000 мг или выше (избыточная доза) гиалуроновой кислоты или ее натриевой соли. Указанная лекарственная схема позволяет значительно увеличить проникновение лекарственного средства в опухолевые клетки, а значит и продуцировать гораздо лучший результат, особенно когда опухоли лишаются глюкозы, а затем подавляются либо с помощью гипертермии, химиотерапии и/или радиоактивного облучения. Аналогично, уже упомянутые цитотоксичные химиотерапевтические средства комбинировали со сравнимыми дозами гиалуроновой кислоты и/или ее солей и вводили либо внутривенно, внутриартериально, внутрибрюшинно, либо внутриплеврально или непосредственно в опухоль путем инъекции иглой при ультразвуковом контроле направления или СТ-контролем.
Комбинация других лекарственных средств с гиалуроновой кислотой и/или ее солями может быть также введена чрескожно, например, инсулин при диабете, эстроген при менопаузах у женщин, прогестерон для контроля фертильных функций и антиметаболиты для предупреждения местной инфекции, например угрей, вызываемых дифтерийной бактерией. Эти средства могут быть также использованы совместно с гиалуроновой кислотой.
Внутривенное введение бронхолитических средств, например аминофиллина и теофиллина, также может быть осуществлено совместно с гиалуроновой кислотой и/или ее солями.
В результате введения бронхолитических средств вместе с гиалуроновой кислотой наблюдалось улучшение действия указанных лекарственных средств. Пероральное введение лекарственных средств вместе с гиалуроновой кислотой также может быть использовано.
Согласно одному из вариантов осуществления настоящее изобретение относится к комбинации неионогенного ПАВ (например, ноноксинол-9 [нонилфенокси-полиэтокси-этанол], содержащийся в DelfenTM контрацептивной пасте) и гиалуроновой кислоты и/или ее солей и других форм, которая предназначена для лечения:
(a) заболеваний, вызываемых вирусом простого герпеса типа I и типа II
(b) опоясывающего лишая
с последующим неожиданно быстрым исчезновением симптомов и поражений ткани.
Неионогенный ПАВ предпочтительно содержит либо эфирную, либо амидную связь между гидрофильной и гидрофобной частями молекулы и является более активным, чем ПАВ, имеющие сложноэфирные связи или связи простой эфир - сложный эфир.
Ниже предлагается на рассмотрение неионогенные ПАВ и идентифицированные связи:
Поверх.-активное вещество (Отсутствует контрольный вирус) - Связь
5% ноноксинол-9 (нонилфенокси-полиэтокси-этанол) - Прос.эфирная
1% Тритон Х-100 (п-диизобутилфенокси-полиэтокси-этанол) - Прос.эфирная
1% Brij-97 (полиоксиэтилен(10)олеиловый эфир) - Прос.эфирная
1% Спан-20 (сорбитранмонокламат) - Сложноэфирная
1% Спан-80 (сорбитанмоноолеат) - Сложноэфирная
1% Твин-20 (полисорбат 20) - Простой эфир-Сложный эфир
1% Твин-80 (полисорбат 80) - Пр.эфир-слож. эфир
1% Ониксол 345 - Амидная
Если в тело человека вводят чужеродные объекты, например, дренажные трубки, которые должны быть там оставлены для дальнейшего использования, то крайне необходимо, чтобы окружающие имплантат ткани не были инфицированы, поскольку, если они становятся инфицированными, то обычно, сколько бы не было затем введено антибиотиков, эта инфекция не исчезает и имплантат должен быть удален. Однако заявители обнаружили, что если инфицированные ткани, окружающие имплантат, обработать антибиотиком, включенным в гиалуроновую кислоту (гиалуронат натрия), то инфекция быстро пропадает и удалять имплантат нет необходимости.
Авторами настоящей заявки также было обнаружено, что при лечении сосудистой ишемии (например, у больных раком, где опухолевая ткань недостаточно перфузирована, у больных диабетом или болезнью Бергера) введение лекарственных средств в гиалуроновой кислоте гиалуроната натрия приводит к усилению ответа на лекарственное средство.
У пациентов, страдающих опухолями головного мозга, размеры опухоли снижаются. Введение диметилсульфоксида (ДМСО) в количествах менее 100 г в день в 10% растворе в гиалуроновой кислоте (гиалуроната натрия) 300 - 500 мг способствует снижению острого отека мозга и спиномозгового отека.
Для лечения мононуклеоза заявители успешно вводили пациенту, страдающему от клиномании в течение некоторого периода времени, витамин C и гиалуроновую кислоту, в результате чего пациент быстро выздоровел.
Одна форма гиалуроновой кислоты и/или ее соли, например натриевой соли, и ее гомологов, аналогов, производных, комплексов, сложных эфиров, фрагментов и субъединиц, а предпочтительно гиалуроновой кислоты и ее солей, подходящих для использования в настоящем изобретении, являлась фракцией, поставляемой Sterivet Laboratories Limited. Одна такая фракция представляла собой 15-мл ампулу с гиалуронатом натрия 20 мг/мл (300 мг на ампулу - Lot 2F3). Фракция гиалуроната натрия представляла собой 2% раствор со средней молекулярной массой около 225000. Эта фракция также содержала воду (дост. кол. ), трижды дистиллированную и стерилизованную в соответствии с требованиями фармакопеи США для изготовления препаратов для инъекций. Ампулы с гиалуроновой кислотой и/или ее солями могут быть изготовлены из боросиликатного стекла Типа 1, закрывающимися пробкой из материала, не вступающего в реакцию с содержимым ампулы.
Фракция гиалуроновой кислоты и/или ее солей, например натриевой соли, и гомологов, аналогов, производных, комплексов, сложных эфиров, фрагментов и субъединиц гиалуроновой кислоты, а предпочтительно гиалуроновой кислоты и ее солей, имеет следующие характеристики:
(a) очищенная, в основном, не содержащая пирогена фракция гиалуроновой кислоты, полученная из натурального источника, имеет по крайней мере одну характеристику, выбранную из группы, включающей в себя:
i) молекулярную массу в пределах 150000-225000;
ii) менее, чем около 1,25% сульфатированных мукополисахаридов по полной массе;
iii) менее, чем около 0,6% белка по полной массе;
iv) менее, чем около 150 ppm железа по полной массе;
v) менее, чем около 15 ppm свинца по полной массе;
vi) менее, чем 0,0025% глюкозамина;
vii) менее, чем 0,025% глюкуроновой кислоты;
viii) менее, чем 0,025% N-ацетилглюкозамина;
ix) менее, чем 0,0025% аминокислот;
x) коэффициент УФ-экстинкции при 257 нм - менее, чем около 0,275;
xi) коэффициент УФ-экстинкции при 280 нм - менее, чем около 0,25; и
xii) pH в пределах 7,3-7,9.
Предпочтительно, если гиалуроновая кислота смешивается с водой, а фракция гиалуроной кислоты имеет среднечисловую молекулярную массу в пределах 150000-225000. А более предпочтительно, если фракция гиалуроновой кислоты включает в себя, по крайней мере, одну характеристику, выбранную из группы, включающей в себя следующие характеристики:
i) менее, чем около 1% сульфатированных мукополисахаридов по полной массе;
ii) менее, чем около 0,4% белка по полной массе;
iii) менее, чем около 100 ppm железа по полной массе;
iv) менее, чем около 10 ppm свинца по полной массе;
v) менее 0,00166% глюкозамина;
vi) менее 0,0166% глюкуроновой кислоты;
vii) менее 0,0166% N-ацетилглюкозамина;
viii) менее 0,00166% аминокислот;
x) Коэффициент УФ-экстинкции при 257 нм - менее, чем около 0,23;
xi) Коэффициент УФ-экстинкции при 280 нм - менее, чем 0,19;
xii) pH в пределах 7,5-7,7.
Другие формы гиалуроновой кислоты и/или ее солей и гомологов, производных, комплексов, сложных эфиров, фрагментов и субъединиц гиалуроновой кислоты могут быть выбраны от других поставщиков (см., например, описания прототипов, указанных выше). Кроме того, авторы настоящей заявки успешно использовали гиалуронат натрия, получаемый и поставляемый LifeCoreTM Biomedical, Инк., который имеет следующие характеристики:
Внешний вид - частицы окрашены от белого до кремового цвета;
Запах - ощутимого запаха не имеет;
Средне-вязкостная молекулярная масса < 750 000 Дальтон;
УФ/визуальное сканирование, 190-820, - согласованная развертка;
Оптич. плотность ОП, 260 нм - 0,25 ед.ОП;
Гиалуронидазная чувствительность - положительная реакция;
ИК-сканирование - согласованная развертка;
pH, 10 мг/г раствора - 6,2-7,8;
Вода - макс. 8%;
Белок - < 0,3 мкг/мг NaHy;
Ацетат - < 10,0 мкг/мг NaHy;
Тяжелые металлы, ppm макс. кол. : As 2,0; Cd 5,0; Cr 5,0; Co 10,0; Cu 10,0; Fe 25,0; Pb 10,0; Hg 10,0; Ni 5,0;
Микробные биовключения - не наблюдались;
Эндотоксин - < 0,07 ед./мг NaHy;
Биологический тест на токсичность - глазной тест на токсичность проводили на кроликах.
В следующих работах описываются источники гиалуроновой кислоты, способы ее получения и выделения.
В патенте США 4141973 описываются фракции гиалуроновой кислоты, включая соли натрия, которые имеют:
"(a) среднюю молекулярную массу, превышающую около 750000, а предпочтительно, превышающую около 1200 000, то есть предельную вязкость свыше около 1400 см3/г, а предпочтительно свыше около 2000 см3/г;
(b) содержание белка менее 0,5 мас.%;
(c) поглощение УФ-излучения 1% раствора гиалуроната натрия составляет менее 3,0 при 257 нм, и менее 2,0 при 280 нм;
(d) кинематическая вязкость 1% раствора гиалуроната натрия в физиологическом буфере составляет более, чем около 1000 сантистокс, а предпочтительно, более чем 10000 сС;
(e) молярное оптическое вращение 0,1 - 0,2% раствора гиалуроната натрия в физиологическом буфере составляет менее -11•103 град. - см2/М дисахарида, измеренное при 220 нм;
(f) отсутствие какой-либо заметной инфильтрации стекловидного тела и передней камеры глаза, отсутствие также какой-либо воспалительной гиперемии во внутриглазной жидкости, отсутствие также помутнения или гиперемии стекловидного тела и никаких патологических изменений роговицы, хрусталика глаза, радужной оболочки глаза, сетчатки и сосудистой оболочки глаза обезьяны дурукули, когда в стекловидное тело приблизительно вместо половины жидкого вещества стекловидного тела HUA вводили 1 мл 1%-ного раствора гиалуроната натрия, растворенного в физиологическом буфере;
(g) стерильность и отсутствие пирогена;
(h) отсутствие антигенных свойств."
В описании канадского патента 1205031, который относится к патенту США 4141973 как прототип, обсуждаются фракции гиалуроновой кислоты, имеющие средние молекулярные массы от 50000 до 100000; 250000 до 350000 и от 500000 до 730000, и способы их получения.
Если используется высокомолекулярная гиалуроновая кислота или ее соли или другие формы, то для осуществления введения ее в организм и гарантии от внутримышечной коагуляции ее необходимо разбавить.
Одна из композиций аскорбиновой кислоты - витамин C для инъекций в соответствии с требованиями USP производится Steris Laboratories, Инк., Феникс, Аризона, 85043 США и содержит 22 мг/мл экв. аскорбату натрия 250 мг/мл в 30 мл, 50 мл или 100 мл отдельных упаковках, однако, предпочтительной является 35-мл упаковка.
Так, например, авторы настоящей заявки комбинировали гиалуроновую кислоту и гиалуронат натрия и/или другие ее формы с лекарственными и/или терапевтическими средствами для лечения состояний и заболеваний, получая при этом неожиданные результаты. (см. табл. 1).
В частности, что касается лечения рака, то согласно настоящему изобретению был получен способ лечения и комбинации лекарственных и химических средств, с помощью которых повышается предполагаемая продолжительность жизни пациента и психологический тонус пациента даже, если пациент оказывается резистентным к стандартному лечению. Авторы настоящей заявки успешно проводили лечение пациентов, у которых в результате лечения наблюдалось увеличение скорости распада опухоли, улучшение функции макрофагов, повышение способности организма к удалению опухолевых клеток, продуктов опухолевого распада, дебриса и токсинов.
Примеры.
Для иллюстрации настоящего изобретения ниже представлены примеры. В основном, во всех случаях лечения рака, это лечение проводили у пациентов, которые оказались невосприимчивыми к стандартному лечению. В приведенных примерах лечения гиалуроновую кислоту также использовали и в других формах, например, в виде гиалуроната натрия.
Случай I.
Больной, 59 лет с эпидермоидом гортани (сквамозный тип опухоли) подвергался первичному лечению хирургическим способом в сочетании с облучением, затем через 7 лет появились метастазы в печени. Были отмечены две большие опухоли 12 см и 6 см в диаметре. После чего лечился методом комбинации системной химиотерапии с добавлением ДМСО для усиления проникновения лекарственных средств, флоретина, солюбилизированного N-метилглюкамидом с добавленным ДМСО для лучшего проникновения и непосредственного введения адриамицина, карбоплатины и метотрексата в опухоль путем общей и внутриопухолевой инъекции, но в этом случае с добавлением гиалуроновой кислоты в дозе 10 - 60 мг для различных лекарственных средств. Побочных эффектов не наблюдалось и через 4 недели пациент был снова обследован. К этому времени меньшая опухоль исчезла полностью. Более крупная опухоль обнаруживала лишь некротический очаг 5 см в диаметре, но без видимого наличия опухоли, что было установлено путем пункционной биопсии. Этот случай иллюстрирует прекрасное действие гиалуроновой кислоты в роли поставщика лекарственного средства к опухоли, что способствует ее деструкции.
Последующие результаты.
Затем пациенту вводили 300 мг индометацина и 300 мг гиалуроновой кислоты ежедневно; после чего пациент имел ремиссию, однако позднее пациент умер от инфекционного заболевания.
Случай II.
Женщина, 42 года, с развитой злокачественной меланомой в верхней части левого бедра, с утолщенными паховыми лимфоузлами, узлами в брюшной полости, печени, легких и основании головного мозга, включая черепно-мозговые нервы. Первичная опухоль была удалена, после чего имел место рецидив, который не поддавался воздействию цитотоксичной или цитостатической химиотерапии, поскольку такая широко распространившаяся опухоль, какая наблюдалась у пациентки, считается неизлечимой. Лечение проводили с помощью комбинации флоретина, солюбилизированного в N-метилглюкамине с добавленной гиалуроновой кислоты,в дозе 10-50 мг/2 - 4 г, вводимой внутривенно, и указанное лекарственное средство вводили в течение 5 дней на протяжении 4-24 час, день. При этом пациентка получала термотерапевтическое лечение, применяемое к различным областям опухоли, и сопутствующую системную терапию с использованием карбоплатины с добавленной гиалуроновой кислотой в дозе 250 мг карбоплатины плюс метил CCNU, введенный в полной дозе 120 мг; это средство пациентка получала перорально в течение 5 дней, при этом она систематически принимала гиалуроновую кислоту. Метотрексат, смешанный с гиалуроновой кислотой, инъецировали в опухоль, которая пальпировалась в левом бедре или паховой области, в дозе 37,5 мг с добавленными 60 мг гиалуроновой кислоты, эти дозы делили на две равные инъекции, вводимые в два дня. После этого у пациентки (через 10-20 дней) наблюдалась резкая и полная регрессия опухолей в верхнем бедре и паховой области, резкое улучшение функции печени, опухоль которой становилась кистообразной, что обычно рассматривается как свидетельство распада опухоли и исчезновение опухоли в легких. Опухоль основания головного мозга также обнаруживала регрессию, о чем свидетельствовало улучшение функции черепных нервов и снижение головных болей. У этой пациентки опухолевое заболевание было невосприимчиво к большинству лекарственных средств, и на этой стадии болезни, благодаря проведенному лечению, вдруг стала развиваться восприимчивость к тем же самым лекарственным средствам, но использованным в сочетании с гиалуроновой кислотой, которая, как очевидно из этого примера, действует как агент-поставщик лекарственного средства.
Последующие результаты
Пациентка получала затем лечение флоретином, индометацином (НСПВС) и гиалуроновой кислотой. После чего наступила стойкая ремиссия.
Случай III.
Больная, 55 лет, страдающая раком желчного пузыря, при этом опухолью была поражена вся правая доля печени. Ранее проводили 3-кратное повторное лечение с помощью химиотерапии с добавлением (ДМСО), флоретином с добавлением (ДМСО) и непосредственным введением цитотоксичных средств с добавлением (ДМСО), а также в сочетании с термотерапией. Начиная с мая 1989 г., пациентка получала лечение с теми же лекарственными средствами, но с добавлением гиалуроновой кислоты в качестве носителя или диспергатора, которые вводили системно и непосредственно путем инъекции в опухоль. Опухоль уменьшалась по краям приблизительно на 20% от ее первоначальных размеров, а затем начала резко уменьшаться до 50%-ного размера от первоначального, и продолжала уменьшаться далее. Эта опухоль была ранее невосприимчива к введению лекарственных средств, используемых в чистом виде и вводимых стандартным способом.
Последующие результаты
К несчастью, опухоль рецидивировала, и пациентка умерла.
Случай IV.
Пациентка, 55 лет, с раком толстой кишки с метастазами в печень, которые представляли собой одну большую опухолевую массу, занимающую всю правую долю печени и средний сегмент левой доли, распространяясь на 1 левую долю. Опухоль классифицировалась хирургами как неоперабельная. Пациентка двумя месяцами ранее получала лечение с помощью системной химиотерапии и инъекции прямо в опухоль химиотерапевтических средств и флоротина, солюбилизированного N-метилглюкамином с гиалуроновой кислотой, а также сопутствующее лечение гипертермией. Пациентка проходила трехдневный курс терапии и получала инъекции непосредственно в опухоль, которые содержали цитотоксичные средства и гиалуроновую кислоту и через три недели после этого была обследована. Ультразвуковое обследование показало полное разжижение опухоли лишь с небольшим валиком видимой живой ткани; после дренажа образовавшейся кистообразной ткани получали 500 см3 желтой жидкости с некротическими остатками опухоли. Это необычный результат для аденокарциномы, которая, как известно, дает очень медленную реакцию на введение лекарственного средства. Как было установлено, 30% пациентов с таким заболеванием обнаруживают прогрессирование болезни при лечении стандартной цитотоксичной или цитостатической химиотерапией. Повышенная деструкция опухоли, имеющая место в течение трех недель, очевидно, обусловлена действием гиалуроновой кислоты как носителя лекарственного средства.
Последующие результаты
Обследование показало полный некроз опухоли. Однако пациентка умерла некоторое время спустя от печеночной недостаточности и эмболии легких.
Случай V.
Пациент, 53 года, с переходно-клеточным раком мочевого пузыря в запущенной форме болезни с метастазами во всей левой области таза и распространившимися узлами в периферические области аорты, панкреатической области и надключичной области, перенес хирургическую операцию в сочетании с облучением, однако, болезнь рецидивировала; и проведение стандартной химиотерапии не показало заметного улучшения. Больному было назначено лечение с использованием флоретина, солюбилизированного в N-метилглюкамине с добавлением гиалуроновой кислоты, в сочетании с непосредственной инъекцией карбоплатины и метотрексата в опухолевую ткань. Также применялась гипертермия областей опухоли. В результате этого лечения у пациента наблюдался резкий ответ с фебрильной реакцией, вследствие распада опухоли и высвобождения бактерий. Эта реакция регулировалась антибиотиками с соответствующей гидратацией, и наблюдение пациента в этой фазе показало уменьшение размера опухоли, которое происходило почти ежедневно, и через 7 дней после лечения опухоль уменьшилась наполовину. Этот результат тем более замечателен, что болезнь находилась в стадии невосприимчивости ко всем средствам лечения, и только использование гиалуроновой кислоты в сочетании с лекарственными средствами, блокирующими транспорт глюкозы, и использование гиалуроновой кислоты в качестве носителя химиотерапевтического средства, вводимого непосредственно в опухоль, дало хороший результат.
Последующие результаты.
В результате наблюдался полный некроз опухоли. Однако, пациент умер от инфекции.
Случай VI.
Пациент с диагнозом опухоли верхней правой доли, подтвержденным биопсией, и опухоль классифицировалась как неоперабельная. Согласно истории болезни химиотерапия и облучение не дали никаких результатов. После чего пациент был подвергнут системной химиотерапии с использованием гиалуроновой кислоты (см. табл. 2).
Пациент также получал лечение флоретином в гиалуроновой кислоте. В опухоль вводили инъекцию химиотерапевтических средств в гиалуроновой кислоте, представленных в табл. 3.
В результате, опухоль, которая не поддавалась лечению обычными средствами, уменьшилась на 50%. Это свидетельствует о том, что невосприимчивые к обычному лечению опухоли могут давать реакцию на введение химиотерапевтических средств в сочетании с гиалуроновой кислотой и/или ее солей, взятыми в качестве носителя для указанных лекарственных средств.
Случай VII.
Пациентка, 58 лет, страдающая обширным раком груди с пальпируемыми узлами в надключичной области и увеличенными вспомогательными лимфоузлами. Диагноз подтверждался биопсией. Пациентка получила комбинированное системное терапевтическое и гипертермическое лечение, но без заметных улучшений. Затем она была подвергнута облучению, начиная с декабря 1988, до января 1989 г. Обследование, проведенное д-ром Фоком 17 мая 1989 г, показало, что лечение не дало существенных результатов. Затем стал развиваться массивный экссудат. Д-р Фок назначил лечение комбинацией химиотерапевтических средств с гиалуроновой кислотой (см. табл. 4).
В качестве гиалуроновой кислоты может быть использован гиалуронат натрия.
Пациентке также делали плевральную пункцию с последующей инстилляцией 5-фторурацила, митомицина C и гиалуроновой кислоты в грудную полость. Плевральный экссудат полностью исчез. Опухоль в груди продолжала уменьшаться, а аденопатия в надключичной области и во вспомогательных лимфоузлах полностью исчезла.
Эта пациентка обнаруживала ответ на относительно низкие дозы гиалуроновой кислоты и/или ее солей, добавляемых к стандартным химиотерапевтическим средствам, которые систематически вводили в опухоль и путем внутриплевральной инстилляции. Ответная реакция повышалась при использовании флоретина в синацидеTM (гиалуроновая кислота и/или ее соли), вводимых одновременно.
Последующие результаты.
Обследование через большой промежуток времени показало стойкую ремиссию.
Случай VIII.
Женщина, 62 года, ранее лечилась с использованием системной химиотерапии, с комбинацией двух различных лекарственных средств, но безрезультатно. Пациентке было назначено лечение, включающее гипертермию и прямую химиотерапевтическую инъекцию, к которому, начиная с сентября, начала появляться ответная реакция.
В апреле-мае было отмечено увеличение опухоли в правой верхней доле легкого. Эта опухоль представляла собой анапластическую мелкоклеточную карциному. Опухоль обрабатывали путем инъекции в место поражения блеомицина с гиалуроновой кислотой и индометацина с гиалуроновой кислотой. Пациентке также систематически вводили 300 мг с 300 мг гиалуроновой кислоты в день. После радиологического лечения через 2 - 4 недели наступило резкое улучшение. Последний рентгеновский снимок показал, что левая половина грудной клетки очистилась. С правой стороны
признаков плевральной реакции не наблюдалось. Сравнение с предыдущими снимками показало, что масса опухоли значительно уменьшилась в размере, но точно на этом снимке определить размеры не удавалось.
Заявители считают, что полученный результат является следствием введения вместе с химиотерапевтическим средством и с нестероидными противовоспалительными средствами (для очистки от некротических тканей опухоли) молекул-переносчиков гиалуроновой кислоты.
СлучаЙ IX.
В июле 1988 г. пациенту диагностировали неоперабельный рак желудка. Было проведено шунтирование по типу гастроэнтероанастомоза. Осмотр пациента был проведен в августе, а лечение начато в сент. 1988. Одновременно было проведено лечение гипертермией и флоретином с очень низкой дозой химиотерапии с использованием 5-FU и иммуностимуляторов.
Это лечение продолжалось до февраля 1989 г, после чего д-р Фок начал использовать (ДМСО) в качестве носителя/агента для усиления проникновения в сочетании с MSN. Пациенту вводили повышенное количество химиотерапевтических средств с использованием 5F лейковорина, митомицина C и метотрексата, а затем в июле и начале августа, поскольку опухоль прогрессировала, пациенту также вводили новатрон.
В мае, когда пациент начал получать указанные лекарственные средства в гиалуроновой кислоте, начальное количество гиалуроновой кислоты было очень мало, средняя доза с первоначальным средством, т.е. флоретином или химиотерапевтическим средством, составляла 10-30 мг. Сначала отмечалось некоторое улучшение состояния больного, но затем в середине августа опухоль начала прогрессировать, вызвав обструкцию желудка, а также обтурацию желчных путей с развивающейся желтухой и повышением биллирубина в крови. После этого, д-р Фок назначил более высокую дозу гиалуроновой кислоты до полной дозы 500-600 мг гиалуроновой кислоты, распределенной среди различных лекарственных средств. Пациент продолжал получать те же самые лекарственные средства.
Хотя состояние пациента вначале ухудшалось, однако серия анализов верхнего желудочно-кишечного отдела, проведенная в сентябре, показала, что его желудочный искусственный канал очистился полностью, хотя до этого любое пероральное введение вызывало у пациента рвоту. С этого времени состояние больного стало постоянно улучшаться.
На основании того факта, что ранее пациент получал идентичные лекарственные средства, можно сделать вывод, что улучшение наступило вследствие повышенной дозы молекул-носителей, усиливающих проникновение лекарственного средства в уже рубцовую фиброзную опухоль и в основном смертельную на этой стадии.
Последующие результаты.
К сожалению, по истечение некоторого времени пациент умер вследствие некроза опухоли и развивающейся рубцовой ткани - но не от рака.
Случай X.
Пациенту диагностировали гепатому, присутствующую в течение 2 лет. Опухоль была относительно стабильной или с минимальным ростом в течение последних 18 месяцев. Пациенту было назначено лечение химиотерапией с низкой дозой и в сочетании с гиалуроновой кислотой, после которого наступило полное излечение. Анализ на щелочную фосфатазу показал 150 междунар.ед, а анализ на функцию печени показал, в основном, норму. Ультразвуковое исследование не обнаружило наличия опухоли в печени. Д-р Фок в дальнейшем повторял лечение каждые 2-3 месяца.
Последующие результаты.
Пациент чувствует себя хорошо.
Случай XI.
Пациентку лечили путем вливания 15 июня 1989 г. химиотерапевтического средства в сочетании с гиалуроновой кислотой. Затем проводили лечение гипертермией. Диагностированный рак груди с метастазами в печени проявлял ригидность к лечению тамоксифеном, эстрагон-блокирующим агентом.
После вышеупомянутого лечения, проведенного всего в течение 8 часов, наблюдалась полная ответная реакция. Ультразвуковое исследование не обнаружило присутствия опухоли в печени, а исследование функции печени показало норму.
Пока дополнительного лечения не требовалось, пациентка продолжала получать тамоксифен для блокирования эстрогенного рецептора.
Последующие результаты.
Наблюдался рецидив после того, как другой врач назначил вагинальный эстрогеновый крем (тамоксифен) от вагинального раздражения. В ответ на это было назначено лечение с использованием 300 мг индометацина в 300 мг гиалуроновой кислоты ежедневно. После чего наступила ремиссия.
Случай XIA.
26 марта 1989 г больная перенесла резекцию матки по поводу массивной леомиосаркомы. Однако, посредством САТ-сканирования было установлено присутствие остаточной опухоли. Д-р назначил комбинированное лечение в сочетании с гипертермией с использованием очень низкой дозы метотрексата, вводимого внутрибрюшинно вместе с гиалуроновой кислотой в качестве носителя, а затем с использованием агента, блокирующего белок, осуществляющий транспорт глюкозы - флоретина, также вместе с гиалуроновой кислотой и с использованием альфа-11-интерферона, вводимого внутрибрюшинно опять же вместе с гиалуроновой кислотой.
Последующее сканирование пациента показало значительное улучшение в размере остаточной массы опухоли. Поскольку саркомы мягких тканей обычно проявляют упорную резистентность ко всем формам лечения, то полученный ответ является весьма неожиданным и со всей уверенностью можно приписать использованию носителя/проникающей молекулы - гиалуроновой кислоты. Далее, д-р Фок проводил лечение пациентки приблизительно каждые 6-8 недель в течение 2 дней, в результате чего опухоль продолжала регрессировать.
Последующие результаты.
Некоторые опухоли начинали снова расти. Пациентка получало лечение Витамином C (50 мг в день), индометацином 300 мг ежедневно в 300 мг гиалуроновой кислоты. В результате лечения пациентка чувствовала себя значительно лучше.
Случай XIB.
Пациент получал лечение с использованием относительно низкой дозы метил CCNU и карбоплатины с метотрексатом, инъецируемых в паховую рецидивирующую меланому. Все эти средства вводили в гиалуроновой кислоте, носителе/усилителе проникающих свойств. Кроме того, пациентка получала лекарственное средство, блокирующее транспорт глюкозы, разработанное д-ром Фоком. Это средство называется флоретином и используется уже несколько лет. Флоретин солюбилизировали в специальном растворе и вводили также вместе с гиалуроновой кислотой, добавление которой усиливает проникновение этого средства в опухоль. После этого д-р Фок проводил гипертермию с использованием пропускной и искусственной радиочастотной и микроволновой гипертермии. В дополнение к этому пациентка получала иммуностимулирующие средства, которые по мнению д-ра Фока являются эффективными лишь в сочетании с другими лекарственными средствами.
В последние 2 курса лечения пациентка получала только карбоплатину с добавленной гиалуроновой кислотой, флоретин с добавленной гиалуроновой кислотой и метотрексат, вводимый внутрибрюшинно в низкой дозе - 25-35 мг также в гиалуроновой кислоте.
Д-р Фок осматривал пациентку через неделю и проводил лечение в течение 2 дней. Клинически пациентка была в хорошем состоянии. Пациентка жаловалась на боли в спине с правой стороны. Осмотр показал болезненность в районе правой почки при надавливании. Ультразвуковое исследование почек показало наличие твердой массы в правой почке, которая, как предполагалось, представляла собой либо гамартому, либо ангиомиолипому.
Исходя из резкой ответной реакции пациента на лечение, д-р Фок провел САТ-сканирование брюшной полости. Оставалось еще небольшое кистообразное поражение в правой доли печени, но функция печени была нормальной.
Последующие результаты.
У пациентки наблюдалась стойкая ремиссия.
Случай XII.
Пациент имел артериальную линию и подкожный вход, установленный во время первичной операции на брюшной полости. Он пришел на осмотр к д-ру Фоку по поводу покраснения и опухлости вокруг подкожного входа. У пациента наблюдалось повышение температуры и уровня лейкоцитов в крови.
Пластмассовую канюлю вводили в эту область и дренировали 75 см3 гнойного материала и культивировали рост E.coli и Pseudomonas aeruginosa. Д-р Фок проводил лечение путем обработки указанного очага поражения путем его орошения комбинацией гиалуроновой кислоты с ампициллином; гиалуроновой кислоты с флагилом и гиалуроновой кислоты с кефлоспорином. Рану обрабатывали ежедневно 1 г ампициллина с 50 мг гиалуроновой кислоты, 500 мг флагила с 50 мг гиалуроновой кислоты и 1 г Анцефа Ancef с гиалуроновой кислотой. В течение 2-3 дней еще можно было отсасывать гнойный материал из поврежденного места. Через 5 дней гнойного материала уже не оставалось, а присутствовала лишь жидкость, и в конце недели уже отсутствовали всякие признаки инфекции. Катетер оставляли на входе еще три месяца.
Этот пример свидетельствует о том, что антибактериальные средства вместе с гиалуроновой кислотой обнаруживают лучшее проникновение указанных лекарственных средств к месту инфекции и есть основание предположить, что указанные комбинации улучшают проникновение лекарственных средств в сами бактерии.
Случай XIII.
В июне (1-го числа) 1989 г. пациента оперировали по поводу резекции части толстой кишки, сигмовидной ободочной кишки и тонких кишок. Через 7 дней после операции наблюдалась опухлость и индурация раневой ткани, в результате чего был проведен дренаж гнойного материала в двух местах. После чего эти места обрабатывали наружным орошением с использованием ампициллина 1 г вместе с 50 мг гиалуроновой кислоты и 500 г флагила вместе с гиалуроновой кислотой. Через 4 дня эти две области инфекции очищались от бактериального заражения. Обычно для такого результата требуется длительное лечение в течение нескольких недель.
Случай XIV.
Пациентка с раком груди имела инфекцию в области линии Hickman. Был постоянно установлен пластиковый катетер в надключичную вену. Указанная инфекция присутствовала в виде гнойного материала с подкожной локализацией, который постоянно вытекал из места входа пластиковой канюли. Исходя из этого, д-р Фок назначил инъекцию, содержащую 1 г ампициллина и 50 мг гиалуроновой кислоты, вводимую непосредственно в катетер. Кроме того, пациентка получала внутривенно флагил с добавленной гиалуроновой кислоты. Инфекция очищалась и катетер присутствовал еще 4 дня.
Случай XV.
Больному диагностировали абсцесс в верхнем правом квадранте брюшной полости на передней абдоминальной стенке. Пациенту проводили дренаж в клинике, но безуспешно. Д-р Фок назначил лечение путем орошения 500 мг ампициллина и 200 мг гиалуроновой кислоты (ежедневно). Хотя, когда абсцесс подвергают дренажу, то в конце концов он все равно поддается лечению, однако, в обычных случаях необходимо слишком много времени для предупреждения возможных рецидивов. В абсцессе обнаружили staphylococcus aureus и E. coli.
Через 2 дня после ирригации ампициллином и гиалуроновой кислотой, как было описано, полость очистилась, освободилась от инфекции и началось гранулирование. Лечение продолжили еще неделю, после чего наступило излечение.
Другим пациентами при лечении опоясывающего лишая и язв вводили местно альфа-2-интерферон в комбинации с гиалуроновой кислотой, после чего также наступало быстрое излечение.
Еще одному пациенту наружно наносили метотрексат в гиалуроновой кислоте при лечении псориаза. Композиция хорошо абсорбировалась и лечение дало хорошие результаты.
Десяти пациентам, страдающим простым герпесом типа I и II, наносили эффективное количество ноноксинола-9 [нонилфенокси-этанол] (DelfenTM) в сочетании с гиалуроновой кислотой и/или ее солями на соответствующие области 2-3 раза в день, в результате чего сразу стихали симптомы боли и пораженные места заживали.
Двум пациентам для лечения опоясывающего лишая назначали эффективное количество ноноксинола-9 в сочетании с гиалуроновой кислотой и/или ее солями, в результате чего наступало выздоровление.
Случай XVI.
Зубной врач, 51 год, с меланомой, страдал опоясывающим лишаем с кожными поражениями в 9-й зоне грудной клетки с левой стороны. Пациент испытывал сильные боли, не стихающие при применении стандартных средств. Д-р Фок назначил пациенту перорально циклофур в качестве противовирусного средства, которое не подействовало сразу. Однако, д-р Фок тогда назначил "DelfenTM" и "LifeCoreTM" (гиалуроновая кислота), смешанные в равных пропорциях, которые применял путем наружного нанесения. В результате этого боль стихла через 5 минут. Боль отсутствовала и последующие 4 дня. Кроме того, кожные поражения также исчезли в течение 24 часов и в последующие 5 дней не появлялись. Этот поразительный эффект можно объяснить противовирусным действием указанной комбинации, которое усиливается благодаря применению гиалуроновой кислоты.
Случай XVII.
Пациент страдал раком желудка с метастазами в печень. Он лечился в течение 7 месяцев с использованием низкой дозы химиотерапии 5-FU, низкой дозы митомицина и неватрона с различным количеством гиалуроновой кислоты, а также витамина C. После указанного лечения опухоли не обнаружили. Наступила ремиссия с кальцификацией всех опухолей.
Случай XVIII.
Пациент попал в серьезную автомобильную катастрофу, после чего у него стал быстро развиваться рак толстой кишки с множественными метастазами в печень. Он обратился к д-ру Фоку в июне 1989 г. Было назначено лечение химиотерапией флоретином в сочетании с гиалуроновой кислотой и термотерапией. В течение года не было заметных результатов, а затем содержание щелочной фосфатазы начало падать. После этого д-р Фок назначил витамин C (50 г в день в течение 3-х дней), гиалуроновую кислоту (до 300 мг в день), индометацин в N-метилглюкамине (300 мг в день) в 300 мг гиалуроновой кислоты, и ТорадолTM (60 мг) один или два раза в день в сочетании с гиалуроновой кислотой (50 мг). После этого лечения наступило улучшение. Содержание щелочной фосфатазы уменьшилось и функция печени улучшилась.
Случай XIX.
Больной, 46 лет, с диагнозом альвеолярная карцинома легких, поставленным три месяца назад, не лечился ни химиотерапией, ни значительной дозой облучения, хотя получал точечное облучение в двух областях; с обеих сторон грудной клетки имелись видимые скелетные поражения.
По поводу этого заболевания пациент обратился в отделение сердечно-легочной трансплантации в Лондоне, где ему сообщили, что трансплантат может быть введен, но надо ждать очереди в течение одного года.
После этого пациент обратился в клинику д-ра Фредерика Доуна в Германии и был помещен на лечение, которое заключалось в: (a) повышении иммунитета путем увеличения уровня Т-клеток; и (b) дезинтоксикации и введении акцептора свободных радикалов.
После лечения наблюдалось некоторое улучшение, а затем через 24 часа началось учащенное дыхание.
После обследования было установлено уменьшение входа для воздуха, что вызывало билатеральные хрипы. Свидетельств надключичной аденопатии не было. Болезненность в области позвоночника отсутствовала, печень не была увеличена.
После этого пациент обратился к д-ру Фоку, который назначил лечение: витамин C (50 мг), нестероидный индометацин НСПВС (100 мг - сниженное количество от 300 мг, вследствие изжоги), растворенный в гиалуроновой кислоте (300 мг). В результате наступило резкое улучшение после первых 5-ти дней лечения, о чем свидетельствовало измерение жизненной емкости легких и рентгеновские снимки.
После этого д-р Фок назначил инъекции гиалуроновой кислоты (300 мг) в сочетании с ТорадоломTM (60 мг), которое он принимал дома ("дома" - не в Канаде).
Затем было проведено сравнение с предыдущими результатами обследования. При предыдущих исследованиях отмечалось некоторое рассасывание увеличенных интерстициальных меток, однако последующее обследование показало, что легкие еще более очистились по сравнению с предыдущим обследованием. Тем не менее, увеличенные интерстициальные точки еще присутствовали в обоих полях легких.
Случай XX.
Пациентка, 74 года, была прооперирована по поводу рака толстой кишки. После операции, однако, появились метастазы в печени, правой доле. На протяжении месяца она дважды получала метотрексат (25 г) в гиалуроновой кислоте (400 мг), внутрибришинно, онкостатин 5х (2 г) в гиалуроновой кислоте (300-500 мг), витамин C (50 мг) в гиалуроновой кислоте (300 мг) и индометацин (НСПВС) два раза, (100 мг) индометацин в (300 мг) гиалуроновой кислоте и (250 мг) индометацина в (500 мг) гиалуроновой кислоте.
Пациентка сразу почувствовала себя хорошо, а опухоль печени регрессировала, уменьшилась в объеме.
Случай XXI.
Пациентка, 51 год, рак матки с метастазами в легкие леомиосаркома. Д-р Фок назначил лечение с использованием различных доз онкостатина - низкие дозы от (0,5 г до 3 мг) с гиалуроновой кислотой (300 - 500 мг), Витамина C (50 мг) в гиалуроновой кислоте (300 мг), индометацина в гиалуроновой кислоте (внутрибрюшинно и внутривенно).
Тазовые опухоли регрессировали, а опухоли легких оставались стабильными.
Случай XXII.
Пациент, 52 года, страдал болезнью Крона и хронической инфекцией кишечника, как следствие болезни Крона. В итоге, у пациента стала развиваться опухоль в брюшной полости аденосаркома. Пациент получил лечение с использованием доз в 2 г и (3 г) онкостатинаTM (флоретина), каждая доза в гиалуроновой кислоте (500 мг) и (ДМСО) (общее кол-во 2000). Дозы индометацина варьировались в пределах от (75 мг) до (450 мг) в 200 - 700 мг гиалуроновой кислоты. Пациент также получал витамин C (50 мг) в гиалуроновой кислоте (300 мг) и напроксен (1 г) в гиалуроновой кислоте (400 мг). Это лечение проводилось посредством нескольких способов введения: внутрибрюшинно, внутривенно, ректально для дезинтоксикации (вставляли катетер и вводили ректально). В результате боли утихли.
Пациенту было проведено СТ-сканирование брюшной полости и тазовой области. В результате диагностировали умеренный стеатоз печени без видимых метастаз. Селезенка, поджелудочная железа, надпочечники и правая почка были в норме. Дренаж левой почки после нефростомии не показал остаточного гидронефроза. Имелась обширная и некротическая опухолевая масса, занимающая большую часть тазовой области с распространением на переднюю стенку мочевого пузыря с некоторой инвазией предстательной железы. Свидетельств деструкции крестца не было, хотя опухоль толстой кишки находилась близко от его поверхности.
Таким образом, имела место обширная некротическая опухолевая масса без деструкции в области крестца, без пара-аортной лимфоаденопатии или без периферических метастаз во внутренние органы. Был введен уретральный стент (чрезкожно).
Пациент обследовался в клинике 1 авг. 1990 г. и чувствовал себя хорошо. Некротическая масса постепенно уменьшалась в размерах и здоровье пациента резко улучшалось.
Случай XXIII.
Пациентке, 47 лет, был установлен диагноз в январе 1990 г. Была осуществлена резекция желудка с заменой пищевода (для глотания). Была обнаружена также опухоль в брюшной полости. Проведенная химиотерапия привела к выпадению волос. Д-р Фок назначил наружное лечение миноксидилом в сочетании с гиалуроновой кислотой и волосы начали отрастать. После осмотра пациентки 6 июня 1990 г д-р Фок назначил пониженные дозы флоретина в сочетании с гиалуроновой кислотой и термотерапией, индометацин в гиалуроновой кислоте и витамин C в гиалуроновой кислоте. После проведенного лечения пациентка почувствовала значительное улучшение. Она прибавила в весе и не ощущала никаких болей. Карциноэмбриональный антиген упал до 25 нг/мл и постоянно уменьшался.
Случай XXIV.
Пациент 45 лет впервые обратился к д-ру Фоку 1 марта 1988 г. и ему был установлен диагноз: рак поджелудочной железы. Он лечился с использованием (ДМСО) в сочетании с термотерапией и низкими дозами химиотерапии. (ДМСО) и другие лекарственные средства были введены непосредственно в опухоль. Более чем через год пациенту было назначено лечение витамином C и другими лекарственными средствами в гиалуроновой кислоте. В результате чего наступила стойкая ремиссия. Более чем 6 месяцев пациент не получал никакого лечения.
Случай XXV.
Д-р Фок осматривал пациентку (62 года) в августе 1989 г. Был поставлен диагноз: рак поджелудочной железы. В результате было назначено лечение низкими дозами химиотерапии 5-FU и митомицин вместе с (300 мг) гиалуроновой кислоты и в сочетании с термотерапией. Пациентка жаловалась на боли в области желчных путей, однако, при операции опухоли в желчных путях обнаружено не было и было проведено лишь шунтирование желчных протоков. Затем пациентке было назначено лечение индометацином и Витамином C в гиалуроновой кислоте, а лечение гипертермией было прекращено. В результате проведенного лечения пациентка прибавила в весе, при этом наличия сколь-нибудь заметной опухоли не было обнаружено.
Случай XXVI.
Пациентка (18 лет) лечилась от инфекционного мононуклеаза. Обследование через три месяца показало положительную реакцию на гетерофильный иммуноглобулиновый тест. Пациентка жаловалась на большую слабость. Было назначено лечение с использованием 50 г Витамина C и 300 мг гиалуроновой кислоты. Через 6 часов состояние резко улучшилось и слабость пропала. Через две недели гетерофильный иммуноглобулиновый тест дал отрицательный ответ.
Случай XXVII.
У пациентки 65 лет была диагностирована опухоль, по поводу которой она лечилась с применением химиотерапии. Терапевты, проводившие лечение, не знали, что они устранили большую часть опухоли. Однако, поскольку опухоль разрушалась, как потом установил д-р Фок, в области опухоли скапливалась водяная жидкость (что можно было видеть с помощью ультразвука). Д-р Фок назначил пациентке лечение термотерапией, флоретином, Витамином C, индометацином и некоторым количеством 5-FU, причем все эти средства вводили в гиалуроновой кислоте. По мнению ее предыдущих лечащих врачей опухоль увеличилась после приема 5-FU и поэтому химиотерапию отменили. Пациентка почувствовала себя лучше, лучше выглядела и отечность исчезла.
Случай XXVIII.
Пациентке был установлен диагноз: рак яичника с полной обтурацией кишечника, который как бы весь "обложен" опухолью и также с большим количеством плевральной жидкости. В данном случае имело место поразительное действие Лазикса (фуросемида), которое было использовано следующим образом. 28 и 29 апреля 1990 г общий объем мочи, выделенный пациенткой в течение 48 часов, составил 2 450 мл, при этом несмотря на то, что пациентке вводили 0,33% раствор хлорида натрия с добавлением хлорида калия в дозе 40 мэкв/л (в объеме 100-125 мл в час). Вес больной составлял 40 кг. В течение этого периода пациентка получала 120-200 мг Лазикса внутривенно.
30 апреля она получала 40 мг Лазикса с добавлением 350 мг гиалуроновой кислоты, вводимой в течение полчаса. Выделение мочи в последующие 5 часов составило 2500 мл. Вечером пациентка не получала дополнительного лазикса, в результате чего выделение мочи резко падало до 400 мл (от 7 часов пополудни 30 апр. до 7 до полудня 1-го мая). В 7 ч 30 мин она получала 40 мг лазикса в 300 мг гиалуроновой кислоты, вводимой внутривенно. Через последующие 8 часов выделенное пациенткой количество мочи составило 2600 мл. Этот факт свидетельствует о том, что даже относительная невосприимчивость к фуросемиду (Лазиксу) может быть преодолена путем добавления гиалуроновой кислоты, которая способствует повышению проникающей способности лекарственного средства в соответствующую область.
Аналогичное явление наблюдалось при лечении пациентов с так называемым "гепаторенальным синдромом", когда имеет место прекращение экскреции мочи вследствие недостаточной функции печени. В этих случаях экскреция мочи может доходить до нуля. Внутривенное введение фуросемида (ЛазиксаTM) в гиалуроновой кислоте дает поразительные результаты, даже если сам Лазикс, введенный отдельно, не дает должного эффекта.
Случай XXIX.
При введении здоровым людям фуросемида (ЛазиксаTM) в дозе 20 мг (внутривенно) с добавлением 300 мг гиалуроновой кислоты наблюдалось повышение экскреции мочи в 3-5 раз по сравнению с мочевыделением, наблюдавшимся при введении лишь одного Лазикса. Это свидетельствует о том, что гиалуроновая кислота способствует повышению проникающей способности лекарственных средств и облегчению их функций.
Случай XXX.
Пациент лечился от облысения путем наружного нанесения на поверхность головы моноксидила (Rogaine). После этого наблюдался совершенно незначительный рост волос. Затем моноксидил наносили вместе с гиалуроновой кислотой постоянно каждые 2-3 дня. В результате этого волосы у пациента стали расти гуще и значительно быстрее.
Случай XXXI.
В клинике Mayo Clinic после обследования пациентке 32 года был установлен диагноз: энителиоидно-клеточная саркома.
Начало истории болезни датируется 12 дек. 1978, когда на левом безымянном пальце была обнаружена узловатая опухоль, после чего палец был удален. После рецидива был ампутирован 4-й палец левой руки. После экстензивного обследования пациентки были обнаружены узловатые образования аналогичного типа в верхней части руки и во вспомогательных лимфоузлах, что было подтверждено биопсией, сделанной в марте 1990 г.
В клинике Mayo пациентка получила три курса химиотерапии с использованием митомицина C, адриамицина, цисплатины в высоких дозах, однако, указанное лечение не дало никаких результатов. Затем пациентка подверглась ампутации левой руки и передней четверти предплечья.
Д-р Фок впервые осматривал пациентку 25 июня 1990 г, после чего назначил лечение с использованием гипертермии, флоретина с гиалуроновой кислотой, витамина C, C-гиалуроновой кислоты, метотрексата с гиалуроновой кислотой, а также солюмедрола, которое проводилось в течение 3 дней. Лечение не дало видимых результатов и улучшения состояния не наблюдалось.
Пациентка вернулась в клинику 23 июля и в течение 3 дней прошла курс лечения со сниженной дозой флоретина, такой же дозой витамина C с гиалуроновой кислотой, а также пациентке подкожно и внутривенно вводили напроксен и индометацин с гиалуроновой кислотой. Затем она выписалась домой, где получала ТоредолTM [Синтекс - нестероидное противовоспалительное средство] (внутримышечно) в суточной дозе 30-120 мг, которое вводили один или два раза в день с 100 мг Hyal (фармацевтический препарат гиалуроновой кислоты).
Затем она проходила обследование 20 авг., в результате которого было установлено резкое уменьшение размеров всех поражений на 50%. Фактически, биопсия не обнаружила присутствия каких-либо жизнеспособных опухолей. Лечение продолжили с применением ТоредолаTM и гиалуроновой кислоты.
Хотя пациентка оказалась маловосприимчивой к гипертермии, флоретину и к комбинации стандартных химиотерапевтических средств и гиалуроновой кислоты, однако, прекрасные результаты дало применение нестероидных противовоспалительных средств всех трех типов: ИндоцидаTM, напроксена и ТоредолаTM в сочетании с гиалуроновой кислотой, которую использовали в качестве носителя/наполнителя, обеспечивающего направленную доставку лекарственного средства к патологической ткани. При применении указанных нестероидных противовоспалительных средств пациентка почти не испытывала обычных для этих средств побочных явлений.
Случай XXXII.
Пациенту диагностировали рак желудка в 1988 г. Опухоль находилась в дистальной трети пищевода у входа в желудок. Посредством интраоперативной процедуры на брюшной полости была установлена трубка Селестина и вшивали в малую кривизну желудка.
Пациент лечился с января 1990 в течение 3-х месяцев и в июне 1990 был обследован. Повторное САТ-сканирование не показало никаких изменений; симптоматически пациент чувствовал себя хорошо. Самое последнее сканирование было сделано 26 июня 1990 г. Были некоторые сомнения относительно нескольких областей печени, однако ультразвуковое исследование эти подозрения исключило.
4-го июля пациент был на пикнике и съел бутерброд с сосиской ("hot dog"). Ночью он проснулся от острой боли в левой области, которая, однако, не сопровождалась тошнотой или рвотой. После этого эпизода больной испытывал боль, которая возникала всякий раз при приеме пищи. Эта боль носила постоянный характер, отдавала в спину и переднюю часть брюшины и распространялась на боковые стороны. Эта боль никогда не ассоциировалась непосредственно с болезненностью в области брюшины, рвотой, диареей, повышением температуры и ознобом. Исследования посредством СТ-сканирования проводили как раз за 8 дней до начала боли, а также проводили серию исследований желудочно-кишечного тракта. Дополнительное САТ-сканировние нельзя было проводить, поскольку желудок был наполнен барием.
Следует отметить, что значительная доза Демерола лишь немного снимала боль. Дальнейшее обследование не дало ничего нового. Узлов в брюшной полости, грудной клетке или лимфе, которые свидетельствовали бы о распространении болезни, обнаружено не было.
Д-ром Фоком было снова проведено рентгеновской обследование в госпитале Торонто вместе с профессором радиологического отделения. Серия исследований верхнего желудочно-кишечного тракта показала классическую картину "спутанности" тонких кишок. По мнению врача, это может быть либо вследствие фиброзного склеивания, либо злокачественного образования, либо вследствие того и другого, что часто бывает при аденокарциноме желудка. Однако, по всей вероятности неопластическая диссеминация была минимальна, поскольку она не была обнаружена при предыдущем САТ-сканировании.
Д-р Фок назначил пациенту лечение путем введения комбинации нестероидного противовоспалительного средства и гиалуроновой кислоты внутривенно в сочетании с гипертермией и онкостатином, причем комбинация флоретина и гиалуроновой кислоты почти мгновенно снимала боль. После лечения больной мог принимать пищу, не опасаясь симптомов боли.
Д-р Фок также назначил пациенту пробантин, который он мог использовать при болях, которые возникали вследствие адгезии кишечника и которые обычно снимаются антихоленергическими средствами. Д-р Фок также предложил пациенту продолжить лечение дома, принимая комбинацию фельдена 10 мг (внутрикожно) и напрозина 500 мг в виде суппозитория один раз в день, а также принимать зантак (150 мг два раза в день).
Помимо этого д-р Фок назначил пациенту вибрамицин (Доксицилин) 200 мг один раз в день и 100 мг ежедневную дозу в течение 14 дней. Это антибактериальное средство, которое также обладает способностью блокировать внутриклеточный и анаэробный гликолиз.
Последующие результаты.
Недавно проведенная биопсия показала хроническое воспаление нижней трети пищевода, трубка в пищеводе была удалена (однако никаких злокачественных образований обнаружено не было.
Случай XXXIII.
Пациент лечился химиотерапией, в результате чего большая часть опухоли регрессировала, однако больной не следовал назначенному режиму лечения. Лечение вначале значительно ухудшило состояние больного; это ухудшение отражалось лишь на некотором изменении функции печени. Содержание щелочной фосфатазы было повышено. Пациент чувствовал общую слабость, разбитость, усталость, потерю аппетита. Это состояние было улучшено путем использования индометацина в гиалуроновой кислоте и лечением с применением дезинтоксифицирующих средств.
Пациент был обследован и чувствовал себя значительно лучше. Ультразвуковое исследование показало, что опухоль практически регрессировала с некротическим разложением. Функция печени нормализовалась.
Случай XXXIV.
Пациент страдал хроническим абсцессом, полость которого располагалась в области таза, с обструкцией толстой кишки, в результате чего была проведена операция 5 янв. 1990 г. Полость подвергали ирригации и дренажу через промежность. После прохождения обычного послеоперационного курса пациент был выписан из госпиталя 18 января 1990.
Однако, после этого у больного поднялась температура, и поскольку больной имел большую полость в тазовой области, то дренаж проводили путем лапаротомии через нижний передний отдел брюшной полости. Лапаротомия была проведена за две недели до визита к врачу.
Д-р Фок осмотрел пациента. По мнению д-ра Фока для заращения такой большой полости потребуется 4 - 6 недели. Д-р Фок назначил ежедневную ирригацию в течение 5 дней ампициллином, флагилом и гиалуроновой кислотой с использованием 500 мг ампициллина и 500 мг флагила. Это гораздо более слабое лечение по сравнению с тем, которое обычно назначал в этом случае д-р Фок.
После последующего осмотра было установлено, что полость абсцесса закрылась. При этом пациент жаловался на то, что медсестра, приходящая в субботу и воскресенье, трудно справляется с введением катетера в полость. Отсюда д-р Фок сделал вывод, что в полости образовалась гранулированная ткань, причем это образование произошло слишком быстро. Имея в виду этот факт, следует учитывать, что при хронических полостях абсцессов получение не слишком быстрых результатов в данном случае более предпочтительно, чем ускоренное заживление.
В связи с этим, д-р Фок посоветовал пациенту обращаться к нему с любым повышением температуры. Пациент также жаловался на легкий зуд кожи, который, по всей вероятности, был реакцией на охлаждение, в связи с чем д-р назначил лечение мазью ежедневно путем нанесения на кожу.
Случай XXXV.
Женщина имела поражение 9-го и 12-го нерва, которое локализовалось сбоку у основания черепа. Было подозрение на метастазы в дентоидной области. Было сделано MR1-сканирование, которое показало некоторую патологию в соответствующей области. СТ-сканировние этой области оказалось безуспешным.
После обследования в Научно-исследовательском раковом центре в Онтарио диагностировали злокачественную меланому в запущенном состоянии и выписали из госпиталя с безнадежным прогнозом.
Позднее коллеги из Вакового центра в Онтарио были удивлены и восхищены невероятным результатом лечения, проведенного д-ром Фоком. Это лечение включало в себя гипертермию и химиотерапию в сочетании с гиалуроновой кислотой. Были использованы обычные дозы Карбопластина и низкие дозы метотрексата в гиалуроновой кислоте.
Грудная клетка была чистой, имели место некоторые стойкие поражения в почке и печени, однако, они хорошо контролировались. В течение лета функция языка нормализовалась. Однако, за последние три или четыре недели с этой стороны имелись некоторые нарушения.
После последнего неврологического осмотра было установлено, что все функции нормализовались за исключением некоторых нарушений с левой стороны гортани, а также наблюдалась некоторая фасцикуляция и атрофия левой стороны языка.
Пациентка чувствовала себя хорошо.
Последующие результаты.
Недавно пациентке была введена комбинация из гиалуроновой кислоты (300 мг в день), НСПВС и Витамин С (50 г в день). Опухоли полностью исчезли.
Случай XXXVI.
Пациент перенес хирургическую операцию по поводу мезотелиомы и получил лечение с использованием адъюванта. Прошло 7 лет после первоначального установления диагноза. Весной этого года во время его пребывания во Флориде болезнь рецидивировала. И хотя д-р Фок проводил биопсию три раза, он не получил клеток, свидетельствующих о злокачественном образовании. Однако в клинических условиях посредством СТ-сканирования и ультразвукового исследования печени этот диагноз был выяснен.
Пациенту было назначено лечение флоретином в гиалуроновой кислоте и местная гипертермия. Вначале заметных улучшений не было. Однако после этого пациент не получал химиотерапии, а получал лишь флоретин в гиалуроновой кислоте в очень больших дозах гиалуроновой кислоты. Реакция на лечение была хорошей, однако, возникла проблема скапливания жидкости, которая, по мнению д-ра Фока, была следствием распада опухоли. Распад опухоли был подтвержден ультразвуковым исследованием; и результатом этого распада было образование жидкости в опухоли.
После этого пациенту назначили на один день лечение гипертермией и флоридзином в гиалуроновой кислоте. Однако затем еще два дня пациент получал витамин C в гиалуроновой кислоте в целях дезинтоксикации. Кроме того, пациенту назначили дополнительно Лазикс (фуросемид, диуретик) в сочетании с гиалуроновой кислотой.
Содержание креатинина у пациента, которое составляло 400 мМ/л, уменьшилось до 155 мМ/л в соответствии с тестом на функцию почки - от высокого значения до почти нормы. По мнению д-ра Фока пациент не нуждался в дальнейшем лечении, поскольку большая часть его опухоли регрессировала посредством его собственной иммунной реакции, чему способствовало введение гиалуроновой кислоты, которая является медиатором лекарственного средства и антител.
В июле 1990 года был зафиксирован умеренный асцит скопление жидкости в организме. Пациенту был назначен фуросемид (ЛазиксTM) и гиалуроновая кислота. С выводом большого количества мочи состояние пациента значительно улучшилось.
Случай XXXVII.
Женщине, 37 лет, был установлен диагноз: карцинома шейки на IIIB стадии. Она лечилась облучением в Раковом центре,но безуспешно. Опухоль продолжала расти, что было засвидетельствовано приблизительно через 1-2 месяца после облучения. Она наблюдалась д-ром Уальдом в госпитале св.Марии. Ей вводили эпирубицин, цисплатину в высоких дозах, которые не вызывали регрессии опухоли, как было установлено путем интравагинального обследования и биопсии, напротив, состояние ухудшалось благодаря болям с частичной обтурацией мочевого пузыря, как было показано СТ-сканированием брюшной полости 28 июня 1990 г.
Лапаротомия показала обширную опухоль с большими некротическими областями, которая распространялась и захватывала подвздошную артерию и вену, обтурируя ее, в результате чего хирурги признали опухоль неоперабельной, так как она распространилась на малый и большой таз. Пациентку осматривали хирурги-урологи и онкологи.
В результате обтурации прямой кишки была осуществлена колостомия. Кроме того, хирурги-урологи использовали участок подвздошной кишки для создания искусственного мочевого пузыря.
Пациентка испытывала острые боли в течение нескольких недель до операции и после операции. Высокие дозы внутривенного введения морфина лишь частично снимали боли. 8 июля было отмечено повышение температуры и САТ-сканирование показало абсцесс в левой части таза. Абсцесс подвергали дренажу при САТ-сканировании и пациентке систематически вводили антибиотики, которые лишь слегка улучшали ее состояние.
После этого ее лечением занялся д-р Фок. Он назначил ампициллин, который вводили через катетер, в сочетании с гиалуроновой кислотой (1 г ампициллина и 500 мг гиалуроновой кислоты). Кроме того, пациентке назначили 1 мг ампициллина внутривенно и флагил систематически в 500 мг "LifeCoreTM" гиалуроновой кислоты. Кроме того, пациентка получала 100 мг индометацина с 500 мг гиалуроновой кислоты ("LifeCoreTM") внутривенно. Через 12 часов боль резко уменьшилась, симптомы инфекции пропали, дренаж полости абсцесса был почти прекращен. Ее массивная левая нога в результате венозной и лимфатической обтурации приняла почти нормальные размеры всего лишь за период в 12 часов.
Пациентка продолжала тот же курс лечения, в результате чего через 3 дня боли полностью утихли, а состояние продолжало улучшаться и 18 июля она была выписана из госпиталя без проведения лечения антибиотиками. Системная аналгезия с помощью морфина была прекращена. При этом пациентке не проводили лечение гипертермией и химиотерапией и/или онкостатином флоретином. Она получала противоокислительную терапию в сочетании с гиалуроновой кислотой и с сопутствующим введением индометацина и гиалуроновой кислоты. Состояние пациентки резко улучшалось, что свидетельствовало о том, что сочетание индометацина и гиалуроновой кислоты обеспечивает направленную доставку препарата к патологической ткани, улучшает функцию макрофагов, повышает иммунитет и способствует деструкции опухоли.
Случай XXXVIII.
Пациенту диагностировали СПИД (ВИЧ) и назначили лечение индометацином (НСПВС), (Витамином C), интерфероном И (ДМСО) и/или гиалуроновой кислотой, в результате чего наступило неожиданное и постоянное улучшение состояния пациента.
Случай XXXIX.
Пациент, страдающий наличием горба, испытывал постоянную боль в спине. Принимая перорально анальгетики и препараты для растирания спины, пациент, однако, не чувствовал заметного улучшения. Использование (НСПВС) в гиалуроновой кислоте гиалуронат натрия, которое пациент применял наружно, путем нанесения на спину, привело к снижению болей, а затем к полному их исчезновению.
Использование индометацина, растворенного в N-метилглюкамине, и напроксена, растворенного в гиалуроновой кислоте, дало побочные явления. Однако, ТорадолTM (+/-)форма трометаминовой соли кеторолака - ингибитора биосинтеза простагландина, аналгетик и противовоспалительное средство позволяет устранить боли и не дает побочных эффектов.
Случай XXXX.
Пациенту диагностировали СПИД и как возможное следствие этого заболевания - опухолевое поражение легких. Перед лечением пациент был на грани смерти; количество лейкоцитов достигало 1,4•109/литр. Пациенту вводили внутривенно индометацин (300 мг), витамин C 50 мг ежедневно и гиалуроновую кислоту гиалуронат натрия (300 мг). После лечения количество лейкоцитов составляло 8,2•109/литр, а количество тромбоцитов составляло 65• 109/литр. Количество лимфоцитов удвоилось.
Дополнительные испытания на животных.
Кроме того, были проведены испытания на животных, которые показали следующие результаты: (на крысах)
Повышенную активность антибиотиков в сочетании с гиалуроновой кислотой. Использовали модель хронического абсцесса у крысы, (крысы Sprague Dawley). Пилюли с бактериями вводили в брюшко каждой крысе, а затем крыс лечили по указанной схеме. В этой модели терапевтическую активность гентамицина сравнивали с гентамицином в гиалуроновой кислоте, в результате чего, было наглядно продемонстрировано значительного улучшение состояния животного при введении указанной комбинации по отношению к антибиотику, применяемому отдельно. При невосприимчивости к антибиотикам могут быть использованы более низкие дозы антибиотика в сочетании с гиалуроновой кислотой.
В другом тесте (имплантаты от AC1-штамма крыс черных, введенные крысам Lewis strain (белым)) была исследована возможность повышения срока жизни имплантата путем использования комбинаций иммунодепрессантов и гиалуроновой кислоты (HA), вводимых крысам Lewis strain. Срок жизни имплантата в большой степени зависит от способности организма к подавлению отторжения имплантата, которая может быть стимулирована с помощью иммуноподавляющих средств с оптимальной активностью, что редко достигается, поскольку их эффективная концентрация не доставляется к месту имплантата. Использование комбинации иммунодепрессанта в сочетании с гиалуроновой кислотой помогает преодолеть указанные трудности. Это может быть осуществлено путем оптимизации иммунодепрессивной/имплантантной активности с помощью комбинации специфических средств и гиалуроновой кислоты. Для испытаний использовали стандартную модель имплантации кожи крысам. В качестве иммунодепрессанта использовали циклоспорин. Результаты испытаний показали, что использование гиалуроновой кислоты значительно увеличивает срок жизни имплантата.
Настоящее изобретение может быть осуществлено и в других вариантах, не выходящих за рамки объема нижеследующей формулы изобретения.






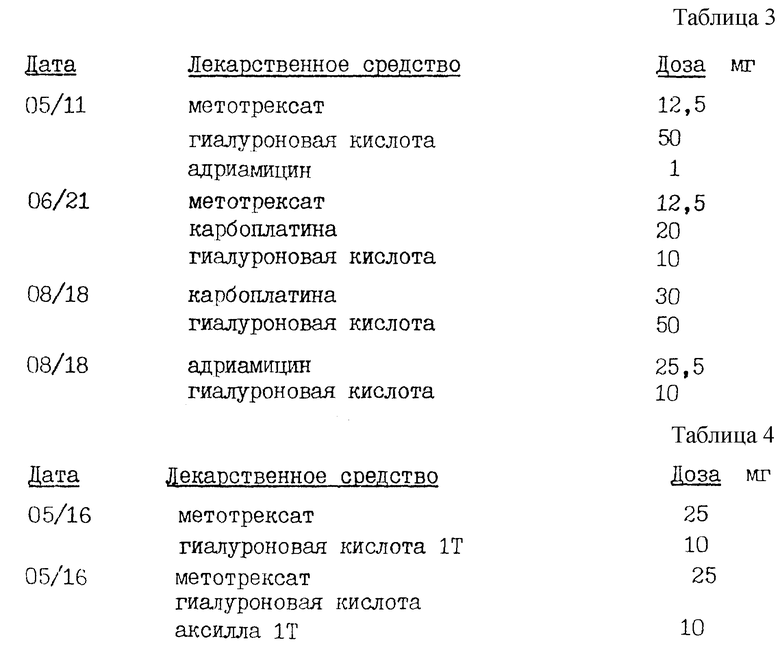

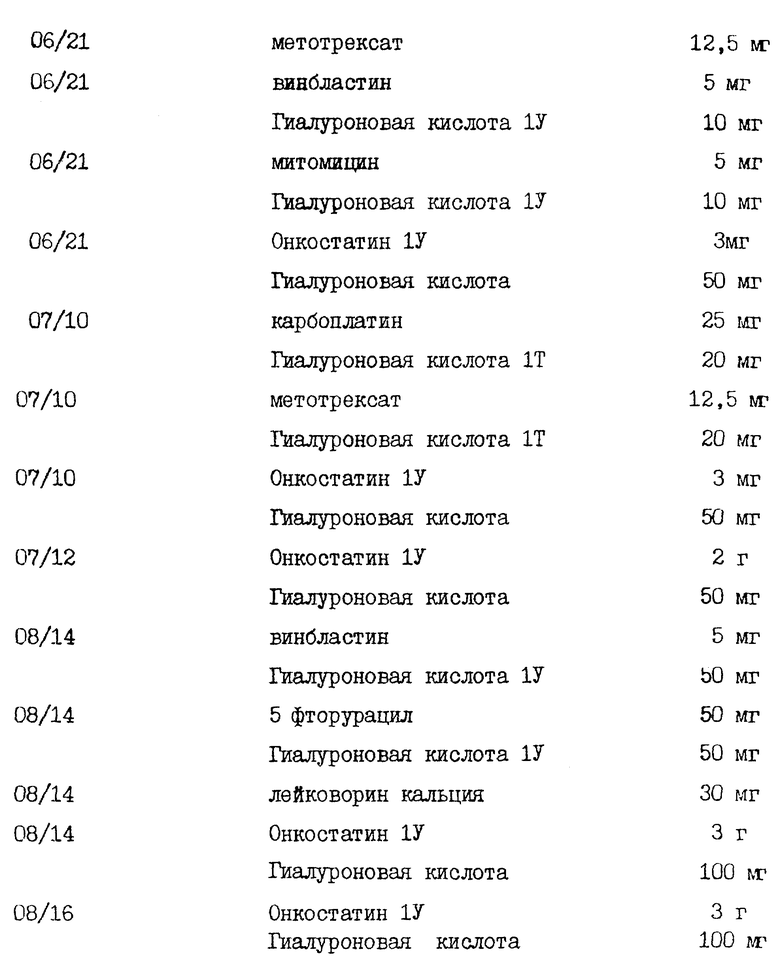
Изобретение относится к медицине и относится к комбинации для введения в организм, содержащей терапевтически эффективное количество лекарственного и/или терапевтического средства для лечения состояния или заболевания и некоторое количество гиалуроловой кислоты, и/или ее солей, и/или ее гомологов, аналогов, производных, комплексов, сложных эфиров, фрагментов субединия, достаточное для облегчения проникновения лекарственного средства через ткань, включая рубцовую ткань в месте отработки, через клеточные мембраны в отдельные целевые клетки. Изобретение обеспечивает повышение эффективности лечения, устранение побочных эффектов. 11 с. и 167 з.п. ф-лы, 4 табл.
| US 4434177 A, 28.02.84 | |||
| "Toxic drug tamed but still potent; Ontario Medicine, v 8, N 16, 21.08.89. |
Авторы
Даты
2000-03-10—Публикация
1990-09-18—Подача