Изобретение относится к химической промышленности, а именно к способам получения боратов бария.
Известны способы получения боратов бария (А.Р. Кешан. Синтез боратов в водном растворе и их исследование. Изд. Ак. наук Латв. ССР Рига, 1955 г.) путем взаимодействия растворов солей бария и борной кислоты.
Недостатками способа являются многостадийность процесса, включающего стадии кристаллизации, фильтрации и промывки продукта, наличие сточных растворов, большая продолжительность и энергоемкость процесса.
Известен способ синтеза боратов металлов в "сгущенном слое" (а.с. СССР N471302, МКИ: C 01 B 35/00), сущность которого заключается в проведении процесса в ограниченном количестве воды при комнатной температуре путем добавки соответствующего оксида или карбоната металла к водной суспензии борной кислоты. Этот способ позволяет исключить стадии кристаллизации, фильтрации и промывки продукта.
Недостатками способа являются использование воды и длительность процесса, равная не менее 4-х часов, а также консистенция (густая, комковатая, влажная масса) готового продукта, требующая длительной сушки.
Известен способ получения боратов бария (патент SU N 1834846, МКИ: C 01 B 35/12) путем взаимодействия увлажненной смеси борной кислоты и гидроксида бария, взятых в стехиометрических количествах при массовом соотношении смеси твердых компонентов и воды в следующих пределах (MeO+H3BO3):H2O = 0,21 - 0,26, при перемешивании в течение 1,5 - 2,5 часов. Уменьшение количества задаваемой воды для синтеза боратов бария по сравнению с известным способом "сгущенного слоя" дает возможность получить за 1,5 - 2,5 часа рассыпчатый порошкообразный продукт. Недостатками данного способа являются значительная продолжительность синтеза и повышенный расход воды, что приводит к инкрустации поверхности лопастей и стенок смесителя из-за кристаллизации боратов бария из жидкой фазы.
Целью настоящего изобретения является упрощение метода и снижение себестоимости продукта.
Поставленная цель достигается тем, что в стехиометрическом соотношении смешивают гидроксид бария и борную кислоту, при этом первым в смеситель загружают твердый гидроксид бария и нагревают его до температуры 35 - 70oC, перемешивают при этой температуре не менее 5 минут, после чего вводят твердую борную кислоту и перемешивают реакционную смесь не менее 55 минут. Оптимальная температура предварительного нагрева 35-45oC, оптимальное время синтеза 55-65 мин.
Предложенный способ получения боратов бария отличается от прототипа следующими показателями:
1. Синтез осуществляют без добавления воды.
2. Первым (исходным компонентом) загружают в смеситель гидроксид бария.
3. Гидроксид бария подвергают кратковременному предварительному нагреву.
В известных способах жидкая фаза - вода вводится в процесс с растворами исходных компонентов или в виде водной суспензии борной кислоты, или смесь твердых веществ увлажняется водой.
Взаимодействие гидроксида бария с борной кислотой идет через жидкую фазу по реакции:
Ba(OH)2•8H2O+6H3BO3--->BaO •3B2O3•4H2O+14H2O
Согласно данной реакции поступающей с исходными компонентами воды достаточно для получения гексабората бария BaO•3B2O3•4H2O и остаются свободными еще 14 молекул воды. Поэтому в данном изобретении вода не вводится, а используется свойство Ba(OH)2•8H2O - гидроксида бария по мере нагревания плавится в своей кристаллизационной воде.
Экспериментально показано, что при введении в нагретую до температуры 70oC и выдержанную при ней 5 минут твердую борную кислоту твердого гидроксида бария, смесь остается сухой, разогревания реакционной массы не происходит, что свидетельствует об отсутствии химической реакции.
При введении твердой борной кислоты при перемешивании в твердый гидроксид бария при температуре 25oC результат аналогичен вышеуказанному.
Химическая реакция между гидроксидом бария и твердой борной кислотой происходит лишь при введении последней в предварительно нагретый гидроксид бария.
Гидроксид бария перед началом загрузки борной кислоты может иметь температуру 35-70oC. Оптимальная температура предварительного нагрева гидроксида бария 35-45oC, так как повышение температуры приводит к увеличению продолжительности операции и расходу электоэнергии и пара. При температуре гидроксида бария 75oC и выше он начинает терять свою кристаллизационную воду, плавиться, покрывать стенки смесителя коркой, накапливаться в застойных зонах, от чего после загрузки в смеситель твердой борной кислоты не происходит равномерного смешения компонентов, что не позволяет получить стандартный продукт по ТУ 113-07-014-91.
Для достаточного увлажнения гидроксида бария необходим нагрев его в течение не менее 5 минут. При меньшей выдержке - 2 минуты и последующем перемешивании с борной кислотой в течение 60 минут не происходит саморазогревания реакционной массы, реакция происходит не полностью и конечный продукт, содержащий более 10% водорастворимых веществ, не соответствует ТУ.
Предварительный нагрев гидроксида бария в течение более 10 минут позволяет получить стандартный продукт, но нецелесообразно увеличивает продолжительность стадии и энергозатраты.
Для полного завершения реакции между гидроксидом бария и борной кислотой необходимо оптимальное время перемешивания реакционной массы 55-65 минут. При времени перемешивания 40 минут продукт содержит значительное количество водорастворимых веществ и не соответствует требованиям ТУ. Увеличение времени перемешивания свыше 60 минут нецелесообразно из-за возрастания энергозатрат и механических потерь продукта при пылеуносе.
Таким образом, в оптимальных условиях процесс получения боратов бария осуществляют следующим образом.
В предварительно нагретый до температуры 35-45oC смеситель загружают твердый гидроксид бария и перемешивают его 5 минут для равномерного прогревания и увлажнения, после чего добавляют твердую борную кислоту и перемешивают смесь 60 минут. В процессе реакции происходит разогрев массы до 60oC, масса меняется от вязкой пастообразной до рассыпчатого порошка. Получаемый продукт соответствует требованиям ТУ 113-07-014-91 и содержит B2O3 не менее 46,5%, BaO не менее 34% и водорастворимых веществ менее 10%.
Используя данный способ, можно получить гексаборат бария состава BaO•3B2O3•4H2O и метаборат бария BaO•B2O3•H2O.
Пример 1.
В предварительно нагретый до 35oC смеситель загружают 17 кг твердого гидроксида бария, перемешивают его 5 минут и загружают 19,4 кг твердой борной кислоты. Массу перемешивают 60 минут. Продукт выгружают и сушат. Получают гексаборат состава BaO•3B2O3•4H2O, соответствующий требованиям ТУ 113-07-014-91 с массовой долей B2O3 - 47,6%, BaO - 34,7% и количеством водорастворимых веществ - менее 10%.
Пример 2.
В предварительно нагретый до 35oC смеситель загружают 19,4 кг твердой борной кислоты, перемешивают ее 5 минут и загружают 17 кг твердого гидроксида бария. Массу перемешивают 60 минут. Продукт содержит 17% водорастворимых веществ и не соответствует требованиям ТУ.
Пример 3.
В предварительно нагретый до 75oC смеситель загружают 17 кг твердого гидроксида бария, перемешивают его 5 минут и загружают 19,4 кг твердой борной кислоты. Массу перемешивают 60 минут. Продукт содержит BaO - 31,6% и не соответствует требованиям ТУ.
Пример 4.
В предварительно нагретый до 35oC смеситель загружают 17 кг твердого гидроксида бария, перемешивают его 20 минут и загружают 19,4 кг твердой борной кислоты. Массу перемешивают 60 минут. Получают гексаборат состава BaO•3B2O3•4H2O, соответствующий требованиям ТУ 113-07-014-91, с массовой долей B2O3 - 47,3%, BaO - 34,5% и количеством водорастворимых веществ менее 10%.
Пример 5.
Аналогично примеру 1. Время перемешивания смеси реагентов 40 минут. Реакционная смесь представляет собой влажную творожистую массу. Продукт содержит 15,4% водорастворимых веществ и не соответствует требованиям ТУ.
Пример 6.
Аналогично примеру 1. Время перемешивания смеси реагентов 70 минут. Продукт содержит B2O3 - 46,9%, BaO - 34,2%, количество водорастворимых веществ - менее 10% и соответствует ТУ. Продукт пылит, что увеличивает механические потери его.
Пример 7.
Аналогично примеру 1. Температура предварительного прогрева смесителя и гидроксида бария 25oC. Продукт содержит водорастворимых веществ 42% и не соответствует ТУ.
Пример 8.
В предварительно нагретый до 35oC смеситель загружают 17 кг твердого гидроксида бария, перемешивают его 2 минуты и загружают 19,4 кг твердой борной кислоты. Массу перемешивают 60 минут.
Продукт содержит водорастворимых веществ 32% и не соответствует ТУ.
Пример 9.
В предварительно нагретый до 70oC смеситель загружают 17 кг твердого гидроксида бария, перемешивают его 5 минут и загружают 19,4 кг твердой борной кислоты. Массу перемешивают 60 минут. Продукт выгружают и сушат. Получают гексаборат состава BaO•3B2O3•4H2O, соответствующий требованиям ТУ 113-07-014-91, с массовой долей B2O3 - 47,5%, BaO - 34,7% и количеством водорастворимых веществ менее 10%.
Пример 10.
В предварительно нагретый до 35oC смеситель загружают 10,2 кг твердого гидроксида бария, перемешивают его 5 минут и загружают 4 кг твердой борной кислоты. Массу перемешивают 60 минут. Продукт выгружают и сушат. Получают метаборат состава BaO•B2O3 •H2O с массовой долей B2O3 не менее 28,8%.
Пример 11.
В предварительно нагретый до 35oC смеситель загружают 4 кг твердой борной кислоты, перемешивают ее 5 минут и загружают 10,2 кг твердого гидроксида бария. Массу перемешивают 60 минут. Взаимодействия между твердыми веществами не происходит, о чем говорит высокое содержание (25%) водорастворимых веществ в конечной пробе смеси.
Пример 12.
Аналогично примеру 10. Продолжительность синтеза 40 минут. Реакционная масса содержит 30% водорастворимых веществ, что свидетельствует о неполном взаимодействии исходных компонентов.
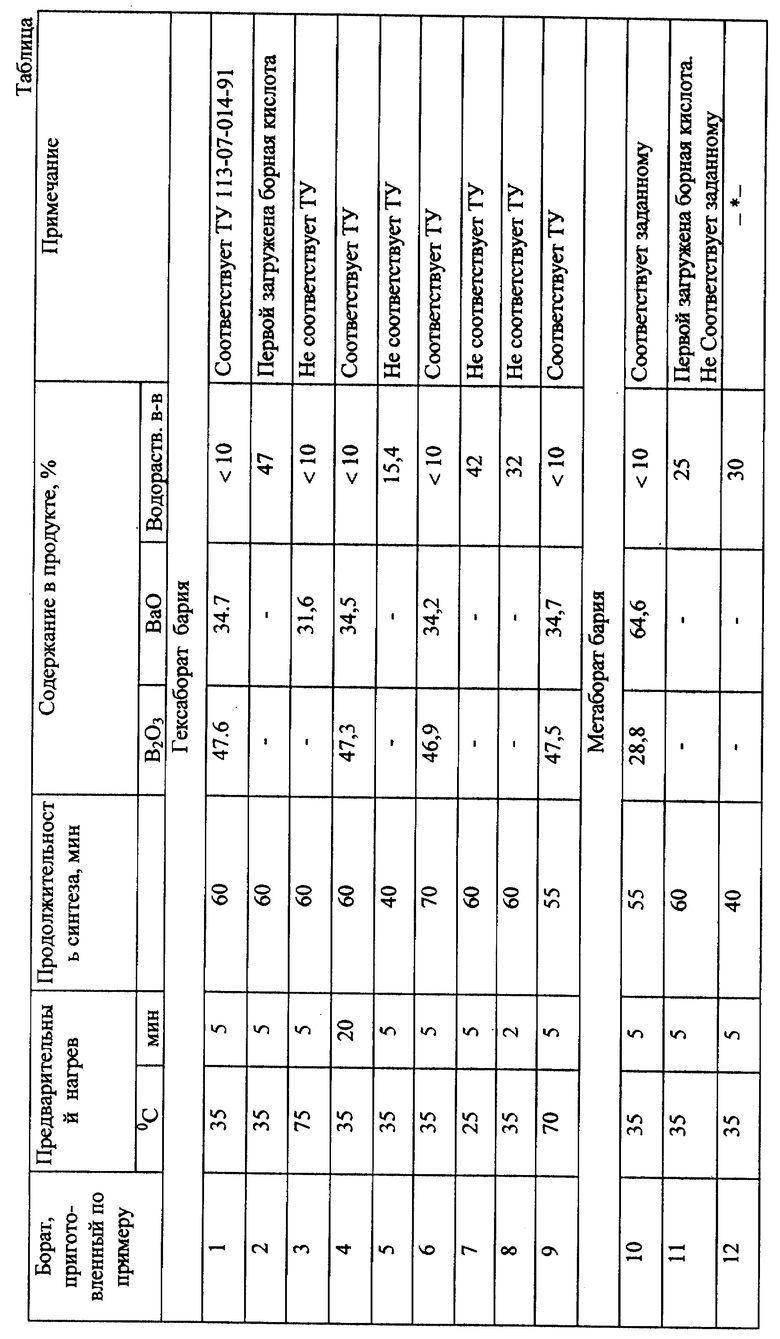
Результаты экспериментов, описанных в примерах 1-12 и демонстрирующих влияние заявляемых параметров на достижение поставленной цели, приведены в таблице.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПЕРБОРАТ КАЛЬЦИЯ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1999 |
|
RU2146645C1 |
| СПОСОБ ПЕРЕРАБОТКИ СОДОСУЛЬФАТНОЙ СМЕСИ | 2001 |
|
RU2188794C1 |
| ХРОМАТ БАРИЯ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2001 |
|
RU2191747C1 |
| УСТРОЙСТВО ДЛЯ ДОЗИРОВАНИЯ | 1999 |
|
RU2200303C2 |
| СОСТАВ ДЛЯ СКРЫТОЙ ЗАПИСИ ИНФОРМАЦИИ И СПОСОБ СКРЫТОЙ ЗАПИСИ ИНФОРМАЦИИ | 2001 |
|
RU2203297C1 |
| АМПЕРОМЕТРИЧЕСКИЙ СПОСОБ ОПРЕДЕЛЕНИЯ ОСТАТОЧНОГО ХЛОРА В ВОДЕ | 1999 |
|
RU2163375C2 |
| СОСТАВ ДЛЯ СКРЫТОЙ ЗАПИСИ ИНФОРМАЦИИ И СПОСОБ СКРЫТОЙ ЗАПИСИ ИНФОРМАЦИИ | 2001 |
|
RU2203296C1 |
| СПОСОБ АМПЕРОМЕТРИЧЕСКОГО КОНТРОЛЯ ПРОЦЕССА НЕЙТРАЛИЗАЦИИ ХРОМА (6+) | 1999 |
|
RU2155331C1 |
| СПОСОБ УТИЛИЗАЦИИ ОТРАБОТАННЫХ АВТОМОБИЛЬНЫХ АНТИФРИЗОВ | 2001 |
|
RU2188212C1 |
| СПОСОБ ПОЛУЧЕНИЯ НИТРИДА БОРА ГРАФИТОПОДОБНОЙ ГЕКСАГОНАЛЬНОЙ СТРУКТУРЫ | 2004 |
|
RU2266865C1 |
Изобретение относится к химической промышленности, а именно к способу получения боратов бария. Сущность изобретения заключается в смешении в стехиометрическом соотношении твердых гидроксида бария и борной кислоты, причем твердый гидроксид бария загружают в смеситель первым, нагревают до 35-70°С и перемешивают при этой температуре не менее 5 мин, далее добавляют твердую борную кислоту и перемешивание смеси продолжают не менее 55 мин. Способ по изобретению прост, себестоимость продукта снижается. 2 з.п. ф-лы, 1 табл.
| Способ получения боратов металлов | 1991 |
|
SU1834846A3 |
| Способ получения боратов щелочноземельных металлов | 1952 |
|
SU96093A1 |
| Способ получения боратов щелочноземельных и щелочных металлов | 1972 |
|
SU471302A1 |
| СПОСОБ ПОЛУЧЕНИЯ БЕЗВОДНОГО МЕТАБОРАТА БАРИЯ | 0 |
|
SU187744A1 |
| Способ получения кристаллического дибората бария | 1988 |
|
SU1611861A1 |
| СПОСОБ ПОДЪЕМА ЗАТОНУВШИХ ОБЪЕКТОВ И КОМПЛЕКС ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2000 |
|
RU2230002C2 |
| US 4897249 A, 30.01.1990. | |||
Авторы
Даты
2000-03-20—Публикация
1999-06-28—Подача